Большая медицинская энциклопедия системная красная волчанка
Большая медицинская энциклопедия
Авторы: Л. В. Кактурский, В. А. Насонова, А. И. Струков, А. С. Тиганов, Л. Я. Трофимова.
Системная красная волчанка – хроническое системное воспалительное заболевание соединительной ткани и сосудов с выраженным аутоиммунным патогенезом и, по-видимому, вирусной этиологией; относится к диффузным болезням соединительной ткани – коллагенозам .
Синонимы: lupus erythematosus systemicus, острая красная волчанка, эритематозный хрониосепсис, болезнь Либмана-Сакса.
Системная красная волчанка – болезнь женщин детородного возраста (20-30 лет), нередко заболевают девочки подросткового возраста. Соотношение женщин и мужчин, страдающих этим заболеванием, по большинству статистических данных – 8:1-10:1.
Современное учение о системной красной волчанке связано с именами P. Klemperer, A. Pollack и G. Baehr, которые в 1941 году привлекли внимание к диффузной коллагеновой болезни (diffuse collagen disease), описав системное поражение соединительной ткани при этой болезни и склеродермии. С открытием LE клеток (Lupus erythematosus cells) M. Hargraves, H. Richmond и R. Morton в 1948 году, а в 1949 году Y. R. Haserick - волчаночного фактора, было обращено внимание на аутоиммунные нарушения.
Популяционные исследования M. Siegel (1962-1965) показали, что заболеваемость в районе Манхеттена (Нью-Йорк) возросла с 25 на 1 миллионов человек в 1955 году до 83 на 1 миллионов в 1964 году. E. L. Dubois (в 1974 году) предполагает, что в США системной красной волчанкой ежегодно заболевает 5200 человек, следовательно, каждые 5 лет накапливается минимально 25 000 больных. T. Leonhardt в 1955 году показал, что заболеваемость системной красной волчанкой в городе Мальме (Швеция) с 1955 по 1960 год была 29 на 1 миллионов. Смертность в США, по данным Cobb (1970 г), – 5,8 на 1 миллионов населения, выше среди женщин в возрасте 25-44 года.
Этиология системной красной волчанки не выяснена, однако гипотеза о роли хронической персистирующей вирусной инфекции получила развитие в связи с обнаружением при электронной микроскопии в поражённых органах (коже, почках, синовиальной оболочке) тубулоретикулярных структур, расположенных в цитоплазме эндотелиальных клеток, а также в лимфоцитах и тромбоцитах периферической крови, которые напоминали нуклеопротеид парамиксовирусов.
При системной красной волчанке были также обнаружены в высоких титрах циркулирующие антитела к вирусам кори, краснухи, парагриппу и другим РНК-вирусам из группы парамиксовирусов. У больных и их родственников выявлены лимфоцитотоксические антитела, являющиеся маркерами персистирующей вирусной инфекции, а, кроме того, в этих же группах и у медперсонала, работающего с больными, – антитела к двуспиральной (вирусной) РНК. В связи с вирусной этиологией системной волчанки обсуждаются такие феномены, как гибридизация генома коревого вируса с ДНК клеток поражённых органов (селезёнки, почек), обнаружение антигенов онкорнавирусов типа С во фракциях селезёнки, плаценты и почки.
Гипотеза о значимости хронической вирусной инфекции при системной красной волчанке базируется также на изучении болезни новозеландских мышей, у которых роль онкорнавируса типа С доказана.
Непереносимость лекарств, фотосенсибилизация, вакцин, становление менструального цикла, роды, беременность, аборты и т. п. рассматриваются как факторы, провоцирующие болезнь или её обострение. Они имеют значение для профилактики и своевременной диагностики, поскольку связь начала или обострений болезни с этими факторами более характерна для системной красной волчанки, чем для других близких болезней.
См. также: Аутоаллергические болезни, Коллагеновые болезни.
Большая медицинская энциклопедия 1979 г.
 |
Последнее обновление страницы: 17.11.2014 Обратная связь Карта сайта
Системная красная волчанка — это хроническое многосиндромное заболевание соединительной ткани и сосудов, развивающееся в связи с генетически обусловленным несовершенством иммунорегуляторных процессов.
Оно вызывает разнородные нарушения, имеющие определенные общие черты, включая воспалительные процессы в коже, суставах и других структурах, богатых соединительной тканью, а также общие черты нарушения иммунной регуляции с образованием антител к собственным тканям (аутоантител), нарушением клеточно-опосредованного иммунитета.
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ
В качестве факторов, способствующих возникновению заболевания, выступают факторы окружающей среды. Существует мнение, что вирусы, токсические вещества и лекарственные средства могут быть причиной развития системной красной волчанки, однако убедительных доказательств этого до сих пор нет. В ряде случаев у больных системной красной волчанкой обнаруживают антитела к вирусу Эпштейна-Барра и другим РНК-содержащим вирусам.
Предрасполагающими факторами являются:
I. Генетические особенности организма.
Роль наследственности подтверждается высокой частотой возникновения болезни у однояйцевых близнецов, в отличие от обычных родных братьев и сестер. Отмечена связь заболевания с наследственным дефектом некоторых генов. II. Гормональные влияния. Системная красная волчанка развивается в основном у женщин детородного возраста, но предполагается, что гормональные факторы больше влияют на проявления заболевания, чем на его возникновение. Для системной красной волчанки характерны разнообразные нарушения иммунорегуляции. Образуются так называемые иммунные комплексы, которые циркулируют по сосудистому руслу и поражают клетки внутренней оболочки сосудов не только в том месте, где образовались, а по всему организму. Откладываясь на базальных мембранах различных органов, вызывают их повреждение и воспаление.
Принято выделять острое, подострое и хроническое течение системной красной волчанки.
Острое течение характеризуется внезапным началом с резким повышением температуры тела, быстрым поражением внутренних органов, включая почки, а также высоким уровнем антител.
Подострое течение характеризуется периодически возникающими обострениями заболевания, выраженными не в такой степени, как при остром течении, и развитием поражения почек в течение первого года болезни.
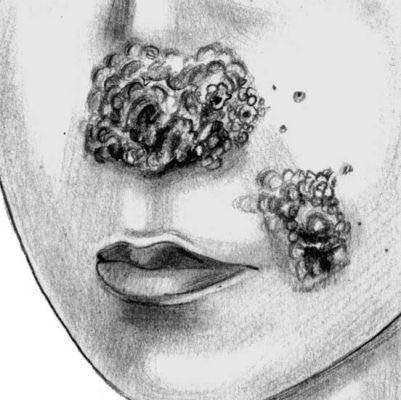
Язвенная форма волчанки
Хроническое течение характеризуется длительным преобладанием одного или нескольких симптомов (поражения кожи, множественные поражения суставов, снижение количества тромбоцитов в крови, снижение количества белка в моче и др.).
В России традиционно применяется деление болезни на три степени активности:
I степень: температура тела нормальная, незначительное похудание, волчаночные очаги на коже, кардиосклероз, небольшое количество белка в моче, гемоглобин 120 г/л и более, небольшие сдвиги лабораторных показателей.
II степень: температура тела менее 38°С, умеренное похудание, покраснения на коже, умеренный миокардит, гемоглобин 110-120 г/л, умеренные сдвиги лабораторных показателей.

Язвенные образования в виде бугорков

Язвенная форма волчанки. Мощные, образовавшиеся от слияния бугорковых элементов мягкие диффузные инфильтраты
Начинается болезнь постепенно, с рецидивирующего полиартрита и астении. Реже бывает острое начало (высокая лихорадка, дерматит, острый полиартрит). В дальнейшем отмечаются рецидивирующее течение и характерная многосиндромность.
Полиартрит, полиартралгии — наиболее частый и ранний симптом заболевания. Поражаются преимущественно мелкие суставы кистей рук, лучезапястные, голеностопные, реже коленные суставы. Характерен неэрозивный (без образования дефектов суставной ткани) тип полиартрита, даже при наличии деформации межфаланговых суставов, которая развивается у 10-15% больных с хроническим течением.
Характерно поражение сердечно-сосудистой системы. Обычно развивается перикардит, к которому присоединяется миокардит. Сравнительно часто наблюдается бородавчатый эндокардит Либмана-Сакса с поражением митральных, аортальных и трикуспидальных клапанов сердца.
Признаки поражения сосудов входят в картину поражения отдельных органов. Тем не менее следует отметить возможность развития синдрома Рейно (задолго до типичной картины болезни), поражение как мелких, так и крупных сосудов с соответствующей клинической симптоматикой.
Поражения легких могут быть связаны с основным заболеванием в виде волчаночного пневмонита, характеризующегося кашлем, одышкой, незвонкими влажными хрипами в нижних отделах легких.
Рентгенологическое исследование у таких больных выявляет усиление и изменение легочного рисунка в нижних отделах легких; временами можно обнаружить очаговоподобные тоны. Поскольку пневмонит обычно развивается на фоне текущего полисерозита, описанная рентгенологическая симптоматика дополняется высоким стоянием диафрагмы с признаками плевродиафрагмальных и плевроперикардиальных сращений и дисковидными ателектазами (линейные тени, параллельные диафрагме).
При исследовании желудочно-кишечного тракта отмечаются афтозный стоматит, диспептический синдром и анорексия. Болевой абдоминальный синдром может быть связан как с вовлечением в патологический процесс брюшины, так и с собственно васкулитом — мезентериальным, селезеночным. Реже развиваются очаговые илеиты. Поражение ретикулоэндотелиальной системы выражается в увеличении всех групп лимфатических узлов (весьма частый и ранний признак системности болезни), а также увеличении печени и селезенки. Собственно волчаночный гепатит развивается крайне редко. Однако увеличение печени может быть обусловлено сердечной недостаточностью при панкардите или выраженном выпотном перикардите, а также развитием жирового истощения печени.
Волчаночный диффузный гломерулонефрит (люпус-нефрит) развивается у половины больных обычно в период распространения процесса. Встречаются различные варианты поражения почек — мочевой, нефритический и нефротический синдромы. Для распознавания люпус-нефрита большое значение имеет прижизненная пункционная биопсия с исследованием образца ткани почки. Развитие почечных нарушений у больных с рецидивирующим суставным синдромом, лихорадкой и стойко повышенной СОЭ требует исключения волчаночного происхождения нефрита. Следует помнить, что почти у каждого пятого больного с нефротическим синдромом имеет место системная красная волчанка.

Поражение нервно-психической сферы встречается у многих больных во всех фазах болезни. В начале болезни наблюдается астеновегетативный синдром, в последующем развиваются признаки поражения всех отделов центральной и периферической нервной системы в виде энцефалита, миелита, полиневрита. Характерно поражение нервной системы. Реже наблюдаются эпилептиформные припадки. Возможны галлюцинации (слуховые или зрительные), бредовые состояния.
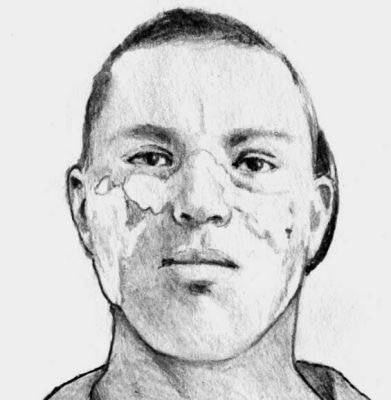
Дискоидная красная волчанка
Лабораторные данные, имеющие диагностическое значение: определение большого числа LE-клеток и высокого количества антител к ДНК. При остром течении уже через 3-6 месяцев выявляется люпус-нефрит, нередко по типу нефротического синдрома. При подостром течении отчетливо наблюдается волнообразное развитие заболевания с вовлечением в патологический процесс различных органов и систем и характерной многосиндромностью.
Хроническое течение заболевания длительное время характеризуется рецидивами полиартрита и (или) полисерозита, синдромами дискоидной волчанки, Рейно; лишь на 5-10-м году постепенно развивается характерная полисиндромность. В соответствии с клинико-лабораторной характеристикой выделяют три степени активности процесса: высокую, умеренную и минимальную.
Включает опрос и физикальное обследование, рентгенологическое исследование, ЭКГ, общий анализ мочи, общий анализ крови, СОЭ, определение в сыворотке крови уровней иммунных белков, антител к гладким мышцам, а также пробу на сифилис. Диагноз достоверен при наличии четырех или более критериев.
ЛЕЧЕНИЕ И ПРОФИЛАКТИКА
Направлено на ограничение воспалительного процесса. Применяют салицилаты (особенно аспирин, покрытый оболочкой, растворимой в кишечнике, по 2-4 г в день в нескольких дозах), нестероидные противовоспалительные средства (ибупрофен по 400- 800 мг 3-4 раза в день) и гидроксихлорохин по 400 мг в день; глюкокортикоиды (преднизон по 1-2 мг/кг массы или его эквиваленты необходимы при состояниях, угрожающих жизни, или при тяжелых проявлениях заболевания); цитостатические препараты (циклофосфамид по 1,5-2,5 мг/кг или азатиоприн по 2-3 мг/кг) применяют в случаях, когда стероиды не обеспечивают подавление симптомов заболевания); внутривенное введение пульс-доз циклофосфамида (10-15 мг/кг каждые 4 недели) — альтернатива ежедневному приему цитостатических средств.
Больные нуждаются в непрерывном, многолетнем и комплексном лечении. Лучшие результаты с развитием стойкой клинической ремиссии достигаются при рано начатом лечении. При хроническом и подостром течении и минимальной степени активности показаны нестероидные противовоспалительные препараты и аминохинолиновые производные. Первые рекомендуются при суставном синдроме. Важен подбор препарата с учетом его индивидуальной эффективности и переносимости: вольтарен (ортофен) по 50 мг 2-3 раза в день, индометацин по 25-50 мг 2-3 раза в день, бруфен по 400 мг 3 раза в день, хингамин (хлорохин, делагил) по 0,25-0,5 г в сутки в течение 10-14 дней, а затем по 0,25 г в сутки в течение нескольких месяцев. При развитии распространенного люпус-нефрита с успехом применяют плаквенил по 0,2 г 4-5 раз в день, длительно, под контролем динамики мочевого синдрома.
При остром течении с самого начала, а при подостром и хроническом течении при III и II степени активности патологического процесса показаны глюкокортикостероиды. Начальная доза этих препаратов должна быть достаточной, чтобы надежно подавить активность патологического процесса. Преднизолон в дозе 40-60 мг в сутки назначают при остром и подостром течении со средней степенью активности и наличием нефротического синдрома или менингоэнцефалита. При этих же вариантах течения со II степенью активности, а также при хроническом течении с III и II степенью активности подавляющая доза должна быть 30-40 мг, а при I степени активности — 15-20 мг в сутки.
Лечение преднизолоном в подавляющей дозе проводят до наступления выраженного клинического эффекта (по данным снижения клинико-лабораторных показателей активности). По достижении эффекта дозу преднизолона медленно снижают. Одной из важнейших задач и залогом эффективности терапии является подбор наименьшей дозы, которая позволяет поддерживать клинико-лабораторную ремиссию. Преднизолон в поддерживающей дозе 5-10 мг в сутки назначают в течение нескольких лет. Для уменьшения побочного эффекта глюкокортикоидов рекомендуется сочетать эту терапию с препаратами калия, анаболическими стероидами, мочегонными и гипотензивными препаратами, транквилизаторами, противоязвенными мероприятиями.
Наиболее серьезные осложнения: стероидная язва, септические инфекции, туберкулез, кандидоз, психозы. При агрессивном течении болезни, высоком количестве аутоантител, иммунных комплексов с успехом используется плазмаферез. При неэффективности глюкокортикоидов назначают иммунодепрессанты (алкилирующего ряда или азатиоприн). Показания к назначению цитотоксических препаратов (обычно в комбинации с умеренными дозами кортикостероидов) следующие: высокая степень активности у подростков и в климактерическом периоде; нефротический и нефритический синдромы; необходимость быстро уменьшить подавляющую дозу преднизолона из-за выраженности побочного действия (быстрая и значительная прибавка массы тела, высокое артериальное давление, стероидный диабет, выраженный остеопороз с признаками спондилопатии); необходимость снизить поддерживающую дозу преднизолона, если она превышает 15-20 мг в сутки. Наиболее часто применяют азатиоприн (имуран) и циклофосфан (циклофосфамид) в дозе 1-3 мг/кг (100-200 мг в сутки) в сочетании с 30 мг преднизолона.
В этой дозе препарат назначают в течение 2-2,5 месяца (обычно в стационаре), затем рекомендуют поддерживающую дозу (50-100 мг в день), которую дают в течение нескольких месяцев и даже года и более. Чтобы обеспечить безопасность лечения, требуется тщательный контроль анализа крови для предотвращения серьезных нарушений кроветворения; необходимо избегать присоединения инфекционных осложнений, расстройств пищеварения; при приеме циклофосфана опасность развития геморрагического цистита можно уменьшить путем назначения обильного питья (2 л жидкости и более в сутки). Поскольку больные нуждаются в многолетнем лечении после выписки из стационара, они должны находиться под наблюдением терапевта или ревматолога в поликлинике.
С целью улучшения переносимости многолетней кортикостероидной терапии в поликлинических условиях рекомендуется делагил по 0,25 г в сутки и витамины группы В, аскорбиновая кислота в виде весенне-осеннего курса. Больным показано лечение в санаториях местного типа (кардиологических, ревматологических). Климатобальнеологическое, физиотерапевтическое лечение противопоказано, так как ультрафиолетовое облучение и гидротерапия могут вызвать обострение болезни.
ВОЛЧАНКА СИСТЕМНАЯ КРАСНАЯ
Системная красная волчанка (СКВ) - диффузное заболевание соединительной ткани аутоиммунной природы с образованием широкого спектра аутоантител и циркулирующих иммунных комплексов, вызывающих повреждение тканей и нарушения функций органов. Типичны поражения кожи, слизистых оболочек, ЦНС, почек и крови. Аутоиммунную природу заболевания подтверждают определением антинуклеарных AT
(АНАТ) в крови и обнаружением фиксированных иммунных комплексов в тканях.
0,02-0,04% населения. Преобладающий возраст - 20-40 лет. Преобладающий пол - женский (8-10:1).
Факторы окружающей среды. Существует мнение, что вирусы, токсические вещества и ЛС могут быть причиной развития СКВ, однако убедительных доказательств не получено. Теоретически вирусы способны вызывать изменения во взаимодействиях лимфоцитов и влиять на проявления заболевания (например, взаимодействие с CD4+- и С08
-клетками влияет на функцию В-лимфоцитов). Ультрафиолетовое облучение способно изменить антигенные свойства ДНК
Генетические факторы. Исследования семейных случаев заболевания и исследования близнецов позволяют предположить генетическую предрасположенность к СКВ. Болезнь часто появляется в семьях с дефицитом отдельных компонентов комплемента. Аг HLA-DR2 и HLA-DR3 у больных СКВ отмечают намного чаще, чем в общей популяции
Аутоиммунитет. Утрату толерантности к аутоантигенам считают центральным звеном патогенеза СКВ. У пациентов обнаруживают тенденцию к выработке аутоантител, повышенной активности В-лимфоцитов и дисфункции Т-лимфоцитов. Эта тенденция не связана с Аг главного комплекса гистосовместимости
Гормональные влияния. СКВ развивается в основном у женщин детородного возраста, но гормональные факторы, возможно, больше влияют на проявления заболевания, чем на его возникновение. Считают, что эстрогены усиливают, а андрогены тормозят выработку AT.
Все клинические проявления СКВ - следствие нарушений гуморального и клеточного иммунитета.
Иммунные комплексы. Циркулирующие комплексы Аг-АТ фиксируются в кровеносных сосудах и почечных клубочках, приводя к повреждению тканей. Эти комплексы считают характерным признаком активности болезни, а их размеры, растворимость, концентрация и способность к фиксации комплемента определяют отложение комплексов в тканях организма.
Длительная циркуляция иммунных комплексов приводит к потере способности к их удалению. СКВ чаще наблюдают у лиц с дефектным геном С4а компонента комплемента,
Образуемые аутоантитела вызывают различные патологические нарушения
Спектр образуемых AT - АНАТ, анти-ДНК, анти-Sm (к полипептидам коротких ядерных РНК), анти-RNP (к полипептидам рибонуклеопротеидов), анти-Ro (к РНК-полимеразе), анти-La (к протеину в составе РНК), антигистоны, антикардиолипин (к фосфоли-пидам), антиэритроцитарные, антитромбоцитарные, антилимфоци-тарные, антинейрональные
Повреждение тканей. AT к эритроцитам, лейкоцитам и тромбоцитам приводят к иммунным цитопениям
Клеточная дисфункция. AT к лимфоцитам нарушают функцию и межклеточные взаимодействия; антинейронные AT, проникая через ГЭБ, повреждают нейроны
Образование иммунных комплексов. Комплексы AT и нативной ДНК способствуют возникновению аутоиммунного поражения почек у больных СКВ.
Патологические клеточные реакции
Уменьшение соотношений Т-хелперы/Т-индукторы и Т-супрессоры/цитотоксические клетки
Замедление элиминации иммунных комплексов вследствие наследственных и приобретённых дефектов рецепторов макрофагов.
Характерные микроскопические изменения
Гематоксилиновые тельца. В очагах повреждения соединительной ткани определяют аморфные массы ядерного вещества, окрашиваемые гематоксилином в пурпурно-синий цвет. Нейтрофилы, поглотившие такие тельца и vitro, называют LE-клетки
Фибриноидный некроз. Иммунные комплексы в соединительной ткани и стенках сосудов, состоящие из ДНК, AT к ДНК и комплемента, окрашиваются (как и фибрин) эозином, образуя картину фибриноидного некроза
шелухи наблюдают в сосудах селезёнки больных СКВ с характерным периваскулярным концентрическим отложением коллагена.
Изменения в тканях
Кожа. При незначительных повреждениях кожи наблюдают лишь неспецифическую лимфоцитарную инфильтрацию. В более тяжёлых случаях происходит отложение иммуноглобули-нов, комплемента и возникает некроз(область дермоэпидермально-го соединения). В области классических дискоидных участков обнаруживают фолликулярные пробки, гиперкератоз и атрофию эпидермиса. Встречают и повреждения стенок мелких сосудов кожи
Почки. Отложения иммунных комплексов в почках способны вызывать различные воспалительные изменения. Характерный кардинальный признак поражения почек при СКВ - периодическое изменение гистологической картины нефрита в зависимости от активности болезни или проводимой терапии
Мезангиальный нефрит (возникает вследствие отложения иммуноглобулинов) считают наиболее частым поражением почек при СКВ
Очаговый пролиферативный нефрит характеризуется вовлечением лишь сегментов клубочков в менее чем 50% клубочков
Диффузный пролиферативный нефрит протекает с клеточной пролиферацией большинства сегментов клубочков в более чем 50% клубочков
Мембранозный нефрит -следствие отложения иммуноглобулинов в эпителии и периферических капиллярных петлях без пролиферации клеток клубочков, хотя у части больных встречают комбинации пролиферативных и мембранозных изменений
Интерстициальное воспаление может возникать при всех описанных выше нарушениях
ЦНС. Наиболее типичны периваскулярные воспалительные изменения сосудов среднего калибра (хотя возможно поражение сосудов крупного калибра), микроинфаркты и микрокровоизлияния, не всегда коррелирующие с находками при КТ, МРТ и неврологическом обследовании
Васкулит. Повреждение тканей при СКВ происходит вследствие воспалительных, иммунокомплексных поражений капилляров, ве-нул и артериол
Часто возникают неспецифический синовит и лим-фоцитарная мышечная инфильтрация. Нередко возникает абактери-альный эндокардит, протекающий в типичных случаях без симптомов.
Дискоидное поражение - очаги напоминают по форме монеты с гиперемированными краями, атрофией в центре и депигментацией
Нодулярное волчаночное поражение кожи
Эритематозный дерматит носа и скул по типу бабочки (эритема на щеках и в области спинки носа)
Фотосенсибилизация - кожные высыпания в результате необычной реакции на солнечный свет
Алопеция (генера-лизованная или очаговая)
Поражения кожи, обусловленные васкулитом: панникулит, крапивница, микроинфаркты, сетчатое ливедо (древовидный рисунок на коже нижних конечностей вследствие венулита).
Поражение слизистых оболочек: хейлит, эрозии.
Симметричный неэрозивный артрит без деформаций. В синовиальной жидкости лейкоцитов не более 2,0x1О9/л, нейтрофилов менее 50%
Артропатия (синдром Жакку) со стойкими деформациями возникает за счёт вовлечения связок и сухожилий, а не вследствие эрозивного артрита.
Плеврит - шум трения плевры, выпот и значительное ограничение подвижности диафрагмы
Пнев-монит - инфильтраты при СКВ двусторонние, летучие и нередко сопровождаются кровохарканьем
Лёгочная гипер-тёнзия при изолированном поражении лёгочных артерий.
Эндокардит Либмана- Сакса может сопровождаться эмболиями, нарушениями функции клапанов и присоединением инфекции
Миокардит с нарушениями проводимости, аритмиями и сердечной недостаточностью
Вальвулит при антифосфолипидном синдроме
При остром прогрессирующем течении СКВ возможен васкулит коронарных сосудов, однако основная причина ИМ у больных СКВ - атеросклероз вследствие длительной терапии глюкокортикоидами.
Мембранозный, мезангиомембранозный гломерулонефрит
Мезангиокапилляр-ный, мезангиопролиферативный гломерулонефрит
Ослабление перистальтики пищевода
Изъязвление слизистой оболочки желудка и двенадцатиперстной кишки
Увеличение печени без существенного нарушения функций
Интестинальный васкулит может сопровождаться инфарктами кишечника, перфорациями и кровотечениями.
Поражение ЦНС - у 50% пациентов возникают очаговые или диффузные нарушения
Генерализованные проявления - депрессия, психозы, нарушения познавательных способностей и судороги. У некоторых больных возникновение психозов связывают с появлением AT к рибосомальному Р-белку
Возможны гемипарезы, дисфункции черепных нервов, миелиты и нарушения движений. Даже серьёзные неврологические проявления болезни могут спонтанно исчезнуть
Периферическая невропатия (синдром Гийена-Баррё, множественные мононевриты)
Кровь. Часто выявляют анемию (как при острых, так и при хронических вариантах течения СКВ). Антилейкоцитарные AT вызывают развитие аутоиммунной лимфопении, реже -нейтропении. AT к тромбоцитам способствуют развитию острой или хронической иммунной тромбоцитопении. Увеличение СОЭ считают характерным признаком СКВ, коррелирующим с активностью заболевания
Увеличение СРВ не характерно
Обнаружение АНАТ, AT к ДНК, AT к РНК-полимеразе, протеину, входящему в состав РНК
Обнаружение в крови LE-клеток (лейкоциты, фагоцитировавшие ядерный материал)
Ложноположительная реакция фон Вассермана у пациентов с антифосфолипидным синдромом (см. Синдром антифос-фолипидный)
Показатели коагуляции. AT к фосфолипидам способны воздействовать на свёртывание крови, вызывая увеличение показателя тромбопластинового времени. Несмотря на это, у пациентов с подобными нарушениями выше риск возникновения тромбозов, чем кровотечений
Специальные методы исследования - биопсия почек, рентгенологическое исследование органов грудной полости, эхокар-диография.
Клинико-иммунологические формы СКВ
СКВ у пожилых пациентов: кожный, суставной синдромы и поражение почек возникают реже, часто развиваются синдром Шёгрена, поражение лёгких, периферические невропатии. Часто обнаруживают AT к РНК-полимеразе
Неонатальная СКВ у детей, родившихся от матерей, больных СКВ: эритематозная сыпь, полная АВ блокада, гемолитическая анемия; серологический маркёр - AT к РНК-полимеразе
Подострая кожная красная волчанка характеризуется выраженным дерматитом, обусловленным фотосенсибилизацией. Чаще возникает у мужчин. Характерны
полиартрит, серозит; обнаруживают AT к РНК-полимеразе (Ro-Ar) и протеину, входящему в состав РНК (La-Ar)
Серонегативная СКВ (отсутствуют АНАТ) клинически близка к подострой кожной, редко происходит поражение почек.
При умеренно выраженной и волнообразно текущей СКВ
При артралгии, лихорадке - НПВС (см. Артрит ревматоидный)
При поражении суставов и кожи -противомалярийные препараты (производные аминохинолина) t При тяжёлой форме СКВ (поражение почек, ЦНС, гематологические нарушения) - активная иммуносупрессивная терапия (глюкокортикоиды, цитостатики)
При СКВ любой тяжести после подавления воспалительного процесса назначают минимальные поддерживающие дозы глюкокортикоидов или других препаратов (дозу подбирают, постепенно снижая её на 10% каждые 1-4 нед)
Симптоматическая терапия: препараты, улучшающие мозговое кровообращение и метаболизм клеток головного мозга (кавинтон, ноотропил, церебролизин), противосудорожные препараты, транквилизаторы t Больным противопоказана инсоляция.
Плаквенил (гидроксихло-рохин) от 200-400 мг/сут до 200 мг 2 р/нед, или
Хлоро-хин от 250 мг/сут до 250 мг 2 р/нед.
Преднизолон 1 мг/кг/сут внутрь в течение 4-6 нед с постепенным снижением дозы до поддерживающей (5-7,5 мг/сут). При гломерулонефрите, острых церебральных нарушениях, гемолитическом кризе дозу повышают до 80-100 мг/сут. Улучшение обычно наступает через 4-12 нед.
При активном люпус-нефрите, гематологическом кризе, острых нейропсихических расстройствах как дополнение к систематическому приёму преднизолона - пульс-терапия; метилпреднизолон 1 г в/в капельно в течение 30 мин три дня подряд; возможно повторение инъекций ежемесячно в течение 3-6 мес. После проведения пульс-терапии дозу преднизолона следует снижать медленно во избежание уменьшения клубочковой фильтрации.
Иммунодепрессивные препараты (всегда в сочетании с глю-кокортикоидами) - при активном люпус-нефрите, генера-лизованном васкулите (поражениях лёгких, ЦНС, язвенных поражениях кожи), резистентности к глюкокортикоидам.
Азатиоприн 2,5 мг/кг/сут внутрь.
Циклофосфамид (циклофосфан) 1,0-4,0 мг/кг/сут внутрь.
При активном люпус-нефрите, генерализованном васкулите высокоэффективна сочетанная пульс-терапия: 1 000 мг циклофосфана и 1 000 мг метилпреднизолона с последующим введением последнего в течение ещё 2 дней. После окончания сочетанной пульстерапии циклофосфан применяют по 200 мг/нед в течение 3-6 мес в сочетании с преднизолоном по 20-25 мг/сут.
Хлорбутин 0,1-0,2 мг/кг/сут.
Сочетание азатиоприна 100мг внутрь ежедневно и циклофосфана 1 000 мг в/в 1 раз в 3 мес (при люпус-нефрите).
При рефрактерной тромбоцитопении - даназол 10-15 мг/кг/сут.
При резистентной к лечению СКВ, выраженной тромбоцитопении - иммуноглобулин 0,4 г/кг/сут в/в в течение 5 дней.
При интеркуррентных вирусных или бактериальных инфекциях - рекомбинантные интерфероны в течение 3-6 мес.
При синдроме Рейно - см. Синдром Рейно.
При антифосфолипидном синдроме - см. Синдром анти-фосфолипидный.
При нарушении функций почек - гемодиализ.
При резистентном к лечению гломерулонефрите или генерализованном васкулите - плазмаферез и гемосорбция курсами по 6-8 процедур дополнительно к иммуносупрессивной терапии.
Особенности течения при беременности
Частые спонтанные выкидыши свидетельствуют о наличии антифосфолипидного синдрома
Обострения СКВ чаще возникают в 1 триместре и в первые 6 нед после родов. Если отсутствуют тяжёлые поражения сердца и почек, а течение СКВ контролируемо, беременность заканчивается благополучно
Не противопоказано назначение глюкокортикоидов. Неона-тальная СКВ развивается редко.
См. также Артрит ревматоидный, Волчанка, Волчанка дискоидная красная. Синдром антифосфолипидный, Синдром Рейно
Читайте также:


