Что такое ятрогенный путь передачи инфекции
Существуют 5 основных путей передачи инфекции, которые будут перечислены ниже.
Артифициальный путь передачи инфекции это…
Артифициальный путь передачи инфекции — это искусственное заражение, при котором распространение инфекционного агента происходят в результате ятрогенной деятельности человека. В качестве примера можно привести заражение ВИЧ-инфекцией или гепатитом при проведении операций или гемоплазмотрансфузии.
Трансмиссивный путь передачи инфекции это…

Трансмиссивный путь передачи инфекции — это заражение через насекомых:
- мух (болезнь Боткина, брюшной тиф, дизентерия, сибирская язва),
- вшей (сыпной тиф),
- клопов (возвратный тиф),
- блох (чума),
- комаров — анофелес (тропическая малярия).
Необходимо уничтожать этих насекомых, не допускать их в жилые помещения и предупреждать соприкосновение мух с водой и пищей.
Парентеральный путь передачи инфекции это…
Парентеральный путь передачи инфекции — это разновидность артифициального механизма заражения, при котором возбудитель попадает непосредственно в кровь.
Воздушно-капельный путь передачи инфекции это…

Воздушно-капельный путь передачи инфекции — это заражение через воздух, в который попадают на расстояние 1-1,5 м при разговоре, кашле и чихании больных мельчайшие брызги и капли слюны и носовой слизи, содержащие возбудителей болезней — капельная инфекция (грипп, ангина, дифтерия, коклюш, корь, скарлатина, туберкулез). При высыхании этих брызг и капель возбудители болезни долго сохраняются в пыли (туберкулез) — пылевая инфекция. Заражение происходит при вдыхании возбудителей болезней.
Контактный путь передачи инфекции это…

Контактный путь передачи инфекции — это, как можно понять из названия, распространение инфекционного агента при непосредственном контакте. Он может осуществляться несколькими механизмами:
- Соприкосновением с больным человеком (оспа натуральная, оспа ветряная, корь, скарлатина, свинка, болезнь Боткина и др.). Поэтому запрещается входить в квартиру, где имеются больные.
- Заражением от бациллоносителей. В организме выздоровевшего человека долго продолжают жить возбудители некоторых инфекционных болезней (брюшной тиф, дифтерия, скарлатина). Бациллоносителями могут быть и люди, не болевшие данной инфекционной болезнью, но несущие в себе ее возбудителя, например, во время эпидемии дифтерии до 7% здоровых школьников имеют в зеве или носу дифтерийных бацилл. Бациллоносители являются распространителями возбудителей.
Фекально-оральный путь передачи инфекции это…

Фекально-оральный путь передачи инфекции — это такой механизм заражения, при котором возбудитель попадает в ЖКТ. Инфекционисты выделяют три основных механизма передачи инфекции:
- Через выделения больных: испражнения (брюшной тиф, дизентерия), мочу (гонорея, скарлатина, брюшной тиф), слюну, носовую слизь. Заражение происходит и при попадании возбудителей болезней в рот, поэтому нужно обязательно воспитать у детей привычку тщательно мыть руки перед едой.
- Соприкосновением с предметами, к которым касался заразный больной (белье, вода, пищевые продукты, посуда, игрушки, книги, мебель, стены комнаты). Поэтому производится дезинфекция и рекомендуется пользоваться только своими посудой и вещами.
- Через некипяченую воду и молоко, немытые фрукты и овощи в организм проникают возбудители желудочно-кишечных болезней (паратифов, брюшного тифа, дизентерии, болезни Боткина) и туберкулеза. Вода и молоко должны быть обязательно кипячеными, а фрукты и овощи облиты кипятком или со снятой кожурой.
Ятрогенные инфекции — результат попадания микроорганизмов (бактерий) в верхний отдел репродуктивного тракта при проведении медицинских манипуляций, таких как регуляции менструального цикла, аборты, введение ВМС или во время родов. Аборты — частая причина ятрогенных инфекций. Согласно данным ВОЗ, каждый год имеют место 20 млн абортов, из которых большая часть приходится на развивающиеся страны (ВОЗ, 2000). Частота осложнений во время абортов составляет 10-50% . Причинами развития ятрогенной инфекции являются:
— использование нестерильных материалов и медицинского инструментария (вагинального зеркала);
— присутствие эндогенных инфекций или ИППП в нижнем отделе репродуктивного тракта.
Ятрогенные инфекции могут инфицировать матку, эндометрий, фаллопиевы трубы и яичники, и поэтому приводят к, серьезным осложнениям. Настораживающими симптомами являются боли внизу живота, подъем температуры тела, озноб, болезненные
месячные, патологические выделения из половых путей и боли во время coitusa.
По месту локализации инфекции репродуктивного тракта подразделяют на два вида: инфекции верхнего отдела репродуктивного тракта и инфекции нижнего отдела репродуктивного тракта (рис. 13.2).
К инфекциям верхнего отдела репродуктивного тракта относятся инфекции матки, фаллопиевых труб и яичников. К инфекциям нижнего отдела репродуктивного тракта относят инфекции вульвы, вагины и цервикса.
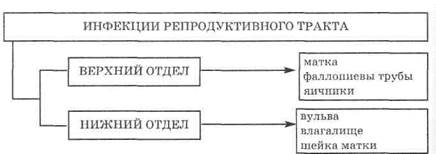
Рис. 13.2. Инфекции репродуктивного тракта
Инфекции нижнего отдела репродуктивного тракта
Инфекции репродуктивного тракта, которые поражают наружную половую область и нижний репродуктивный тракт женщины, часто упоминаются как вульвовагинит. Клинически это проявляется воспалением вульвы / вагины и может сопровождаться зудом или болезненностью при пальпации.
Причинами вульвовагинита являются эндогенные инфекции (кандидоз или бактериальный вагиноз), хотя некоторые инфекции, передающиеся половым путем, типа трихомониаза, могут также вызывать подобные клинические признаки.
Следует отметить, что некоторые инфекционные агенты (например, микроорганизмы, связанные с бактериальным вагинозом) могут мигрировать по репродуктивному тракту вверх и вызывать
воспалительные процессы органов малого таза, а впоследствии и более серьезные осложнения (эктопическую беременность, бесплодие). Распространению инфекции способствуют трансцервикаль-ные процедуры — например, регуляция менструального цикла, аборты или введение ВМС. Предшествующие воспалительные явления в фаллопиевых трубах также предрасполагают к последующему инфицированию или развитию хронической инфекции.
Цервицит
Причиной цервицита, как правило, являются микроорганизмы, передающиеся половым путем, типа gonorrhea и chlamydia trachomatis.
Цервициты рассматриваются как более серьезные состояния, чем вагиниты, поскольку они могут чаще осложняться инфицированием верхнего репродуктивного тракта с развитием серьезных последствий. Часто они не имеют клинических проявлений и трудно диагностируются.
Инфекции верхнего отдела репродуктивного тракта
Инфицирование верхнего репродуктивного тракта, включая матку, фаллопиевы трубы и яичники, — это, как правило, результат попадания инфекционного агента из нижнего отдела репродуктивного тракта. Очень часто такими инфекционными агентами являются микроорганизмы, передающиеся половым путем, типа gonorrhea и chlamydia, которые, проникая в верхний отдел репродуктивного тракта, вызывают воспалительные заболевания органов малого таза (ВЗОТ). Результатом этого могут быть хронические тазовые боли, эктопические беременности, нарушения менструального цикла, бесплодие в результате повреждения фаллопиевых труб и длительно протекающих хронических эндометритов.
Следует отметить, что серьезным осложнением инфицирования верхнего отдела репродуктивного тракта является эктопическая беременность, которая требует оперативного вмешательства, поскольку может вызвать смерть женщины.
Профилактика
Самая лучшая стратегия по ограничению вредного воздействия инфекций репродуктивного тракта — это предотвращение нового
инфицирования, т. е. их профилактика. Пути профилактики зависят от пути инфицирования.
Профилактика инфекций, передающихся половым путем, делится на первичную и вторичную.
Первичная профилактика заключается в изменении сексуального поведения, в первую очередь это сексуальное воздержание и задержка полового дебюта, а также уменьшение числа половых партнеров, пропаганда моногамного образа жизни, использование барьерных методов контрацепции.
Вторичная профилактика заключается в быстром выявлении и лечении инфицированных, своевременной диагностике асимпто-матических инфекций, лечении половых партнеров.
Профилактика эндогенных инфекций состоит в ликвидации факторов, которые способствуют их развитию. В частности, исключить применение вагинального душа, использование низкодозиро-ванных оральных контрацептивов, устранить риск иммунодефицита. Эндогенные инфекции легко диагностируются и лечатся оральными антимикробными или местными интравагинальными кремами. И хотя они не являются инфекциями, передающимися половым путем, у половыхпартнеров может наблюдаться некоторый дискомфорт, связанный с кандидозом. Поэтому иногда мужчины проходят лечение, что является профилактикой реинфекции у женщин. Следует отметить, что в случае отсутствия лечения эндогенные инфекции могут быть потенциальными причинами осложнений, таких как преждевременный разрыв плодных оболочек и преждевременные роды при беременности. Бактериальный ваги-ноз может приводить к воспалительным процессам органов малого таза, а также ассоциируется с увеличением частоты гетеросексуальной и перинатальной передачи ВИЧ-инфекции.
Профилактика ятрогенных инфекций состоит в использовании медицинского инструментария после соответствующей стерилизации, выявлении и лечении инфекций нижнего репродуктивного тракта перед проведением трансцервикальных манипуляций.
Выводы
1.В настоящее время инфекции репродуктивного тракта из-за широкой распространенности и тяжести осложнений рассматриваются как серьезная и глобальная проблема здоровья женщин и мужчин, семьи и общества.
2. Инфекции репродуктивного тракта являются причиной многочисленных серьезных осложнений у женщин: воспалительные заболевания органов малого таза, бесплодие, эктопическая беременность, синдром хронической тазовой боли.
3. Инфекции репродуктивного тракта во время беременности могут быть причиной внутриутробного инфицирования и осложнений течения беременности.
4. Некоторые инфекции могут увеличивать возможность передачи ВИЧ-инфекции.
5. Инфекции репродуктивного тракта, в зависимости от пути передачи, подразделяют на три типа: инфекции, передающиеся половым путем, эндогенные инфекции и ятрогенные инфекции.
6. По месту локализации инфекции репродуктивного тракта подразделяют на два вида: инфекции верхнего отдела репродуктивного тракта и инфекции нижнего отдела репродуктивного тракта.
7. Самая лучшая стратегия по ограничению вредного воздействия инфекций репродуктивного тракта — это предотвращение нового инфицирования, т. е. профилактика, которая зависит от пути инфицирования.

Общие сведения
Частота регистрации ИСМП в разных странах варьирует в широких пределах. Так, в РФ этот показатель составляет 1-1,5% (40-60 тыс. случаев/год), США — 3-5 % (2,5 млн. случаев/год), Великобритании — 5-6 %, Германии —3,5 %, Китае — 7-8 %. Однако, эти показатели, особенно в странах СНГ и, в частности, России не отражают реальную эпидемиологическую ситуацию. Результаты научных исследований ведущих специалистов-эпидемиологов РФ свидетельствуют, что реальное количество ИСМП составляет в среднем около 10% и находится на уровне 2-2,5 миллионов случаев/год. Присоединение ИСМП к основному заболеванию увеличивает продолжительности лечения (пребывания в стационаре) пациента на 7-10 дней, а прямые затраты лечебных учреждений на 65-85 млрд рублей в год. Летальность при различных нозологических формах ИСМП варьирует в пределах 3,5-35%.
Наибольший удельный вес ИСМП приходится на хирургические и акушерские стационары (отделения травматологии, урологии, реанимации, абдоминальной хирургии, гинекологии, ожоговой травмы, стоматологии, отоларингологии, онкологии). Наиболее драматичны проявления ИСМП в отделениях интенсивной терапии и реанимации, где они в различных нозологических формах регистрируются в 25-30% случаев.
Патогенез
Патогенез внутрибольничных инфекций существенно различается и определяется видом заболевания, этиологическим фактором (видом возбудителя, факторами его вирулентности), механизмом и путями передачи инфекции.
Классификация
Прежде всего, различают две больших группы ИСМП (рис. ниже):
- Экзогенная инфекция — обусловлена заражением пациента инфекционным агентом в условиях посещения/нахождения в ЛПУ.
- Эндогенная инфекция — инфекции, вызванных условно-патогенными микроорганизмами, вегетирующими в пищеварительном тракте, на кожных и слизистых покровах, которые при неблагоприятных условиях становятся патогенными. В структуре ВБИ роль эндогенной инфекции незначительна.
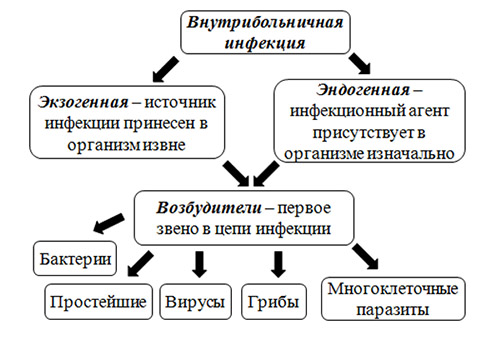
Группы и этиологический фактор ИСМП
В основу классификации ВБИ положены различные факторы. В зависимости от путей/факторов передачи различают воздушно-капельные, контактно-бытовые, контактно-инструментальные, постоперационные, постинфекционные, постэндоскопические, послеродовые, посттрансфузионные, постдиализные, посттравматические, постгемосорбционные и другие инфекции.
В зависимости от степени распространения инфекции различают:
- Генерализованные: бактериемия, септицемия, септикопиемия, токсико-септическая инфекция.
- Локализованные инфекции, включающие:
- Респираторные инфекции (ОРЗ, бронхит, плеврит, пневмония, легочный абсцесс и др.).
- Инфекции подкожной клетчатки/кожи (послеожоговые, послеоперационные, послетравматические), дерматомикозы, постинъекционные — абсцессы/флегмоны подкожной.
- Стоматологические инфекции (абсцесс, стоматит).
- ЛОР-инфекции (ринит, отиты, синуситы, ангина, ларингит, фарингит).
- Урологические инфекции.
- Инфекции пищеварительного тракта (энтерит, колит, гастроэнтероколит, холецистит, гепатиты др.).
- Постоперационные инфекции (перитонит, абсцессы брюшины).
- Инфекции глаза (конъюнктивит).
- Инфекции урологической и половой системы (пиелонефрит, уретрит, цистит, бактериурия, эндометрит, сальпингоофорит).
- Инфекции костно-cуставного аппарата (остеомиелит, бурсит, артрит).
- Инфекции сердечно-сосудистой системы (миокардит, эндокардит, перикардит, инфекции артерий и вен).
- Инфекции ЦНС (менингит).
- По характеру течения: острые, подострые, хронические. По тяжести течения: легкие, тяжёлые и среднетяжелые.
Причины
Этиологическим фактором ИСМП может быть чрезвычайно широкий спектр микроорганизмов (около 250 видов), принадлежащих к разным таксономическим группам: бактерии, вирусы, простейшие, грибы. При этом, инфекционным агентом могут быть патогенные, условно-патогенные микроорганизмы, а в ряде случаев и сапрофитная микрофлора. Наибольшей удельный вес в этиологической структуре ИСМП принадлежит возбудителям гнойно-септических инфекций (80-85%), кишечных инфекций (8-10%), вирусам гепатитов В, С, D (6-7%), инфекции дыхательных путей (2-3%). В целом, структура ВБИ изменчива и зависит преимущественно от профиля отделения/вида стационара и микробного пейзажа конкретного лечебного отделения (рисунок ниже).
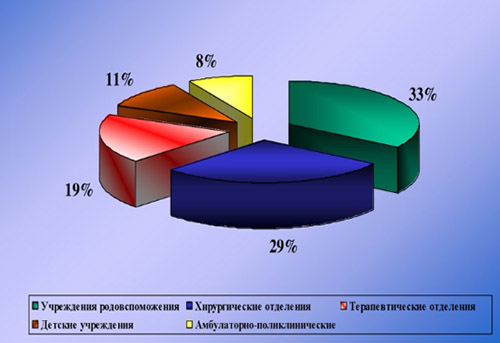
К возбудителям ВБИ, имеющими наибольшее значение относятся:
- грамположительная флора: стафилококки (золотистый, эпидермальный), стрептококки (пневмококк, энтерококк, пиогенный стрептококк);
- грамотрицательная флора: энтеробактерии (эшерихия, сальмонелла, шигелла, синегнойная палочка, клебсиелла, протей, иерсиния).
- вирусы (аденовирусной инфекции, простого герпеса, кори, ветряной оспы, гриппа, парагриппа, респираторно-синцитиальной инфекции, эпидпаротита, ротавирусы, риновирусы, энтеровирусы, возбудители вирусных гепатитов);
- грибы (рода Candida, аспергиллы).
Значимость различных видов ИСМП во многом определяется профилем ЛУ. Так, в гинекологических и родильных отделениях ведущую роль играет стафилококковая инфекция (золотистый стафилококк), кишечная палочка, энтерококки, диплоидный грибок (молочница); в ожоговых стационарах — синегнойная инфекция; в урологических отделениях — грамотрицательная микрофлора: кишечная, синегнойная палочка; в детских отделениях — вирусы краснухи, кори, эпидемического паротита, ветряной оспы.
Формирование госпитального штамма (с приобретенной устойчивостью) обеспечивается за счет их преимущества (доминирования) перед другими представителями микробной популяции. Основными отличиями госпитального штамма микроорганизма от стандартного являются: повышенная вирулентность (патогенность), формирующаяся за счет многократного пассажа через организм больных ЛПУ, высокая устойчивость к воздействию неблагоприятных факторов (дезинфектантам, антисептикам, химиопрепаратам, применяемым в конкретном мед. учреждении) и способность к длительному выживанию, постоянная циркуляция в среде больничного стационара среди больных и персонала.
Основную массу всех форм ВБИ (около 80%) составляют:
- инфекции мочевыделительной системы;
- ОРЗ и вентилятор-ассоциированные пневмонии;
- послеоперационные раневые гнойно-септические инфекции;
- кожные инфекции;
- интраабдоминальные инфекции;
- ангиогенные катетер-ассоциированные инфекции.
Любая нозологическая форма ВБИ развивается только при наличии всех звеньев эпидемического процесса: источника инфекции, механизма (факторов) передачи и восприимчивого организма человека.
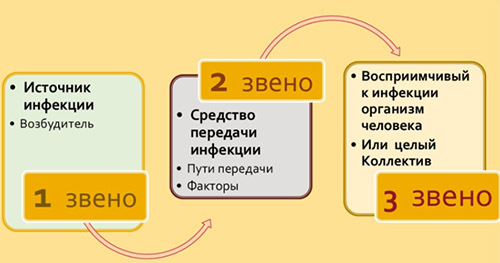
Основные источники внутрибольничной инфекции:
- больные и носители, находящиеся в стационаре;
- персонал лечебных учреждений;
- лица, ухаживающие за больными и посетители стационаров (студенты, лица, навещающие пациентов).
Аэрогенный — процесс заражения осуществляется через воздушную среду. Выделяют:
- воздушно-капельный путь (этим путем возбудитель передается при большинстве ОРЗ, пневмониях) при разговоре, кашле;
- воздушно-пылевой путь (передаются заболевания, возбудитель которых устойчив во внешней среде — кишечные инфекции, туберкулез, зоонозы).
- Контактно-бытовой путь – инфекционный агент передается через грязные рук, предметы личной гигиены, игрушки, посуду.
- Пищевой (реализуется через зараженные продукты питания при нарушениях технологии приготовления или хранения готовых блюд и пищевых продуктов).
- Водный (через воду).
- Прямой — передача возбудителя непосредственно через физический контакт между резервуаром инфекции (инфицированный индивидуум/контаминированный предмет) с кожей, слизистой или раневой поверхностью восприимчивого организма человека.
- Непрямой — посредством механического переноса инфекционного агента через руки медицинского персонала, предметы обихода, инструменты и оборудование лечебного учреждения. Непрямой контакт является наиболее часто задействованным путем распространения. Этот путь передачи часто называют артифициальным (искусственным) или парентеральным путем передачи возбудителя, который реализуется путем проведения различных инвазивных манипуляций (инъекции, забор крови, инструментальные манипуляции, вакцинацию, местные/общие операции) или использовании специальной аппаратуры при проведении гемодиализа, ИВЛ.
- Гемоконтактный — передается через кровь при обширных хирургические вмешательствах, инфузионной терапии, программном гемодиализе.
Заболеваемость ИСМП носит преимущественно эндемический характер и обусловлена индивидуальными факторами риска и клиническими процедурами. Значительно реже ИСМП протекают в виде локальных эпидемий. Развитию эпидемических вспышек способствует несвоевременная диагностика стертых форм заболевания и выявление носителей инфекционных агентов, как среди поступающих пациентов, так и среди медицинского персонала, контаминация предметов общего пользования, систематическое нарушение методов асептики при выполнении инструментальных процедур.
Специфичны для каждого вида инфекционного возбудителя. Однако, в целом для большинства нозологических форм ИСМП определяющими факторами являются параметры, характеризующие организм хозяина:
- возраст (пожилой/старческий, дети — новорожденные и раннего возраста, особенно недоношенные, со сниженной сопротивляемостью организма и перенесшие родовую травму);
- пациенты, страдающие тяжелыми хроническими заболеваниями, с алиментарной дистрофией;
- длительно находящиеся в стационаре и особенно на постельном режиме;
- беременные/роженицы;
- пациенты, получающие лучевую/иммуносупрессивную терапию;
- имунноскомпрометированные лица;
- больные после обширных хирургических операций, получающие кровезаместительную/инфузионную терапию, с программным гемодиализом, находящиеся на ИВЛ.
Факторы риска ИСМП, связанные с предметами окружающей среды (загрязнение поверхностей, воздуха, воды в распространении инфекции) имеют меньшую значимость.
Возникновению и распространению ИСМП способствуют:
Симптомы
Симптоматика внутрибольничных инфекций определяется конкретной нозологической формой и симптомами основного заболевания, формой и тяжестью их течения, вирулентностью инфекционного агента и состоянием организма больного.
Анализы и диагностика
К ВБИ относятся случаи, отвечающие следующим критериям:
- Повторное поступление пациента в стационар с установленной инфекцией (с клиническими признаками, данными инструментальных и лабораторных методов исследовани — микробиологических, серологических и методов экспресс-диагностики), являющееся следствием предыдущей госпитализации.
- Период развития клинической симптоматики заболевания ВБИ после поступления в лечебный стационар должен составлять не менее 48 часов и более.
- Выявляется четкая взаимосвязь между симптоматикой заболевания и проведенными вмешательства инвазивного типа (после ингаляции, инъекций, перевязки и т.д.) или в ряде случаев — с выявленным источником инфекционного агента (поступивший больной со стертой формой заболевания/носитель) и фактором ее распространения.
Для точной диагностики заболевания и определения конкретного штамма возбудителя инфекции, требуется проведение лабораторных—бактериологических/серологических исследований различных биоматериалов (мазок из зева, мокрота, кровь, моча, кал, раневое отделяемое).
Лечение
Проблема лечения госпитальных инфекций представляет значительную трудность, что обусловлено неэффективностью большинства широко применяемых антибиотиков, в частности цефалоспоринов. Для лечения таких инфекций применяются карбапенемы (Меропенем, Дорипенем), имеющие широкий спектр антимикробной активности, в частности к микроорганизмам, устойчивым к пенициллинам/цефалоспоринам или в ряде случаев комбинированные лекарственные препараты пенициллинов с ингибиторами бета-лактамаз (Пиперациллин + Тазобактам, Тикарциллин, Амоксициллин-Клавуланат и др.).
Карбапенемы используются для лечения тяжелых нозокомиальных пневмоний и других инфекций верхних дыхательных путей; инфекций органов малого таза, гинекологических, абдоминальных, мочеполовых инфекций; кожи и мягких тканей; сепсиса. Однако, препараты этой группы могут вызывать побочные реакции в виде крапивницы, сыпи, диспепсических расстройств, поражения печени и почек, дисбактериоза.
При выявлении метициллинрезистентных штаммов золотистого стафилококка, являющегося частым возбудителем внутрибольничных резистентных стафилококковых инфекций для лечения, используются гликопептидные антибиотики (Ванкадицин, Тейкопланин-Тева, Ликованум, Таргоцид и др.), которые высокоактивны по отношению к грамположительным аэробным/анаэробным инфекционным агентам — стафилококкам, стрептококкам, пневмококкам, энтерококкам, клостридиям, листериям, коринебактериям и другим. Показаниями к назначению являются тяжелые инфекции, вызванные энтерококками, инфекционный эндокардит, ассоциированный с зеленящими стрептококками, менингит и пневмонии, вызванные пневмококком, катетер-ассоциированный сепсис, перитонит, антибиотик-ассоциированная диарея и других инфекций, угрожающих жизни. В ряде случае гликопептидные антибиотики сочетаются с цефалоспоринами 3 поколения (Цефтибутен, Цефиксим, Цефотаксим, Цефоперазон, Цефтазидим и др.) или фторхинолонами (Офлоксацин, Ципрофлоксацин, Пефлоксацин, Норфлоксацин, Левофлоксацин и другие).
Необходимо отметить, что спектр возбудителей внутригоспитальных осложнений, а также их антибиотикорезистентность существенно различаются в отделениях различного профиля, поэтому при выборе антибиотика следует ориентироваться на чувствительность выделенной микрофлоры к ним, в также учитывать эпидемиологическую ситуацию в каждом конкретном лечебном учреждении.
Кроме антибиотикотерапии назначается специфическое лечение при той или иной конкретной нозологической форме ВБИ с учетом клинических проявлений, тяжести течения, риска развития осложнений. В индивидуальном порядке проводится симптоматическое лечение. В качестве дополнительной терапии назначают иммуностимуляторы: интерферон; бактериофаги, витаминно- минеральные комплексы.
В настоящее время для борьбы с тяжелыми проявлениями ВБИ разработана стратегия деэскалационной терапии, базирующаяся на нескольких принципах:
- Безотлагательное начало проведения антибактериальной терапии.
- Выбор антимикробных препаратов (АМП) с учетом чувствительности микроорганизмов и способности проникать в ткани, при отсутствии таких данных — использование антибиотиков широкого спектра действия.
- Назначение высоких доз антибиотиков, подбираемых индивидуально.
Эта стратегия предполагает безотлагательное назначение стартового антибиотика широкого спектра действия (комбинации антибиотиков) с целью максимально полного охвата спектра вероятных возбудителей с последующим переходом на антибиотик, к которому отсутствует устойчивость согласно данным микробиологического исследования. Именно своевременная и адекватная антимикробная терапия является ключевым условием и благоприятным прогностическим фактором, увеличивающей вероятность благоприятного исхода заболевания.
4. Комбинация различных антибиотиков.
Внутрибольничные инфекции — Внутрибольничные инфекции … Википедия
Гнойные (гноеродные) инфекции — инфекции, сопровождающиеся развитием гнойного или серозно гнойного воспаления (нагноением). Г. и. наблюдаются во всех тканях и полостях тела. По локализации Г.и. разделяют на общие сепсис(см.), септикопиемия (см.) и местные. Важно помнить, что… … Словарь микробиологии
Внутриутробные инфекции — МКБ 10 P35.35. P39.39. МКБ 9 771 … Википедия
Микробиология клиническая – — раздел мед. микробиологии, исследующий микробиол. аспекты этиологии, патогенеза, иммунологии оппортунистических микробных заболеваний и разрабатывающий методы их микробиол. д ки, специфической терапии и профилактики. Объектами исследования М. к.… … Словарь микробиологии
Ятрогении — (греч. ятрос врач, генус происхождение) любые болезни и травмы, к рые возникают у пациентов и мед. работников в результате оказания мед. помощи. Проявления и причины Я. многообразны. В зависимости от причинного фактора их разделяют на психогенные … Словарь микробиологии
| Внутрибольничные инфекции | |
|---|---|
| МКБ-10 | Y 95 95. |
| MeSH | D003428 |
Внутрибольничные инфекции (также госпитальные, нозокомиальные) — согласно определению ВОЗ, любые клинически выраженные заболевания микробного происхождения, поражающие больного в результате его госпитализации или посещения лечебного учреждения (ЛПУ) с целью лечения, либо после выписки из больницы (например, раневая инфекция), а также больничный персонал в силу осуществления им деятельности, независимо от того, проявляются или не проявляются симптомы этого заболевания во время нахождения данных лиц в стационаре [1] .
Инфекция считается внутрибольничной, если она впервые проявляется через 48 часов или более после нахождения в больнице, при условии отсутствия клинических проявлений этих инфекций в момент поступления и исключения вероятности инкубационного периода [2] . На английском языке такие инфекции называются nosocomial infections, от др.-греч. νοσοκομείον — госпиталь (от νόσος — болезнь, κομέω — забочусь).
Госпитальные инфекции следует отличать от часто смешиваемых с ними смежных понятий ятрогенных и оппортунистических инфекций.
Ятрогенные инфекции — инфекции, занесенные при диагностических или терапевтических процедурах.
Оппортунистические инфекции — инфекции, развивающиеся у больных с поврежденными механизмами иммунной защиты [2] .
Содержание
История [ править | править код ]
Со времени учреждения первого родильного дома в XVII веке и вплоть до середины XIX века в европейских роддомах свирепствовала родильная горячка, во время эпидемий которой смертность уносила в могилу до 27 % рожениц [3] . Справиться с родильной горячкой удалось только после того, как была установлена ее инфекционная этиология и внедрены методы асептики и антисептики в акушерстве.
Примеры внутрибольничных инфекций [ править | править код ]
- Вентилятор-ассоциированная пневмония (ВАП)
- Туберкулез
- Инфекции мочевыводящих путей
- Госпитальная пневмония
- Гастроэнтерит
- Золотистый стафилококк
- Метициллин-резистентный золотистый стафилококк (MRSA)
- Синегнойная палочка
- Acinetobacter baumannii
- Stenotrophomonas maltophilia
- Ванкомицин-резистентные энтерококки
- Clostr > Эпидемиология [ править | править код ]
В США, по оценкам Центров контроля и профилактики заболеваний, около 1,7 миллиона случаев внутрибольничных инфекций, вызванных всеми типами микроорганизмов, приводят или сопутствуют 99 000 смертям ежегодно [4] .
В Европе, по результатам проведенных госпитальных исследований, смертность от внутрибольничных инфекций составляет 25 000 случаев в год, из них две трети вызваны грам-отрицательными микроорганизмами.
В России официально фиксируется около 30 тысяч случаев ежегодно, что свидетельствует о недостатках статистики [5] . Исследование, проведенное в 32 скоропомощных больницах страны, показало, что госпитальные инфекции развиваются у 7,6 процентов больных, находящихся на лечении в стационаре. Если учесть, что примерное количество пролеченных в стационарах в России составляет 31—32 миллиона пациентов, то госпитальных инфекций у нас должно быть 2 миллиона 300 тысяч случаев в год [6] .
Внутрибольничными агентами могут вызываться тяжёлые пневмонии, инфекции мочевыводящих путей, крови и других органов.
Для ВБИ характерны свои особенности эпидемиологии, отличающие её от классических инфекций. К ним относятся: своеобразие механизмов и факторов передачи, особенности течения эпидемиологического и инфекционного процессов, важная роль медицинского персонала ЛПУ в возникновении, поддержании и распространении очагов ВБИ.
Многие типы инфекций трудно поддаются лечению по причине антибиотикорезистентности, которая постепенно начинает распространяться и среди грам-отрицательных бактерий, опасных для людей во внебольничной среде [7] .
Для возникновения ВБИ необходимо наличие следующих звеньев инфекционного процесса:
- источник инфекции (хозяин, пациент, медработник);
- возбудитель (микроорганизм);
- факторы передачи[8] ;
- восприимчивый организм.
Источниками в большинстве случаев служат:
- медицинский персонал;
- носители скрытых форм инфекции;
- больные с острой, стёртой или хронической формой инфекционных заболеваний, включая раневую инфекцию.
Посетители стационаров очень редко бывают источниками ВБИ [1] .
Факторами передачи чаще всего выступают пыль, вода, продукты питания, оборудование и медицинские инструменты.
Ведущими путями заражения в условиях ЛПУ являются контактно-бытовой, воздушно-капельный и воздушно-пылевой. Также возможен парентеральный путь (характерно для гепатитов B, С, D и др.)
Механизмы передачи инфекции: аэрозольный, фекально-оральный, контактный, гемоконтактный [8] .

К факторам внутрибольничной среды, способствующим распространению ВБИ относятся:
- недооценка эпидемической опасности внутрибольничных источников инфекции и риска заражения при контакте с пациентом;
- перегрузка ЛПУ;
- наличие невыявленных носителей внутрибольничных штаммов среди медперсонала и пациентов;
- нарушение медперсоналом правил асептики и антисептики, личной гигиены;
- несвоевременное проведение текущей и заключительной дезинфекции, нарушение режима уборки;
- недостаточное оснащение ЛПУ дезинфекционными средствами;
- нарушение режима дезинфекции и стерилизации медицинских инструментов, аппаратов, приборов и т. д.;
- устаревшее оборудование;
- неудовлетворительное состояние пищеблоков, водоснабжения;
- отсутствие фильтрационной вентиляции.
Лица с повышенным риском заражения ВБИ:
- Больные:
- без определенного места жительства, мигрирующее население;
- с длительными недолеченными хроническими соматическими и инфекционными заболеваниями;
- не имеющие возможность получать специальную медицинскую помощь;
- Лица, которым:
- назначена терапия, подавляющая иммунную систему (облучение, иммунодепрессанты);
- проводятся обширные хирургические вмешательства с последующей кровезаместительной терапией, программный гемодиализ, инфузионная терапия;
- Роженицы и новорождённые, особенно недоношенные и переношенные;
- Дети с врождёнными аномалиями развития, родовой травмой;
- Медперсонал ЛПУ.
Этиология [ править | править код ]
Всего насчитывается более 200 агентов, которые могут быть причиной ВБИ. До появления антибиотиков основными из них были стрептококки и анаэробные палочки. Однако после начала клинического применения антибиотиков возбудителями основных ВБИ стали ранее непатогенные (или условно-патогенные) микроорганизмы: St. aureus, St. epidermidis, St. saprophiticus, Escherichia coli, Enterococcus faecalis, Enterococcus durans, Klebsiella sp., Proteus mirabilis, Providencia spp, Acinetobacter, Citrobacter, Serratia marcescens.
Так же установлено, что внутрибольничное инфицирование может быть связано с распространением ротавирусной, цитомегаловирусной инфекции, кампилобактера, вирусов гепатита B, С и D, а также ВИЧ-инфекции.
В результате циркуляции микроорганизмов в отделении происходит их естественный отбор и мутация с образованием наиболее устойчивого госпитального штамма, являющегося непосредственной причиной ВБИ.
Основные черты приспособления — это устойчивость к одному или нескольким антибиотикам широкого спектра действия, устойчивость в условиях внешней среды, снижение чувствительности к антисептикам [9] . Госпитальные штаммы очень разнообразны, в каждой больнице или отделении возможно появление своего характерного штамма со свойственным только ему набором биологических свойств.
Классификация [ править | править код ]
- В зависимости от путей и факторов передачи ВБИ классифицируют:
- Воздушно-капельные (аэрозольные);
- Вводно-алиментарные;
- Контактно-бытовые;
- Контактно-инструментальные;
- Постинъекционные;
- Постоперационные;
- Послеродовые;
- Посттрансфузионные;
- Постэндоскопические;
- Посттрансплантационные;
- Постдиализные;
- Постгемосорбционные;
- Посттравматические инфекции;
- Другие формы.
- От характера и длительности течения:
- Острые;
- Подострые;
- Хронические.
- По степени тяжести:
- Тяжелые;
- Средне-тяжелые;
- Легкие формы клинического течения.
- В зависимости от степени распространения инфекции:
- Генерализованные инфекции: бактериемия (виремия, микемия), септицемия, септикопиемия, токсико-септическая инфекция (бактериальный шок и др.).
- Локализованные инфекции
- Инфекции кожи и подкожной клетчатки (ожоговых, операционных, травматический ран, Постинъекционные абсцессы, омфалит,рожа, пиодермия, абсцесс и флегмона подкожной клетчатки, парапроктит, мастит, дерматомикозы и др.);
- Респираторные инфекции (бронхит, пневмония, легочный абсцесс и гангрена, плеврит, эмпиема и др.);
- Инфекции глаза (конъюнктивит, кератит, блефарит и др.);
- ЛОР-инфекции (отиты, синуситы, ринит, мастоидит, ангина, ларингит, фарингит, эпиглоттит и др.);
- Стоматологические инфекции (стоматит, абсцесс, др.);
- Инфекции пищеварительной системы (гастроэнтероколит, энтерит, колит, холецистит, гепатиты, перитонит, абсцессы брюшины и др.);
- Урологические инфекции (бактериурия, пиелонефрит, цистит, уретрит, др.);
- Инфекции половой системы (сальпингоофорит, эндометрит, др.);
- Инфекции костей и суставов (остеомиелит, инфекция сустава или суставной сумки, инфекция межпозвоночных дисков);
- Инфекции ЦНС (менингит, абсцесс мозга, вентрикулит и др.);
- Инфекции сердечно-сосудистой системы (инфекции артерий и вен, эндокардит, миокардит, перикардит, постоперационный медиастинит).
Профилактика [ править | править код ]
Профилактика внутрибольничных инфекций является сложным и комплексным процессом, который должен включать три составляющие:
- минимизация возможности заноса инфекции извне [источник?] .;
- исключение распространения инфекции между больными внутри учреждения;
- исключение выноса инфекции за пределы ЛПУ.
Лечение [ править | править код ]
В идеале следует назначить антимикробный препарат узкого спектра активности, который действует на конкретный микроорганизм, выделенный при микробиологическом исследовании. Однако, на практике внутрибольничная инфекция, особенно в первые дни, практически всегда лечится эмпирически. Выбор оптимальной схемы антимикробной терапии зависит от преобладающей микрофлоры в отделении и спектра её антибиотикорезистентности.
С целью снижения антибиотикорезистентности возбудителей следует практиковать регулярную ротацию антибактериальных препаратов (когда определённые антибиотики, используются в отделении для эмпирической терапии в течение нескольких месяцев, а затем заменяются следующей группой).
Внутрибольничная инфекция, вызванная грамположительными микроорганизмами, наиболее эффективно лечится ванкомицином, а отношении грамотрицательных бактерий наибольшей активностью обладают карбапенемы (имипенем и меропенем), цефалоспорины IV поколения (цефепим, цефпиром) и современные аминогликозиды (амикацин).
Из сказанного не следует делать вывод о том, что внутрибольничная инфекция поддаётся только вышеперечисленным средствам. Например, возбудители инфекций мочевыводящих путей сохраняют высокую чувствительность к фторхинолонам, цефалоспоринам III поколения и др.
Но серьёзная внутрибольничная инфекция, действительно, требует назначения карбапенемов или цефалоспоринов IV поколения, так как они обладают наиболее широким спектром активности и действуют на полимикробную флору, в том числе на полирезистентных грамотрицательных возбудителей и многих грамположительных микроорганизмов. Недостатком препаратов обеих групп является отсутствие активности в отношении метициллинрезистентных стафилококков, поэтому в тяжёлых случаях их приходится комбинировать с ванкомицином.
Кроме того, все указанные средства не действуют на грибковые патогенны, роль которых в развитии внутрибольничных инфекций существенно возросла. Соответственно, при наличии факторов риска (например, выраженный иммунодефицит) следует назначать противогрибковые средства (флуконазол и др.)
Рекомендации по эмпирическому лечению некоторых внутрибольничных грамотрицательных инфекций приведены в нижеследующей таблице.
имипенем, амикацин, ципрофлоксацин
При преобладании E.coli и Proteus spp. возможно применение цефалоспоринов III поколения, пиперациллина/тазобактам
В 90-е годы XX века было показано, что эффективность стартовой антибактериальной терапии оказывает непосредственной влияние на летальность госпитализированных больных. Летальность среди больных, получавших неэффективную стартовую терапию, была выше, чем у пациентов, которым назначали антибиотики, активные в отношении большинства возбудителей. Более того, в случае неадекватной стартовой терапии даже последующая смена антибиотика уже с учётом микробиологических данных не приводила к снижению летальности.
На основании этих данных была разработана концепция деэскалационной терапии. Суть её заключается в том, что в качестве стартовой эмпирической терапии, которую начинают сразу после установления диагноза, используют комбинацию антимикробных средств, действующих на всех возможных возбудителей инфекции. Например, карбапенем или цефепим сочетают с ванкомицином (плюс флуконазол) в зависимости от состава вероятных возбудителей.
Доводом в пользу комбинированной терапии служат:
- более широкий спектр активности;
- преодоление устойчивости, вероятность которой выше при применении одного препарата;
- наличие теоретических данных о синергизме определённых средств.
До начала применения антибиотиков необходимо провести забор образцов биологических жидкостей для микробиологического исследования. После получения результатов микробиологического исследования и клинической оценки эффективности лечения через 48—72 ч возможна коррекция терапии, например, отмена ванкомицина, если выявлен грамотрицательный возбудитель. Теоретически возможна смена всей комбинации на препарат более узкого спектра действия, хотя у тяжёлого больного, ответившего на терапию, любой врач предпочтёт оставить назначенные антибиотики.
Возможность внедрения деэскалационной терапии зависит от эффективной работы микробиологической службы и степени доверия к её результатам. Если возбудитель остаётся неизвестным, то эта концепция теряет смысл и может привести к ухудшению результатов лечения. Целесообразность деэскалационной терапии следует в первую очередь обсуждать у больных с серьёзными инфекциями, угрожающими жизни (например, вентилятор-ассоциированная пневмония, сепсис).
Следует учитывать, что обратный подход (то есть эскалация терапии) в подобных ситуациях может закончиться смертью больного ещё до получения результатов микробиологического исследования.
Читайте также:


