Эндопротез для берцовой кости
Онкологическое эндопротезирование единственная возможность сохранить хорошее качество жизни после удаления злокачественной опухоли костей. Остеосаркомой, саркомой Юинга, хондросаркомой болеют преимущественно подростки и лица молодого возраста. Имплантация эндопротеза позволяет им вести нормальную жизнь после выздоровления.
Установка импланта никак не влияет на эффективность противоопухолевого лечения.
Органосохраняющие операции как золотой стандарт
Хирургические вмешательства в онкоортопедии начали применять еще в 80-90х годах. Тогда врачи сохраняли нижнюю конечность по строгим показаниям. Эффективность противоопухолевого лечения довольно высока (пятилетняя выживаемость составляет 75-85%).
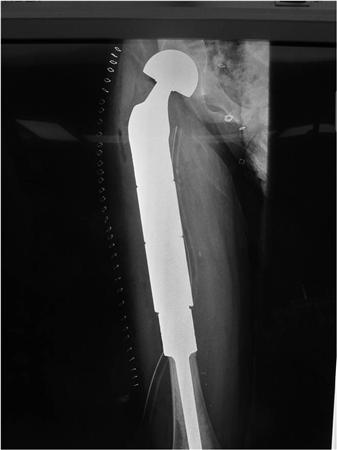
Онкологический имплант бедренной кости.
Эндопротезы устанавливают после удаления опухоли любого крупного сустава (коленного, тазобедренного, голеностопного, плечевого, локтевого). Пациентам со злокачественными новообразованиями плечевых, бедренных, большеберцовых костей выполняют их тотальное или диафизарное эндопротезирование — заменяя не сустав, а часть трубчатой кости.
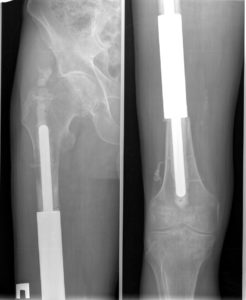
Суть онкологического эндопротезирования заключается в замене удаленных частей сустава искусственными имплантами. Это восстанавливает функции нижней конечности. Операция спасает в 85-90% случаев.
Противопоказания к хирургии
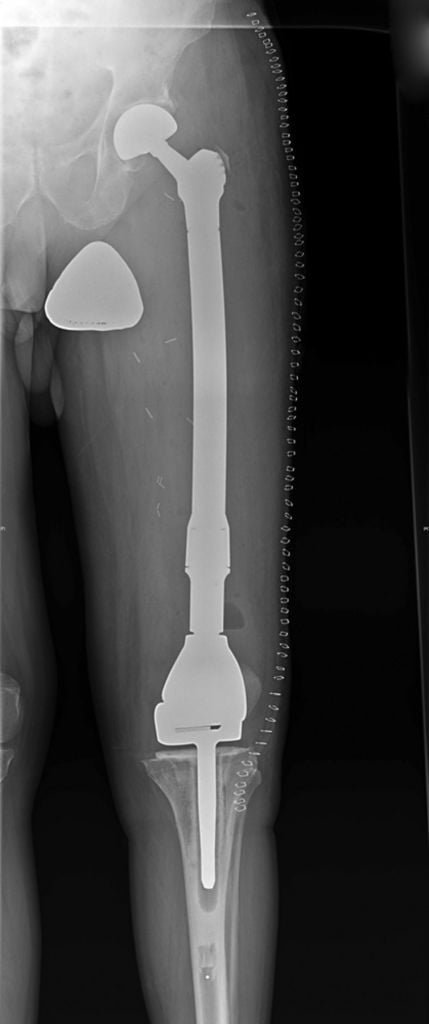
Операция по полной замене бедренной кости с имплантом коленного сустава.
Существует ряд ситуаций, когда ампутация ноги необходима. Иногда отказ от органосохраняющей операции спасает жизнь человека, а попытка сохранить нижнюю конечность приводит к его скорой гибели.
Абсолютные показания к ампутации:
- распад злокачественного новообразования;
- диссеминация (распространение) опухолевых клеток вследствие некачественно выполненной биопсии;
- поражения магистральных сосудов или нервов конечности.
Зачастую врачи рекомендуют ампутацию больным с патологическими переломами, осложнениями химиотерапии и тяжелыми поражениями жизненно важных органов, сопровождающимися декомпенсацией их функций. В этих случаях удаление нижней конечности дает человеку намного больше шансов.
Противопоказанием является невозможность сформировать мышечный футляр для импланта. Это ставит под угрозу приживление протеза и дает риск развития инфекционных осложнений.
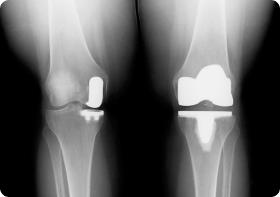
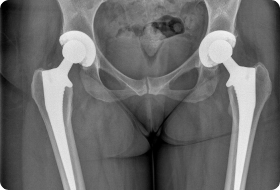
Особенности онкологического эндопротезирования
Если при обычной замене сустава врачи выполняют стандартную резекцию, то при злокачественных опухолях объем удаления костной ткани увеличивается. Врачам нужно подбирать особый имплант каждому больному. Онкологические эндопротезы имеют гораздо больший размер, чем ортопедические.
Таблица 1. Основные различия между онкологическим и обычным эндопротезированием.
| Традиционное | Онкологическое | |
| Предоперационная подготовка | Общеклинические и визуализирующие методы исследования. | Объемное обследование, включающее биопсию, ангиографию, сцинтиграфию, КТ, МРТ и другие нужные методы. |
| Особенности устанавливаемых эндопротезов | Стандартные моноблочные или модульные протезы с цементной или бесцементной фиксацией. | Модульные эндопротезы, форму и размер которых можно отрегулировать в ходе операции. Подобные мегапротезы могут полностью заместить удаленную фрагменты костей. |
| Ход операции | Больному удаляют деструктивно измененные части сустава, а на их место устанавливают эндопротез. | После полноценного обследования пациенту удаляют опухоль вместе с прилегающими тканями. Кости и сустав замещают протезом. Выполняют пластику мягких тканей нижней конечности. |
| Ожидаемые результаты | Полное восстановление функции сустава. Возможны осложнения, устранить которые можно консервативным или хирургическим путем. | Пятилетняя выживаемость после органосохраняющей операции составляет 80%. Онкологическое эндопротезирование позволяет восстановить функции сустава. Риск осложнений в этом случае выше, чем при выполнении обычной ортопедической операции. |
Обследование перед операцией
Перед началом лечения пациента тщательно обследуют. Это помогает выявить злокачественное новообразование, установить его локализацию и размеры.
- Рентгенография. Позволяет подтвердить наличие опухоли и ориентировочно оценить ее размеры. Не дает представления о состоянии магистральных сосудов, нервов, мягких тканей конечности.
- Сцинтиграфия костей скелета. Необходима для выявления метастазов злокачественного новообразования. Обнаруживает опухоли костей любой локализации.
- Биопсия. Наиболее точные результаты дает трепанационная и открытая биопсия. Пункционная и аспирационная менее информативны, поскольку в полученном в их ходе материале не всегда содержатся опухолевые клетки.
- КТ/МРТ. Детальный анализ структуры кости, оценить степень ее разрушения и состояние мягких тканей нижней конечности. Это помогает наиболее точно определить объем резекции и спрогнозировать результаты операции.
- Ангиография. Выявляет дефекты и опухолевые повреждения магистральных сосудов.
- Общеклинические исследования (общий анализ крови и мочи, биохимический анализ крови, ЭКТ, флюорография, УЗИ органов брюшной полости). Необходимы для оценки общего состояния пациента и выявления тяжелых сопутствующих заболеваний.
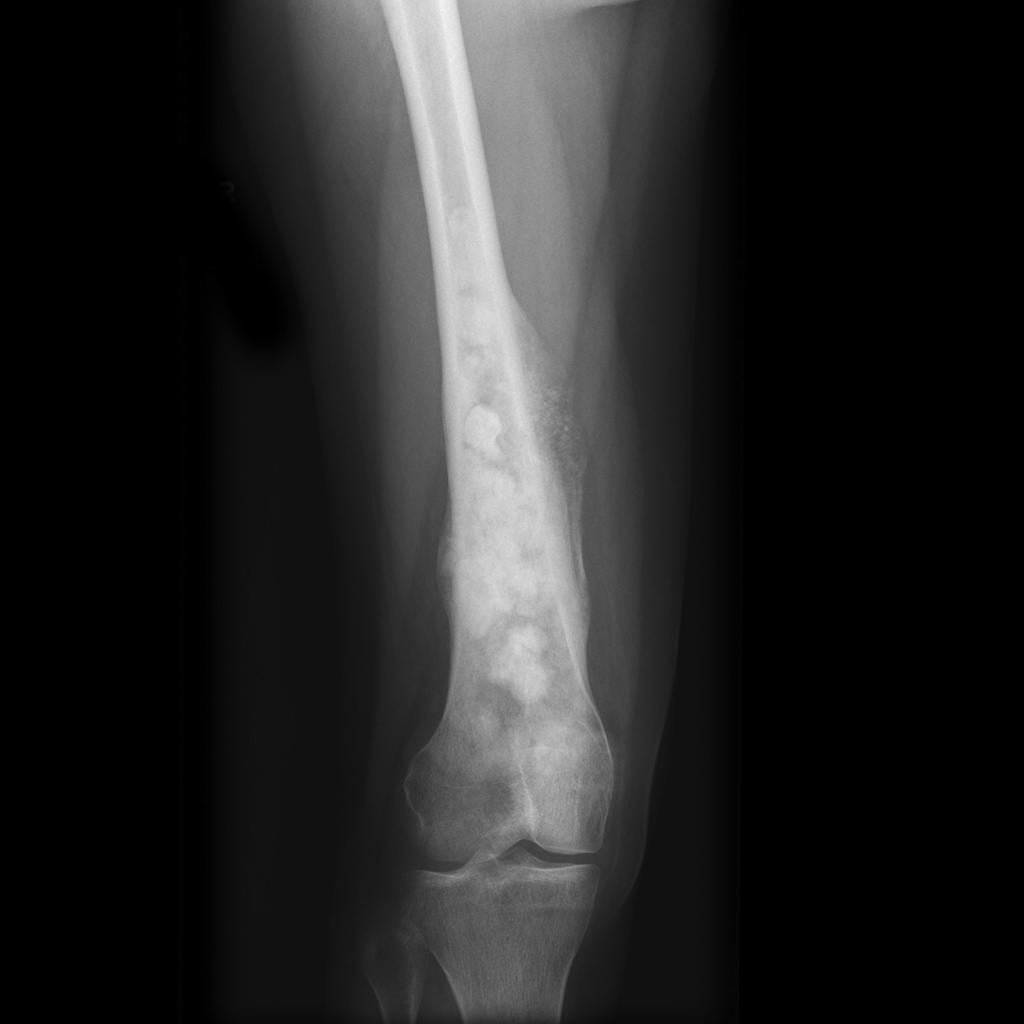
Остеосаркома на рентгене.
Комбинированное лечение опухоли
Для борьбы с опухолями костей используют химиотерапию, лучевую терапию и хирургическое лечение. Их умелое сочетание позволяет проводить органосохраняющие операции даже в тех ситуациях, в которых ранее ампутировали конечность. Химиотерапия позволяет нивелировать последствия перелома или неудачной биопсии.
Онкологические эндопротезы
Импланты, которые используются в онкоортопедии, обычно имеют гораздо больший размер. Это необходимо для замещения удаленных костных тканей. Логично, что мегапротезы нарушают биомеханику сустава, что приводит к нестабильности импланта. При опухолях нижней конечности пациентам могут замещать не только суставы, но и кости. Вид импланта зависит от локализации и размера злокачественного новообразования.
Виды онкологических протезов нижней конечности:
- заменяющие ТБС и часть бедренной кости;
- заменяющие коленный сустав и часть бедренной или большеберцовой кости;
- полностью замещающие бедренную кость;
- спейсеры – замкнутые эндопротезы коленного сустава;
- частично заменяющие и удлиняющие бедренную кость.

Основное отличие онкологических имплантов заключается в их массивности и сложности конструкции.
Производством онкологических протезов занимается несколько компаний: Stryker, ImplantCast, Biomet. Фирмы выпускают модульные эндопротезы, которые можно фиксировать цементным или бесцементным способом.
Особенностью модульных протезов является возможность собрать их во время операции. Это позволяет реконструировать дефекты костей любого размера. Применение модульных эндопротезов дает возможность избежать изготовления индивидуального импланта.
Неожиданные интраоперационные находки в онкологии нередки. Они вынуждают врачей удалять больше костной ткани, чем планировалось. Применение модульных протезов позволяет справиться с этой проблемой с минимальным ущербом для пациента. Чтобы заместить дефект, достаточно всего лишь раздвинуть эндопротез до нужного размера.
Любопытно! В онкоортопедии становятся все популярней эндопротезы с серебряным покрытием. Содержащиеся в нем ионы серебра оказывают антибактериальное действие и снижают риск развития инфекции.
Выполнение операции
Удаление костной ткани и установка протеза при злокачественных новообразованиях происходит совсем не так, как при обычном эндопротезировании. Во время хирургического вмешательства врачи придерживаются целого ряда правил.
Основные правила онкологического эндопротезирования:
- Соблюдение принципа футлярности. Злокачественную опухоль удаляют вместе с окружающими ее фрагментами здоровой костной ткани. Резекцию кости выполняют на расстоянии 5-6 см от новообразования. Вместе с опухолью удаляют зону предшествующей биопсии и все очаги возможной диссеминации.
- Соблюдение правил абластики и асептики. Во время хирургического вмешательства врачи тщательно следят за тем, чтобы опухолевые клетки не проникли в здоровые ткани. Чтобы избежать диссеминации, вначале перевязывают артерии и вены, а лишь затем иссекают опухоль. Параллельно с этим медработники проводят тщательную профилактику инфицирования операционной раны.
- Восстановление двигательной функции конечности. После установки протез прикрывают мышечными лоскутами и делают необходимую пластику. Это позволяет избежать развития инфекционных осложнений и некроза тканей в будущем.
- Адекватное послеоперационное ведение больных. Качественная реабилитация и правильное поведение пациента в послеоперационном периоде помогает восстановить функцию сустава и снизить риск возникновения непредвиденных осложнений.
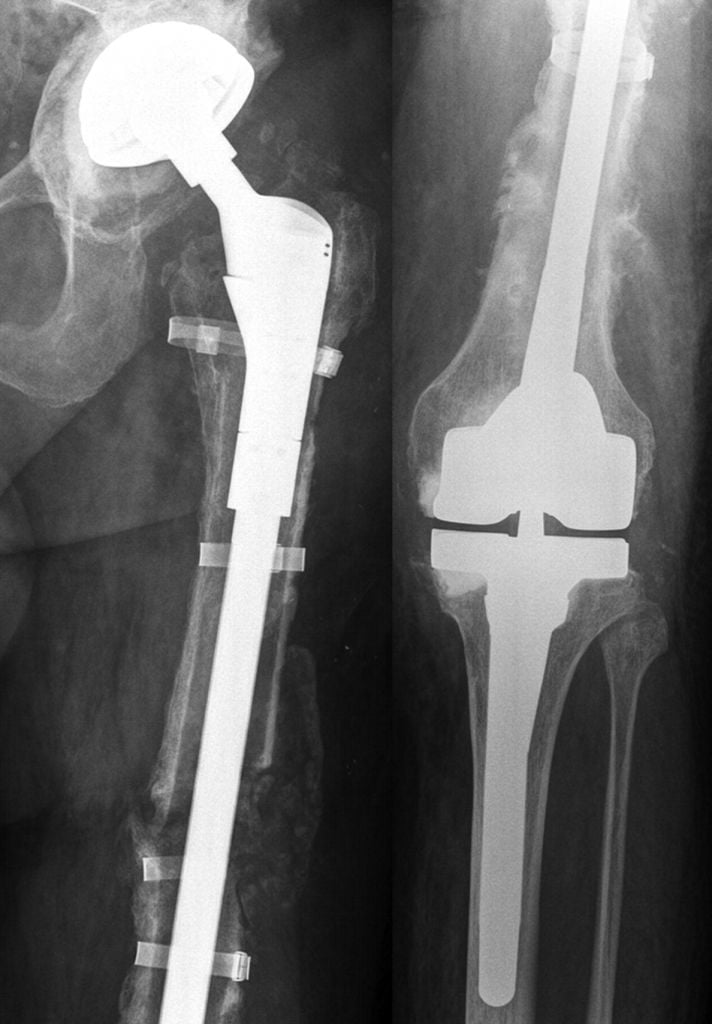
Массивный онкологический эндопротез ТБС.
Факт! Результаты органосохраняющей операции зависят от размера опухоли, степени ее злокачественности, поражения мягких тканей, сосудов и нервов конечности. Немалую роль в успехе лечения играет и внимательность, добросовестность и опытность врачей.
Процедура по замене коленного сустава — действенный способ восстановления подвижности конечностей, утерянной по ряду причин. Часто этот метод – единственное, что поможет при сильных травмах. Эндопротезирование практикуется, если консервативная терапия не дает результатов, а пациент испытывает сильную, непрекращающуюся боль, что негативно сказывается на психологическом состоянии.

На медицинском рынке нет недостатка в производителях, выпускающих коленные протезные устройства. Несмотря на единую цель – заменить больную кость, устранить болезненность, каждый из имплантатов имеет ряд отличий. Разработчики предлагают модели с различными функциями, размерами, уровнем активности пациента. Для успешности процедуры замены важно выбрать оптимальный протез.
Процесс выбора имплантата
Важно знать! Врачи в шоке: "Эффективное и доступное средство от боли в суставах существует. " Читать далее.
Проявите интерес к процессу подбора устройства, вживляемого в ваше тело. На рынке их представлено около 150 видов. Консультирующий хирург должен ответить на имеющиеся вопросы, подвести к выбору идеального протеза, соответствующего возрасту, весу, особенностям анатомии, активности пациента.
Производители обучают и поддерживают специалистов, применяющих на практике их продукты. Возможно, у оперирующего хирурга не будет опыта в установке выбранного вами приспособления.

Учитывайте, что некоторые виды устройств сочетаются только с определенными хирургическими методами. Если вы выбрали малоинвазивную хирургию, придется сузить выбор хирургов и доступных имплантатов.

- Делает доступным обычный диапазон движений;
- носится 15-20 и более лет;
- имеет отличные отзывы, используется на практике минимум 5-10 лет;
- отвечает вашему состоянию, потребностям, любым дополнительным требованиям (например, подходит для людей с аллергией на никель);
- бренд, стиль выбранного устройства знакомы оперирующему хирургу.

Естественный коленный сустав состоит из трех отсеков:
- медиального (внутренняя сторона колена);
- бокового (внешняя сторона);
- бедренного (под коленной чашечкой).
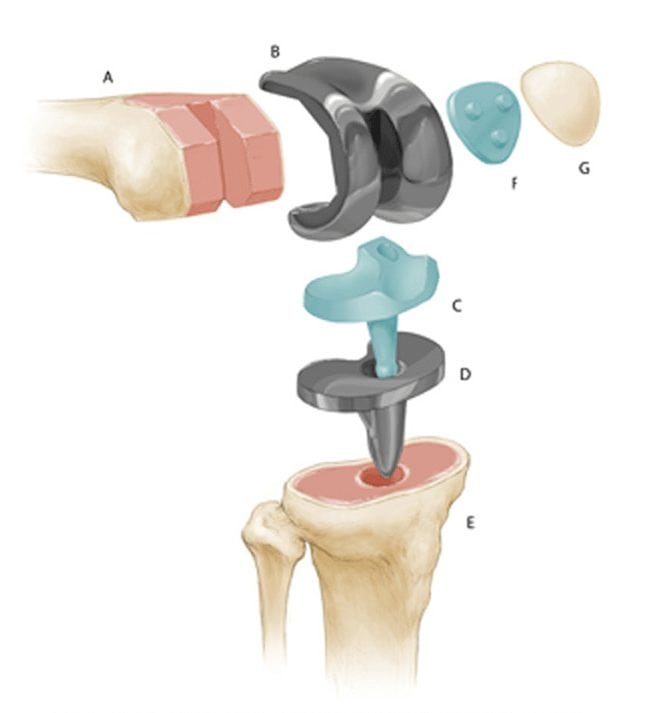
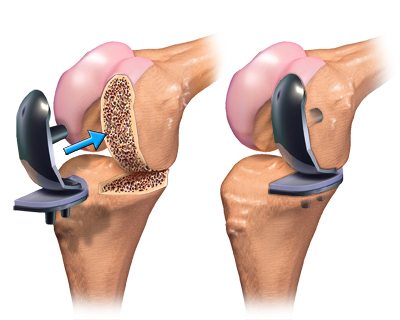
При полном эндопротезировании замене подлежат все три отсека, при частичном – только один из них. Большинство искусственных имплантатов состоят из четырех компонентов:
Частичное и полное эндопротезирование колена.
- Большеберцовый компонент. Плоский элемент, закрепляемый к верхней части голени. Изготавливается в виде металлической платформы с полиэтиленовой (пластиковой) вставкой. Материалом для изготовления — мягкий металл, например, титановый сплав.
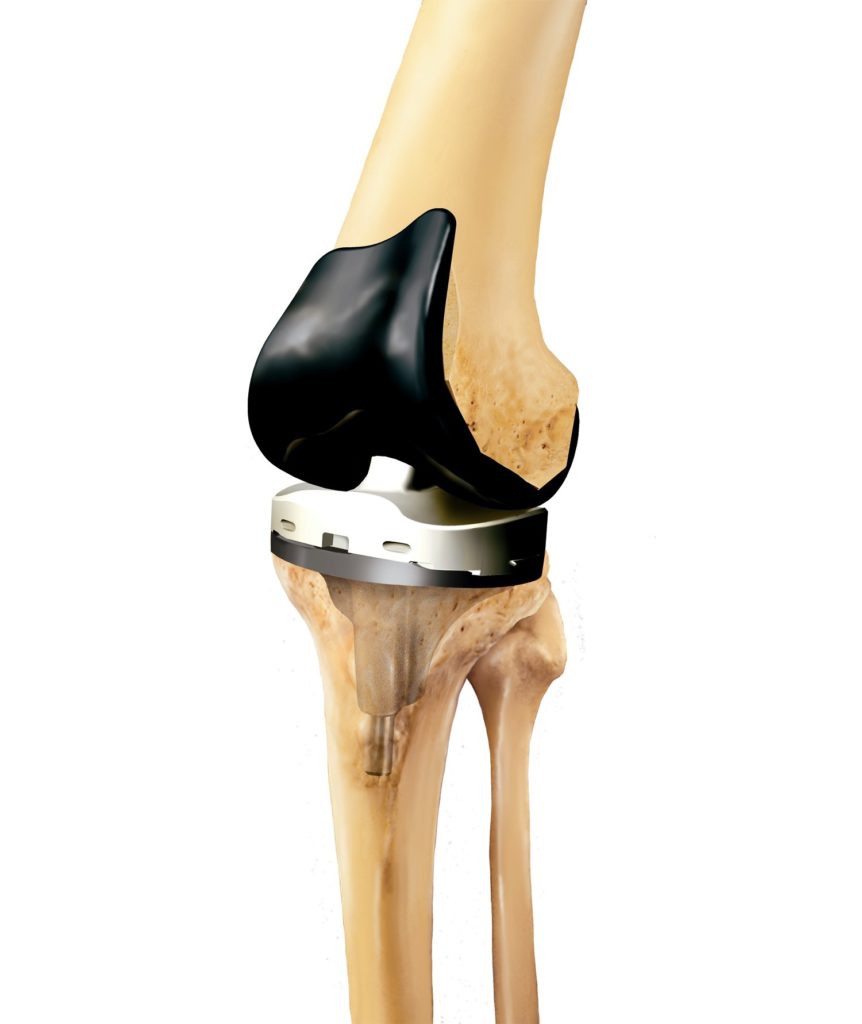
- Бедренный компонент – крупная, изогнутая часть имплантата, закрепляемая в бедренной кости. Изготавливается из металла или керамики, чаще из прочных сплавов кобальта и хрома, потому что эта часть участвует в большинстве движений.
- Коленный компонент – куполообразная часть, заменяющая поврежденную коленную чашечку, трущуюся о бедренную кость. Используется не при всех видах суставной хирургии, изготавливается из полиэтилена (прочного пластика).
- Пластиковая прокладка. Располагается между большеберцовой и бедренной частью. Изготавливается из пластика (полиэтилена). Эта гибкая распорка обеспечивает гладкую, скользящую поверхность для обновленного коленного сустава, позволяет ему изгибаться и гнуться.
Классификация эндопротезов
Существует целый ряд факторов, различающих коленные имплантаты между собой. Беседа с оперирующим хирургом поможет понять, какой из них подойдет вам.
- Протез с фиксированной опорой. Традиционный тип эндопротеза, используется для пожилых пациентов, ведущих малоактивный образ жизни. Большеберцовый компонент изготавливается из полиэтилена, прикрепляется к нижней металлической детали. Бедренный компонент обладает мягкой поверхностью. У пациентов с подобными имплантатами диапазон доступных движений расширяется на 20-50%;
- подвижный подшипниковый протез. Обеспечивают колену дополнительные градусы вращения по сравнению с предыдущим вариантом. Мобильность обеспечивается за счет полиэтиленовой вставки. Этот тип эндопротеза требует поддержки со стороны окружающих его мягких тканей, в том числе связок — так уменьшается риск вывиха. Исследования показывают примерно одинаковую эффективность обоих типов протезов, однако врачи предпочитают использовать эту разновидность для более молодых, активных пациентов. Процедура установки требует большого практического опыта хирурга.

Протезы могут различаться не только конструкцией, но и используемыми материалами. Большинство из них состоят из нескольких компонентов, различных по медицинскому классу.
Металлические части состоят из титана или кобальт-хромовых сплавов, известных своей прочностью, стабильными (инертными) химическими свойствами, отсутствием взаимодействия с человеческим телом.
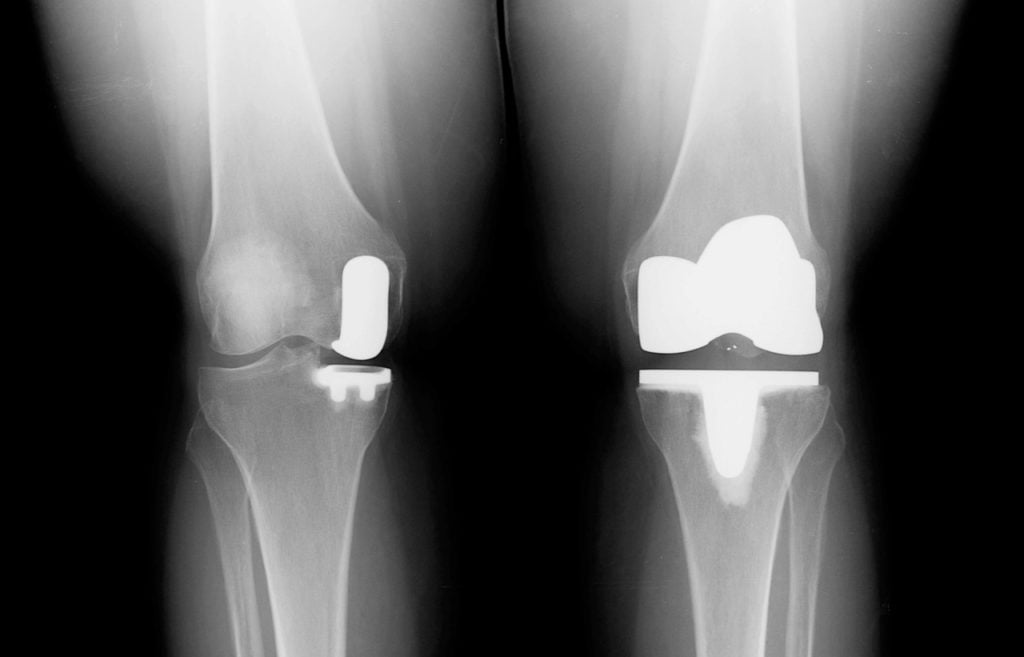
В ряде случаев у пациентов могут наблюдаться аллергические реакции на некоторые металлы.
Перед тем как лечь на хирургический стол, обязательно следует пройти диагностическое обследование, выявить общее состояние организма, наличие скрытых и явных аллергических реакций.
Полиэтилен с высокой молекулярной массой – распространенный материал для изготовления пластиковых компонентов. Его широкое распространение объясняется способностью плавного скольжения в пределах механического соединения, имитирующего естественные движения коленного сустава.

При выборе имплантата имеет значение биосовместимость. Важно, чтобы ваше тело не отвергало материалы, входящие в состав протеза. Искусственный элемент должен длительное время выдерживать вес и нагрузки тела, продолжая нормально сгибаться.
Даже "запущенные" проблемы с суставами можно вылечить дома! Просто не забывайте раз в день мазать этим.
В хирургии используется два основных метода, обеспечивающих фиксацию имплантата с костями, позволяя им двигаться, как единое целое:
- цементный. На эндопротезе есть поверхность, на которую накладывается специальный костный цемент для надежного сцепления с костями. Соединение успешно используется для всех типов замены коленного сустава. У некоторых молодых и более активных пациентов наблюдались проблемы ослабления цементного состава, однако этот материал в последнее время доработан и улучшен;
- бесцементный. Имплантаты имеют специальную текстурированную, пористую поверхность, через которую костная масса свободно прорастает во внутреннюю полость эндопротеза. Винты и штифты стабилизируют соединение, пока не произошло врастание. При установке приспособления требуется более длительный период восстановления. Не применяются для пациентов с остеопорозом, поскольку врастающая кость должна быть в хорошем состоянии.
Некоторыми хирургами используется гибридный метод с элементами обоих типов фиксации, однако он применяется при тазобедренном эндопротезировании.
Гендерные имплантаты
Производители разрабатывают имплантаты на основании усредненных размеров. Это обычно сужает выбор до 2-3 подходящих протезов. Однако некоторые компании, например, Zimmer и Biomet, производят модели, различаемые по признаку пола. По их словам, продукция позволяет учитывать и корректировать анатомические различия между мужчинами и женщинами.
Не существует убедительных доказательств большей эффективности гендерных эндопротезов. Многие эксперты уверены, что такой подход – не более чем маркетинговый ход, призванный повысить продажи.
Особенности устройств и их производители
По данным ВОЗ, частичное эндопротезирование колена подходит лишь 10% пациентов. Решение об оптимальном для вас методе лечения принимается хирургом.
Факторы, определяющие правильность выбора имплантата:
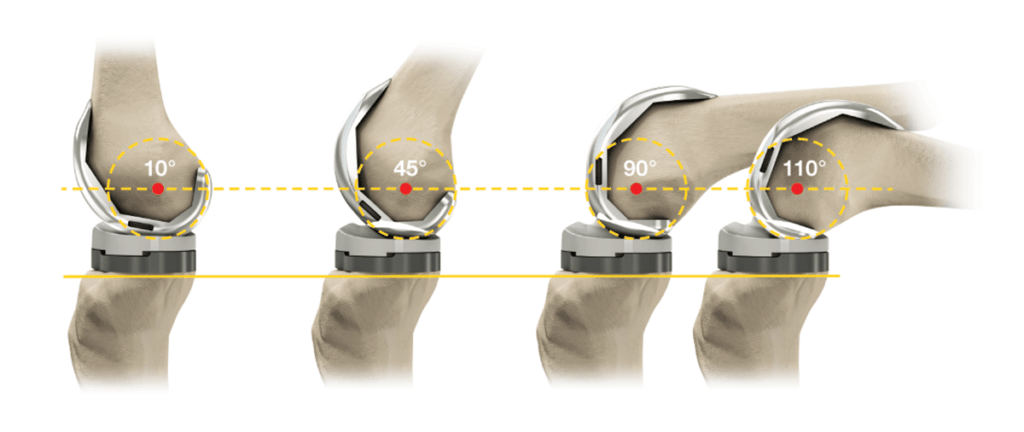
- доступный диапазон движений (максимальное сгибание, разгибание);
- настраиваемость (размер, форма, половые различия);
- стабильность;
- уровень активности пациента.
Обсудите с хирургом важные функции, уточните, какой именно тип устройства максимально отвечает потребностям, анатомии, типу заболевания. Решающие факторы — успешность эндопротеза, длительность его эксплуатации во врачебной практике и срок использования.

Срок службы эндопротеза
Срок эксплуатации искусственного коленного сустава составляет 10-30 лет. Зависит он от качества используемого материала, типа протеза, применяемой методики, периода реабилитации, соблюдения пациентом правил эксплуатации и предписаний врача, наличия повторных травм, веса пациента. Лучшие отзывы получили титановые сплавы; гарантийный срок таких протезов — 15-20 лет.
75% пациентов пользуются искусственным протезом на протяжении всей жизни без необходимости замены.
Онкологический эндопротез
Бедренная и большая берцовая кость часто становятся местом развития опухолей, онкологических заболеваний. Раньше такой диагноз считался однозначным противопоказанием к процедуре эндопротезирования, но производители разработали онкологические эндопротезы, обеспечивающие выдающиеся результаты даже при наличии обширных костных дефектов.
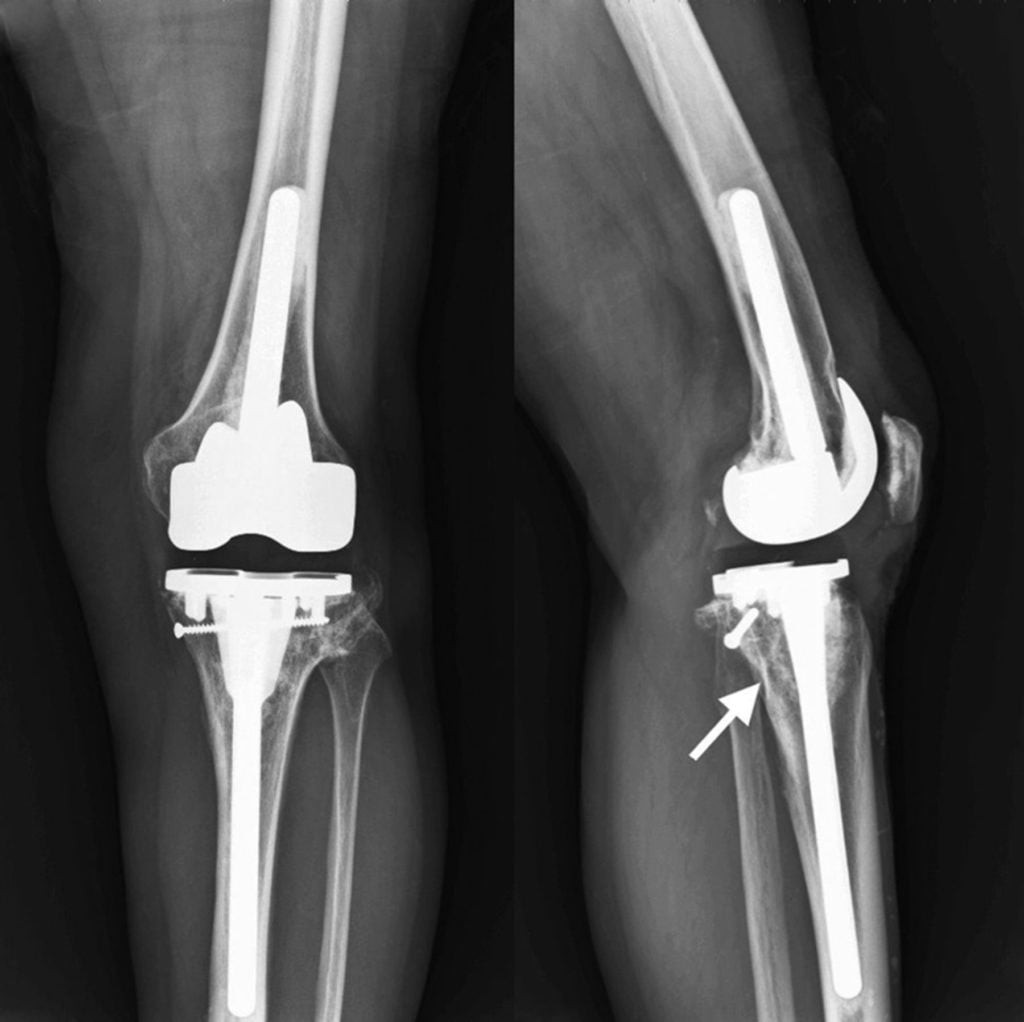
Костные отделы подвергаются резекции, заменяются на искусственные имплантаты. Если заболевание пациента носит злокачественный характер, устройства позволяют сохранить ему жизнь, вернуть подвижность.
Отечественные протезы
Говоря о российской практике эндопротезирования, отметим наличие ряда центров с опытными хирургами, проводящими свыше 1000 операций в год. Такой прорыв обеспечен федеральной программой финансирования операций. Поэтому утверждение, что хороших хирургов можно найти только за границей, не соответствует действительности.

К сожалению, нельзя то же самое сказать об имплантатах. Несмотря на проводимые разработки, отечественные эндопротезы уступают импортным по качеству, надежности, хотя остаются в одном с ними ценовом сегменте.
Подойдите к выбору подходящего имплантата ответственно, изучите информацию о доступных моделях, и вы обязательно подберете подходящий вид. Учитывайте мнение оперирующего хирурга, собственную активность, отзывы о предлагаемых моделях и успешности протезирования. При таком подходе продолжительный срок эксплуатации и ваше хорошее самочувствие гарантировано!
Как забыть о болях в суставах?
- Боли в суставах ограничивают Ваши движения и полноценную жизнь…
- Вас беспокоит дискомфорт, хруст и систематические боли…
- Возможно, Вы перепробовали кучу лекарств, кремов и мазей…
- Но судя по тому, что Вы читаете эти строки - не сильно они Вам помогли…
Но ортопед Валентин Дикуль утверждает, что действительно эффективное средство от боли в суставах существует! Читать далее >>>

По данным литературы, доля заболеваний коленного сустава среди всех случаев дегенеративно-дистрофических заболеваний суставов конечностей составляет от 21,9 до 29%, причем в 86% случаев страдают лица трудоспособного возраста, у которых прогрессирование заболевания в течение 10-15 лет приводит к инвалидности в 6,2-14,6% случаев [1]. Зачастую методом выбора при лечении пациентов с дегенеративно-дистрофическими заболеваниями суставов становится тотальное эндопротезирование. Одной из проблем, которую нужно решить в процессе тотального эндопротезирования сустава, это замещение костных дефектов в ложе эндопротеза. Их доля при заболеваниях коленного сустава составляет от 25 до 31% [2].
Причинами формирования дефектов и, как следствие, грубых деформаций являются:
- асептический некроз мыщелков, который, по данным различных авторов, составляет от 8 до 22% всех дегенеративно-дистрофических заболеваний коленного сустава,
- кистовидная перестройка эпифизов бедренной и большеберцовой костей,
- посттравматическая импрессия суставной поверхности 3.
Существует достаточное количество классификаций костных дефектов при первичном и ревизионном эндопротезировании коленного сустава [7]. Мы используем наиболее удобную, нашедшую широкое клиническое и научное применение классификацию AORI, разработанную G.A. Engh в Anderson Ortopaedic Research Institute (AORI США, 1997) [8]. Классификация основана на дооперационной рентгенологической оценке состояния костей, с помощью предварительно заданных критериев. В соответствии с этой классификацией выделяют четыре типа состояния бедренной или большеберцовой костей:
1 тип – интактная кость;
2А тип – повреждённая губчатая кость, кость противоположного мыщелка остается неизменной;
2В тип – симметричная потеря костной массы с вовлечением обоих мыщелков или плато;
3 тип – повреждение губчатой и кортикальной кости.
Классификация AORI достаточно четко показывает корреляцию наличия и размеров костных дефектов с ростом потребности использовать металлические блоки, клинья и/или структурированные трансплантаты. У данной методики существует лишь один минус. По современным данным, в группах I и IIA дефекты кости до 5 мм в 46% случаев посредством дооперационных рентгенограмм диагностированы не были [9].
При выполнении тотального эндопротезирования коленного сустава (ТЭКС) преследуется основная цель – создание долговременной надежной опоры для компонента эндопротеза. В случае имеющегося костного дефекта она может достигаться такими способами, как:
- резекция по дну дефекта,
- цементная пластика с армированием или без армирования,
- замещение металлическим блоком,
- костная аллопластика 10.
При детальном рассмотрении у каждого метода отмечаются свои преимущества и недостатки. Преимуществом замещения костного дефекта путем выполнения резекции по дну дефекта является простота и быстрота выполнения. Недостатком становится снижение количества ткани большеберцовой кости в дистальном направлении. Не исключена ситуация, что на максимальном вкладыше стабильность сустава не будет достигнута. Кроме того, при возникновении необходимости выполнения реэндопротезирования у этой группы пациентов хирург может столкнуться с такой проблемой, как обширный дефект большеберцовой кости. Таким образом, этот вариант замещения костного дефекта не является методом выбора. Его применение допустимо при неглубоких дефектах [12]. По нашим данным, резекция по дну дефекта выполнена у 5% пациентов с имеющимся костным дефектом.
Замещение костного дефекта путем цементной пластики с армированием или без армирования винтами также отличается простотой и дешевизной. Недостатки метода заключаются в том, что непросто добиться адекватной прессуризации цемента при нарушении целостности кортикальной кости. Изменение объема цемента во время полимеризации может достигать 2%. Неравномерное распределение нагрузки на подлежащую кость при эксцентрически действующих силах может приводить к нарушению прочности фиксации. Этот метод используется для замещения достаточно глубоких дефектов, при условии соблюдения правил прессуризации цемента и планирования вектора нагрузки [12]. По нашим данным, такое замещение выполнено у 82% пациентов с имеющимся костным дефектом.
Преимущество метода замещения костного дефекта путем костной аутопластики заключается в максимальном сохранении костной ткани метаэпифиза. К недостаткам метода относятся: существенные ограничения в выборе размера трансплантата, риск коллапса, если структура трансплантата повреждена патологическим процессом, и риск несращения. Метод применяется при наличии трансплантата с соответствующими характеристиками (размер, плотность). По нашим данным, такое замещение выполнено у 7% пациентов с имеющимся костным дефектом.
Достоинством замещения костного дефекта металлическим блоком или клином следует считать быстрое создание надежной опоры для имплантата, даже в условиях обширных дефектов. К недостаткам метода относятся ограничения по размеру и форме трансплантата, необходимость специальных инструментов и компонентов эндопротеза. Увеличивается общая стоимость имплантата. При наличии специального инструментария и соблюдении правил имплантации метод применим для замещения любых дефектов [12; 13]. По нашим данным, замещение костного дефекта этим методом выполнено у 6% пациентов.
Цель исследования: улучшить результаты первичного эндопротезирования коленного сустава у пациентов, имеющих костный дефект большеберцовой кости до 2А по AORI.
Материал и методы. В Новосибирском НИИТО за 2012-2015 годы выполнено 7096 операций первичного эндопротезирования коленных суставов. В 2157 (30,4%) случаях был диагностирован требующий замещения костный дефект как бедренной, так и большеберцовой кости [14].
С целью восстановления биомеханики коленного сустава и создания долговременной надежной опоры для компонентов эндопротеза у пациентов, имеющих костный дефект большеберцовой кости до 2А по AORI, нами разработан и внедрен в клиническую практику способ аутопластики большеберцовой кости при первичном эндопротезировании коленного сустава.
Данная методика выполняется соответственно стандартным этапам эндопротезирования, но имеет некоторые особенности: после выполнения резекции суставной поверхности большеберцовой кости определяется остаточный костный дефицит мыщелка большеберцовой кости. По классификации AORI для аутопластики допускается дефицит не больше T2А. При формирования межмыщелкового бокса бедренной кости производится одновременный забор аутокости. Производится обработка костного аутотрансплантата до придания ему правильной геометрической формы (рис. 1).
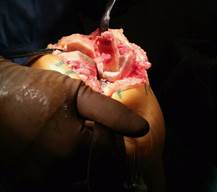
Рис. 1. Забор аутотрансплантата, придание ему правильной геометрической формы
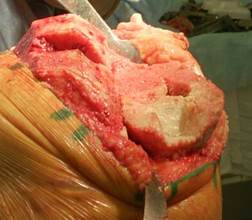
Рис. 2. Обработанный дефект большеберцовой кости со
сформированной опорной площадкой
В последующем аутотрансплантат устанавливается в сформированное ложе и производится импакция до фиксации (рис. 3).
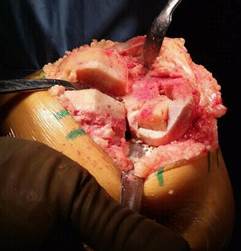
Рис. 3. Импакция аутотрансплантата в сформированном ложе
Дальнейший ход операции соответствует стандартным этапам при первичном эндопротезировании коленного сустава. Восстановительный период не имеет каких-либо особенностей по сравнению со стандартным течением [15].
Клинический пример. Пациент С., 65 лет. Диагноз: левосторонний посттравматический гонартроз 3 степени. Дефект медиального мыщелка левой большеберцовой кости. Варусная деформация левой нижней конечности. Комбинированная контрактура левого коленного сустава. Синдром левосторонней гоналгии (рис. 4).
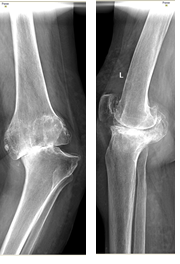
Рис. 4. Рентгенограмма коленного сустава в прямой и боковой проекциях
Пациенту проведено оперативное лечение: эндопротезирование левого коленного сустава с аутопластикой медиального мыщелка большеберцовой кости. Послеоперационный период протекал без особенностей, пациенту была проведена стандартная реабилитация.
На контрольных осмотрах через 6 месяцев, 1 и 2 года после проведенного хирургического лечения пациент отметил хороший результат проведенного лечения, выражающийся в увеличении объема движений в коленном суставе, повышении его стабильности и восстановлении нормальной оси конечности. На контрольной рентгенограмме коленного сустава через 2 года после операции аутотрансплантат состоятелен (рис. 5).
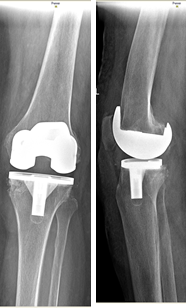
Рис. 5. Контрольная рентгенограмма коленного сустава в прямой и
боковой проекциях через 2 года после операции
Таким образом, у пациентов, имеющих костный дефект большеберцовой кости 2А по AORI, при первичном эндопротезировании коленного сустава выполнение аутопластики по разработанной методике приводит к хорошим результатам, выражающимся в создании долговременной надежной опоры для компонентов эндопротеза, что увеличивает срок его службы за счет нормализации распределения нагрузок в прооперированном коленном суставе.
1. При первичном эндопротезировании коленного сустава максимальное сохранение костной ткани облегчает хирургическую тактику при последующих хирургических вмешательствах, что очень важно у молодых пациентов.
3. Аутопластика должна выполняться при отсутствии противопоказаний.
Читайте также:


