Инфекции в свежезамороженной плазме
Плазму можно получить:
• фракционированием дозы консервированной крови методом центрифугирования;
• на сепараторах (автоматический аферез);
• фильтрацией консервированной крови через специальные мембраны, задерживающие клеточные элементы;
• путем спонтанного оседания клеточной массы крови под действием силы тяжести (малоэффективен и практически не используется).
Из одной стандартной дозы крови — 450—500 мл получают 200—250 мл плазмы. Различаются два вида плазмы: нативная и свежезамороженная.
Практически всю плазму получают из консервированной крови в пределах 6 ч после забора крови. Полученная плазма сразу же подвергается глубокому замораживанию при температуре —45 °С. При —30 °С СЗП может храниться до одного года. Такие условия позволяют сохранить с минимальными потерями факторы V и VIII, а также другие неустойчивые факторы свертывающей системы крови.
Нативная плазма, так же как и СЗП, содержит весь комплекс стабильных и лабильных факторов гемостаза, фибринолиза, системы комплемента и пропердина, разномолекулярные белковые комплексы, обеспечивающие онкотическое давление; антитела и другие факторы, составляющие иммунологическую часть крови.
Белки плазмы обладают высокой иммуногенностью, что может явиться причиной сенсибилизации больных, особенно в результате многократных трансфузий. В период или непосредственно после трансфузии СЗП у больных, сенсибилизированных к белковым комплексам плазмы, могут возникнуть осложнения в виде анафилактических трансфузионных реакций. Больные с дефицитом иммуноглобулина А в этом отношении должны находиться под особым наблюдением, поскольку входят в группу повышенного риска предрасположенности к анафилактическим реакциям.
В рамках анализа лабораторных показателей в трансфузии СЗП нет необходимости (стандарты американских патологов, 1994) при условии, что:
• протромбиновое время превышено не более чем в 1,5 раза (> 18 с) среднего нормального показателя;
• активированное парциальное протромбиновое время (АПТВ) превышено не более чем в 1,5 раза верхней границы нормы (> 50-60 с);
• выявляется менее 25 % активности фактора свертывания. При назначении СЗП необходимо помнить, что:
• не определена эффективность СЗП у больных с тяжелым заболеванием печени при активном кровотечении;
• не определена роль трансфузии СЗП у больных, оперированных на печени, в послеоперационном периоде;
• СЗП не может корригировать коагуляционные нарушения, связанные с тяжелыми заболеваниями печени;
• в целях купирования кровотечения у больных с поражением печени необходимы большие объемы СЗП — не менее 5 доз;
• СЗП малоэффективна при лечении иммунодефицитных состояний;
• одна доза СЗП для лечения взрослого больного во многих случаях малоэффективна;
• СЗП не должна назначаться профилактически без лабораторных исследований;
• СЗП поддерживает коагуляционные тесты в нормальных границах у больных с дефицитом факторов XI, VII, V, протеина С, протеина S, антитромбина III (AT-III).
При лечении тромботической тромбоцитопенической пурпуры рекомендуется плазмообмен с замещением СЗП.
Гиповолемия не требует трансфузий СЗП. Безопаснее, дешевле и доступнее в этих случаях инфузии коллоидных кровезаменителей в сочетании с кристаллоидами и (или) растворов альбумина. При отсутствии активного кровотечения больной не должен получать СЗП, если протромбиновое время не более чем на 3 с выше верхней границы нормы.
Число патологических состояний, при которых установлена эффективность трансфузий СЗП, весьма велико. СЗП обладает большой лечебной эффективностью при кровотечениях и кровоточивости, вызванных дефицитом комплекса свертывающих факторов, коагулопатиями.
В нашей стране в условиях недостаточного количества специфических концентрированных компонентов плазмы, соответствующих фармакологических препаратов трудно переоценить значение трансфузий СЗП как эффективного лечебного средства при ряде заболеваний. Особо следует отметить следующее обстоятельство — основная масса данных об эффективности СЗП была получена в тот период, когда на рынке отсутствовали факторы гемостаза в виде лекарственных препаратов. В настоящее время в большинстве из перечисленных случаев при наличии препаратов плазмы (белковых и специфических концентратов факторов свертывания) и кровезаменителей использование СЗП можно ограничить, а в ряде случаев предпочтительно обойтись без трансфузий плазмы.
К процедуре гемотрансфузии (переливанию крови, плазмы) нельзя относится беспечно. Для того чтобы манипуляция принесла ожидаемую терапевтическую пользу, важно правильно подобрать донорский материал и подготовить реципиента.
Успешность проведения данной манипуляции зависит от ряда незаменимых факторов. Весомую роль играет тщательность предварительной оценки показаний к гемотрансфузии, правильная поэтапность выполнения операции. Несмотря на развитие современной трансфузиологии, со стопроцентной долей вероятности исключить риск такого последствия переливания плазмы крови, как летальный исход, невозможно.
Вкратце об истории манипуляции
В Москве, начиная с 1926 года, функционирует НМИЦ гематологии – ведущий научный центр России. Оказывается, первые попытки переливания крови были зафиксированы еще в средневековье. Преимущественная часть из них успехом не увенчалась. Причиной тому можно назвать практически полное отсутствие научных знаний в области трансфузиологии и невозможность установления групповой и резус-принадлежности.

Переливание плазмы крови при несовместимости антигенов обречено на смерть реципиента, поэтому в наши дни от практики введения цельной крови врачи отказались в пользу имплантации ее отдельных составляющих. Этот метод считается более безопасным и эффективным.
Риски для реципиента
Даже если переливание крови чем-то напоминает введение физраствора или медикаментов капельным путем, эта процедура является более сложной. Гемотрансфузия – это манипуляция, приравненная к трансплантации биологической живой ткани. Имплантируемые материалы, в том числе и кровь, содержат множество разнородных клеточных составляющих, которые несут чужеродные антигены, белки, молекулы. Идеально подобранная ткань ни при каких условиях не будет идентичной с тканями пациента, поэтому риск отторжения присутствует всегда. И в данном смысле ответственность за последствия переливания плазмы крови лежат исключительно на плечах специалиста.
Любое вмешательство несет в себе риски, не зависящие ни от квалификации врача, ни от предварительной подготовки к процедуре. При этом на любом этапе переливания плазмы (пробы или непосредственной инфузии) недопустимо поверхностное отношение медперсонала к работе, спешка или отсутствие достаточного уровня квалификации. В первую очередь врач должен убедиться, что без этой манипуляции не обойтись. При наличии показаний к переливанию плазмы доктор должен быть уверен, что исчерпаны все альтернативные способы терапии.
Кому показана гемотрансфузия
Данная манипуляции преследует четкие цели. В большинстве случаев вливание донорского материала обусловлено необходимостью восполнения потерянной крови при обширных кровотечениях. Также гемотрансфузия может быть единственным способом повышения уровня тромбоцитов для улучшения показателей свертываемости. Исходя из этого, показаниями к переливанию плазмы крови являются:
- смертельно опасная кровопотеря;
- шоковое состояние;
- анемия тяжелой степени;
- подготовка к плановому хирургическому вмешательству, предположительно сопровождающемуся внушительными кровопотерями и осуществляемому с использованием приборов для искусственного кровообращения (операции на сердце, сосудах).
Эти показания являются абсолютными. Кроме них, послужить поводом к проведению гемотрансфузии может сепсис, заболевания крови, химическое отравление организма.
Переливание для детей
Возрастных ограничений к проведению гемотрансфузии нет. При объективной необходимости манипуляцию могут назначить и новорожденному. Переливание плазмы крови в раннем возрасте имеет аналогичные показания. Кроме того, при выборе метода лечения решение в пользу гемотрансфузии принимается в случае стремительного прогрессирования болезни. У детей первого года жизни переливание крови может быть вызвано желтухой, увеличением размеров печени или селезенки, а также повышением уровня эритроцитов.
Основным аргументов в пользу данной манипуляции считают показатель билирубина. Например, если у новорожденного он превышает 50 мкмоль/л (материал для исследований берут из пуповинной крови), за состоянием малыша начинают пристально следить, так как данное нарушение сигнализирует о необходимости введения донорской крови в ближайшем будущем. Врачи следят не только за показателями билирубина, но и за скоростью его накопления. Если она значительно превосходит норму, ребенку назначают гемотрансфузию.
Противопоказания
Определение противопоказаний — не менее важный этап в процессе подготовки к процедуре. Согласно правилам переливания плазмы крови, основными препятствиями к данной манипуляции относятся:
- сердечная недостаточность;
- перенесенный в недавнем прошлом инфаркт миокарда;
- ишемическая болезнь сердца;
- врожденные сердечные пороки;
- бактериальный эндокардит;
- гипертонический криз;
- острое нарушение мозгового кровообращения;
- тромбоэмболический синдром;
- отек легких;
- гломерулонефрит на стадии обострения;
- печеночная и почечная недостаточность;
- склонность к аллергии на множество раздражителей;
- бронхиальная астма.
В некоторых случаях, когда трансфузия – единственный способ сохранить больному жизнь, отдельные противопоказания могут игнорироваться. При этом ткани реципиента и донора с целью подтверждения совместимости должны пройти множество проб. Переливанию плазмы также должна предшествовать комплексная диагностика.
Донорская кровь для аллергиков
Биоматериал для трансфузии
В качестве жидкости для переливания могут быть использованы:
- цельная донорская кровь, что применяется крайне редко;
- эритроцитная масса, содержащая мизерное количество лейкоцитов и тромбоцитов;
- тромбоцитарная масса, которая может сберегаться не более трех дней;
- свежезамороженная плазма (к переливанию прибегают в случае осложненной стафилококковой, столбнячной инфекции, ожогов);
- компоненты для улучшения показателей свертывания.
- Внутривенное восполнение недостающих составляющих крови.
- Обменное переливание – часть крови реципиента заменяют донорской жидкой тканью. Данный метод актуален при интоксикациях, заболеваниях, сопровождающихся гемолизом, острой почечной недостаточностью. Чаще всего осуществляется переливание свежезамороженной плазмы.
- Аутогемотрансфузия. Подразумевается вливание собственной крови пациента. Такую жидкость собирают при кровотечениях, после чего материал очищают и консервируют. Такой вид гемотрансфузии актуален для больных с редкой группой, при которой возникают сложности с поиском донора.
О совместимости
Переливание плазмы или цельной крови подразумевает использование материалов одной группы, совпадающих по резус-принадлежности. Но, как известно, у любого правила есть исключение. Если подходящей донорской ткани нет, в экстренной ситуации больным с IV группой разрешено вводить кровь (плазму) любой группы. При этом важно соблюдать только совместимость резус-факторов. Еще одна интересная особенность касается крови I группы: пациентам, нуждающимся в восполнении объема эритроцитов, 0,5 л этой жидкой ткани могут заменить 1 л отмытых эритроцитов.
До начала процедуры персонал должен убедиться в пригодности трансфузионной среды, проверить срок годности материала, условия его хранения, герметичность емкости. Оценить важно и внешний вид крови (плазмы). Если в жидкости присутствуют хлопья, странные примеси, свертки, пленка на поверхности, вводить ее реципиенту нельзя. Перед непосредственным проведением манипуляции специалист обязан еще раз уточнить группу и резус-фактор крови донора и больного.
Подготовка к переливанию
Процедура начинается с формальностей. В первую очередь больной должен ознакомиться с вероятными рисками данной манипуляции и подписать все необходимые документы.
Следующий этап – проведение первичного исследования групповой принадлежности и резус-фактора крови по системе АВО с применением цоликлонов. Полученные сведения фиксируются в специальном регистрационном журнале медучреждения. Затем изъятый образец ткани отправляют в лабораторию для уточнения фенотипов крови по антигенам. Результаты исследования указываются на титульном листе истории болезни. Для больных, имеющих в анамнезе осложнения переливания плазмы или других компонентов крови, а также беременных и новорожденных трансфузионную среду подбирают индивидуально в лаборатории.
В день проведения манипуляции у реципиента берут кровь из вены (10 мл). Половину помещают в пробирку с антикоагулянтом, а остальную отправляют в емкость для проведения ряда анализов и биологических проб. При переливании плазмы или любых других компонентов крови, помимо проверки по системе АВО, материал тестируют на предмет индивидуальной совместимости по одному из методов:
- конглютинации с полиглюкином;
- конглютинации с желатином;
- непрямой реакции Кумбса;
- реакции на плоскости при комнатной температуре.
Это основные виды проб, какие проводят при переливании плазмы, цельной крови или ее отдельных компонентов. Другие анализы назначаются больному по усмотрению врача.
С утра нельзя ничего есть обоим участникам процедуры. Переливание крови, плазмы совершают в первой половине дня. Реципиенту рекомендуется очистить мочевой пузырь и кишечник.
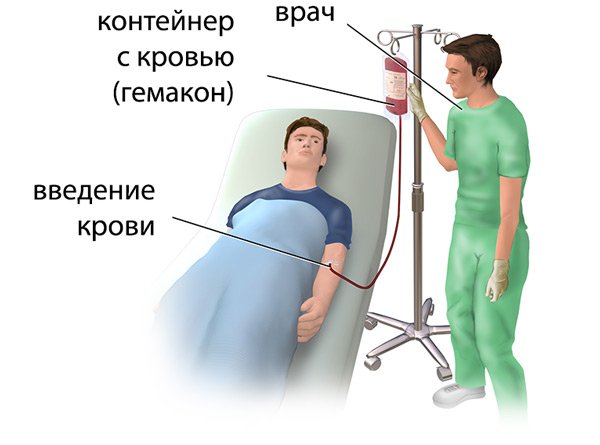
Как проходит процедура
Сама по себе операция не представляет собой сложного вмешательства, требующего серьезного технического оснащения. Для обменного переливания крови пунктируют подкожные сосуды на руках. Если предстоит долгая трансфузия, используют крупные артерии – яремную или подключичную.
Перед тем, как приступить к непосредственному вливанию крови, доктор не должен иметь ни малейших сомнений в качестве и пригодности внедряемых компонентов. Обязательно проводится детальный осмотр контейнера и его герметичность, корректность оформления сопроводительных документов.
Первым этапом при переливании плазмы крови является однократное введение 10 мл трансфузионной среды. Жидкость вводится в кровоток реципиенту неспешно, при оптимальной скорости 40-60 капель в минуту. После вливания пробных 10 мл донорской крови за состоянием больного наблюдают в течение 5-10 минут. Биологическую пробу повторяют дважды.
Опасными признаками, которые указывают на несовместимость биоматериалов донора и реципиента, являются внезапная одышка, учащение сердцебиения, сильное покраснение кожи лица, снижение артериального давления, удушье. В случае появления такой симптоматики манипуляцию останавливают и сразу же оказывают больному необходимую лечебную помощь.
Если никаких негативных изменений не произошло, приступают к основной части гемотрансфузии. Одновременно с поступлением в организм человека компонентов крови необходимо следить за температурой его тела, осуществлять динамический кардиореспираторный мониторинг, контролировать диурез. Скорость введения крови или ее отдельных компонентов зависит от показаний. В принципе допускается струйное и капельное введение со скоростью около 60 капель ежеминутно.
В ходе переливания крови иглу может застопорить тромб. В этом случае нельзя проталкивать сгусток в вену. Процедуру приостанавливают, тромбированную иглу извлекают из кровеносного сосуда и заменяют ее новой, которую уже вводят в другую вену и восстанавливают подачу жидкой ткани.
После трансфузии
Когда все необходимое количество донорской крови поступит в организм пациента, в емкости оставляют немного крови (плазмы) и хранят ее на протяжении двух-трех дней в холодильнике. Это необходимо на тот случай, если у больного внезапно возникнут посттрансфузионные осложнения. Препарат позволит выявить их причину.
Основная информация о манипуляции заносится в историю болезни. В документах отмечается объем введенной крови (ее компонентов), состав, результат предварительных проб, точное время манипуляции, описание самочувствия пациента.
После процедуры больному нельзя сразу вставать. Последующие несколько часов придется провести лежа. За это время медперсонал должен тщательно следить за сердцебиением, температурными показателями. Спустя сутки после вливания, реципиент сдает анализы мочи и крови.
Малейшее отклонение в самочувствии может говорить о непредвиденных негативных реакциях организма, отторжении донорской ткани. При учащении сердцебиения, резком снижении давления и болезненности в груди пациента переводят в отделение реанимации или интенсивной терапии. Если в течение следующих четырех часов после переливания плазмы или других компонентов крови у реципиента не повышается температура тела, а показатели давления и пульса находятся в пределах нормы, можно говорить об успешном проведении манипуляции.
Какие могут быть осложнения
При соблюдении верного алгоритма и правил переливания крови процедура абсолютно безопасна для человека. Малейшая погрешность может обойтись человеческой жизни. Так, например, при попадании воздуха через просвет сосудов возможно развитие эмболии или тромбоза, которые проявляются нарушениями дыхания, синюшностью кожных покровов, резкими падением артериального давления. Подобные состояния требуют проведения экстренных реанимационных мероприятий, так как являются смертельно опасными для пациента.
Посттрансфузионные осложнения, о которых было сказано выше, крайне редко угрожают жизни и зачастую представляют собой аллергическую реакцию на компоненты донорской ткани. Справиться с таковыми помогают антигистаминные средства.

Более опасным осложнением, имеющим фатальные последствия, является несовместимость крови по группе и резусу, в результате которой происходит разрушение эритроцитов, наступает полиорганная недостаточность и смерть больного.
Бактериальное или вирусное инфицирование во время процедуры – сравнительно редкое осложнение, но все же полностью исключать его вероятность нельзя. Если трансфузионная среда хранилась не в карантинных условиях, а при ее заготовке не были соблюдены все правила стерильности, минимальный риск заражения гепатитом или ВИЧ все же имеет место.
Фарм. группа
Аналоги (дженерики, синонимы)
растворы желатина, желатиноль, модежель, гелофузин, полифер, реоглюман, инфукол гэк
Рецепт (международный)
Фармакологическое действие
Заменители крови и растворы для переливания. Содержит факторы свертывания крови. Обладает гемостатическим эффектом.
Снижает риск кровоизлияний в желудочки головного мозга у недоношенных детей (до 32-й недели гестации или менее 1500 г массы тела).
Способ применения
Для взрослых: Доза плазмы зависит от требуемого уровня факторов свертывания. Количество плазмы выражают в единицах; одна единица плазмы (обычно около 250 мл) соответствует таковой цельной крови, потребовавшейся для ее изготовления.
Перед использованием необходимо тщательно проверить целостность флаконов, наличие этикетки. Затем снять покрытие с горлышка флакона, колпачок обработать 96 % этанолом и стерильным пинцетом отогнуть створки колпачка, резиновую пробку смазать йодом - в таком виде, если плазма нативная, она годна для переливания. Если плазма сухая, то после обработки резиновую пробку следует проколоть двумя короткими стерильными иглами. Одну иглу присоединить к флакону с растворителем, вторая служит для отвода воздуха при переливании растворителя во флакон с плазмой. Плазму можно разводить до разных концентраций и, в зависимости от показания для переливания, готовить в виде гипертонического или изотонического раствора. Нативная бесцитратная плазма пригодна для использования в течение 3 суток. Растворять сухую бесцитратную плазму следует только перед ее применением. Она растворяется в дистиллированной воде, 0,9 % растворе натрия хлорида или в 5 % растворе декстрозы в течение не более 10 мин при комнатной температуре.
Переливание производят через стандартные системы для переливания крови с фильтрами. Для переливания используется только одногруппная (по системе AB0 и резус-фактор) бесцитратная плазма с кровью реципиента. Переливать можно внутривенно и внутрикостно. Перед переливанием проводят троекратную биологическую пробу на индивидуальную совместимость. С этой целью больному быстро вводят 15-20 капель, затем 10 и 20 мл, с перерывом между каждым введением 3 мин. При отсутствии реакции у больного вводят всю дозу.
При шоке, в зависимости от величины сопутствующей кровопотери и показателей гемодинамики, вводят струйно до 2 л. При травмах черепа рекомендуется использовать концентрированные (в 2-3 раза) растворы сухой бесцитратной плазмы.
С гемостатической целью следует вводить плазму ранних сроков хранения по 250-500 мл. При необходимости дозу можно увеличить. При белковой недостаточности, явлениях интоксикации, поражении печени и почек - в дозах до 500 мл.
В раннем детском возрасте - 8-15 мл/кг массы тела ребенка в зависимости от показаний.
Перед переливанием свежезамороженную плазму необходимо разморозить в
течение 15 - 20 минут.
Разморозка осуществляется в два этапа:
1. Пакет с плазмой помещают в холодную воду на 5-7 минут;
2. Постепенно (10-15 минут) доводят температуру воды до 37-380С.
Размораживать пакет с замороженной плазмой в горячей воде нельзя!
Длительная разморозка при комнатной температуре приводит к выпадению
фибрина.
Показания
- Восстановление гемодинамики и коррекция гемостаза (шок, кровопотеря, коагулопатии).
- Плазму используют для возмещения альбумина, антитромбина III, факторов свертывания крови, иммуноглобулинов, тромбоцитов.
Противопоказания
- гиперчувствительность
- тромбоэмболические заболевания.
Побочные действия
- Перегрузка сердечно-сосудистой системы и отек легких - при быстром переливании больших объемов.
- Гипотермия, ацидоз, гипокальциемия и гиперкалиемия, сердечная токсичность - при массивных переливаниях холодной плазмы.
- Диссеминированное внутрисосудистое свертывание - при переливании больших объемов.
- Гемолиз, почечная недостаточность - при переливании несовместимой плазмы.
- Тяжелые анафилактические реакции, гипертермия, крапивница или озноб.
- Инфицирование вирусами гепатита В, С, ВИЧ, цитомегаловирусом, возбудителями болезни
- Крейтцфельдта-Якоба, болезни Чагаса, малярии, сифилиса.
- Со стороны легких: редкое, но жизнеугрожающее осложнение - острое повреждение легких, развивается через 1-6 ч после начала инфузии и протекает как острый респираторный дистресс-синдром, разрешается спустя 2-4 дня при проведении интенсивной терапии. Предполагается, что причиной являются HLA-специфичные антитела в плазме неоднократно рожавших женщин.
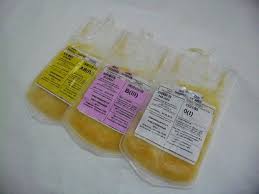
Форма выпуска
Плазма свежезамороженная расфасовывается в контейнеры объемом 50 – 300 мл.
ВНИМАНИЕ!
Информация на просматриваемой вами странице создана исключительно в ознакомительных целях и никак не пропагандирует самолечение. Ресурс предназначен для ознакомления сотрудников здравоохранения с дополнительными сведениями о тех или иных медикаментах, повысив тем самым уровень их профессионализма. Использование препарата "Свежезамороженная плазма" в обязательном порядке предусматривает консультацию со специалистом, а также его рекомендации по способу применения и дозировке выбранного вами лекарства.
СЗП является компонентом крови, содержит в физиологической концентрации все факторы коагулянтной и антикоагулянтной систем, за исключением лабильных – V и VIII, концентрация которых зависит от качества заготовки. Также содержит плазменные белки в физиологической концентрации (т.е. является примерно 4-5% раствором альбумина).
Показанием для введения СЗП являются любые ситуации, когда лабораторно подтвержден дефицит любого из компонентов (факторов) коагулянтной и антикоагулянтной систем.
Рекомбинантные препараты
Применение этих препаратов показано только при гипокоагуляционных коагулопатиях с целью профилактики возможных кровотечений или при уже развившемся геморрагическом синдроме. Необоснованное применение чревато избыточным тромбообразованием в ненужных местах и развитием таких смертельных осложнений как ТГВ, ТЭЛА, ОИМ.
НовоСевен (NovoSeven, Эптаког альфа (активированный), РАФVII).
Для остановки кровотечений и профилактики их развития при проведении хирургических вмешательств и инвазивных процедур у пациентов со следующей патологией:
- наследственной гемофилией с титром ингибиторов факторов свертывания VIII или IX более 5 БЕ (единиц Бетезда);
- наследственной гемофилией с ожидаемой иммунной реакцией на введение фактора VIII или фактора IX на основании анамнеза;
- врожденным дефицитом фактора VII;
- тромбастенией Гланцмана при наличии антител к гликопротеинам IIb-IIIa и рефрактерностью (в настоящем или в прошлом) к трансфузиям тромбоцитарной массы.
- кровотечение (в т.ч. профилактика при хирургических операциях) у больных наследственной или приобретенной гемофилией с ингибиторами к факторам коагуляции (FVIII или FIX).
ФЕЙБА(FEIBA, Фейба Тим 4 Иммуно)
Антиингибиторный коагулянтный комплекс со стандартной активностью FEIBA (Factor Eight Inhibitor Bypass Activity). Содержит факторы II, IX и X (в основном в неактивированной форме), активированный фактор VII, VIII.
ПОКАЗАНИЯ. Кровотечения при ингибиторных формах гемофилии A и B; тяжелые или угрожающие жизни кровотечения у пациентов на фоне приобретенной недостаточности факторов VII, VIII, IX и XII.
Гемоконтактные инфекции
ВИЧ – инфекция в медицинской практике. Стандартные меры предосторожности
Проблема ВИЧ-инфекции, роль которой документально подтверждена как представителя одной из трех основных гемоконтактных инфекций (ВИЧ, ВГВ и ВГС), актуальна для врачей и среднего медицинского персонала всех специальностей, особенно специалистов хирургического профиля, при выполнении ими инвазивных медицинских вмешательств. В связи с необходимостью непосредственного контакта с ранами при травмах, переломах, операциях, других видах манипуляций, медицинские работники находятся под риском инфицирования, в связи с чем, они должны владеть основными базовыми сведениями как о природе ВИЧ-инфекции и других гемоконтактных инфекций, так и мерах собственной защиты и защиты пациентов.
Главной целью при этом остается обеспечение качества медицинских вмешательств в интересах здоровья пациентов, и все медицинские работники несут ответственность за предупреждение передачи инфекций при оказании медицинской помощи. То есть, проводимые медицинские процедуры НЕ должны наносить вред пациенту, НЕ подвергать медицинского работника риску инфицирования и НЕ приводить к образованию отходов, потенциально опасных для окружающих людей. Это основные требования к практике безопасных инъекций и медицинских манипуляций.
По глобальным оценкам, на только на 2000 год в результате применения практики небезопасных инъекций было зарегистрировано:
▪ 21 миллион случаев заболевания ВГВ (32% новых случаев ВГВ)
▪ 2 миллиона случаев заболевания ВГС (40% новых случаев ВГС)
▪ 260 000 случаев заболевания ВИЧ - вирус иммунодефицита человека (5% новых случаев ВИЧ-инфекции)
▪ Эти патогены (ВГВ/ВГС/ВИЧ) стали причиной заболевания и среди медперсонала.
▪ Почти 4.4% случаев заболевания медицинских работников ВИЧ и 39% случаев заболевания ВГВ и ВГС были связаны с производственными травмами (ВОЗ, 2010).
ВИЧ-инфекция и СПИД. Общие сведения.
Основные факты по ВИЧ/СПИД.
Первые случаи ВИЧ/СПИД официально были зарегистрированы в 1982 году в США. Первоначально, они рассматривались как специфическое заболевание отдельных групп населения (гомосексуалисты, инъекционные наркопотребители), однако в последующем болезнь распространилась и на другие слои населения.
1983 – Люк Монтанье (Франция) и Роберт Галло (США) изолируют культуру ВИЧ.
1987-1989гг. – зарегистрированы первые случаи ВИЧ-инфекции в Казахстане
2013 – официально зарегистрировано свыше 20 тысяч случаев ВИЧ-инфекции в Казахстане.
ВИЧ-инфекция остается одной из основных проблем общественного здравоохранения, так как за последние три десятилетия она унесла более 25 миллионов человеческих жизней:
●В 2011 году в мире насчитывалось примерно 34 миллиона людей, живущих с ВИЧ
●Наиболее пораженным регионом является Африка к югу от Сахары, где почти каждый двадцатый взрослый человек имеет ВИЧ и в этом регионе живет 60% всех людей с ВИЧ
●ВИЧ-инфекцию обычно диагностируют с помощью тестирования крови, выявляющего наличие или отсутствие антител к ВИЧ
● В 2012 году в странах с низким и средним уровнем доходов АРТ получало 10 миллионов человек и масштабы АРТ дальше будут расширяться до 25 миллионов к 2015г.
Ситуация по ВИЧ/СПИД в Восточной Европе и Центральной Азии
●В регионе ВЕиЦА отмечается рост показателя распространенности ВИЧ, появления новых случаев ВИЧ и смертей вследствие СПИДа
● Основными факторами, способствующими развитию эпидемии в регионе ВЕиЦА остаются употребление инъекционных наркотиков и передача ВИЧ половым
путем партнерам ПИН
●С 2001по 2011 годы оценочное число людей, живущих с ВИЧ в регионе, увеличилось с 970 000 до 1,4 миллиона человек
●Показатель распространенности ВИЧ среди молодых людей в возрасте 15-24 лет увеличился с 0,2% до 0,5% среди женщин и с 0,3% до 0,7% среди мужчин
●С 2005 по 2011 годы число смертей, связанных со СПИДом, увеличилось в регионе на 21% с 76 000 до 92 000 случаев
● Охват лечением в регионе остается на низком уровне: лишь 25% людей, которым показано лечение в связи с ВИЧ, получают АРТ (ЮНЭЙДС, бюллетень 2012).
Ситуация по ВИЧ/СПИД в Казахстане.На начало 2013 года в Казахстане кумулятивно зарегистрировано 19748 ВИЧ-инфицированных, из них детей до 14 лет 400 (2%). Большее число случаев ВИЧ-инфекции выявлено в г.Алматы, Павлодарской, Восточно-Казахстанской и Карагандинской областях. В эпидемию вовлечены и другие области республики. Доля мужчин в этот период составляла 69%, женщин 31%. В основном ВИЧ-инфекция выявляется среди молодых людей в возрасте от 15-39 лет – 16106 (82%). Основным путем передачи ВИЧ остается внутривенное употребление наркотиков (63%), однако отмечается рост полового пути передачи ВИЧ (32%).
Понятия ВИЧ/СПИД
ВИЧ-инфекция – это болезнь, вызванная ВИЧ, хроническое инфекционное заболевание, характеризующееся поражением иммунной системы, приводящим к формированию синдрома приобретенного иммунодефицита (СПИД), сопровождающегося развитием оппортунистических инфекций и вторичных злокачественных новообразований.
СПИД–это состояние, развивающееся на фоне ВИЧ-инфекции и характеризующееся появлением одного или нескольких заболеваний, отнесенных к СПИД-индикаторным. СПИД является самой поздней стадией ВИЧ-инфекции, который у разных людей может развиться через 2-15 лет от момента инфицирования. Согласно существующей клинической классификации, стадия СПИД соответствует 4 стадии ВИЧ-инфекции.
Структура ВИЧ(рис. 54.)
ВИЧ относится к подсемейству лентивирусов. Лентивирусы вызывают хронические инфекции с длинным латентным течением, персистирующей репродукцией вируса и поражением ЦНС. В настоящее время известны три типа вируса - ВИЧ-1, ВИЧ-2 и ВИЧ-3, из них широко распространены два типа ВИЧ-1 и ВИЧ-2, оба вируса патогенны, но ВИЧ-2 инфекция протекает легче. Как и все ретровирусы, ВИЧ характеризуется высокой изменчивостью.
Морфология ВИЧ
Диаметр ВИЧ-1 составляет 100 нм. Снаружи вирус окружен липидной мембраной, в которую встроены 72 гликопротеидных комплекса. Каждый из этих комплексов образован поверхностным гликопротеидом (gp120) и трансмембранным (gp41). Внутри к оболочке прилежит белок p17. Сердцевину вируса (капсид) составляет белок p24, который окружает белковонуклеиновый комплекс: две молекулы вирусной РНК, связанные с протеидом p7 и обратной транскриптазой p66. Вирус содержит все необходимые ферменты для репликации: обратную транскриптазу, интегразу p32 и протеазу p11.
Геном ВИЧ.Репродукция большинства ретровирусов определяется тремя генами: gag, pol и env. Название генов произошло от кодируемых ими белков: gag - "group-antigen"(капсидный белок), pol - "polymerase" (полимераза), env - "envelope" (оболочка).
Структурные гены (3):
· Gag-ген отвечает за синтез трёх протеинов сердцевины
· Роl-ген кодирует синтез ревертазы;
· Еnv-ген кодирует синтез двух гликопротеидов: gp120 и gp41.
Рис. 54. Схема строения ВИЧ
Источником ВИЧ-инфекции являются люди, инфицированные ВИЧ на любой стадии заболевания, в том числе в инкубационном периоде в связи с постоянной репликацией (размножением) вируса. В сутки вырабатывается до 7-10 миллиардов вирусных частиц (рис. 55).
Рис. 55. Стадии репликации ВИЧ
Факторы риска.
Формы поведения и условия, повышающие риск заражения людей ВИЧ, включают следующие моменты:
● незащищенный вагинальный или анальный секс;
● наличие другой инфекции, передаваемой половым путем, такой как сифилис, герпес, хламидиоз, гонорея и бактериальный вагиноз;
● совместное использование нестерильными (контаминированными кровью инфицированных лиц) игл, шприцев и другого инъекционного оборудования и растворов
● небезопасные инъекции, переливания крови, медицинские процедуры, включающие нестерильные разрезы или прокалывание;
● случайные травмы от укола иглой, острыми инструментами при оказании помощи пациентам медицинскими работниками
Пути, механизм и факторы передачи ВИЧ-инфекции.
Пути передачи ВИЧ-инфекции:
n Половой (гетеросексуальный, гомосексуальный)
n Парентеральный (через кровь, инструментарий)
n От матери к ребенку
ВИЧ-инфекция может передаваться при реализации как естественного, так и искусственного механизма передачи.
К естественному механизму передачи ВИЧ относятся:
- Контактный, который реализуется преимущественно при половых контактах (как при гомо-, так и гетеросексуальных) и при контакте слизистой или раневой поверхности с кровью.
-Вертикальный: инфицирование ребенка от ВИЧ-инфицированной матери во время беременности, в родах и при грудном вскармливании.
К искусственному механизму передачи относятся:
- Артифициальный при немедицинских инвазивных процедурах, в том числе внутривенном введении наркотиков наркопотребителями (совместное использование игл и шприцев, другого инъекционного оборудования и материалов).
- Артифициальный при инвазивных вмешательствах в ЛПО. При этом инфицирование ВИЧ может осуществляться при переливании крови и ее компонентов в результате небезопасных переливаний крови, пересадке органов и тканей, использовании донорской спермы, донорского грудного молока от ВИЧ-инфицированного донора, а также при небезопасной практике медицинских инъекций и манипуляций через медицинский инструментарий для парентеральных вмешательств, изделий медицинского назначения, контаминированных ВИЧ и не подвергшиеся обработке в соответствии с требованиями нормативных документов.
Основными факторами передачи ВИЧ являются следующие биологические жидкости человека: кровь и компоненты крови, семенная жидкость (сперма), вагинальное отделяемое, грудное молоко). Остальные жидкости не опасны в передаче ВИЧ, если нет примеси крови. Люди не могут заразиться при обычных повседневных контактах, таких как поцелуи, объятия и пожатие рук, или при употреблении продуктов питания и воды (рис.56).
Рис. 56. Содержание ВИЧ в биологических жидкостях
Уязвимыми группами населения(УГН) для ВИЧ-инфекцииявляются: потребители инъекционных наркотиков (ПИН), коммерческие секс-работники (КСР), мужчины, имеющие секс с мужчинами (МСМ). Группу повышенного риска заражения ВИЧ представляют клиенты КСР, половые партнеры ПИН, заключенные, беспризорные дети, лица, имеющие большое число половых партнеров, мигранты.
В целях профилактики ВИЧ-инфекции, важным моментом является консультирование и тестирование населения на ВИЧ, включая в первую очередь лиц из УГН, в соответствии с действующими нормативными документами (алгоритм тестирования взрослых в РК, приложение 1).
Последнее изменение этой страницы: 2016-07-14; Нарушение авторского права страницы
Читайте также:


