Из чего делают протезы для костей
2019. Украинский стартап будет печатать человеческие кости на 3D-принтере

Украинский стартап Kwambio, который производит 3D-принтеры, совместно с фондом WeFund Ventures представил проект по печати человеческих костей и органов ADAM. Основатель стартапа Владимир Усов (на фото) говорит, что они работают над созданием цифрового 3D-атласа организма с помощью снимков КТ и МРТ. Это позволит быстро распечатывать необходимую кость или орган для пациента прямо в больнице. Также, в рамках проекта Kwambio с партнерами создал два новых биоматериала — керамическое биостекло и модифицированный биополимер. Они будут использоваться для печати разных типов костей, а также, со временем, мягких тканей, сосудов и сложных органов.
2016. Новый биопластик для 3D-печати костей обрастает живыми клетками

Обычно протезы костей делают из биоинертных металлов или вырезают из малоберцовой кости самого пациента. Однако, теперь, когда появились 3D-принтеры, позволяющие с высокой точностью распечатать любую косточку, эти старые методы - морально устарели. Осталась одна проблема - найти материал, который может служить одновременно и биоинертной основой для клеток костной ткани и чернилами для 3D-принтера. И исследователи Университета Джона Хопкинса такой материал создали. Это легкоплавкий пластик. Он превращается в жидкость при температуре 80−100 градусов, и добавленные в него живые клетки не успевают разрушиться. В качестве клеточного материала прекрасно сработали стволовые клетки из жировой ткани, собранной при липосакции, смешанные с костной пылью. Через три недели биоматериал опытного образца начал накапливать кальций — а значит, полностью превратился в клетки костной ткани.
2016. В США создали технологию выращивания человеческих костей и мышц
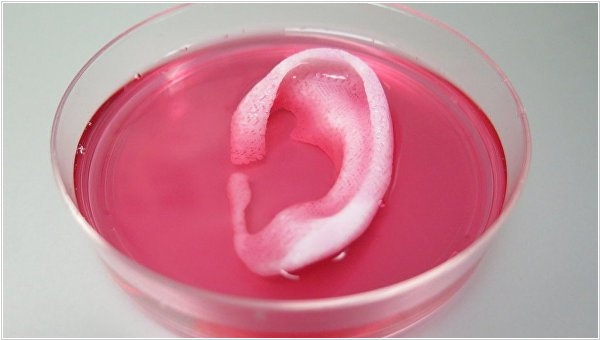
Биоинженеры из Института регенеративной медицины в Уэйк-Форесте (США) разработали необычную технологию трехмерной печати, которая позволяет создавать полноценные копии отдельных костей, мышц и хрящей из стволовых клеток. До сих пор ученым удавалось распечатывать только очень тонкие слои живой ткани (до 200 мкм) - иначе ткань начинала гибнуть, так как питательные вещества и кислород не могут проникнуть на такую глубину без наличия кровеносных сосудов. В данном случае биоинженеры использовали особый полимер, позволявший укладывать клетки слоями и при этом сохранять небольшой просвет между ними. А после печати, ученые помещают органоид в организм мыши, где он постепенно "зарастает" кровеносными сосудами, а полимер постепенно разлагается, уступая им место. В конечном итоге на месте заготовки возникает полноценный орган, обладающий нужной трехмерной формой и всеми необходимыми видами ткани.
2015. Кости для трансплантации будут выращивать из собственных клеток пациента

Оказывается, по статистике, кость - самая часто пересаживаемая человеческая ткань после крови. И, как в случае со всеми трансплантантами, донорские кости часто отвергаются телом пациентов. Американская компания EpiBone разработала технологию выращивания костей из стволовых клеток самого пациента. Для этого они проводят компьютерную томографию поврежденного участка, создают персонализированный трехмерный каркас, а потом берут у больного образец жировой ткани, откуда извлекают стволовые клетки и внедряют их в уже сделанный каркас. После чего тот отправляется в камеру роста, биореактор, симулирующий условия внутри человеческого тела. Через три недели после помещения в биореактор там формируется живая человеческая кость, имеющая размеры и форму, необходимые для пациента. Сейчас технология проходит стадию проверки на животных и официального одобрения для работы на людях.
2015. Человеку имплантировали протез грудной клетки, распечатанный на 3D-принтере

2014. Человеку впервые имплантировали напечатанный на 3D-принтере позвонок
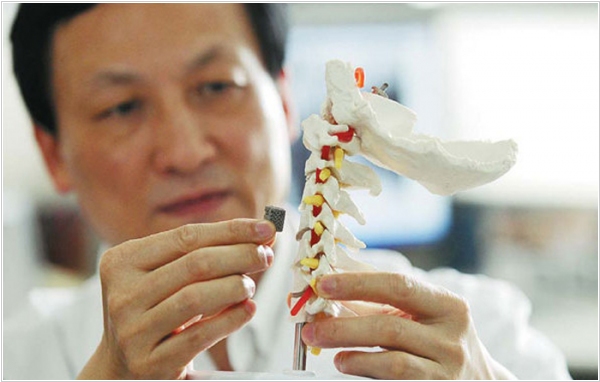
Команда врачей из Третей клинической больницы Пекинского университета заявила об успешной имплантации позвонка, напечатанного на 3D принтере. Операция была проведена для 12-летнего пациента со злокачественной опухолью спинного мозга. Позвонок создан путем спекания титанового порошка. Причем, в отличии от традиционных имплантатов, он - не монолитный, а пористый. По расчетам ученых, через эти поры будет расти костная ткань, при этом не требуется замена протеза с возрастом,т.к. костная ткань покроет позвонок, который станет естественной частью позвоночника мальчика.
2014. Видео: Эндопротезирование тазобедренного сустава, распечатанного на 3D-принтере
Британские хирурги впервые напечатали тазобедренный сустав для эндопротезирования на 3D-принтере и использовали стволовые клетки пациентки, чтобы зафиксировать его на месте. Имплантат для 71-летней пациентки больницы при Саутгемптонском университете был напечатан на основе 3D-файлов, изготовленных по подробным КТ-сканам. В качестве материала использовался титановый порошок, тонкие слои которого спекались под воздействием лазерного луча. А в качестве "клея", который позволит надежно зафиксировать имплантат на месте использовался материал из стволовых клеток пациентки. Хирурги уверены, что технология трехмерной печати может кардинально изменить ход проведения сложных ортопедических операций. Однако, как и другие инновационные технологии, сейчас она далеко не всем по карману. 3D-печатный имплантат и операция обошлись пациентке в 12000 фунтов.
2014. Пациенту имплантировали лицевую кость, выращенную из его стволовых клеток
2014. Пациентке установили искусственный череп, распечатанный на 3D-принтере
У 22-летней пациентки Университетского медицинского центра Утрехта (это в Нидерландах) было редкое заболевание черепа - он рос вовнутрь и давил на мозг, что вызывало нарушение зрения и головные боли. И серьёзные повреждения мозга или смерть были бы неизбежны в ближайшем будущем, если б врачи не придумали заменить верхнюю часть черепа на искусственную, распечатанную на 3D-принтере. Имплантат изготовлен по индивидуальному заказу из прочного пластика, название которого не называется. После операции к пациентке вернулось зрение, она не проявляет никаких симптомов болезни и полностью работоспособна.
2013. Японские ученые вырастили хрящевую ткань из клеток кожи

Японским ученым из университета Киото удалось воссоздать хрящевую ткань за счет перепрограммирования клеток эпидермиса кожи. Для этого в клетки кожи (с помощью специального вируса) был пересажен ген SOX9, который отвечает за образование хрящевой ткани. В результате через две недели ученые смогли получить ее подобие. Преимуществом данного метода является быстрота: использование стволовых клеток дает подобный результат только через месяц. Ученые отмечают, что выращенный хрящ был успешно пересажен лабораторным мышам. Ученые отмечают, что новый метод имеет еще одно преимущество - онкобезопасность. Старые методы преобразования обладают существенным минусом: довольно часто на пересаженных участках возникает онкологический процесс, который по тяжести может превосходить основное заболевания. Новый метод лишен столь серьезного недостатка.
Требования к металлам при изготовлении эндопротезов. Особенности использования сталей и сплавов цветных металлов. Описание керамики, полиэтилена, костного цемента как материалов для имплантатов. Описание печатькальций-фосфатных протезов на 3d принтере.
| Рубрика | Медицина |
| Вид | реферат |
| Язык | русский |
| Дата добавления | 16.12.2016 |
| Размер файла | 26,3 K |
- посмотреть текст работы
- скачать работу можно здесь
- полная информация о работе
- весь список подобных работ
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
Владимир 2016 Министерство образования и науки Российской Федерации
Федеральное государственное бюджетное образовательное учреждение высшего образования
Студент группы БТС-114
Проверил: Фролова Т. Н.
Содержание
1. Металы и сплавы
1.1 Нержавеющие стали
1.2 Титан и его сплавы
1.3 Кобольтохромовые сплавы
1.4 Сплавы циркния и тантала
1.5 Поверхности металлических компонентов
2.1 Взаимодействия с тканями организма
2.2 Виды керамики
4. Костный цемент
5. Печатькальций-фосфатных протезов на 3d принтере
Список используемой литературы
Введение
Выбор материала при создании любого имплантата является важным этапом, нередко определяющим успех всего комплекса опытно-конструкторских исследований и производственных работ. При этом следует учитывать два основных принципа, которые, отражая тесную взаимосвязанность дизайна и материала, могут быть положены в основу медицинского материаловедения:
1) технические и биологические особенности конструкции зависят от соответствующих особенностей материала;
2) новые материалы позволяют реализовывать новые варианты дизайна имплантата.
Главной дизайнерской задачей при создании тотального эндопротеза является получение постоянного, длительно функционирующего имплантата, позволяющего устранить болевой синдром и улучшить функциональные возможности путем воспроизведения искусственными сочленяющимися компонентами нормальной пространственной геометрии, подвижности и опороспособности. протез имплантат сплав керамика
Вторичными задачами общего плана наиболее часто считают:
· простоту дизайна и применения,
· сберегательное отношение к тканям при имплантации,
· надежность и высокую устойчивость к разрушению и износу,
· долговечность функционирования, удобство в применении,
· минимизацию технических трудностей при замене изношенных,
· разрушенных имплантатов, удобство для промышленного производства,
. Основным требованием, предъявляемым к материалам для изготовления эндопротеза, является биосовместимость, определяемая как способность материала вызвать приемлемый ответ макроорганизма или не вызывать его совсем. Негативное влияние материала и продуктов его износа или деградации не должны приводить к значимым местным, системным и отдаленным эффектам, а положительное влияние может заключаться в виде ряда полезных, требуемых для решения задач эндопротезирования, проявлений, например, адгезии или врастания костной ткани.
Основные материалы компонентов для изготовления эндопротезов (см. таблица 1)
1. Металлы и сплавы
Общими требованиями к металла ,применяемым для изготовления эндопротезов, являются:
· устойчивость к коррозии,
· возможность создавать требуемую структуру поверхности и биосовместимость.
1.1 Нержавеющие стали
Нержавеющие стали (Fe, С, Or, Ni, Mo) характеризуются низким содержанием углерода, что определяет устойчивость к коррозии и механическим нагрузкам. Прочность нержавеющей стали может быть повышена холодной ковкой. Сплав стали BioDur108, содержащий Ni, с высоким содержанием азота и обладающий значительной коррозионной устойчивостью и лучшими прочностными характеристиками, применяют для изготовления цементных ножек эндопротезов.
1.2 Титан и его сплавы
Титан и его сплавы (CP-Ti (чистый титан - 98 - 99,6%), Ti-6AI-4V и др.) характеризуются высокой коррозионной устойчивостью и биосовместимостью. Чистый титан более вязкий, применяется для пористых покрытий, фиброметалла. Сплав Ti-6A1 -4V имеет большую механическую прочность. Модули торсионной и аксиальной жесткости наиболее близки к кости. Сплав чувствителен к разрушениям, связанным с образованием микрокаверн, обладает высокой поверхностной мягкостью.
Новые титановые сплавы - Я-титан (Я-Ti) - характеризуются преобладанием Я-фазы сплава, часто за счет высокого содержания Мо (более 10%), что позволяет повысить устойчивость к разрушению, в первую очередь к усталостному, а также на 20% снизить модуль упругости, приблизив его к модулю упругости кости. Ti-5AI-2,5Fe, Ti-6AI-17 Niobium не содержат относительно токсичный V, имеют более низкий модуль упругости. Ti-Ta30 имеет модуль термического расширения, близкий к керамике, что снижает риск ее разрушения при сочетании с металлическими имплантатами. Все титановые сплавы малоустойчивы к образованию дебриса. Чаще их применяют для изготовления бесцементных ножек, иногда после поверхностного упрочнения оксидированием или протонной бомбардировкой, и реже - цементных.
1.3 Кобольтохромовые сплавы
Сплавы Co-Cr (Co-Cr-Mo, Co-Ni-Cr-Mo, Co-Cr-Ni- W, Co-Ni-Cr-Mo-W-Fe) отличаются высокой коррозионной устойчивостью, возможно, обладают некоторой токсичностью и иммуногенностью за счет наличия никеля. Co-Ni-Cr имеет плохие фрикционные свойства, образует большое количество дебриса. Со-Сг-Мо обладает высокой твердостью и прочностью, применим в парах трения при изготовлении головок эндопротезов, а также в парах трения металл-металл. Последние характеризуются чрезвычайно низким износом, не образуют большого количества дебриса, однако их применение ограничивают существенные недостатки: излишняя жесткость (частично преодолима при установке металлического вкладыша в полиэтиленовую основу), повышающая риск расшатывания бедренного и вертлужного компонентов эндопротеза; длительность приработки трущихся поверхностей; повышение концентрации ионов металлов в биологических жидкостях и тканях (токсичность, аллергенность, возможно, онкогенность и тератогенность); высокая чувствительность к импинджменту; риск остеолитических реакций костной ткани, высокая стоимость. Вариантом пары трения металл-металл является Со-Сг пара с интеграцией корундовых кристаллов (Metasul), обеспечивающих еще более низкий износ.
1.4 Сплавы циркния и тантала
Сплавы Zr и Та обладают высокими коррозионной устойчивостью, биосовместимостью, поверхностной жесткостью и малым образованием дебриса. Возможно создание трабекулярного металла. Истинный трабекулярный металл на основе тантала позволяет значительно повысить возможности остеоинтеграции, при этом не создавая проблемы зон соединения разнопрочностных сред.
Поверхность металлических компонентов эндопротезов может быть:
полированной (головки, вкладыши чашек при парах трения металл-металл, ножки цементной фиксации);
шероховатой, которую создают путем обработки в струе песка (ножки и чашки бесцементной фиксации 5-8 мкм);
пористой, которую создают путем спекания шариков или проволоки (ножки и чашки бесцементной фиксации);
трабекулярной, получаемой путем плазменного напыления металлом (чашки, а также ножки бесцементной фиксации);
с покрытием из гидроксиапатита, фосфата кальция
1.5 Поверхности металлических компонентов
· полированной (головки, вкладыши чашек при парах трения металл-металл, ножки цементной фиксации);
· шероховатой, которую создают путем обработки в струе песка (ножки и чашки бесцементной фиксации 5-8 мкм);
· пористой, которую создают путем спекания шариков или проволоки (ножки и чашки бесцементной фиксации);
· трабекулярной, получаемой путем плазменного напыления металлом (чашки, а также ножки бесцементной фиксации);
· с покрытием из гидроксиапатита, фосфата кальция
2. Керамика
Совершенствование керамических материалов позволило рассматривать их как некоторую альтернативу металлическим сплавам, а по некоторым своим характеристикам, прежде всего трибологическим, пара керамика-керамика обладает уникальными свойствами.
2.1 Взаимодействия с тканями организма
· инертная керамика, сохраняющая форму имплантата и поверхностную структуру без врастания тканей;
· биоактивная керамика, сохраняющая форму имплантата и его внутреннюю структуру с врастанием окружающих тканей;
· биодеградируемая, которая теряет форму, поверхностную и внутреннюю структуру имплантата с врастанием в нее, частичным или полным замещеием окружающими тканями.
2.2 Виды керамики
· На основе оксидов Al, Zr, Ti (Аl2O3 ZrO, TiO): биоинертные, с высокой биологической совместимостью и поверхностной прочностью, применимы при создании пар трения керамика-полиэтилен и керамика-керамика. Циркониевая керамика за счет примеси иттрия характеризуется некоторой токсичностью.
· Карбоновая керамика (Сс различной структурой, C-Si): биоинертная, с хорошей биологической совместимостью и поверхностной прочностью. Применима для покрытия ножек и чашек протезов, а также в создании пар трения.
· Кальция фосфаты и алюминаты (Cryst-Са5(РO)3(O), СаАl2O3): биоактивные, небиодеградируемые. Могут обеспечивать взаимодействие между костью и другими биоматериалами, быть носителями лекарственных и биологически активных веществ (короткого срока действия, поверхностное высвобождение). Применимы для биоматериал-индуцированной и биоматериал-зависимойостеоинтеграции.
· Кальция сульфаты, алюминаты и фосфаты (CaSO4, СаАl2O3, Amorph-Ca5(PO4)3(OH)): биодеградируемые, с различным сроком замещения, могут быть носителями лекарственных и биологически активных веществ (длительного срока высвобождения). Аналогичная роль в создании эндопротезов.
3. Полиэтилен
Существуют полиэтилены низкой, средне-низкой, высокой, ультравысокой плотностей и ультравысокой плотности с поперечными связями. Полиэтилен применяют для создания пары трения. В настоящее время широкое распространение получил полиэтилен ультравысокой плотности и его производные, как правило, для изготовления вертлужного компонента. Пара трения металл (головка эндопротеза) - полиэтилен (чашка или вкладыш) до настоящего времени является эталонной. Для модификации полиэтилена ультравысокой плотности в конце 1970-х годов применяли углеродные волокна, повышающие модуль упругости и износостойкость, снижающие способность к деформациям (продукт Poly II, Zimmer). Однако опыт применения показал более высокую частоту разрушений элементов из Poly II, в том числе поверхностных. Частично это было связано с плохой воспроизводимостью технологии изготовления. В начале 90-х годов прошлого века появилась технология кристаллизации полиэтилена ультравысокой плотности без разрыва молекулярных цепей и потери молекулярной массы (Hylamer, DePuy), характеризовавшаяся повышением прочности продукта и его устойчивости к оксидации.
Стерилизация изделий из полиэтилена путем высокодозовогогамма-облучения приводит к возникновению в них оксидативных реакций в виде двух основных направлений: разрыва молекулярных цепей и образования поперечных связей. Причем, если на поверхности образца преобладают реакции деградации полиэтилена, то в глубине растет уровень поперечных сшивок между его молекулами.
Технология создания полиэтилена с поперечными связями, позволяющая обеспечить образование их во всем объеме вещества, а также подавить реакции деградации, привела к получению высокопрочного и износостойкого материала, приближающегося по этим параметрам к парам трения металл-металл, однако позволяющего избежать таких недостатков металлических сочленений, как жесткость, токсичность и аллергенность (за счет повышения концентрации ионов кобальта, никеля и хрома в крови). Однако опыт применения полиэтилена с поперечными связями показал, что при всей перспективности экспериментальных и первых клинических результатов, существует нестабильность технологии производства этого материала, а также повышенный риск разрушения изделий из него при ударных нагрузках.
Таким образом, до настоящего времени наиболее применимым остается стандартный полиэтилен ультравысокой плотности, в том числе с вариантом рекристаллизации, а полиэтилен с поперечными связями сохраняет высокую перспективность как новый вариант высокопрочной пары трения.
4. Костный цемент
Многочисленными исследованиями доказано, что к преимуществам цементного протезирования можно отнести возможность использования простых моделей имплантатов, отсутствие сплошного контакта металлических элементов протеза с костью, возможность создания депо антибиотиков в зоне операции, обеспечение стабильной фиксации элементов протеза при наличии посттравматических и диспластических дефектов костного ложа и остеопороза различного генеза.
Выделены основные факторы, улучшающие механическое качество микросцепления цемента с костью: тщательность очистки костного ложа перед цементированием, прочность и местные регенеративные возможности кости, качество смешивания цемента, использование устройства герметичной подачи цемента. Для комплексного решения задачи по улучшению качества цементной фиксации разработана система мероприятий. Основными из них являются: дистальная заглушка канала бедренной кости, ретроградное заполнение бедренного канала костным цементом, дренирование бедренного костномозгового канала в процессе его заполнения цементом, формирование отверстий в вертлужной впадине для фиксации вертлужного компонента, вакуумное смешивание цемента, промывание цементируемой поверхности кости пульсирующей струей (пульсационный лаваж), чистка цементируемой поверхности нейлоновыми щеточками, дегидратация костной поверхности перед цементированием, прессуризация цемента при установке протеза. Имеются сведения о повышении эффективности цементирования при центрифугировании в процессе смешивания, Высокое качество подготовки цемента, его закладки в кость и равномерность распределения цементной мантии обеспечивается целым рядом разработанных устройств и оборудования, К ним относят: вакуумные смесители различных типов, предотвращающих формирование воздушных пузырей в цементной массе; специальные шприцы для ретроградной подачи цемента в полости, и, прежде всего, в канал бедренной кости; полиэтиленовые ограничительные заглушки и направители, формирующие цементную мантию в бедренном канале; наконец, устройства для прессуризации или вдавливания цемента в костные поры при его закладке. Применение усовершенствованной технологии цементирования позволило сократить количество ревизий по поводу инфекционных осложнений и замен имплантатов из-за асептического расшатывания.
Основные марки цемента различных фирм-производителей и тип полимера, виды мономера, соотношение жидкой и твердой частей основных марок костного цемента и максимальная температура их полимеризации (см. таблицу 2).

Остеопластика в стоматологии – наращивание костной ткани, необходимой для удачной имплантации. После того, как человеку удалили зуб, твердая ткань имеет свойство рассасываться, а новый искусственный зуб должен надежно держаться в челюсти. Наращивание кости для имплантации зубов успешно решает эту проблему, но требует дополнительных затрат и больше времени (чем, например, при одномоментной имплантации, когда объема ткани достаточно).
Остеопластика – что это такое, и зачем она нужна?
При внедрении титанового корня очень важно, чтобы он со всех сторон был окружен костью. Если есть дефицит ткани, то титановый штифт будет отторгаться. Более того, если корень установлен в верхнюю челюсть, есть риск задевания верхнечелюстных пазух, что может привести к серьезным ЛОР-заболеваниям. Также при недостатке кости имплантат будет расшатываться, опустится ниже десны, что скажется на эстетике протеза и общей картине.
Остеопластика рекомендована в таких случаях:
- если необходимо установить корень в зону, где свой зуб был удален несколько лет (или месяцев) тому назад;
- если у пациента анатомически большие гайморовые пазухи;
- когда физиологически у человека минимальный объем твердой ткани.
Операция не выполняется, если:
- у пациента хронические ЛОР-заболевания (гаймориты, синуситы, риниты);
- нехватка кальция в организме;
- есть патологии в строении дыхательной системы;
- онкология;
- полипы и другие образования в носу;
- сахарный диабет.
Также остеопластика не выполняется беременным и кормящим женщинам. В остальном, операция делается относительно быстро и с гарантией.
Во многих случаях пациентам перед операцией рекомендуют пропить курс гормональных препаратов и антибиотиков, чтобы нейтрализовать отечные состояния и возможные воспаления.
Как наращивается костный материал в стоматологии?
- вводится местная анестезия;
- надрезается часть десны и надкостницы, тем самым обнажая кость;
- в зависимости от выбранной методики, наращивается твердая ткань;
- на рану накладываются швы;
- стоматолог рекомендует пациенту несколько дней принимать противовоспалительные средства и обезболивающие таблетки.
Типы костной ткани в стоматологии
- аллотрансплантат – синтетическая костная ткань в стоматологии, которая создается в лабораторных условиях. Это искусственный материал, который не всегда успешно приживается;
- внутриротовой аутотрансплантат – собственная костная ткань пациента, которая была взята из других зон ротовой полости. Например, из самой дальней части зубного ряда. Подобная процедура наращивания называется аутотрансплантацией;
- аллогенный костный материал в хирургической стоматологии – человеческая кость, донором которой является другой пациент. Высокие показатели приживаемости, но пациента может смущать, что этот материал взят из трупной кости, хоть и хранился в стерильной упаковке;
- ксенотрансплантат – заменитель костной ткани в современной стоматологии, материал животного происхождения. Заимствуется из костей крупного рогатого скота. Один из самых востребованных материалов для трансплантации, когда требуется большой объем твердой ткани;
- гранулы гидроксиапатита – искусственный костный трансплантат в стоматологии.
Определить конкретный вид костного материала в стоматологии вам поможет опытный стоматолог-имплантолог, который изучит состояние пациента, особенности ткани и оценит будущий фронт работ по восстановлению зубного ряда.
Плюсы и минусы костной пластики при имплантации
Конкурентные преимущества костной пластики:
- восстановление функций, даже если у пациента утрачен большое количество твердой ткани;
- нормализуется внешний вид десневой ткани и ротовой полости в целом;
- восстановление жевательных функций – все виды костной ткани в стоматологии адаптированы под большие нагрузки;
- возможность восстановить зубной ряд, даже в самых запущенных ситуациях.
Недостатки костной пластики:
- реабилитация занимает несколько месяцев;
- высок риск отторжения блока;
- болевые ощущения в процессе приживления тканей;
- немалая цена операции.
Стоимость костной пластики в Москве
Цена операции зависит от следующих факторов:
- какие используются остеопластические материалы в хирургической стоматологии;
- сколько ткани необходимо внедрить;
- метода остеопластики;
- выбранной клиники.
В среднем, замещающий материал стоит от 17 000 р. за один грамм. К этой сумме еще необходимо добавить цену мембраны (около 10 000 р.), забор и подсадку блока – от 90 000 р. Бюджет немалый (с учетом того, что еще необходимо доплатить за искусственный корень, абатмент и коронку), но он окупается надежностью и гарантией длительной эксплуатации нового зуба.
Если у вас есть симптомы описанные в этой статье, обязательно запишитесь на приём в нашу клинику.
Не занимайтесь самолечением! Даже самая маленькая проблема, при не правильном лечении, может значительно осложнить вашу жизнь.
Обращаясь к нам, вы можете быть уверены что:
В России создали искусственный скелет. Он поднимет на ноги тысячи людей
Тонкая работа
Пациентке, 52-летней женщине, два года назад удалили опухоль вместе с тканями и органами малого таза. В 2019 году произошел рецидив онкологического заболевания в более агрессивной и быстро прогрессирующей форме. Новообразование возникло в шейке мочевого пузыря, затронуло прямую кишку, матку и лобковую кость, которую пришлось удалить для спасения жизни больной. Лобковая кость удерживает подвздошные кости и замыкает собой тазовое кольцо, а также позволяет нижним конечностям поддерживать тело, поэтому ее резекция приводит к тому, что пациент больше не может ходить и сидеть и остается прикованным к постели.
Чтобы дать женщине возможность ходить, врачи провели третью операцию, целью которой было вживление протеза лобковой кости. Для этого они создали титановую конструкцию, которая по форме соответствует удаленной части таза, но гораздо прочнее. Компьютерная томография позволила определить размеры реплики, необходимой для замены костного материала, а 3D-принтер на основе этих данных распечатал имплантат. Выбор металла обусловлен тем, что титан не окисляется в организме, что обеспечивает его долговечность. Пористая структура эндопротеза позволяет оставшимся костям таза крепко срастись с ним.
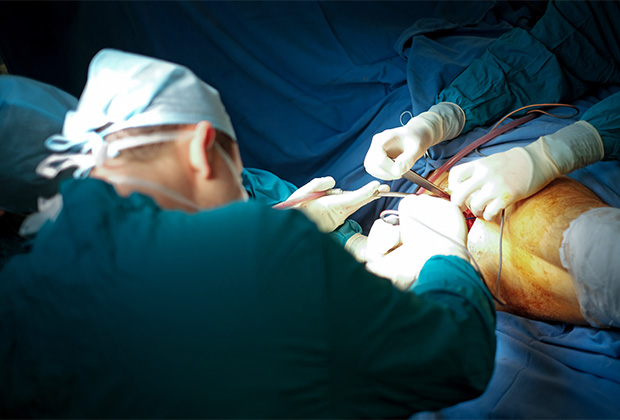
Фото: Николай Хижняк / РИА Новости
Операция прошла успешно, а реабилитация, по оценкам специалистов, продлится не более трех месяцев. Подобные хирургические вмешательства выполняются в нескольких медицинских учреждениях России, однако эндопротезирование передних костей таза проводится впервые. Врачи уверены, что в скором времени титановые импланты, распечатанные на 3D-принтере, станут более доступными, и такие операции начнут проводить повсеместно.
Титановые скелеты
Эндопротезы — это протезы, которые располагаются внутри человеческого тела. Они, как правило, анатомически соответствуют той части организма, которую заменяют, например, кости или суставу. Имплантат, вживленный вместо поврежденного сустава, позволяют человеку совершать обычные движения, срок его службы достигает нескольких десятилетий, после чего его заменяют новым. Протезы изготавливают из титана, металлических сплавов, устойчивых к изнашиванию и окислению, керамики или особо прочных пластмасс. Иногда используют кусочки костей самого пациента, которые фиксируются для дальнейшего роста костной ткани и сращения.
Титан является одним из лучших материалов для этих целей, так как обладает высокой прочностью и долговечностью. Он биологически инертен, то есть не вступает в реакцию с тканями организма. Предпочтение обычно отдается чистому титану (или некоторым специфическим сплавам вроде никелида титана), поскольку смешивание с другими металлами может способствовать гальванической коррозии. Для изготовления протезов с помощью 3D-принтера используется металлический порошок, который спекается с помощью лазеров в строго контролируемых условиях.
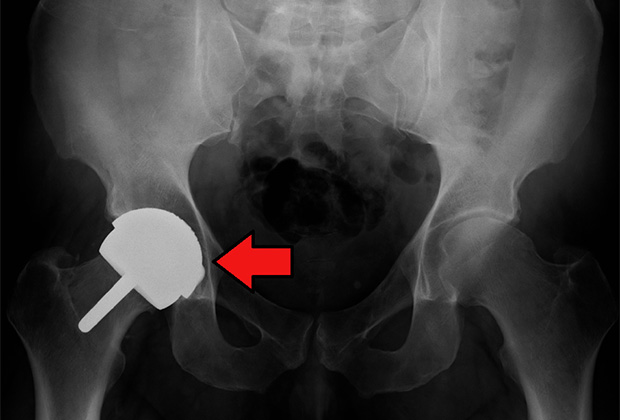
Эндопротез тазобедренного сустава
Технология будущего
При 3D-печати детали печатаются послойно, а каждый новый слой спекается с помощью лазерного луча, что позволяет придать протезу нужную форму. В других случаях используется электронно-лучевая плавка, при которой вместо лазеров применяются электронные пушки — устройства, излучающие пучки электронов с заданной кинетической энергией. Результаты различных экспериментов продемонстрировали, что аддитивные технологии позволяют создавать протезы сложной конфигурации, такие как, например, череп, позвонки и грудная клетка. Эти имплантаты уже использовались для успешного лечения пациентов с онкологическими заболеваниями костной ткани.
Поры позволяют живым тканям организма крепко закрепиться в имплантате. Клетки проникают во внутренние структуры протеза и, разрастаясь там, обеспечивают прочность соединения. Кроме того, поры можно наполнять лекарственными веществами, предотвращающими гибель клеток, ускоряющими заживление и препятствующими инфицированию патогенными микроорганизмами. В результате приживаемость протезов увеличивается в несколько раз по сравнению с традиционными имплантатами.

Фото: Amir Cohen / Reuters
Не хуже других
В США и других странах протезирование распечатанных на принтере имплантатов начали проводить довольно давно, что позволило пациентам, казалось бы, обреченным на инвалидность, вернуться к нормальной жизни. В последнее десятилетие 3D-печать в России тоже стала очень популярной, но только сейчас она стала активно внедряться в эндопротезировании. Это объясняется тем, что развитие технологии способствовало удешевлению оборудования, которое раньше из-за своей дороговизны (десятки миллионов рублей) не было доступно отечественным клиникам. Операции с использованием 3D-принтеров, несмотря на высокую потребность пациентов в качественных протезах, были очень редкими.
В 2017 году ученые из Тюменского государственного медицинского университета (ТГМУ) распечатали полимерный протез бедренной кости для замены изношенного импланта. В том же году в Самаре врачи провели тестирование методов печати суставных протезов для лечения пациентов с артрозом. В 2018 году в ТГМУ был протестирован аддитивный подход для создания заменителей костей из титанового сплава. Похоже, российские врачи стали понимать, что 3D-печать обладает рядом преимуществ перед обычными методами протезирования, а первые успешные операции доказывают конкурентоспособность технологии.
Читайте также:


