Костная пластика большеберцовой кости
КОСТНАЯ ПЛАСТИКА (греч, plastike ваяние, пластика; син. остеопластика) — хирургическая операция, производимая для восстановления целости или изменения формы кости, а также с целью стимуляции регенераторных процессов в костной ткани и связанная с перемещением собственных или чужеродных костных фрагментов. Существует три основных вида Костной пластики: аутопластика (см.), при к-рой используют собственные кости оперируемого; аллопластика [прежний термин — гомопластика (см.)], когда используют кости другого индивидуума, принадлежащего к тому же виду, и ксенопластика [прежний термин — гетеропластика (см.)] — пересадка кости, взятой от организма другого биол. вида. Костная пластика может быть свободной, когда пересаживаемый фрагмент полностью отделяют от материнской кости, и несвободной — трансплантат сохраняет связь с материнской костью. К. п. применяется: как самостоятельная операция с целью возмещения дефекта кости, восстановления целости или изменения формы кости; для стимуляции костной регенерации как компонент основной операции, напр, как дополнение при металлоостеосинтезе; как комбинированная Костная пластика, когда один костный трансплантат (обычно алло-) служит фиксатором костных фрагментов, а второй (чаще ауто-) является строительным материалом для мозоли и стимулятором костной регенерации.
Попытки пересадки костной ткани человеку производились в глубокой древности. Научно обоснованные пластические пересадки кости были начаты в 19 р. Вальтер (Ph. Walther, 1821) и Вольфф (J. Wolff, 1863) сообщили об успешной трансплантации костных отломков черепа. Макъюин (W. Macewen, 1882) удалил у трехлетнего мальчика почти весь диафиз плечевой кости, пораженной остеомиелитом. Через два года образовавшийся дефект плечевой кости был замещен аллотрансплантатом, полученным из ампутированной конечности другого больного. А. Понсе (1887) при лечении ложного сустава большеберцовой кости произвел пересадку фаланги большого пальца стопы, взятого из ампутированной конечности.
Основоположником костно-пластической хирургии в нашей стране является Н. И. Пирогов, который в 1852 г. произвел ампутацию стопы, пересадив на резецированную суставную поверхность большеберцовой кости задний отдел пяточной кости вместе с мягкими тканями. Своей операцией Н. И. Пирогов положил начало трансплантации кости на питающей ножке.
В 1910 —1914 гг. H. Н. Петровым, Н. И. Башкирцевым и А. А. Немиловым были произведены эксперименты для выяснения вопроса об источниках регенерации пересаженной кости. Согласно этим исследованиям, при свободной пластике костей постепенно отмирают все элементы трансплантата.
В образовании новой кости принимают участие как клеточные элементы костного ложа и отчасти самого трансплантата, так и клетки окружающей внекостной соединительной ткани. Костный трансплантат, как правило, постепенно замещается костной тканью, происходящей из тканей ложа реципиента, сам же трансплантат исполняет роль каркаса для этого регенерата.
Считается установленным, что костная ткань трансплантата при пересадке хотя и лишается своих остеоцитов, но сохраняет свои жизненные свойства в основном веществе, проявляющиеся в процессах рассасывания и созидания. Ткань трансплантата, рассасываясь, замещается новообразованной костью. Этот процесс означает не гибель трансплантата в обычном понимании этого слова, а перестройку его, т. е. процесс физиологический. Возникающий на основе трансплантата регенерат не является его полной копией. Форма регенерата определяется функциональными особенностями области трансплантации. Для ауто- и аллопластики характерны общие закономерности регенерации, но при аллопластике она протекает более замедленно, что связано с необходимостью преодоления иммунол, несовместимости ткани (см. Несовместимость иммунологическая). Поэтому более благоприятными для Костной пластики являются аутотрансплантаты. Быстрее других перестраиваются трансплантаты, богатые спонгиозной тканью,— их используют преимущественно для стимулирования регенерации. Вид трансплантата определяется целью К. п. Так, при лечении ложных суставов применяют прочные массивные кортикальные трансплантаты. Для замещения костных полостей обычно применяют фрагментированные трансплантаты в виде щебенки или стружки. Трансплантаты берут обычно из большеберцовой кости, из крыла подвздошной кости и реже из других костей. Несмотря на то что по биол, свойствам аутопластика является лучшим методом, она не может полностью удовлетворить возрастающие запросы костно-пластической хирургии из-за своих ограниченных возможностей в смысле количества, размеров и формы трансплантатов. Поэтому все большее значение в травматологии и ортопедии приобретает костная аллопластика.
Способы заготовки и консервации аллогенной костной ткани изучены подробно, благодаря чему алло-трансплантация широко вошла в практику костно-пластической хирургии. Разработаны методы консервации трансплантатов в жидких и плотных средах, консервации охлаждением, замораживанием, лиофилизацией и т. д. (см. Консервирование органов и тканей). Большое практическое значение имела организация костных банков для заготовки и хранения аллотрансплантатов. Определенное распространение получила разновидность аллопластики — брефопластика (см.).
Ксенопластика применяется крайне редко. Ксеногенные ткани заготавливают для клин, целей от животных. Ксенотрансплантаты используют в виде вываренной, мацерированной или консервированной кости. Антигенные свойства ксеногенных тканей, как и аллотрансплантатов, могут быть в значительной степени ослаблены консервированием. Ксенотрансплантаты также замещаются новообразованной костью, но этот процесс длится значительно дольше, чем при аутопластике. В связи с этим возможно (при необходимости) сочетание медленно рассасывающегося ксенотрансплантата как фиксатора и более ценного в биол, отношении аутотрансплантата.
Показания и Противопоказания
Костная ауто- и аллопластика показана при оперативном лечении несросшихся переломов, ложных суставов и дефектов костей, при проведении переднего или заднего спондилодеза (см.), артродеза (см.), пластических операций на суставах, при ампутациях и различных реконструктивных операциях на костях.
Замещение суставных концов костей диафизов или целиком отдельных костей (напр., при злокачественных опухолях последних) получило заметное распространение, что связано с развитием методов приготовления костных аллотрансплантатов больших размеров.
Противопоказанием для К. п. является наличие сопутствующих воспалительных явлений, кожных поражений в виде язв, фурункулов, пиодермии и т. д. Однако К. п. в некоторых случаях используется при оперативном лечении остеомиелита и инфицированных ложных суставов.
Техника
Общие требования, предъявляемые к технике операции, сводятся к строгой асептике, бережному обращению с тканями, тщательной остановке кровотечения, правильной подгонке трансплантата для плотного его контакта с ложем реципиента на возможно большей площади, тщательному покрытию его мягкими тканями с послойным ушиванием раны и наложением фиксирующей повязки. Выбор способа К. п. определяется в основном особенностями местного процесса.
Внедрение в практику ультразвуковых инструментов для резки и соединения костей значительно облегчило выполнение многих костнопластических операций. С помощью ультразвука стало возможным готовить трансплантаты и ложе для них любой необходимой формы, а также прочно соединять костные фрагменты (см. Ультразвук в травматологии).

Пластика скользящим трансплантатом по Xахутову производится гл. обр. при ложных суставах большеберцовой кости без диастаза. Из передневнутренней поверхности кости после продольного разреза надкостницы циркулярной пилой выпиливают широкую костную пластинку длиной в 15—20 и шириной в 1 —1,5 см (из обоих концов кости до костномозгового канала). После получения трансплантата края отломков освобождают от рубцовой ткани, щель ложного сустава заполняют костной стружкой. Трансплантат поворачивают на 180° (дистальный конец его становится проксимальным), перекрывая место ложного сустава, и укрепляют его кетгутовыми швами и, если необходимо, винтами (рис. 1).
Пластику по Гревсу—Бруну применяют при ложных суставах с дефектом кости. После поднадкостничного выделения отломков вскрывают костномозговые полости, костный дефект заполняют трансплантатом, взятым из большеберцовой кости вместе с надкостницей и слоем губчатого вещества. Свободное пространство между отломками, кроме того, заполняют костными стружками и осколками, полученными при обработке концов отломков. Эта операция применяется редко.
Пластика по Матти. При этом виде К. п. производят освежение концов отломков, вскрывают костномозговые полости и в отломках выдалбливают глубокие желоба длиной 6—8 см. После сопоставления отломков желоба заполняют губчатым веществом кости, взятого из большого вертела или из большеберцовой кости, а также стружками, полученными при образовании желобов.

Пластика по Фемистеру показана при фиброзных ложных суставах без смещения отломков. Поднадкостнично освобождают в зоне ложного сустава отломки и, не нарушая фиброзного соединения, укладывают трансплантат, перекрывая щель ложного сустава. Трансплантат берут из крыла подвздошной кости или из большеберцовой кости (рис. 2).

Пластика пристеночным трансплантатом по Богданову производится в сочетании с металлическим остеосинтезом (см.). Поднадкостнично выделяют концы отломков, составляющих ложный сустав, вскрывают костномозговые полости, сопоставляют отломки и фиксируют их металлическим штифтом внутрикостно или металлической пластинкой. После этого на освеженную боковую поверхность обоих отломков укладывают ауто- или аллотрансплантат из компактного вещества кости и фиксируют его кетгутом (рис. 3). Этот метод часто применяют при диафизарных ложных суставах без большого укорочения.

Интраэкстрамедуллярную пластику по Чаклину применяют для лечения ложных суставов и обширных дефектов длинных трубчатых костей. Производят экономное освежение концов отломков и их сопоставление. Интрамедуллярный трансплантат берут из проксимального конца большеберцовой кости без надкостницы, экстрамедуллярный — с надкостницей. Трансплантат без надкостницы вбивают поочередно в костномозговую полость обоих отломков, а трансплантат с надкостницей укладывают снаружи в подготовленное ложе и укрепляют кетгутом (рис. 4).
Костная пластика по типу вязанки хвороста. В 1961 г. М. В. Волков предложил метод замещения костных дефектов и полостей тонкими пластинами замороженной кортикальной аллогенной кости без надкостницы, фиксированными друг с другом кетгутовыми циркулярными швами в связку, напоминающую вязанку хвороста.
Несвободная пластика. Для замещения дефекта одной из двух парных костей голени (большеберцовой) или предплечья (лучевой кости) производят несвободную пересадку одной кости в другую. Напр., метод Гана заключается в замещении дефекта большеберцовой кости фрагментом малоберцовой. После пересадки малоберцовая кость значительно утолщается и выполняет функцию большеберцовой кости. Операцию производят в два этапа. Обнажают проксимальный фрагмент большеберцовой кости и на передней ее поверхности выдалбливают желоб, в который помещают дистальный конец резецированной на этом же уровне малоберцовой кости. Вторым этапом производят подобную же операцию и на дистальных фрагментах большеберцовой и малоберцовой костей.
Реконструктивная костная пластика. К. п. входит составным элементом в различные реконструктивные операции, напр, исправление деформаций, замещение суставных концов костей, удлинение конечности и др. Исправление деформации и удлинение кости производят с помощью дистракционно-компрессионных аппаратов (методы Илизарова, Дедовой, Вассерштейна) или с помощью различного вида остеотомий (методы Богданова, Богораза, Шпрингера).

Метод замещения дефектов трубчатых костей путем удлинения одного из отломков был предложен Г. А. Илизаровым в 1967 г. Он основан на том, что постепенная дистракция костных отломков активизирует костную регенерацию на месте возникновения диастаза. Производят косую остеотомию одного из отломков, чаще всего в области верхнего метаэпифиза. Отделенный фрагмент низводят в зону дефекта направляющими спицами по 0,25 мм 3—4 раза в день до контакта с противостоящим концом отломка. После окончания дистракции создают компрессию на стыке отломков (рис. 5).
Оперативное удлинение голени по методу Дедовой заключается в Z-об-разном удлинении пяточного (ахиллова) сухожилия, сухожилий длинной, короткой малоберцовой мышц и передней большеберцовой, косой остеотомии малоберцовой кости, Z-образной остеотомии большеберцовой кости с фиксацией костных фрагментов на дистракционном аппарате Гудушаури. Удлинение следует начинать не ранее 10— 12 дней после операции и проводить его постепенно. По окончании периода растяжения конечность фиксируют тем же аппаратом в течение 3 мес.
Метод Вассерштейна — дистракционно-компрессионным метод удлинения бедра или голени при укорочении конечности не менее 4 см с применением трубчатого аллотрансплантата. Операцию производят в два этапа. Сначала удлиняют сухожилия функционирующих мышц, а затем делают поперечную остеотомию бедренной кости и вводят интрамедуллярно металлический штифт. С помощью дистракционного аппарата через 7 дней после операции производят дистракцию ежедневно по 2 мм до величины необходимого удлинения. На втором этапе диастаз между отломками замещается костным трубчатым аллотрансплантатом. На трансплантате предварительно создается продольный паз соответственно толщине сечения металлического штифта. Отломки с трансплантатом подвергают компрессии тем же аппаратом.
Сегментарная остеотомия по Богданову заключается во множественном поперечном рассечении кости, исправлении деформации и фиксации костных фрагментов металлическим штифтом, который создает условия для восстановления структуры и формы трубчатой кости.
Сегментарная остеотомия по Богоразу производится при необходимости исправления укорочения и искривления бедра. Бедренную кость чрезнадкостнично рассекают двумя сечениями на косые сегменты и затем подвергают дистракции скелетным вытяжением.
Операцию Шпрингера производят для исправления больших рахитических искривлений голени. Поднадкостнично обнажают и резецируют большеберцовую кость у верхней и нижней границы искривления. Свободный фрагмент кости вынимают и распиливают на сегменты высотой в 1—2 см. Малоберцовую кость пересекают и голень выравнивают. В периостальный футляр укладывают один за другим костные сегменты в одну линию, для чего часть из них поворачивают на 180°.
Библиография:
Волков М. В. Костная патология детского возраста, с. 65, М., 1968; Имамалиев А. С. Гомопластика суставных концов Костей, М., 1975, библиогр.; Коваленко П. П. Клиническая трансплантология, Ростов н/Д., 1975, библиогр.; Консервирование и трансплантация тканей и органов, под ред. Г. Крыстинова, пер. с болг., т. 2, с. 203, София, 1975, библиогр.; Надеин А. П. Биологические обоснования трансплантации костной гомоткани и методы ее консервации, Л., 1969, библиогр.; Пирогов Н. И. Костнопластическое удлинение костей голени при вылущении стопы, Воен.-мед. журн., ч. 63, № 2, отд. 2, с. 83, 1854; Радзимовский И. В. О реплантации и трансплантации костей, дисс., Киев, 1881; Tкаченко С. С. Костная гомопластика, Л., 1970, библиогр.; Чрескостный компрессионный и дистракционный остеосинтез в травматологии и ортопедии, под ред. Г. А. Илизарова, в. 2, Курган, 1976; Axhausen G. Die histologischen und. klinischen Gesetze der freien Osteoplastik auf Grund von Tierversuohen, Arch. klin. Chir., Bd 88, S. 23, 1909; Cech O. Paklouby dlouhych kosti, Praha. 1976; Inclan A. Use of preserved bone graft in orthopaedic surgery, J. Bone Jt Surg.,v. 24, p. 81, 1942; Oilier L. Traite experimental et clinique de la regeneration des os et de la production artificielle du tissu osseux, t. 1—2, P., 1867.
В. А. Чернавский, А. С. Имамалиев.

По данным литературы, доля заболеваний коленного сустава среди всех случаев дегенеративно-дистрофических заболеваний суставов конечностей составляет от 21,9 до 29%, причем в 86% случаев страдают лица трудоспособного возраста, у которых прогрессирование заболевания в течение 10-15 лет приводит к инвалидности в 6,2-14,6% случаев [1]. Зачастую методом выбора при лечении пациентов с дегенеративно-дистрофическими заболеваниями суставов становится тотальное эндопротезирование. Одной из проблем, которую нужно решить в процессе тотального эндопротезирования сустава, это замещение костных дефектов в ложе эндопротеза. Их доля при заболеваниях коленного сустава составляет от 25 до 31% [2].
Причинами формирования дефектов и, как следствие, грубых деформаций являются:
- асептический некроз мыщелков, который, по данным различных авторов, составляет от 8 до 22% всех дегенеративно-дистрофических заболеваний коленного сустава,
- кистовидная перестройка эпифизов бедренной и большеберцовой костей,
- посттравматическая импрессия суставной поверхности 5.
Существует достаточное количество классификаций костных дефектов при первичном и ревизионном эндопротезировании коленного сустава [7]. Мы используем наиболее удобную, нашедшую широкое клиническое и научное применение классификацию AORI, разработанную G.A. Engh в Anderson Ortopaedic Research Institute (AORI США, 1997) [8]. Классификация основана на дооперационной рентгенологической оценке состояния костей, с помощью предварительно заданных критериев. В соответствии с этой классификацией выделяют четыре типа состояния бедренной или большеберцовой костей:
1 тип – интактная кость;
2А тип – повреждённая губчатая кость, кость противоположного мыщелка остается неизменной;
2В тип – симметричная потеря костной массы с вовлечением обоих мыщелков или плато;
3 тип – повреждение губчатой и кортикальной кости.
Классификация AORI достаточно четко показывает корреляцию наличия и размеров костных дефектов с ростом потребности использовать металлические блоки, клинья и/или структурированные трансплантаты. У данной методики существует лишь один минус. По современным данным, в группах I и IIA дефекты кости до 5 мм в 46% случаев посредством дооперационных рентгенограмм диагностированы не были [9].
При выполнении тотального эндопротезирования коленного сустава (ТЭКС) преследуется основная цель – создание долговременной надежной опоры для компонента эндопротеза. В случае имеющегося костного дефекта она может достигаться такими способами, как:
- резекция по дну дефекта,
- цементная пластика с армированием или без армирования,
- замещение металлическим блоком,
- костная аллопластика 10.
При детальном рассмотрении у каждого метода отмечаются свои преимущества и недостатки. Преимуществом замещения костного дефекта путем выполнения резекции по дну дефекта является простота и быстрота выполнения. Недостатком становится снижение количества ткани большеберцовой кости в дистальном направлении. Не исключена ситуация, что на максимальном вкладыше стабильность сустава не будет достигнута. Кроме того, при возникновении необходимости выполнения реэндопротезирования у этой группы пациентов хирург может столкнуться с такой проблемой, как обширный дефект большеберцовой кости. Таким образом, этот вариант замещения костного дефекта не является методом выбора. Его применение допустимо при неглубоких дефектах [12]. По нашим данным, резекция по дну дефекта выполнена у 5% пациентов с имеющимся костным дефектом.
Замещение костного дефекта путем цементной пластики с армированием или без армирования винтами также отличается простотой и дешевизной. Недостатки метода заключаются в том, что непросто добиться адекватной прессуризации цемента при нарушении целостности кортикальной кости. Изменение объема цемента во время полимеризации может достигать 2%. Неравномерное распределение нагрузки на подлежащую кость при эксцентрически действующих силах может приводить к нарушению прочности фиксации. Этот метод используется для замещения достаточно глубоких дефектов, при условии соблюдения правил прессуризации цемента и планирования вектора нагрузки [12]. По нашим данным, такое замещение выполнено у 82% пациентов с имеющимся костным дефектом.
Преимущество метода замещения костного дефекта путем костной аутопластики заключается в максимальном сохранении костной ткани метаэпифиза. К недостаткам метода относятся: существенные ограничения в выборе размера трансплантата, риск коллапса, если структура трансплантата повреждена патологическим процессом, и риск несращения. Метод применяется при наличии трансплантата с соответствующими характеристиками (размер, плотность). По нашим данным, такое замещение выполнено у 7% пациентов с имеющимся костным дефектом.
Достоинством замещения костного дефекта металлическим блоком или клином следует считать быстрое создание надежной опоры для имплантата, даже в условиях обширных дефектов. К недостаткам метода относятся ограничения по размеру и форме трансплантата, необходимость специальных инструментов и компонентов эндопротеза. Увеличивается общая стоимость имплантата. При наличии специального инструментария и соблюдении правил имплантации метод применим для замещения любых дефектов [12; 13]. По нашим данным, замещение костного дефекта этим методом выполнено у 6% пациентов.
Цель исследования: улучшить результаты первичного эндопротезирования коленного сустава у пациентов, имеющих костный дефект большеберцовой кости до 2А по AORI.
Материал и методы. В Новосибирском НИИТО за 2012-2015 годы выполнено 7096 операций первичного эндопротезирования коленных суставов. В 2157 (30,4%) случаях был диагностирован требующий замещения костный дефект как бедренной, так и большеберцовой кости [14].
С целью восстановления биомеханики коленного сустава и создания долговременной надежной опоры для компонентов эндопротеза у пациентов, имеющих костный дефект большеберцовой кости до 2А по AORI, нами разработан и внедрен в клиническую практику способ аутопластики большеберцовой кости при первичном эндопротезировании коленного сустава.
Данная методика выполняется соответственно стандартным этапам эндопротезирования, но имеет некоторые особенности: после выполнения резекции суставной поверхности большеберцовой кости определяется остаточный костный дефицит мыщелка большеберцовой кости. По классификации AORI для аутопластики допускается дефицит не больше T2А. При формирования межмыщелкового бокса бедренной кости производится одновременный забор аутокости. Производится обработка костного аутотрансплантата до придания ему правильной геометрической формы (рис. 1).
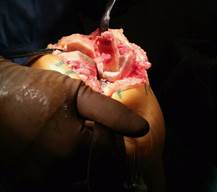
Рис. 1. Забор аутотрансплантата, придание ему правильной геометрической формы
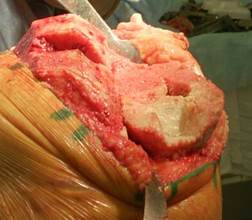
Рис. 2. Обработанный дефект большеберцовой кости со
сформированной опорной площадкой
В последующем аутотрансплантат устанавливается в сформированное ложе и производится импакция до фиксации (рис. 3).
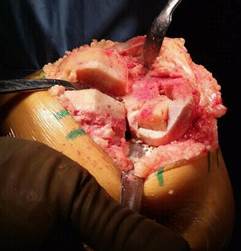
Рис. 3. Импакция аутотрансплантата в сформированном ложе
Дальнейший ход операции соответствует стандартным этапам при первичном эндопротезировании коленного сустава. Восстановительный период не имеет каких-либо особенностей по сравнению со стандартным течением [15].
Клинический пример. Пациент С., 65 лет. Диагноз: левосторонний посттравматический гонартроз 3 степени. Дефект медиального мыщелка левой большеберцовой кости. Варусная деформация левой нижней конечности. Комбинированная контрактура левого коленного сустава. Синдром левосторонней гоналгии (рис. 4).
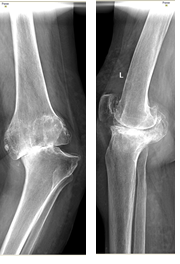
Рис. 4. Рентгенограмма коленного сустава в прямой и боковой проекциях
Пациенту проведено оперативное лечение: эндопротезирование левого коленного сустава с аутопластикой медиального мыщелка большеберцовой кости. Послеоперационный период протекал без особенностей, пациенту была проведена стандартная реабилитация.
На контрольных осмотрах через 6 месяцев, 1 и 2 года после проведенного хирургического лечения пациент отметил хороший результат проведенного лечения, выражающийся в увеличении объема движений в коленном суставе, повышении его стабильности и восстановлении нормальной оси конечности. На контрольной рентгенограмме коленного сустава через 2 года после операции аутотрансплантат состоятелен (рис. 5).
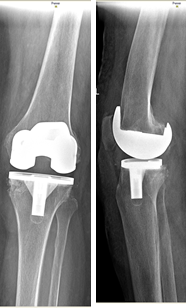
Рис. 5. Контрольная рентгенограмма коленного сустава в прямой и
боковой проекциях через 2 года после операции
Таким образом, у пациентов, имеющих костный дефект большеберцовой кости 2А по AORI, при первичном эндопротезировании коленного сустава выполнение аутопластики по разработанной методике приводит к хорошим результатам, выражающимся в создании долговременной надежной опоры для компонентов эндопротеза, что увеличивает срок его службы за счет нормализации распределения нагрузок в прооперированном коленном суставе.
1. При первичном эндопротезировании коленного сустава максимальное сохранение костной ткани облегчает хирургическую тактику при последующих хирургических вмешательствах, что очень важно у молодых пациентов.
3. Аутопластика должна выполняться при отсутствии противопоказаний.
Костная пластика (греч. plastike ваяние, пластика; син. остеопластика) — хирургическая операция, производимая для восстановления целости или изменения формы кости человека, а также с целью стимуляции регенераторных процессов в костной ткани и связанная с перемещением собственных или чужеродных костных фрагментов.
Виды костной пластики
Существует три основных вида костной пластики:
- аутопластика, при которой используют собственные кости оперируемого;
- аллопластика, когда используют кости другого индивидуума, принадлежащего к тому же виду;
- ксенопластика [прежний термин — гетеропластика] — пересадка кости, взятой от организма другого биологического вида.
Костная пластика может быть:
- свободной, когда пересаживаемый фрагмент полностью отделяют от материнской кости,
- и несвободной — трансплантат сохраняет связь с материнской костью.
Костная пластика применяется:
- как самостоятельная операция с целью возмещения дефекта кости, восстановления целости или изменения формы кости;
- для стимуляции костной регенерации как компонент основной операции, например как дополнение при металл остеосинтезе;
- как комбинированная КП, когда один костный трансплантат (обычно алло-) служит фиксатором костных фрагментов, а второй (чаще ауто-) является строительным материалом для мозоли и стимулятором костной регенерации.
Показания для костной пластики
Костная ауто- и аллопластика показана при:
- оперативном лечении несросшихся переломов, ложных суставов и дефектов костей,
- проведении переднего или заднего спондилодеза, артродеза, пластических операций на суставах,
- ампутациях и различных реконструктивных операциях на костях.
Замещение суставных концов костей диафизов или целиком отдельных костей (напр., при злокачественных опухолях последних) получило заметное распространение, что связано с развитием методов приготовления костных алло трансплантатов больших размеров.
Противопоказанием для К. п. является наличие сопутствующих воспалительных явлений, кожных поражений в виде язв, фурункулов, пиодермии и т. д. Однако К. п. в некоторых случаях используется при оперативном лечении остеомиелита и инфицированных ложных суставов.
Пластика скользящим трансплантатом по Xахутову производится гл. обр. при ложных суставах большеберцовой кости без диастаза. Из передневнутренней поверхности кости после продольного разреза надкостницы циркулярной пилой выпиливают широкую костную пластинку длиной в 15—20 и шириной в 1—1,5 см (из обоих концов кости до костномозгового канала). После получения трансплантата края отломков освобождают от рубцовой ткани, щель ложного сустава заполняют костной стружкой. Трансплантат поворачивают на 180° (дистальный конец его становится проксимальным), перекрывая место ложного сустава, и укрепляют его кетгутовыми швами и, если необходимо, винтами.
Пластику по Гревсу — Вруну применяют при ложных суставах с дефектом кости. После под надкостничного выделения отломков вскрывают костномозговые полости, костный дефект заполняют трансплантатом, взятым из большеберцовой кости вместе с надкостницей и слоем губчатого вещества. Свободное пространство между отломками, кроме того, заполняют костными стружками и осколками, полученными при обработке концов отломков. Эта операция применяется редко.
Пластика по Матти. При этом виде К. п. производят освежение концов отломков, вскрывают костномозговые полости и в отломках выдалбливают глубокие желоба длиной 6—8 см. После сопоставления отломков желоба заполняют губчатым веществом кости, взятого из большого вертела или из большеберцовой кости, а также стружками, полученными при образовании желобов.
Пластика по Фемистеру показана при фиброзных ложных суставах без смещения отломков. Поднадкостнично освобождают в зоне ложного сустава отломки и, не нарушая фиброзного соединения, укладывают трансплантат, перекрывая щель ложного сустава. Трансплантат берут из крыла подвздошной кости или из большеберцовой кости.
Пластика пристеночным трансплантатом по Богданову производится в сочетании с металлическим остеосинтезом. Поднадкостнично выделяют концы отломков, составляющих ложный сустав, вскрывают костномозговые полости, сопоставляют отломки и фиксируют их металлическим штифтом внутрикостно или металлической пластинкой. После этого на освеженную боковую поверхность обоих отломков укладывают ауто- или алло трансплантат, метод часто применяют при ложных суставах без большого укорочения.
В зоне ложного сустава долотом сбивают тонкие пластинки кортикального слоя вместе с покрывающей их надкостницей и мышцами. Т. о., вокруг зоны повреждения кости создается костно-надкостничный футляр с сохраненной васкуляризацией и иннервацией, что обеспечивает благоприятные условия остеогенеза. После производства основной костно-пластической операции рану послойно зашивают.
Интраэкстрамедулярную пластику по Чаклину применяют для лечения ложных суставов и обширных дефектов длинных трубчатых костей. Производят экономное освежение концов отломков и их сопоставление. Интрамедуллярный трансплантат берут из проксимального конца большеберцовой кости без надкостницы, экстрамедуллярный — с надкостницей. Трансплантат без надкостницы вбивают поочередно в костномозговую полость обоих отломков, а трансплантат с надкостницей укладывают снаружи в подготовленное ложе и укрепляют кетгутом (рис. 4).
Костная пластика по типу вязанки хвороста. В 1961 г. М. В. Волков предложил метод замещения костных дефектов и полостей тонкими пластинами замороженной кортикальной аллогенной кости без надкостницы, фиксированными друг с другом кетгутовыми циркулярными швами в связку, напоминающую вязанку хвороста.
Кожная пластика. Показания. Виды и способы кожной пластики.
Кожная пластика — пересадка кожи разными способами, применяемая для закрытия раневой поверхности при свежих ранах.
Все виды кожной пластики можно разделить на два принципиальных варианта:
1) Свободная кожная пластика;
2) Несвободная кожная пластика.
а) ожоги III—IV степени (первичная пластика после ранней некрэктомии),
б) обширные кожные раны,
в) вяло гранулирующие и длительно не заживающие раны и язвы,
г) рубцовые деформации кожи различного происхождения,
д) устранение дефектов после удаления пигментных пятен и т. П
Свободная кожная пластика
Свободная кожная пластика имеет столетнюю историю. В 1869 г. Дж.Л. Реверден (J.L. Reverden) впервые перенёс несколько маленьких кусочков кожи на незаживающую гранулирующую поверхность в области локтя. Впоследствии С. Шкляровский (1870), А.С. Яценко (1871),
М.С. Янович-Чаинский (1871), а также Дж.С. Дэвис (J.S. Davis, 1917) подробно разработали и усовершенствовали пересадку кожи мелкими кусочками на гранулирующие поверхности ран.
Способ Яценко-Ревердена
Под местным обезболиванием скальпелем или бритвой срезают мелкие трансплантаты (тонкий слой эпидермиса) диаметром 0,3-0,5 см с наружной поверхности бедра, предплечья или передней брюшной стен- ки и переносят черепицеобразно на рану. Затем на рану с трансплантатами накладывают повязку с индифферентным жиром (вазелиновым маслом) на 8-10 сут. Метод применяют редко в связи с быстрым разрушением эпидермиса.
Последнее изменение этой страницы: 2016-07-11; Нарушение авторского права страницы
Читайте также:


