Микоплазмоз как внутриутробная инфекция
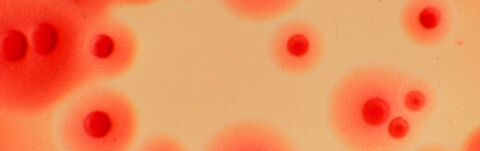
Микоплазмы — это такие микроорганизмы, которые занимают промежуточное звено между бактериями, вирусами и грибами. По свой форме такие бактериальные клетки напоминают мелкие шары или коротки нити, они лишены клеточной стенки и имеют небольшой размер, примерно 125-150 нм.
В большинстве случаев микоплазмы внедряются в клеточный эпителий мочеполовой и дыхательной системы человека, то есть паразитируют в клетках хозяина.
Виды микоплазм
Микоплазма относится к семейству Mycoplasmataceal. Данное семейство можно разделить на 2 вида.
К виду Mycoplasma относится свыше 100 видов микроорганизмов, но наиболее широко известны:
- Mycoplasma genitalium;
- Mycoplasma pneumonia;
- Mycoplasma hominis;
- Mycoplasma species.
Ureaplasma в свою очередь делится на 2 вида: ureaplasma parvum и ureaplasma urealiticum.
На сегодняшний день существует 6 видов микоплазм, которые наиболее часто вызывают различные заболевания: Mycoplasma pneumonia, Ureaplasma urealiticum, Mycoplasma genitalium, Mycoplasma species, Mycoplasma hominis и Mycoplasma incognita, которую выделили у больных СПИДом.
По сравнению со всеми другими видами микоплазм, Mycoplasma genitalium имеет наиболее выраженный патогенный потенциал.
У мужчин с гомосексуальными наклонностями Mycoplasma genitalium наблюдается намного чаще, примерно на 30%, по сравнению гетеросексуальными мужчинами, у которых микоплазма бывает только в 11% случаев.
Mycoplasma hominis менее патогенна, но встретить ее можно намного чаще при инфекционно воспалительных заболеваниях мочеполовой системы. Микроорганизм рода Mycoplasma hominis очень часто наблюдается при воспалительных заболеваниях у женщин, нежели у мужчин.
Mycoplasma pneumoniae является возбудителем атипичных форм пневмонии и служит причиной возникновения внутриутробных инфекций.
Как передается микоплазма
Данный микроорганизм занимает лидирующую позицию в отношении заболеваний урогенитальной системы, которые передаются половым путем. Заражение микоплазмой может происходить и непрямым путем, это касается женщин и девочек.
Инфекционный агент может быть занесен с помощью предметов домашнего обихода, например, через постельное белье, медицинский инструментарий в гинекологических и урологических кабинетах. Микроорганизмы могут проникать и в верхние отделы половых органов - в цервикальный канал, эндометрий, фаллопиевы трубы вместе с зараженной микоплазмой спермой.
Имеются сведения о внутриутробном инфицировании плода и заражении новорожденных во время прохождения сквозь инфицированные микоплазмой родовые пути матери.
Если говорить о микоплазмозе, то его можно встретить повсеместно. Довольно часто наблюдаются смешанные формы микоплазменных инфекций при гонококковых, трихомонадных и хламидийных заболеваниях мочеполовой системы, а также при острых и рецидивирующих воспалительных заболеваниях женских половых органов.
Симптомы микоплазмоза
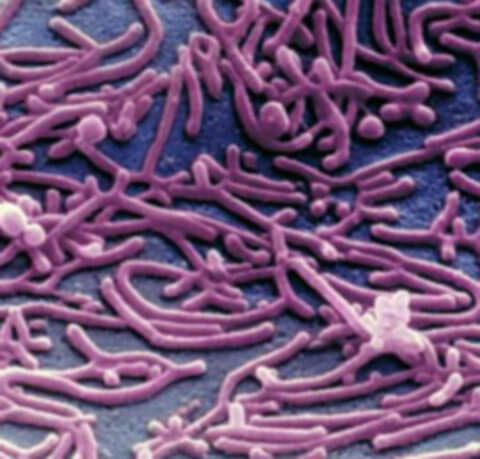
Существует бессимптомная форма заболевания (микоплазмозоносительство). В группу риска входят:
- Женщины фертильного возраста;
- Пациенты с воспалительными процессами генитальной области;
- Беременные женщины.
Клиническая картина микоплазмоза
Микоплазмоз характеризуется специфической локализацией, чаще всего наблюдается микоплазменный уретрит, цервицит, простатит, эндометрит, а также сальпингит. Микоплазменные мочеполовые инфекции могут протекать в острой, хронической и бессимптомной форме.
Если говорить о бессимптомном течении микоплазмоза, то цервициты, вульвовагиниты и уретриты очень часто имеют длительное течение с периодическими ремиссиями, например, негонококковый уретрит и воспалительные процессы в фаллопиевых трубах.
У пациентов, больных микоплазмозом, возникает специфическая симптоматика: зуд в области половых органов, необильные серозные выделения, которые отличаются переменным течением. Если говорить об остром урогенитальном микоплазмозе, то данная форма наблюдается крайне редко.
У мужской половины населения микоплазменные инфекции вызывают поражения предстательной железы, мочеиспускательного канала, придатков яичек, семенных пузырьков, а также почек и мочевыводящих путей. При подозрении на мужское бесплодие следует провести исследование (бактериальный посев) на предмет наличия микоплазм и уреаплазм.
Именно женщины являются скрытыми носителями данного инфекционного агента. Под воздействием определенных факторов бессимптомное течение заболевание может перерасти в острую форму.
Существуют следующие факторы риска:
- Присоединение вторичной бактериальной, вирусной или грибковой инфекции;
- Изменения в гормональном фоне в связи с овуляцией или беременностью.
Принято различать микоплазменные поражение наружных и внутренних органов, к наружным относится уретрит и вульвовагинит, к внутренним — андексит, сальпинит, эндометрит и абсцесс яичников.
Если говорить о микоплазменном эндометрите, то данное заболевание протекает по той же схеме, как и эндометриты, вызванные иными инфекционными агентами. Основные проявления такого эндометрита заключаются в нарушениях менструального цикла и ановуляторных кровотечениях. Под осложнениями микоплазменного эндометрита подразумевается бесплодие и самопроизвольные выкидыши.
Заражение Mycoplasma hominis наблюдается при пиелонефритах и циститах. Скрытая инфекция вызванная этим видом микоплазмы представляет собой большую опасность, она имеет свойство постоянно активизироваться и является причиной тяжелых заболеваний крови, к примеру, перитонит, а также послеродовой и послеабортный сепсис.
Присутствие Mycoplasma hominis у беременных женщин и пациенток с инфекционными гинекологическими заболеваниями представляет собой определенную опасность в связи с повышенным риском внутриутробного инфицирования плода. В связи с этим у таких женщин возрастает перинатальная смертность плода.
Информация о распространенности микоплазмоза
Лидирующую позицию занимает вид Mycoplasma hominis, его обнаруживают на половых органах примерно у 25% грудных детей, преимущественно девочек. У мальчиков данный показатель значительно ниже.
Довольно часто, у детей, с внутриутробным заражением со временем происходит самоизлечение. Особенно часто это наблюдается у мальчиков. У девочек, которые не живут половой жизнью, Mycoplasma hominis обнаруживается в 9 -17% случаев.
У людей, живущих активной половой жизнью, риск инфицирования Mycoplasma hominis значительно возрастает, это связано с заражением во время половых контактов.
Носителями Mycoplasma hominis в 20-50% являются женщины. У мужчин данный микроорганизм встречается реже.
Если говорить о Mycoplasma genitalium, то данный вид распространен значительно реже, по сравнению с Mycoplasma hominis.
Наиболее часто встречаемое заболевание — уретрит (воспаление мочеиспускательного канала), чаще всего вызывается Mycoplasma genitalium.
Бактериальный вагиноз, воспалительные заболевания матки и придатков, пиелонефрит в большинстве случаев вызывает Mycoplasma hominis.
Существуют мнение что микоплазма играет роль и в развитии простатита у мужчин, но это пока не имеет точного подтверждения.
С целью выявления бактериальных агентов, то есть микоплазм, применяется ПЦР. Методики диагностирования ИФА и ПИФ хоть широко и распространены в нашей стране, но отличаются невысокой степенью точности (примерно 50-70%).
Данные зарубежных авторов относительно возможности развития внутриутробного микоплазмоза говорят о том, что данное заболевание развивается у 8-25% детей. Довольно часто клиническая картина имеет крайне тяжелый характер и прогноз не всегда бывает благоприятным.
Микроорганизм может поражать дыхательную систему, к примеру, бронхопневмония, а также глаза, ЦНС, печень, почки, в некоторых случаях может иметь место снижение массы тела новорожденных. Микоплазма может проникать как из наружных половых органов, так и передаваться через кровь матери.
Течение микоплазменной урогенитальной инфекции у каждого ребенка протекает по-разному, с частыми ремиссиями и обострениями. Микоплазмоз может иметь и бессимптомное течение, микоплазмоносительство в данном случае может проявиться и в период полового созревания еще до наступления половых контактов.
Для того чтобы поставить диагноз необходим материал для исследования из цервикального канала или влагалища, но у детей до полового созревания взять такой анализ довольно трудно.
Профилактика микоплазмоза заключается в целенаправленном обследовании всех беременных женщин на разных этапах беременности. В случаях, если результат на микоплазменную инфекцию оказывается положительным необходимо провести санацию беременной женщины, а также ее супруга.
Микоплазмозы — это инфекционные заболевания, которые вызываются микоплазмами, характеризующиеся полиморфизмом клинических проявлений с преимущественным поражением органов дыхания, урогенитального тракта и ЦНС.
Этиология. Микоплазмы являются мельчайшими свободно живущими прокариотами, способными к автономному росту и репродукции, занимают промежуточное положение между вирусами, риккетсиями, бактериями и простейшими. Они относятся к семейству Mycoplasmatacae, которое включает 2 рода — Ureaplasma и Mycoplasma. Микоплазмы представляют собой мелкие полиморфные грамотрицательные микроорганизмы размерами от 0,1 до 10 мкм, содержат РНК и ДНК, подвижные.
Уникальными свойствами микоплазм являются отсутствие клеточной стенки (вместо нее имеют трехслойную мембрану), наименьший для прокариот размер генома (500-1000 МД), наличие минимального количества органелл, мембранный паразитизм. Последнее свойство связано с неспособностью микоплазм синтезировать холестерин, что заставляет их использовать пластический материал клетки хозяина. Прикрепление к поверхности клетки происходит за счет актиноподобного белка-адгезина. Возможно проникновение микоплазм внутрь клеток — в альвеолоциты, фагоциты и др. Возбудители способны к длительной персистенции в организме человека. Микоплазмы выделяют факторы патогенности — гемолизин, нейротоксин и перекись водорода, U.uralyticum — фермент уреазу, которая расщепляет мочевину до аммиака. Возбудители обладают иммунодепрессивной активностью, стимулируют репликацию вирусов в клетке (ВИЧ, онкогенных вирусов и др.). Основными клетками-мишенями являются эпителий респираторного и урогенитального трактов, ротовой полости, альвеолоциты, фагоциты, эндотелий капилляров и др.
Для человека патогенны 16 видов микоплазм. М.pneumoniae является возбудителем респираторного микоплазмоза, U.urealyticum, M.hominis и M.genitalium — заболеваний урогенитального тракта, M.incognitis — генерализованного микоплазмоза, M.orale и M.salivamm — периодонтитов, пульпитов, стоматитов, остеомиелитов, M.artritidis и M.fermentas — артритов.
Микоплазмы неустойчивы во внешней среде, погибают под действием низкой и высокой температур, при изменении pH, действии ультразвука, УФО, стандартных дезинфектантов, моющих средств. Чувствительны к макролидам, тетрациклинам, фторхинолонам, устойчивы к пенициллину и другим (3-лактамам, цефалоспоринам, карбапенемам, сульфаниламидам.
Эпидемиология. Микоплазмы занимают 4—6-е место в этиологической структуре острых респираторных инфекций. Они являются этиологическими агентами 5-30% острых респираторных инфекций и 6-25% пневмоний (в период эпидемического подъема — 30—60%).
Источником являются больные манифестными и субклиническими формами микопдазмоза. Выделение микоплазм реконвалесцентами продолжается в течение нескольких недель.
Пути передачи — воздушно-капельный, половой и вертикальный. С учетом низкой устойчивости микоплазм в окружающей среде воздушно-капельный путь реализуется только в условиях тесного контакта, поэтому очаги заболевания регистрируются в семьях, закрытых и полузакрытых коллективах (детских дошкольных и школьных учреждениях, общежитиях, казармах и др.).
Для респираторного микоплазмоза характерна осенне-зимне-весенняя сезонность. Эпидемические подъемы отмечаются один раз в 4—8 лет. Чаще болеют школьники (11-15 лет) и молодые люди. Постинфекционный иммунитет сохраняется в течение 5—10 лет, поэтому возможны повторные заболевания.
Патогенез. В патогенезе микоплазмозов выделяют несколько этапов.
1. Внедрение и размножение в месте входных ворот. Входными воротами для М.pneumoniae является слизистая респираторного тракта, для U.urealiticum, M.hominis и M.genitalium — слизистая урогенитального тракта, для M.orale и M.salivarum — слизистая ротовой полости. В месте входных ворот происходит размножение возбудителей на поверхности клеток и внутри них.
2. Диссеминация. В результате накопления микоплазмы и их токсины попадают в кровь. Диссеминация возбудителей происходит также в составе инфицированных нейтрофилов и макрофагов. Отмечается прямое поражение различных органов — ЦНС, сердца, печени, почек, суставов и др. Кроме того, неблагоприятное действие оказывают выделяемые микоплазмами токсины. Гемолизин повреждает клетки реснитчатого эпителия, вызывает гемолиз эритроцитов, нарушение микроциркуляции, развитие васкулитов и тромбозов. Нейротоксин оказывает токсическое влияние на ЦНС и сердечно-сосудистую систему, повышает проницаемость гемато-энцефалического барьера. Токсическими свойствами обладают перекись водорода и аммиак, которые выделяют микоплазмы.
3. Развитие серозного воспаления. Адгезия микоплазм к клеткам-мишеням приводит к нарушению тканевой архитектоники, межклеточных контактов, клеточного метаболизма и структуры клеточных мембран. В результате возникают дистрофия, метаплазия, гибель и десквамация эпителиоцитов, нарушение микроциркуляции, повышенная экссудация, некрозы, у грудных детей — гиалиновые мембраны. В генезе повреждения клеток на ранних этапах инфекционного процесса ведущую роль играет прямое цитодеструктивное действие микоплазм. В дальнейшем присоединяется иммунный компонент воспаления, связанный с отложением иммунных комплексов и инфильтрацией тканей клетками, участвующими в иммунном ответе. Формируется перибронхиальная, периваскулярная и интерстициальная инфильтрация пораженных тканей лимфоцитами, плазматическими клетками, гистиоцитами, макрофагами, моноцитами и единичными нейтрофилами. Кроме того, имеет значение тесный контакт микоплазм с клеточной мембраной, в условиях которого ответные защитные реакции неизбежно приводят к повреждению клеток. С 5—6-й недель болезни на первый план выдвигается аутоиммунный механизм воспаления, который играет особо важную роль при хронической форме микоплазмоза.
4. Развитие иммунного ответа, индукция ИДС и аутоиммунных реакций. В антимикоплазменной защите участвуют факторы врожденной резистентности (мукоцилиарный клиренс, нейтрофилы, макрофаги, комплемент, интерфероны) и иммунный ответ по клеточному (СЕ)8-лимфоциты) и гуморальному типам (антитела классов IgM, IgA, IgG). Микоплазмы эффективно противостоят защитным реакциям макроорганизма. Они парализуют движение ресничек мерцательного эпителия. Тесная связь с клетками и антигенная мимикрия приводят к нарушению распознавания микоплазм макрофагами. Возбудители инфицируют нейтрофилы и макрофаги, индуцируя тем самым незавершенный фагоцитоз. Кроме того, это ведет к нарушению кооперации клеток, участвующих в иммунном ответе по клеточному и гуморальному типам. Развитие вторичного ИДС способствует формированию микст-инфекции с участием хламидий, бактерий, вирусов, грибков и простейших. В последние годы доказано прямое активирующее влияние микоплазм на репликацию ВИЧ, онкогенных вирусов и др. В настоящее время установлено, что микоплазмы вызывают поликлональную активацию Т- и В-лимфоцитов, что в сочетании с наличием перекрестных антигенов с тканями легких, мозга, печени, поджелудочной железы, гладких мышц, лимфоцитов и эритроцитов приводит к развитию аутоиммунных реакций.
5. Исходы. Исходами первичной инфекции с учетом состояния иммунной системы являются выздоровление, переход в хроническую или латентную формы. При нормальном состоянии иммунного статуса происходит санация организма от микоплазм. У пациентов с ИДС развивается латентная форма микоплазмоза, при которой возбудители длительно сохраняются в организме. Происходит выключение гена, кодирующего синтез белка Р, (адгезина), что позволяет микоплазмам ускользать от иммунного ответа. В условиях иммуносупрессии возбудитель снова начинает размножаться. При глубоком ИДС микоплазмоз приобретает хроническое течение с локализацией воспаления в месте входных ворот и/или с формированием широкого спектра заболеваний — ревматоидного артрита, бронхиальной астмы, хронического интерстициального легочного фиброза, иммунных цитопений и др.
Классификация. А.П. Казанцев (1997) выделяет следующие клинические формы микоплазмоза:
1. Острое респираторное заболевание (ринофарингит, ларинготрахеит, бронхит). 2. Острая пневмония. 3. Абактериальный уретрит. 4. Воспалительные заболевания малого таза у женщин. 5. Менингеальная форма. 6. Внутриутробная инфекция.
Продолжительность инкубационного периода составляет 3—11 дней.
Клиническими формами являются ринит, фарингит, ларинготрахеит, бронхит, отит, мирингит, евстахеит, синусит. Наиболее часто встречается микоплазменный фарингит. Заболевание начинается остро или постепенно. Температура тела нормальная, субфебрильная или фебрильная.
Симптомы интоксикации выражены умеренно. Характерны жалобы на сухость, першение и боли в горле, сухой кашель, заложенность носа. Реже встречаются насморк, конъюнктивит, склерит, гиперемия лица. При фарингоскопии обнаруживают разлитую гиперемию и зернистость задней стенки глотки. Течение заболевания благоприятное. Лихорадка купируется, как правило, через 3—5 дней, однако субфебрилитет может сохраняться в течение 1—2 недель. Катаральные симптомы исчезают через 7— 10 дней. Наиболее частым осложнением является отит, реже встречаются мирингит, евстахеит и синусит.
Микоплазменный ларингит проявляется лающим кашлем, осиплостью голоса, иногда присоединяется инспираторная одышка. Характерным симптомом трахеобронхита является сухой навязчивый приступообразный кашель без реприз, который сопровождается болями в груди и животе, иногда заканчивается рвотой. Кашель может сохраняться в течение нескольких недель и даже месяцев. Иногда у больных бронхитом развивается бронхообструктивный синдром.
Микоплазменная пневмония наряду с хламидийной и пневмоцистной относится к группе атипичных пневмоний, для которых характерны отсутствие выраженной лихорадки и четких физикальных данных, приступообразный кашель, наличие интерстициальных очагов на рентгенограмме.
Микоплазменная этиология пневмонии имеет место у 9—22% детей и у 6% взрослых. Заболевание чаще развивается у детей старше 7 лет жизни. Инкубационный период составляет 8—40 дней. Микоплазменная пневмония начинается чаще постепенно (у 75% пациентов), реже — остро. Начальный период продолжается от 2 до 12 дней. Появляется симптоматика поражения верхних дыхательных путей (фарингит, конъюнктивит, ринит). Температура тела субфебрильная, реже нормальная или фебрильная, симптомы интоксикации выражены слабо.
В общем анализе крови обнаруживают лейкоцитоз, нейтрофилез со сдвигом влево, повышение СОЭ. При рентгенологическом исследовании выявляют интерстициальные изменения: усиление сосудистого и бронхолегочного рисунка, мелкие инфильтраты линейного или петлистого характера, интерстициальный отек, ателектазы. У детей раннего возраста пневмония двусторонняя, у подростков — чаще односторонняя (правосторонняя). У трети пациентов диагностируют очаговые, сегментарные и долевые пневмонии. Возможно вовлечение в патологический процесс плевры.
Свидетельством системного характера заболевания являются экстрарес-пираторные симптомы. У половины больных выявляют гепатомегалию, у 25% — спленомегалию, у 15% — полиморфную экзантему (мелкоточечную, розеолезную, пятнистую или пятнисто-папулезную). К экстрареспиратор-ным проявлениям относятся лимфаденопатия (чаще увеличены переднешейные лимфоузлы), патология печени (гепатит, фокальный некроз), сердца (миокардит, фокальный некроз, перикардит), суставов (артрит, полиартрит), почек (нефрит), крови (гемолитическая анемия, тромбоци-топения), нервной системы (менингит, менингоэнцефалит, полирадику-лонейропатия), поджелудочной железы (панкреатит), глаз (увеит), изменения на коже (узловатая эритема, полиморфная эритема, синдром Стивенса—Джонсона), диспепсический синдром (тошнота, рвота, боли в животе, диарея), синдром Рейтера.
Патология нервной системы возникает достаточно редко. Симптомы серозного менингита или менингоэнцефалита появляются одновременно с поражением органов дыхания или предшествуют ему. Микоплазмы могут являться причиной развития миелопатии и полирадикулоневропатии.
Микоплазмы вызывают уретриты, простатиты, вульвовагиниты, кольпиты, цервициты, метроэндометриты, сальпингоофориты, эпидидимиты, циститы и пиелонефриты. Патология урогенитального тракта чаще возникает у сексуально активных подростков.
Заболеваемость урогенитальным микоплазмозом женщин детородного возраста составляет 13,3%, при наличии хронической урогенитальной патологии — 23,6-37,9%. Во время беременности инфицированность микоплазмами возрастает в 1,5—2 раза (40—50%). Риск вертикальной трансмиссии, по данным различных авторов, колеблется от 3,5 до 96%. Внутриутробный микоплазмоз диагностируют у 5,5—23% новорожденных. Наиболее частым этиологическим агентом является M.hominis.
Инфицирование может произойти в анте- и интранатальном периодах. Антенатальное заражение реализуется гематогенным, восходящим, нисходящим, трансплацентарным путями, при аспирации инфицированных околоплодных вод. Помимо прямого повреждающего действия микоплазмы вызывают хромосомные аберрации в клетках плода. Они индуцируют выработку простагландинов, приводящих к сокращению матки и прерыванию беременности. Кроме того, неблагоприятную роль играют вызываемый микоплазмами спазм сосудов пуповины, воздействие вредных продуктов метаболизма и гипертермии, что ведет к внутриутробной гипоксии и задержке развития плода. Интранатальное инфицирование происходит в результате контакта слизистых оболочек ребенка с родовыми путями матери и аспирации околоплодных вод.
В связи с отсутствием патогномоничных симптомов важное значение для своевременной диагностики приобретает анализ данных акушерско-гинекологического анамнеза матери — наличие кольпита, вульвовагинита, цервицита, метроэндометрита, сальпингооофорита, уретрита, цистита, пиелонефрита, бесплодия, привычного невынашивания беременности, аномалии плацентации, преждевременной отслойки плаценты, угрозы прерывания беременности, позднего гестоза, многоводия, хорионамини-онита, преждевременного отхождения околоплодных вод, преждевременных родов, послеродового эндометрита, сепсиса.
При заражении в антенатальном периоде клиническая симптоматика имеет место при рождении — развивается врожденный микоплазмоз. Инфицирование в первые две недели беременности приводит к бластопатии — гибели зародыша или формированию системной патологии, сходной с генетическими заболеваниями. При инфицировании в сроке гестации 15-75 дней возникает эмбриопатия — истинные пороки развития на органном или клеточном уровне, в сроке гестации 76—180 дней — ранняя фетопатия (ложные пороки развития, связанные с кистозно-склеротической деформацией органов). Особенностью врожденного микоплазмоза является достаточно высокая частота пороков развития различных органов (ЦНС, сердечно-сосудистой, дыхательной, мочевыделительной систем, опорно-двигательного аппарата и др.), которые регистрируются у 63,4% детей.
Инфицирование при сроке гестации более 180 дней приводит к развитию генерализованной формы врожденного микоплазмоза. Достаточно часто встречаются недоношенность, задержка внутриутробного развития, гипоксически-травматическое поражение ЦНС, асфиксия. Симптомы имеют место при рождении или появляются в ближайшие часы после родов. Возникают клиника поражения органов дыхания, сердечно-сосудистой системы, ЦНС, геморрагический и лимфопролиферативный синдромы. Отмечаются одышка с участием вспомогательной мускулатуры, бледно-серый колорит кожи, цианоз, у половины детей — пенистые кровянистые выделения изо рта. При аускультации выслушивают мелкопузырчатые влажные хрипы и крепитации. На рентгенограмме выявляют расширение корней легких, пневмонические очаги, ателектазы, эмфизему. Развиваются сердечно-сосудистая недостаточность, чаще по правожелудочковому типу, отечный синдром, склерема. Симптомами микоплазменного менингита и менингоэнцефалита являются снижение двигательной активности, тремор, судороги, запрокидывание головы, гипорефлексия. Одним из первых проявлений может быть острая гидроцефалия, которая возникает уже на первой неделе жизни. В дальнейшем у половины детей после перенесенного менингоэнцефалита имеют место остаточные явления — отставание в психомоторном развитии, очаговые знаки, слепота, абсцесс мозга и др. У 20% детей с генерализованной формой врожденного микоплазмоза увеличена печень, у 10% — селезенка. У части пациентов возникают желтуха и геморрагический синдром — кровотечения, кровоизлияния в кожу, подкожную клетчатку, внутренние органы (чаще в легкие и в печень), кефалогематомы.
При интранатальном инфицировании чаще всего развивается пневмония, особенно у недоношенных детей, у которых она характеризуется тяжелым течением и может закончиться летальным исходом. Кроме того, возможно появление конъюнктивита, вульвовагинита, патологии ЦНС (менингита, менингоэнцефалита), кардита, абсцессов и некрозов кожи.
Диагностика микоплазмоза основана на учете данных эпидемического анамнеза, клинической симптоматики и лабораторного обследования, которое включает следующие методы.
1. Культуральный метод — культивирование микоплазм на питательных средах и определение их чувствительности к антибиотикам. Материалами являются носоглоточная слизь, мокрота, ликвор и др. 2. Реакция иммунофлуоресценции. Чувствительность метода составляет 55—66%, поэтому его используют для скрининговых исследований. 3. Полимеразная цепная реакция. Чувствительность метода составляет 92—100%, в связи с чем ПЦР наряду с культуральным методом может быть использована в качестве подтверждающего теста. 4. Иммуноферментный анализ. Позволяет раздельно определять антитела классов IgA, IgM и IgG. При первичной инфекции сначала появляются антитела IgM, затем IgG, в последнюю очередь — IgA. Антитела IgM определяются через 7 дней после первичного инфицирования. В течение 2—3 недель их титр увеличивается, затем снижается. Антитела этого класса могут сохраняться в течение 6—8 месяцев. При реинфекции они не синтезируются. Титр антител классов IgG и IgA при первичной инфекции увеличивается со 2—3-й недели болезни. При санации организма титр антител IgG и IgA снижается, при хронической инфекции — остается на высоком уровне, при реактивации и реинфекции — повторно увеличивается.
Большую важность представляют данные о связи микоплазменной инфекции с осложненной беременностью, преждевременными родами, спонтанными абортами. С 1967 г. появились публикации об обнаружении М. hominis и Т-штаммов микоплазм в тканях плодного яйца при спонтанных абортах.
M. А. Башмакова и соавт. при микробиологическом исследовании плодного яйца показали, что М. hominis выделяется в 10,6% случаев самопроизвольного выкидыша и не выделяется при искусственных абортах; инфицирование плода происходит в период до 20 нед беременности. По данным этих авторов, М. hominis чаще выделяется из мозга, легких, кишечника, оболочек плода и плаценты, реже — из селезенки и печени. При гистологическом исследовании обнаруживаются воспалительные изменения в легких, печени, миокарде, оболочках плода и в плаценте.
Интересное наблюдение внутриутробного инфицирования приводят P. Brunell и соавт. (1969): у 33-летней женщины при кесаревом сечении из амниотической жидкости была выделена М. hominis I. Новорожденный мальчик умер через 27 ч от прогрессирующей дыхательной недостаточности, с которой он и родился.
Рентгенологически в легких ребенка обнаруживались неясные инфильтраты, а посмертно при гистологическом исследовании была диагностирована интерстициальная пневмония. P. Pease и соавт. (1967), R. Kundsin и соавт. (1970) сообщили о выделении цитопатогенного штамма М. hominis I из органов, мертворожденных детей, а Н. Harwick и соавт. (1971)— со слизистой оболочки глаз при воспалительных процессах глаз у новорожденных М. А. Башмакова при обследовании новорожденных детей выяснила, что обсемененность недоношенных детей микоплазмами в 3 раза выше, чем доношенных. У некоторых недоношенных детей были обнаружены вульвит, пневмония, энцефалит — заболевания, которые этиологически могли быть связаны с М. hominis.

P. Braun и соавт. (1970), J. Di Musto (1973) показали, что средняя масса новорожденных от матерей, инфицированных микоплазмами, ниже, чем детей контрольной группы. Этот факт свидетельствует о менее благоприятных условиях внутриутробного развития плодов. А. В. Цинзерлинг описал генерализованный микоплазмоз с поражением легких и печени у недоношенного ребенка, родившегося на 33-й неделе беременности у женщины, страдавшей многоводием.
Урогенитальные микоплазмы могут быть также причиной нарушения репродуктивной функции человека. H. Gnarpe и J. Friberg (1975) показали изменение спермограммы при наличии U. urealyticum и, изучая в растровом микроскопе, обнаружили тесное прикрепление микоплазм к сперматозоидам, что, по их мнению, вызывает бесплодие.
В значительном количестве публикаций сообщается о действии микоплазм на хромосомный аппарат клеток в культуре ткани [Кузьмина С. В., 1972; Fogh J., Fogh H., 1973, и др.], причем J. Fogh и Н. Fogh в эксперименте на модели МП-инфекции амниотических клеток человека показали необратимость хромосомных изменений.
Учитывая это, можно предположить, что микоплазмы, как и близкие к ним вирусы, патогенные для человека, могут быть причиной нарушения эмбриогенеза и рождения детей с аномалиями развития. Имеются немногочисленные наблюдения обнаружения микоплазменного антигена у умерших новорожденных с врожденными пороками путем выделения либо методом иммунофлюоресценции. Е. А. Трепаков и соавт. (1978) выявили, что генитальиые микоплазмы играют определенную роль в генезе развития врожденных пороков ЦНС человека.
О. Вое и соавт. (1973) выделили М. hominis из спинномозговой жидкости новорожденных детей с гидроцефалией.
В последнее десятилетие появились сообщения о том, что при введении М. hominis в дыхательный тракт волонтерам у части из них развивается фарингит. В публикациях Clyde W. и соавт. (1966), Hendley J. н соавт. (1968) указывается на связь развития фарингитов у детей и взрослых с М. hominis. Пневмонии у плодов и новорожденных, вызванные М. hominis, описаны в единичных работах [Башмакова М. А. и др., 1971, 1972; Brunell P., 1969]. Патогенность М. hominis для респираторного тракта подопытных животных доказана морфологическими исследованиями Б. С. Гусман и соавт. (1973, 1977).
Читайте также:


