Можно ли принимать фуразолидон при дисбактериозе
Что понимают под дисбактериозом? Какие методы диагностики являются современными и достоверными? Какие лекарственные препараты применяются при дисбактериозе? Вкишечнике человека находится свыше 500 различных видов микробов, общее количество которых
Вкишечнике человека находится свыше 500 различных видов микробов, общее количество которых достигает 10 14 , что на порядок выше общей численности клеточного состава человеческого организма. Количество микроорганизмов увеличивается в дистальном направлении, и в толстой кишке в 1 г кала содержится 10 11 бактерий, что составляет 30% сухого остатка кишечного содержимого.
В тощей кишке здоровых людей находится до 10 5 бактерий в 1 мл кишечного содержимого. Основную массу этих бактерий составляют стрептококки, стафилококки, молочнокислые палочки, другие грамположительные аэробные бактерии и грибы. В дистальном отделе подвздошной кишки количество микробов увеличивается до 10 7 –10 8 , в первую очередь за счет энтерококков, кишечной палочки, бактероидов и анаэробных бактерий. Недавно нами было установлено, что концентрация пристеночной микрофлоры тощей кишки на 6 порядков выше, чем в ее полости, и составляет 10 11 кл/мл. Около 50% биомассы пристеночной микрофлоры составляют актиномицеты, примерно 25% — аэробные кокки (стафилококки, стрептококки, энтерококки и коринеформные бактерии), от 20 до 30% приходится на бифидобактерии и лактобациллы.
Количество анаэробов (пептострептококки, бактероиды, клостридии, пропионобактерии) составляет около 10% в тонкой и до 20% в толстой кишке. На долю энтеробактерий приходится 1% от суммарной микрофлоры слизистой оболочки.
До 90-95% микробов в толстой кишке составляют анаэробы (бифидобактерии и бактероиды), и только 5-10% всех бактерий приходится на строгую аэробную и факультативную флору (молочнокислые и кишечные палочки, энтерококки, стафилококки, грибы, протей).
Кишечные палочки, энтерококки, бифидобактерии и ацидофильные палочки обладают выраженными антагонистическими свойствами. В условиях нормально функционирующего кишечника они способны подавлять рост несвойственных нормальной микрофлоре микроорганизмов.
Площадь внутренней поверхности кишечника составляет около 200 м 2 . Она надежно защищена от проникновения пищевых антигенов, микробов и вирусов. Важную роль в организации этой защиты играет иммунная система организма. Около 85% лимфатической ткани человека сосредоточено в стенке кишечника, где продуцируется секреторный IgA. Кишечная микрофлора стимулирует иммунную защиту. Кишечные антигены и токсины кишечных микробов значительно увеличивают секрецию IgA в просвет кишки.
Расщепление непереваренных пищевых веществ в толстой кишке осуществляется ферментами бактерий, при этом образуются разнообразные амины, фенолы, органические кислоты и другие соединения. Токсические продукты микробного метаболизма (кадаверин, гистамин и другие амины) выводятся с мочой и в норме не оказывают влияния на организм. При утилизации микробами неперевариваемых углеводов (клетчатки) образуются короткоцепочечные жирные кислоты. Они обеспечивают клетки кишки энергоносителями и, следовательно, улучшают трофику слизистой оболочки. При дефиците клетчатки может нарушаться проницаемость кишечного барьера вследствие дефицита короткоцепочечных жирных кислот. В результате кишечные микробы могут проникать в кровь.
Под влиянием микробных ферментов в дистальных отделах подвздошной кишки происходит деконъюгация желчных кислот и преобразование первичных желчных кислот во вторичные. В физиологических условиях от 80 до 95% желчных кислот реабсорбируется, остальные выделяются с фекалиями в виде бактериальных метаболитов. Последние способствуют нормальному формированию каловых масс: тормозят всасывание воды и тем самым препятствуют излишней дегидратации кала.
В понятие дисбактериоза кишечника входит избыточное микробное обсеменение тонкой кишки и изменение микробного состава толстой кишки. Нарушение микробиоценоза происходит в той или иной степени у большинства больных с патологией кишечника и других органов пищеварения. Следовательно, дисбактериоз является бактериологическим понятием. Он может рассматриваться как одно из проявлений или осложнение заболевания, но не самостоятельная нозологическая форма.
Крайней степенью дисбактериоза кишечника является появление бактерий желудочно-кишечного тракта в крови (бактериемия) или даже развитие сепсиса.
Состав микрофлоры кишечника нарушается при болезнях кишечника и других органов пищеварения, лечении антибиотиками и иммунодепрессантами, воздействиях вредных факторов внешней среды.
Клинические проявления дисбактериоза зависят от локализации дисбиотических изменений.
При дисбактериозе тонкой кишки численность одних микробов в слизистой оболочке тонкой кишки увеличена, а других уменьшена. Отмечается увеличение Eubacterium (в 30 раз), α-стрептококков (в 25 раз), энтерококков (в 10 раз), кандид (в 15 раз), появление бактерий рода Acinetobacter и вирусов герпеса. Уменьшается от 2 до 30 раз количество большинства анаэробов, актиномицетов, клебсиелл и других микроорганизмов, являющихся естественными обитателями кишечника.
Причиной дисбактериоза могут быть: а) избыточное поступление микроорганизмов в тонкую кишку при ахилии и нарушении функции илеоцекального клапана; б) благоприятные условия для развития патологических микроорганизмов в случаях нарушения кишечного пищеварения и всасывания, развития иммунодефицита и нарушений проходимости кишечника.
Повышенная пролиферация микробов в тонкой кишке приводит к преждевременной деконъюгации желчных кислот и потере их с калом. Избыток желчных кислот усиливает моторику толстой кишки и вызывает диарею и стеаторею, а дефицит желчных кислот приводит к нарушению всасывания жирорастворимых витаминов и развитию желчнокаменной болезни.
Бактериальные токсины и метаболиты, например фенолы и биогенные амины, могут связывать витамин В12.
Некоторые микроорганизмы обладают цитотоксическим действием и повреждают эпителий тонкой кишки. Это ведет к уменьшению высоты ворсинок и углублению крипт. При электронной микроскопии выявляется дегенерация микроворсинок, митохондрий и эндоплазматической сети.
Состав микрофлоры толстой кишки может меняться под влиянием различных факторов и неблагоприятных воздействий, ослабляющих защитные механизмы организма (экстремальные климатогеографические условия, загрязнение биосферы промышленными отходами и различными химическими веществами, инфекционные заболевания, болезни органов пищеварения, неполноценное питание, ионизирующая радиация).
В развитии дисбактериоза толстой кишки большую роль играют ятрогенные факторы: применение антибиотиков и сульфаниламидов, иммунодепрессантов, стероидных гормонов, рентгенотерапия, хирургические вмешательства. Антибактериальные препараты значительно подавляют не только патогенную микробную флору, но и рост нормальной микрофлоры в толстой кишке. В результате размножаются микробы, попавшие извне, или эндогенные виды, устойчивые к лекарственным препаратам (стафилококки, протей, дрожжевые грибы, энтерококки, синегнойная палочка).
Клинические проявления чрезмерного роста микроорганизмов в тонкой кишке могут полностью отсутствовать, выступать в качестве одного из патогенетических факторов хронической рецидивирующей диареи, а при некоторых болезнях, например, дивертикулезе тонкой кишки, частичной кишечной непроходимости или после хирургических операций на желудке и кишечнике, приводить к тяжелой диарее, стеаторее и В 12 -дефицитной анемии.
Особенностей клинического течения заболевания у больных с различными вариантами дисбактериоза толстой кишки, по данным бактериологических анализов кала, в большинстве случаев установить не удается. Можно отметить, что больные хроническими заболеваниями кишечника чаще инфицируются острыми кишечными инфекциями по сравнению со здоровыми. Вероятно, это связано со снижением у них антагонистических свойств нормальной микрофлоры кишечника и, прежде всего, частым отсутствием бифидобактерий.
Особенно большую опасность представляет псевдомембранозный колит, развивающийся у некоторых больных, длительно лечившихся антибиотиками широкого спектра действия. Этот тяжелый вариант дисбактериоза вызывается токсинами, выделяемыми синегнойной палочкой Clostridium difficile, которая размножается в кишечнике при угнетении нормальной микробной флоры.
Очень редко наблюдается молниеносное течение псевдомембранозного колита, напоминающее холеру. Обезвоживание развивается в течение нескольких часов и заканчивается летальным исходом.
Таким образом, оценка клинической значимости дисбиотических изменений должна основываться прежде всего на клинических проявлениях, а не только на результатах исследования микрофлоры кала.
Диагностика дисбактериоза представляет собой сложную и трудоемкую задачу. Для диагностики дисбактериоза тонкой кишки применяют посев сока тонкой кишки, полученного с помощью стерильного зонда. Дисбактериоз толстой кишки выявляют с помощью бактериологических исследований кала.
Микробная флора образует большое количество газов, в том числе водорода. Это явление используют для диагностики дисбактериоза. Концентрация водорода в выдыхаемом воздухе натощак находится в прямой зависимости от выраженности бактериального обсеменения тонкой кишки. У больных с заболеваниями кишечника, протекающими с хронической рецидивирующей диареей и бактериальным обсеменением тонкой кишки, концентрация водорода в выдыхаемом воздухе значительно превышает 15 ppm.
Для диагностики дисбактериоза применяют также нагрузку лактулозой. В норме лактулоза не расщепляется в тонкой кишке и метаболизируется микробной флорой толстой кишки. В результате количество водорода в выдыхаемом воздухе повышается (рис. 1).
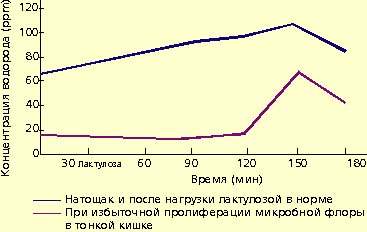 |
| Рисунок 1. Концентрация водорода в выдыхаемом воздухе |
Наиболее частыми бактериологическими признаками дисбактериоза толстой кишки являются отсутствие основных бактериальных симбионтов — бифидобактерий и уменьшение количества молочнокислых палочек. Увеличивается количество кишечных палочек, энтерококков, клостридий, стафилококков, дрожжеподобных грибов и протея. У отдельных бактериальных симбионтов появляются патологические формы. К ним относятся гемолизирующая флора, кишечные палочки со слабо выраженными ферментативными свойствами, энтеропатогенные кишечные палочки и т. д.
Углубленное изучение микробиоценоза показало, что традиционные методы не позволяют получить истинную информацию о состоянии микрофлоры кишечника. Из 500 известных видов микробов в целях диагностики обычно изучаются лишь 10-20 микроорганизмов. Важно, в каком отделе — в тощей, подвздошной или толстой кишках — исследуется микробный состав. Поэтому перспективы разработки клинических проблем дисбактериоза в настоящее время связывают с применением химических методов дифференциации микроорганизмов, позволяющих получить универсальную информацию о состоянии микробиоценоза. Наиболее широко для этих целей используются газовая хроматография (ГХ) и газовая хроматография в сочетании с масс-спектрометрией (ГХ-МС). Этот метод позволяет получить уникальную информацию о составе мономерных химических компонентов микробной клетки и метаболитов. Маркеры такого рода могут быть определены и использованы для детектирования микроорганизмов. Главным преимуществом и принципиальным отличием этого метода от бактериологических является возможность количественного определения более 170 таксонов клинически значимых микроорганизмов в различных средах организма. При этом результаты исследования могут быть получены в течение нескольких часов.
Проведенные нами исследования микробиоценоза в крови и биоптатов слизистой оболочки тонкой и толстой кишок у больных с синдромом раздраженного кишечника позволили обнаружить отклонения от нормы до 30-кратного увеличения или уменьшения многих компонентов. Существует возможность оценки изменений микрофлоры кишечника на основании данных анализа крови методом ГХ-МС-микробных маркеров.
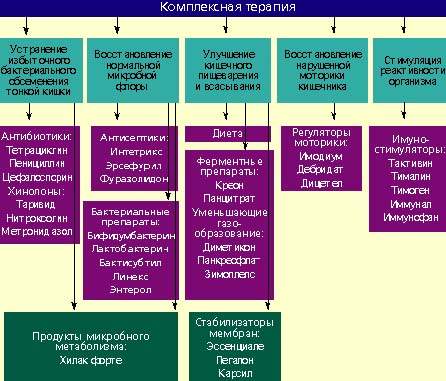 |
Лечение дисбактериоза должно быть комплексным (схема) и включать в себя следующие мероприятия:
- устранение избыточного бактериального обсеменения тонкой кишки;
- восстановление нормальной микробной флоры толстой кишки;
- улучшение кишечного пищеварения и всасывания;
- восстановление нарушенной моторики кишечника;
- стимулирование реактивности организма.
Антибактериальные препараты необходимы в первую очередь для подавления избыточного роста микробной флоры в тонкой кишке. Наиболее широко применяются антибиотики из группы тетрациклинов, пенициллинов, цефалоспорины, хинолоны (таривид, нитроксолин) и метронидазол.
Однако антибиотики широкого спектра действия в значительной степени нарушают эубиоз в толстой кишке. Поэтому они должны применяться только при заболеваниях, сопровождающихся нарушениями всасывания и моторики кишечника, при которых, как правило, отмечается выраженный рост микробной флоры в просвете тонкой кишки.
Антибиотики назначают внутрь в обычных дозах в течение 7–10 дней.
При заболеваниях, сопровождающихся дисбактериозом толстой кишки, лечение лучше проводить препаратами, которые оказывают минимальное влияние на симбионтную микробную флору и подавляют рост протея, стафилококков, дрожжевых грибов и других агрессивных штаммов микробов. К ним относятся антисептики: интетрикс, эрсефурил, нитроксолин, фуразолидон и др.
При тяжелых формах стафилококкового дисбактериоза применяют антибиотики: таривид, палин, метронидазол (трихопол), а также бисептол-480, невиграмон.
Антибактериальные препараты назначают в течение 10–14 дней. В случае появления в кале или кишечном соке грибов показано применение нистатина или леворина.
У всех больных с диареей, ассоциированной с антибиотиками, протекающей с интоксикацией и лейкоцитозом, возникновение острой диареи следует связывать с Cl. difficile.
В этом случае срочно делают посев кала на Cl. difficile и назначают ванкомицин по 125 мг внутрь 4 раза в сутки; при необходимости доза может быть увеличена до 500 мг 4 раза в день. Лечение продолжают в течение 7-10 суток. Эффективен также метронидазол в дозе 500 мг внутрь 2 раза в сутки, бацитрацин по 25 000 МЕ внутрь 4 раза в сутки. Бацитрацин почти не всасывается, в связи с чем в толстой кишке можно создать более высокую концентрацию препарата. При обезвоживании применяют адекватную инфузионную терапию для коррекции водно-электролитного баланса. Для связывания токсина Cl. difficile используют холестирамин (квестран).
Живые культуры нормальной микробной флоры выживают в кишечнике человека от 1 до 10% от общей дозы и способны в какой-то мере выполнять физиологическую функцию нормальной микробной флоры. Бактериальные препараты можно назначать без предварительной антибактериальной терапии или после нее. Применяют бифидумбактерин, бификол, лактобактерин, бактисубтил, линекс, энтерол и др. Курс лечения длится 1-2 месяца.
Возможен еще один способ устранения дисбактериоза — воздействие на патогенную микробную флору продуктами метаболизма нормальных микроорганизмов. К таким препаратам относится хилак форте. Он создан 50 лет назад и до настоящего времени применяется для лечения больных с патологией кишечника. Хилак форте представляет собой стерильный концентрат продуктов обмена веществ нормальной микрофлоры кишечника: молочной кислоты, лактозы, аминокислот и жирных кислот. Эти вещества способствуют восстановлению в кишечнике биологической среды, необходимой для существования нормальной микрофлоры, и подавляют рост патогенных бактерий. Возможно, продукты метаболизма улучшают трофику и функцию эпителиоцитов и колоноцитов. 1 мл препарата соответствует биосинтетическим активным веществам 100 млрд. нормальных микроорганизмов. Хилак форте назначают по 40–60 капель 3 раза в день на срок до 4 недель в сочетании с препаратами антибактериального действия или после их применения.
Совсем недавно появились сообщения о возможности лечения острой диареи, ассоциированной с антибактериальной терапией и Cl. difficile, большими дозами пре- и пробиотиков.
У больных с нарушением полостного пищеварения применяют креон, панцитрат и другие панкреатические ферменты. С целью улучшения функции всасывания назначают эссенциале, легалон или карсил, т. к. они стабилизируют мембраны кишечного эпителия. Пропульсивную функцию кишечника улучшают имодиум (лоперамид) и тримебутин (дебридат).
Для повышения реактивности организма ослабленным больным целесообразно применять тактивин, тималин, тимоген, иммунал, иммунофан и другие иммуностимулирующие средства. Курс лечения должен составлять в среднем 4 недели. Одновременно назначаются витамины.
Первичная профилактика дисбактериоза представляет очень сложную задачу. Ее решение связано с общими профилактическими проблемами: улучшением экологии, рациональным питанием, улучшением благосостояния и прочими многочисленными факторами внешней и внутренней среды.
Вторичная профилактика предполагает рациональное применение антибиотиков и других медикаментов, нарушающих эубиоз, своевременное и оптимальное лечение болезней органов пищеварения, сопровождающихся нарушением микробиоценоза.
П.Я. Григорьев, Э.П. Яковенко
Российский медицинский университет и Федеральный гастроэнтерологический центр
Распространенность и причины
Данные о частоте распространенности СРК среди взрослых колеблются от 14-22% до 30-48%, а соотношение женщин и мужчин - 2-4:1. Чаще болеют женщины в репродуктивном возрасте, несколько реже первичное развитие болезни начинается после 40 лет, но тогда для исключения органической патологии эти больные нуждаются в особенно тщательном обследовании. Очевидно, сведения о частоте и распространенности СРК не являются достоверными, так как не более 10% больных, страдающих этим заболеванием, обращаются за медицинской помощью. К тому же в России в отличие от некоторых других стран СРК среди врачей не является “излюбленным” диагнозом и только в последнее время становится более популярным.
К факторам, вызывающим раздражение рецепторов кишечника и в результате этого его функциональные расстройства, обычно относят лактозу и другие сахара, жирные кислоты с короткой цепью, пищевые агенты, слабительные средства, инфекцию в связи с избыточным бактериальным ростом и дисбактериозом и др.
СРК нередко возникает после перенесенных острых кишечных инфекций с развитием дисбактериоза у пациентов с неустойчивым психоэмоциональным статусом. Специальные электрофизиологические исследования показали, что у больных СРК нарушена моторика (в частности, изменен ответ на холецистокинин, на введение в просвет кишки баллона и т.д.).
В патогенезе СРК большое значение придают аномальной моторике кишечника, психологическому дистресс-синдрому, дисгормональным нарушениям. Лица, страдающие СРК, характеризуются высоким уровнем тревоги, повышенной возбудимостью, расстройством сна, подвержены депрессии, склонны к “хроническому болезненному поведению”. Однако многие симптомы не предшествуют СРК, а присоединяются в процессе его развития и регрессируют на фоне лечения. Существенную роль в возникновении некоторых симптомов при СРК (например, гипомоторной кишечной дискинезии) играют особенности режима питания. Известно, что нормальная пропульсивная моторика кишечника предполагает наличие необходимого объема кишечного содержимого, возбуждающего рецепторы стенки кишки. В первую очередь объем кишечного химуса определяется содержанием в нем балластных веществ, удерживающих воду, абсорбирующих токсины, стимулирующих моторику и т.д., однако моторные расстройства, характерные для СРК, могут быть связаны и с другими алиментарными факторами. Так, наибольший пик двигательной активности левых отделов ободочной и прямой кишки отмечается утром после завтрака, менее высокий - после обеда и совсем незначительный - после ужина. Этим объясняется, почему в большинстве случаев стул, как правило, бывает утром, после еды. Отказ многих людей от полноценного завтрака и торопливость в приеме пищи подавляют нормальное функционирование желудочно-кишечного рефлекса и ведут к формированию запора, являющегося частым симптомом при СРК.
Определенное место среди факторов, приводящих к развитию СРК, очевидно, занимают гинекологические заболевания. Симптомы СРК часто обнаруживаются у женщин, страдающих дисменореей, причем выраженность и периодичность возникновения клинических проявлений СРК обычно корригируют с течением гинекологических расстройств.
По нашим данным, у большинства больных СРК (89 человек), находящихся под нашим наблюдением в течение 3 лет и более, в 68,8% случаев имелась избыточная микробная контаминация тонкой кишки и в 98,4% случаев - дисбактериоз толстой кишки. При этом обнаруживаются гемолизирующая флора, кишечные палочки со слабовыраженными ферментативными свойствами, энтеропатогенные кишечные палочки и другие изменения микрофлоры толстой кишки с преобладанием условно-патогенных микробов или их ассоциаций (стафилококки, протей, дрожжеподобные грибы, лактозонегативные или гемолитические ишерихии, синегнойная палочка, клебсиеллы и др.), т.е. те или иные дисбиотические изменения микрофлоры толстой кишки в сочетании с избыточным бактериальным ростом в тонкой кишке. Изменения микробного биоценоза, выявленные у обследованных больных СРК, несомненно, являются важнейшими патогенетическими механизмами в развитии этого синдрома. Так, в результате жизнедеятельности избыточного количества бактерий в тонкой кишке могут образовываться и накапливаться свободные (деконъюгированные) желчные кислоты, гидроксиды жирных кислот, бактериальные токсины, протеазы и различные метаболиты (фенолы, биогенные амины и др.). Следствием этих процессов могут стать нарушения двигательной, секреторной, пищеварительной и других функций тонкой кишки, нарушения гидролиза дисахаридов (например, лактозная недостаточность), жиров, белков, всасывания витаминов, макро- и микроэлементов. Таким образом, в толстую кишку поступает химус, обладающий агрессивными свойствами, к тому же и в самой толстой кишке, особенно в ее начальных отделах, в силу дисбиотических изменений микрофлоры (отсутствие или дефицит основных бактериальных симбионтов - бифидобактерий, уменьшение количества молочно-кислых палочек) также редуцируются процессы пищеварения (в основном нарушается гидролиз клетчатки) и всасывания, а оставшаяся “субстанция” в силу агрессивности приводит к расстройству моторно-секреторной функции ободочной и прямой кишки.
При дисбактериозе не только изменяется общее количество микроорганизмов за счет уменьшения или увеличения количества основных групп микроорганизмов, но и изменяются их свойства (усиливаются их инвазивность и агрессивность по отношению к слизистой оболочке), что в дальнейшем может привести к развитию воспалительного процесса.
Критерии диагностики СРК
Критериями диагностики СРК являются следующие постоянные или рецидивирующие, но сохраняющиеся в течение 3 мес и более симптомы: абдоминальные боли, расстройство стула, вздутие живота или чувство распирания. Они могут сочетаться и варьировать, а иногда значительно различаться у одного и того же больного в разные периоды течения заболевания. СРК может проявляться астеническим, астеноневротическим и даже психостеническим симптомами (головная боль, усталость, недомогание, депрессия, беспокойство, чувство тревоги, повышенная раздражительность и др.).
В зависимости от ведущего клинического симптома принято различать три основных варианта СРК:
Первый вариант (с преобладанием диареи):
- Жидкий стул 2-4 раза в день, преимущественно в утренние часы после завтрака, иногда с примесью слизи и остатков непереваренной пищи.
- Неотложные (императивные) позывы на дефекацию (изредка).
- Отсутствие диареи в ночное время.
Второй вариант (с преобладанием запоров):
- Отсутствие дефекации в течение 3 сут и более.
- Чередование запоров с поносами.
- Чувство неполного опорожнения кишечника (стул в виде овечьего кала или лентообразный в виде карандаша).
Третий вариант (с преобладанием абдоминальных болей и вздутия живота):
- Схваткообразные абдоминальные боли и вздутие живота (метеоризм).
- При пальпации живота отмечается напряжение передней брюшной стенки и болезненность по ходу всех отделов кишечника).
- Боли, как правило, усиливаются перед актом дефекации и уменьшаются после опорожнения кишечника. Появление болей нередко провоцируется приемом пищи.
Диагностика и дифференциальная диагностика
Однако представленные клинические симптомы хотя и встречаются при СРК довольно часто, но не являются патогномоничными только для этого синдрома. Они нередко имеют место и при многих других заболеваниях кишечника: опухолях, дивертикулезе, болезни Крона, язвенном колите, ишемическом колите и других. При наличии диареи необходимо проводить дифференциальную диагностику с целиакией, псевдомембронозным колитом, болезнью Уипла, с передозировкой слабительных средств. С этой целью прежде всего необходимо определить объем испражнений (для СРК характерно наличие частого стула с малым объемом испражнений - меньше 300 см3 за сутки).
При варианте СРК с преобладанием запора необходимо исключить “инертную кишку” с аноректальными дисфункциями, энтероцеле и ректоцеле. С этой целью по показаниям проводят соответствующие исследования (ректосигмоскопия, колоноскопия, аноректальная манометрия и др.). При варианте СРК с преобладанием абдоминальных болей и вздутия живота следует провести дифференциальную диагностику с истинной или ложной обструкцией тонкой кишки, подтвердить или исключить лактазную недостаточность и органическую патологию (полипоз, дивертикулез, опухоли). Для этого необходимо провести рентгеновское, а иногда и компьютерное исследование брюшной полости, соответствующие эндоскопические и копрологические исследования, включая посев кала на бактериальную флору.
При любом варианте СРК необходимо тщательно проанализировать все имеющиеся симптомы и особо обращать внимание на наличие или отсутствие примеси крови в кале, лихорадки, анемии, немотивированное похудание, повышение СОЭ и другие так называемые симптомы тревоги, наличие которых является основанием заподозрить органическую патологию. С этой целью первичное обследование таких больных должно включать общий клинический и биохимический анализ крови, копрограмму, посев кала на бактериальную флору (сальмонеллы, шигеллы, иерсинии и др.), а также ректоманоскопию и колоноскопию, по показаниям с биопсией.
Это позволит исключить такие заболевания, как рак толстой и прямой кишки, язвенный колит, болезнь Крона, ишемический и псевдомембранозный колит, дивертикулез и полипоз кишечника. При подозрении на целиакию и болезнь Уипла производят гастродуоденоскопию с глубокой прицельной биопсией из дистальных отделов двенадцатиперстной кишки. В необходимых случаях для выявления внекишечных и ретроперитонеальных изменений проводят УЗИ, компьютерную томографию, ангиографию и лапароскопию. Однако в подавляющем большинстве случаев при подозрении на СРК можно ограничиться тщательно собранным анамнезом, анализом жалоб и оценкой результатов физикального обследования, включая пальцевое и эндоскопическое исследование прямой кишки, копрограмму, исследование кала на гельминты и скрытую кровь, клинический анализ крови и мочи. При осмотре этих больных нередко обнаруживаются признаки хронического прогрессирующего заболевания, такие как потеря массы тела, анемия, лихорадка, часто отмечается пальпаторная болезненность в проекции брыжейки тонкой кишки и левой подвздошной области, наполненная газами слепая кишка, отмечается болезненность при исследовании прямой кишки.
При подозрении на СРК обязательным методом исследования является ректосигмоскопия. Она важна не только для исключения органической или воспалительной патологии в прямой и ободочной сигмовидной кишке, но и для обнаружения типичных признаков, характерных для СРК: спазмированная сегмовидная кишка, возможное наличие гиперемии слизистой оболочки дистальных отделов ободочной и прямой кишки.
Само исследование иногда может спровоцировать развитие симптомов болезни. При обнаружении эндоскопических признаков проктосигмондита рекомендуется проведение прицельной биопсии и гистологическое исследование с целью исключения неспецифического язвенного, превдомембранозного, микроскопического (коллагенозного) колита. Наличие микроскопической картины проктосигмондита не является основанием для исключения СРК.
У больного истинной диареей необходимо определять в кале содержание жира, исследовать функцию щитовидной железы, проводить бактериологическое исследование.
При наличии болей в верхней половине живота требуется проведение УЗИ печени и поджелудочной железы, эзофагогастродуоденоскопии. При болях в нижней половине живота может возникнуть необходимость в УЗИ органов малого таза и лапароскопии.
Лечение больных СРК, ассоциированного с дисбактериозом
Лечение больных СРК, ассоциированного с дисбактериозом, предусматривает:
1) устранение микробной контаминации тонкой кишки и восстановление нормальной кишечной микрофлоры в толстой кишке (микробного циноза кишечника);
2) восстановление нарушенных процессов пищеварения и всасывания, а также устранение гипо- и авитаминоза и дефицита микро- и макроэлементов;
3) нормализацию моторно-эвакуаторной функции толстой кишки и акта дефекации.
Лечение этих больных включает также нормализацию режима питания, проведение разъяснительных психотерапевтических бесед, назначение различных симптоматических лекарственных средств.
При СРК, протекающем:
1) с позывом на дефекацию после еды (гастроколитический рефлекс) используют антихолинергические препараты в обычных дозах (гиосцин бутилбромид, метацин, пирензепина гидрохлорид и др.);
2) с выраженной тревожной депрессией применяют антидепрессанты в малых дозах;
3) с вегетативными расстройствами - сульпирид 50-100 мг в сутки;
4) с нарушениями сна (затрудненное засыпание, ночные пробуждения и др.) - снотворные препараты (в частности, золпидем по 5-10 мг перед отходом ко сну).
Обследование и начальное лечение больных целесообразно провести в условиях стационара (например, в дневном стационаре поликлиники), а пролонгированное лечение и наблюдение продолжить в амбулаторно-поликлинических условиях.
Наиболее эффективными лекарственными комбинациями для терапии СРК являются следующие[используется одна из перечисленных комбинаций]:
- Нифуроксазид 200 мг (капсула) 4 раза в день внутрь непосредственно перед едой в течение 7 дней.
- Метронидазол 0,5 мг 2 раза в день после еды в течение 10 дней.
- Сульпирид (желательно использовать раствор для приема внутрь) по 50 мг 3 раза в день перед едой в течение 2-3 нед. Курс может повторяться, если симптомы рецидивируют.
- Фуразолидон 0,05 г 4 раза в день непосредственно перед едой, в течение 7 дней.
- Комбинированный препарат интетрикс по 2 капсулы 3 раза в день после еды в течение 7 дней.
- Сульпирид (желательно использовать раствор для приема внутрь) по 50 мг 3 раза в день перед едой в течение 2-3 нед. Курс может повторяться, если симптомы рецидивируют.
Подбор препаратов, оказывающих минимальное влияние на симбионтную микробную флору и подавляющих рост условно-патогенной микробной флоры, является сложной задачей.
При синдроме избыточного бактериального роста в тонкой кишке обычно используется один из следующих противомикробных препаратов: тетрациклина гидрохлорид (250 мг 4 раза в сутки с едой), ципрофлоксацин (250 мг 2 раза в сутки), метронидазол (0,5 г 2 раза в сутки с едой), фуразолидон (0,1 г 3-4 раза в сутки), нифуроксазид (200 мг 4 раза в сутки после еды), комбинированный препарат интетрикс (1 капсула 4 раза в сутки), цефалексин (0,25 г 4 раза в день), реже - левомицетин (0,25 г 4 раза в сутки). В ряде случаев можно использовать противодиарейный препарат биологического происхождения энтерол (2-4 капсулы или пакета в сутки).
При синдроме избыточного роста микрофлоры в толстой кишке предпочтение отдается одному из следующих препаратов противомикробных препаратов: фталазол или сульгин (1 г/сут), нифуроксазид (800 мг/сут), интетрикс (4 капсулы в сутки), метронидазол (1 г/сут). При тяжелых формах стафиллококкового дисбактериоза применяют кларитромицин, цефалексин и другие антибиотики. В случае обнаружения в кале или кишечном соке грибов показано назначение нистатина или леворина.
После окончания курсов(а) антибактериальной терапии назначаются пробиотики, т.е. препараты, содержащие нормальные штаммы кишечной флоры и пребиотики, способствующие их росту.
Для восстановления нормального состава микрофлоры тонкой кишки используются пробиотики, содержащие аэробные штаммы (колибактерин 5-10 доз в сутки или лактобактерин 5-10 доз в сутки), толстой кишки - пробиотики, включающие анаэробные штаммы (бифидумбактерин 5-10 доз в сутки и др.), толстой и тонкой кишки - комбинированные препараты (бификол 5-10 доз в сутки, бифиформ 2-4 капсулы в сутки, линекс 6 капсул в сутки). Продолжительность приема составляет 2-4 нед.
Одновременно с приемом пробиотиков назначаются пребиотики (хилак-форте 30-60 капель 3 раза в день в течение 2 нед).
При спастической дискинезии толстой кишки дополнительно назначается препарат со спазмолитическим и анальгетическим эффектом (комбинированные спазмоанальгетики): метеоспазмил по 1 капсуле 3 раза в день в течение 2 нед или дебридат по 200 мг 3 раза в день в течение 2 нед. Также с этой целью используют такие препараты, как но-шпа, папаверин, спазмол, дицител и другие. Но-шпа применяется в дозе 40-80 мг. В настоящее время применяется форма с повышенным содержанием действующего вещества (но-шпа форте - 80 мг в таб.). Благодаря тому, что но-шпа является миотропным спазмалитиком и не обладает антихолинергической активностью, препарат крайне редко вызывает побочные эффекты, что установлено при анализе большого числа наблюдений.
При преобладании запора дополнительно может быть назначен препарат, обладающий слабительным эффектом (лактулоза 30-60 мл/сут или макроголь 20 г/сут или др.).
При гипомоторной дискинезии используется цизаприд внутрь по 20 мг 2 раза в день обычно в сочетании с ламинаридом или мукофальком - 4 чайных ложки гранул в сутки.
При диарее дополнительно назначают: 1) цитопротектор смекту (1 пакет 3 раза в день после еды); 2) буферные антациды (маалокс, гастал, протаб, альмагель, фосфалюгель и другие) по 1 дозе 3-4 раза в сутки через 1 ч после еды; 3) антидиарейный препарат, замедляющий перистальтику кишки - лоперамид от 2 мг до 4 мг на прием (не более 16 мг/сут) до прекращения поноса.
При синдроме мальдигестии назначают дополнительно ферментные препараты (панкреатин, мезим, панцитрат или креон) по 1 дозе в начале еды 3-4 раза в день в течение 2-3 нед.
Ориентировочная схема назначений при СРК, ассоциированным с дисбактериозом:
1-я неделя: нифуроксазид и/или метронидазол + ферментный препарат + препараты, нормализующие моторику кишки;
2-я неделя: бифиформ + хилак-форте + ферментный препарат + препараты, нормализующие моторику кишки;
Читайте также:


