Оперативное лечение ложного сустава лечение
 |  |  |  |

Формирование такого осложнения как ложные суставы чаще всего наблюдается на большеберцовой кости и костях предплечья, нередко — на бедренной и плечевой костях.
С точки зрения патоморфологической картины и выбора метода лечения ложные суставы можно разделить на две группы: фиброзные ложные суставы и истинные ложные суставы (фиброзно-синовиальиый ложный сустав).
Фиброзные ложные суставы являются промежуточной стадией между замедленной консолидацией и истинным ложным суставом. Клинически отмечается удовлетворительное стояние, костных фрагментов, незначительная (до 1 мм) щель между отломками, которая заполнена плотной фиброзной тканью без явлений оссификации. Концы кости порозны с частым образованием остеофитов, имеют костные пластинки, закрывающие костномозговой канал. Реже образуется фиброзно-синовиальный ложный сустав и в этом случае происходит также закрытие костномозговых каналов костной пластинкой, а концы костей покрываются хрящевой тканью. Оба костных отломка охватываются соединительнотканной муфтой, выполняющей функцию капсулы. Между отломками скапливается синовиальная жидкость. Таким образом, на концах кости формируется подобие сустава. Отмечается склероз суставных концов и особенно верхнего отломка (рис. 59).

Рис. 59. Схема фиброзно-синовиального ложного сустава. 1 — суставные поверхности; 2 — фиброзно-синовиальная оболочка.
Причины образования ложного сустава
- 1.Недостаточная иммобилизация по качеству и срокам перелома.
- 2.Интерпозиция тканей между отломками (мышечная, костная, надкостничная и т. д.).
- 3.Дефект костной ткани.
- 4.Плохое стояние костных отломков.
- 5.Ошибки при остеосинтезе — использование неподходящего для остеосинтеза материала. Нередки при остеосинтезе грубая травматизация тканей и плохая послеоперационная иммобилизация, что приводит к образованию ложного сустава.
Из так называемых трофических причин в образовании ложного сустава играют роль:
- 1) инфекция (сифилис острые инфекционные заболевания, малярия и др.);
- 2) рефлекторные трофические расстройства на месте перелома вследствствие поражения концевых нервных ветвей;
- 3) нарушение обмена веществ, особенно кальция и фосфора в тканях, а также при диабете, аддисоновой болезни, акромегалии, авитаминозах и др.;
- 4) сосудистая недостаточность (при слоновости, ранениях магистральных сосудов и т. д.). Считают, что для образования ложного сустава большое значение имеет повреждение периферической иннервации кровеносных сосудов, предрасполагающее к развитию ложного сустава;
- 5) рентгеновское облучение в значительных дозах, так как лучи Рентгена способны угнетать процесс остеогенеза.
Клиническая картина ложного сустава
Клиническая картина ложного сустава очень характерна — подвижность в месте перелома, атрофия мышц, припухлость тканей на месте ложного сустава (разрастание рубцово-соединитель-ной ткани). Рентгенологически отмечаются наличие щели между отломками, склероз концов костей, заращение костномозгового канала.
Лечение ложного сустава
Несмотря на ряд предложенных консервативных средств (введение препаратов, стимулирующих остеогенез, магнитотерапия, электростимуляция и т. д.), основным в лечении ложных суставов остается оперативное лечение. Ведущим среди оперативных методов лечения ложных суставов является компрессионный остеосинтез. В тех случаях, когда используется внеочаговый остеосинтез компрессионно- дистракционными аппаратами, обнажение, освежение костных отломков и костная пластинка необязательны. Если же применяется остеосинтез ложного сустава погружным фиксатором, то операция должна включать "следующие три основных элемента:
- 1) освежение костных концов в месте перелома;
- 2) плотное соединение отломков в правильном положении;
- 3) биологическая стимуляция регенерации с помощью костной пластики (предпочтительна аутопластика).
Общие принципы, оперативного лечения ложного сустава
1.Операция должна производиться не ранее чем через 6—12 мес посае стойкого заживления раны (при осложненных переломах).
2.При наличии спаянных с костью рубцов необходимо их иссечь и произвести кожную пластику для закрытия дефекта. Эти два положения не касаются случаев, если предпринимается внеочаговый компрессионный остеосинтез.
3. Отломки должны быть точно сопоставлены.
4. Обязательно освежение концов костных фрагментов, восстановление проходимости костномозговых каналов и иссечение Рубцовых тканей.
Из многих способов лечения ложных суставов наиболее распространены следующие.

Остеосинтез костными трансплантатами. Лучшие результаты дает пластика аутогенными трансплантатами: используют также аллотрансплантаты. Хуже всего результаты применения ксенотрансплантатов, которые практически не используются при ложных суставах. После операции костной пластики, при которой непременным условием является создание полной неподвижности пересаженной костной ткани и хорошее ее укрытие мышцами, необходимо произвести надежную иммобилизацию на время, нужное для перестройки трансплантата. При ложных суставах показана также операция Чаклина с применением экстра- и интрамедуллярных трансплантатов (рис. 61).

Рис. 61. Метод интра-экстрамедуллярной костной пластики по Чаклину. а — экономное освежение концов; б — снятие надкостницы с интрамедуллярного трансплантата; в — экстрамедуллярный трансплантат (с надкостницей), г — интрамедуллярный трансплантат введен в костномозговой канал; д — экстрамедуллярный трансплантат уложен в приготовленное ложе; е - место пластики укрывают мышцами.
В последнее время при ложных суставах широко применяют компрессионные аппараты Гудушаури, Илизарова и др. Сочетая плотное соприкосновение отломков и их прочное удержание при помощи аппаратов с элементами костной пластики, удается добиться улучшения результатов лечения.
Наибольшие трудности возникают при ложных суставах больше-берцовой кости. В этих случаях применение внеочагового компрессионно-дистракционного остеосинтеза имеет преимущества по сравнению с другими методами. Оно позволяет получить сращение без вмешательства на ложном суставе, ликвидировать воспалительный процесс при ложных суставах, осложненных свищевой формой остеомиелита. Средняя длительность пребывания конечности в аппарате и окончательного сращения составляет 5—8 мес. Нагрузку на конечность можно давать спустя 2 мес. после операции.
Лечение обычно оперативное. В тех случаях, когда операция не показана, рекомендуется носить шинно-гильзовые ортопедические аппараты.
Операции при болтающихся суставах в основном бывают двух типов — костная пластика и обходная костная пластика.
Костная пластика производится чаще всего после подготовки кожи в зоне операции. Подготовка заключается в иссечении кожных и более глубоких рубцов с последующей заменой дефекта кожной пластикой на питающей ножке. Процесс подготовки мягких тканей непосредственно к основной операции, костной пластики обычно длителен (9—12 нед).
После кожной пластики, если она необходима, производится операция непосредственно на болтающемся суставе: освежают измененные концы отломков, иссекают фиброзную ткань, в костномозговые каналы отломков внедряют массивный костный трансплантат, дополнительно по бокам трансплантата помещают один или два костных трансплантата.
При дефектах большеберцовой кости проводят операцию по Гану — Гентингтону: отсекают участок малоберцовой кости, чаще всего в ее средней части и внедряют этот фрагмент соответственно в верхний и нижний фрагменты большеберцовой кости (рис. 62).

Рис. 62. Замещение дефекта большеберцовой кости по Гану — Генталнгтону.
При замедленной консолидации перелома, а также ложных и болтающихся суставах показаны общеукрепляющее лечение, рациональное питание, витамин В12.
При лечении псевдоартрозов возможны ошибки. Не следует при разнообразных нарушениях сложного процесса регенерации всегда применять какой-либо один метод. Ошибочным и необоснованным считается остеосинтез металлическим штифтом без добавочного экстрамедуллярного трансплантата. Также ненадежны интрамедуллярный гомотрансплантат или гетеротрансплантат без добавочного наружного аутотрансплантата. Ошибкой следует считать укладку экстрамедуллярного трансплантата на неосвеженные поверхности кортикального слоя отломков. При освежении надо соблюдать чувство меры: нельзя обнажать широко без необходимости отломки, нарушать кровообращение, травмировать надкостницу. Без освежения ложа, в которое погружается наружный трансплантат, и без надежной фиксации может не наступить его приживления, что очень важно для развития экстрамедуллярной мозоли. Трансплантат, пересаженный в рубцовую ткань, особенно после инфекционного процесса, не прикрытый мышцами и здоровой кожей, находится в неблагоприятных условиях приживления. Возможны рецидивы, нагноения и секвестрация трансплантата.
Травматология и ортопедия. Юмашев Г.С., 1983г.
Несмотря на ряд предложенных консервативных средств (введение препаратов, стимулирующих остеогенез, магнитотерапия, электростимуляция и др.) основным в лечении ложных суставов остается оперативное вмешательство.
Ведущим среди оперативных методов лечения ложных суставов является компрессионный остеосинтез. В тех случаях, когда используется внеочаговый остеосинтез компрессионно-дистракционными аппаратами, обнажение, освежение костных отломков и костная пластика необязательны. Если же применяется остеосинтез ложного сустава погружным фиксатором, то операция должна включать следующие три основных элемента:
1) освежение костных концов в месте перелома;
2) плотное соединение отломков в правильном положении;
3) биологическая стимуляция регенерации с помощью костной пластики (предпочтительна аутопластика).
Общие принципы оперативного лечения:
1. Операция должна проводиться не раннее чем через после стойкого заживления раны (при осложненных переломах).
2. При наличии спаянных с костью рубцов необходимо их иссечь и произвести кожную пластику для закрытия дефекта. Эти два положения не касаются случаев, когда предпринимается внеочаговый компрессионный остеосинтез.
3. Отломки должны быть точно сопоставлены.
4. Обязательное освежение концов костных фрагментов, восстановление проходимости костномозговых каналов и иссечение рубцовых тканей.
Из многих способов лечения ложных суставов наиболее распространены следующие.
Остеосинтез костными транслантатами. Лучшими результаты дает пластика аутогенными трансплантатами; используют также аллотрансплантаты. Наименее эффективно применение ксенотрансплантатов, которые практически при ложных суставах не используются. После костной пластики, при которой непременным условием является создание полной неподвижности пересаженной костной ткани и хорошее ее укрытие мышцами, необходимо произвести надежную иммобилизацию конечности на весь период перестройки трансплантата.
Показана также операция Чаклина с применением экстра- и интрамедуллярных костных трансплантатов.
В последнее время при ложных суставах широко применяют компрессионные аппараты Гудушаури, Илизарова, Калнберза и др. Сочетая плотное соприкосновение отломков и их прочное удержание при помощи аппаратов с элементами костной пластики, добиваются заметного улучшения результатов лечения.
При ложных суставах большеберцовой кости применение внеочагового компрессионно-дистракционного остеосинтеза имеет преимущества по сравнению с другими методами, так как позволяет достигнуть сращения без вмешательства на ложном суставе, ликвидировать воспалительный процесс при ложных суставах, осложненных свищевой формой остеомиелита. Средняя длительность пребывания конечности в аппарате и окончательного сращения Нагрузку на конечность можно разрешить спустя 2 мес. после операции.
Лечение в этих случаях обычно хирургическое. В тех случаях, когда операция не показана, рекомендуется носить ортопедические аппараты (ортезы).
Костную пластику производят чаще всего после подготовки кожи в зоне операции. Эта подготовка заключается в иссечении кожных и более глубоких рубцов с последующей заменой дефекта кожной пластикой на питающей ножке. Процесс подготовки мягких тканей непосредственно к основной операции (костная пластика) обычно длителен
При дефектах большеберцовой кости проводят операцию по Гану-Гентингтону: отсекают участок малоберцовой кости, чаще всего в ее средней части, и внедряют этот фрагмент соответственно в верхний и нижний фрагменты большеберцовой кости.
При лечении псевдоартрозов возможны ошибки. Не следует при разнообразных нарушениях сложного процесса регенерации всегда применять какой-либо один метод лечения. Ошибочным и необоснованным считается остеосинтез металлическим штифтом без добавления экстрамедуллярного трансплантата, как и применение интрамедуллярного гомотрансплантата или аллотрансплантата без наложения на кость наружного аутотрансплантата.
Ошибкой следует считать также укладку экстрамедуллярного трансплантата на неосвеженные поверхности кортикального слоя отломков кости. При освежении костных концов в зоне ложного сустава нельзя обнажать широко без необходимости отломки, нарушать кровообращение, травмировать надкостницу.
Одним из важных условий, обеспечивающих сращение, является прочность длительной внутренней и наружной фиксации отломков.

Консолидация костных отломков после перелома происходит по биологическим законам, через определенные временные сроки и зависит от многих факторов.
К местным факторам, способствующим консолидации относятся:
Нарушения процессов консолидации обусловлены как внешними факторами (несоблюдение сроков и правил иммобилизации, отклонения в режимах клинического ведения пациентов), так и внутренними (нарушения минерального, белкового, гормонального обменов). Они ведут к замедлению сращения переломов. Развивается процесс неполноценной консолидации или патологическая репаративная регенерация.
Процесс остеорепарации значительно ускоряется при использовании стабильной фиксации костных отломков и хорошем кровообращении. В тех случаях, когда сохраняется подвижность отломков, происходит микротравматизация капиллярной сети и пролиферация тканей, устойчивых к гипоксии,– волокнистой соединительной и хрящевой. Это обстоятельство может привести к рубцовой интерпозиции в зоне перелома, замедленной консолидации и образованию ложного сустава. Важным фактором сращения перелома кости является состояние местного кровообращения.

При переломах повреждаются не только сосуды окружающих мягких тканей, но и сосуды, проходящие в самой кости. В области метафизов костей, где большой мышечный массив, кровоснабжение, как правило, хорошее. Поэтому переломы этой локализации хорошо срастаются. Однако нижняя треть большеберцовой кости, локтевая кость и некоторые другие при переломе могут быть лишены кровоснабжения, так как повреждается внутрикостная артерия, которая является основным источником питания.
Замедленная консолидация переломов

В тех случаях, когда по истечении максимального срока, необходимого для сращения перелома данной локализации, консолидация не наступает – говорят о замедленной консолидации. При этом отмечается задержка в перестройке фиброзной мозоли в костную.Данный патологический процесс может продолжаться в течение 1,5–2 сроков, необходимых для сращения перлома. Клинически отмечается незначительная эластическая подвижность в месте перелома, боль при нагрузке. Рентгенологические признаки косной мозоли недостаточно выражены, хорошо прослеживается линия перелома.
Лечение замедленной консолидации может быть консервативным и оперативным. Консервативное лечение состоит в продлении иммобилизации перелома на срок, необходимый для его сращения, как если бы он был свежим.
При лечении замедленной консолидации необходимо учитывать, что длительное отсутствие функциональной нагрузки на травмированный сегмент приводит к стойкой мышечной атрофии, ограничению подвижности в иммобилизированных суставах. Эти нарушения даже при сращении перелома потребуют очень длительного реабилитационного периода.
Поэтому попытки консервативного лечения при замедленной консолидации оправданы только тогда, когда клинически и рентгенологически процесс консолидации хорошо прослеживается, но ещё не завершен. Если прогнозируемые сроки консолидации увеличиваются более чем на 1–1,5 месяца, предпочтительно оперативное лечение.
Способы оперативного лечения замедленной консолидации:
- 1. Туннелизация по Беку. Спицей Киршнера или сверлом малого диаметра формируют в различных направлениях каналы, проходящие через линию перелома от одного отломка в другой. По этим каналам прорастают сосуды, что способствует сращению перелома.
- 2. Внеочаговый компрессионно-дистракционный остеосинтез (ВКДО) позволяет долгое время прочно удерживать отломки при плотном их соприкосновении, а так же выполнять попеременно компрессию и дистракцию регенерата. Чаще используют аппарат Илизарова.
- 3. Стабильно-функциональный погружной остеосинтез с использованием интрамедуллярных фиксаторов с блокированием. Этот метод допускает раннюю функциональную нагрузку сегмента до полной костной консолидации. Использование накостного остеосинтеза пластинами LCP – пластины с ограниченным контактом.
- 4. Костная пластика.
Ложные суставы
Ложный сустав – это стойкое нарушение целостности кости, имеющее клинические и рентгенологические признаки. Если консолидация перелома не состоялась в более чем двойной срок сращения для данной локализации и произошло закрытие костномозговых каналов, можно констатировать формирование ложного сустава.
Различают нормотрофический, гипертрофический, гипотрофический, атрофический, истинный фиброзно-синовиальный ложный сустав (неоартроз).
В нормотрофическом ложном суставе сохраняются процессы формирования костной мозоли, но они протекают больше двойного срока сращения для данной локализации.
В гипертрофическом ложном суставе идет усиленное костеобразование, которое сопровождается образованием избыточной костной мозоли, узкой плохо прослеживаемой линией ложного сустава.
Признаки истинного фиброзно-синовиального ложного сустава (неоартроза):
Лечение
В лечении ложных суставов сочетают консервативные и оперативные методы. К консервативным способам лечения относят физиотерапевтические методы: электростимуляция образования костной мозоли, волновое лечение (лазеротерапия, магнитотерапия, светотерапия, теплотерапия), медикаментозное лечение, оптимизирующее минеральный баланс. Нередко применяют анаболические стероиды, которые стимулируют все виды обменов.
При оперативном лечении ложных суставов могут быть использованы все методы, изложенные в разделе хирургического лечения замедленной консолидации.
Оперативные методы делят на очаговые (с вмешательством на патологичесой зоне) и внеочаговые (без вмешательства). К внеочаговым относят применение аппаратов внешней фиксации. При использовании аппаратов внешней фиксации после его наложения чередуют дистракцию и компрессию, а затем стабилизируют аппарат. Как правило, нормотрофические и гипертрофические ложные суставы лечатся без вмешательства на очаге аппаратным остеосинтезом и консервативными методами.
Оперативное лечение с вмешательством на очаге бывает нескольких видов: малоинвазивное и инвазивное. К малоинвазивным методикам относят введение остеогенных материалов (костного матрикса) или остеогенных клеток (остеобластных и стволовых) в костную мозоль либо параоссально в проекции ложного сустава.
Из инвазивных методов применяется декортикация костных концов отломков с резекцией патологической зоны и обязательным восстановлением костномозгового канала. Декортикация производится в области концов костных отломков путём отсечения пластинок кортикальной кости с сохранением их связи с окружающими мягкими тканями. Фрагменты отщеплённого кортикального слоя служат дополнительными стимуляторами костеобразования. При образовании костного дефекта он замещается костными трансплантатами. Фиксация кости осуществляется погружными металлическими конструкциями, либо аппаратами внешней фиксации.
Сроки восстановления, как правило, превышают в два – три раза средние сроки характерные для сращения переломов данной локализации.
КОСТНАЯ ПЛАСТИКА
Костная пластика – это оперативное вмешательство, направленное на восстановление целостности кости, с использованием костно-пластических материалов. В зависимости от разновидности костно-пластических материалов костную пластику подразделяют на: аутопластику, аллопластику, ксенопластику (гетеропластику), брефопластику и комбинированную пластику.
Костная пластика выполняется различными материалами: аутопластика – использование тканей самого пациента, аллопластика – использование трупных тканей или препаратов из этих тканей, ксенопластика (гетеропластика) – использование тканей животных (пересадка тканей от особей другого биологического вида), брефопластика (от греческого brephos – плод) – аллопластика с применением тканей мертворожденных плодов или погибших новорожденных.
Показаниями к костной пластике являются дефекты костной ткани травматического и послеоперационного генеза, нарушения консолидации, деформации развившейся вследствие патологической консолидации, ортопедические заболевания – костные кисты, отдельные формы остеобластокластом, фиброзная дисплазия, последствия остеомиелита.
Использование аутогенных тканей подразумевает пересадку как свободных трансплантатов (лишённых кровоснабжения), так и трансплантатов на сосудистой ножке. Пересаживают кортикальную либо губчатую кость. Свободные трансплантаты являются матриксом для формирования на месте трансплантации новой костной ткани. При этом отмечается рассасывание пластического материала и замещение вновь сформированной костной тканью. Успех костной пластики сопряжён с синхронностью процессов рассасывания старой и формированием новой костной ткани. Костные трансплантаты на сосудистой ножке используются в расчете на полное приживление пересаженной костной ткани. При дефектах большого объёма используют комбинацию кортикальных и губчатых трансплантатов.
Под аллопластикой понимают трансплантацию трупных тканей. Возможна пересадка кортикальной и губчатой костной ткани. Наиболее часто используются кортикальные аллотрансплантаты.
Губчатые аллотрансплантаты обладают более высокой антигенной активностью, которая может привести к развитию воспаления в области пластики и секвестрации трансплантата. Это обусловлено сохранением в губчатой костной ткани элементов костного мозга, обладающего высокой антигенностью. Достаточно широко используют аллогеный деминерализованный костный матрикс – лишённая клеток и минералов белковая строма костной ткани.
При пересадке аллогенных костей, как правило, используют консервированный материал. Целью консервации материала являются стерилизация, снижение антигенности и увеличение сроков хранения пластического материала. С целью стерилизации применяют гамма излучение, химическую стерилизацию, низкие температуры и др. Хранение трансплантатов возможно в жидких, газообразных средах. Наиболее эффективна консервация пластического материала в жидких средах с одновременной стерилизацией материала, снижением антигенности и длительными сроками хранения. К таким консервантам относят жидкие среды на основе растворов формальдегида слабой концентрации.
Заготовка тканей проводится у лиц, скоропостижно скончавшихся от травм, острой сердечно-сосудистой патологии, асфиксии, отравления алкоголем.
Забор материала осуществляется впервые 12 часов, перед изъятием тканей труп подвергается санитарной обработке. При заборе тканей нет необходимости в соблюдении правил асептики и антисептики. Изъятые ткани тщательно промывают проточной водой. Костная ткань освобождается от остатков мягких тканей и костного мозга.
Методика консервации костных тканей: готовят растворы 0,2–0,4% формолового и 0,1–0,2% глутарового альдегида, растворы смешивают в отношении 1:1, pН среды доводят до 7,0–7,4 путем введения фосфатного буфера 20–40 мл на литр консервирующей смеси. Приготовленный к консервации материал помещают в смесь в соотношении 1 часть материала на 5–10 частей консерванта в герметически закрывающейся стеклянной посуде. Хранение проводится в условиях бытового холодильника при t +2°–+4° по Цельсию. В течение первого месяца консервант меняют 2 раза в неделю, далее 1 раз в 1–2 месяца.
Стерилизация биологических объектов наступает в течение 6–12 часов при воздействии на них смеси растворов 0,2– 0,4% формолового и 0,1–0,2% глутарового альдегидов. Биологические ткани, консервированные в смеси ФА и ГА, подавляют рост золотистого, эпидермального стафиллококков, кишечной, синегнойной палочек и спорогенной клостридии. Выявленный синергизм действия смеси растворов формолового и глутарового альдегидов на микрофлору позволяет надежно стерилизовать заготовленные биологические ткани без соблюдения правил асептики в течение 18–72 часов и обеспечивать их устойчивость к инфекции после трансплантации в организм реципиента.
Согласно исследованиям, проведенным на кафедре травматологии, ортопедии и ВПХ ГрГМУ, решающую роль в реваскуляризации консервированных аллотрансплантатов играет сосудистое русло параоссальных тканей и окружающих мышц. Радиологическими исследованиями с помощью радионуклида кальция (45-Са) установлено, что, начиная с 2–3 недель, консервированные в смеси альдегидов кости после их трансплантации в дефекты скелета вступают в минеральный обмен. К двухнедельному сроку наблюдений изотоп регистрировался в области стыков, через месяц – в самом реплантате. Наиболее выраженное накопление зарегистрировано к 4–6 месяцам, что связано с активной перестройкой аллотрансплантата. К 6–9 месяцам содержание 45-Са в реплантированной кости постепенно снижалось, а через 12 месяцев и в более поздние сроки на всем протяжении реплантированной кости и костей ложа реципиента накопление изотопа было равномерным.
Рентгенологическими исследованиями оперированных пациентов выявлена определенная закономерность перестройки аллотрансплантатов. Так, в первом периоде (до 4 недель после операции) не определялось заметных изменений, аллотрансплантат сохранял присущую ему форму и плотность кости. Во втором периоде (1–6 месяцев после трансплантации) выявлялись признаки наличия периостальной мозоли, идущей со стороны кости реципиента. Отмечалось сращение трансплантата с костным ложем и постепенное исчезновение границы между ними. В это время происходило изменение интенсивности тени трансплантата, связанное с его частичным рассасыванием и с замещением собственной костью реципиента. Третий период (6 месяцев – 2 года) характеризуется полной консолидацией аллотрансплантата с костью реципиента и завершением окончательной перестройки костной структуры.
Ксенопластика используется достаточно редко ввиду высокой антигенности тканей. Чаще используют костный матрикс из этих материалов.
Брефоматериалы применяются также редко ввиду ограниченной доступности этого вида пластического материала.
Комбинированная пластика подразумевает совместное применение ауто- и аллотканей в различных вариантах.
Источник: Травматология и ортопедия : пособие для студентов лечебного и педиатрического факультетов / под ред. В.В. Лашковского. – Гродно

Сращение переломов: репаративная регенерация кости после травмы, фазы, стадии срастания перелома
Репаративная регенерация кости после травмы представляет собой сложный биологический процесс, который начинается непосредственно после перелома и развивается на основе физиологической регенерации
Материал применяется только с целью обучения и ознакомления, и используется в рамках цитирования и/или как объект обсуждения.
Внимание! Все материалы размещенные на странице не являются рекламой,
а есть не что иное как мнение самого автора,
которое может не совпадать с мнением других людей и юридических лиц!
Ложный сустав – это массивный дефект кости, который возникает из-за неправильного сращения перелома. Чаще всего он формируется в области голени. Реже поражается надколенник, ключица, ладьевидная, плечевая, лучевая, локтевая или бедренная кости. По статистике, псевдоартроз выявляют у 0,5-27% людей с переломами в анамнезе. От патологии чаще страдают лица, перенесшие открытые или огнестрельные ранения.
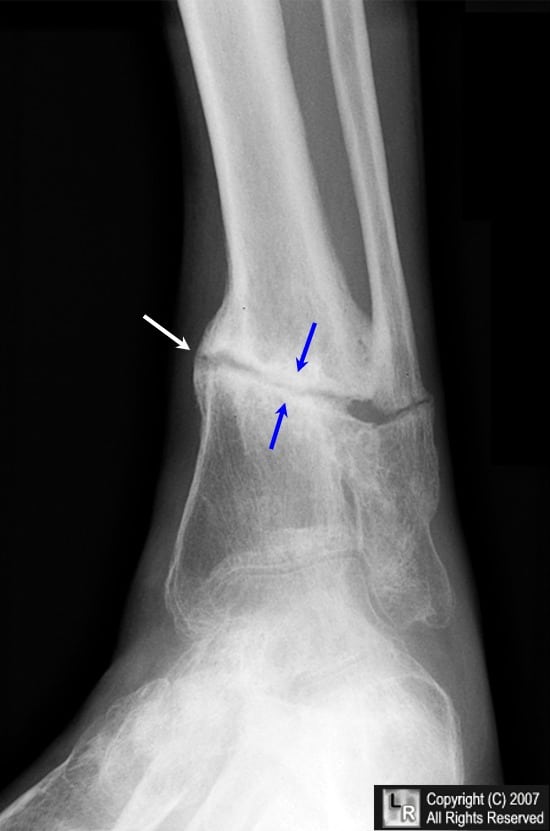
Выясним, что такое ложный сустав при переломе, почему он формируется, как от него можно избавиться.
В редких случаях болезнь может иметь врожденный характер. Врожденные ложные суставы локализуются на границе между средней и нижней частями голени. Подобные дефекты строения костей возникают из-за грубых нарушений внутриутробного развития плода.
Какой сустав можно назвать ложным
Важно знать! Врачи в шоке: "Эффективное и доступное средство от АРТРОЗА существует. " Читать далее.
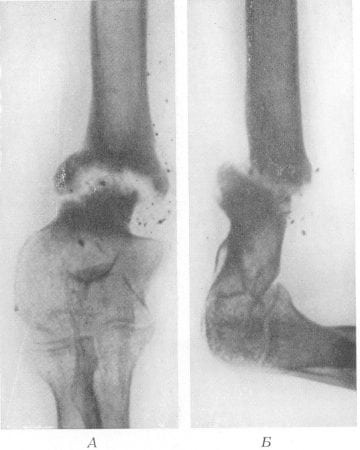
Если выразиться проще, псевдоартроз – это патологический сустав, возникший в том месте, где его быть не должно. К примеру, он может сформироваться в теле большеберцовой кости и привести к аномальной подвижности ее фрагментов. На рентгенограммах можно увидеть четкую щель между отломками и полное закрытие костномозговых каналов замыкательными пластинками.
Поначалу ложный сустав имеет мало общего с истинным. Однако со временем замыкательные пластины покрываются хрящевой тканью, превращаясь в типичные суставные поверхности. Вокруг дефекта разрастается фиброзная ткань, которая в итоге образует что-то вроде суставной капсулы. Псевдоартроз становится все больше похожим на настоящий сустав.
Причины образования ложных суставов
Дефект формируется из-за нарушения сращения костных фрагментов. Причиной могут быть ухудшение кровоснабжения кости, снижение минеральной плотности костной ткани, неправильное сопоставление костных отломков или плохая фиксация места перелома. К появлению ложных суставов также могут приводить инфекционные осложнения, системный остеопороз, асептический некроз кости и т. д.
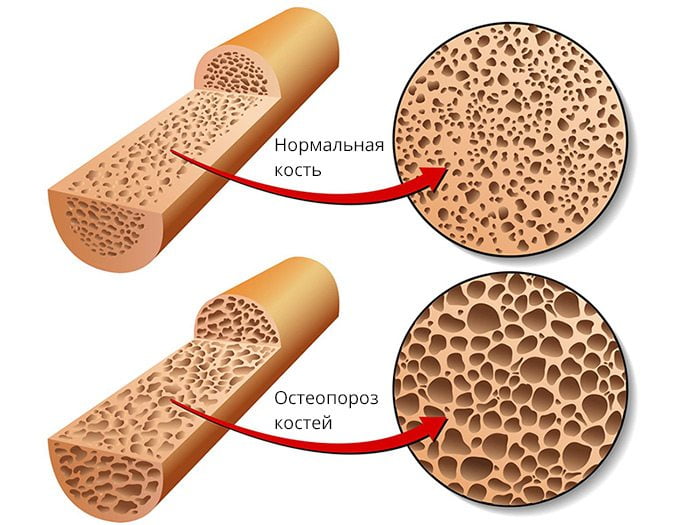
Основные причины несращения костных фрагментов:
- Недостаточный контакт между отдельными частями кости, мешающий им прочно срастись друг с другом.
- Несостоятельность костной ткани, препятствующая ее нормальному ремоделированию. Причиной чаще всего бывает остеопороз и аваскулярный некроз.
Таблица 1. Факторы риска, повышающие вероятность развития псевдоартроза
Связанные с человеком
Признаки формирования ложного сустава после перелома
Даже "запущенный" АРТРОЗ можно вылечить дома! Просто не забывайте раз в день мазать этим.
Больные с псевдоартрозом практически всегда жалуются на открытые или закрытые переломы в анамнезе. На протяжении многих месяцев после травмы их беспокоит постоянная боль, аномальная подвижность кости и характерные щелчки при движениях. Если ложный сустав локализуется на нижней конечности, больному становится трудно ходить и вести привычный образ жизни.
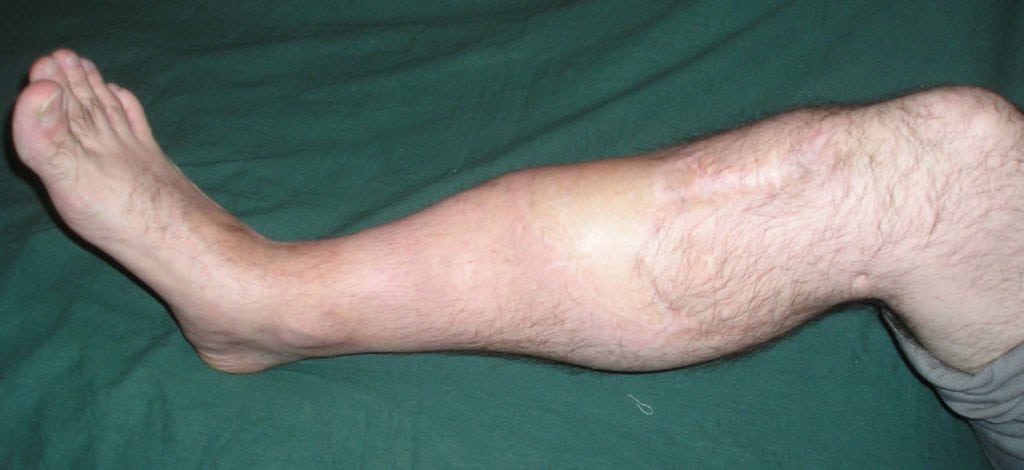
В большинстве случаев врачи диагностируют псевдоартроз без особых трудностей. Если у них появляются сомнения или возникает потребность в уточнении характера дефекта, они назначают дополнительные методы исследования. Чаще всего пациентам делают рентгенографию или компьютерную томографию.
Методы лечения патологии
Псевдоартроз лечат исключительно оперативным путем. Хирурги иссекают фиброзную и хрящевую ткань, расположенную между костными фрагментами. Затем они заново сопоставляют отломки и фиксируют их системами чрескостной, накостной или интрамедуллярной фиксации. После этого пациент проходит полноценную реабилитацию.
Для стабилизации костных фрагментов могут использовать такие приспособления:
- аппарат Илизарова;
- штифты;
- винты;
- накостные пластины;
- интрамедуллярные стержни.
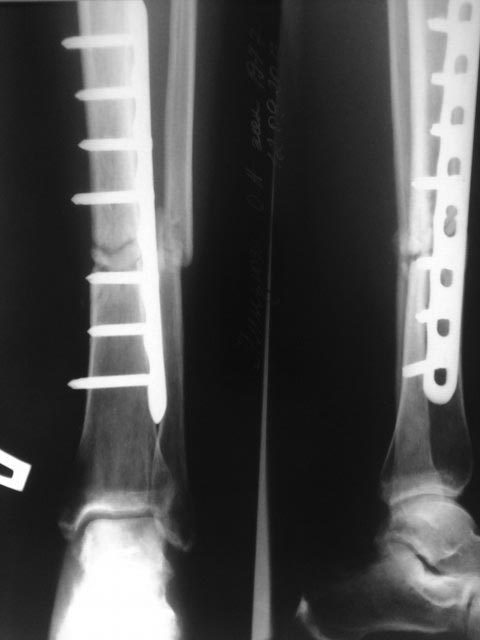
Реабилитация после подобных операций длится гораздо дольше, чем после репозиции обычных переломов.
Лечение ложных суставов у больных с остеопорозом
При лечении псевдоартроза у лиц с остеопенией большое значение имеет ранняя мобилизация. Динамические и весовые нагрузки на кость ускоряют ремоделирование костной ткани и препятствуют развитию вторичного иммобилизационного остеопороза. Поэтому врачи следят за тем, чтобы в послеоперационном периоде человек начинал как можно раньше вставать с постели и выполнять специальные упражнения.
Хирургическое лечение пациентов данной группы всегда дополняет медикаментозная терапия. Им обязательно дают препараты кальция, активные метаболиты витамина D3 и антирезорбтивные средства. Вместе с этим пациентам назначают лечебную физкультуру и массаж. Такое лечение позволяет гораздо быстрее восстановить функции поврежденной конечности.
Что будет, если не лечиться
Отсутствие квалифицированной медицинской помощи может иметь для человека ужасные последствия. В лучшем случае его будут беспокоить постоянные боли, а функция конечности останется нарушенной. В худшем у больного разовьется выраженная деформация ноги или руки, что приведет к инвалидности.
Как забыть о болях в суставах и артрозе?
- Боли в суставах ограничивают Ваши движения и полноценную жизнь…
- Вас беспокоит дискомфорт, хруст и систематические боли…
- Возможно, Вы перепробовали кучу лекарств, кремов и мазей…
- Но судя по тому, что Вы читаете эти строки - не сильно они Вам помогли…
Но ортопед Валентин Дикуль утверждает, что действительно эффективное средство от АРТРОЗА существует! Читать далее >>>
Читайте также:


