Папилломавирусная инфекция что это дискариоз клеток
Папилломавирусная инфекция (ПВИ) половых органов — группа заболеваний, ассоциированных с вирусом папилломы человека - ВПЧ.
Генитальные бородавки, генитальные кондиломы.
КОД ПО МКБ-10 В97.7 Папилломавирусы. А63.0 Аногенитальные (венерические) бородавки.
По данным МЗСР РФ за 2001 г., заболеваемость наиболее известной формы папилломавирусной инфекции — остроконечных кондилом — 26 на 100 000 населения. В мире около 300 млн инфицированных ВПЧ. ПВИ гениталий выявлена у 30,3% населения европейской части РФ.
Пик заболеваемости папилломавирусной инфекцией половых органов регистрируют у 15–25летних сексуально активных женщин. Через три года после начала половой жизни 70% женщин инфицированы ВПЧ. Частота папилломавирусной инфекции прямо пропорциональна числу половых партнёров.
Международное агентство по исследованию рака объявило ВПЧ типов 16 и 18 канцерогенными факторами, а типов 31, 33 и 35 — возможными канцерогенами.
Клиникоморфологическая классификация ВПЧ - ассоциированных поражений нижнего отдела половых органов:
- Клинические формы (видимые невооружённым глазом).
-Экзофитные кондиломы (остроконечные типичные, папиллярные, папуловидные).
-Симптоматические ЦИН. - Субклинические формы (невидимые невооружённым глазом и бессимптомные, выявляемые только при кольпоскопии
и/или при цитологическом или гистологическом исследовании).
-Плоские кондиломы (типичная структура с множеством койлоцитов).
-Малые формы (различные поражения многослойного плоского и метапластического эпителия с единичными
койлоцитами).
-Инвертирующие кондиломы (с локализацией в криптах).
-Кондиломатозный цервицит/вагинит. - Латентные формы (обнаружение ДНК ВПЧ при отсутствии клинических, морфологических или гистологических
изменений). - ЦИН или ПИП:
-ЦИН I (ПИП низкой степени) — слабовыраженная дисплазия +/– койлоцитоз, дискератоз;
-ЦИН II (ПИП высокой степени) — выраженная дисплазия +/– койлоцитоз, дискератоз;
-ЦИН III или CIS — тяжёлая дисплазия или карцинома in situ +/– койлоцитоз, дискератоз;
-микроинвазивная плоскоклеточная карцинома.
Возбудитель папилломавирусной инфекции — вирус папилломы человека (ВПЧ). Известно более 100 типов ВПЧ, подробно описано около 80 типов. Из всех идентифицированных типов 34 поражают аногенитальную область.
ВПЧ — мукозотропные высококонтагиозные вирусы с инкубационным периодом 1–8 мес. Передача ВПЧ происходит при непосредственном контакте кожных покровов и слизистых оболочек, преимущественно при половом контакте (в том числе нетрадиционном): ВПЧносители передают половому партнёру в 46–67% случаев, причём при гомосексуальных контактах в 5–10 раз чаще, чем при гетеросексуальных. Кроме того, ВПЧ передаётся от матери к плоду, вызывая папилломатоз гортани плода; поражает клетки трофобласта, приводя к спонтанным абортам. Не исключена возможность контактной трансмиссии ВПЧ через руки и медицинские инструменты. ВПЧ попадает в клетки слизистых оболочек и (или) кожных покровов при контакте через микроповреждения и поражает базальные слои эпителия.
В заражённых клетках вирусный геном может существовать в двух формах: эписомальной (вне хромосом) и интегрированной в клеточный геном. Интеграция вирусной ДНК ведёт к нестабильности клеточного генома и хромосомным нарушениям.
Присутствуя в макроорганизме, вирусы не всегда вызывают заболевание. Установлено транзиторное и постоянное носительство ВПЧ. На трансформацию латентного носительства ВПЧ в клинические и субклинические формы влияют следующие факторы:
- вирусный фактор (типы 16 и 18 персистируют в организме дольше, чем низкоонкогенные);
- иммунологическая реакция организма женщины на внедрение вируса (генетически детерминированная или приобретённая под влиянием факторов окружающей среды);
- кофакторы опухолевой трансформации (гормональный фон и курение).
Носительство ВПЧ не пожизненное. По данным ВОЗ (1997), при отсутствии отягощающих факторов в течение 3 лет ПИП низкой степени, содержащие ВПЧ, подвергаются регрессии в 50–62% наблюдений. У 70% молодых ВПЧ-инфицированных женщин ДНК ВПЧ перестают обнаруживать на протяжении первых 24 месяцев наблюдения, у пожилых пациенток ВПЧ персистирует более продолжительное время. Скорость элиминации зависит от иммунореактивности клеток организма хозяина и значительно снижается при инфицировании несколькими типами ВПЧ.
Клиническая картина ПВИ обусловлена типом вируса и состоянием иммунитета. Папилломавирусная инфекция половых органов — полиморфная многоочаговая патология кожи и слизистых оболочек нижнего отдела полового тракта.
Экзофитные кондиломы могут быть бессимптомными или сопровождаться такими симптомами, как зуд, бели, болезненность. Во время беременности наблюдают склонность к росту кондилом, после родов — к спонтанной регрессии. Субклинические формы папилломавирусной инфекции обычно бессимптомны, в редких случаях наблюдают зуд, жжение, бели. Малые формы папилломавирусной инфекции характеризует небольшая выраженность цитопатического действия ВПЧ (наличие единичных койлоцитов) на фоне различных изменений многослойного плоского и метапластического эпителия, включая гипер и паракератоз, гиперплазию базального слоя, акантоз, цервицит. Предполагают, что малые формы папилломавирусной инфекции (ПВИ) — одна из стадий развития или регресса плоской кондиломы.
Латентные формы папилломавирусной инфекции (бессимптомное вирусоносительство) выявляют при обследовании здоровых женщин или пациенток, обратившихся по поводу другого заболевания.
Симптоматические ЦИН определяют невооружённым глазом, они представлены участками выраженного ороговения (в виде белёсых бляшек), экзофитными образованиями или изъязвлениями. При кондиломатозном цервиците и вагините при осмотре отмечают волнистую (негладкую) поверхность эпителия шейки матки и влагалища.
Субклинические формы диагностируют при кольпоскопическом и цитологическом исследованиях.
Специфического комплекса кольпоскопических признаков папилломавирусной инфекции нет. Наиболее характерными кольпоскопическими признаками субклинических форм папилломавирусной инфекции считают: ацетобелый эпителий, мозаика, пунктация, атипичная зона трансформации.
Выраженные (грубые) кольпоскопические признаки папилломавирусной инфекции:
- грубая лейкоплакия;
- грубые мозаика и пунктация.
Малые кольпоскопические признаки папилломавирусной инфекции:
- тонкая лейкоплакия;
- нежные мозаика и пунктация.
Основной цитологический признак папилломавирусной инфекции — наличие в мазке клеток с койлоцитозом и дискератозом. Обнаружение в мазке клеток с дискариозом предполагает наличие ЦИН. Койлоциты образуются в тканях в результате цитоспецифического эффекта ВПЧ и представляют собой клетки многослойного плоского эпителия промежуточного типа с увеличенными ядрами и обширной околоядерной зоной просветления за счёт дегенеративных изменений и некроза разрушенных цитоплазматических органелл.
К гистологическим проявлениям папилломавирусной инфекции шейки матки относят экзофитные и типичные плоские кондиломы, маловыраженные изменения плоского эпителия (единичные койлоциты при наличии различных изменений эпителия, в том числе кондиломатозный цервицит/вагинит), ЦИН различной степени и без них, РШМ.
- Иммунограмма.
- Обследование половых партнёров.
Эффективность диагностики папилломавирусной инфекции может быть высокой только в случае комплексного применения кольпоскопии, типирования ВПЧ и цитологического исследования.
Экзофитные кондиломы дифференцируют с другими кожными заболеваниями (широкими кондиломами при сифилисе, плоскоклеточными кондиломами, псориазом, контагиозным моллюском и др.), небольшие кондиломы у входа во влагалище — с разрастаниями гимена. Субклинические формы дифференцируют с доброкачественными процессами вульвы (воспалительными и дистрофическими).
- Дерматовенеролог — при наличии экзофитных кондилом атипичного вида.
- Иммунолог — при рецидивирующих и обширных повреждениях.
- Онкогинеколог — пациенткам с ЦИН III.
Плоские кондиломы промежности.
- Деструкция экзофитных кондилом и атипически изменённого эпителия.
- Коррекция иммунного гомеостаза.
- Лечение сопутствующих генитальных инфекций и дисбиоза влагалища.
- Лечение половых партнёров.
Для биопсии, для хирургического лечения. В большинстве случаев лечение проводят амбулаторно или в стационаре одного дня.
Для деструкции атипически изменённого эпителия применяют физические методы (диатермо крио, лазерный и радиоволновый методы), в ряде случаев — химическую коагуляцию и лечение цитотоксическими препаратами. Деструкцию экзофитных кондилом проводят после локальной инфильтрационной анестезии 0,5% раствором лидокаина (или в виде спрея).
При появления гиперемии, зуда, болезненности интервалы между процедурами можно увеличить до 2–3 дней. Цитостатические лекарственные средства: фторурацил (5% крем) применяется самостоятельно в домашних условиях. Смазывать пораженные участки кожи и слизистых оболочек 1 раз в сутки на ночь в течение 7 дней. При отсутствии эффекта от курса лечения химическими коагулянтами и цитотоксическими препаратами показано применение других деструктивных методов.
Показаниями к иммуномодуляции и противовирусной терапии являются рецидивы папилломавирусной инфекции, обширные и множественные поражения.
Иммуномодулирующие препараты (системного и локального действия) при папилломавирусной инфекции гениталий применяются как в монотерапии, так и в сочетании с деструктивными методами. Иммуномодулирующую терапию проводят под контролем иммунограммы. Применяют интерфероны и их индукторы, синтетические иммуномодуляторы, иммуноглобулины. Патогенетически обоснованным является применение иммуномодуляторов с противовирусным и антипролиферативным действием. Иммуномодуляторы применяются за 10 дней до деструкции патологического очага. По показаниям второй курс иммуномодулирующей терапии проводят после деструкции экзофитных кондилом и атипически изменённого эпителия.
Иммуномодулирующие и противовирусные препараты не рекомендуют применять во время беременности и лактации.
При адекватном лечении прогноз благоприятный.
Дискариоз шейки матки или ядер ее клеток (не путать с дискератозом — лейкоплакией) — такое заключение женщины могут прочесть в результатах анализа мазка на онкоцитологию. Данное исследование помогает довольно достоверно определить у женщины предраковые и раковые заболевания шейки. Этот вид онкологии очень распространен, в том числе у молодых женщин, младше 30 лет. Но развивается медленно. И злокачественным процесс становится не сразу. Имеются предпосылки.
Наглядно это выглядит так.
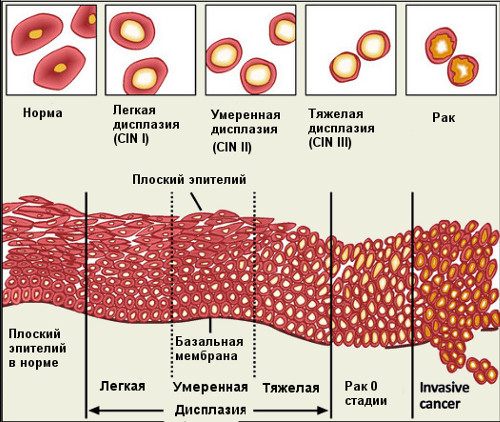
Обратите внимание на внешний вид клеток и на их видоизменение. При легкой дисплазии есть отдельные клетки с немного увеличенным относительно цитоплазмы ядром. При умеренной — таких клеток уже больше, и они имеются в слое эпителия, плотно прилегающего к базальной мембране — своеобразной перегородкой между эпителиальной и соединительной тканью. Когда этих клеток становится еще больше, причем в области базальной мембраны с внедрением в нее, это уже рак. Но только нулевой степени. Carcinoma in situ так называемая. При таком диагнозе врачи могут рекомендовать ампутацию всей матки вместе с больной шейкой. Но только если у пациентки нет репродуктивных планов, то есть она не планирует в будущем детей. В противном случае, если женщина молода и бездетна, проводится только частичное удаление шейки. Однако предупреждают, что рано или поздно, но рак вернется…
Всегда ли легкий дискариоз это начало рака и приговор для женщины? Нет, отнюдь. Нередко изменения в клетках возникают из-за воспалительного процесса. По этой причине цитограмма должна выполняться на здоровой шейке.
Причины дискариоза
Кроме банальной молочницы или дисбактериоза влагалища, провоцирующих изменения в клетках, причиной дискариоза могут стать пив — папилломавирусная инфекция (ВПЧ), это уже серьезнее, так как некоторые штаммы ВПЧ являются онкогенными и женщина, ими зараженная, должна проходить профилактическое обследование у гинеколога чаще.
Изменять внешний вид клеток могут трихомонады, гонококки, дрожжевые грибки, вирус герпеса.
Часто дискариоз диагностируется у беременных женщин. Это вариант нормы. У будущих мам клетки изменяются из-за гормонального фона. После родов все приходит в норму.
Играет роль и день цикла, когда был взят мазок. Так, не слишком информативными считаются мазки, взятые за три дня до и после менструации. Лучше всего сдавать цитограмму в середине менструального цикла.
Как лечить дискариоз шейки матки
Итак, если у вас взяли мазок с воспаленной шейки и в заключении написали, что имеется умеренный или слабо выраженный дискариоз отдельных, единичных клеток, гинеколог обязан прописать вам лечение. Обычно используются вагинальные свечи. После лечения цитологический мазок повторяется. И если дискариоз обнаруживается вновь, даже легкой степени, проводится кольпоскопия.
Что делать при выраженном дискариозе, дисплазии второй или третьей степени (CIN II или III)? Обычно в этом случае врачи рекомендуют сделать конизацию шейки матки — удалить довольно большой ее участок хирургическим путем. А удаленный материал обязательно отправить на гистологию. Забеременеть после такого обширного лечения можно. А вот возникнут ли проблемы во время вынашивания или родов с большой долей вероятности предположит гинеколог после заживания шейки.
Легкий дискариоз, дисплазия первой степени обычно требует только наблюдения. Сдачи раз в 6 месяц мазка на онкоцитологию. Нередко легкая дисплазия проходит самостоятельно без лечения.
Симптомы и профилактика болезней шейки матки
Каковы симптомы дискариоза? К сожалению, их нет. Так же, как не имеет в большинстве случаев их карцинома (злокачественная опухоль), не распространяющаяся дальше шейки матки. Но она лечится, пусть и хирургическим путем. Но женщина продолжает жизнь, без рака.
Чтобы избежать рака шейки матки, женщина должна не менее 1 раза в год сдавать мазок на онкоцитологию (цитограмму). А врач или медицинская сестра при сборе материала должны соблюдать технику.
- Использовать специальную цервикальную щеточку.
- Брать мазок с зоны трансформации (зоны стыка плоского и цилиндрического эпителия), где чаще всего находят атипичные клетки.
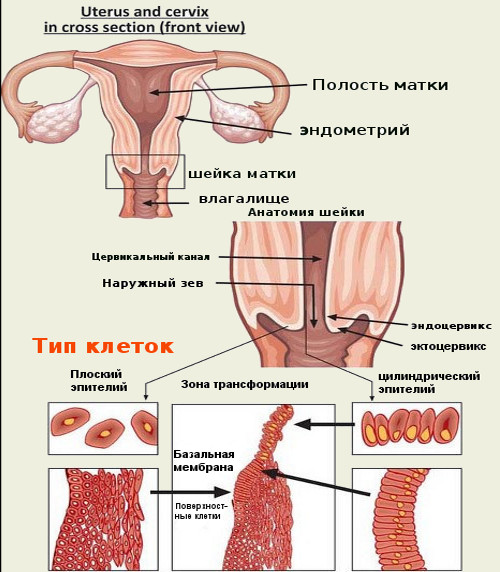
Планируйте свой визит к гинекологу именно на это время!
Также полезная информация на тему подготовки к сдаче информативного анализа смотрите на видео от гинеколога.
Визуальный осмотр шейки матки с помощью гинекологического зеркала, ее пальпация не могут дать ответ на вопрос о наличии или отсутствии атипичных клеток. Поэтому, при следующем профилактическом осмотре у гинеколога обязательно поинтересуйтесь — взял ли он у вас цитологический мазок (в некоторых клиниках уже доступна жидкостная цитология — более информативный метод исследования мазка) и когда будет готов результат.
Дисплазия шейки матки является предраковым процессом, протекающим в эпителии шейки матки. Дисплазия шейки матки развивается из-за вируса ВПЧ. При попадании в клетки многослойного плоского эпителия шейки матки, этим вирусом изменяется их строение. Кроме этого, ВПЧ может стать причиной возникновения на руках и половых органах бородавок, чем вызывается образование рака анального прохода. Дисплазия шейки матки опасна тем, что с течением времени происходит перерождение измененных клеток в раковые, вследствие чего у женщины осуществляется развитие рака шейки матки.
Дисплазия шейки матки
Дисплазия шейки матки является патологическим процессом, характеризующимся нарушением строения шеечного эпителия. Диспластический процесс может переходить в онкологический в течение не одного десятка лет. В связи с этим в случае раннего выявления и правильного лечения дисплазии возможна профилактика развития её осложнений.
В большинстве случаев дисплазиями вызывается ВПЧ "высокоскоростного риска". Рост числа дисплазий шейки матки и иных воспалительных заболеваний генитального тракта может происходить из-за:
- частой смены половых партнеров;
- наличия хронических инфекционно-воспалительных заболеваний органов половой системы;
- возникновения венерических заболеваний в анамнезе, в частности ВПЧ и генитального герпеса;
- длительного использование оральных контрацептивов (в течение более 5-ти лет);
- незащищенного секса;
- наличия вредных привычек — табакокурения, употребления спиртных напитков, токсикомании и др.
Профилактика развития дисплазии шейки матки
В качестве профилактики развития дисплазии шейки матки можно воспользоваться вакциной от ВПЧ. Такая прививка может делаться девочкам, девушкам и женщинам, возраст которых лежит в пределах от 9-ти до 46-ти лет. Кроме этого, в некоторых странах вакцинируются и представители мужского пола, поскольку они выступают в качестве переносчиков ВПЧ, передаваемого половым путем. У дисплазии шейки матки нет симптомов, по которым ее можно было бы без проблем распознать. Для выявления заболевания женщине рекомендуется раз в год не пропускать посещения врача-гинеколога и периодическое выполнение ПАП-тестов для обнаружиения дисплазии и рака шейки матки, пока они находятся на ранних стадиях.
Лечение дисплазии шейки матки
На сегодняшний день не существует лекарства, с помощью которого можно было бы избавиться от ВПЧ, соответственно, и от дисплазии шейки матки. Рекомендуется применение противовирусных препаратов в периоды обострения дисплазии. В случае обнаружения дисплазии на поздней стадии развития пораженный участок шейки матки удаляется с помощью электроконизации.
Высокую эффективность лечения дисплазия шейки матки следует ожидать в том случае, если заболевание было обнаружено на слабо выраженной и умеренно выраженной степенях. При лечении используются современные противовирусные средства.
В случае лечения тяжелой дисплазии шейки матки необходимо его сочетание с хирургическим лечением, когда удаляется атипический эпителий с помощью электрокоагуляции, радиоволновой или лазерной терапии, механического удаления участка шейки майки.
Течение заболевания
В большинстве случаев для дисплазии шейки матки характерно бессимптомное течение на протяжении длительного времени. Дисплазия начинает проявляться тогда, когда к ней присоединяются воспалительные процессы во влагалище и в шейке матки. Тогда для клинической картины характерно появление из влагалища выделений, обладающих необычным цветом и консистенцией, возникновением жжения и зуда, контактных кровотечений, развивающихся в травматизации шейки матки посредством использования гигиенических тампонов или полового акта. Крайне редко могут наблюдаться болезненные ощущения и чувство дискомфорта в области малого таза.
В зависимости от того, какова степень повреждения эпителия, выделяется 3 степени тяжести дисплазий:
- слабо выраженную дисплазию — изменениями затрагивается нижняя треть эпителия;
- умеренно выраженную дисплазию — изменениями затрагивается более 1/3, но менее 2/3 эпителия;
- тяжелую дисплазию — изменениями затрагиваются все слои эпителия, но при этом они не задевают базальную мембрану.
Диагностика дисплазии шейки матки
При диагностике дисплазии шейки матки не возникает затруднений. В обследование входят инструментальные, клинические и лабораторные методики, при которых:
- осуществляется осмотр шейки в зеркалах;
- выполняется кольпоскопия;
- проводится цитологическое исследование мазка;
- выполняется ПЦПР;
- осуществляется гистологическое исследование.
ДИСПЛАЗИЯ ШЕЙКИ МАТКИ – ЭТО ПРЕДРАКОВЫЙ ПРОЦЕСС, ХАРАКТЕРИЗУЮЩИЙСЯ НАРУШЕНИЕМ СОЗРЕВАНИЯ МНОГОСЛОЙНОГО ПЛОСКОГО ЭПИТЕЛИЯ В РЕЗУЛЬТАТЕ ДЛИТЕЛЬНОЙ ПЕРСИСТЕНЦИИ ВИРУСА ПАПИЛЛОМЫ ЧЕЛОВЕКА.
Синонимы: цервикальная интраэпителиальная неоплазия (CIN), плоскоклеточное интраэпителиальное поражение (SIL).
Если коротко, дисплазия шейки матки — это заболевание, которое в будущем может привести к раку. Вероятность этого тем выше, чем выше степень дисплазии. К дисплазии 1 степени (CIN 1, LSIL) относят любые изменения эпителия, порой даже минимальные и субъективные. Это позволяет взять женщину под контроль и не допустить прогрессирования процесса. На практике, для диагностики дисплазии 1 степени достаточно поражение эпителиальных клеток вирусом папилломы человека. Опасаться этого не стоит! Легкая степень дисплазии самостоятельно проходит у 70% женщин в течение нескольких лет. За это время собственная иммунная система уничтожает вирус и заболевание регрессирует. Обычно дисплазия 1 степени требует только наблюдения, в части случаев может назначаться прижигание. Дисплазия 2 и 3 степени (CIN 2-3, HSIL) — это уже предопухолевый процесс с высоким риском, поэтому требует серьезного лечения. В таких случаях показана широкая эксцизия или конизация шейки матки. Диагностировать дисплазию эпителия можно с помощью мазка на цитологию или биопсии. В принятии решения и тактике лечения важную роль играет тест на ВПЧ.
Подробнее читайте ниже, а также посмотрите комментарии, там Вы найдете ответы на свои вопросы.
Основной причиной развития дисплазии шейки матки является вирус папилломы человека, а именно его онкогенные штаммы — 14 серотипов, среди которых наиболее важными являются 16 и 18. Зрелый многослойный плоский эпителий, покрывая наружную часть шейки, создает непреодолимую преграду для вируса. Единственным же уязвимым местом является граница с железистым эпителием у наружного зева, называемая зоной трансформации . При эрозии (эктопии) шейки матки зона трансформации смещается на наружную часть шейки матки, что создает предпосылки для инфицирования.
Более 80% случаев дисплазии и рака шейки матки развивается именно в зоне трансформации.
Большинство женщин переносит ВПЧ-инфекцию без каких либо изменений со стороны организма. В течение нескольких лет иммунная система самостоятельно избавляется от вируса. Однако 10% женщин не могут уничтожить вирус, который в свою очередь встраивается в ДНК эпителиальных клеток и модифицирует их, приводя к опухолевой трансформации. Это может быть связано как с индивидуальной предрасположенностью, так и с иммунодефицитом или длительными стрессами. Также известно, что курение способствует снижению специфического иммунитета против ВПЧ.
Дисплазия шейки матки — это качественное изменение клеток плоского эпителия, которое указывает на возможное начало опухолевой трансформации.
Различают несколько степеней дисплазии шейки матки по тяжести, что обычно выражается в числовых значениях от 1 до 3. Каждая степень отражает прогноз патологического процесса и позволяет выбрать соответствующий алгоритм лечения. Так, дисплазия 1 степени имеет низкий потенциал к малигнизации и в большинстве случаев самостоятельно регрессирует в течение нескольких лет без какого-либо вмешательства. В противоположность, дисплазия 3 степени в течение одного года обязательно трансформируется в рак и требует уже специализированного хирургического лечения.

Прогрессирование дисплазии шейки матки
В международной практике термин “дисплазия шейки матки” имеет различные синонимы. Наиболее широко распространена аббревиатура CIN – цервикальная интраэпителиальная неоплазия, что означает развитие неоплазии (новообразования) в пределах эпителиального пласта. В отличие от рака, CIN не обладает способностью к инвазивному росту и метастазированию. На этом этапе можно предотвратить развитие злокачественной опухоли.
1) LSIL (low grade squamous intraepithelial lesion) — плоскоклеточное интраэпителиальное поражение легкой степени. LSIL соответствует CIN 1 или дисплазии 1 степени.
| Pap class System 1954 | Классификация ВОЗ 1956 | Классификация Bethesda 1988 |
| Class | Дисплазия/CIN (ЦИН — цервикальная интраэпителиальная неоплазия) | SIL (плоскоклеточное интраэпителиальное поражение) |
| Class 3 | Дисплазия 1 степени/CIN 1 | LSIL — плоскоклеточное интраэпителиальное поражение легкой степени |
| Class 4 | Дисплазия 2 степени/CIN 2 | HSIL — плоскоклеточное интраэпителиальное поражение тяжелой степени |
| Дисплазия 3 степени/CIN 3 | ||
| Рак in situ (рак в пределах эпителиального пласта, без инвазивного роста) |

Первым методом в диагностике дисплазии шейки матки чаще всего является мазок на онкоцитологию . Это скрининговый метод для обследования большого количества женщин. Является самым простым и безопасным для женщины, однако не самым точным. Чувствительность метода составляет 60-70%, и только трехкратное исследование позволяет с высокой точностью определить или опровергнуть дисплазию эпителия. Кроме этого у молодых женщин часто бывают ложно-отрицательные результаты, когда дисплазия может быть пропущена; а у пожилых женщин часты ложно-положительные результаты, когда мазок показывает наличие дисплазии, в то время как более качественные методы ее исключают.
При определении LSIL в мазке необходимо только лишь активное наблюдение. Под этим диагнозом подразумеваются клеточные изменения с низким потенциалом опухолевой трансформации. К LSIL относятся различные дегенеративные изменения клеток при раздражении, воспалении или вирусном поражении. Гинеколог, получив такое заключение может порекомендовать проведение кольпоскопии с последующей точечной биопсией.
При наличии HSIL в мазке на цитологию проведение кольпоскопии с гистологическим подтверждением становится обязательным!
Кольпоскопия — это метод осмотра наружной поверхности шейки матки с помощью специального микроскопа. Кольпоскопия является достаточно субъективным методом диагностики, сильно зависящим от опыта и умения врача. Кольпоскопические картины дисплазии шейки матки размыты и очень часто ее можно спутать с банальными физиологическими процессами, такими как плоскоклеточная метаплазия, вирусным поражением или лейкоплакией. Несмотря на это, кольпоскопия позволяет определить подозрительные места на шейке матки и взять биопсию — участок ткани для дальнейшего гистологического исследования.
К кольпоскопическим признакам дисплазии относятся: ацетобелый эпителий, йод-негативные зоны, изъеденность или нерегулярность эпителиального покрова, атипичные сосуды, мозаика, пунктация, контактная кровоточивость и др. Гинеколог должен оценить не только степень, но и скорость наступления тканевой и сосудистой реакции при обработке уксусной кислотой или йодом.
Цель кольпоскопии — это определить анатомическую локализацию зоны трансформации, что имеет решающее значение для дальнейшей тактики диагностики и лечения.
Биопсия является “золотым” стандартом диагностики дисплазии и рака шейки матки. Гистологическое исследование позволяет определить качество плоского эпителия и степень его созревания. Биопсия может быть точечной, получаемой с помощью специального инструмента — конхотома, или широкой (эксцизионной), получаемой с помощью электропетли.
Изменения при дисплазии 1 степени обычно носят характер цитопатического действия вируса папилломы человека. В эту категорию так же относят остроконечную и плоскую кондиломы. Морфологические изменения при CIN 1 (LSIL) включают: нарушение стратификации плоского эпителия преимущественно в базальных отделах, нарушение поляризации клеток относительно базальной мембраны, единичные делящиеся клетки, незначительный дискариоз, а также признаки вирусного поражения — койлоцитарную атипию в поверхностных отделах эпителия, дискератоз, пара- и гиперкератоз эпителия.

Патологическая эпидермизация желез с CIN III
Морфологические изменения при CIN 2-3 (HSIL) носят уже неопластический характер, а цитопатическое действие вируса может проявляться слабо. Нарастает клеточная атипия, которая затрагивает весь пласт плоского эпителия с минимальными признаками созревания. Клетки активно делятся, замещая нормальный эпителий цервикальных желез, в ряде случаев пролиферирующий плоский эпителий может замещать выстилку цервикального канала. Характерно обилие как нормальных, так и патологических митозов.
Тяжелая дисплазия шейки матки отличается от рака отсутствием инвазивного роста.
Тест на ВПЧ помогает в диагностике дисплазии шейки матки и выборе тактики лечения в сложных ситуациях.
ВПЧ тест рекомендуется делать женщинам после 25 лет, поскольку имеется большая вероятность, что инфекция уже длительное время персистирует в организме и могла вызвать какие-либо изменения в шейке. В более молодом возрасте при нормальном мазке на цитологию ВПЧ-тистирование не дает полезной информации.
С возрастом ВПЧ-тестирование приобретает все большую значимость. К примеру, при наличии 16 или 18 штаммов ВПЧ у 50 летней женщины можно с высокой вероятностью утверждать, что у нее уже имеется тяжелое интраэпителиальное поражение эпителия. Мазок на цитологию менее эффективен в данном случае. Женщине тот час может рекомендоваться диагностическая биопсия и выскабливание цервикального канала.
Тактика лечения и ведения пациенток с дисплазией зависит от гистологического заключения, кольпоскопической картины, типа зоны трансформации, возраста и планирования беременности. Основными методами являются абляция (прижигание), или эксцизия (удаление тканей). Эти методы могут проводиться с помощью различных инструментов, использующих низкие или высокие температуры, электро-, лазеро- или радиоволновую энергию.
По западным протоколам LSIL необходимо динамически наблюдать. Так как LSIL обладает низким злокачественным потенциалом и часто регрессирует самостоятельно, женщине рекомендуется проходить цитологическое исследование не менее 2 раз в год. В отечественной медицине часто рекомендуют абляцию (прижигание), хотя это не всегда оправдано. С прижиганием связывают некоторое повышение риска невынашивания беременности. Однако, часть авторов, опровергает это.
Наиболее оптимальным является радиоволновая абляция Сургитроном. Патологический эпителий и подлежащая строма выпариваются радиоволнами, после чего пораженная зона эпителизируется заново. Минусом абляции является отсутствие материала для последующего гистологического исследования, плюсом — сохранение анатомического строения шейки матки и небольшое количество осложнений.
HSIL обладает высоким злокачественным потенциалом, поэтому в данном случае показано удаление патологически изменненых тканей. Обычно, рекомендуется широкая эксцизионная биопсия или конизация шейки матки — это конусообразное удаление тканей, включающая наружную часть шейки матки и ткани вокруг цервикального канала. Весь удаленный материал отправляется на гистологическое исследование для подтверждения и уточнения диагноза. В удаленном материале гистолог оценивает края резекции, так как важно, чтобы патологический эпителий был удален в пределах здоровых тканей. При наличии в краях резекции патологии, или глубоком поражении цервикального канала, а также наличии инвазивного роста может быть принято решение об ампутации шейки матки.
Изредка, если женщина молода и планирует беременность, допускается лечение HSIL абляцией. Это возможно только лишь в случае 1 или 2 типа зоны трансформации при кольпоскопии, когда гинеколог видит глазом все измененные ткани и может обеспечить полную их абляцию. Если зона трансформации смещена глубоко в цервикальный канал — показана только глубокая конизация или ампутация шейки матки.
Читайте также:


