Сепсис инфекционный эндокардит пархоменко
• Септический (бактериальный) эндокардит — особая форма сепсиса, для которой характерно наличие септического очага на клапанах сердца и гиперергии, поэтому ее рассматривают как бактериальную септицемию.
Этиология и патогенез.Наиболее частые возбудители — белый и золотистый стафилококк, зеленящий стрептококк (его L-формы и мутанты), энтерококки. В последние годы возросла этиологическая роль грамотрицательных бактерий — кишечной и синегнойной палочек, протея, клебсиеллы, а также патогенных грибов. В ответ на антигены всех перечисленных возбудителей образуются антитела, и в кровь больных поступают циркулирующие токсические иммунные комплексы. В связи с воздействием циркулирующих токсических иммунных комплексов развиваются реакции гиперчувствительности, которые и составляют сущность гиперергии при бактериальном эндокардите.
Классификация.Септический (бактериальный) эндокардит разделяют по характеру течения и по наличию (или отсутствию) фонового заболевания.
По характеру течения выделяют острый, подострый и затяжной (хронический) бактериальный эндокардит. Острый эндокардит в настоящее время практически не встречается, продолжительность его около 2 нед. Продолжительность подострого — около 3 мес и затяжного (хронического) — несколько месяцев, а иногда и несколько лет.
В зависимости от наличия или отсутствия фонового заболевания различают 2 вида септического эндокардита:
1) первичный септический эндокардит, или болезнь Черногубова. Эта форма сепсиса характеризуется тем, что развивается на
неизмененных клапанах. Она составляет 20—30 % случаев септического эндокардита и в последние годы эта цифра увеличивается;
2) вторичный септический (бактериальный) эндокардит. Эта форма сепсиса встречается гораздо чаще (70—80 % всех случаев септического эндокардита) и характеризуется тем, что развивается на фоне порока сердца чаще всего при ревматизме, реже при атеросклерозе, сифилисе и еще реже — на фоне врожденного порока сердца. Особое место занимает эндокардит, который развивается на протезированных клапанах.
Патологическая анатомия.Складывается из местных и общих изменений.
Местные изменения— это изменения в септическом очаге, т.е. на клапанах. Обычно поражены клапаны аорты, реже — левый предсердно-желудочковый (митральный) клапан или оба эти клапана вместе. Процесс на неизмененных и на склерозированных клапанах носит название полипозно-язвенного эндокардита. На клапанах появляются обширные изъязвления, иногда часть створки клапана отрывается или же возникают отверстия в створках (фенестры) в связи с перфорацией их; на язвах появляются крупные в виде полипов тромботические наложения, которые легко крошатся и пропитываются известью. В ряде случаев тромботические наложения располагаются не только на клапанах, но и на пристеночном эндокарде, а при поражении аортальных клапанов — распространяются на внутреннюю оболочку аорты.
При микроскопическом исследовании в створках клапанов выявляются обширные очаги некроза, вокруг которых наблюдается лимфогистиоцитарная инфильтрация, при этом среди клеток инфильтрата видны колонии бактерий. В участках некроза выявляются массивные старые организованные тромбы, иногда с отложениями кальция.
Описанные морфологические изменения характерны для первичного септического эндокардита. При вторичном септическом эндокардите отличие заключается лишь в том, что макро- и микроскопически выявляется, в дополнение к описанному, яркая морфология порока — склероз, гиалиноз, обызвествление и выраженная деформация створок клапана.
Общие измененияхарактеризуются поражением внутренних органов. Селезенка при септическом эндокардите увеличена, с резко напряженной капсулой. Пульпа ее малинового цвета, дает обильный соскоб. Гистологически выявляется выраженная гиперплазия лимфоидной ткани и полнокровие красной пульпы — септическая селезенка. Часто в ней обнаруживают инфаркты разной давности.
В связи с циркуляцией иммунных комплексов отмечается генерализованное поражение сосудов, в них развивается алътеративно-продуктивный заскулит, при этом воспалительные изменения отмечают прежде всего в сосудах микроциркуляторного русла в виде эндо- или периваскулита. В результате диффузного поражения возможно развитие аневризм в сосудах мелкого и среднего калибра, разрыв которых в жизненно важных органах (например, в головном мозге) может оказаться смертельным. В стенках сосудов нередко развивается фибриноидный некроз, что приводит к резкому повышению сосудистой проницаемости, развивается плазморрагия и появляются многочисленные диапедезные кровоизлияния. Множественные петехиальные кровоизлияния появляются на коже, слизистых и серозных оболочках, в конъюнктиве глаза развивается геморрагический синдром.
В почках при септическом эндокардите развивается иммунокомплексный диффузный гломерулонефрит, а также нередко возникают инфаркты и рубцы после них.
В связи с наличием массивных тромботических наложений на клапанах при септическом эндокардите неизбежно развиваются тромбоэмболические осложнения, а так как источником тромбоэмболии являются аортальный и/или митральный клапаны, то развиваются многочисленные инфаркты в органах большого круга кровообращения — в почках, селезенке, головном мозге, т.е. речь идет о тромбоэмболическом синдроме.
Циркулирующие иммунные комплексы нередко оседают на синовиальных оболочках, поэтому при септическом эндокардите развиваются артриты.
Очень характерны периферические признаки септического эндокардита. Среди них выделяют:
1) пятна Лукина—Либмана — петехиальные кровоизлияния в конъюнктиве глаз нижнего века у внутреннего угла;
2) узелки Ослера — узелковые утолщения на ладонных поверхностях кистей;
3) пальцы в виде барабанных палочек;
4) очаги некроза в подкожной клетчатке;
5) пятна Джейнуэя — кровоизлияния в кожу и подкожную клетчатку.
Патоморфоз. За последние десятилетия значительно изменились и клиническая, и морфологическая картины септического эндокардита. В частности, на фоне массивной антибактериальной терапии клиницисты успешно ликвидируют септический очаг на клапанах сердца, в связи с чем резко снизилась летальность. Практически исчезли острые формы течения бактериального эндокардита. Однако массивная противовоспалительная терапия усиливает и ускоряет развитие и созревание вегетации на створках и в створках клапанов. Это приводит к значительному склерозу и деформации створок клапанов. В результате у людей с первичным септическим эндокардитом после "успешного" лечения сепсиса происходит формирование порока сердца, а у лиц с уже имеющимся пороком последний после излечения сепсиса становится значительно тяжелее, более выраженным — усиливаются склероз, гиалиноз и резкая деформация клапанов. Все это в очень короткие сроки приводит к инвалидизации больных.
Патоморфоз бактериального эндокардита коснулся не только морфологии — изменилась этиология (раньше был только зеленящий стрептококк), клинические проявления и исходы заболевания.
Не нашли то, что искали? Воспользуйтесь поиском:
Инфекционный (бактериальный, септический) эндокардит – воспаление эндокарда – это бактериальное поражение сердечных клапанов или эндокарда, вызванное проникновением бактерий. Заболевание может развиваться под влиянием врожденных или приобретенных пороках сердца, а так же инфицировании артериально-венозной фистулы.
Заболевание может протекать по разному: остро развиваться, иметь скрытую форму или переходить в затяжной процесс. Если во время не начать лечение септический эндокардит приводит к летальному исходу. Инфекция может иметь острую или подострую форму, в зависимости от степени патогенности бактерий.
На современном этапе до 80% случаев инфекционного эндокардита успешно излечиваются, но в 20% возникают осложнения в виде сердечной недостаточности, которая, если не принять соответствующих мер, приводит к летальному исходу.
Уровень заболеваемости постоянно увеличивается в мире. Часто болеют люди с протезированными клапанами сердца, искусственными водителями ритма, така как на инородном теле легче развивается инфекция. Также к группе риска относятся пациенты с различными повреждениями клапанов (пороки сердца, травмы, атеросклероз, ревматические) и наркоманы.
Причины заболевания и факторы риска
Кариес и эндокардит
До широкого распространения антибиотиков эндокардит чаще всего был вызван стрептококами. В наше время основными возбудителями эндокардита являются стафилококки, грибки, синегойная палочка. Наиболее тяжелое течение имеет эндокардит грибкового происхождения.
Стрептококком часто заражаются пациенты в течении 2 месяцев после протезирования сердечных клапанов и люди с врожденными и приобретенными пороками сердца. Но инфекция может поразить эндокард и полностью здорового человека – при сильном стрессе, пониженном иммунитете, ведь в крови каждого человека множество микроорганизмов, которые могут разжиться на любых органах, даже на клапанах сердца.
Существуют факторы, значительно влияющие на вероятность возникновения эндокардита:
- врожденные пороки сердца, особенно сердечных клапанов;
- протезированные (искусственные) клапаны сердца;
- ранее перенесенный эндокардит;
- трансплантваиця сердца или иискусственноговодителя ритма;
- гипертрофическая кардиомиопатия;
- инъекционное введение наркотиков;
- проведение процедуры гемодиализа;
- СПИД.
Если пациент относится к группе риска, он обязан предупреждать об этом при проведении различных медицинских, стоматологических манипуляций и других процедур, связанных с риском попадания инфекции (татуировки). В таком случае, возможно, следует применять антибиотики в качестве профилактики — делать это можно исключительно по назначению врача.
Симптомы и признаки
В целом, симптомами инфекционного поражения являются повышенная температура, озноб, слабость, анорексия, потливость, артралгия. У пожилых людей или больных почечной недостаточностью, лихорадка может отсутствовать. Заболевание характеризуется наличием шумов в сердце, анемией, гематурией, спленомегалией, петехиями кожи и слизистых оболочек, иногда эмболиями. Может развиваться острая сердечная недостаточность, аневризмы.
Чаще всего (примерно у 85% пациентов) наблюдаются лихорадка и слышны шумы в сердце.
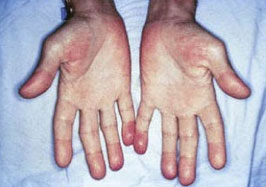
Ладони пациента страдающего инфекционным эндокардитом.
Кроме того, существуют классические признаки септического эндокардита находятся. Те или иные признаки наблюдаются в среднем у 50% пациентов:
- кровоизлияния;
- подкожные узелки рядом с кончиками пальцев;
- безболезненные пятна на ладонях и подошвах;
- болезненные уплотнения кончиков пальцев (узелки Ослера).
Следующие признаки заболевания, встречаются примерно у 40% пациентов:
- микроабсцессы,
- внутримозговое кровоизлияние.
Реже наблюдаются следующие симптомы:
- напряжение затылочных мышц,
- паралич,
- бред,
- потливость (особенно ночью),
- одышка,
- бледность кожи,
- аритмия.
Симптомы раннего подострого эндокардита, как правило, выражены слабо неспецифически — они включают в себя следующее:
- температура тела около 37,5 градусов, наблюдается у 85% пациентов;
- анорексия и потеря в весе;
- гриппоподобные ощущения в теле;
- возможна рвота после приема пиши и боль в животе.
Острая форма
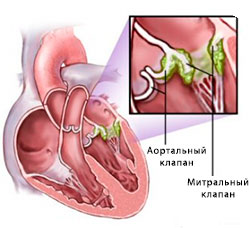
Бактериальное поражение клапанов при эндокардите
Длится до шести недель, является одним из признаков заражения крови, потому обладает схожими симптомы. Заболевание может протекать как осложнение гнойного отита, синусита, цистита, сальпингоофорита.
Симптомы и признаки
Первыми тревожными симптомами инфекционного эндокардита являются тахикардия, приглушенные сердечные тона.
Острая форма характеризуется:
- повышенной температурой,
- головной болью,
- потливостью,
- увеличенной печенью и селезенкой,
- состоянием схожим с тяжелым отравлением,
- кровоизлияниями на слизистых оболочках, коже.
В некоторых случаях могут наблюдаться инфекционные эмболии различных органов с очагами гнойных поражений. Анализ крови показывает нездоровые показатели по многим параметрам.
Подострая форма
Практически всегда инфекция проникает в слабые места сердца — инфекция возникает в местах пороков сердца. Здоровые клапаны поражаются гораздо реже. Очень важное влияние на вероятность возникновения заболевания оказывает здоровье организма в целом, а также его иммунитет.
Симптомы и признаки
Клиническая картина подострой формы эндокардита характеризуется признаками инфекционного течения, иммунных нарушений, поражения клапанов сердца.
Наиболее распространенные симптомы:
- лихорадка,
- озноб,
- сильная потливость,
- интоксикационные проявления – суставные, мышечные боли, слабость, стремительная потеря веса.
Иногда в первые недели или даже 2 месяца поражения клапанов сердца большинство симптомов может не проявляться клинически. В дальнейшем обнаруживаются симптомы аортальной либо митральной недостаточности, наблюдаются изменения имевшегося врожденного порока сердца при аускультативном обследовании. Могут появиться васкулиты, тромбоэмболические усложнения. Поводом для неотложной госпитализации могут стать инфаркты почки, легкого, селезенки, инфаркт миокарда или геморрагический инсульт.
Диагностика
Диагностика заболевания базируется на клинических данных и, при характерных симптомах не вызывает затруднений. Основными методами диагностики заболевания является анализ крови на бактериальную флору и общий анализ крови, а также эхо-кардиограмма, с помощью которой возможно обнаружить микробные колонии на сердечных клапанах.
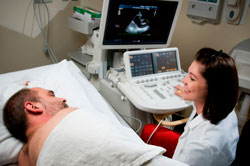
УЗИ сердца может помочь в диагностике эндокардита.
Подозревают септический эндокардит обычно в случаях лихорадки неизвестного происхождения и шумах в сердце. Хотя в некоторых случаях, при пристеночном эндокардите или поражении правых отделов сердца шумы могут отсутствовать. Классические признаки заболевания — изменение характера шумов или появление новых — обнаруживаются только в 15% случаев. Самым надежным методом диагностики является посев крови на бактериальную флору. Этот тест дает возможность выявить возбудителя в 95% случаев.
До появления антибиотиков в 90% случаев заболевания было вызвано зеленящим стрептококком, преимущественно у людей молодого возраста с ревматическими пороками сердца. В настоящее время болеют люди старшего возраста, чаще мужчины с пороками сердца. Возбудителями, кроме зеленящего стрептококка может быть золотистый стафилококк, дифтериеподобная бактерия, энтерококки, а также другие штаммы.
Заболевание диагностируется на основании наличия двух основным признаков:
- в посевах крови пациента обнаруживаются типичные для инфекционного эндокардита возбудители;
- на эхокардиографии наблюдаются признаки поражения эндокарда — подвижные произрастания на клапанах сердца, гнойные воспаления в области протеза клапана;
Кроме того, существуют второстепенные признаки:
- обнаружение в крупных артериях веществ, не находящихся там в норме (эмболия);
- инфекционные инфаркты легких;
- внутричерепные кровоизлияния;
- иммунологические феномены;
- фебрильная лихорадка и другие проявления системной инфекции.
Таким образом, диагноз инфекционный эндокардит при наличии двух главных критериев в сочетании с несколькими второстепенными.
Лечение
Во всех случаях септического эндокардита или подозрения диагноза требуется госпитализация больного. После интенсивного стационарного лечения в течении 10-14 суток, стабилизации состояния и отсутствии значительного риска осложнений (отсутствие лихорадки, отрицательный посев крови, отсутствие нарушений ритма и эмболий) лечение продолжают в амбулаторных условиях.
При лечении эндокардита используются специально подобранные антибиотики.
Лечение при инфекционном эндокардите состоит, главным образом, из интенсивной антибактериальной терапии. Также, в первую очередь, лечится основное заболевание – ревматизм, сепсис, системная красная волчанка. Антибактериальное лечение должно быть тщательно подобрано, то есть выбранный антибиотик должен соответствовать бактериальной флоре и начинаться как можно раньше. Терапия может длиться от 3-6 недель до 2 месяцев в зависимости от степени поражения и типа инфекции.
Препараты, для их постоянной концентрации в крови вводятся внутривенно. Важно осуществлять мониторинг концентрации антибиотиков в плазме, которая должна держаться на терапевтическом уровне, но не становится токсической для организма. Для этого в каждом случае определяют минимальный (перед введением четвертой дозы) и максимальный (через полчаса-час после четвертой дозы) уровни концентрации.
Обязательно проводится лабораторное исследование чувствительности бактерии-возбудителя к антибиотикам. Регулярно проводят также биохимический и общий анализ крови, оценивают бактерицидную активность сыворотки, следят за деятельностью почек.
При подостром септическом эндокардите терапию осуществляют высокими дозами натриевой соли бензилпенициллина или полусинтетическими пенициллинами (оксациллин, метициллин). Лечение антибиотиками, преимущественно парентеральное, продолжают до совершенного бактериологического и клинического выздоровления. При длительной инфекции, нарастающей сердечной недостаточности, проводят хирургическое вмешательство – иссечение поврежденных тканей, протезирование клапанов. Также применяют хирургическое вмешательство если антимикробное лечение проходит успешно, но клапаны сердца уже сильно повреждены.
Инфекционный эндокардит — опасное заболевание, которое требует своевременной профилактики. Это предупреждение сепсиса и инфекционных осложнений, особенно при врожденных и приобретенных пороках сердца.
Осложнения
При отсутствии адекватного антибактериального лечения, существует вероятность осложнений инфекционного эндокардита, часто заканчивающихся с летальным исходом. Среди них септический шок, острая сердечная недостаточность, нарушения работы и функций всего организма.
Профилактика
Для предотвращения инфекционного эндокардита следует соблюдать несложные правила гигиены:
- Следите за здоровьем ваших зубов.
- Относитесь максимально серьёзно к косметическим процедурам, которые могут занести инфекцию (татуировки, пирсинг).
- Старайтесь незамедлительно обращаться к врачу, если вы обнаружили какую-либо кожную инфекцию или имеете незаживающую рану.
Перед согласием на медицинские и стоматологический процедуры, обговорите с врачом необходимость заблаговременного принятия антибиотиков, способных предотвратить развитие случайно занесённой инфекции. Особенно это касается людей уже перенёсших эндокардит, имеющих пороки сердца, искусственные клапаны сердца. Обязательно сообщите врачу о своих заболеваниях.
Прогноз
Микробы, размножаясь, могут полностью разрушить сердечный клапан или его части, что гарантирует развитие сердечной недостаточности. Также инфекция или поврежденные участки клапанов могут с кровотоком попадать в головной мозг и вызывать инфаркт ли паралич мозга.
Для исцеления без серьезных последствий требуется ранняя госпитализация с целенаправленным лечением инфекции. Наличие у пациента заболеваний сердца также серьёзно ухудшают прогноз инфекционного эндокардита.
Существует вероятность перехода заболевания в хроническую форму с периодическими обострениями.
При правильном подборе лечения и отсутствии значительных сопутствующих патологий показатель 5-летней выживаемости составляет 70%.
Что же такое инфекционный эндокардит? Это серьезный инфекционный процесс в организме с преимущественным поражением эндокарда — внутренней оболочки сердца, которая и образует клапаны. Это системное (распространенное) заболевание, по сути — сепсис (заражение крови), при котором страдают многие внутренние органы, не только сердце.
Причины инфекционного эндокардита
Как и при любой инфекции, для возникновения инфекционного эндокардита необходимо наличие двух факторов:
- Возбудитель. Наиболее часто причиной инфекционного эндокардита являются стафилококк, энтерококк, зеленящий стрептококк. Реже встречаются кишечная, синегнойная палочки, протей, микоплазмы, хламидии, грибы (кандиды, аспергиллы) и пр.
- Нарушение (ослабление) иммунитета, которое может быть вызвано каким-либо предшествующим хроническим заболеванием, неблагоприятной экологией, алкоголизмом и т.д.
Для того чтобы вызвать эндокардит, патогенные микроорганизмы должны попасть в системный кровоток. Кровь в норме у человека стерильна, т.е. в ней нет никаких микробов. На их пути стоит множество заслонов.
Факторы риска развития инфекционного эндокардита
- Все стоматологические процедуры, особенно удаление кариозных зубов. Почему? Во рту полно микробов. И рот невозможно стерилизовать при всем желании. При удалении зуба повреждаются сосуды, через эти повреждения могут проникнуть свои же микробы.
- Удаление миндалин (тонзилэктомия).
- Операции на пищеводе, кишечнике.
- Урологические манипуляции и операции, особенно при мочекаменной болезни и сопутствующем пиелонефрите, необходимость установки мочевого катетера на длительный срок и пр.
- Гинекологические вмешательства, особенно аборты.
- Длительная катетеризация вены.
- Искусственная вентиляция легких (ИВЛ), интубация (установка дыхательной трубки в трахею).
Также выделяют еще один мощный фактор риска эндокардита — наличие предшествующего заболевания сердца, крупных сосудов (например, аневризма аорты) или порока сердца ревматического, атеросклеротического происхождения. На таких измененных, уже затронутых болезнью клапанах и эндокарде, легко гнездится инфекция. Возникает так называемый вторичный инфекционный эндокардит. Поражает он и искусственные клапаны.
Как формируется порок сердца?
Симптомы инфекционного эндокардита
Один из главных и первых симптомов — это длительное повышение температуры как бы без видимой причины. Лихорадка может быть постоянной и высокой, а может — волнообразной с периодическими подъемами в течение суток. Температура не снижается при применении жаропонижающих и обычных коротких курсов антибиотиков, сопровождается сильными ознобами и потливостью. В некоторых случаях лихорадка небольшая, либо отсутствует совсем.
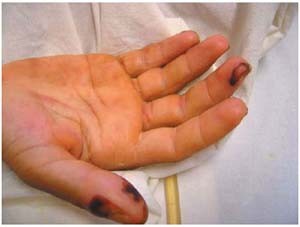
Геморрагии на правой руке. Возникает сильная слабость, боли в мышцах, снижение аппетита и похудание, бледность из-за интоксикации. Часто на коже появляются точечные высыпания буроватого цвета — геморрагии. Усиливаются или впервые появляются признаки сердечной недостаточности: сердцебиение и одышка при ходьбе, отеки.
У трети пациентов страдает нервная система из-за эмболии вегетациями. Это проявляется слабостью в правой или левой половине тела, нарушениями зрения, сильными головными болями.
Диагностика инфекционного эндокардита
Для подтверждения диагноза врачом-кардиологом назначаются:
Принципы лечения инфекционного эндокардита
Лечение проводят в стационаре. Основная терапия, это конечно, применение антибиотиков. Выбирают препараты широкого спектра действия в зависимости от вида возбудителя:
- Пенициллины (ампициллин, амоксициллин с клавулановой кислотой);
- Цефалоспорины III, IV поколений (цефтриаксон, цефотаксим, цефтазидим);
- Аминогликазиды (гентамицин, амикацин);
- Ванкомицин, даптомицин.
Длительность первого курса лечения индивидуальна, от 3 до 8 недель большими дозировками, внутривенно и внутримышечно. Часто используют комбинацию двух антибактериальных препаратов.
В дополнение используют жаропонижающие и антигистаминные (противоаллергические) средства, глюкокортикоиды, иммунокорректоры, препараты для лечения сердечной недостаточности. Помогают в выздоровлении плазмаферез и облучение крови ультрафиолетом, активная дезинтоксикационная терапия.
Если клапаны необратимо разрушены и сердечная недостаточность нарастает, не корригируется медикаментозно, то выполняют операцию на сердце по удалению зараженных участков и протезированию клапанов.
Прогноз
Выздоровление (с формированием порока) наблюдается приблизительно в половине процентов случаев. В 15-30% болезнь переходит в хроническую форму, с периодами обострения инфекции и ремиссии. К сожалению, несмотря на усилия врачей, часто бывает и летальный исход — в 20-30%.
Патологоанатомическая диагностика сепсиса : методические рекомендации / О.Д.Мишнёв, А.И.Щёголев, О.А.Трусов. — Москва, 2004.
библиографическое описание:
Патологоанатомическая диагностика сепсиса : методические рекомендации / Мишнёв О.Д., Щёголев А.И., Трусов О.А. — 2004.
код для вставки на форум:
Российское общество патологоанатомов
О.Д.Мишнев, А.И.Щеголев, О.А.Трусов
ПАТОЛОГОАНАТОМИЧЕСКАЯ ДИАГНОСТИКА СЕПСИСА
Сепсис – полиэтиологическое инфекционное заболевание, характеризующееся генерализованным характером, ацикличностью течения и особым образом измененной реактивностью. Сепсис развивается из местных очагов инфекции и рассматривается, как правило, в качестве осложнения заболеваний, послуживших причиной генерализации инфекции. Последние годы, несмотря на интенсивную терапию, характеризуются ростом числа больных сепсисом и высокой летальностью.
Сепсис представляет собой заболевание, в отношении этиологии, патогенеза, патологической анатомии, диагностики, лечения которого всегда были и ещё будут проводиться дискуссии. Клиницисты обращаются к патологоанатомам в надежде получить желаемое и в то же время, по их мнению, объективное и адекватное объяснение летального исхода при сепсисе. Однако, справедливости ради, следует констатировать, что, как правило, такое объяснение для них a priori, до вскрытия, в современных клиниках уже имеется, и оно может быть получено на основании комплекса клинических и лабораторных признаков доказательной медицины.
Именно эти показатели, очевидно, следует использовать и патологоанатому при анализе истории болезни и результатов вскрытия для решения своих диагностических проблем. Многие клиницисты интересуются на вскрытии, т.е. a posteriori, не столько познанием на морфологическом субстрате причины и действия, сколько прагматичным согласованием формальных параметров, определяемых при сличении клинического и патологоанатомического диагнозов. Это определяет первоочередную задачу совместной междисциплинарной работы – нахождения общих точек соприкосновения клиницистов и патологоанатомов для полноценного и современного анализа результатов патологоанатомического исследования умерших от сепсиса.
Теоретические аспекты проблемы сепсиса, представленные в мировой литературе конца ХХ – начала нынешнего века и воспринимаемые как революционные и во многом совершенные, дающие основания для разработки оптимальных методов лечения и недопущения летальных исходов при сепсисе, не были неожиданными для патологоанатомов России. В этом заслуга наших Учителей и в первую очередь И.В. Давыдовского, а также А.В.Смольянникова, Д.С.Саркисова, А.П.Авцына, Н.К.Пермякова и других, которые первоочередное внимание уделяли макробиологической составляющей сепсиса, не забывая при этом об этиопатогенетической роли возбудителей инфекции.
Принятие и выполнение решений Согласительной конференции пульмонологов и специалистов по интенсивной терапии (ACCP/SCCV), состоявшейся в 1991 году в Чикаго, привело к унификации терминологии и к упрощению клинической диагностики сепсиса. Однако отсутствие рандомизированных патологоанатомических исследований и, соответственно, клинико-морфологических сопоставлений является одной из важных причин неполного взаимопонимания клиницистов и патологоанатомов при оценке формы и танатогенеза заболевания, а также при обсуждении расхождений клинического и патологоанатомического диагнозов. К сожалению, до настоящего времени предметом дискуссий является отнесение тех или иных клинических и морфологических признаков к проявлениям сепсиса.
Также следует остановиться на распространённой ныне тенденции считать условным выделение разновидностей сепсиса по входным воротам, поскольку генерализованная реакция организма на инфекцию по своей сути является единой и требует незамедлительного лечения, а в Международной классификации болезней отсутствует подразделение сепсиса на разновидности по данному основанию. Возможно, что такой прагматичный подход является обоснованным, однако мы рекомендуем патологоанатомам не забывать о морфологических особенностях различных форм сепсиса в зависимости от входных ворот.
Действительно, для патологоанатома и клинициста не будет представлять большой сложности достижение взаимопонимания при анализе результатов секции больного, погибшего от сепсиса при наличии типичных морфологических признаков и соответствующих клинических данных. Гораздо большие трудности возникнут в том случае, когда больного лечили от сепсиса (и по результатам вскрытия довольно успешно – именно так!), а смерть наступила от другой причины, видимо не связанной с сепсисом. В этом случае необходимо учитывать не только медицинские составляющие (организационные, научно–практические), но также социальные и экономические вопросы, которые в настоящее время никогда не следует упускать из вида. Также сложными для патологоанатомической диагностики являются наблюдения лечённого сепсиса в плане танатогенеза и установления непосредственной причины смерти. Наконец, наблюдения посмертно диагностированного сепсиса, который не был выявлен в клинике, должны стать предметом обсуждения на клинико–патологоанатомических конференциях.
Сепсис (в переводе с греческого sēpsis – гниение) – представляет собой особую форму тяжелой генерализованной инфекции, при которой макроорганизм не способен локализовать инфекционный процесс (Белянин В.Л., Рыбакова М.Г., 2004).
Бактериемия – симптом, обозначающий наличие в крови живых микроорганизмов (не обязательно только при сепсисе).
Входные ворота инфекции – место внедрения инфекции в организм.
Диссеминация – употребляется, как правило, для характеристики распространения поражений при инфекционном процессе в пределах одного органа (например, диссеминированный туберкулез легких).
Генерализация – обозначает, как правило, поражение многих органов и систем (например, генерализованная вирусная, туберкулезная инфекция).
Синдром системного воспалительного ответа (ССВО) (Systemic Inflammatory Response Syndrome (SIRS), синдром системной воспалительной реакции (ССВР)) патологическое состояние, обусловленное одной из форм хирургической инфекции или альтерации ткани неинфекционной природы (травма, панкреатит, ожог, ишемия или аутоиммунные повреждения тканей и др.). Это понятие предложено классификацией ACCP/SCCV, что привело к существенному пересмотру концептуальных положений о патогенезе, клинике, лечении, профилактике возникновения сепсиса и его осложнений. ССВР (SIRS) характеризуется наличием более чем одного из четырёх следующих основных клинических признаков: гипертермия, тахикардия, тахипноэ, лейкоцитоз (или лейкопения). Подобные клинические признаки встречаются при сепсисе, но при этом обязательным является наличие инфекционного очага поражения в тканях или органах. Патологоанатомическая характеристика SIRS является объектом перспективных научных исследований.
Септицемия – клинико–патологоанатомическая форма сепсиса, при которой отсутствуют метастатические септические очаги. Септицемия – это сепсис без гнойных метастазов. По поводу правомочности применения этого понятия в качестве диагноза одной из форм сепсиса до сих пор продолжается дискуссия. Некоторые клиницисты и патологоанатомы советуют вообще отказаться от этого термина (Пермяков Н.К., 1992). Этот термин не представлен и в классификации ACCP/SCCV. Тем не менее, он рекомендован МКБ-10 как унифицированный для всех разновидностей сепсиса, и вплоть до нового пересмотра он должен применяться клиницистами и патологоанатомами при определении шифра большинства клинико–патологоанатомических форм сепсиса.
Септикопиемия – клинико–патологоанатомическая форма сепсиса. Для неё характерно наличие гнойного воспаления (абсцессов, апостем, флегмон, интерстициального гнойного воспаления) в различных органах и тканях, возникающего в результате гематогенного распространения микробных эмболов из септического очага. Септикопиемия – это сепсис с гнойными метастазами.
Термин септикопиемия не представлен в МКБ–10.
Термин сепсис носит обобщающий характер, как и термин септический процесс. Классификация ACCP/SCCV рекомендует в клинике использовать термин сепсис, а не септицемия или септикопиемия. В настоящее время не рекомендуется использовать термин септическое состояние, лишенный конкретной основы.
Тяжёлый сепсис (или сепсис-синдром) – форма сепсиса, предложенная в классификации ACCP/SCCV, при котором отмечаются признаки полиорганной недостаточности. В.Л.Белянин и М.Г.Рыбакова (2004) считают, что с точки зрения патоморфолога понятие тяжёлый сепсис (сепсис–синдром) нельзя признать удачной терминологической находкой.
Септический шок – другая форма тяжёлого сепсиса в классификации ACCP/SCCV, сопровождающаяся артериальной гипотонией, не устраняющейся с помощью инфузионной терапии и требующей назначения катехоламинов.
Септический (бактериальный, инфекционный) эндокардит (острый и подострый) характеризуется, прежде всего, воспалительными поражениями клапанного аппарата сердца, развивающимися наряду с септическими проявлениями. Представляет собой самостоятельное заболевание (первоначальную причину смерти) и имеет собственный шифр. Следует отличать от поражений эндокарда при других формах сепсиса.
Септический очаг – различают первичный и метастатические септические очаги. Первичный септический очаг представляет собой фокус воспаления, преимущественно гнойного, в котором происходит накопление микроорганизмов, распространяющихся затем гематогенно и лимфогенно по тканям и органам. Метастатические септические очаги (вторичные септические очаги, метастатические очаги при сепсисе, септические метастазы, метастатические гнойники, гнойные метастазы) представляют собой очаги воспаления, возникающие вследствие гематогенного перемещения септического процесса в ткани и органы из другого очага.
Системный инфекционный процесс – поражение какой-либо системы органов (например: нервной при клещевом энцефалите; пищеварительной при шигеллезе и т.д.).
Гнойно-резорбтивная лихорадка. Понятие гнойно-резорбтивной лихорадки предложено И.В.Давыдовским для обозначения клинических и патологоанатомических проявлений местного гнойно-некротического процесса, морфологически ограниченного демаркационным валом (в отличие от септических очагов) от окружающих тканей. В настоящее время этот термин почти не используется, а состояние больного обозначается как интоксикация или разновидность эндотоксикоза.
Эндотоксикоз – очень широкое понятие для обозначения осложнений и проявлений заболеваний и состояний организма. Основным фактором патогенеза эндотоксикоза является воздействие на организм токсических продуктов, образующихся в нем в результате нарушения тех или иных функций.
Возбудителями сепсиса могут являться многие микроорганизмы (табл. 1). Это многочисленные бактерии: стрептококки, стафилококки, менингококки, пневмококки, кишечная палочка, синегнойная палочка, клебсиеллы, протей, сальмонеллы, а также грибы преимущественно Кандида и аспергиллус. Сепсисом может осложниться течение туберкулеза, сыпного тифа, брюшного тифа и других инфекционных заболеваний, возбудителями которых являются патогенные микроорганизмы. Генерализованные вирусные инфекции не принято рассматривать в качестве сепсиса, хотя об этом имеются указания в современных зарубежных клинических исследованиях.
Таблица. 1. Наиболее вероятная этиология сепсиса в зависимости от локализации первичного очага инфекции
Локализация первичного очага
Streptococcus spp., Staphylococcus spp., анаэробы
Читайте также:


