Трансплантация хрящей сустава россия
Суставной хрящ любого сустава, в том числе и коленного, обладает крайне низким потенциалом самовосстановления. Глубокие дефекты хряща с высокой вероятностью приводят к остеоартриту. Частота таких дефектов составляет около 5% в общей структуре повреждений коленного сустава.
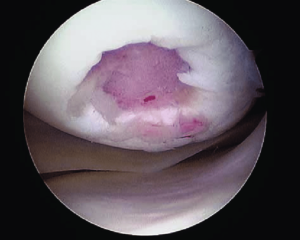
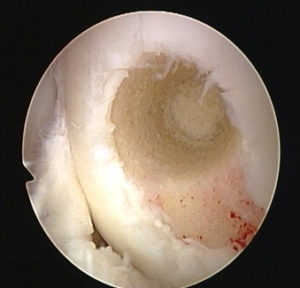
Локальное травматическое повреждение коленного сустава, вид через артроскоп.
Лечение локальных хондральных дефектов до сих пор остается сложной и противоречивой проблемой ортопедии. Многолетние усилия врачей и исследователей направлены на поиск оптимального решения, которое позволило бы восстанавливать “изношенный” гиалиновый хрящ в области максимальной нагрузки.
В начале 60-х годов была предложена технология сверления субхондральных отверстий, с целью стимуляции роста стволовых клеток, которые, как казалось, должны были обеспечить регенерацию хряща. Эта техника получила достаточно широкое распространение в 90-х годах и получила название “микрофрактурирование”. Она нашла свое применение у достаточно ограниченной группы пациентов — у молодых людей с небольшим и “свежим” повреждением хряща.
В 1983 году М. Бриттберг, Л. Петерсон начали применять аутологичные культивируемые хондроциты для лечения повреждений хряща. Суть этого метода состоит в получении и культивации хондроцитов пациента, и дальнейшую их трансплантацию на периостальном лоскуте. Результаты этой технологии вполне удовлетворительны, но сам метод технически достаточно сложный. В настоящее время чаще используется матричная имплантация аутологичных хондроцитов артроскопическим методом.
В 90-х годах прошлого века также были предложены и активно использовались разнообразные техники остеохондральных транспалантаций. Под этим термином подразумевается пересадка костно-хрящевых фрагментов из одной области сустава в другую, где имеется участок разрушенного хряща.
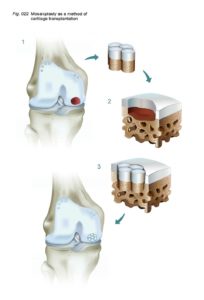
Схематичное изображение мозаичной пластики.
Исторические аспекты мозаичной пластики коленного сустава
Сначала были разработаны процедуры трансплантации крупных остеохондральных трансплантатов, полученных из надколенника, медиальной и латеральной поверхностей мыщелков, межмыщелковой борозды. Эти методы были слишком инвазивны и не позволяли получить достаточно конгруэнтные трансплантаты, и к тому же часто приводили к нарушению биомеханики сустава.
Поэтому было предложено использовать нескольких цилиндрических остеохондральных трансплантатов. Успешная операция с использованием этой техники была продемонстрирована Matsusue et al. в 1993 году. В ходе операции был успешно закрыт дефект бедренного мыщелка размером в 15 мм, обусловленный разрывом передней крестообразной связки. Эта методика получила название мозаичная пластика хряща (“Mosaicplasy”).
Мозаичная пластика — вопросы по биомеханике и гистологии
Есть несколько вопросов к мозаичной пластике коленного сустава:
Каков минимальный размер дефекта хряща, который можно закрывать мозаичной пластикой?
Исследования на трупах показывает, что максимальное давление на периферии дефекта отмечается при его размере более 10 мм. Поэтому это пороговое значение и используется для определения показаний к операции.
Снижает ли нагрузку на хрящ мозаичная пластика?
Было установлено, что деструкция хряща на площади в 16 мм (около 2 см2) приводит к росту периферического напряжения на 92%, что еще больше усиливает разрушение хряща и способствует усилению болевого синдрома. При трансплантации трех 8-мм трансплантатов периферическое напряжение увеличивается только на 35%
Откуда лучше всего брать трансплантаты?
Оптимальным местом забора являются участки с наименьшей нагрузкой, достаточной толщиной и кривизной поверхности аналогичной участку-получателю.
Исследования показали, что наименьшую нагрузку в коленном суставе испытывают боковая и латеральная поверхности мыщелков бедренной кости. Именно из этих участков и забирают трансплантаты.
Имеет ли значение кривизна трансплантатов?
Восстановление кривизны сустава, максимально приближенной к исходной, очень важно для равномерного распределения нагрузки. Поэтому очень важно подбирать кривизну трансплантатов.
Важна ли толщина хряща на донорском фрагменте?
Толщина хряща напрямую зависит от нагрузки и варьируется в разных отделах сустава. Естественно, что в донорских участках хрящ несколько тоньше(в среднем 1,8 мм), а в участках, требующих восстановления, толще — до 2,5 мм. Однако больших проблем эта разница не доставляет.
Артроскопия или артротомия — что лучше при заборе трансплантата?
В исследовании Keeling et al. было показано, что трансплантаты, полученные с помощью артроскопии, имели несоответствие размером до 1 мм в 69% случаев, а с помощью артротомии — в 57%. Было отмечено, что артроскопия более сложна при заборе трансплантата с боковой поверхности мыщелков, к тому же она повышает риск краевых переломов.
От чего зависит стабильность трансплантата?
В исследованиях на животных были установлены следующие факты:
- трансплантаты диаметром 11 мм и длиной 15 и 20 мм обладают лучшей вертикальной стабильностью;
- идеальная подгонка длины трансплантата к глубине “посадочного гнезда” обеспечивает повышение стабильности в 2-3 раза;
- трансплантаты с фиксацией press-fit более стабильны (этот эффект достигается за счет того, что сам пересаживаемый костнохрящевой фрагмент чуть шире отверстия для имплантации).
Что будет, если кривизна трансплантата не соответствует кривизне восстанавливаемого участка?
В исследовании на овцах было показано, что несоответствие кривизны до 1 мм допустимо — хрящ сохраняется; если же несоответствие достигает 2 мм и более, то происходит асептический некроз трансплантата и он постепенно рассасывается.
Зависит ли жизнеспособность хряща трансплантата от усилия при его фиксации?
При силе надавливания при фиксации до 10 МПа хондроциты не страдают, если же надавливать с усилием выше 15 МПа происходит повреждение хряща. Поэтому рекомендуется вводить трансплантат несколькими несильными надавливаниями, чем одни интенсивным.
Каковы результаты мозаичной пластики?
Исследователям удалось подвергнуть гистологическому изучению хрящевые структуры мыщелка через 3 года после мозаичной пластики. Были отмечены следующие факты:
- костная интеграция была отличной;
- поверхностный гиалиновый хрящ оставался жизнеспособным;
- конгруэнтность поверхности была сохранена, но между трансплантатом и смежным хрящом участка-реципиента сохранялась небольшая трещина.
Что происходит с донорским участком?
Контрольная артроскопия показала, что донорский участок остается пустым, лишь через достаточно продолжительное время происходит его незначительное опускание и образование фиброзной ткани в глубине.
Проводились эксперименты по заполнению дефекта остеопериостальной пробкой из большеберцовой кости, но это все равно не обеспечивает заполнения кости.
Кратко резюмируя все вышесказанное, можно сделать следующие выводы:
- остеохондральные трансплантаты с боковых и медиальных поверхностей мыщелков, а также из области межмыщелковой борозды позволяют успешно исправлять хрящевые дефекты;
- диаметр трансплантата должен быть чуть больше посадочного отверстия;
- длина трансплантата должна быть равна глубине отверстия;
- предпочтительна посадка методом press-fit;
- остеохондральный имплантат долгое время остается жизнеспособным и обеспечивает нормальное функционирование сустава.
Видео процедуры
Преимущества и недостатки применения остеохондральных трансплантатов
Краткий перечень преимуществ:
- остеохондральный трансплантат, используемый для мозаичной хондропластики, это вполне жизнеспособная функциональная единица, позволяющая восстанавливать разрушенный гиалиновый хрящ;
- размер трансплантата достаточно легко подгоняется под размер посадочного участка;
- процедура носит одностадийный характер — не требуется промежуточных этапов в виде выращивания клеток в лаборатории;
- низкий риск осложнений.
- сложность в выборе участков с необходимой кривизной для обеспечения лучшей конгруэнтности;
- при взятии большого числа донорских трансплантатов высок риск послеоперационной боли в суставе.
Кому показана мозаичная хондропластика коленного сустава
Этот вид операций предпочтительно выполнять у пациентов с очаговым разрушением суставного хряща в местах наибольшей нагрузки. Происходит это обычно в результате прямого травмирующего воздействия и при остеохондрите. Предположить локальное повреждение можно клинически — на основании боли, усиливающейся в определенном положении сустава.
Пациенту обязательно проводится рентгенография колена. Желательно проведение КТ и МРТ коленного сустава. При этом Кт обладает большей специфичностью и позволяет выявлять поверхностные хрящевые дефекты, МРТ же больше подходит для оценки степени остеохондрита и для подбора донорских участков.
Противопоказания
- Деструктивный остеоартрит.
- Воспалительные артропатии.
- Инфекция коленного сустава в анамнезе.
- Злокачественные опухоли.
- Возраст пациентов старше 50 лет.
Относительными противопоказаниями считаются избыточная масса тела и низкая приверженность лечению.
Техника мозаичной хондропластики
Положение пациента — на спине с согнутой под 120° ногой. Рентгеновский снимок с контрольной меткой позволяет убедиться, что степень сгибания колена достаточна для доступа к донорскому участку кости.
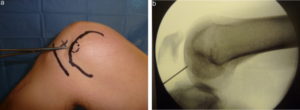
Далее осуществляется артроскопический доступ к мыщелку бедренной кости с поврежденным участком хряща. Производится очистка участка кюреткой и иссечение краев для получения ровного здорового контура. Затем вводится зонд с метками — с его помощью измеряют точный размер дефекта. Если дефект слишком большой или расположен очень далеко, операцию делают с помощью артротомии (открытым доступом).
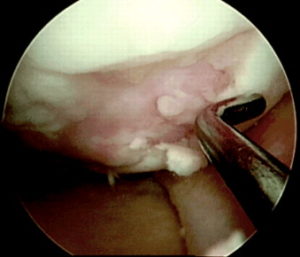
Следующим этапом делают разрез тканей и получают доступ к тому участку кости, откуда будут брать трансплантат. Используется перекрестный принцип: если восстанавливают дефект на медиальном мыщелке, то трансплантат берут с боковой поверхности латерального и наоборот. Забор ткани осуществляется трубчатым долотом. Очень важно в момент “вбивания” долота сохранять точную перпендикулярность по отношению к поверхности хряща.
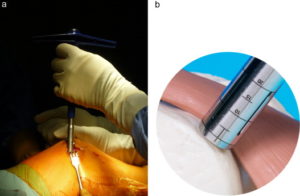
Количество забираемых цилиндрических костно-хрящевых фрагментов варьируется от трех до пяти и зависит от их размера: чем больше трансплантат, тем меньше их требуется. Обычно берут 3 трансплантата диаметром 10-11 мм или 5-6 диаметром 5-7 мм.
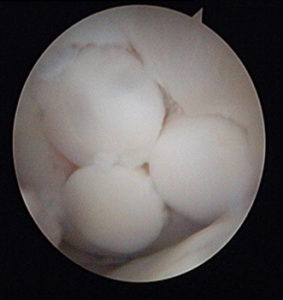
После получения необходимого количества костно-хрящевых фрагментов выполняется сверление первого “посадочного гнезда” на дефектном участке хряща. Осуществляется это также трубчатым долотом, но диаметр его на 1 мм меньше того, которое применялось для извлечения трансплантатов. Длина посадочного отверстия измеряется, под него подгоняется длина трансплантата, который осторожно фиксируется на предназначенное для него место способом press-fit. Процедуру повторяют необходимое количество раз. При этом отверстия сверлят таким образом, чтобы они были не параллельны и расходились веером от гипотетического центра кривизны мыщелка, это позволяет максимально точно восстановить кривизну суставной поверхности.
Мозаичная хондропластика надколенника и большеберцовой суставной поверхности
Как мы знаем, в коленном суставе имеется еще две суставных поверхности — внутренняя сторона надколенника и суставная поверхность большеберцовой кости. Они также могут повреждаться и требовать “ремонта”.
В случае с надколенником мозаичная хондропластика не представляет сложностей. Она всегда проводится открытым способом, так как требует вывихивания надколенника. Источником трансплантатов обычно служит межмыщелковая бороздка, а сами костно-хрящевые фрагменты имеют меньшую толщину — не более 12 мм (при операции на бедренных надмыщелках их длина составляет 15-18).
Провести мозаичную хондропластику суставной поверхности большеберцовой кости коленного сустава технически достаточно сложно. Для этого необходима направляющая лигаментопластика передней крестообразной связки — этим обеспечивается доступ к месту операции. Источники трансплантатов все те же.
Послеоперационный период и реабилитация
В раннем послеоперационном периоде к оперированному колену прикладывают пузыри со льдом — это снижает риск гемартроза. Также нежелательно применение антикоагулянтов, так как они увеличивают риск гемартроза.
Нагружать сустав можно уже на следующий день, если проводилась пластика с одним трансплантатом, но только с ограничением объема сгибания. В противном случае рекомендуется полностью исключить нагрузку на сустав сроком до 3-х недель, а в дальнейшем на протяжении 3-4 постепенно ее увеличивать. Через 10 недель пациенту разрешается бегать.
Что показывает МРТ-контроль
МРТ — лучший способ отслеживать динамику мозаичной хондропластики. При нормальном процессе заживления через несколько недель происходит полная остеоинтеграция костной части фрагмента и заживление хрящевой. МРТ в режиме T2-взвешенных изображений (FSE) позволяет своевременно отслеживать осложнения.
Возможные осложнения
При мозаичной хондропластике осложнения отмечаются достаточно редко. Перечень осложнений:
- перелом трансплантата во время извлечения;
- слишком глубокое погружение — “проваливание” — трансплантата в донорское отверстие;
- послеоперационный гемартроз;
- болезненность в области участка-донора ( в области извлечения костно-хрящевых фрагментов);
- некроз трансплантата;
- псевдоартроз трансплантата.
Результаты мозаичной пластики коленного сустава
Недавно Ласло Хангоди с соавторами (Hangodi et al.) опубликовал результаты крупного исследования, включившего почти 1000 пациентов: 789 человек с повреждением хряща мыщелков бедренной кости, 31 — суставной поверхности большеберцовой кости, 147 — надколенника). В 81% случаев отмечалась сопутствующая патология — травмы менисков, костей, связок.
Через 15 лет наблюдения отмечено:
- 92% отличных результатов при мозаичной пластике мыщелков бедра;
- 87% — при пластике суставной поверхности большеберцовой кости;
- 74% — при пластике надколенника.
В ходе исследования по тем или иным причинам были проведены 83 биопсии пересаженных трансплантатов. В 83% биоптатов была отмечена отличная остеоинтеграция и образование прекрасной хрящевой матрицы богатой коллагеном 2 типа и гликозаминогликанами.
Авторы исследования, а также ряд других авторов отмечают относительную простоту мозаичной пластики, относительно низкую стоимость и тот факт, что переносится живой аутологический хрящ.
Сравнение результатов мозаичной пластики и трансплантации аутологичных культивированных хондроцитов проводилось лишь в краткосрочной перспективе (срок наблюдений до 1 года после операции). Поэтому объективный анализ пока не доступен.

- Суть метода
- Показания
- Как проходит процедура?
- Использование стволовых клеток
- Как делают уколы стволовых клеток?
- Механизмы действия
- Трансплантация стволовых клеток в сустав
Терапия стволовыми клетками в России стремительно развивается. Это мировая тенденция. В клеточных технологиях врачи видят основные достижения, которые ждут медицину в двадцать первом веке. Они в наибольшей мере внедрены в онкогематологическую практику. На втором месте по частоте и эффективности использования клеточных технологий стоит ортопедия и травматология. В России уже есть клиники, врачи которых вводят стволовые клетки в сустав колена с целью лечения артроза, и достигают хороших результатов терапии. Эти клетки они получают из жировой ткани.
Суть метода

Закачивание собственного жира в суставы – новый метод лечения артроза, травматических повреждений хрящей и связок. Он является источником стволовых клеток, которые способны восстанавливать практически любые ткани.
Стволовые клетки выделяются костным мозгом и постоянно циркулируют в крови. Они принимают участие в регенераторных процессах: восстанавливают органы человека в случае их повреждения. Но сустав кровоснабжается плохо. Туда стволовые клетки в адекватных количествах попросту не попадают. В такой ситуации на помощь приходит жировая ткань. Она хорошо васкуляризирована (содержит много кровеносных сосудов) и является одним из лучших источников стволовых клеток.
Они способны встраиваться в костную, хрящевую ткань, помогают быстрее сращивать сухожилия и связки в случае их разрыва. Поэтому они идеально подходят для лечения болезней суставов.
Показания
Чаще всего практикуется введение жира в сустав при артрозе. Процедура также используется при травматических повреждениях крупных суставов, остеонекрозе бедренной кости. Лечение гонартроза жировыми клетками пока что не внедрено повсеместно. Это не методика первого выбора, потому что она новая. Но процедура уже хорошо себя зарекомендовала в развитых странах, таких как Германия и США, где одобрена для использования в ортопедии с 2016 года.
Лечение артроза коленного сустава стволовыми клетками обычно используется в таких случаях:

начальные стадии заболевания, когда необходимости в хирургическом лечении ещё нет, но пациента мучают хронические боли в суставе;
неэффективность консервативных методов: физиотерапии, лечебной физкультуры, обезболивающих препаратов;
поздние стадии остеоартроза, когда операция противопоказана по медицинским причинам, либо пациент от неё отказывается.
Лечение гонартроза стволовыми клетками позволяет уменьшить боль, снизить выраженность функциональных нарушений (улучшить подвижность сустава), замедлить развитие болезни. Клеточная терапия способствует регенерации хрящевой ткани. Вполне вероятно, что её широкое внедрение позволит в будущем уменьшить потребность населения в эндопротезировании – травматичной операции, при которой собственный сустав человека полностью удаляют, а на его место ставят искусственный эндопротез.
Как проходит процедура?
Лечение суставов жиром из живота проходит в два этапа. Вначале доктор проводит забор жира из передней жировой стенки. Он отсасывает его через небольшой прокол. Процедура не болезненная благодаря использованию местной анестезии или общего наркоза. При выборе способа обезболивания врач учитывает пожелания пациента.
После забора жировая ткань препарируется с использованием специального устройства. Полученный материал вводится внутрь колена. Жир находится там длительное время, являясь источником мезенхимальных стволовых клеток.
Преимущества:
минимально инвазивная операция, которая длится 30 минут;
может быть выполнена без общего наркоза;
не требуется госпитализация: пациент возвращается домой в день проведения процедуры, а затем лишь посещает врача для выполнения перевязки;
так как пересаживаются собственные жировые клетки, а не донорские, риск иммунных реакций сведен к нулю;
жировая ткань не центрифугируется, что позволяет сохранить наибольшее количество функциональных стволовых клеток.
Использование стволовых клеток
Не только уколы жира в коленный сустав, но и трансплантация выделенных из жировой ткани стволовых клеток помогает восстановить целостность хрящевой поверхности. Эта методика позволяет продлить жизнь собственному суставу, отсрочив необходимость в эндопротезировании, либо вовсе отказавшись от него.

Основными источниками получения мезенхимальных стволовых клеток в настоящее время являются жировая ткань и костный мозг. Причем в жировой ткани их содержится в 100-1000 раз больше на единицу объема. Выделяемые из жира стволовые клетки:
генетически более стабильны при длительном культивировании;
имеют низкий коэффициент старения;
обладают высокой пролиферативной активностью.
Жировую ткань легко получить под местной анестезией. Из липоаспирата получают стромально-васкулярную фракцию. Она используется в качестве источника не только мезенхимальных стволовых клеток, но и других типов клеток, принимающих участие в регенерации тканей. В их числе предшественники:
Стволовые клетки не только замещают дефекты гиалинового хряща. Они также оказывают иммуномодулирующее и противовоспалительное действие.
Клеточная терапия стволовыми клетками имеет доказанную высокую безопасность. Ряд исследований подтвердили эффективность метода при начальных стадиях деформирующего остеоартроза. Установлено, что процедура введения увеличивает толщину гиалинового хряща. При необходимости возможно замещение дефектов хрящевой поверхности путем артроскопической трансплантации (пересадки) стволовых клеток, закрепленных на фибриновом клее (матрице).
Как делают уколы стволовых клеток?

Врач получает липоаспират в ходе проведения процедуры липосакции. Его отмывают физраствором и забуференными фосфатами. Затем подвергают ферментативной диссоциации. После завершения инкубации фермент инактивируют, клеточную суспензию отмывают. Нерасщепленные жировые фрагменты удаляют при помощи специального фильтра.
В результате получают ядросодержащие клетки. Их называют стромально-васкулярной фракцией. Для введения в колено может изготовляться суспензия, содержащая стволовые клетки. Перед введением оценивается их количество и жизнеспособность.
В сустав вводят несколько миллилитров суспензии. Врач может выполнять внутрисуставную инъекцию под контролем УЗИ. В дальнейшем оцениваются результаты. Обычно через 1 неделю у пациента уменьшается боль, через 1 месяц улучшается качество жизни, через 6 месяцев всё ещё сохраняются положительные эффекты, достигнутые с помощью введения в сустав стволовых клеток из жировой ткани. Через 3 месяца на УЗИ можно увидеть утолщение гиалинового хряща, что свидетельствует о том, что под действием терапии он действительно лучше регенерирует.
Механизмы действия
Стромально-васкулярная фракция, полученная из жировой ткани, работает в первую очередь за счет присутствия в ней мезенхимальных стволовых клеток. Они оказывают выраженное трофическое действие за счет секреции:
О лечении артроза стволовыми клетками в Москве отзывы можно встретить разные, но в большинстве своём они позитивные. У пациентов быстро уменьшается боль, а через несколько месяцев обнаруживается положительная динамика по данным инструментальных исследований. Быстрый и выраженный клинический эффект во многом связан с тем, что полученные из жировой ткани клетки вводятся именно в сустав, а не в кровоток пациента. Хондрогенез усиливает не только стромально-васкулярная фракция, но и синовиальная жидкость, реагирующая на введение препарата.
Трансплантация стволовых клеток в сустав

В лечении суставов стволовыми клетками в Москве могут использоваться технологии, позволяющие замещать небольшие дефекты гиалинового хряща. Они нередко формируются в результате травмы. При этом самостоятельное восстановление хрящевой ткани практически невозможно. Без использования медицинских процедур хрящ регенерирует очень плохо, потому что практически не кровоснабжается. Метаболические процессы в нем протекают очень медленно. Поэтому хрящ быстрее разрушается под действием трения, чем восстанавливается.
Дефекты хрящевой поверхности вызывают хроническую боль. К тому же, патологические изменения продолжают прогрессировать. В качестве паллиативной меры может быть использован метод трансплантации стволовых клеток из жировой ткани. Они фиксируются на фибриновом клее. В результате заполнения дефекта стволовые клетки преобразуются в хрящевую ткань и замещают дефект.
В процессе лечения проводится две хирургические операции. Вначале врач берет 100-300 мл подкожного жира из области живота. Процедура обычно выполняется под местной анестезией. Затем из жировой ткани получают около 10 миллионов стволовых клеток. Они фиксируются фибриновым клеем. В ходе артроскопической операции врач вводит фиксированные стволовые клетки в область хрящевого дефекта. Клинические исследования этого метода лечения показывают сохранение терапевтического эффекта даже через 4-5 лет наблюдения.
Инъекции жира в коленный сустав в Москве используются всё чаще. Это эффективный метод восстановления разрушенного патологическим процессом хряща. Цена введения жира в коленный сустав сопоставима с другими оперативными методиками лечения остеоартроза или других заболеваний суставов. При этом эффективность этого способа терапевтического воздействия достаточно высокая: через несколько месяцев наблюдается не только снижение боли, но и увеличение толщины гиалинового хряща. Таким образом, процедура лечения стволовыми клетками влияет не только на симптоматику заболевания, но и на его исход. Она позволяет отсрочить потребность в эндопротезировании или вовсе избежать операции по замене сустава.

Коленный сустав соединяет бедренную кость с большеберцовой и надколенником. Это сложно структурированное сочленение является одним из самых крупных в опорно-двигательном аппарате. Если бы, например, наши органы передвижения — нижние конечности — были наиболее совершенными колёсами или гусеничными цепями, то мы не смогли бы использовать и сотой доли тех возможностей, которые имеем благодаря сложности строения коленного сустава. Он выдерживает значительные нагрузки и обеспечивает высокую, разнообразную двигательную активность. Но постоянная и напряжённая работа приводит его к износу быстрее, чем другие суставы человеческого организма.
Хрящ коленного сустава не имеет кровоснабжения, его питание происходит за счёт суставной жидкости. Серьёзные повреждения хрящевой ткани приводят к тяжёлым осложнениям. Поэтому в немецких клиниках взяли на вооружение новую технологию — пересадку хрящевых клеток в коленный сустав. Такой метод лечения хрящей суставов стал отличной альтернативой эндопротезированию.
Прежде чем приступить к практическому воплощению инновационной методики восстановления хряща коленного сустава, опытные доктора проводят полное клиническое обследование больного и устанавливают точный диагноз. Затем следуют консервативные лечебные мероприятия, направленные на устранение хрящевых повреждений. И если этого оказывается недостаточно, назначают хирургическое вмешательство.
Выращивание хряща в лаборатории и его последующая трансплантация приносит положительные результаты более чем в 90% случаев. Успешное лечение хряща коленного сустава устраняет боль, повышает переносимость нагрузок, улучшает подвижность колена, восстанавливает хрящевой слой, позволяет отказаться от искусственного сустава.
Трансплантация хряща коленного сустава: в чём же суть методики?
На протяжении многих лет существовало мнение, что можно замедлить процесс разрушения хрящевой ткани, а восстановить её нельзя. Разработки немецких специалистов дают возможность реализовать наращивание хрящей в суставах на месте их дефекта, используя клетки самого пациента.
Наращивание хряща в коленном суставе начинается с малоинвазивного вмешательства при эндоскопической визуализации, помогающей оценить состояние суставных поверхностей, объём повреждения, а также взять клетки из здоровой хрящевой ткани. Затем они отправляются в лабораторию, где происходит выращивание хряща.
Процедура трансплантации хряща коленного сустава осуществляется минимально инвазивно посредством артроскопической техники. Делается два надреза величиной 1—2 см, через них при помощи специального аппарата вводятся клетки. Артроскопия предполагает иссечение патологических участков, сверление или шлифовку для образования молодой хрящевой ткани. Сустав очищается для улучшения регенерации.
Когда врачи имеют дело с глубоким повреждением до кости, проводится микрофрактурный метод. Специальным инструментарием создают маленькие отверстия в повреждённом отделе. Благодаря такой хирургической манипуляции новые молодые клетки выходят на поверхность, способствуя образованию хряща.
Аутогенная трансплантация хондроцитов в Германии продолжает усовершенствоваться. Настоящий фурор произвела АТХ 3D c применением хондросфер, предотвращающая необходимость замены суставов на ранних этапах. Она заключается во внесении шариков со специальным покрытием, состоящих из хрящевых клеток, в область предварительно обработанного дефекта.
Предшествующий способ АТХ требовал для того, чтобы пересаженные клетки не размывались, переносную субстанцию. С этой целью выращивалась и пришивалась к хрящу коллагеновая матрица, либо приходилось использовать надкостницу пациента.
Таким образом, сфероиды обеспечили больным максимально щадящее лечение хрящей суставов и минимальные риски, связанные с операцией. В данном случае, помимо артроскопического контроля применяется техника микроартротомии.
Лица молодого возраста, имеющие обширные поражения хряща, могут надеяться на полное восстановление сустава и хряща, а также на сохранение функций колена. То же самое касается пожилых пациентов, не страдающих остеоартритом. Противопоказанием считается возраст больного до 16 лет.
В Германии существуют высокоспециализированные лаборатории для выращивания клеточных культур в абсолютно стерильных условиях. У пациента берётся 120—150 мл крови для получения сыворотки.
Для забора хрящевых тканей наиболее подходящими являются здоровые, не подверженные большим нагрузкам участки сустава. Немецкие врачи выполняют амбулаторную операцию за 30 минут.
На этапе культивирования клеток происходит их размножение в сыворотке крови пациента. Преимущества этого метода:
- исключается контакт с чужеродными белками,
- обеспечивается стабильный уровень клеточного роста,
- максимально исключается риск отторжения хряща,
- используются клетки человека, который хорошо подготовлен к лечению.
За 3—4 недели новые клетки созревают, после чего отправляются в специальных сосудах к лечащему врачу. На это уходит несколько часов, качество клеток сохраняется.
На следующем этапе происходит трансплантация с хондросферами, описанная выше. Клетки быстро фиксируются, заполняют дефект и устраняют его. В процессе врастания хрящевых клеток принимают участие адгезивные белки, являющиеся связующим звеном. На это вмешательство уходит от 30 до 60 минут.
Польза замены хряща коленного сустава посредством культивированных клеток в Германии подтверждена многочисленными научными исследованиями. Имплантированный биологический материал не чужероден для организма и имеет все свойства, присущие натуральному хрящу.
Такое наращивание хрящей в суставах приводит к тому, что живые хондроциты строят новый функциональный слой. Сфероиды способствуют размножению клеток именно в тех местах, где они особенно необходимы. Появившаяся аутогенная хрящевая ткань обладает защитной функцией, которой так не хватало больному суставу.
Дефект закрывается живыми клетками за шесть недель. Они ещё не имеют такой большой плотности и стойкости к нагрузкам, как у окружающих тканей. Можно использовать трость для уменьшения нагрузки на сустав, но нельзя играть в футбол. Достаточная подвижность в коленном суставе и улучшение кровообращения должны достигаться регулярной щадящей нагрузкой. Интенсивность физических упражнений наращивается постепенно. Очень полезны физиотерапевтические процедуры.
Через три месяца после операции трансплантации хряща коленного сустава разрешается заниматься спортом. Начинать нужно с плавания, катания на велосипеде, быстрой ходьбы. Это значительно улучшает питание хряща. При сдавливании высвобождаются шлаки, при разгрузке в ткани поступают питательные вещества.
Полная регенерация дефекта наступает примерно через год после лечения хрящей суставов методом пересадки клеток. Можно заниматься любыми видами спорта.
Длительная эволюция сделала движение естественной потребностью человека. Однако, техногенный путь развития привёл к тому, что в настоящее время люди страдают от недостатка движений. Темп жизни требует напряжения, постоянна нехватка времени. Чтобы успеть за быстро бегущей жизнью, современному человеку нужны активные движения — лыжи, бег, спортивные игры. А как жить с больными коленями?

Тэджон считается научно-технической столицей Южной Кореи. Клиника Сон первая в стране.

Оказывает услуги по протезированию самых разных направлений. К предлагаемым протезам.

В центре столицы Чехии располагается одна из лучших клиник Европы, занимающаяся ортопедией.
+7 (863) 29-888-08 (круглосуточно).
Считаете материал полезным? Поделитесь статьей о лечении за рубежом с друзьями:
Укажите свои контакты, и мы обязательно с Вами свяжемся !!
Если у Вас есть что добавить по теме, или Вы можете поделиться своим опытом, расскажите об этом в комментарии или отзыве.
ИМЕЮТСЯ ПРОТИВОПОКАЗАНИЯ, ТРЕБУЕТСЯ КОНСУЛЬТАЦИЯ СПЕЦИАЛИСТА
Много лет западная медицина привлекает внимание наших соотечественников своей эффективностью. Мы знаем громкие успехи онкологов Германии, ортопедов Швейцарии, отоларингологов Польши, реабилитологов Венгрии и прочих европейских специалистов. Особенно стоит отметить интерес наших женщин к возможностям акушерства в США. Помимо высокого уровня обслуживания и безопасности процесса даже с наличием осложнений в анамнезе, рожениц привлекает второе гражданство малыша со всеми вытекающими из этого широкими возможностями. Но и заплатить за такую привилегию придётся хорошую сумму. Достойной альтернативой прайсам медицинских центров Европы и США являются цены в клиниках стран Ближнего Востока и Азии. Здесь эффективность терапии не уступает, а иногда и превосходит результаты конкурентов по многим направлениям. Например, доступно по цене и эффективно лечение поджелудочной в Израиле, когда помимо грамотно подобранной медикаментозной терапии обоснованно применяют малоинвазивные и роботизированные методы хирургии. Качество жизни пациентов с острым или хроническим панкреатитом, онкологией органа существенно улучшается. Более подробно о возможностях медицины за рубежом узнаете в компании "МедЭкспресс".
Читайте также:


