Анатомия бодрствования и сознания. Внутричерепная дислокация и вклинение
Добавил пользователь Алексей Ф. Обновлено: 27.01.2026
Под неотложными состояниями в неврологии понимаются все острые патологические состояния, протекающие, как правило, с нарушением сознания и требующие экстренной диагностики и лечения.
Существует следующая этиологическая классификация неотложных состояний:
I. Первичные (обычно органические) повреждения головного мозга:
А. Сотрясение головного мозга;
Б. Ушиб головного мозга;
В. Проникающее ранение и травматическая внутримозговая гематома;
Г. Субдуральная гематома;
Е. Эпидуральная гематома.
2. Сосудистые заболевания:
А. Внутримозговое кровоизлияние:
1) Артериальная гипертония;
2) Разрыв аневризмы;
4) Иные (геморрагический диатез, амилоидная ангиопатия , опухолевая эрозия сосудов).
Б. Субарахноидальное кровоизлияние:
1) Разрыв аневризмы;
В. Ишемический инсульт:
1) Тромбоз внутри- и внечерепных сосудов;
1) Первичные внутричерепные опухоли;
2) Метастатические опухоли;
4) Неметастатические осложнения злокачественных новообразований ( прогрессирующая мультифокальная лейкоэнцефалопатия ).
5. Эпилептический статус.
II. Вторичные поражения головного мозга:
1. Метаболические энцефалопатии:
2) Диабетический кетоацидоз ;
3) Гипергликемическое гиперосмолярное состояние без кетоацидоза ;
5) Печеночная недостаточность;
8) Гип о - и гиперкальциемия .
2. Гипоксическая энцефалопатия:
1) Тяжелая сердечная недостаточность;
2) Декомпенсация хронических обструктивных заболеваний легких;
3) Гипертоническая энцефалопатия.
1) Тяжелыми металлами;
2) Угарным газом;
3) Фармакологическими средствами ( опиоиды , барбитураты, кокаин);
4. Температурные повреждения:
1) Тепловой удар;
5. Поражения мозга вследствие нарушений питания (энцефалопатия Вернике ).
Одним из основных синдромов при неотложных состояниях является нарушение сознания.
Сама функция сознания включает два компонента – активацию и содержание сознания (т.е. осмысленное восприятие внутреннего и внешнего мира в результате интегративной деятельности мозга). За содержание сознания отвечают сложные нейронные структуры, рассеянные по всей коре головного мозга. Активация сознания обеспечивается сетью ядер и волокон восходящей активирующей ретикулярной формации (ВАРС). Действует ретикулярная формация через релейные ядра таламуса, диффузно проецируясь на все отделы коры головного мозга. В норме циклическая активность ВАРС обеспечивает чередование сна и бодрствования.
При патологии возможное развитие нарушений сознания реализуется тремя механизмами.
1. Двустороннее диффузное повреждение коры головного мозга, приводящее к нарушению сознания, несмотря на сохранность механизмов активации. Данное состояние называется вегетативным состоянием и наблюдается при диффузной гипоксии мозга.
2. Поражение ствола мозга с нарушением функций ВАРС. Развивается беспробудный патологический сон. Поражение ствола возникает при первичных повреждениях ствола (инсульт) или вторичных повреждениях ствола при смещениях внутричерепных структур ( височно-тенториальное или мозжечковое вклинение).
3. Сочетание стволового и двустороннего коркового поражения. Встречается при отравлениях и метаболических энцефалопатиях.
Степень нарушений сознания может варьировать от легкой спутанности до полной ареактивности . Четких переходов между этими состояниями нет. На практике степень нарушения сознания определяют по реакции больного на раздражители. Термины, обозначающие степени нарушения сознания (такие, например, как заторможенность, сомноленция или оглушенность ), часто понимаются по-разному, поэтому в истории болезни лучше подробно описать реакции больного.
А. Оглушенность определяют как утрату связности мыслей или действий. В основе оглушенности лежит нарушение внимания, то есть – способности отбирать необходимую информацию и координировать ответные реакции таким образом, чтобы не нарушалась логическая последовательность мыслей и поступков. Внимание связано как с активацией, так и с содержанием сознания, поэтому оглушенность может наблюдаться при поражении и коры, и ВАРС. Наиболее распространенные причины оглушенности – метаболические и токсические расстройства, но иногда она может наблюдаться и при очаговых поражениях коры, особенно правой теменной доли. При оглушенности больной находится в состоянии бодрствования, но не может выполнить задание, требующее устойчивого внимания, например, последовательно отнимать от ста по семь. Оглушенность может также сопровождаться грубым нарушением письма.
Делирий характеризуется сочетанием оглушенности , повышенной активности симпатической нервной системы (тахикардии, повышенного потоотделения, тремора, расширения зрачков и артериальной гипертонии) и галлюцинаций или бреда. В чистом виде оглушенность , как правило, возникает при метаболических энцефалопатиях и при легкой интоксикации седативными средствами; делирий же обычно вызывают расстройства, сопровождающиеся повышением содержания в крови катехоламинов, например, интоксикация психостимуляторами ( амфетаминами ), высокая лихорадка, отмена седативных средств ( бензо-диазепинов , барбитуратов) или алкогольная абстиненция.
Б. Патологическая сонливость. Больной постоянно пребывает в состоянии сна или дремоты, но его легко можно разбудить, после чего он способен отвечать на вопросы и выполнять инструкции.
В. Сопор. Больного невозможно полностью разбудить даже с помощью болевых раздражений. Реакция на словесные инструкции слабая или отсутствует, от больного невозможно добиться ответного слова или звука. В то же время он может реагировать целенаправленными защитными двигательными реакциями.
Г. Кома I ( поверхностная кома). Болевое раздражение вызывает лишь простейшие, беспорядочные движения. Разбудить больного не удается. Роговица сочная, сохранятся роговичный рефлекс. Нарушений витальных функций организма нет. Может наблюдаться тах и - или брадикардия, тахипноэ (частота дыхания 12-24 в 1 минуту). Частота дыхания более 30 в 1 минуту является неблагоприятным прогностическим признаком. Мышечный тонус в норме, сухожильные рефлексы нормальные или повышены.
Кома II ( глубокая кома). Сохраняется реакция на болевое раздражение. Снижен роговичный рефлекс. Выявляется анизокория и двусторонний рефлекс Бехтерева. Мышечный тонус или снижен, или наблюдается децеребрационная ригидность.
Кома III ( запредельная ). Наблюдается арефлексия, адинамия, гипотония мышц, паралитический мидриаз , сухая роговица, отсутствуют роговичные рефлексы. Нарушены витальные функции организма, нет самостоятельного дыхания.
При выходе из коматозного состояния может наблюдаться один трех синдромов:
1) Апаллический синдром. В данном случае функционируют подкорковые ядра. Нормализуется дыхательная и сердечно-сосудистая деятельность, есть реакция на болевые раздражители. Однако отсутствуют спонтанные движения. Больной не выполняет команды. Гипотония мышц может перейти в гипертонию и горметонические судороги, усиливающиеся в такт дыхательным движениям.
2) Акинетический мутизм . Имеется четкая смена сна и бодрствования. Больной реагирует на речь, фиксирует взгляд. Нет активных движений, нет речи. Тонус мышц близок к нормальному . Данное состояние носит название вегетативного и может продолжаться длительно.
3) Длительное состояние оглушенности . Сохраняется заторможенность, вялость, сонливость.
Для оценки уровня сознания используется шкала Глазго. По 5-балльной шкале оценивается каждый из трех признаков:
· Реакция на укол
Сумма баллов составляет от 3 до 15 баллов. 3 – смерть мозга, 4-8 – кома, 9-12 – сопор, 13-14 – оглушение, 15 – ясное сознание.
Лечение неотложных состояний в неврологии
1. Восстановление функции дыхания.
Восстанавливается проходимость дыхательных путей. Извлекаются зубные протезы, устраняется западение языка, удаляется слизь из воздухопроводящих путей, вводятся воздуховоды. Эвакуация содержимого желудка проводится через назогастральный зонд.
Показания к интубации: 1) сопор, кома; 2) выраженные расстройства дыхания; 3) тахипноэ больше 35.
Противопоказанием для интубации трахеи является повреждение шейного отдела позвоночника.
2. Кардиальная реанимация.
Может возникнуть асистолия, острая сердечная недостаточность, отек легких, кардиогенный шок, нарушение ритма сердца, нарушение сердечного ритма, острая сосудистая недостаточность.
При асистолии лечение проводится путем внутрисердечной инъекции адреналина, непрямого и прямого массажа сердца и электрической дефибрилляцией .
При острой сердечной недостаточности внутривенно вводят сердечные гликозиды ( строфантин , коргликон , дигоксин ).
При острой левожелудочковой недостаточности развивается отек легких. В данном случае эффективно полусидячее положение, вдыхание кислорода, введение сердечных гликозидов, мочегонных средств и нейролептиков в сочетании с наркотическими анальгетиками ( таламонал ). При высоком АД вводятся ганглиоблокаторы . При снижении АД эффективны глюкокортикостероиды (гидрокортизон, преднизолон ).
При правожелудочковой недостаточности эффективно введение эуфиллина .
При кардиогенном шоке возникает инверсия АД и пульса. АД может быть 60 мм рт ст , а пульс 120 уд. в 1 минуту. В данном случае необходимо экстренное введение вазопрессоров внутривенно (адреналин, норадреналин, кортикостероидов).
При желудочковых нарушениях сердечного ритма внутривенно вводится лидокаин .
При острой сосудистой недостаточности также производится введение вазопрессоров .
Лечение отека мозга проводится в следующих направлениях:
· Поддержание адекватной легочной вентиляции и гемодинамики. Вдыхается чистый кислород. Это приводит к спазму артериальных сосудов мозга и уменьшению отека мозга.
· Для нормализации венозного оттока из полости черепа больной находится в лежачем положении со слегка приподнятым верхним краем кровати.
· Использование диуретиков . В настоящее время для этого используются осмодиуретики ( маннитол 20%, глицерин). При опухолях головного мозга для дегидратации используются глюкокортикостероиды ( дексаметазон ).
· Хирургическое лечение при резко выраженной внутричерепной гипертензии и отеке мозга. Проводится бифронтальная краниотомия. Это спасет больному жизнь, но приводит к появлению грубого необратимого неврологического дефекта.
4. Нормализация гомеостаза.
Проводится коррекция КЩР. Как правило, развивается метаболический ацидоз. Для этого вводится бикарбонат натрия 4% 150-200 мл в сутки.
Для коррекции водно-электролитного баланса используются препараты, содержащие макро- и микроэлементы ( дисоль , ацесоль , трисамин , квартасоль , раствор Рингера и др.).
Для профилактики гипоксии проводится назначение ноотропила , цербролизина , гаммалона , окибутирата натрия.
5. Профилактика экстрацеребральных осложнений.
Для предотвращения гипостатической пневмонии используется перкуссионный массаж грудной клетки.
Для профилактики пролежней используются частые повороты в постели и устранение складок на простыне.
Для профилактики уросепсиса проводится катетеризация мочевого пузыря и промывание его антисептическими растворами.
Проводится опорожнение кишечника.
6. Парентеральное питание. При нарушении сознания утрачивается способность самостоятельного питания, поэтому производится внутривенное введение растворов глюкозы с добавлением препаратов калия и витаминов. Имеются специальные смеси для парентерального питания ( липанор , липантил ).
7. Симптоматическое лечение.
Проводится купирование судорожного синдрома. Для этого назначаются противоэпилептические средства ( реланиум , ГОМК, тиопентал натрия, закись азота).
Коррекция вегетативных расстройств – артериальной гипертензии, гипертермии.
Купирование психомоторного возбуждения ( реланиум , нейролептические средства).
При отеке мозга может возникать явление дислокации стволовых мозговых структур.
Различают супратенториальное (верхнее) и субтенториальное (нижнее) вклинение.
При супратенториальном типе в вырезку намета мозжечка вклинивается височная доля и ущемляет верхние отделы ствола. Наблюдается две фазы верхнего вклинения:
- Диэнцефальная стадия. Наблюдается головная боль, двигательное беспокойство, дезориентация в пространстве, жажда, нарушение сна, причмокивание губ. Затем нарушается сознание, увеличивается выраженность очаговых симптомов, наблюдается экстензия нижних конечностей. Выявляется миоз или синдром Горнера. Парез взора вверх. Плавающие движения глазных яблок. Тахикардия, эктрасистолия , гипергидроз . Дыхание типа Чейн-Стокса .
- Мезенцефальная стадия. Происходит сдавление среднего мозга. Происходит расширение зрачка с той стороны, где находится очаг поражения. Утрачивается рефлекс на свет. Может быть птоз, косоглазие. При сдавлении среднего мозга возникает гемипараз на стороне, противоположной очагу.
- При прогрессировании процесса симптомы становятся двусторонними.
При центральном вклинении отек мозга приводит к двустороннему вклинению и двусторонней симптоматике.
При субтенториальном типе происходит вклинение нижних ножек мозжечка в большое затылочное отверстие. Симптоматика характеризуется головной болью в шейно-затылочной области, головокружением, рвотой, мозжечковыми расстройствами, ригидностью затылочных мышц, нистагмом. На глазном дне выявляются застойные диски зрительных нервов. Мышечный тонус снижен. Дыхание редкое, поверхностное. Исчезают стволовые рефлексы.
Диагностика при вклинениях включает проведение обзорной рентгенографии. По смещению обызвествленной шишковидной железы можно косвенно судить о вклинении. Проводят Эхо-ЭГ , КТ, МРТ. Люмбальная пункция противопоказана.
Лечение. Экстренная терапия отека мозга, либо проведение хирургического лечения.
Анатомия бодрствования и сознания. Внутричерепная дислокация и вклинение
Анатомия бодрствования и сознания. Внутричерепная дислокация и вклинение
Анатомическим субстратом поддержания бодрствования служит восходящая ретикулярная активирующая система и ее корковые проекции. Основной составляющей системы является ретикулярная формация. Она располагается вокруг силъвиева водопровода на всем протяжении от гипоталамуса до покрышки моста. F.e дорсальные проекции следуют с обеих сторон через интраламинарные ядра таламуса к коре больших полушарий. Вентральные проекции направляются к базальным отделам переднего мозга.
При двустороннем нарушении функционирования этой системы наступает угнетение сознания, независимо от того, является ли нарушение функциональным и обратимым или представляет собой структурное и в большинстве случаев необрагимое расстройство. Кома может развиваться при двустороннем структурном поврежаении или дисфункции покрышки моста, околоводопроводной зоны среднего мозга, таламуса, белого вещества или коры обоих полушарий.
Супра- или инфратенториальные объемные образования в головном мозге могут быть причиной смещения (дислокации) как прилегающих, так и удаленных участков мозга. При односторонних супратенториальных образованиях, например опухоли, гематоме или абсцессе, постепенно происходит смешение структур головного мозга в противоположную сторону. Это обычно легко определить при нейровизуализации по боковому смещению срединных структур мозга, Таких как обызвествленное шишковидное тело или прозрачная перегородка. Значительная степень смешения срединных структур обычно сопряжена с угнетением сознания.
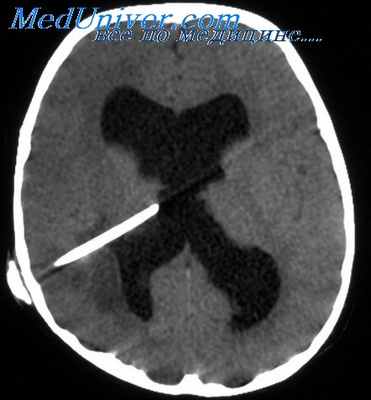
Смещение шишковидной железы на 3—5 мм. как правило, сопровождается состоянием сомноленции, смешение на 5—8 мм — сопором, смешение свыше 8 мм характерно для комы. По мере нарастания масс-эффекта происходит смешение в противоположную сторону поясной извилины с вклинением под мозговой серп, а медиобазальные части височной доли смещаются медиально и вниз, вклиниваясь под мозжечковый намет. Крючок (uncus) гиппокампальной извилины вклинивается между мозжечковым наметом и стволом мозга, что вызывает сдавление в узкой вырезке намета мозжечка как самого крючка, так и ствола мозга и глазодвигательного нерва (латеральное, или ункальное, транстенториальное вшипение).
Наряду с угнетением сознания в этом случае на стороне очага наблюдаются расширение зрачка или парез наружных мышц глаза, иннервируемых глазодвигательным нервом. Двусторонние супратенториальные объемные процессы приводят к смещению промежуточного и среднего мозга вниз по средней линии с вклинением в вырезке намета мозжечка (аксиальное транстенториальное вклинение). Инфратенториальные объемные процессы, например кровоизлияние в мозжечок, непосредственно сдавливают структуры ствола мозга и, соответственно, ретикулярную формацию. Кроме того, они вызывают смешение тканей через вырезку намета мозжечка вверх (восходящее транстенториальное вклинение), а также смещение миндалин мозжечка вниз через большое затылочное отверстие в спинальный канал (тонзиллярное вклинение). Следствием вклинения могут быть вторичные кровоихтияния в средний мозг, так называемые кровоизлияния Дюре.
К другим осложнениям относятся пережатие сосудов и инфаркты мозга, при вклинении под мозговой серп - передней мозговой артерии или ее ветвей, при транстенториальном вклинении — задней мозговой артерии.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Анатомия бодрствования и сознания. Внутричерепная дислокация и вклинение
Городская клиническая больница №12, Москва
ФГБУ МРНЦ Минздрава России, Обнинск
Московский государственный медико-стоматологический университет им. А.И. Евдокимова
ГБУЗ «НИИ СП им. Н.В. Склифосовского» Департамента здравоохранения Москвы, Москва, Россия
Городская клиническая больница №12 Департамента здравоохранения Москвы
Кафедра неврологии и нейрохирургии Российского государственного медицинского университета им. Н.И. Пирогова, Москва
ГБУЗ «Городская клиническая больница №12»
ГБУЗ «Городская клиническая больница №12»
ГБУЗ «Городская клиническая больница №20», Москва
Дислокационный синдром у больных со злокачественным течением массивного ишемического инсульта
Журнал: Журнал неврологии и психиатрии им. С.С. Корсакова. Спецвыпуски. 2015;115(3‑2): 20‑26
Городская клиническая больница №12, Москва
Цель исследования. Проведение сравнительного анализа между выраженностью дислокации головного мозга, темпом ее развития по данным КТ и клиническими проявлениями дислокационного синдрома (ДС) у пациентов со злокачественной формой массивного ишемического инсульта (МИИ). Материал и методы. Проведен анализ результатов обследования и лечения 114 больных со злокачественным течением МИИ. По типу течения ДС больные были разделены на 2 группы: 1-я группа — с неблагоприятным типом течения ДС (91 человек), 2-я группа — больные с благоприятным типом течения ДС (23 человека). Больных обеих групп сравнивали по течению и исходам заболевания, а также темпу развития и выраженности дислокации головного мозга по данным КТ. В 1-й группе 27 пациентам выполнили декомпрессивную краниотомию (ДКТ). Результаты. У всех больных 1-й группы имелась декомпенсация ДС, в связи с чем его течение было расценено как неблагоприятное. Все больные 1-й группы, которым проводили только консервативное лечение, умерли. У больных 1-й группы, которым консервативное лечение было дополнено ДКТ, летальность составила 48%. В этой группе выделили 3 варианта течения ДС: фульминантное, прогредиентное, отсроченное. У пациентов 2-й группы летальность составила 52%. Пациенты умерли от внечерепных осложнений, поэтому тип течения ДС в этой группе был расценен как благоприятный. Заключение. У больных со злокачественным течением МИИ риск летального исхода от височно-тенториального вклинения определяется не только выраженностью, но и темпом развития поперечной дислокации срединных структур головного мозга. ДС у больных со злокачественным течением МИИ может протекать по благоприятному и неблагоприятному типам. При неблагоприятном типе темп развития ДС может быть фульминантным, прогредиентным и отсроченным. Неблагоприятное течение ДС является абсолютным показанием к ДКТ.
Городская клиническая больница №12, Москва
ФГБУ МРНЦ Минздрава России, Обнинск
Московский государственный медико-стоматологический университет им. А.И. Евдокимова
ГБУЗ «НИИ СП им. Н.В. Склифосовского» Департамента здравоохранения Москвы, Москва, Россия
Городская клиническая больница №12 Департамента здравоохранения Москвы
Кафедра неврологии и нейрохирургии Российского государственного медицинского университета им. Н.И. Пирогова, Москва
ГБУЗ «Городская клиническая больница №12»
ГБУЗ «Городская клиническая больница №12»
ГБУЗ «Городская клиническая больница №20», Москва
Заболеваемость ишемическим инсультом (ИИ) в Российской Федерации составляет 350 на 100 000 взрослого населения в год [1]. У 5% больных происходит массивный ИИ (МИИ). К МИИ (обширному полушарному) относят инфаркт головного мозга с вовлечением 50% и более бассейна кровоснабжения средней мозговой артерии (СМА) [2]. Выделяют доброкачественное и злокачественное течение МИИ. При доброкачественном течении МИИ не развиваются полушарный отек и дислокация головного мозга, а при злокачественном течении происходят развитие полушарного отека и дислокация головного мозга с нарушением витальных функций. В подавляющем большинстве случаев злокачественного течения МИИ на 2—3-и сутки от начала заболевания происходит нарастающее снижение уровня бодрствования, отмечаются появление двусторонней пирамидной симптоматики, анизокории, нарушаются функции дыхания и кровообращения. Еще до внедрения в клиническую медицину компьютерной томографии (КТ) многочисленные аутопсийные исследования показали, что дислокационный синдром (ДС) является основной причиной смерти у больных с МИИ [3—7].
Единственным методом лечения жизнеугрожающей дислокации головного мозга у больных с МИИ остается декомпрессивная краниотомия (ДКТ) [8—17]. Однако в случае грубой декомпенсации ДС в виде угнетения уровня бодрствования до глубокой комы хирургическое лечение уже неэффективно. Сроки развития ДС у данной категории больных различны, фатальное височно-тенториальное вклинение может произойти в течение первых суток заболевания. Так, A. Qureshi и соавт. [18] наблюдали 53 пациентов со злокачественным течением МИИ. Авторы отметили разные сроки появления ДС в виде прогрессирующего снижения уровня бодрствования. В 1-е сутки заболевания ДС был отмечен у 35% больных, на 2-е сутки — у 33%, на 3-и сутки — у 19%, на 4-е сутки — у 4%, на 5-е сутки — у 4%, на 6-е сутки — у 5%. По данным ряда авторов [6, 18—22], транстенториальное вклинение с картиной ДС у данной категории больных также развивается в 1—6-е сутки от начала инсульта, но наиболее часто — в первые 48 ч от начала заболевания. Прогностическим фактором риска летального исхода от височно-тенториального вклинения является развитие поперечной дислокации головного мозга. При достижении определенной степени поперечной дислокации ДС приобретает прогредиентную форму. Принципиально важно то, что в этот момент ДС еще может быть обратим в случае проведения ДКТ. Таким образом, возможно прогнозировать риск развития летального исхода при определенной степени дислокации и до развития вклинения экстренно провести ДКТ. Был проведен ряд исследований, посвященных выявлению критического значения поперечной дислокации. По данным M. Pullicino и соавт. [23], фактором риска наступления летального исхода у больных с МИИ является развитие поперечной дислокации головного мозга, равной 9 мм и более на уровне прозрачной перегородки. В исследованиях T. Gerriets и соавт. [24] и С. André и соавт. [25] фактором риска летального исхода у больных с МИИ явилось развитие поперечной дислокации головного мозга, равной 4—5 мм и более на уровне III желудочка. Согласно собственным данным [26, 27], фактором риска наступления летального исхода у больных с МИИ является развитие поперечной дислокации головного мозга на уровне прозрачной перегородки, равной 7 мм и более в первые 48 ч от начала заболевания.
Цель настоящего исследования — сопоставление выраженности дислокации головного мозга по данным КТ с клинической картиной ДС у больных со злокачественным течением МИИ.
Материал и методы
Обследовали 114 больных, 59 мужчин и 55 женщин, со злокачественным течением МИИ, находившихся на лечении в неврологических стационарах в период с 01.10.09 по 01.05.14. Средний возраст больных составил 69±13 лет.
Диагноз МИИ устанавливали при наличии ишемического поражения головного мозга в бассейне СМА объемом свыше 150 см 3 . В исследование включали больных только со злокачественным течением заболевания, основным критерием которого являлось развитие поперечной дислокации более 2 мм на уровне прозрачной перегородки в течение первых 4-х суток от начала инсульта. Критериями исключения из исследования были наличие острой ишемии в противоположном каротидном бассейне, вертебрально-базилярной системе, наличие объемного образования головного мозга. В исследование также не включали пациентов с МИИ, поступавших в крайне тяжелом состоянии, обусловленном внечерепными причинами.
Всем больным при поступлении в стационар и в динамике (в среднем через 24 и через 48 ч от момента поступления) проводили КТ головного мозга. При анализе томограмм определяли наличие поперечной и аксиальной дислокации структур головного мозга. КТ-признаками развития дислокации считали появление и нарастание поперечной дислокации прозрачной перегородки более чем на 2 мм, а также развитие аксиальной дислокации, выраженность которой определяли по степени деформации охватывающей цистерны по классификации В.Н. Корниенко [28]. Проявлением декомпенсации ДС считали развитие прогрессирующего угнетения уровня бодрствования.
Всем пациентам проводили коррекцию артериального давления и деятельности сердечно-сосудистой системы, профилактику внечерепных осложнений. Показанием к искусственной вентиляции легких являлось угнетение уровня бодрствования до сопора и глубже. При развитии у больного дислокации головного мозга по данным КТ проводили мероприятия, направленные на снижение внутричерепного давления: обеспечивали возвышенное положение головного конца кровати, коррекцию гипертермии, болюсно вводили 15% раствор маннитола в дозе 0,25—1,0 г/кг под контролем осмолярности и электролитного состава крови. Выделены 2 группы больных. Больные, у которых произошла декомпенсация ДС, составили 1-ю группу (91 человек). Больные, у которых не произошло декомпенсации ДС, были включены во 2-ю группу (23). Больных обеих групп сравнивали по течению и исходам заболевания, темпам развития и выраженности ДС по данным КТ. В 1-й группе 27 пациентам выполнили оперативное лечение — ДКТ над пораженным полушарием. При проведении ДКТ формировали костный дефект размером не менее 12×14 см с полным удалением чешуи височной кости до основания средней черепной ямки. Площадь полученного дефекта составляла около 170 см 2 .
Статистический анализ полученных данных проводили с использованием программы Statistica 6.0. В описательной статистике данные представлены в формате M±σ (M — среднее арифметическое, σ — стандартное отклонение). Для определения статистической значимости различия признаков между группами больных использовали методы непараметрической статистики, критерий Мак-Нимара, определяли двусторонний точный критерий Фишера. Разницу считали достоверной при уровне критерия значимости p
Результаты
Летальность в 1-й группе составила 70%, умерли все пациенты, которым проводили только консервативное лечение (64 человека). У оперированных пациентов (27 больных) летальность составила 48%. В связи с тем что у всех больных произошла декомпенсация ДС, тип его течения расценили как неблагоприятный. По темпам декомпенсации ДС нами было выделено 3 варианта его течения: фульминантное, прогредиентное и отсроченное. Фульминантное течение ДС наблюдалось у 22 больных. У этих пациентов поперечная дислокация головного мозга превышала 2 мм в первые 24 ч от начала заболевания и в среднем составила 3 мм (рис. 1, 2). При поступлении в стационар уровень бодрствования соответствовал оглушению у 14 (64%), сопору — у 8 (36%) больных. Нарастание угнетения сознания происходило в первые 24 ч от начала инсульта, и ко 2-м суткам уровень бодрствования у всех больных соответствовал коме (рис. 3). При повторной КТ головного мозга к началу 2-х суток от развития инсульта латеральная дислокация в среднем составила 15 мм. Из 22 больных с фульминантным течением ДС были прооперированы 4 пациента, летальность у оперированных больных составила 50%, у неоперированных — 100%.
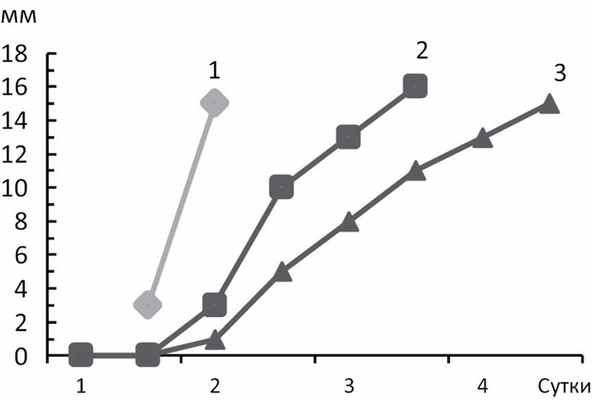
Рис. 1. Динамика латеральной дислокации у больных с неблагоприятным типом ДС на 1—5-е сутки от начала инсульта. Кривая 1 — фульминантный вариант, кривая 2 — прогредиентный вариант, кривая 3 — отсроченный вариант. По оси ординат — величина дислокации (мм), по оси абсцисс — сутки от начала заболевания.
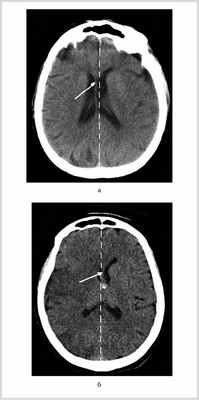
Рис. 2. КТ головного мозга больных с МИИ с фульминантным течением ДС. а — КТ больного П., 6 ч от начала заболевания. На фоне незначительного сужения конвекситальных субарахноидальных борозд левого полушария отмечено смещение срединных структур вправо на 4 мм (указано белой стрелкой, пунктиром показана средняя линия); б — КТ больного В., 8 ч от начала заболевания. На фоне незначительного сужения конвекситальных субарахноидальных борозд и минимальной гиподенсивности правого полушария отмечено смещение срединных структур влево на 2,5 мм.
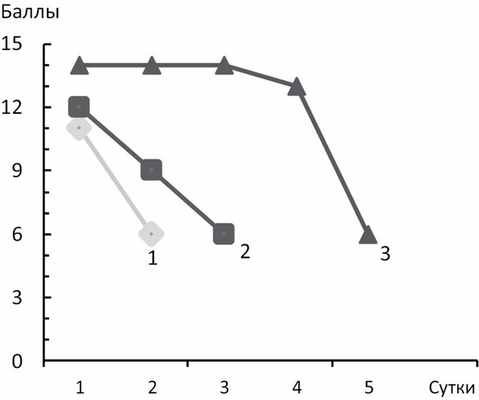
Рис. 3. Динамика уровня бодрствования у больных с неблагоприятным типом ДС на 1—5-е сутки от начала инсульта. Кривая 1 — фульминантный вариант, кривая 2 — прогредиентный вариант, кривая 3 — отсроченный вариант. По оси ординат — балл по шкале комы Глазго, по оси абсцисс — сутки от развития инсульта.
Прогредиентное течение ДС наблюдалось у 54 больных. У этих пациентов отсутствовала поперечная дислокация головного мозга в первые 24 ч от начала заболевания, однако при повторной КТ головного мозга на 2-е сутки было отмечено развитие поперечной дислокации до 7 мм и более (в среднем 10 мм) (см. рис. 1). При госпитализации уровень бодрствования соответствовал оглушению у 44 (81%) больных, сопору — у 10 (19%). Угнетение уровня бодрствования развивалось в промежуток от 24 до 48 ч от развития инсульта, а на 3—4-е сутки уровень бодрствования у всех больных соответствовал коме (см. рис. 3). При повторной КТ на 3—4-е сутки латеральная дислокация в среднем составила 16 мм. Из 54 больных с прогредиентным течением ДС прооперировали 20 пациентов. Летальность у оперированных больных составила 45%, у неоперированных — 100%.
Отсроченное течение ДС отмечено у 15 пациентов. У всех больных не было поперечной дислокации головного мозга в первые 24 ч от начала заболевания, а при повторной КТ головного мозга на 2-е сутки поперечная дислокация была менее 7 мм (в среднем 5 мм, см. рис. 1). У 6 (40%) больных уровень бодрствования при госпитализации соответствовал ясному сознанию, у 9 (60%) — оглушению. У всех больных отмечено прогрессирующее снижение уровня бодрствования на 4-е сутки от начала заболевания, на 5-е сутки у всех развилось коматозное состояние (см. рис. 3). При проведении КТ на 5-е сутки отмечены поперечная дислокация (в среднем 18 мм), деформация охватывающей цистерны, соответствующая 2-й и 3-й степени по классификации В.Н. Корниенко, выраженный отек интактного полушария в виде сужения или сглаженности конвекситальных субарахноидальных пространств (рис. 4). Из 15 больных с отсроченным течением ДС были прооперированы 3, летальность у оперированных больных составила 67%, у неоперированных — 100%.
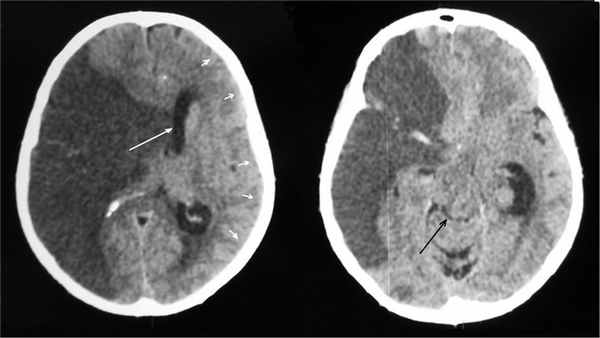
Рис. 4. КТ головного мозга больного 1-й группы с МИИ с отсроченным развитием ДС (5-е сутки от начала заболевания, угнетение уровня бодрствования до комы). Отмечаются смещение срединных структур влево на 16 мм (указано большой белой стрелкой), отек левого полушария в виде сужения конвекситальных субарахноидальных борозд (указано малыми белыми стрелками), видна деформация охватывающей цистерны 2-й степени по классификации В.Н. Корниенко (черная стрелка).
Летальность во 2-й группе составила 52%. В связи с тем что летальный исход у всех больных был обусловлен внечерепными причинами, течение ДС расценивали как благоприятное. У больных не было отмечено поперечной дислокации головного мозга в первые 24 ч от начала заболевания, а при повторной КТ головного мозга в промежуток от 24 до 48 ч от начала заболевания она в среднем составляла 2 мм. На 3-и сутки при повторной КТ латеральная дислокация в среднем достигала 6 мм. У 16 больных при КТ, проведенной на 4-е сутки от дебюта инсульта, латеральная дислокация не нарастала. У этих пациентов динамики уровня бодрствования также не наблюдали. У 7 больных латеральная дислокация продолжила нарастать и на 5-е сутки в среднем достигала 10 мм. У 3 больных с поперечной дислокацией, равной 11, 12 и 15 мм было отмечено угнетение уровня бодрствования до глубокого оглушения. У этих пациентов, несмотря на выраженную поперечную дислокацию, деформация охватывающей цистерны не превышала 1-й степени по классификации В.Н. Корниенко, отека интактного полушария не было (рис. 5). На 6-е сутки от дебюта инсульта по данным КТ латеральная дислокация не увеличивалась и не нарастала аксиальная дислокация. У больных отмечали восстановление уровня бодрствования до ясного сознания в среднем через 5 сут, на 11-е сутки от развития инсульта. В итоге все больные 2-й группы пережили ДС, а угнетение уровня бодрствования до оглушения как проявление субкомпенсации ДС наблюдалось только у 3 (13%) больных, у которых он оказался обратим при проведении консервативного лечения. Средние значения поперечной дислокации во 2-й группе составили 8 мм (4—15 мм), однако ни у одного больного поперечная дислокация не превышала 2 мм в первые 24 ч от начала инсульта или 7 мм в первые 48 ч (pp
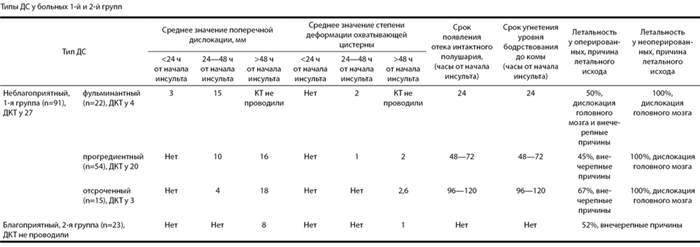
Типы ДС у больных 1-й и 2-й групп
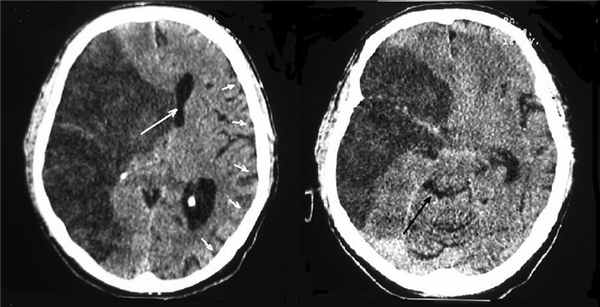
Рис. 5. КТ головного мозга больного 2-й группы с МИИ с благоприятным течением ДС (5-е сутки от начала заболевания, уровень бодрствования соответствует оглушению). Отмечается смещение срединных структур влево на 15 мм (белая стрелка). Отека левого полушария нет, конвекситальные субарахноидальные борозды не изменены (указаны малыми белыми стрелками), видна деформация охватывающей цистерны 1-й степени по классификации В.Н. Корниенко (черная стрелка).
Таким образом, на основании полученных данных нами были выявлены 2 типа ДС: благоприятный и неблагоприятный. Больные с благоприятным типом ДС пережили дислокацию головного мозга, а летальность у них определялась внечерепными осложнениями. У больных с неблагоприятным типом ДС были отмечены различные темпы его течения: фульминантный, прогредиентный и отсроченный. Больные с неблагоприятным типом ДС, которым не было проведено оперативное лечение, умерли от дислокации головного мозга. Летальность у прооперированных больных с неблагоприятным типом ДС составила 48%. Основными причинами летального исхода явились внечерепные осложнения. Таким образом, проведение ДКТ больным с МИИ с неблагоприятным типом течения ДС позволило уменьшить летальность на 52%.
Заключение
У больных со злокачественным течением МИИ риск летального исхода от височно-тенториального вклинения определяется не только выраженностью, но и темпом развития поперечной дислокации срединных структур головного мозга. ДС у больных со злокачественным течением МИИ может протекать по благоприятному и неблагоприятному типам. При неблагоприятном типе темп развития ДС может быть фульминантным, прогредиентным и отсроченным. Неблагоприятный тип течения ДС является абсолютным показанием к ДКТ.
Вклинение головного мозга
Дислокация головного мозга возникает при аномальном выпячивании мозговой ткани через отверстия ригидных преград внутри черепа (например, вклинение в тенториальную выемку), из-за повышенного внутричерепного давления.
После младенческого возраста череп становится жестким, поэтому внутричерепные объемные образования или отек мозга приводят к повышению ВЧД, что может стать причиной выпячивания (вклинения) ткани мозга через ригидные отверстия костей черепа или твердой мозговой оболочки (вырезка намета мозжечка, серп большого мозга, большое затылочное отверстие). При значительном повышении ВЧД, в независимости от причины этого явления, развивается рефлекс Кушинга и другие вегетативные нарушения. Рефлекс Кушинга включает в себя повышение систолического артериального давления и пульсового давления, нарушение дыхания и брадикардию.
Вклинение головного мозга может привести к гибели пациента.
Дислокацию головного мозга классифицируют в зависимости от анатомической структуры, через которую происходит выпячивание ткани. Типы дислокаций мозга включают следующее (см. рисунок Вклинение головного мозга [Brain herniation] Вклинение головного мозга Дислокация головного мозга возникает при аномальном выпячивании мозговой ткани через отверстия ригидных преград внутри черепа (например, вклинение в тенториальную выемку), из-за повышенного. Прочитайте дополнительные сведенияВосходящее транстенториальное вклинение
Вклинение миндалин мозжечка
Вклинение головного мозга
Повышенное внутричерепное давление иногда может стать причиной выпячивания (вклинения) ткани мозга через ригидные отверстия костей черепа или твердой мозговой оболочки (вырезка намета мозжечка, серп большого мозга, большое затылочное отверстие).
Дислокацию головного мозга классифицируют в зависимости от анатомической структуры, через которую происходит выпячивание ткани.
Транстенториальное (ункальное) вклинение: медиальная часть височной доли вклинивается унилатеральной массой сквозь и под мозжечковый намет, поддерживающий височную долю.
Подсерповидное вклинение : угловая извилина вклинивается под серп большого мозга при давлении на нее нарастающего очага в полушарии головного мозга.
Центральное вклинение: Грыжа обеих височных долей через вырезку намета мозжечка из-за билатеральных опухолевых эффектов или диффузного отека головного мозга.
Восходящее транстенториальное вклинение: этот тип развивается в том случае, когда субтенториальное объемное образование (например, опухоль в задней черепной ямке, внутримозговая гематома) сдавливает ствол головного мозга, что приводит к формированию множественных ишемических очагов в стволе.
Вклинение миндалин мозжечка: обычно связано с увеличивающимся инфратенториальным объемным образованием (например, кровоизлиянием в мозжечок), которое смещает миндалины мозжечка в большое затылочное отверстие.
Транстенториальное вклинение
Медиальная часть височной доли вклинивается унилатеральной массой сквозь и под мозжечковый намет, поддерживающий височную долю. При сдавлении поражаются следующие структуры:
Ипсилатеральный нерв III пары (как правило, он поражается первым) и задняя мозговая артерия
По мере прогрессирования вклинения, ипсилатеральная ножка мозга
У приблизительно 5% пациентов – контрлатеральный нерв III пары и ножка мозга
В конечном итоге, ствол головного мозга и области, окружающие таламус
Подсерповидное вклинение
Угловая извилина вклинивается под серп большого мозга при давлении на нее нарастающего очага в полушарии головного мозга. Вследствие этого сдавливаются одна или обе передние мозговые артерии, что приводит к инфаркту в парамедианной коре. По мере увеличения в размерах зоны инфаркта нарастает риск транстенториального и/или центрального вклинения.
Центральное вклинение
Обе височные доли смещаются через вырезку намета мозжечка вследствие билатеральных опухолевых эффектов или диффузного отека головного мозга. В конечном итоге наблюдается смерть мозга.
Восходящее транстенториальное вклинение
Восходящее транстенториальное вклинение развивается в том случае, когда субтенториальное объемное образование (например, опухоль в задней черепной ямке, внутримозговая гематома) сдавливает ствол головного мозга, что приводит к формированию множественных ишемических очагов в стволе. Сдавливаются задние отделы III желудочка. При этом виде вклинения также страдает кровоснабжение среднего мозга, сдавливаются вены Галена и Розенталя и развивается окклюзия верхних мозжечковых артерий с развитием инфаркта верхних отделов мозжечка.
Вклинение миндалин мозжечка
Обычно вклинение миндалин мозжечка связано с увеличивающимся инфратенториальным объемным образованием (например, кровоизлиянием в мозжечок). Миндалины мозжечка при вклинении в большое затылочное отверстие сдавливают ствол мозга и перекрывают ток спинномозговой жидкости (СМЖ).
Этиология
Дислокация головного мозга является осложнением заболевания, из-за которого повышается внутричерепное давление (ВЧД). Повышение внутричерепного давления может быть вызвано
Объёмные новообразования (например, опухоль головного мозга, отек или абсцесс, ушибы, гематомы)
Генерализованный отек головного мозга (например, в результате острой печеночной недостаточности или гипертонической энцефалопатии)
Повышенное венозное давление (например, вызванное сердечной недостаточностью, обструкцией верхних средостенных или яремных вен или тромбозом венозных синусов)
Нарушение циркуляции спинно-мозговой жидкости (например, в результате гидроцефалии или обширных поражениях твердой оболочки мозга)
Клинические проявления
Симптомы и признаки вклинения мозга перечислены в таблице ниже. Обычно у пациентов также наблюдаются признаки заболевания, которое вызывает дислокацию мозга; эти признаки могут быть неспецифическими (например, нарушение сознания, заторможеность).
Диагностика
После стабилизации состояния пациента, требуется визуализация головного мозга с помощью КТ или МРТ для выявления объемных новообразований, идентификации смещения ткани головного мозга и определения типа дислокации.
Лечение
Немедленное принятие мер для стабилизации состояния (по правилу ABC – обеспечение проходимости дыхательных путей, дыхания и кровообращения)
Госпитализация в отделение интенсивной терапии (ICU)
Поддерживающее лечение, включая контроль и коррекцию ВЧД
Лечение основного заболевания
Лечение вклинения головного мозга аналогично лечению комы Лечение Кома – это состояние ареактивности, из которого пациент не может быть выведен с помощью стимуляции и при котором глаза пациента остаются закрытыми. К другим нарушениям сознания относятся сходные. Прочитайте дополнительные сведенияСледует корректировать артериальную гипотонию. С целью мониторирования дыхания и неврологического статуса, пациента необходимо перевести в отделение интенсивной терапии.
Пациентов необходимо стабилизировать. Обеспечение проходимости дыхательных путей, дыхания и кровообращения должно проводиться незамедлительно.
При подозрении на повышенное ВЧД, следует интубировать пациента путём быстрой последовательной оральной интубации (используя миорелаксант), а не назотрахеальной; назотрахеальная интубация у пациента с самопроизвольным дыханием в большей степени вызывает кашель и рвоту, повышая тем самым ВЧД, которое и так повышено из-за внутричерепной патологии.
При повышенном ВЧД следует мониторировать показатели внутричерепного и церебрального перфузионного давления (см. Мониторинг внутричерепного давления [Intracranial Pressure Monitoring] Контроль внутричерепного давления (ВЧД) Мониторинг пациентов реанимационных отделений зависит от непосредственного наблюдения и объективного обследования и является периодическим, в зависимости от болезни пациента. Непрерывное наблюдение. Прочитайте дополнительные сведения Меры контроля ВЧД Контроль внутричерепного давления Кома – это состояние ареактивности, из которого пациент не может быть выведен с помощью стимуляции и при котором глаза пациента остаются закрытыми. К другим нарушениям сознания относятся сходные. Прочитайте дополнительные сведенияСедация: применение седативных средств может быть необходимым для контроля возбуждения, чрезмерной мышечной активности (например, при делирии) или боли, которые могут повысить ВЧД.
Гипервентиляция приводит к гипокапнии, которая вызывает сужение сосудов и глобальное снижение мозгового кровотока.
Восполнение потери жидкости: используются изотонические растворы. Поступление в организм свободной воды за счет внутривенного введения жидкости (например, 5%-го раствора глюкозы, 0,45%-го раствора натрия хлорида) может привести к усугублению отека головного мозга, поэтому такие растворы использовать не следует. Объем вводимой жидкости может быть до некоторой степени ограничен, но у пациентов должна поддерживаться эуволемия. При отсутствии признаков дегидратации или перегрузки жидкостью внутривенное введение жидкости может начинаться с физиологического раствора со скоростью 50–75 мл/ч. Скорость может быть увеличена или уменьшена в зависимости от содержания натрия в сыворотке, осмоляльности, количества выделяемой мочи и признаков задержки жидкости (например, отека).
Диуретики: осмоляльность сыворотки должна поддерживаться на уровне от 295 до 320 мОсмоль/кг. Осмотические диуретики (например, маннитол) могут вводиться внутривенно с целью снижения ВЧД и поддержания осмоляльности сыворотки крови. Эти препараты не проникают через гематоэнцефалический барьер. Они перемещают воду из тканей мозга в плазму за счет осмотического градиента, что в итоге приводит к достижению равновесия. При использовании осмотических диуретиков необходимо тщательно следить за балансом жидкости и электролитов. 3% физиологический раствор является еще одним потенциальным осмотическим агентом для контроля ВЧД (внутричерепного давления).
>Контроль артериального давления (АД): системные антигипертензивные средства необходимы только при тяжелой гипертонии (> 180/95 мм рт. ст.). Степень снижения артериального давления зависит от клинического контекста. Системное артериальное давление должно быть достаточно высоким, чтобы поддерживать церебральное перфузионное давление даже при повышенном ВЧД.
Кортикостероиды: лечение вазогенного отека кортикостероидами эффективно только при опухолях и иногда – при абсцессах головного мозга (вследствие нарушения гематоэнцефалического барьера). Кортикостероиды неэффективны при цитотоксическом отеке (возникающем в результате гибели и разрушения клеток) и могут повышать уровень глюкозы в плазме крови, усиливая церебральную ишемию.
Если ВЧД продолжает расти, несмотря на предпринятые меры по его контролю, можно использовать следующее:
Титрованная гипотермия: Когда ВЧД увеличивается вследствие травмы головы или остановки сердца, гипотермия в диапазоне от 32-35° C используется для уменьшения ВЧД до < 20 мм рт. ст. Однако использование гипотермии для снижения ВЧД является спорным; некоторые доказательства ( 1 Справочные материалы по лечению Дислокация головного мозга возникает при аномальном выпячивании мозговой ткани через отверстия ригидных преград внутри черепа (например, вклинение в тенториальную выемку), из-за повышенного. Прочитайте дополнительные сведенияПентобарбиталовая кома: Пентобарбитал может приводить к снижению церебрального кровотока и метаболических потребностей головного мозга. Тем не менее, его использование является спорным, поскольку лечение пентобарбиталом может привести к осложнениям (например, гипотонии) и конечный результат лечения не всегда является положительным. У некоторых пациентов с трудно поддающейся лечению внутричерепной гипертензией, которая не поддается стандартной гиперкапнической и гиперосмолярной терапии, лечение пентобарбиталом может улучшить функциональный результат.
Декомпрессивная краниотомия: для освобождения пространства при отеке мозга возможно проведение краниотомии с дурапластикой. Это вмешательство может предотвратить гибель пациента, однако общий функциональный исход заболевания может улучшиться в незначительной степени, также оно может приводить к осложнениям, таким как гидроцефалия у некоторых пациентов ( 2 Справочные материалы по лечению Кома – это состояние ареактивности, из которого пациент не может быть выведен с помощью стимуляции и при котором глаза пациента остаются закрытыми. К другим нарушениям сознания относятся сходные. Прочитайте дополнительные сведенияВклинение мозга при опухолевом поражении лечат вводимым внутривенно маннитолом в дозе 25–100 г, кортикостероидами (например, дексаметазон 16 мг внутривеннно, затем по 4 мг перорально или внутривенно каждые 6 часов), и таких пациентов интубируют. Гипервентиляция до парциального давления углекислого газа (PCO2) от 26 до 30 мм рт. ст. может помочь временно снизить ВЧД в чрезвычайных ситуациях. Как можно раньше проводят хирургическую декомпрессию, удаляя объемное образование.
Справочные материалы по лечению
Основные положения
Дислокация головного мозга является результатом повышенного внутричерепного давления (ВЧД), которое может быть вызвано объёмными новообразованиями, генерализованным набуханием или отеком мозга, повышенным венозным давлением или нарушением циркуляции спинно-мозговой жидкости (СМЖ).
Специфические симптомы варьируются в зависимости от того, какие структуры скомпрессированны; у пациентов также наблюдаются нарушения сознания и другие неврологические расстройства, вызванные заболеванием, приведшим к вклинению мозга.
После стабилизации состояния пациента сделайте визуализирующее исследование мозга.
Обеспечьте мониторинг и контроль ВЧД используя седативные препараты, эндотрахеальную интубацию, гипервентиляцию, регидратационную терапию, диуретики, меры по контролю артериального давления, и, в некоторых случаях, – кортикостероиды.
Лечение должно быть направлено на устранение причины.
Авторское право © 2022 Merck & Co., Inc., Rahway, NJ, США и ее аффилированные лица. Все права сохранены.
Анатомия бодрствования и сознания. Внутричерепная дислокация и вклинение
Facebook Если у вас не работает этот способ авторизации, сконвертируйте свой аккаунт по ссылке ВКонтакте Google RAMBLER&Co ID
Авторизуясь в LiveJournal с помощью стороннего сервиса вы принимаете условия Пользовательского соглашения LiveJournal
Entries by tag: внутричерепная гипертензия
Идиопатическая внутричерепная гипертензия
статью в формате PDF
Дефиниция. Идиопатическая внутричерепная гипертензия (ИВГ) - состояние, которое характеризуется повышением интракраниального (внутричерепного) давления, без наличия объемного образования, венозного тромбоза или инфекционного поражения головного мозга.
На сегодняшний день под первичным синдром ИВГ (истинная ИВГ) принято считать состояние, которое сопровождается повышением внутричерепного давления (ВЧД) без каких-либо этиологических факторов, возможно на фоне ожирения [90% женщин с ИВГ страдает ожирением] (см. далее раздел «этиология»). Для описания вторичного повышения ВЧД на фоне некоторых редких причин (см. далее раздел «этиология») используется термин «pseudotumor cerebri». Эпидемиологические исследования (см. далее) указывают на достоверно большую распространенность ИВГ по сравнению с pseudotumor cerebri, 90 и 10% соответственно.
Эпидемиология. ИВГ встречается во всех возрастных группах, в т.ч. в детском и пожилом возрасте (чаще всего - в возрасте 30 - 40 лет), у женщин - приблизительно в 8 раз чаще, чем у мужчин (1 случай на 100 тыс. населения и 19 случаев на 100 тыс. молодых женщин с избыточной массой тела). В настоящее время продолжается пересмотр данных по распространенности ИВГ, согласно базовому эпидемиологическому исследованию средняя ежегодная заболеваемость ИВГ составляет 2 случая на 100 000 населения. Нельзя исключить, что на фоне глобальной эпидемии ожирения распространенность ИВГ будет увеличиваться, особенно в целевой группе женщин молодого возраста.
Обратите внимание! Ранее синонимом «ИВГ» (помимо «pseudotumor cerebri») являлась «доброкачественная внутричерепная гипертензия (ДВЧГ)». В настоящее время от использования термина «ДВЧГ» (который ввел в практику Foley в 1955 г.) отказались, поскольку последний не точно отображает суть процесса. Доброкачественность заключается только в том, что это не опухолевый процесс. Учитывая резкое снижение зрительных функций при развитии вторичной атрофии зрительных нервов, о доброкачественности речь не идет ([ . ] при несвоевременной диагностике около 2% пациентов необратимо теряют зрение).
Этиология и патогенез ИВГ недостаточно изучены. Среди наиболее значимых предрасполагающих факторов отмечается роль ожирения, преимущественно у женщин молодого возраста (доказано, что снижение массы тела является одним из наиболее эффективных методов терапии ИВГ). Выявленная достоверная ассоциация ИВГ с избыточной массой тела ставит новые вопросы относительно патогенеза (патофизиологических механизмов) данного заболевания. Большинство теорий (патогенеза) сводится к обсуждению нарушений венозного оттока и/или абсорбции цереброспинальной жидкости (ЦСЖ). При этом не получено каких-либо доказательств, указывающих на ее избыточную секрецию. В настоящее время продолжается обсуждение роли венозных микротромбов, нарушения метаболизма витамина А, жиров и эндокринной регуляции обмена натрия и воды в развитии ИВГ. В последнее время в качестве возможного механизма развития ИВГ все чаще рассматривают интракраниальную венозную гипертензию, связанную с различными стенозами синусов твердой мозговой оболочки (Higgins, 2002; Ogungbo, 2003; Stranding, 2005) и приводящую к нарушению абсорбции ЦСЖ (ликвора). Сужение чаще всего встречается в дистальных отделах поперечного синуса либо в месте перехода поперечного синуса в сигмовидный с одной стороны, либо с обеих сторон.
Причину развития pseudotumor cerebri (вторичной внутричерепной гипертензии) связывают с рядом патологических состояний, перечень которых продолжает пополняться. Ведущее место отводят именно протромбофилическому статусу, перенесенным тромбозам синусов и центральных вен, дефициту протеинов C и S, постинфекционным (менингит, мастоидит) осложнениям. В редких случаях pseudotumor cerebri развивается во время беременности и при приеме оральных гормональных контрацептивов, в том числе вследствие нарушений системы гемостаза. Продолжает обсуждаться ассоциация некоторых метаболических и эндокринных расстройств с pseudotumor cerebri - болезнь Аддисона, гипер-, гипотиреоз, анемия, прием тетрациклинов, витамина А, солей лития и анаболических стероидов. В итоге можно выделить 5 основных этиологических групп вторичного синдрома pseudotumor cerebri: [1] нарушение или блок венозного оттока (внешняя или внутренняя компрессия, тромбофилии, системная патология, инфекционные причины); [2] эндокринные и метаболические причины (болезнь Аддисона, гипер-, гипотиреоз, дефицит витамина D); [3] прием лекарственных препаратов, токсических веществ (тетрациклины, амиодарон, циметидин, ретинол, циклоспорин, лития карбонат и др.); [4] на фоне отмены некоторых лекарственных средств (глюкокортикостероиды, гонадотропный гормон, даназол); [5] системные заболевания (саркоидоз, системная красная волчанка, тромбоцито-пеническая пурпура и др.).
Клиника. Синдром ИВГ характеризуется следующими признаками(Dandy, 1937, модификация Wall, 1991): [1] симптомы внутричерепной гипертензии (включая односторонний или двусторонний отек диска зрительного нерва); [ 2] при люмбальной пункции определяется повышение ВЧД выше 200 мм вод. ст.; [3] отсутствие очаговой неврологической симптоматики (за исключением, в некоторых случаях, пареза VI пары черепно-мозговых нервов); [4] отсутствие деформации, смещения или обструкции желудочковой системы; другой патологии головного мозга по данным магнитно-резонансной томографии, за исключением признаков повышения давления цереброспинальной жидкости; [5] несмотря на высокий уровень ВЧД, сознание пациента, как правило, сохранено; [6] отсутствие других причин повышения ВЧД.
Основным клиническим проявлением заболевания является головная боль (>90%) различной интенсивности. Для головной боли характерны все типичные черты цефалгического синдрома при повышении ВЧД: более выраженная интенсивность в утренние часы, тошнота, иногда рвота, усиление боли при кашле и наклоне головы. Согласно данным Международного общества головной боли, цефалгический синдром при ИВГ должен точно совпадать с дебютом заболевания и регрессировать по мере снижения ВЧД.
Транзиторные зрительные нарушения в виде потемнения (затуманивание) перед глазами встречаются в 35 - 72% случаев. Симптомы зрительных нарушений могут предшествовать головной боли, и в начале заболевания проявляться в виде эпизодов кратковременного затуманивания зрения, выпадения полей зрения или горизонтальной диплопии. Среди других клинических проявлений ИВГ отмечаются шум в голове (60%), фотопсии (54%), ретробульбарная боль (44%), диплопия (38%), прогрессирующее снижение зрения (26%). В неврологическом статусе иногда отмечаются признаки поражения VI пары, часто низкой степени выраженности в виде ограничения движения глазных яблок кнаружи. При офтальмоскопии выявляется двусторонний или односторонний отек диска зрительного нерва различной степени выраженности. В 10% случаев это приводит к необратимому снижению зрения, особенно при несвоевременно начатом лечении.
Диагностика. Алгоритм обследования пациентов с подозрением на ИВГ и pseudotumor cerebri включает в себя:
I. ИВГ с отеком диска зрительного нерва . A . Отек диска зрительного нерва. B . Отсутствие отклонений в невроло-гическом статусе, за исключением патологии черепных нервов (ЧМН). C . Данные магнитно-резонансной томографии (МРТ). Отсутствие изменений оболочек и паренхимы головного мозга по данным МРТ без/с контрастным усилением гадолинием для пациентов группы риска (молодые женщины с избыточной массой тела). Отсутствие отклонений по данным МРТ головного мозга без/с контрастного усиления гадолинием и МР-венографии во всех остальных группах пациентов. D . Нормальный состав ЦСЖ. E . Увеличение давления ЦСЖ при выполнении любмальной пункции >250 мм вод.ст. у взрослых и >280 вод. ст. у детей (>250 мм вод.ст. при выполнении люмбальной пункции без наркоза и у детей без избыточной массы тела). Диагноз ИВГ является достоверным при соблюдении всех критериев A - E. Диагноз ИВГ считается вероятным при положительных критериях A - D, но при меньшем, чем указано в пункте E, давлении ЦСЖ.
II. ИВГ без отека диска зрительного нерва . Диагностика ИВГ в случае отсутствия отека диска зрительного нерва возможна при соблюдении критериев B - E и выявлении признаков одно- или двустороннего поражения отводящего нерва. При отсутствии признаков отека зрительного нерва и пареза VI пары ЧМН диагноз ИВГ может быть только предположительным при условии выполнения пунктов B - E и дополнительных МР-критериев (минимум 3 из 4): «пустое турецкое седло»; уплощение задней поверхности глазного яблока; расширение периоптического субарахноидального пространства с (или без) повышенной извитостью зрительного нерва; стеноз поперечного синуса.
Лечение. Для эффективной терапии ИВГ должен быть использован мультидисциплинарный подход, который включает динамическое наблюдение невролога, офтальмолога, участие диетолога и реабилитолога. Пациентам обязательно необходимо объяснить высокий риск развития осложнений ИВГ, в первую очередь потери зрения, при отсутствии своевременной терапии. Основными направлениями консервативной терапии ИВГ является снижение массы тела (в т.ч. доказана эффективность бариатрической хирургии при ИВГ) и применение ингибитора карбоангидразы ацетазоламида (диакарб). Препаратами второй линии для фармакотерапии ИВГ являются топирамат, фуросемид и метилпреднизолон. Топирамат и петлевой диуретик фуросемид могут быть использованы при развитии нежелательных лекарственных реакций на фоне приема диакарба (парестезия, дисгевзия, утомляемость, снижение уровня CO 2 , тошнота, рвота, диарея и шум в ушах). Кроме того, следует учитывать снижение массы тела на фоне приема топирамата. Только в случае рефрактерности к лекарственной терапии или быстропрогрессирующем злокачественном течении ИВГ рассматривается вопрос оперативного нейрохирургического лечения с проведением шунтирования (относительно эффективности стентирования поперечных синусов у пациентов с ИВГ и стенозом или окклюзией по данным МР-венографии в настоящее время имеются противоречивые данные). Метод повторных люмбальных пункций в настоящее время используется достаточно редко.
Подробнее об ИВГ в следующих источниках:
статья «Идиопатическ ая внутричерепная гипертензия» А.В. Сергеев, ГБОУ ВПО «Первый Московский государственный медицинский университет им. И.М. Сеченова», Москва, Россия (Журнал неврологии и психиатрии, №5, 2016);
клинические рекомендации «Диагностика и лечение доброкачественной внутричерепной гипертензии», обсуждены и утверждены на Пленуме Правления Ассоциации нейрохирургов России г. Казань, 02.06.2015 [читать];
статья «Идиопатическая внутричерепная гипертензия и место ацетазоламида в лечении» Автор: Н.В. Пизова, д.м.н., проф. каф. неврологии и медицинской генетики с курсом нейрохирургии ГБОУ ВПО ЯГМУ (Consilium Medicum, Неврология и ревматология, №01 2016) [читать];
статья «Начальный опыт эндоваскулярного стентирования поперечного синуса при идиопатической внутричерепной гипертензии» А.Г. Луговский, М.Ю. Орлов, Ю.Р. Яроцкий, В.В. Мороз, И.И. Скорохода, Е.С. Егорова, ГУ «Институт нейрохирургии имеми акад. А.П. Ромоданова НАМН Украины», г. Киев (журнал «Ендоваскулярна нейрорентгенохірургія» №4, 2014) [читать];
статья «Доброкачественная внутричерепная гипертензия (pseudotumor cerebri)» Ю.С. Астахов, Е.Е. Степанова, В.Н. Бикмул-лин (РМЖ, «Клиническая Офтальмология» №1 от 04.01.2001 стр. 8) [читать];
статья «Доброкачественная внутричерепная гипертензия: клинические наблюдения» Р.В. Магжанов, А.И. Давлетова, К.З. Бахтиярова, Е.В. Первушина, В.Ф. Туник; ФГБОУ ВО «Башкирский государственный медицинский университет» Минздрава РФ, Уфа, Россия; ГБУЗ «Республиканская клиническая больница им. Г.Г. Куватова», Уфа, Россия (журнал «Анналы клинической и экспериментальной неврологии» №3, 2017 ) [читать]
Читайте также:
