Диагностика хронического миелолейкоза. Критерии ХМЛ
Добавил пользователь Валентин П. Обновлено: 24.01.2026
Стадия акселерации хронического миелолейкоза (ХМЛ) - клиника, анализы
В стадии акселерации хронического миелолейкоза (ХМЛ) у большинства больных нет новых характерных клинических симптомов или они выражены неотчетливо. Состояние больного, как правило, остается вполне удовлетворительным. Иногда появляются периодические небольшие «немотивированные» подъемы температуры тела, больной быстрее чувствует усталость при выполнении привычной работы, можно пальпировать прежде неуве-личенную селезенку.
Основной признак перехода заболевания в стадию акселерации — изменение картины крови, отражающее снижение чувствительности к проводимой и ранее эффективной терапии. Появляется тенденция к нарастанию количества лейкоцитов при терапии, которая до этого полностью контролировала лейкоцитоз, увеличивается количество миелоцитов и метамиелоцитов, появляются промиелоциты, часто — 2— 10 % бластных клеток.
Очень нередко происходит характерное изменение лейкоцитарной формулы: если ранее сумма зрелых гранулоцитов заметно превышала сумму незрелых, то в этой стадии ХМЛ прослеживается отчетливая тенденция к уравниванию суммы зрелых и незрелых гранулоцитов или преобладанию незрелых. У некоторых больных в это время миелоциты составляют 50—60 % от всех лейкоцитов крови. Нередко увеличивается количество базофилов, иногда значительно (до 30—50 %), особенно у больных, у которых и ранее отмечалась базофилия.
Больные с большим количеством базофилов нередко жалуются на кожный зуд, периодическое чувство жара и учащенный жидкий стул, что связано с увеличением в крови количества гистамина, продуцируемого базофилами. Увеличение дозы лечебного препарата не всегда ведет к снижению процента базофилов, что является плохим прогностическим признаком, нередко предвещающим скорое наступление терминальной стадии болезни.
Реже в стадии акселерации отмечается нарастающее увеличение количества эозинофилов или моноцитов.
Нередко в этой стадии, особенно в ее начале, количество тромбоцитов возрастает до 1500—2000 • 10 9 /л, иногда выше. Мы наблюдали двух больных, у которых в стадии акселерации число тромбоцитов достигало огромных цифр — в одном случае 6970•10 9 /л, в другом — 10 640•10 9 /л.
В то же время у ряда больных, наоборот, появляется тромбоцитопения с количеством тромбоцитов менее 100•10 9 /л и даже менее 50•10 9 /л.

Исследование костно-мозгового пунктата может не выявить каких-либо новых признаков или обнаружить некоторое увеличение бластных клеток — до 8—15 %. Как и в крови, отмечается увеличение количества молодых гранулоцитов — миелоцитов и промиелоцитов.
В позднем периоде стадии акселерации нередко появляются ноющие боли в костях или суставах, снижение массы тела, склонность к инфекционным «простудным» заболеваниям.
Цитогенетическое исследование в этой стадии чаще всего выявляет лишь t(9;22)(q34;q11), однако у некоторых больных, помимо t(9;22), обнаруживается небольшое количество (2—12 %) клеток с добавочными изменениями хромосом, чаще всего с добавочной Ph-хромосомой, трисомией хромосомы 8 или появлением изохромосомы 17q. Обнаружение даже небольшого числа этих клеток имеет неблагоприятное прогностическое значение, свидетельствуя о появлении нового, более злокачественного клеточного клона. Подтверждением этому является тот факт, что нередко в терминальной стадии преобладающим оказывается именно тот клон, который в небольшом проценте клеток определялся в фазе акселерации.
Существуют международные принятые признаки стадии акселерации:
1) обнаружение, помимо t(9;22), других хромосомных аберраций;
2) 10—15 % и более бластных клеток в крови;
3) 30 % и более в сумме бластных клеток и промиелоцитов в крови;
4) 20 % и более базофилов в крови;
5) количество тромбоцитов менее 100•10 9 /л, не обусловленное терапией;
6) увеличение размеров селезенки и числа лейкоцитов, не чувствительных к проводимой терапии.
Достаточно наличия одного из этих признаков для определения данной стадии.
Стадию акселерации удается диагностировать у 70—80 % больных. У 20—30 % ее проследить не удается, и переход в терминальную стадию совершается как бы внезапно, когда ни клинические симптомы, ни анализы крови еще за 1—2 нед до терминальной стадии не позволяли предполагать ее столь скорого развития. По нашим наблюдениям, внезапное развитие терминальной стадии часто наблюдается у больных с длительной (более 8—10 лет) хронической стадией болезни.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Хронический лейкоз
Хронический лейкоз – это первичное опухолевое заболевание системы кроветворения, субстратом которого выступают зрелые и созревающие клетки миелоидного или лимфоидного ряда. Различные формы хронического лейкоза протекают с преобладанием интоксикационного (слабость, артралгии, оссалгии, анорексия, похудание), тромбогеморрагического (кровоточивость, тромбозы различной локализации), лимфопролиферативного синдромов (увеличение лимфоузов, спленомегалия и др.). Решающее значение в диагностике хронического лейкоза принадлежит исследованию ОАК, биоптатов костного мозга и лимфоузлов. Лечение хронических лейкозов проводится методами химиотерапии, лучевой терапии, иммунотерапии, возможна трансплантация костного мозга.
МКБ-10
Общие сведения
Хронический лейкоз – хронические лимфопролиферативные и миелопролиферативные заболевания, характеризующиеся избыточным увеличением количества кроветворных клеток, сохраняющих способность к дифференцировке. В отличие от острых лейкозов, при которых происходит пролиферация низкодифференцированных гемопоэтических клеток, при хронических лейкозах опухолевый субстрат представлен созревающими или зрелыми клетками. Для всех типов хронических лейкозов характерна длительная стадия доброкачественной моноклоновой опухоли.
Хронические лейкозы поражают преимущественно взрослых в возрасте 40-50 лет; мужчины болеют чаще. На долю хронического лимфоидного лейкоза приходится около 30% случаев, хронического миелоидного лейкоза - 20% всех форм лейкемии. Хронический лимфолейкоз в гематологии диагностируется в 2 раза чаще, чем хронический миелолейкоз. Лейкозы у детей протекают в хроническом варианте крайне редко - в 1-2% случаев.
Причины
Истинные причины, приводящие к развитию хронического лейкоза, неизвестны. В настоящее время наибольшее признание получила вирусно-генетическая теория гемобластозов. Согласно данной гипотезе, некоторые виды вирусов (в числе которых – вирус Эбштейна-Барр, ретровирусы и др.) способны проникать в незрелые кроветворные клетки и вызывать их беспрепятственное деление.
Не подвергается сомнению и роль наследственности в происхождении лейкозов, поскольку доподлинно известно, что заболевание нередко носит семейный характер. Кроме этого, хронический миелолейкоз в 95% случаев ассоциирован с аномалией 22-й хромосомы (филадельфийской или Рh-хромосомы), фрагмент длинного плеча которой транслоцирован на 9-ю хромосому.
Факторы риска
Наиболее значимыми предрасполагающими факторами к различным видам и формам хронических лейкозов выступают воздействия на организм:
- высоких доз радиации;
- рентгеновского облучения;
- производственных химических вредностей (лаков, красок и др.);
- лекарственных препаратов (солей золота, антибиотиков, цитостатиков);
- длительный стаж курения.
Риск развития хронического лимфоцитарного лейкоза повышается при длительном контакте с гербицидами и пестицидами, а хронического миелоидного лейкоза – при радиационном облучении.
Патогенез
В патогенезе хронического лимфолейкоза значимая роль принадлежит иммунологическим механизмам – об этом свидетельствует его частое сочетание с аутоиммунной гемолитической анемией и тромбоцитопенией, коллагенозами. Вместе с тем, у большинства больных хроническими лейкозами причинно значимых факторов выявить не удается.
Классификация
В зависимости от происхождения и клеточного субстрата опухоли хронические лейкозы делятся на:
- Лимфоцитарные: хронический лимфолейкоз, болезнь Сезари (лимфоматоз кожи), волосатоклеточный лейкоз, парапротеинемические гемобластозы (миеломная болезнь, макроглобулинемия Вальденстрема, болезни легких цепей, болезни тяжелых цепей).
- Миелоцитарные (гранулоцитарные): хронический миелолейкоз, эритремия, истинная полицитемия, хронический эритромиелоз и др.
- Моноцитарные: хронический моноцитарный лейкоз и гистиоцитозы.
В своем развитии опухолевый процесс при хроническом лейкозе проходит две стадии: моноклоновую (доброкачественную) и поликлоновую (злокачественную). Течение хронического лейкоза условно подразделяется на 3 стадии: начальную, развернутую и терминальную.

Симптомы хронического лейкоза
Хронический миелоидный лейкоз
В начальном периоде хронического миелолейкоза клинические проявления отсутствуют или неспецифичны, гематологические изменения выявляются случайно при исследовании крови. В доклиническом периоде возможно нарастание слабости, адинамии, потливости, субфебрилитета, болей в левом подреберье.
Переход хронического миелоидного лейкоза в развернутую стадию знаменуется прогрессирующей гиперплазией селезенки и печени, анорексией, похуданием, выраженными болями в костях и артралгиями. Характерно образование лейкемических инфильтратов на коже, слизистых полости рта (лейкемический периодонтит), ЖКТ. Геморрагический синдром проявляется гематурией, меноррагией, метроррагией, кровотечениями после экстракции зубов, кровавыми поносами. В случае присоединения вторичной инфекции (пневмонии, туберкулеза, сепсиса и др.) температурная кривая приобретает гектический характер.
Терминальная стадия хронического миелоидного лейкоза протекает с резким обострением всех симптомов и выраженной интоксикацией. В этот период может развиваться плохо поддающееся терапии и угрожающее жизни состояние – бластный криз, когда из-за резкого увеличения количества бластных клеток течение заболевания становится похожим на острый лейкоз. Для бластного криза характерна агрессивная симптоматика: лейкемиды кожи, тяжелые кровотечения, вторичные инфекции, высокая температура, возможен разрыв селезенки.
Хронический лимфолейкоз
Долгое время единственным признаком хронического лимфолейкоза может быть лимфоцитоз до 40-50%, незначительное увеличение одной-двух групп лимфоузлов. В развернутый период лимфаденит принимает генерализованную форму: увеличиваются не только периферические, но и медиастинальные, мезентериальные, забрюшинные узлы. Возникает сплено- и гепатомегалия; возможно сдавление холедоха увеличенными лимфатическими узлами с развитием желтухи, а также верхней полой вены с развитием отеков шеи, лица, рук (синдром ВПВ). Беспокоят упорные оссалгии, кожный зуд, рецидивирующие инфекции.
Тяжесть общего состояния больных хроническим лимфоидным лейкозом обусловлена прогрессированием интоксикации (слабость, потливость, лихорадка, анорексия) и анемического синдрома (головокружение, одышка, сердцебиение, обморочные состояния).
Терминальная стадия хронического лимфоидного лейкоза характеризуется присоединением геморрагического и иммунодефицитного синдромов. В этот период развивается тяжелая интоксикация, возникают кровоизлияния под кожу и слизистые, носовые, десневые, маточные кровотечения.
Осложнения
Иммунодефицит, обусловленный неспособностью функционально незрелых лейкоцитов выполнять свои защитные функции, проявляется синдромом инфекционных осложнений. У больных хроническим лимфолейкозом часты легочные инфекции (бронхиты, бактериальные пневмонии, туберкулезные плевриты), грибковые поражения кожи и слизистых, абсцессы и флегмоны мягких тканей, пиелонефриты, герпетическая инфекция, сепсис.
Нарастают дистрофические изменения внутренних органов, кахексия, почечная недостаточность. Летальный исход при хроническом лимфоидном лейкозе наступает от тяжелых инфекционно-септических осложнений, кровотечений, анемии, истощения. Возможна трансформация хронического лимфолейкоза в острый лейкоз или лимфосаркому (неходжкинскую лимфому).
Диагностика
Предполагаемый диагноз устанавливается на основании анализа гемограммы, с результатами которой пациент должен быть немедленно направлен к врачу-гематологу. Для подтверждения диагноза проводится:
- Общий анализ крови. Типичные для хронического миелоидного лейкоза изменения включают: анемию, присутствие единичных миелобластов и гранулоцитов на разной стадии дифференцировки; в период бластного криза количество бластных клеток увеличивается более чем на 20%. При хроническом лимфолейкозе определяющими гематологическими признаками выступают выраженный лейкоцитоз и лимфоцитоз, наличие лимфобластов и клеток Боткина-Гумпрехта.
- Пункции и биопсии. С целью определения морфологии опухолевого субстрата показано выполнение стернальной пункции, трепанобиопсии, биопсии лимфоузлов. В пунктате костного мозга при хроническом миелолейкозе увеличено количество миелокариоцитов за счет незрелых клеток гранулоцитарного ряда; в трепанобиоптате определяется замещение жировой ткани миелоидной. При хроническом лимфоидном лейкозе миелограмма характеризуется резким усилением лимфоцитарной метаплазии.
- Инструментальные исследования. Для оценки выраженности лимфопролиферативного синдрома применяются УЗИ лимфатических узлов, селезенки, рентгенография грудной клетки, лимфосцинтиграфия, МСКТ брюшной полости и ряд других.
Лечение хронического лейкоза
На ранней доклинической стадии лечение неэффективно, поэтому больные подлежат динамическому наблюдению. Общережимные мероприятия предполагают исключение физических перегрузок, стрессов, инсоляции, электропроцедур и теплолечения; полноценное витаминизированное питание, длительные прогулки на свежем воздухе.
В развернутом периоде миелолейкоза назначается химиотерапевтическое лечение (бусульфан, митобронитол, гидроксимочевина и др.), при выраженной спленомегалии проводится облучение селезенки. Подобная тактика, хоть и не приводит к полному излечению, но существенно тормозит прогрессирование болезни и позволяет отсрочить наступление бластного криза. Кроме медикаментозной терапии, при хроническом миелоцитарном лейкозе используются процедуры лейкафереза. В ряде случаев излечение достигается с помощью трансплантации костного мозга.
При переходе хронического миелолейкоза в терминальную стадию назначается высокодозная полихимиотерапия. В среднем после установления диагноза больные хроническим миелолейкозом живут 3-5 лет, в отдельных случаях – 10-15 лет. Также проводится цитостатическая терапия (хлорбутин, циклофосфамид), иногда в сочетании со стероидной терапией, облучением лимфоузлов, селезенки, кожи. При значительном увеличении селезенки выполняется спленэктомия. Применяется трансплантация стволовых клеток, однако ее эффективность еще требует подтверждения.

Прогноз
Продолжительность жизни больных хроническим лимфоидным лейкозом может составлять от 2-3 лет (при тяжелых, неуклонно прогрессирующих формах) до 20-25 лет (при относительно благоприятном течении).
Хронический миелолейкоз
Хронический миелолейкоз – это злокачественное миелопролиферативное заболевание, характеризующееся преимущественным поражением гранулоцитарного ростка. Может долгое время протекать бессимптомно. Проявляется склонностью к субфебрилитету, ощущением полноты в животе, частыми инфекциями и увеличением селезенки. Наблюдаются анемия и изменение уровня тромбоцитов, сопровождающиеся слабостью, бледностью и повышенной кровоточивостью. На заключительной стадии развиваются лихорадка, лимфоаденопатия и кожная сыпь. Диагноз устанавливается с учетом анамнеза, клинической картины и данных лабораторных исследований. Лечение – химиотерапия, радиотерапия, пересадка костного мозга.
Хронический миелолейкоз – онкологическое заболевание, возникающее в результате хромосомной мутации с поражением полипотентных стволовых клеток и последующей неконтролируемой пролиферацией зрелых гранулоцитов. Составляет 15% от общего количества гемобластозов у взрослых и 9% от общего числа лейкозов во всех возрастных группах. Обычно развивается после 30 лет, пик заболеваемости хроническим миелолейкозом приходится на возраст 45-55 лет. Дети до 10 лет страдают исключительно редко.
Хронический миелолейкоз одинаково распространен у женщин и у мужчин. Из-за бессимптомного или малосимптомного течения может становиться случайной находкой при исследовании анализа крови, взятого в связи с другим заболеванием или во время профилактического осмотра. У части больных хронический миелолейкоз выявляется на заключительных стадиях, что ограничивает возможности терапии и ухудшает показатели выживаемости. Лечение проводят специалисты в области онкологии и гематологии.
Хронический миелолейкоз считается первым заболеванием, при котором достоверно установлена связь между развитием патологии и определенным генетическим нарушением. В 95% случаев подтвержденной причиной хронического миелолейкоза является хромосомная транслокация, известная как «филадельфийская хромосома». Суть транслокации заключается во взаимной замене участков 9 и 22 хромосом. В результате такой замены формируется устойчивая открытая рамка считывания. Образование рамки вызывает ускорение деления клеток и подавляет механизм восстановления ДНК, что увеличивает вероятность возникновения других генетических аномалий.
В числе возможных факторов, способствующих появлению филадельфийской хромосомы у больных хроническим миелолейкозом, называют ионизирующее облучение и контакт с некоторыми химическими соединениями.
Итогом мутации становится усиленная пролиферация полипотентных стволовых клеток. При хроническом миелолейкозе пролиферируют преимущественно зрелые гранулоциты, но аномальный клон включает в себя и другие клетки крови: эритроциты, моноциты, мегакариоциты, реже – В- и Т-лифоциты. Обычные гемопоэтические клетки при этом не исчезают и после подавления аномального клона могут служить основой для нормальной пролиферации кровяных клеток. Для хронического миелолейкоза характерно стадийное течение.
- При первой, хронической (неактивной) фазе отмечается постепенное усугубление патологических изменений при сохранении удовлетворительного общего состояния.
- Во второй фазе хронического миелолейкоза – фазе акселерации изменения становятся явными, развиваются прогрессирующие анемия и тромбоцитопения.
- Заключительной стадией хронического миелолейкоза является бластный криз, сопровождающийся быстрой экстрамедуллярной пролиферацией бластных клеток.
Источником бластов становятся лимфатические узлы, кости, кожа, ЦНС и т. д. В фазе бластного криза состояние больного хроническим миелолейкозом резко ухудшается, развиваются тяжелые осложнения, завершающиеся гибелью больного. У некоторых пациентов фаза акселерации отсутствует, хроническая фаза сразу сменяется бластным кризом.
Симптомы хронического миелолейкоза
Клиническая картина определяется стадией заболевания. Хроническая фаза в среднем продолжается 2-3 года, в некоторых случаях – до 10 лет. Для этой фазы хронического миелолейкоза характерно бессимптомное течение или постепенное появление «легких» симптомов: слабости, некоторого недомогания, снижения трудоспособности и чувства переполнения живота. При объективном осмотре больного хроническим миелолейкозом может обнаруживаться увеличение селезенки. По анализам крови выявляется повышение количества гранулоцитов до 50-200 тыс./мкл при бессимптомном течении заболевания и до 200-1000 тыс./мкл при «легких» признаках.
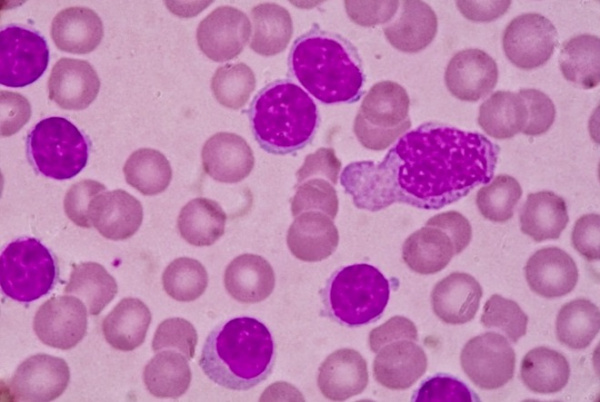
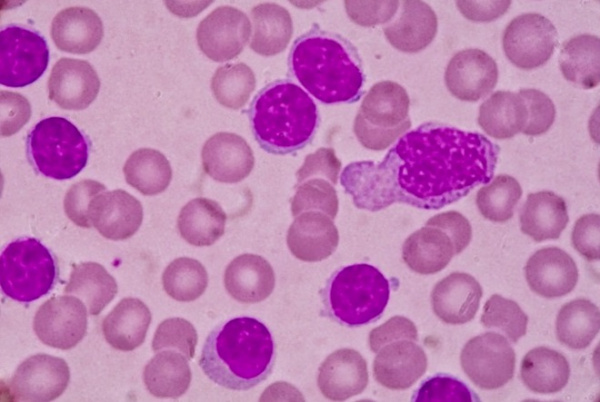
На начальных стадиях хронического миелолейкоза возможно некоторое снижение уровня гемоглобина. В последующем развивается нормохромная нормоцитарная анемия. При исследовании мазка крови пациентов с хроническим миелолейкозом отмечается преобладание молодых форм гранулоцитов: миелоцитов, промиелоцитов, миелобластов. Наблюдаются отклонения от нормального уровня зернистости в ту или иную сторону (обильная или очень скудная). Цитоплазма клеток незрелая, базофильная. Определяется анизоцитоз. При отсутствии лечения хроническая фаза переходит в фазу акселерации.
О начале фазы акселерации может свидетельствовать как изменение лабораторных показателей, так и ухудшение состояния пациентов. Возможно нарастание слабости, увеличение печени и прогрессирующее увеличение селезенки. У больных хроническим миелолейкозом выявляются клинические признаки анемии и тромбоцитопении или тробоцитоза: бледность, быстрая утомляемость, головокружения, петехии, кровоизлияния, повышенная кровоточивость. Несмотря на проводимое лечение, в крови пациентов с хроническим миелолейкозом постепенно увеличивается количество лейкоцитов. При этом отмечается возрастание уровня метамиелоцитов и миелоцитов, возможно появление единичных бластных клеток.
Бластный криз сопровождается резким ухудшением состояния больного хроническим миелолейкозом. Возникают новые хромосомные аномалии, моноклоновое новообразование трансформируется в поликлоновое. Отмечается нарастание клеточного атипизма при угнетении нормальных ростков кроветворения. Наблюдаются ярко выраженные анемия и тромбоцитопения. Суммарное количество бластов и промиелоцитов в периферической крови составляет более 30%, в костном мозге – более 50%. Пациенты с хроническим миелолейкозом теряют вес и аппетит. Возникают экстрамедуллярные очаги незрелых клеток (хлоромы). Развиваются кровотечения и тяжелые инфекционные осложнения.
Диагноз устанавливается на основании клинической картины и результатов лабораторных исследований. Первое подозрение на хронический миелолейкоз часто возникает при повышении уровня гранулоцитов в общем анализе крови, назначенном в порядке профилактического осмотра или обследования в связи с другим заболеванием. Для уточнения диагноза могут использоваться данные гистологического исследования материала, полученного при стернальной пункции костного мозга, однако окончательный диагноз «хронический миелолейкоз» выставляется при выявлении филадельфийской хромосомы при помощи ПЦР, флюоресцентной гибридизации или цитогенетического исследования.
Вопрос о возможности постановки диагноза хронический миелолейкоз при отсутствии филадельфийской хромосомы остается дискутабельным. Многие исследователи считают, что подобные случаи могут объясняться комплексными хромосомными нарушениями, из-за которых выявление данной транслокации становится затруднительным. В ряде случаев филадельфийскую хромосому можно обнаружить при использовании ПЦР с обратной транскрипцией. При отрицательных результатах исследования и нетипичном течении заболевания обычно говорят не о хроническом миелолейкозе, а о недифференцированном миелопролиферативном/миелодиспластическом расстройстве.
Лечение хронического миелолейкоза
Тактику лечения определяют в зависимости от фазы заболевания и выраженности клинических проявлений. В хронической фазе при бессимптомном течении и слабо выраженных лабораторных изменениях ограничиваются общеукрепляющими мероприятиями. Больным хроническим миелолейкозом рекомендуют соблюдать режим труда и отдыха, принимать пищу, богатую витаминами и т. д. Лечение может включать:
- Монохимиотерапию. При повышении уровня лейкоцитов используют бусульфан. После нормализации лабораторных показателей и уменьшения селезенки пациентам с хроническим миелолейкозом назначают поддерживающую терапию или курсовое лечение бусульфаном. При бластных кризах осуществляют лечение гидроксикарбамидом.
- Радиотерапию. Облучение обычно используют при лейкоцитозе в сочетании со спленомегалией. При снижении уровня лейкоцитов делают паузу продолжительностью не менее месяца, а затем переходят на поддерживающую терапию бусульфаном. Радиотерапию также назначают при хлоромах.
- Полихимиотерапию. В прогрессирующей фазе хронического миелолейкоза возможно использование одного химиопрепарата или полихимиотерапии. Применяют митобронитол, гексафосфамид или хлорэтиламиноурацил. Как и в хронической фазе, проводят интенсивную терапию до стабилизации лабораторных показателей, в последующем переходят на поддерживающие дозы. Курсы полиохимиотерапии при хроническом миелолейкозе повторяют 3-4 раза в год.
- Гемокоррекцию. При неэффективности терапии используют лейкоцитаферез. При выраженной тромбоцитопении, анемии выполняют переливания тромбоконцентрата и эритроцитарной массы.
- ТКМ.Пересадку костного мозга проводят в первой фазе хронического миелолейкоза. Продолжительной ремиссии удается достичь у 70% пациентов.
- Удаление селезенки. При наличии показаний осуществляют спленэктомию. Экстренная спленэктомия показана при разрыве или угрозе разрыва селезенки, плановая – при гемолитических кризах, «блуждающей» селезенке, рецидивирующих периспленитах и резко выраженной спленомегалии, сопровождающейся нарушением функций органов брюшной полости.
Прогноз при хроническом миелолейкозе зависит от множества факторов, определяющим из которых является момент начала лечения (в хронической фазе, фазе активации или в период бластного криза). В качестве неблагоприятных прогностических признаков хронического миелолейкоза рассматривают значительное увеличение печени и селезенки (печень выступает из-под края реберной дуги на 6 и более см, селезенка – на 15 и более см), лейкоцитоз свыше 100x10 9 /л, тромбоцитопению менее 150x10 9 /л, тромбоцитоз более 500х10 9 /л, повышение уровня бластных клеток в периферической крови до 1% и более, повышение суммарного уровня промиелоцитов и бластных клеток в периферической крови до 30% и более.
Вероятность неблагоприятного исхода при хроническом миелолейкозе возрастает по мере увеличения количества признаков. Причиной гибели становятся инфекционные осложнения или тяжелые геморрагии. Средняя продолжительность жизни пациентов с хроническим миелолейкозом составляет 2,5 года, однако при своевременном начале терапии и благоприятном течении заболевания этот показатель может увеличиваться до нескольких десятков лет.
Диагностика хронического миелолейкоза. Критерии ХМЛ
Диагностика хронического миелолейкоза - анализы
Клинигеский анализ крови при хроническом миелолейкозе. В периферической крови на момент диагностики выявляется лейкоцитоз, обычно более 50 • 10 9 /л (возможен и более низкий уровень лейкоцитов — 15-20 • 109/л) со сдвигом влево за счет палочкоядерных нейтрофилов, метамиелоцитов, миелоцитов, редко — промиелоцитов.
Могут выявляться единичные бластные клетки (прогностически неблагоприятный признак). Характерна эозинофильно-базофильная ассоциация — увеличение количества эозинофилов и базофилов, часто морфологически аномальных. В 30% случаев определяется нормохромная нормоцитарная анемия легкой степени, у 30% больных выявляется тромбоцитоз; реже — тромбоцитопения (неблагоприятный признак).
Миелограмма при хроническом миелолейкозе. При исследовании миелограммы (которая не всегда необходима для постановки диагноза) выявляются гиперклеточный костный мозг и гиперплазия нейтрофильного ростка (лейкоэритробластическое соотношение достигает 10-20:1 и более). Гранулоциты при хроническом миелолейкозе обладают практически нормальной фагоцитарной и бактерицидной активностью.
Количество клеток базофильного и эозинофильного рядов увеличено, нередко встречаются аномальные формы; возможен мегакариоцитоз.
Гистологигеское исследование костного мозга при хроническом миелолейкозе. При исследовании костного мозга методом трепанобиопсии выявляется его гиперклеточность и выраженная миелоидная гиперплазия (лейко-эритробластическое соотношение более 10:1); количество предшественников эритроцитов уменьшено. Мегакариоцитоз отмечается у 40-50%, возможен морфологический атипизм клеток. При прогрессировании (фаза акселерации) нередко развивается ретикулиновый, реже — коллагеновый фиброз костного мозга.
Цитогенетическое и молекулярно-генетическое исследование при хроническом миелолейкозе. При цитогенетическом исследовании у 95-97% больных выявляется Ph-хромосома. При отсутствии Ph-хромосомы методом флюоресцентной гибридизации in situ (FISH) можно обнаружить 1 клетку с транслокацией BCR-ABL на 200-500 нормальных клеток. Метод удобен для мониторинга минимальной остаточной болезни, выполняется на образцах периферической крови, цитологических и морфологических препаратах крови и костного мозга, срезах гистологических препаратов.
Для диагностики и мониторирования заболевания используется также ПЦР, которая позволяет выявить одну патологическую клетку среди 10 4 -10 6 нормальных.
При отрицательных результатах обоих методов (цитогенетического и молекулярно-генетического) диагностируется один из вариантов МДС/МПЗ.
При молекулярно-генетических исследованиях у больных в фазе акселерации и бластном кризе выявляются повреждения ряда генов (ТР53, RBI, MYC, RAS, pl6, AML1, EVI1), однако их роль в трансформации заболевания пока не установлена.

Биохимические исследования при хроническом миелолейкозе. Характерно увеличение уровня сывороточного витамина В12 и витамин В12-связывающей способности сыворотки крови вследствие увеличенной продукции транскобаламина гранулоцитами. Повышенное разрушение клеток приводит к гиперурикемии, особенно при цитостатической терапии. Может выявляться также повышение железосвязывающей способности сыворотки крови, уровня гистамина, снижение лейцинаминопептидазы.
Диагноз хронического миелолейкоза ставится на основании клинико-лабораторных данных (спленомегалия, лейкоцитоз со сдвигом в лейкоцитарной формуле влево и наличием промежуточных форм нейтрофилов, эозинофильно-базофильная ассоциация, усиленный миелопоэз в костном мозге, низкий уровень щелочной фосфатазы нейтрофилов) и подтверждается обнаружением Ph-хромосомы, t(9;22)(q34;qll.2) или гена BCR-ABL (цитогенетическими или молекулярно-генетическими методами).
Выделяют 3 стадии хронического миелолейкоза: хроническую, фазу акселерации и бластный криз.

Критерии для определения стадии хронического миелолейкоза (ВОЗ)
- Хроническая фаза хронического миелолейкоза: нет признаков других фаз заболевания; нет симптомов (после лечения).
- Фаза акселерации (при наличии одного и более признаков) хронического миелолейкоза:
1) 10-19% бластов в крови или костном мозге;
2) количество базофилов в периферической крови не менее 20%;
3) персистирующая тромбоцитопения (меньше 100 • 10 9 /л), не связанная с лечением, или персистирующий тромбоцитоз больше 1000 • 10 9 /л, резистентный к терапии;
4) нарастающие спленомегалия и лейкоцитоз, резистентные к терапии (удвоение количества лейкоцитов меньше 5 дней);
5) новые хромосомные изменения (появление нового клона).
Наряду с одним из вышеперечисленных признаков фазы акселерации обычно выявляется пролиферация мегакариоцитов, ассоциирующаяся с ретикулиновым или коллагеновым фиброзом, или выраженная дисплазия гранулоцитарного ростка.
- Бластный криз хронического миелолейкоза:
1) не менее 20% бластов в крови или костном мозге;
2) экстрамедуллярная пролиферация властных клеток;
3) большое количество агрегатов бластных клеток в трепанобиоптате.
Основной лабораторный признак фазы акселерации и бластного криза — прогрессирующее увеличение промиелоцитов и бластов в периферической крови и костном мозге. При цитохимических исследованиях в фазе бластного криза у 70% пациентов определяется миелоидный, у 30% — лимфоидный вариант, которые имеют сходные черты соответственно с ОМЛ и ОЛЛ:
а) средний возраст больных с лимфоидным кризом меньше, чем больных с миелоидным;
б) нейролейкоз чаще развивается у больных с лимфоидным кризом;
в) непосредственные результаты лечения при лимфоидном варианте криза существенно лучше.
Диагноз хронического миелолейкоза (ХМЛ) в большинстве случаев установить или, во всяком случае, заподозрить нетрудно по характерным изменениям картины крови. Эти изменения выражаются в постепенно нарастающем лейкоцитозе, небольшом в начале заболевания (10— 15 • 10 9 /л) и достигающем по мере течения болезни без лечения огромных цифр — 200—500—800 • 10 9 /л и даже более.
Одновременно с нарастанием числа лейкоцитов отмечаются характерные изменения лейкоцитарной формулы: увеличение содержания гранулоцитов до 85—95 %, наличие незрелых гранулоцитов — миелоцитов, метамиелоцитов, при значительном лейкоцитозе — нередко промиелоцитов, а иногда единичных бластных клеток. Очень характерно увеличение содержания базофилов до 5—10 %, нередко с одновременным повышением уровня эозинофилов до 5—8 % («эозинофильно-базофильная ассоциация», не встречающаяся при других заболеваниях) и уменьшением числа лимфоцитов до 10—5 %.
Иногда количество базофилов достигает значительных цифр— 15—20 % и более.
В литературе 15—20-летней давности в таких случаях заболевание обозначалось как базофильный вариант хронического миелолейкоза, который встречается у 5—8 % больных. Описан эозинофиль-ный вариант, при котором в крови постоянно 20— 40 % эозинофилов. В настоящее время эти варианты не выделяют, а увеличение числа базофилов или эозинофилов рассматривается как признак продвинутой стадии болезни.
У большинства больных увеличено количество тромбоцитов до 400—600 • 10 9 /л, а иногда и более — до 800—1000 • 10 9 /л, редко — еще выше. Содержание гемоглобина и эритроцитов может долго оставаться нормальным, снижаясь только при очень высоком лейкоцитозе. У некоторых больных в начале заболевания наблюдается даже небольшой эритроцитоз — 5,0-5,5•10 12 л.
Исследование костно-мозгового пунктата обнаруживает увеличение числа миелокариоцитов и процента незрелых гранулоцитов с увеличением миелоидно/эритроидного соотношения до 20—25/1 вместо нормального 3—4/1. Обычно увеличено количество базофилов и эозинофилов, особенно у больных с высоким содержанием этих клеток в крови. Как правило, отмечается большое количество фигур митоза.
У некоторых больных, чаще при значительном гиперлейкоцитозе, в костно-мозговом пунктате обнаруживаются голубые гистиоциты и клетки, напоминающие клетки Гоше. Это макрофаги, захватывающие глюкоцереброзиды из распадающихся лейкоцитов. Число мегакариоцитов обычно увеличено, как правило, они имеют признаки дисплазии.
При морфологическом исследовании не обнаруживается каких-либо изменений в строении клеток гранулоцитарного ряда при ХМЛ по сравнению с нормальными, однако при электронной микроскопии выявляется асинхронизм в созревании ядра и цитоплазмы: на каждом этапе созревания гранулоцита ядро отстает в своем развитии от цитоплазмы.
Из цитохимических особенностей очень характерно резкое снижение или полное исчезновение щелочной фосфатазы в нейтрофилах крови и костного мозга.
При трепанобиопсии обнаруживаются выраженная гиперплазия миелоидного ростка, резкое уменьшение содержания жира, у 20—30 % больных уже в начале заболевания — та или иная степень миелофиброза.
Морфологическое исследование селезенки обнаруживает инфильтрацию красной пульпы лейкемическими клетками.
Из биохимических изменений характерным является увеличение содержания витамина В12 в сыворотке крови, которое превышает нормальное иногда в 10—15 раз и нередко остается повышенным при клинико-гематологической ремиссии. Другое существенное изменение — увеличение содержания мочевой кислоты. Оно оказывается высоким практически у всех нелеченых больных при значительном лейкоцитозе и может повышаться еще больше при проведении цитостатической терапии.
У некоторых больных постоянное повышение уровня мочевой кислоты приводит к образованию уратовых мочевых камней и подагрических артритов, отложению кристаллов мочевой кислоты в тканях ушных раковин с образованием видимых узелков. У подавляющего числа больных отмечается высокий уровень лактатдегидрогеназы сыворотки.
Начало заболевания в большинстве случаев почти или совсем бессимптомно. Обычно при уже появившихся изменениях крови селезенка не увеличена. По мере развития болезни она прогрессивно увеличивается, иногда достигая огромных размеров. Лейкоцитоз и размеры селезенки не всегда коррелируют между собой. У некоторых больных селезенка занимает всю левую половину живота, спускаясь в малый таз, при лейкоцитозе 65—70 • 10 9 /л, у других больных с лейкоцитозом, достигающим 400—500 • 10 9 /л, селезенка выступает из-под края реберной дуги всего на 4—5 см. Большие размеры селезенки особенно характерны для ХМЛ с высокой базофилией.
При выраженной спленомегалии обычно увеличена и печень, но всегда в значительно меньшей степени, чем селезенка. Увеличение лимфатических узлов для ХМЛ не характерно, оно встречается иногда в терминальной стадии болезни и обусловлено инфильтрацией лимфатического узла бластными клетками.
Жалобы на слабость, чувство тяжести, иногда боли в левом подреберье, потливость, субфебрильную температуру появляются только при развернутой клинической и гематологической картине заболевания.
У 20—25 % больных ХМЛ выявляется случайно, когда еще нет клинических признаков болезни, а имеются лишь нерезко выраженные гематологические изменения (лейкоцитоз и небольшой процент незрелых гранулоцитов в крови), которые обнаруживают при анализе крови, сделанном по поводу другого заболевания или при профилактическом обследовании. Отсутствие жалоб и клинических симптомов иногда приводит к тому, что характерные, но умеренные изменения крови, к сожалению, не привлекают внимания врача, и истинное начало заболевания удается установить лишь ретроспективно при обращении больного с уже выраженной клинико-гематологической картиной болезни.
Подтверждением диагноза ХМЛ является обнаружение в клетках крови и костного мозга характерного цитогенетического маркера — Ph-хромосомы. Этот маркер имеется у всех больных ХМЛ и не встречается при других заболеваниях.
Хронический миелолейкоз — первое онкологическое заболевание, при котором у человека были описаны специфические изменения хромосом и расшифрованы молекулярные механизмы, лежащие в основе развития болезни.
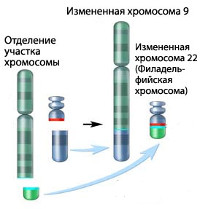
В 1960 г. два цитогенетика из г. Филадельфии в США P. Nowell и D. Hungerford у всех обследованных ими больных ХМЛ обнаружили укорочение длинного плеча одной из, как они ошибочно считали, хромосом 21-й пары. По названию города, где было сделано открытие, эта хромосома была названа филадельфийской, или Ph-хромосомой. В 1970 г., используя более совершенную технику окрашивания хромосом, Т. Caspersson и соавт. установили, что при ХМЛ имеется делеция длинного плеча одной из хромосом, не 21-й, а 22-й пары. Наконец, в 1973 г. было сделано важнейшее открытие, ставшее отправной точкой в исследовании патогенеза ХМЛ: J. Rowley показала, что образование Ph-хромосомы обусловлено реципрокной транслокацией (взаимный обмен частью генетического материала) между хромосомами 9 и 22.
При такой транслокации происходит перенос большей части длинного плеча хромосомы 22 на длинное плечо хромосомы 9, а маленькой терминальной части длинного плеча хромосомы 9 — на хромосому 22. В результате возникает характерная цитогенетическая аномалия — удлинение длинного плеча одной из хромосом 9-й пары и укорочение длинного плеча одной из хромосом 22-й пары. Именно эта хромосома из 22-й пары с укороченным длинным плечом и обозначается как Ph-хромосома.
К настоящему времени установлено, что Ph-хромосома — t(9;22)(q34;q11) обнаруживается в 95— 100 % метафаз у 90-95 % больных ХМЛ. Примерно в 5 % случаев выявляются вариантные формы Ph-хромосомы. Чаще всего это сложные транслокации, вовлекающие хромосомы 9, 22 и какую-либо третью хромосому, а иногда добавочно 2 или 3 хромосомы. При сложных транслокациях всегда имеются такие же молекулярные изменения, как при стандартной t(9;22)(q34;q11). Стандартные и вариантные транслокации могут одновременно обнаруживаться у одного и того же больного в разных метафазах.
Иногда встречается так называемая маскированная транслокация с такими же, как при типичной, молекулярными изменениями, но не определяемая обычными цитогенетическими методами. Это обусловлено переносом меньших, чем при стандартной транслокации, участков хромосом. Описаны также случаи, когда при обычном цитогенетиче-ском исследовании не обнаруживается t(9; 22), однако методом FISH или RT-PCR (ПЦР в реальном времени) удается установить, что в типичном участке хромосомы 22 имеется стандартная для ХМЛ перестройка генов — образование химерного гена BCR-ABL. Исследования таких случаев показали, что иногда происходит перенос участка хромосомы 9 на хромосому 22, но отсутствует транслокация участка хромосомы 22 на хромосому 9.
В начальном периоде цитогенетического изучения хронического миелолейкоза выделяли два его варианта — Ph-позитивный и Ph-негативный. Впервые Ph-негативный ХМЛ описан S. Krauss и соавт. в 1964 г.. Авторы обнаружили Ph-негативный ХМЛ почти у половины больных, которых они наблюдали. В дальнейшем по мере совершенствования методов исследования доля Ph-негативного ХМЛ неуклонно сокращалась. В настоящее время признается, что истинного Ph-негативного (BCR-ABL-негативного) ХМЛ не существует, а описанные ранее наблюдения в большинстве случаев относились к BCR-ABL-позитивному ХМЛ, но с таким типом хромосомных перестроек, которые не могли быть выявлены известными в то время цитогенетическими методами.
Таким образом, полученные к настоящему времени данные позволяют считать, что во всех случаях ХМЛ существуют изменения хромосом 9 и 22 с одинаковой перестройкой генов в определенной области хромосомы 22. В тех случаях, когда характерных цитогенетических изменений не удается обнаружить, речь идет о других заболеваниях, похожих на ХМЛ по клиническим проявлениям (спленомегалия) и картине крови (гиперлейкоцитоз, нейтрофилез). Чаще всего это хронический миеломоноцитарный лейкоз (ХММЛ), который в классификации ВОЗ 2001 г. относится к болезням, имеющим как миелопролиферативные, так и миелодиспластические черты. При ХММЛ всегда повышено количество моноцитов в крови и костном мозге.
При хроническом миелолейкозе у многих больных обнаруживаются транслокации с участием хромосомы 5: t(5;7), t(5;10), t(5;12), при которых образуются слитные гены, вовлекающие расположенный на хромосоме 5 ген PDGFbR (ген b-рецептора ростового фактора, продуцируемого тромбоцитами, — platelet-derived growth factor receptor b). Продуцируемый этим геном белок имеет домен с функцией тирозинкиназы, активирующейся при транслокации, чем обусловлен нередко значительный лейкоцитоз.
При наличии лейкоцитоза, нейтрофилеза и молодых форм гранулоцитов в крови, дисплазии всех ростков миелопоэза, но отсутствии моноцитоза заболевание, согласно классификации ВОЗ, обозначают как атипичный ХМЛ, также рассматриваемый в рубрике миелодиспластических/миелопролиферативных болезней. В 25—40 % случаев это заболевание, как и другие формы миелодиспластических синдромов, заканчивается острым лейкозом. Характерных цитогенетических изменений не обнаруживается.
К этой же категории болезней в настоящее время отнесен и так называемый ювенильный ХМЛ, который встречается в основном у детей моложе 14 лет, причем у мальчиков вдвое чаще, чем у девочек. Для этого заболевания обычны низкое содержание гемоглобина, эритроцитов и тромбоцитов, повышенное количество моноцитов, в крови нередко присутствуют бластные клетки и нет базофилии и эозинофилии. В костном мозге часто увеличено содержание моноцитов и бластных клеток. Уровень щелочной фосфатазы нейтрофилов нормальный или повышен. Характерны сплено- и гепатомегалия и лимфаденопатия. Цитогенетическое исследование не обнаруживает Ph-хромосомы или гена BCR-ABL. У 30—40 % больных имеется характерная для миелодиспластических синдромов моносомия хромосомы 7.
Похожим на хронический миелолейкоз по уровню лейкоцитоза и гепатоспленомегалии является и так называемый хронический нейтрофильный лейкоз (ХНЛ). Это редкое заболевание (всего описано не более 100 случаев), при котром в отличие от ХМЛ в крови даже при высоком лейкоцитозе обычно очень небольшое количество незрелых элементов миелоидного ряда. Специфических хромосомных изменений при ХНЛ неизвестно.
Читайте также:
