Гемангиома печени. Гемангиосаркома печени.
Добавил пользователь Валентин П. Обновлено: 27.01.2026
Сегодня основной метод лечения злокачественных новообразований печени при первичных опухолях и метастазах колоректального рака – анатомическая лапароскопическая резекция печени. Такая методика используется в странах Западной Европы, в Израиле, в США и в LISOD. При метастазах других видов рака применяют атипичную резекцию, радиочастотную абляцию.
Рак печени или печеночноклеточный рак – злокачественная опухоль, которая локализуется в печени. Новообразование происходит из клеток печени или является метастазом другой (первичной) опухоли. Метастазы в печени развиваются намного чаще, чем первичные опухоли. Это связано с характером кровообращения и функцией печени в организме. Метастазы злокачественного новообразования – это тяжелое осложнение, которое более опасно, чем сама первичная опухоль. Метастатический рак выявляют как метастазы злокачественной опухоли при ее первичной локализации в других органах.
Первичный рак печени имеет следующие типы: гепатоцеллюлярная карцинома, ангиопластическая саркома (ангиосаркома), гепатобалстома и гемангиосаркома, холангиокарционома.
Саркома печени — редкое и опасное заболевание. Очень быстро происходит развитие опухоли, распространение на соседние органы. Особенностью сарком является их возникновение преимущественно у людей молодого возраста и у детей. В частности, ангиосаркома печени – это редкая форма злокачественной опухоли. Новообразование имеет агрессивное течение, проявляется инвазивным, очень быстрым ростом, метастазирует.
Холангиокрацинома или рак желчного протока может развиться как в области печени, так и за пределами органа. Опухоль может образоваться в любой части протока. В зависимости от локализации образования существуют три группы: рак внутрипеченочных протоков, рак желчного протока в области ворот печени, рак дистальных желчных протоков.
Причины и механизм развития заболевания еще недостаточно изучены. Исследовалось влияние географического положения, климата, рациона питания, некоторых медицинских препаратов. У больных алкоголизмом первичный печеночноклеточный рак нередко развивается на фоне цирроза. Рак печени может обнаружиться в любом возрасте, чаще им заболевают после 40 лет.
Диагностика
В LISOD для диагностики рака печени применяют современные методы, соответствующие международным медицинским стандартам.
Ультразвуковое исследование (УЗИ) позволяет обнаружить опухоль и в некоторых случаях определить ее тип.
Биопсия опухоли является наиболее достоверным методом диагностики рака печени. Как правило, применяют тонкую длинную иглу, которую вводят через кожу в печень в область опухоли под контролем УЗИ-аппарата. Если во время исследования участка новообразования под микроскопом обнаруживают раковые клетки, диагноз рака печени считается подтвержденным.
Компьютерная томография (КТ) очень эффективна при диагностике опухолей печени, позволяет обнаружить даже маленькие новообразования, незаметные на УЗИ. В LISOD для улучшения изображения проводится КТ с контрастированием – внутривенно вводится контрастное вещество, что дает возможность специалистам изучить расположение сосудов в печени. Во время компьютерной томографии аппарат получает изображение тонких срезов, что позволяет специалистам тщательно обследовать структуру органа и выявить даже небольшие опухоли.
Лапароскопия. Лапароскопический метод позволяет поставить точный и правильный диагноз. Метод щадящий, быстрый и безболезненный. Через небольшой разрез, под короткодействующим наркозом, врач вводит специальный прибор в брюшную полость, осматривает опухоль (на мониторе) и берет кусочек ткани на исследование.
Исследование крови. Определение уровней альфа-фетопротеина (АФП) в крови полезно как на этапе диагностики опухолей печени, так и после лечения для контроля эффективности терапии и возможного рецидива заболевания.
Лечение
Полную информацию о диагностике и лечении этого вида рака Вам предоставят консультанты Информационной службы LISOD:
- 0-800-500-110 (бесплатно для звонков со стационарных телефонов по Украине)
- или +38 044 520 94 00 – ежедневно с 08:00 до 20:00.
Прежде всего, врачи уточняют диагноз опухоли и степень ее распространения. План лечения разрабатывается на междисциплинарной онкологической конференции.
Если опухоль операбельна, то начинается подготовка к серьезному хирургическому вмешательству. Удаление метастазов в печени – эффективный метод лечения. Печень «умеет» регенерироваться, и удаленная часть постепенно восстанавливается. Таким образом, ведущим методом остается радикальное оперативное вмешательство (например, гемигепатэктомия или атипичные резекции печени) в сочетании с последующей химиотерапией.
Радиотерапия также применяется в лечении рака печени, лечении метастазов в печень, так как снижает темпы роста опухоли. Радиотерпия – эффективный метод лечения метастазов в печени. Радиотерапия может быть использована в сочетании с хирургическим лечением либо с химиотерапией. Эмболизация печеночной артерии подразумевает блокировку артериальной крови, которая переносится к карциноидным опухолям с последующим проведением химиотерапии для уменьшения размеров оставшихся очагов.
Ранее выявление болезни является залогом успешного лечения. Операция, проведенная на ранних стадиях рака печени, как правило, дает хорошие результаты.
Симптомы
Рак печени симптомы проявляет, как правило, на фоне хронических болезней (вирусный гепатит, цирроз и т.д.). В результате, на признаки уже существующего недуга накладываются новые.
Появление боли в животе или ее усиление – симптом рака, часто свидетельствующий о больших размерах новообразования или его распространения за пределы печени.
Ощущение тяжести в правом подреберье может быть признаком рака печени.
Повышенная температура тела (выше 37.5 градусов Цельсия), которая держится длительное время и не объясняется другими причинами.
Появление водянки (асцит) – это скопление в брюшной полости жидкости, возникающее при раке печени и циррозе. Т.е. появление асцита у больного с циррозом может быть как осложнением основной болезни, так и признаком рака печени.
Желтуха – пожелтение склер глаз, слизистых оболочек и кожи тела. Возникает при разных состояниях, но, в том числе, при циррозе и при раке печени. Желтуха у больного может проявляться как осложнение цирроза, но так же может быть признаком рака печени.
Вздутие живота, снижение массы тела, отсутствие аппетита, выраженная слабость – это симптомы рака печени, но могут встречаться и при других болезнях.
Факторы риска
Известны факторы риска, которые могут способствовать развитию рака печени.
Пол. Мужчины болеют чаще, чем женщины. Возможно, это связано с большим употреблением ими алкоголя.
Заболевания печени. Хроническая инфекция (гепатит С или В) – очень значимый фактор риска. Есть некоторые наследственные заболевания, которые повышают вероятность возникновения рака печени.
Цирроз. Болезнь, развивающаяся в результате формирования в печени рубцовой ткани и часто приводящая к раку. Наиболее существенные причины цирроза – употребление алкоголя и заболевание гепатитом С и В. Другая причина – это накопление в печени избыточного количества железа.
Употребление табака. Доказана связь между курением и возникновением рака печени. При сопутствующем употреблении алкоголя риск увеличивается.
Афлатоксины. Употребление продуктов, которые из-за неправильного хранения поражены афлотоксином В1(митотоксин гриба Аspergilis flavus), повышает риск заболевания. К таким продуктам относятся: пшеница, рис, кукуруза, соевые бобы, земляные орехи и пр.
Анаболические стероиды – это мужские гормоны, которые иногда используют спортсмены. Их длительное применение может несколько увеличить риск развития злокачественной опухоли печени.
Мышьяк. Есть страны, где употребляется вода, загрязненная мышьяком, что повышает риск возникновения рака печени.
Профилактика
Основными мерами профилактики рака печени являются:
- своевременная вакцинация от гепатита В;
- своевременное и качественное лечение гепатита В и С;
- лечение алкоголизма и полный отказ от алкоголя;
- регулярное наблюдение у гепатолога для больных циррозом и хроническими вирусными гепатитами (не реже 2-3 раз в год).
Особое значение имеет борьба с алкоголизмом, поскольку цирроз печени (особенно крупноузловая форма) обнаруживают примерно у 60-90% больных с гепатомой.
Вопросы и ответы
В разделе публикуются вопросы пациентов и ответы наших специалистов. Вопрос каждого человека касается конкретной проблемы, связанной с его заболеванием. Пациентам отвечают израильские клинические онкологи и главный врач LISOD, д.м.н., профессор Алла Винницкая.
Ответы специалистов основаны на знаниях принципов доказательной медицины и профессиональном опыте. Ответы соответствуют исключительно предоставленным сведениям, имеют ознакомительный характер и не являются врачебной рекомендацией.
Основная цель раздела – дать информацию пациенту и его семье, чтобы вместе с лечащим врачом принять решение о виде лечения. Предложенная Вам тактика лечения может отличаться от принципов, изложенных в ответах наших специалистов. Не стесняйтесь задать лечащему врачу вопрос о причинах отличий. Вы должны быть уверены, что получаете правильное лечение.
Без гистологической верификации диагноза (биопсии) ничего определенного сказать нельзя. Это может быть первичная опухоль печени (печеночноклеточная или из желчных протоков), может быть вторичная опухоль (метастаз) из другого источника, или другая, более «экзотическая» опухоль. Параллельно следует сделать стадирование (определить распространенность процесса). После того как у нас будет гистологический диагноз и понятие о том местный ли это процесс или распространенный (метастатический) можно будет выстраивать план лечения.
Дорогая Людмила! Гемангиома - это доброкачественное образование из кровеносных сосудов. Оно не требует лечения при расположении в печени. Для дифференциальной диагностики от опухоли возможно проведение МРТ печени или сканирования с меченными радиоизотопом эритроцитами. Судя по тому что вы описываете (образования в печени и Th11 без динамики с марта 2010) речь не идет об онкологическом заболевании. Находка в 11 грудном позвонке может быть простым так называемым "костным островком".
Гемангиома печени. Гемангиосаркома печени.
Гемангиома печени. Гемангиосаркома печени.
Представлена одиночными, реже множественными четко отграниченными узлами багрово-синюшного цвета, нередко располагающимися под капсулой печени. Микроскопически узлы чаще всего имеют строение кавернозной гемангиомы.
Инфантильная гемангиоэндотелиома макроскопически выглядит в виде солитарных или множественных, не имеющих капсулы узлов, диаметром 0,5—15 см, желтоватого или багрово-синюшного цвета, губчатого вида, с зонами уплотнения или обызвествления в центре. Обычно наблюдают у грудных детей до 6 мес, часто сочетается с врожденными пороками развития, преимущественно сердца и нервной системы, а также с множественными гемангиомами кожи (45%) или других органов и тканей. Микроскопически опухоль представлена большим количеством взаимосвязанных, переплетающихся сосудистых каналов, более крупных сосудов и сосудистых пространств, заполненных кровью и выстлапных эндотелиальными клетками.
Последние могут располагаться в один или несколько слоев либо выступают в просвет в виде псевдососочков. Ядра разнообразны по форме, чаще гиперхромные. Фигуры митоза встречаются редко. При наличии большого их количества, а также атипии и полиморфизма следует провести дифференциальный диагноз с гемангиосаркомой. Между сосудистыми элементами выявляют пролиферирующие желчные протоки или островки печеночных клеток. Разрастаясь опухоль может замещать всю ткань печени. В редких случаях описано ее метастазирование.
Гемангиосаркома (гемангиоэндотелиома, ангиобластическая саркома, ангиопластическая саркома, ангиосаркома, саркома из клеток Кунфера, первичная саркома, метастазирующая гемангиома, злокачественная гемангиоэндотелиома, эндотелиобластома, эндотелиома и др.) - злокачественная опухоль, представленная клетками вытянутой формы, выстилающими просветы предсущеетвующих сосудистых пространств, таких как печеночные синусоиды или мелкие вены, или растущими внутри них. Чаще встречается у мужчин пожилого возраста, нередко в цирротически измененной печени. Макроскопически обнаруживают множество нечетко очерченных геморрагических узлов, иногда с полостями, напоминающими кавернозную гемангиому. Описаны случаи, когда опухолевые узелки сливаются друг с другом, вовлекая в процесс всю ткань печени.
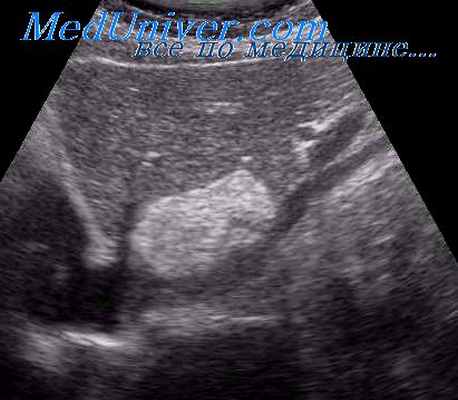
Микроскопически видны вытянутой формы опухолевые клетки с нечеткими ядрами; клетки образуют неправильно сформированные сосудистые полости. Часть клеток набухшая, иногда видны причудливые или многоядерные клетки, фигуры митоза. Клетки врастают в окружающуюткань по поверхности предсуществующих печеночных трабекул, которые подвергаются атрофии. С помощью импрегнации выявляют большое количество аргирофильных волокон. Местами встречаются солидные поля из вытянутых клеток. Такие участки трудно отличить от фибросаркомы. Нередко отмечают признаки экстрамедуллярного кроветворения.
Дифференциальный диагноз в основном должен проводиться с инфантильной гемангиоэндотелиомой и карциномой с обширными очагами некроза и кровоизлиянии.
Эмбриональная, или «недифференцированная» саркома печени (недифференцированная мезенхимальная саркома, мезенхимома)- злокачественная опухоль, представленная недифференцированной соединительной тканью. Встречается преимущественно у детей 5—10 лет. Макроскопически это четко отграниченная опухоль диаметром 10—18 см с участками кистозного строения, зонами кровоизлияний и некроза. Микроскопически опухолевая ткань состоит из анаплазированных недифференцированных клеток звездчатой, округлой или вытянутой формы, рыхло лежащих в отечном миксоидном матриксе и напоминающих эмбриональную мезенхиму. Иногда встречаются уродливые и многоядерные формы. Часто среди опухолевой ткани обнаруживают сформированные желчные протоки и кистозные полости, выстланные кубическим или уплощенным эпителием без признаков опухолевой трансформании.
На ультраструктурном уровне характерно наличие недифференцированных мезенхимальных клеток, в некоторых из которых могут отмечаться начальные признаки липобластической и фибробластической дифференцировки. Дифференциальный диагноз необходимо проводить с мезенхимальной гамартомой печени. При обнаружении в клетках опухоли поперечной исчерченности ее следует верифицировать как рабдомиосаркому.
В литературе описаны отдельные наблюдения некоторых доброкачественных (например, липома, ангиомиолипома, мезотелиома) и злокачественных неэпителиальных опухолей (лейомиосаркома, фибросаркома, остеогенная саркома и др.), гистологическое строение которых совпадает с таковым у аналогичных опухолей, имеющих типичную для них локализацию.
Тератома печени — редко встречающаяся опухоль, которая, согласно классификации ВОЗ, состоит, как правило, из нескольких типов тканей, производных различных зародышевых листков. Обычно встречается у детей до 3 лет и у женщин. Может протекать доброкачественно или злокачественно. До настоящего времени в литературе описано около 15 наблюдений тератомы печени (в большинстве из них обнаруживалась зрелая тератома).
Карциносаркома — опухоль, представленная сочетанием элементов рака (гепатоцеллюлярного или холангиокарциномы) и саркоматозных элементов. Эту опухоль следует отличать от анаплазированных форм рака.
Другие типы опухолей. Крайне редко встречаются первичные новообразования печени, имеющие строение карциноидов, опухолей надпочечников, хорионэпителиомы, опухоли желточного мешка и др.
Дисплазия печеночных клеток — многоочаговый процесс, характеризующийся увеличением размеров печеночных клеток (как ядра, так и цитоплазмы). Нередко встречаются двуядерные, реже многоядерные клетки, часто отмечают полиморфизм и гиперхроматоз ядер.
Аномалии желчного протока. Согласно классификации ВОЗ, к ним относят гиперплазию, метаплазию и дисплазию желчного протока, которые отмечают вокруг опухолевых узлов при паразитарных заболеваниях, образовании камней и т. д.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Гемангиома печени

Гемангиома печени – опухолевое образование доброкачественного характера, которое появляется на одной или обеих долях внутреннего органа. В среднем, размер новообразования достигает 5 см.
Классификация
В мировой медицинской практике существует несколько разновидностей данной опухоли:
- кавернозная гемангиома печени, представляющая собой сразу несколько свободных полостей, соединяющихся в единую;
- капиллярная гемангиома печени образует большое число маленьких полостей, в каждой из которых размещается кровеносный или венозный сосуд.
Наряду с самыми распространенными также могут встречаться венозная, гроздевидная гемангиома, гемангиоэндотелиома.
Симптоматика недуга
Симптомы гемангиомы печени появляются далеко не сразу. Из-за небольших размеров образования даже в лабораторных условиях не всегда можно заметить наличие новых клеток. Это же касается клинических проявлений.
При разрастании опухоли до размеров от 10 см можно обнаружить нехарактерные для здорового состояния особенности:
- увеличение печени в объемах;
- тошнота, небольшая рвота;
- неприятные, болезненные ощущения под ребрами с правой стороны.
Все эти симптомы возникают в результате того, что новообразование давит на соседние органы и сдавливает расположенные рядом сосуды.
В некоторых случаях гемангиома печени может проявить себя после травмы живота (например, сильного удара) или интенсивной физической нагрузки тела. Разорвавшись от натуги, она вызывает внутреннее кровотечение и острую боль в области живота.
Причины появления
Признаки гемангиомы печени может ощутить на себе абсолютно каждый человек вне зависимости от возраста или пола. Тем не менее, отмечено, что у женщин она может разрастаться интенсивнее ввиду повышенного уровня гормона эстрогена.
Несмотря на огромное количество проведенных исследований данного образования, точная причина его появления до сих пор не выявлена. Ученые-медики считают, что предпосылки формируются еще во внутриутробном периоде развития плода.
Существует мнение о том, что разрастание клеток, образующих впоследствии гемангиому печени, активизируется в результате перенесенных организмом кровоизлияний, а также склонности к увеличению капиллярных и венозных сосудов и тромбозам.
Диагностика образования
В исключительно резких случаях, лишь при случайном стечении обстоятельств, гемангиома печени у ребенка или взрослого может быть обнаружена на ранней стадии. В подавляющем большинстве случаев ее находят, когда размеры достигают серьезных объемов.
В качестве методов диагностики применяются следующие:
- и печени (может показать опухоль круглой формы с четкими границами); (помимо очертаний образования покажет и его содержимое); (послойно продемонстрирует границы и содержимое опухоли).
При обнаружении опухоли необходимо определить ее качественные особенности. Для подтверждения гемангиомы проводится ангиография чревного ствола, может также понадобиться статическая сцинтиграфия печени. Чтобы определить степень доброкачественности (злокачественности) атипичных клеток, назначается гепатосцинтиграфия.
Наряду с этим проводятся клинические анализы:
- печеночные пробы; , биохимия крови;
- анализ крови на генетические маркеры.
Особенности лечения
Методика избавления от новообразования во многом зависит от его размеров и формы.
Небольшие опухоли (до 5-6 см в объеме) не требуют особенных действий. За ними осуществляется наблюдение и УЗ-контроль спустя 3 месяца с момента обнаружения. При отсутствии какой-либо динамики ультразвуковая диагностика назначается каждые 6-12 месяцев.
Необходимость в хирургическом удалении определяется индивидуально. К такому ходу событий приводят:
- стремительное разрастание гемангиомы печени – более чем на 50% от первоначальных размеров за год;
- объем более 5-6 см;
- кровотечение атипичной ткани;
- агрессивное проявление симптомов;
- неточное определение доброкачественности опухоли.
Питание
Питание при гемангиоме печени играет существенную роль в избавлении от нее. Пациенту в обязательном порядке назначается диета, чтобы не спровоцировать ухудшение ситуации (резкое разрастание атипичных клеток).
Диета при гемангиоме печени у взрослых и детей подразумевает исключение из рациона таких продуктов, как:
- газированные напитки;
- алкоголь и слабоалкогольные напитки;
- любой шоколад;
- яичные желтки;
- острые специи;
- груши, дыни;
- свежий хлеб.
Следует ограничить потребление жирной, жареной, копченой, соленой пищи.
Вместо этого необходимо сделать упор на:
- нежирные сорта рыбы;
- печень;
- молочные продукты;
- вязкие каши;
- овощи;
- не кислые фрукты.
Может быть дополнительно назначен прием витамина В12.
Ответы на распространенные вопросы
Какая профилактика при гемангиомах?
Так как точная причина появления гемангиомы не определена, грамотной профилактической мерой является проведение один раз в год ультразвуковой диагностики печени. При наличии каких-либо сомнений следует дополнительно сделать КТ или МРТ.
Обязательно ли соблюдать диету при гемангиоме печени?
Правильный подбор питания обязателен в случае, если пациент настроен на положительный результат. Употребление недопустимых в рационе заболевшего продуктов может спровоцировать резкий рост и разрыв гемангиомы.
Чем опасна гемангиома печени?
Ее главная опасность заключается в возможном разрыве тканей и последующим за ним кровотечением. Также существует вероятность, что из-за больших размеров опухоли будут сдавлены соседние органы, в связи с чем будет нарушена их работа.
Как лечить гемангиому печени?
Лечение данного недуга подбирается в зависимости от его размеров и скорости разрастания. Специалист может подобрать гормональную терапию, малоинвазивные методы (например, лучевую терапию), а также хирургическое вмешательство. Для закрепления эффекта от лечения необходимо соблюдать специальную диету.
Новообразования печени. Диагностика и лечение
Опухоли печени имеют значительную распространенность среди собак и кошек. По данным Денисенко В.Н. и Кесаревой Е.А. (2003) они встречаются у 4.4% собак, поступивших в клинику с признаками функциональных расстройств печени. Нами, за период с 2002 по октябрь 2009 г., они выявлены у 7% собак и 3% кошек поступивших в клинику с признаками патологий печени.
Из проведенных в нашей клинике 7500 онкологических операций 44 были сделаны по поводу новообразований печени, что составляет менее 1%.
Ткань печени могут поражать как первичные, так и вторичные опухоли. Метастатическое поражение печени по данным различных авторов встречается в 2.5 – 30 раз чаще первичных новообразований печени (4,6,7). Такой разброс данных связан, вероятно, с отсутствием единого подхода к диагностике новообразований печени.
Опухоли печени чаще диагностировали у собак, средний возраст которых составлял 8.6 лет, а средняя масса тела – 19.4 кг. У кошек с онкологическим поражением печени средний возраст составлял 14.3 года, а средняя масса тела 3.4 кг. У самок указанную патологию выявляли чаще, чем у самцов.
Этиология
По современным представлениям, развитие первичных опухолей печени у собак и кошек связано с действием разных этиологических агентов. Отмечается роль физических, химических, бактериальных, вирусных, паразитарных, возрастных, генетических и других факторов. Особая роль в возникновении опухоли отводится действию мутагенов, которые воздействуя на генетический аппарат клетки, вызывают мутацию и превращение нормальной клетки в опухолевую.
Метастазируют в печень чаще всего опухоли молочных желез, яичников, а также всех органов, дренируемых воротной веной печени. Очень редко бывают метастазы в печень при раке полости рта, глотки, предстательной железы, мочевого пузыря и практически не бывают при раке кожи.
Патогенез
В отношении патогенеза первичных опухолей единого мнения в литературе нет.
Метастазы в печени развиваются когда опухолевая клетка, отделившись от первичной опухоли проникают в кровеносные сосуды и циркулируют в сосудистом русле. Далее происходит фиксация их в капиллярах печени, разрушение стенок сосудов и проникновение опухолевых клеток в экстраваскулярное пространство, где они размножаются и образуется метастатический узел.
Диагностика
На первых стадиях развития онкологического процесса болезнь протекает без выраженных клинических признаков.
Клинические симптомы при новообразованиях печени, как правило, появляются при поражении более 70% гепатоцитов, что значительно осложняет лечебный процесс.
Клиническое проявление опухолей печени у собак характеризовалось угнетением общего состояния, рвотой, кахексией, болезненностью в области печени, гепатомегалией, аллопециями, кожным зудом.
У кошек при наличии опухолей в печени регистрировали наличие высыпаний на коже, частичную анорексию, кахексию, иктеричность слизистых оболочек и кожи, рвоту.
Инструментальная диагностика
Для диагностики опухолей печени используются рентгенографические исследования, УЗИ, магнитно-резонансная томография (МРТ), компьютерная томография (КТ) и сцинтиграфия.
Результаты, полученные указанными методами диагностики играют ведущую роль при постановке окончательного диагноза. При этом ведущими задачами диагностики являются определение локализации опухоли, ее вид, степень инвазии опухоли в окружающие ткани и состояние лимфоузлов ворот печени.
При использовании современной аппаратуры рентгенографическое исследование органов брюшной полости в латеральной и вентро-дорсальной проекциях позволяет визуализировать опухоли в 86% и 73% случаев, соответственно.
УЗИ позволяет дифференцировать солидные образования и кисты, гемангиомы и злокачественные опухоли. Метод высоко информативен для определения локализации поражения и распространенности процесса.
Эхографическое изображение новообразований печени зависит от их типа и стадии развития. Печеночноклеточный рак визуализируется в виде единичных или множественных образований неправильной формы с неоднородной эхоструктурой, окруженных тонким гипоэхогенным ободком (рис. ). Капиллярная гемангиома на эхограмме представляется в виде овальных образований с повышенной эхогенностью и ровными четкими краями. Часто визуализируются также питающие опухоль кровеносные сосуды (рис. ). Кавернозная гемангиома характеризуется неоднородной внутренней структурой и наличием эхонегативных зон различной формы и разного размера (рис. ). Метастазы визуализируются в виде единичных или множественных образований неопределенной формы с неопределенной структурой и неровными краями. При наличии некроза и распада опухоли на эхограмме выделяется участки паренхимы печени со смешанной эхогенностью.
Компьютерная томография в настоящее время в гуманной и ветеринарной практике считается одним из классических методов диагностики различных новообразований печени(4, 6,7).
Магнитно-резонансную томографию можно считать одним из лучших методов выявления новообразований печени. Однако, из-за отсутствия аппаратов МРТ в ветеринарной практике он используется крайне редко.
К современным методам оценки функционального состояния печени в гуманной медицине является динамическая сцинтиграфия, которая заключается в введении больному изотопа препарата радия и одновременном проведении динамической сцинтиграфии. Этот метод позволяет точнее определить поглотительно-выделительную функцию печени, оценивая ее функциональные возможности. К сожалению, в доступной литературе данных об использовании данного метода в ветеринарной практики мы не обнаружили.
Лабораторные методы
Они включают общий клинический анализ крови и биохимические исследования сыворотки крови.
При гематологических исследования отмечается, как правило, умеренный лейкоцитоз и эритропения.
В табл. 1 приведены данные об изменении показателей крови у собак и кошек со злокачественным поражением печени.
Табл.1 Изменение биохимических показателей крови у собак и кошек со злокачественным поражением печени (Денисенко В.Н., Кесарева Е.А., 2003).
Собаки
Щелочная фосфотаза МЕ\л
Кошки
Щелочная фосфотаза МЕ\л
Анализ таблицы показывает, что при наличии опухолей печени у собак отмечают более высокие, чем при другой патологии уровни общего билирубина, АЛТ, АСТ и ЩФ. Содержание глюкозы у больных животных понижено.
У кошек при наличии онкологических поражений печени статистически достоверно повышена активность АЛТ, АСТ, ЩФ, а также содержание глюкозы и общего билирубина.
Отмеченные изменения биохимических показателей при неоплазии печени у собак и кошек являются следствием усиленного разрушения гепатоцитов и нарушения динамики желчи.
К дополнительным методам исследования можно отнести проведение различных функциональных проб. К ним относятся антипириновая проба, определение клиренса лидокаина, проба нагрузки аммонием, а также бромсульфалеиновая (БСФ) и индоцианиновая пробы.
Проба с бромсульфалеином основана на способности гепатоцитов улавливать из крови и выделять в желчь бромсульфолеин. При наличии патологических изменений в гепатоцитах процесс экскреции замедляется и БСФ удерживается в крови долгое время. Для проведения теста животному вводят в/в 5% раствор БСФ 5 мг/кг. Берут кровь из вены через 45 мин. К 1мл сыворотки добавляют 2,39 мл р-ра NaСI и 0,1 мл 5%-го КОН. При наличии БСФ – фиолетовый цвет. Обнаружение БСФ через 45 мин после введения свидетельствует о нарушении поглотительно-выделительной функции, что значительно ухудшает прогноз и осложняет реабилитацию животных после проведениях объемных или экономных резекций печени(1,4).
Индоцианин зеленый удаляется из сосудистого русла только печенью в не конъюгированном виде. Клиренс индоцианина менее 0.4 мг/кг/мин даже после небольших резекций печени ассоциируется с достоверно более высокой частотой острой печеночной недостаточности в послеоперационном периоде(4,5).
При постановке пробы нагрузки аммонием вследствии снижения детоксицирующей функции печени содержание аммиака в сыворотке крови через 30 мин увеличивается в 2-30 раз по сравнению с исходным.
Определение онкомаркеров на сегодняшний день не находит широкого применения. Хотя, по данным авторов, увеличение альфафетопротеина у собак может свидетельствовать о наличии гепатоцеллюлярного рака, гепатита или цирроза (4,7).
Морфологическое исследование
Для диагностики и дифференциальной диагностики в ветеринарной практики проводят цитологические и гистологические исследования.
Для получения материала с целью проведения цитологического исследования используется спинальная игла Spinocan 25 Gx. Биоптаты для гистологического анализа получают при помощи иглы типа «tru-cut».
Наиболее частым осложнением биопсии печени является кровотечение. Из 32 биопсий, проведенных в нашей клинике при использовании вышеописанных игл нами не получено ни одного случая серьезного.
Наиболее эффективным для постановки диагноза является комплекс: «Рентгенологическое исследование + УЗИ + развернутая лабораторная диагностика + пункционная биопсия печени». Причем лабораторная диагностика должна проводиться в максимально полном объеме, особенно, если планируется оперативное вмешательство, т.к. это позволяет максимально снизить риск послеоперационных осложнений, а также определить прогноз. Также не следует пренебрегать таким современным методом диагностики, как интраоперационное УЗИ, которое выявляет невидимые глазом и непальпируемые опухоли печени, а также позволяет, в сложных случаях, определить расположение крупных сосудов, что значительно облегчает операцию и минимизирует риск кровотечений.
Макро- и микроскопическое строение опухолей печени
Опухоли печени, в соответствии классификации опухолей ВОЗ подразделяются на:
- А.Эпителиальные доброкачественные: печеночно-клеточная аденома, аденома внутрипеченочных желчных протоков, цистоаденома внутрипеченочных желчных протоков.
Б.Эпителиальные злокачественные: гепатоцеллюлярный рак, холангиокарцинома, цистоаденокарцинома желчных протоков, смешанный гепатохолангиоцеллюлярный рак, гепатобластома, недифференцированный рак.
- Неэпителиальные опухоли: гемангиома, инфантильная гемангиоэндотелиома, гемангиосаркома, эмбриональная саркома и др.
- Различные другие типы опухолей: тератома, карциносаркома и др.
- Неклассифицируемые опухоли.
- Опухоли кроветворной и лимфоидной тканей.
- Метастатические опухоли
В табл. 2 и 3 представлены наши результаты морфологического исследования первичных и метастатический поражений печени у собак и кошек, подвергшихся хирургическому лечению
Табл.2 Морфологические виды первичных опухолей печени у собак и кошек (n=23)
Первичная опухоль печени
Табл. 3 Морфологические виды метастатических поражений печени у собак и кошек (n=21)
Метастаз в печень из
Рака молочной железы
Рака тела матки
Саркомы мягких тканей
Анализ таблицы показывает, что из первичных опухолей печени чаще всего встречается гепатоцеллюлярный рак, что совпадает с данными международной ветеринарной литературы. Метастазы рака молочных желез превалируют над метастазами из других органов. Это, вероятно, связано с большим количеством животных, страдающих опухолями молочных желез.
Макрокартина опухолей печени
Гемангиомы печени представляли собой образования с ограниченными контурами и разрастаниями патологической ткани в виде скопления пузырьков различного диаметра.
Кисты печени представляли собой ограниченные полости с серозной или серозно-геморрагической жидкостью.
Остальные типы опухолей печени, по нашим данным, не имеют специфической макрокартины.
Гистологическая картина
Гемангиома – тонкостенные каналы сосудов разнообразные по размеру, чаще крупные, ход их резко развитой. Выстилающие эндотелиальные клетки уплощены, в некоторых местах слущены. Сосудистые каналы поддерживаются фиброзной стромой.
Гепатоцеллюлярный рак – клеточные элементы опухолевой ткани крупные полигональные со средним ядерно-цитоплазматическим соотношением, клетки с эозинофильной цитоплазмой, имеющие центральные везикулярные ядра с четко выраженными ядрышками. Клетки располагаются в виде трабекул или неупорядоченно. Между трабекулами и скоплениями клеток располагаются синусоиды, выстланные эпителием. Могут определяться фигуры митозов.
Фибросаркома печени - опухолевая ткань построена из средних мономорфных веретеновидных и овальных клеток, формирующих тяжи, ленты и завихрения. Строма представлена равномерно в виде тонких коллагеновых волокон. Рост инвазивный.
Метастаз тубулярного рака молочной железы в печень – опухоль построена из железистого эпителия, формирующего тубулярные и псевдокистозные структуры. Клеточные элементы опухоли округлой формы, умеренно полиморфные со средним ядерно-цитоплазматическим соотношением. Ядра окргулые, крупные, содержат гиперхромный хроматин. Выявляются признаки пролиферации митозов, в том числе атипичных.
Метастаз аденокарциномы яичника – опухоль чаще построена из железистых структур, разделенных перегородками, клетки имеют кубическую или овальную форму со средним ядерно-цитоплазматическим соотношением и располагаются на тонких перегородках стромы. Ядра окргуглые, гиперхромные, содержат грубодисперсный хроматин, цитоплазма эозинофильная.
Лечение
Хирургический метод является наиболее эффективным при лечении новообразований печени.
Использование химиотерапии при первичных опухолях печени в медицине не привело к ожидаемым результатам и также плохо зарекомендовала себя в ветеринарии. Химиотерапию применяют при лечении системных заболеваний, таких как лимфосаркома. По данным различных авторов (Уейс и др., 2005) лимфосаркома составляет 7% от всех онкологических заболеваний печени. При ней применяют схемы СОР (винкристин и циклофосфан) и АСОР (винкристин, циклофосфан, доксорубицин). Также химиотерапию в сочетании с хирургической операцией используют при метастатическом поражении печени опухолями, чувствительными к химиотерапии. При метастатическом процессе, например, из рака молочной железы одна из возможных схем включает в себя несколько препаратов: 5 –фторурацил, циклофосфан и доксорубицин. Выбор схем и доз химиотерапевтических препаратов зависит от морфогенеза опухоли, общего состояния больного животного, результатов анализов крови, степени дегидратации.
Оценка применения радиотерапии у животных с опухолями гепато-билиарной системы изучена недостаточно.
При неудовлетворительном общем состоянии животных начинать хирургическое лечение необходимо только после стабилизации состояния при помощи инфузионной терапии с применением антибактериальных препаратов, гепатопротекторов и др.
При единичном поражении печени в независимости от морфологической ее принадлежности проводили лобэктомию, либо краевую резекцию пораженной доли. При первичной опухоли – лечение только хирургическое, при метастатическом процессе в послеоперационном периоде решали вопрос о применении химиотерапии.
Для проведения лобэктомии рекомендуется проводить комбинированный доступ в брюшную полость, который включает в себя срединную лапаротомию, боковой разрез параллельно каудальному краю последнего ребра, резекцию серповидной связки. По нашим данным 80% опухолей локализовалась в левой половине печени.
После вышеуказанного доступа выделяли пораженную долю и на ее основание накладывали две обвивные лигатуры. При наложении узла нить прорезала паренхиму печени и лигировала основные сосудистые магистрали.
При множественных поражениях печени следует минимизировать объем резекции печени и сочетать его с методами локального воздействия, такими как склеротерапия и криодеструкция. При этом доступ удобнее сочетать с ранорасширителем Сигала.
Криодеструкция
В основе криодеструкции лежит быстрое замораживание опухоли жидким азотом с последующим оттаиванием, что приводит к повреждению клеток и их гибели. Этот метод может быть использован в качестве монотерапии, также он используется как дополнение к лобэктомии, при невозможности абластичного удаления опухоли.
Алкоголизация (склеротерапия)
96* спирт вызывает тромбоз артерий, питающих опухоль, ее ишемию и некроз. Размер опухоли не должен превышать 5 см. Количество очагов не более – 3-5, а максимальная доза не должна быть выше 0.5 мл на килограмм массы тела. Введение спирта необходимо делать по краю опухоли до изменения цветовой гаммы очага.
Как правило, при множественных опухолях печени, повторное вмешательство путем лапароскопии, выполненное через 30 суток после операции, позволяет оценить эффект от проведенного лечения, и, при необходимости, повторить локальное воздействие.
Результаты лечения и прогноз
При доброкачественных поражениях печени, а также при первичных злокачественных, при единичном поражении прогноз от благоприятного до осторожного. При множественном поражении печени или при метастатическом процессе прогноз зависит от общего состояния животного, функциональных резервов печени, а также состояния других жизненно важных органов.
Опухоли печени (рак печени , гепатоцеллюлярный рак и др.)
Для диагностики рака печени применяются: анализ крови, ультразвуковое исследования (УЗИ) печени с прицельной тонкоигольной пункционной биопсией. В подавляющем большинстве случаев правильный диагноз можно поставить в течение одного дня. Выявление метастатических опухолей печени основано на иммунохимическом и инструментальном мониторинге за больными, ранее получавшими лечение по поводу опухолей любых локализаций. Здесь неоценимую услугу также может оказать исследование опухолевых маркеров, уровень которых может повышаться еще до клинически определяемых метастазах. Применяется также спиральная или мультиспиральная рентгеновская компьютерная томография (РКТ), ангиография, радионуклидные методы. В последние годы, диагностический ряд дополнился такими высокоинформативными методами как магнитно-резонансная томография (МРТ), позитронная эмиссионная томография (ПЭТ), комбинированное ПЭТ/КТ сканирование.
Какие термины приняты в онкологической практике
Гепатоцеллюлярный рак (ГЦР) – печеночно-клеточный рак, гепатома, злокачественная гепатома. ГЦР занимает пятое место у мужчин и восьмое место у женщин среди всех злокачественных новообразований в мире.
Холагиокарценома (ХК) – эпитальная злокачественная опухоль печени.
Холангиоцеллюлярный рак (ХЦР) – аденокарценома внутрипеченочных желчных протоков.
Факторы, оказывающие влияние на развитие рака печени
У 80% больных ГЦР имел место цирроз печени. Самой частой причиной развития цирроза являются гепатиты В и С, поэтому многие исследователи фокусируют свое внимание именно на этих заболеваниях. Алкогольный цирроз печени также предрасполагает к развитию ГЦР, но в гораздо меньшей степени, чем гепатиты В и С.
Профилактика рака печени
Наиболее действенная профилактика первичного рака печени – это избегать влияния факторов, вызывающих хронические заболевания печени. При ГЦР это, прежде всего вирусы гепатитов, злоупотребление алкоголем. При ХК – гельминты класса трематод. Максимальный эффект для профилактики рака оказывает предотвращение воздействия на организм, но даже при возникновении заболевания своевременное его лечение также очень важно.
Гистологическая классификация опухолей печени предложена Всемирной организацией здравоохранения (ВОЗ) в 1983 г. и используется в настоящее время. Она предусматривает следующие варианты:
- Эпителиальные доброкачественные:
- печеночноклеточная аденома;
- аденома внутрипеченочных желчных протоков;
- цистаденома внутрипеченочных желчных протоков.
- Эпителиальные злокачественные:
- гепатоцеллюлярный рак;
- холангиокарцинома;
- цистаденокарцинома желчных протоков;
- смешанный гепатохолангиоцеллюлярный рак;
- гепатобластома;
- недифференцированный рак.
- Неэпителиальные опухоли:
- гемангиома;
- инфантильная гемангиоэндотелиома;
- гемангиосаркома;
- эмбриональная саркома и др.
- Различные другие типы опухолей:
- тератома
- карциносаркома и др.
- Неклассифицируемые опухоли.
- Опухоли кроветворной и лимфоидной тканей.
- Метастатические опухоли.
Первичный рак печени
Наибольшее практическое значение среди первичных злокачественных опухолей печени имеет первичный рак печени.
Первичный рак печени макроскопически представлен 3-мя разными видами: массивной, узловой и диффузной формами. Это деление предложено в 1901 г., оно поддерживается большинством исследователей и употребляется до настоящего времени:
- Массивная форма первичного рака печени имеет два варианта. В первом она представлена одним крупным узлом (массивная простая форма), во втором – одним крупным узлом с метастазами по периферии (массивная форма с сателлитом).
- Узловая форма рака – в паренхиме печени обычно находят несколько сравнительно одинаковых по размеру опухолевых узлов, располагающихся в одной или обеих долях печени. Решить, какой из опухолевых узлов является основным, не представляется возможным. Вокруг основных больших узлов могут быть мелкие, по всей вероятности, метастатические узлы. Иногда в печени находят мелкие опухолевые узелки одинаковой величины, разбросанные по всему органу. В центре опухолевых узлов как крупных, так и мелких, наблюдаются очаги некроза с кровоизлияниями. Возможно слияние отдельных узлов и образование крупных конгломератов самой разнообразной формы.
- Диффузная макроскопическая форма по внешнему виду и некоторым другим признакам значительно отличается от двух предыдущих форм. Она встречается реже предыдущих видов, представлена опухолью в виде неравномерной инфильтрации печени или множественными мелкими опухолевыми узлами, с трудом дифференцирующимися от узлов регенераторной гиперплазии, причем у всех больных имеет место поражение обеих долей и в большинстве случаев протекает на фоне цирроза печени.
Микроскопические формы первичного рака печени
Злокачественная опухоль представлена клетками, напоминающими нормальные клетки печени – гепатоциты. У мужчин встречается в два раза чаще, чем у женщин. Нередко сочетается с циррозом печени.
Микроскопически наиболее частым вариантом является трабекулярный, при котором опухолевые клетки выглядят крупнее и лишь в редких случаях мельче нормальных гепатоцитов.
Пути метастазирования и места наиболее характерной локализации метастазов, первичного рака печени:
- Гематогенный путь (основной): чаще – в печень, легкие; реже – в кости, надпочечники, почки;
- Лимфогенный путь – в лимфатические узлы гепатодуоденальной связки, панкреатодуоденальные лимфоузлы;
- Имплантационный путь – париетальная и висцеральная брюшина, диафрагма.
Клинико-анатомическая классификация первичного рака печени по TNM
В настоящее время используется пятое издание классификации опухолей (1998 г.), одобренное всеми национальными комитетами TNM. Классификация применима только для первичного ГЦР и ХЦР. Обязательно гистологическое подтверждение диагноза и разделение по гистологическим подвидам.
Скрининг первичного рака печени нуждается в совершенствовании и основан на определении в крови обследуемых лиц в группах риска один раз в 6 месяцев альфа-фетопротеина (АФП) и, в случае повышении его концентрации свыше 15 нг/мл (мкг/л) (для большинства взрослых лиц, исключая беременных женщин), выполнении ультразвукового исследования (УЗИ) печени. При этом обнаружение образования в печени практически свидетельствует о наличии у пациента печеночно-клеточного рака.
Группа риска первичного рака печени в регионах с низким и средним уровнем заболеваемости данной патологией состоит из больных хроническими заболеваниями печени. В регионах эндемичных по вирусному гепатиту В и С группа риска включает лиц обоего пола старших возрастных групп – носителей поверхностного антигена вируса гепатита В (HBsAg) и гепатита С.
Выявление метастатических опухолей печени основано на иммунохимическом и инструментальном мониторинге за больными, ранее получавшими лечение по поводу опухолей любых локализаций. Здесь неоценимую услугу также может оказать исследование опухолевых маркеров, уровень которых может повышаться еще до клинически определяемых метастазах.
Опухолевые маркеры представляют собой макромолекулы, главным образом белки с углеводным или липидным компонентом, наличие и концентрация которых в периферической крови коррелирует в определенной степени с наличием и ростом злокачественной опухоли.
Идеальный маркер для диагностики должен обладать двумя характерными чертами:
1) секретироваться в кровь в достаточном для выявления количестве;
2) обнаружение его должно позволить делать заключение о локализации продуцирующей его опухоли.
Пока не существует идеальных маркеров опухоли, обладающих 100% чувствительностью и специфичностью. Тем не менее, помимо указанного выше АФП, целый ряд маркеров может с успехом использоваться в целях диагностики.
Наиболее известным маркером колоректального рака является раково-эмбриональный антиген (РЭА) открытый в 1965г Gold and Freedman. РЭА – гликопротеин, располагающийся в периферических слоях клеточной мембраны. Его ген относится к семейству генов, ответственных за синтез иммуноглобулинов. РЭА – не обязательный маркер. У 40% больных раком толстой кишки он не выявляется. Он обнаруживается и при других злокачественных опухолях (рак молочной железы, поджелудочной железы, легкого, яичников и даже саркомах), а также в эмбриональной ткани и при незлокачественных заболеваниях (гепатотоксичность, гидронефроз, желчнокаменная болезнь). При метастазах рака РЭА чаще позитивный, при локальном раке – негативный. После радикальных операций систематическое определение РЭА позволяет выявить в 47% случае рецидивы (в том числе и бессимптомные).
Обнаружение повышенного уровня маркеров должно служить поводом для углубленного обследования, в том числе и печени.
Выявить наличие злокачественного поражения печени при современном техническом оснащении медицинских учреждений не представляет большой проблемы. Для этого необходимо провести ультразвуковое исследование печени и в случае выявления очагового образования в ней выполнить тонкоигольную пункцию его с последующим цитологическим исследованием полученного материала. С помощью УЗИ и прицельной тонкоигольной пункционной биопсии в подавляющем большинстве случаев правильный диагноз можно поставить в течение одного дня.
Еще одним важным аргументом в пользу необходимости пункции опухоли является тот факт, что не всегда наличие очагового образования в печени даже в тех случаях, когда больной был оперирован по поводу злокачественной опухоли, означает, что этот очаг является метастазом. Установление истинной картины характера изменений в печени может существенно повлиять на выбор тактики лечения.
Радиологические методы диагностики опухолевых поражений печени
Как известно, в настоящее время для оценки анатомического и функционального состояния печени существует целый ряд самых различных диагностических методов, в числе наиболее распространенных: ультразвуковое исследование (УЗИ), спиральная или мультиспиральная рентгеновская компьютерная томография (РКТ), ангиография, радионуклидные методы. В последние годы, диагностический ряд дополнился такими высокоинформативными методами как высокопольная магнитно-резонансная томография (МРТ), позитронная эмиссионная томография (ПЭТ), комбинированное ПЭТ/КТ сканирование.
Рентгеновская компьютерная томография (РКТ) (пошаговая, спиральная или мультиспиральная) в настоящее время считается одним из классических методов диагностики опухолевых и опухолевидных поражений печени. Указанные модификации РКТ значительно различаются между собой по объему и скорости сбора исходных данных, необходимых для построения КТ-изображений.
Магнитно-резонансную томографию (МРТ) по праву можно считать одним из лучших методов диагностики опухолевых и опухолевидных изменений в печени. Для оценки состояния органов брюшной полости МРТ стала применяться лишь после разработки быстрых и сверхбыстрых МР-последовательностей (протоколов исследования), позволяющих исследовать одну анатомическую область за время одной задержки дыхания (т.е. за 25-30 сек).
К ярким достоинствам МРТ следует отнести возможность получения высококачественных изображений в любой, произвольно определяемой плоскости, что значительно повышает наглядность отображения патологических процессов в сложных анатомических областях и облегчает их топическую диагностику.
Радионуклидные методы
Важное значение в клинической практике (в том числе, в гепатологии) имеют результаты применения различных радионуклидных методов и методик. Здесь, в первую очередь, следует упомянуть позитронную эмиссионную томографию (ПЭТ). Данный метод, довольно сложный и дорогой (справедливо относят к передовым направлениям ядерной медицины), представляет собой комплекс из небольшого циклотрона, радиохимической лаборатории и собственно позитронного эмиссионного томографа. С помощью циклотрона нарабатываются ультракороткоживущие, позитрон-излучающие радионуклиды (18F, 11C, 13N, 15O и др.) с периодом полураспада от 2 мин. до 2 час., поэтому циклотрон должен находиться либо в самой клинике, либо непосредственно рядом с ней. Радиохимическая лаборатория обеспечивает синтез и контроль качества нарабатываемых радиофармпрепаратов, вводимых внутривенно. А уже с помощью позитронного эмиссионного томографа проводится сканирование пациентов для получения анатомо-топографических изображений пространственно-временного распределения позитрон-излучающих меченых соединений.
Разработан многочисленный ряд ПЭТ-методик, позволяющих изучать различные биологические характеристики опухолей, но наиболее широкое применение в онкологии получили исследования клеточной энергетики с 18F-диоксиглюкозой. Принцип методики основан на общеизвестном факте, что опухолевая ткань по сравнению с нормальной обладает более высокой скоростью «аэробного гликолиза», т.е. поглощает значительно большее количество глюкозы, чем нормальные ткани. Меченая глюкоза, введенная внутривенно, аккумулируется в опухолевых клетках в количестве, позволяющем выявлять очаги повышенного ее накопления детекторной системой позитронного эмиссионного томографа. И уже количественное определение степени интенсивности накопления лежит в основе дифференцировки опухолевых и неопухолевых процессов. Исследование начинается через 60-90 мин после внутривенного введения радиофармпрепарата.
Одним из ярких достоинств метода является то, что одно единственное исследование позволяет (за 40-60 минут) выявлять очаги опухолевого процесса и в печени, и в тканях головного мозга, в легких, в различных отделах скелета, лимфатических узлах. Т.е. формально применение ПЭТ в определенных случаях может исключить применение всех других диагностических методов.
Целесообразно упомянуть также об эмиссионной компьютерной томографии печени с мечеными эритроцитами, которая применяется для дифференциальной диагностики сосудистых новообразований (гемангиом) и несосудистых опухолей печени. Методика основана на использовании меченых эритроцитов (посредством внутривенного введения специальных радиофармпрепаратов). Последующая сцинтиграфия позволяет визуализировать анатомические органы и структуры, содержащие значительное количество крови (сердце, кровеносные сосуды, селезенку и гемангиомы).
Одним из наиновейших методов исследования печени считается сочетанное ПЭТ/РКТ сканирование (PET/CT Imaging). Соответствующая аппаратура представляет собой комбинацию ПЭТ-сканера и рентгеновского компьютерного томографа, что позволяет получать отображение очагов гиперфиксации радиофармпрепарата в организме человека с уточненной пространственной локализацией. По данным ряда авторов, показатели чувствительности и специфичности ПЭТ/КТ сканирования превышают аналогичные показатели КТ или ПЭТ исследований, применяемых по отдельности. Пространственное разрешение ПЭТ – около 5-7 мм.
ПЭТ/КТ превосходно отображает метастазы в печень целого ряда первичных опухолей, в частности метастазы рака легкого, рака молочной железы и колоректального рака, кроме того, метод высоко информативен в отображении местной и регионарной распространенности первичных опухолей желчных путей (метастазов в печень и регионарные лимфатические узлы). В то же время, метод имеет ограниченные возможности в отображении гепатоцеллюлярного рака.
В связи с широким внедрением в клиническую практику ультразвуковых методов исследования печени, компьютерной и магнитно-резонансной томографии ангиография, как диагностическая процедура, отходит на второй план. Тем не менее, артериография имеет весьма специфическую картину при ГЦР, некоторых видах сарком печени (прежде всего ангиосаркома). Что касается диагностики метастатического поражения печени, то здесь степень визуализации зависит от васкуляризации узлов. Чаще всего гиперваскулярные метастазы наблюдаются при карциноидных опухолях, меланоме, светлоклеточном раке почки, раке яичников, реже при раке поджелудочной железы.
Метастатические опухоли печени
Метастазирование – это сложный процесс, состоящий из цепи последовательных этапов, при прохождении которых опухолевые клетки, отделившись от первичной опухоли, инвазируют окружающие ткани, проникают в лимфатические и кровеносные сосуды (интравазация), циркулируют в сосудистом русле. Далее происходит фиксация их в лимфатических сосудах и кровеносных капиллярах различных органов, пенетрация (проникновение) стенок сосудов и проникновение опухолевых клеток в экстраваскулярное пространство (экстравазация), «дремлющее» состояние их и, наконец, размножение опухолевых клеток с возникновением метастатического узла.
Важнейшим путем для возникновения отдаленных органных метастазов является гематогенный – по кровеносному руслу. Печень – наиболее частая локализация гематогенных метастазов опухолей независимо от того, дренируется ли первичная опухоль системой воротной вены или другими венами большого круга кровообращения. Но все же самым частым путем проникновения метастазов в печень является система воротной вены, поэтому все злокачественные опухоли, связанные с этой системой, являются основным источником метастазов в печень.
Патологоанатомические характеристики метастатических опухолей печени повторяют таковые первичных опухолей – источников метастазирования в печень. В ряде случаев метастазы отличаются от первичных опухолей степенью дифференцировки опухолевых клеток, что затрудняет установление органной принадлежности первичной опухоли. Весьма схожими могут оказаться патологоанатомические данные первичных и метастатических опухолей печени, имеющих схожий гистогенез. Например, холангиоцеллюлярный рак печени и метастазы в печень аденокарциномы пищеварительного тракта. Иммуногистохимические исследования помогают в решении этой задачи.
Наиболее частые локализации рака при метастазах в печень: желудок, поджелудочная железа, толстая кишка, молочная железа, легкое.
Более редкие локализации первичных опухолей, метастазирующих в печень: пищевод, яичники, меланома кожи, предстательная железа, почки. Наиболее значимый путь метастазирования: портальная эмболия опухолевых клеток в печень.
Очень редко метастазы в печень возникают при раке полости рта, глотки, предстательной железы, мочевого пузыря и практически не бывает при раке кожи.
Читайте также:
