Как свертывается кровь
Добавил пользователь Владимир З. Обновлено: 27.01.2026
Когда мы в быту говорим о свертывании крови, мы чаще всего обсуждаем проблемы гемостаза. Гемостаз – это сложная биологическая система, которая поддерживает жидкое состояние крови в организме в норме и остановку кровотечения при повреждении целостности сосудов. Проще говоря, организм настроен на то, чтобы не потерять ни капли крови.
Существуют два механизма гемостаза:
- 1. Сосудисто-тромбоцитарный (первичный).
- 2. Коагуляционный гемостаз (вторичный, свертывание крови). От латинского коагуляцио – свертывание, сгущение.
Нарушения сосудисто-тромбоцитарного гемостаза
Нарушения в этом звене гемостаза чаще всего проявляются повышенной кровоточивостью, наклонностью к образованию гематом (синяков) при самом незначительном контакте или вообще спонтанно, без видимой причины. В некоторых ситуациях, наоборот появляется наклонность к избыточно легкому тромбообразованию.
Существуют факторы, стимулирующие образование первичного тромба, и нарушающие его. К стимуляторам относится воспалительный процесс, потому что при воспалении повышается содержание биологически активных веществ в крови. Можно сказать, что есть готовность к формированию тромба, дело только за местным повреждением сосуда. Поэтому при тяжелых инфекционных болезнях может произойти закупорка сосудов. Повышена готовность к тромбообразованию при беременности, а так же при некоторых наследственных болезнях (тромбофилия). Из продуктов питания повышают активность тромбоцитов столовый уксус (маринады), кофе.
Нарушается процесс образования первичного тромба при снижении количества тромбоцитов (тромбоцитопения) и при качественной неполноценности тромбоцитов (тромбоцитопатия). Тромбоцитопатия может возникнуть при приеме некоторых лекарств. В первую очередь это противовоспалительные препараты: аспирин, анальгин, бруфен, некоторые антибиотики. Тромбоцитопатия развивается также при болезнях почек. Специи, крепкий алкоголь также могут снижать полноценность тромбоцитов.
Свёртывающая система крови – это фактически несколько взаимосвязанных реакций, протекающих в виде каскада, или цепной реакции. На каждой стадии этого процесса происходит активация профермента (неактивной формы фермента). Тринадцать таких белков (факторы свёртывания крови) составляют систему свёртывания. Их принято обозначать римскими цифрами от I до XIII.
Нарушения в системе коагуляции
Уменьшение содержания или активности факторов свёртывания может сопровождаться повышенной кровоточивостью (например гемофилия А, гемофилия B, болезнь Виллебранда). Избыточная активация коагуляционного гемостаза, (например, Лейденская мутация фактора V) приводит к развитию тромбозов (тромбофилии).
Гемостаз и беременность
Среди всех причин невынашивания беременности на втором месте по частоте стоят проблемы в системе гемостаза. На втором после акушерско-гинекологических причин. В чем же дело?
В ходе беременности организм будущей мамы готовится к родам. Готовится и система гемостаза, чтобы максимально сократить кровопотерю в родах. Гемостаз активируются прогрессивно вместе с увеличением срока беременности. Если гемостаз женщины изначально повышенно активен, то в ходе беременности могут образоваться микротромбы в сосудах матки или плаценты, что приводит к выкидышу, либо к замершей беременности.
При каких состояниях это может произойти?
1. При наследственной тромбофилии, чаще при нарушении обмена фолиевой кислоты и ее соединений (фолатов), когда в крови повышается количество гомоцистеина. Причинами повышения уровня гомоцистеина могут быть недостаток в рационе фолиевой кислоты и витамина В12, болезни щитовидной железы, почек. Он также может повышаться у курильщиков, любителей кофе и на фоне приема таких медикаментов, как теофиллин (кстати, родственник кофеина), никотиновая кислота. Гомоцистеин повреждает эндотелий (внутренний слой) сосудов, а эти повреждения запускают тромбообразование.
2. При антифосфолипидном синдроме (АФС) – так называют аутоиммунное заболевание, при котором вырабатываются антитела к своим собственным факторам свертывания. В результате также спонтанно образуются тромбы в сосудах.
Профилактика нарушений свертываемости при беременности
Для того, чтобы избежать осложнений беременности, у всех беременных необходимо проводить лабораторное исследование – клинический анализ крови, коагулограмму (параметры свертывания крови), определение уровня гомоцистеина.
Женщины, у которых ранее были выкидыши или замершая беременность, а также беременные в результате ЭКО, относятся к группе риска по развитию нарушений в системе гемостаза. Для пациентов из группы риска рекомендуется проводить полное исследование системы гемостаза, кровь на антифосфолипидные антитела. В случае ЭКО (экстракорпорального оплодотворения) контроль параметров свертывания крови необходимо выполнять в течение всей беременности. В соответствии с рекомендациями комитета экспертов ВОЗ (всемирной организации здравоохранения) контроль коагулограммы и D-димера необходимо выполнять не реже, чем 1 раз в 2 недели. Коррекцию подобных нарушений проводят совместно гинеколог и гематолог.
В идеальном случае полное обследование целесообразно выполнять не после наступления беременности, а на стадии планирования семьи.
В Клинике высоких медицинских технологий им. Н. И. Пирогова налажена и действует система диагностики и лечения пациентов с проблемами в системе гемостаза. Лабораторная диагностика, включая генетические исследования, позволяет выявить причины нарушений. Лечение подобных пациентов на стадии планирования семьи и ведение их во время беременности (как физиологической, так и в результате ЭКО) осуществляют квалифицированные гинекологи совместно с гематологом.
Оформите заявку на сайте, мы свяжемся с вами в ближайшее время и ответим на все интересующие вопросы.
Как свертывается кровь
Ткани и органы. Кровь
При нарушении целостности кровеносной системы уменьшение кровопотери обеспечивает система гемостаза. Гемостаз поддерживается двумя путями: остановкой кровотечения с помощью тромбоцитов и свертыванием крови . В данном разделе основное внимание уделено ферментативным реакциям свертывания крови. Повторное растворение сгустков крови, фибринолиз , рассмотрен на с. 284.
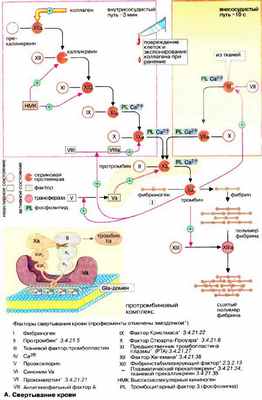
Номенклатура факторов свертывания крови несколько запутана. Факторы нумеруются римскими цифрами, при этом активированная форма фактора в наименовании содержит дополнительно букву «а» после римской цифры. Многие факторы являются протеиназами. На схеме неактивные предшественники протеиназ представлены в виде окружностей, а активные ферменты — окрашенными кружочками с вырезанным сектором. Вспомогательные факторы показаны в виде прямоугольников.
При свертывании крови происходит ферментативное превращение растворимого белка плазмы фибриногена (фактора I, см. рис. 71) в фибриновый полимер, сеть волокон нерастворимого белка. В этой реакции принимает участие фермент тромбин (фактор IIа), который протеолитически отщепляет от молекулы фибриногена небольшой пептидный фрагмент, в результате чего освобождаются участки связывания, что позволяет молекуле фибрина агрегировать в полимер . Затем с помощью глутамин-трансферазы (фактора XIII) образуются изопептидные связи боковых цепей аминокислот фибрина, что приводит к формированию нерастворимого фибринового сгустка (тромба).
Свертывание крови может запускаться двумя различными путями: вследствие нарушения целостности ткани ( внесосудистый путь, на схеме справа) или процессами, которые начинаются на внутренней поверхности сосуда ( внутрисосудистый путь , на схеме слева). В обоих случаях запускается каскад протеолитических реакций: из неактивных предшественников ферментов (зимогенов, условно обозначаемых на схеме окружностями) путем отщепления пептидов образуются активные сериновые протеиназы (обозначаемые на схеме окрашенными кружочками с вырезанным сектором), которые в свою очередь действуют на другие белки. Оба реакционных пути нуждаются в ионах Са 2+ и фосфолипидах [ФЛ (PL)] и оба завершаются активацией фактором Ха протромбина (фактора II) с образованием тромбина (IIа).
Внутрисосудистый путь инициируется коллагеном, который в норме не экспонирован на внутренней поверхности кровеносных сосудов; его контакт с кровью приводит к активации фактора XII. Внесосудистый путь активации начинается с освобождения фактора III (тканевого тромбопластина) из поврежденных клеток ткани. В течение нескольких секунд этот фактор приводит к свертыванию крови в области раны.
Факторы свертывания II, VII, IX и X содержат необычную аминокислоту, γ-карбоксиглутаминовую (Gla). Остатки Gla, которые образуются в результате посттрансляционного карбоксилирования остатков глутаминовой кислоты, группируются в особых белковых доменах. Они присоединяют ионы Са 2+ и вследствие этого связывают соответствующие регуляторные факторы с фосфолипидами на поверхности плазматической мембраны. На рисунке это схематически представлено на примере протромбинового комплекса (Va, Ха и II). Вещества, способные связывать свободные ионы Са 2+ в виде комплекса, например цитрат, предотвращают это взаимодействие с фосфолипидами и тормозят свертывание. Для синтеза остатков Gla необходим в качестве кофактора витамин К (см. с. 342). Антагонисты витамина К, такие, как дикумарин, подавляют синтез активных факторов коагуляции и действуют поэтому также как ингибиторы свертывания.
Генетически обусловленный дефицит отдельных факторов свертывания приводит к кровоточивости (гемофилия).
Контроль за свертыванием крови (не показан на схеме). Процесс свертывания крови находится в постоянном равновесии между активацией и торможением. Для торможения в плазме имеются очень эффективные ингибиторы протеиназ. Сериновые протеиназы системы свертывания инактивируются антитромбином. Его действие усиливается сульфатированным глюкозаминогликаном — гепарином (см. с. 336). Тромбомодулин, расположенный на внутренней стенке кровеносных сосудов, инактивирует тромбин, образуя с ним стехиометрический комплекс. За протеолитическое разрушение факторов V и VIII в плазме отвечает белок с. Этот белок в свою очередь активируется тромбином и, тем самым, реализуется самотормозящийся механизм свертывания крови.
Гемостаз крови
Кровь выполняет несколько жизненно важных функций, в том числе — транспортную. Благодаря разветвленной системе кровообращения каждая клетка постоянно получает кислород, необходимые ей питательные вещества и отдает продукты обмена. Стоит лишить клетки головного мозга притока обогащенной кислородом крови на 30 секунд, и сознание может нарушиться. Чтобы все ткани и органы работали слаженно, кровь, насыщенная кислородом, должна постоянно, неуклонно двигаться по артериям на периферию и по венам — обратно, к сердцу.
Любые преграды на ее пути, например, атеросклеротические бляшки, тромбы или повреждения сосудов сопряжены с риском для здоровья или жизни. Предотвратить их образование, обеспечить беспрепятственное проникновение крови к каждой клетке помогает мудрая и сложная система — гемостаз.
Гемостаз с древнегреческого языка можно перевести как «остановка крови».
Кровь циркулирует в замкнутой системе под давлением. Система гемостаза поддерживает ее жидкое состояние, останавливает кровотечение, если сосуд поврежден, таким образом сохраняя баланс между свертывающей и противосвертывающей активностью.
Как работает гемостаз?
Гемостаз «включается в работу» автоматически, как только нарушается целостность кровеносного сосуда. При этом объем кровопотери значения не имеет — даже самая маленькая царапина «запускает» полную программу свертывания крови.
Свертывание протекает последовательно в три стадии 1 .
Повреждение сосудов, независимо от их размеров, — чрезвычайное происшествие, на которое первыми реагируют рецепторы боли, запускающие развитие рефлекторного сужения сосудов. Благодаря уменьшению их просвета снижается скорость кровотока и, соответственно, уменьшается кровопотеря.
В работу по остановке кровотечения включается сама сосудистая стенка, которая в норме ведет себя по отношению к крови, которая перемещается по сосудам, абсолютно нейтрально, играя роль «проводника». Но как только сосуд оказывается поврежденным, он моментально становится активным участником событий. Одна из главных ролей в таком сценарии «спасения» достается коллагену, который содержится внутри сосудистой стенки. Даже при небольшой зоне повреждения волокна коллагена «обнажаются», к ним дружно направляются клетки крови - тромбоциты.
Коллаген и один из факторов свертывания крови «запускают» сложный биохимический процесс —активацию и агрегацию (то есть склеивание между собой) тромбоцитов с образованием тромбоцитарного или «белого» тромба, помогающего восстановить целостность сосуда.
Однако борьба с кровотечением на этом еще не заканчивается.
После того как сгусток сформирован, происходит активация факторов свертывания крови — специальных белков, которые содержатся в плазме и тромбоцитах и обеспечивают свертывание. В результате из неактивного белка плазмы крови фибриногена образуется фибрин — белок в форме волокон. С его помощью вокруг сгустка тромбоцитов формируется фибриновая сеть, которая способна удерживать тромбоциты и другие клетки крови, включая эритроциты, формируя прочный красный тромб. Он качественно «латает» рану, стягивая ее края и окончательно восстанавливая целостность поврежденного сосуда.
На первый взгляд, на этом «ремонтные работы» закончены, но это не совсем так, ведь сформировавшийся тромб может нарушать кровоток за счет уменьшения просвета «отремонтированного» сосуда. Чтобы этого не происходило, когда задача тромба выполнена, – нужно, чтобы произошло его растворение — фибринолиз
Что такое фибринолиз?
Система фибринолиза, функционирующая в организме, предотвращает чрезмерное тромбообразование. Она же включается в работу, когда приходит пора растворить тромб, образовавшийся при повреждении сосудов. Ее еще называют антисвертывающей (фибринолитической) системой.
Когда в гемостазе происходят нарушения?
К сожалению, иногда в системе гемостаза появляются сбои, которые проявляются или патологической склонностью к кровотечениям, или, напротив, повышенным патологическим образованием тромбов — тромбозом.
Повышенная кровоточивость из-за имеющихся нарушений коагуляции может быть результатом ряда заболевания и состояний, среди которых 2 :
- Дефекты в самой сосудистой стенке
- Низкое количество тромбоцитов
- Недостаточность факторов свертывания
- Избыточный фибринолиз, который приводит к растворению «нужных» тромбов.
В обратной ситуации, когда нарушения связаны с избыточным образованием тромбов, проблема может быть обусловлена такими факторами 2 :
- Слишком высокое содержание веществ, активирующих тромбоциты
- Блокирование процесса фибринолиза (растворения тромбов)
- Застой крови и другие.
Виды нарушений гемостаза
Известно несколько состояний и заболеваний, которые способствуют нарушению разных звеньев гемостаза
Нарушение тромбоцитарного гемостаза 2
Тромбоцитопении — уменьшение количества тромбоцитов Снижение уровня тромбоцитов может быть следствием целого ряда заболеваний, в том числе:
- Апластические анемии
- Острый лейкоз
- Терапия цитостатиками (препаратами для лечения злокачественных опухолей), лучевая терапия
- Дефицит витамина В12, В9
- Тромбоцитопеническая пурпура.
Кроме того, снижение уровня тромбоцитов может быть вызвано сильным кровотечением.
Тромбоцитопатии — нарушение функции тромбоцитов, приводящие к повышенной кровоточивости. Могут быть обусловлены наследственными заболеваними, приемом лекарственных препаратов (например, приемом ацетилсалициловой кислоты) и другими факторами.
Нарушение коагуляционного гемостаза 2
К этому типу нарушений относятся коагулопатии — геморрагические диатезы, при которых кровь нормально не сворачивается. Они бывают наследственными и приобретенными.
К наследственным заболеваниям относится гемофилия, при которой отсутствуют или содержатся в недостаточном количестве некоторые факторы свертывания, вследствие чего кровь не сворачивается нормально.
У больных с приобретенными коагулопатиями может возникать дефицит сразу нескольких факторов свертывания крови. К нарушениям коагуляционного гемостаза относится гиперкоагуляция, при которой повышается способность крови к образованию тромбов.
К коагулопатиям также относится ДВС-синдром (диссеминированное внутрисосудистое свёртывание, синонимы: коагулопатия потребления, тромбогеморрагический синдром).
При ДВС-синдроме последовательно происходят два патологических процесса 2 :
- Нарушение свертывания крови, вследствие которого нарушается циркуляция в мелких сосудах
- Нарушение образования кровяных сгустков вследствие нарушений в системе гемостаза и, как результат, неконтролируемые кровотечения.
Яркое свидетельство ДВС-синдрома — образование в мелких сосудах тромбов.
Причинами развития ДВС-синдрома могут быть инфекции, сепсис, шок, ожоги, нарушение течения беременности, острый лейкоз, другие состояния и заболевания.
При подозрениях на нарушения гемостаза врачом могут быть назначены различные лабораторные исследования крови, позволяющие выявить указанные нарушения.
Система свертывания крови и инфекция: любовь или ненависть
Бактерия не позволяет образоваться тромбу вокруг себя
Реакция нашего организма на появившуюся в кровотоке бактериальную инфекцию — комплексный ответ, в котором участвуют клетки и компоненты иммунной системы, системы свертывания крови, обязательно подключаются клетки эндотелия, выстилающие кровеносные сосуды, и все это дополняется ответами печени и эндокринной системы.

Фото: Виталий Волобуев, Коммерсантъ / купить фото
Фото: Виталий Волобуев, Коммерсантъ / купить фото
Даже реакция одной из перечисленных систем — системы свертывания крови — многосторонняя. Система свертывания крови традиционно делится на два взаимосвязанных звена — тромбоцитарное и плазменное. Тромбоцитарное свертывание — это активация, адгезия (прилипание) к поверхности и агрегация (слипание друг с другом) клеток — тромбоцитов. Плазменное свертывание — это последовательная активация белков-протеаз (ферменты, расщепляющие другие белки), приводящая к полимеризации белка плазмы крови фибриногена в длинные разветвленные нити фибрина и образованию сгустка (этот процесс напоминает образование желе).
На бактериальную инфекцию реагирует оба звена свертывания крови. Тромбоциты образуют агрегаты вокруг бактерий и могут их поглощать (фагоцитоз). Также тромбоциты «узнают» бактериальные паттерны и выпускают тромбоцитарные антимикробные вещества. Во всех перечисленных случаях тромбоциты запускают активацию иммунной системы организма. В свою очередь, бактерии образуют колонии на тромбоцитах и тромбах, таким образом закрепляясь в кровотоке. Свертывание плазмы не менее сложно взаимодействует с бактериальной инфекцией: кроме запуска от чужеродной поверхности — бактериальной стенки, образование фибринового сгустка запускается специфическими бактериальными протеазами, также подавляющими фибринолиз — физиологический процесс деградации тромбов. Причем все перечисленные ответы на молекулярном уровне специфичны для рода, а то и вида патогенных бактерий.
Наша команда, базирующаяся в Национальном медицинском исследовательском центре детской гематологии, онкологии и иммунологии им. Дмитрия Рогачева, исследует все аспекты активации системы свертывания крови как при физиологических процессах, так и при патологии. Один из проектов, который мы вели несколько лет, был посвящен вопросам ответа системы свертывания крови на липополисахариды (ЛПС) — компоненты клеточной стенки грамотрицательных бактерий (например, кишечной палочки). Уровень этого ответа оказывается жизненно важным при острых бактериальных инфекциях, вызывающих спонтанную коагуляцию крови — диссеминированное внутрисосудистое свертывание (ДВС), когда слишком бурная реакция системы приводит к резкому снижению концентрации белков и тромбоцитов и, как следствие, геморрагии в сочетании с нарушением микроциркуляции в органах. В настоящее время в клинической практике лечение ДВС в зависимости от фазы проводится антиагрегантами (такими как аспирин), антикоагулянтами (производные гепарина), компонентами плазмы и тромбоконцентратами, то есть лечение не нормализует свертывание, а сдвигает баланс в сторону его ослабления или усиления (подробнее — «Практическая коагулология», ред. А. И. Воробьев, Москва, 2012). Понимание молекулярных механизмов реакции системы свертывания крови на бактерии позволит существенно улучшить современные подходы к терапии ДВС.
В этом проекте мы стартовали с взаимодействия плазменного звена свертывания крови с ЛПС. После нескольких серий экспериментов мы пришли к выводу, что воздействие ЛПС является достаточно слабым и сильно зависит от донора. При анализе данных с помощью компьютерного моделирования был сделан вывод, что свертывание крови может «стартовать» с образованных (в результате работы иммунной системы) агрегатов ЛПС, однако одиночные молекулы ЛПС, связываясь с белками-протеазами, скорее подавляют свертывание крови.
Отдельно рассматривались механизмы активации свертывания крови в результате вызванного бактериями воспаления, когда либо сами клетки эндотелия, либо клетки иммунной системы на своей поверхности выставляют белок — тканевый фактор, запускающий всю систему свертывания крови. С помощью компьютерного моделирования мы показали, что при гибели таких клеток, когда образуется множество мембранных везикул — «пузырьков» размером 10–100 нм, свертывание плазмы крови запускается наиболее интенсивно из-за повышенной аффинности («любви») протеаз свертывания к искривленной поверхности.
Клетки крови, тромбоциты, могут взаимодействовать с ЛПС через специальные белки-рецепторы на своей поверхности, так называемые Toll-подобные рецепторы. Кстати, такие же рецепторы отвечают за активацию ЛПС клеток иммунной системы и приводят к развитию воспаления. Однако, к нашему удивлению, для тромбоцитов прямой активации ЛПС мы не смогли идентифицировать, несмотря на наличие функциональных Toll-подобных рецепторов. После множества экспериментов в коллаборации с группой профессора С. П. Гамбаряна из Института эволюционной физиологии и биохимии им. И. М. Сеченова (Санкт-Петербург) мы показали, что ЛПС даже вызывают небольшое подавление активации тромбоцитов.
Таким образом, мы получили, что компоненты бактериальной клеточной стенки, липополисахариды, сами по себе либо не воздействуют на систему свертывания крови, либо вызывают подавление активации свертывания. Такое поведение — подавление свертывания крови — характерно для многих бактерий, ведь образование тромба вокруг бактерии может помешать ее распространению в организме. Описанная выше острая реакция на бактериальную инфекцию для случая кишечной палочки, скорее всего, связана с активацией системы свертывания в результате общего процесса воспаления, запущенного бактериями в организме. В настоящее время мы продолжаем изучение активации системы свертывания крови при воспалении и при других взаимодействиях с иммунной системой, по проектам, поддержанным РФФИ и РНФ, а также фонда «Врачи, инновации, наука — детям».
Результаты получены в рамках проекта «Выявление мишеней для фармакологического воздействия на свертывание крови при бактериальной инфекции», поддержанного совместно РФФИ и правительством Москвы.
Анастасия Свешникова, руководитель проекта, д.ф.-м.н., в.н.с. лаборатории клеточного гемостаза и тромбоза НМИЦ ДГОИ
Как свертывается кровь
При помощи гемостаза организм прекращает кровотечение из поврежденных кровеносных сосудов. Гемостаз включает свертывание крови.
Слишком низкое свертывание может вызвать чрезмерное кровотечение от незначительной травмы.
Слишком интенсивное свертывание также может приводить к закупорке кровеносных сосудов, которые не кровоточат.
Таким образом, в организме имеются контролирующие механизмы, ограничивающие свертывание и растворяющие ненужные сгустки. Аномалия, возникающая в любой компоненте контролирующей свертывание системы, может привести к избыточному кровотечению Кровоподтеки и кровотечение Появление кровоподтеков или кровотечения после травмы является нормальным (см. также Как свертывается кровь). Но у некоторых людей имеются расстройства, в результате которых кровоподтеки или. Прочитайте дополнительные сведения . Фрагменты сгустков из вен на ногах, в области малого таза или брюшной полости могут перемещаться с током крови в легкие и закупоривать расположенные там крупные артерии ( тромбоэмболия легочной артерии Тромбоэмболия легочной артерии (ТЭЛА) Тромбоэмболия легочной артерии — это закупорка артерии в легком (легочной артерии) твердым веществом (эмболом), поступившим с кровотоком, как правило, кровяным сгустком (тромбом) или реже другими. Прочитайте дополнительные сведения ).
Гемостаз состоит из трех главных процессов:
Сужение (сокращение) кровеносных сосудов
Активация клеткоподобных частиц крови, которые способствуют свертыванию ( тромбоцитов Тромбоциты Основные компоненты крови включают: плазму; эритроциты; лейкоцитов; тромбоциты. Прочитайте дополнительные сведенияАктивация присутствующих в крови белков, которые вместе с тромбоцитами участвуют в свертывании (факторов свертывания крови)
Сгустки крови: Закупоривание разрывов
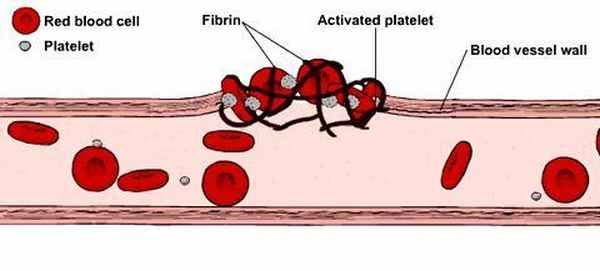
Тромбоциты активируются в том случае, если травма приводит к разрыву стенок кровеносного сосуда. Они меняют форму с круглой на игольчатую, приклеиваются к стенкам пораженного сосуда и друг к другу и начинают закупоривать разрыв. Также они взаимодействуют с другими белками крови, что приводит к образованию фибрина. Нити фибринов образуют сеть, которая захватывает большее количество тромбоцитов и клеток крови, формируя сгусток, который закупоривает разрыв.
Факторы кровеносного сосуда
Поврежденный кровеносный сосуд сокращается, поэтому кровь проходит по нему медленней, что позволяет запустить процесс свертывания. В то же время кровь, скопившаяся за пределами кровеносного сосуда (гематома), давит на сосуд, помогая предотвратить дальнейшее кровотечение.
Факторы тромбоцитов
При повреждении стенок кровеносного сосуда серия реакций активирует тромбоциты Тромбоциты Основные компоненты крови включают: плазму; эритроциты; лейкоцитов; тромбоциты. Прочитайте дополнительные сведенияФакторы свертывания крови
Образование тромба также включает активацию каскада факторов свертывания крови, которые представляют собой белки, вырабатываемые преимущественно в печени. Существует более десятка факторов свертывания крови. Они взаимодействуют в сложной цепи химических реакций, которые в конечном итоге приводят к образованию тромбина. Тромбин превращает фибриноген (фактор свертывания, в нормальных условиях растворенный в крови), в длинные цепи фибринов, которые отходят от слипшихся тромбоцитов и формируют сеть, захватывающую большее количество тромбоцитов и клеток крови. Нити фибринов делают формирование сгустка крови более интенсивным и помогают удерживать его на месте, оставляя стенки сосуда закупоренными.
При тяжелом заболевании печени (например, циррозе Цирроз печени Цирроз — обширная деформация внутренней структуры печени, которая возникает при необратимой замене большого количества нормальной ткани печени нефункционирующей рубцовой тканью. Рубцовая ткань. Прочитайте дополнительные сведения . Поскольку печень нуждается в витамине К для синтеза некоторых факторов свертывания крови, недостаточность витамина К Дефицит витамина К Дефицит витамина К чаще всего встречается у младенцев, особенно получающих кормление грудью. Этот дефицит может вызвать кровотечение, поэтому все новорожденные должны получать инъекцию витамина. Прочитайте дополнительные сведения может вызвать чрезмерное кровотечение.
Прекращение свертывания
Реакции, приводящие к формированию сгустков крови, уравновешиваются другими реакциями, останавливающими процесс свертывания крови и растворяющими сгустки после заживления кровеносных сосудов. Если такая система контроля не функционирует, даже незначительные повреждения кровеносных сосудов могут запускать масштабное свертывание крови во всем организме, как это и происходит при некоторых заболеваниях.
Лекарственные препараты и сгустки крови
Взаимосвязь между лекарственными препаратами и способностью организма контролировать кровотечения (гемостазом) является достаточно сложной. Способность организма формировать сгустки крови имеет критическое значение для гемостаза, но слишком интенсивное свертывание крови увеличивает риск инфаркта миокарда Острые коронарные синдромы (Боль в сердце; Инфаркт миокарда; Нестабильная стенокардия) Острые коронарные синдромы развиваются в результате внезапной блокады венечной артерии. Такая блокада вызывает нестабильную стенокардию или инфаркт миокарда, в зависимости от локализации и выраженности. Прочитайте дополнительные сведенияНекоторые люди находятся в зоне высокого риска формирования сгустков крови и целенаправленно принимают лекарственные препараты, позволяющие снизить такой риск. Также люди могут принимать лекарственные препараты, которые уменьшают сцепляемость тромбоцитов, благодаря чему тромбоциты не связываются друг с другом, блокируя кровеносные сосуды. К числу лекарственных препаратов, которые снижают активность тромбоцитов, относятся аспирин, тиклопидин, клопидогрел, прасугрел, абциксимаб и тирофибан.
Другим людям с риском формирования сгустков крови могут назначаться антикоагулянты Антикоагуляция Тромбоэмболия легочной артерии — это закупорка артерии в легком (легочной артерии) твердым веществом (эмболом), поступившим с кровотоком, как правило, кровяным сгустком (тромбом) или реже другими. Прочитайте дополнительные сведения — лекарственные препараты, подавляющие активность белков крови, которые называют факторами свертывания крови. Антикоагулянты часто называют «препаратами, разжижающими кровь», но в действительности они не делают кровь более жидкой. К числу антикоагулянтов, используемых чаще всего, относятся варфарин, принимаемый внутрь, и гепарин, который вводится в виде инъекции. Прямые пероральные антикоагулянты (ППАК) ингибируют непосредственно тромбин или активированный фактор X — высокоактивные белки, необходимые для свертывания крови. Примеры ППАК включают дабигатран, апиксабан, эдоксабан и ривароксабан.
Людям, получающим варфарин или гепарин, необходимо тщательное медицинское наблюдение. Врачи контролируют воздействие этих препаратов при помощи анализов крови, измеряющих время, которое необходимо для формирования сгустка, и регулируют дозу в соответствии с результатами анализов. Слишком низкие дозы могут оказаться неэффективными с точки зрения предотвращения формирования сгустков крови, а слишком высокие дозы могут приводить к серьезным кровотечениям. Другой тип антикоагулянтных препаратов, таких как низкомолекулярный гепарин, не требует такого тщательного наблюдения. Пациентам, получающим ППАК, не требуются частые лабораторные исследования свертываемости.
Если у человека уже имеется сгусток крови, то для ускорения растворения такого сгустка могут использоваться тромболитики (фибринолитические лекарственные препараты). Тромболитики, включая стрептокиназу и тканевой активатор плазминогена, в некоторых случаях используются для лечения сердечных приступов и инсультов, вызванных сгустками крови. Эти лекарственные препараты могут спасти жизнь, но иногда повышают риск возникновения серьезных кровотечений. Гепарин, лекарственный препарат, который назначают для снижения риска формирования сгустков крови, в некоторых случаях оказывает непредсказуемое парадоксальное воздействие и активирует тромбоциты, что приводит к увеличению вероятности образования сгустков крови ( гепарин -индуцированной тромбоцитопении-тромбозу).
Эстроген , принимаемый отдельно или в составе пероральных контрацептивов, может оказывать непредусмотренное воздействие и повышать свертываемость крови. Определенные лекарственные препараты, которые используются для лечения злокачественных заболеваний (химиотерапевтические препараты), также могут увеличивать риск формирования сгустков крови.
ПРИМЕЧАНИЕ: Это — пользовательская версия ВРАЧИ: Нажмите здесь, чтобы перейти к профессиональной версии
Авторское право © 2022 Merck & Co., Inc., Rahway, NJ, США и ее аффилированные лица. Все права сохранены.
Читайте также:
- Язва желудка - диагностика
- Склеродермия пищевода - диагностика
- Допплерографические синдромы мозгового кровотока. Внутричерепная гипотензия
- Хроническое отравление метгемоглобинобразователями. Показатели хронического отравления аминами
- Папилломатозный мягкий эпидермальный невус. Бородавчатый эпидермальный невус.
