КТ, МРТ при денервационной гипертрофии
Добавил пользователь Владимир З. Обновлено: 30.01.2026
Идиопатические воспалительные миопатии (ИВМ)- гетерогенная группа аутоиммунных заболеваний, общим признаком которых является воспаление поперечно-полосатой мускулатуры с развитием слабости, преимущественно проксимальных групп мышц конечностей. К ИВМ относятся дерматомиозит (ДМ) (в том числе ювенильный и паранеопластический), полимиозит (ПМ), спорадический миозит с включениями (СМВ) и иммуно-зависимая некротизирующая миопатия (ИЗНМ).
ИВМ – относятся к редким заболеваниям, так заболеваемость ДМ 1.4 на 100 000 населения, ПМ 3.8 на 100 000. СМВ наиболее часто встречающаяся миопатия после 50-ти лет. Его распространенность колеблется от 9.3 до 51.3 на миллион лиц после 50-ти лет.
Учитывая редкость ИВМ, разнообразие их клинических проявлений, наличие большого числа нервно-мышечных заболеваний с похожей симптоматикой, а также отсутствие простых диагностических тестов, подтверждающих диагноз, выявление их может представлять определенную сложность.
Длительное время диагноз ДМ и ПМ устанавливался на основании критериев Bohan и Peter 1975г. В 2017г были опубликованы классификационные критерии ИВМ, предложенные EULAR/ACR. Новые критерии впервые рассчитаны и на взрослых, и на детей, а также могут быть применены у больных без биопсии мышц. Критерии включают две части – клинические признаки и лабораторные и/или морфологические признаки, оцениваемые в баллах. (таблица 1)
Если биопсия мышц не проводилась, диагноз вероятной воспалительной миопатии устанавливается при общей сумме балов ≥ 5.5, если данные биопсии учитывались – при сумме балов ≥ 6.7. Диагноз определенной ИВМ устанавливается без биопсии при сумме балов ≥ 7.5, а с биопсией ≥ 8.7.
Возможность установить диагноз ИВМ без проведения биопсии можно отнести к преимуществам данных критериев, так как биопсия не всегда доступна. Она является инвазивным вмешательством, способным вызвать осложнения, особенно у больных, получающих ГК, и не всегда является информативной. Диагноз ИВМ достаточно прост в случае классического дебюта заболевания, типичного распределения мышечной слабости, наличия кожных изменений, характерных для дерматомиозита. Однако, при медленно-прогрессирующей мышечной слабости, отсутствии изменений кожи и других признаков системного заболевания клинических (конституциональных симптомов, полиартрита, интерстициального поражения легких или синдрома Рейно) и иммунологических, могут возникать диагностические ошибки. Наиболее сложным в клинической практике может быть дифференциальный диагноз между полимиозитом, спорадическим миозитом с включениями и заболеваниями группы поясно-конечностных мышечных дистрофий (ПКМД) с поздним дебютом. Так у пациентов с ИВМ и ПКМД отмечается прогрессирующая мышечная слабость, повышен уровень мышечных ферментов, миографическая картина характеризуется первично-мышечным уровнем поражения, а световая микроскопия может выявлять признаки мышечного воспаления. Маммен проанализировал, какие варианты невоспалительных миопатий наиболее часто могут имитировать ПМ. Наиболее часто за ПМ принимают дисферелинопатию, калпаинопатию и лице-лопаточно-плечевую мышечные дистрофии, т.к. при данных заболеваниях в мышечном биоптате можно выявить признаки воспаления. Также диагноз ПМ может быть ошибочно установлен при гликогенозах (болезнь МакАрдла, Помпе). СМВ также часто принимают за ПМ, что приводит к необоснованному назначению глюкокортикоидов этой категории больных. А гипотиреоидная и самолимитирующаяся статиновая миопатия могут быть неверно трактованы как ИЗНМ. У ревматолога также возникают сложности в дифференциальном диагнозе ПМ с другими нервно-мышечными заболеваниями, для которых характерен иной, не мышечный уровень поражения периферического нервно-мышечного аппарата (болезнь двигательного нейрона, нарушение нервно-мышечной передачи, или полинейропатии), для которых также типично развитие мышечной слабости и, изредка, может встречаться повышение уровня «мышечных» ферментов. В таких случаях осмотр невролога и комплексное электромиографическое (ЭМГ) исследование позволяет исключить ПМ. В тоже время, в редких случаях ПМ может иметь медленно-прогрессирующее течение, в связи с чем пациенту предполагают наследственный характер болезни и иммуносупрессивная терапия не назначается вовремя. Таким образом, врачи ревматологи и неврологи нуждаются в дополнительных методах обследования, позволяющий оценить состояние мышц. В клинической практике используются различные методы визуализации мышц, основным из которых является магнитно-резонансная томография.
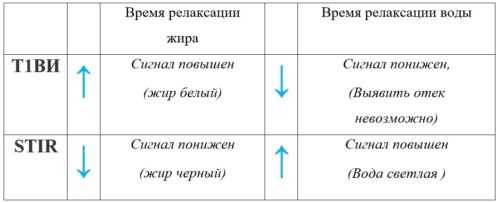
Более 20 лет при нервно-мышечных заболеваниях в клинической практике используется МРТ скелетных мышц. Данный метод дает объективную информацию о локализации и распространенности, симметричности патологического процесса, а также выявляет гипо- или гипертрофии различных мышц или мышечных групп. С помощью МРТ возможно более точно оценить избирательность поражения отдельных мышц в составе мышечных групп, которая не всегда выявляется при клиническом неврологическом обследовании. МРТ мышц — неинвазивный диагностический метод, позволяющий четко разграничить анатомические структуры исследуемой области: можно выделить отдельные мышцы, сосудисто-нервные пучки, подкожно-жировую клетчатку, фасции, кости. Кроме анатомических характеристик, МРТ позволяет оценить некоторые патофизиологические нарушения, в частности дегенеративные изменения, жировое замещение мышцы, наличие отека и воспалительных изменений скелетной мускулатуры. С помощью МР-томографа во фронтальной и аксиальной ориентации срезов и использованием Т1- и Т2-импульсных последовательностей мышц бедра и голени у больных с миопатиями получают серию изображений, позволяющий оценить состояние основных анатомических структур. Наиболее часто, в диагностике мышечных заболеваний используют аксиальную ориентацию срезов. Т1 взвешенное изображение позволяет оценить структуру мышц, их размер. Режим STIR (short tau inversion recovery) – приводит подавлению сигнала от жира, что позволяет отличить отек мышцы от жирового замещения. Применения режима STIR необходимо при диагностике ИВМ, т к позволяет визуализировать типичный для этой группы болезни воспалительный мышечный отек.
МР-последовательности и основные характеристики сред
При проведении МРТ основными анализируемыми параметрами являются мышечный отек (STIR), жировая дегенерация мышечной ткани и изменение размера мышц.
Мышечный отек – это неспецифический симптом, который может выявляться при ряде состояний: миозиты (аутоиммунный, инфекционный, саркоидный), рабдомиолиз, диабетический мионекроз, сосудистое повреждение (сосудистый инсульт), травматическое повреждение, после чрезмерной физической нагрузки, ранняя стадия оссифицирующего миозита, подострая денервация и радиационная травма.
Замещение мышц жировой тканью. Жировое замещение мышц может возникать как при первично-мышечных заболеваниях (наследственных мышечных дистрофиях), так и при хронических денервационных процессах (нейрональных заболеваниях, полинейропатиях), а также при длительной иммобилизации и на фоне приема глюкокортикоидов. Анализируется паттерн распределения данных изменений в мышцах у пациентов с миопатиями, что позволяет предположить нозологическую принадлежность мышечного заболевания и определить объем генетического исследования. Для определения степени дегенерации мышечной ткани при миопатиях используют шкалу E. Mercuri, в которой анализируются поперечные срезы мышц бедра и голени в режиме Т1.
Увеличение в размерах мышц, масс-эффект. Увеличение в размерах мышц может выявляться при пиомиозите, абсцессах, паразитарных заболеваниях, повреждениях (гематома), оссифицирующем миозите, мионекрозе, доброкачественных и злокачественных опухолях, фокальном пролиферативном миозите.
Преимуществом МРТ является большой объем анализируемых мышц, в отличие от мышечной биопсии, когда маленький по размеру биоптат берут из одной мышцы. В любом случае, при планировании выполнения биопсии мышц целесообразно провести МРТ, для более точного определения места взятия биоптата. При проведении биопсии важно, чтобы мышца имела признаки активного воспаления, но при этом с сохраненную мышечную структуру в Т1, т.к. при выраженным замещении мышцы жиром биопсия не информативна (что имеет значение в диагностике СМВ). Важно, что при подозрении на полимиозит, а МРТ следует направлять тех пациентов, у которых проведено ЭМГ исследование, и подтвержден первично-мышечный уровень поражения, т к при развитии денервации при МРТ может выявляться отек мышц, что может привести к неверной трактовке данного феномена и диагностическим ошибкам. Для оценки состояния мышц чаще всего проводится исследование мышц бедер и голеней, но имеется методика выполнения МРТ всего тела. Так, Huang и соавт. провели МРТ всего тела у 129 пациентов с ПМ и ДМ и у 105 пациентов выявили воспалительный отек мышц. Кроме этого были обнаружены 38 случаев интерстициального поражения легких, 12 опухолей (в том числе 5 злокачественных) и у больных 15 – остеонекроз костей. Таким образом, МРТ всего тела позволяет, наряду с отеком мышц, выявить ряд состояний, очень важных и актуальных для пациентов с ДМ и ПМ как в плане оценки состояния, так и терапии. В практическом отношении следует учитывать, что с целью дифференциального диагноза у пациентов с мышечными дистрофиями используется, как наиболее информативная, МРТ мышц бедер и голеней, поэтому в сложных дифференциально-диагностических случаях предпочтение следует отдать именно исследованию мышц нижних конечностей (бедра и голени). Интересно, что в отличие от наследственных миопатий, у больных ДМ/ПМ при исследовании в режиме Т1 в клинически слабых мышцах патологические изменения не выявляются (в течение первых лет от начала заболевания). Исключения составляют СМВ и некротизирующая миопатия, при которых параллельно с признаками воспаления, появляется жировая дегенерация мышцы.
Особенности МРТ в группе ИВМ: Важно подчеркнуть, что МРТ позволяет различить паттерны распределения поражения при разных клинических вариантах ИВМ. Так, при ДМ имеет место периферический отек мышц с паттерном по типу медовых сот, а также подкожный и фасциальный отек, тогда как для ПМ более характерны пятнистый или «туманный» паттерн распределения отека. При анализе МРТ картины мышц бедра у большой группы больных с различными клиническими вариантами ИВМ (101 с ИЗНМ, 176 ПМ, 219 ДМ, 17 пациентов с амиопатическим ДМ и 153 с СМВ) было показано, что в сравнении с пациентами с ДМ и ПМ у пациентов с ИЗНМ отмечается более выраженный мышечный отек, особенностью этих пациентов было раннее появление жирового замещения мышц и атрофии. Жировое замещение в первую очередь, затрагивало латеральный ротатор и ягодичные мышцы. Отек фасций наиболее характерен для пациентов с ДМ. Пациенты с ДМ и ПМ имели более сохранные мышцы бедер, по сравнению с пациентами с ИЗНМ.
Для СМВ типично сочетание как воспалительных изменений (которые выявляются при исследовании в режиме STIR), так и мышечной дегенерации с замещением жировой тканью мышечной. Для СМВ, как и для наследственных миопатий, типична избирательность поражения. Наиболее пораженными мышцами при СМВ четырехглавая мышца (за исключением относительно сохранной прямой мышцы бедра) и медиальная головка икроножной мышцы. Также для СМВ типичным является асимметричность поражения – на доминирующей стороне мышцы отличаются большей сохранностью. Tasca и соавт. выполнили МРТ мышц 17 пациентам с достоверным СМВ, 2 с вероятным СМВ и 118 пациентам с другими миопатиями. Были получены результаты, выявившие особенности поражения мышц при этом заболевании, свидетельствующие о высокой информативности данного метода в диагностике СМВ. Таким образом, МРТ мышц является надежным инструментом для пациентов с подозрением на СМВ, и м б особенно полезным у пациентов с ранней стадией заболевания, когда еще отсутствуют все типичные морфологические признаки этого заболевания. Продолжается сравнение информативности МРТ и биопсии мышц. В этом плане интересные данные получены норвежскими учеными, которые проанализировали 230 пациентов с ДМ и ПМ и выявили, что у 87% пациентов с полимиозитом и 82% пациентов с дерматомиозитом имеют место изменения по результатам МРТ, тогда как достоверные морфологические признаки получены у 70% пациентов с ПМ и 70% пациентов с ДМ. Для полимиозита и дерматомиозита типичным является повышение МР- сигнала в режиме STIR, что отражает наличие воспалительного отека в них. При ДМ признаки воспаления могут выявляться в коже и подкожно-жировой клетчатке (что отражает наличие панникулита в рамках ДМ). Учитывая высокую частоту выявления патологических изменений в мышцах при МРТ обсуждается возможность включения МРТ в диагностические критерии ИВМ. Недостатком данного метода исследования при ИВМ является отсутствие патогномоничных для ПМ и ДМ изменений. Для ВМ характерно наличие мышечного отека, который выглядит как усиление сигнала в режиме STIR, однако аналогичные изменения могут выявляться при денервационных процессах, повреждении, ишемии, мионекрозе и после чрезмерных физических нагрузок.
Клинический пример №1. Полимиозит. Пациентка Ф 73 лет: Впервые консультирована ревматологом в сентябре 2014г, когда стала отмечать небольшую мышечную слабость в мышцах бедер, тогда имели место жалобы на утомляемость и общую слабость. В течение 2014г года отмечала некоторое уменьшение мышечной силы, хотя при этом активно двигалась, могла поднять внука, но изредка чувствует неустойчивость при приседании на низкое и стало труднее вставать с низкого стула. В сентябре 2013г впервые в биохимическом анализе отмечались повышение АЛТ до 87 АСТ до 80 ед (КФК не исследовано), калий, СРБ – норма, Препараты, в том числе статины не принимает. В дальнейшем АЛТ и АСТ продолжало нарастать, уровень калия в норме, незначительная ТТГ 4,45 (норма до 4). 27.08.14 КФК 4340, миоглобин 849 (норма 73), АЛТ 232, АЛТ 158, ЛДГ креатинин 88, мочевина 4,8, о. белок 67г/л, СРБ в норме, калий 4,4, онкомаркеры в норме. Общий анализ мочи – норма, в повторном анализе 240, АСТ 153, КФК 3850, ЛДГ 1362. При осмотре в сентябре 2014: нормального питания. Кожные покровы чистые, мышечная сила 10 баллов во всех группах мышц. Чувствительных нарушений нет. В легких дыхание везикулярное, хрипов нет. Тогда мышечная слабость отсутствовала, пациентка была направлена к неврологу при и ЭМГ – признаки генерализованного активного первично-мышечного процесса, проведено МРТ мышц: практически норма, минимальный отек мышц в STIR. К лету 2015г пациентка не могла встать с корточек. С ноября 2015г – значительное прогрессирование мышечной слабости в мышцах плечевого пояса и бедер, туловища, стало трудно вставать с низкого стула, причесываться, снимать одежду через голову, (КФК 9500ед). Повторно МРТ выявило значительное повышение МР сигнала от мышц бедер и голеней. Проведен онкопоиск: гастроскопия, маммография, УЗИ полости малого таза, ранее КТ органов брюшной полости – без признаков ЗНО. При осмотре: Нормального питания, походка миопатическая, со стула встает с приемами Говерса, руки выше горизонтального уровня поднимает с затруднением. Мышечная сила снижена в дельтовидых и трехглавых мышцах до 6 баллов, в подвздошно-поясничных, четырехглавых мышцах до 7 баллов, в двуглавой мышце бедра до 8 баллов, при перемене положения из горизонтального в вертикальное положение – пользуется вспомогательными приемами.
КТ, МРТ при денервационной гипертрофии
а) Терминология:
1. Синоним:
• Нейрогенная мышечная гипертрофия
2. Определения:
• Псевдогипертрофия: генерализованное увеличение размеров мышц с увеличением объема внутримышечной жировой ткани
• Истинная гипертрофия: генерализованное увеличение размеров мышц, обусловленное увеличением объема мышечной ткани
б) Визуализация:
1. Общая характеристика:
• Лучший диагностический критерий:
о Генерализованное увеличение размеров мышц без нарушения структуры
• Локализация:
о Чаще поражаются нижние конечности:
- Типична изолированная денервация:
Обычно развивается псевдогипертрофия нижней конечности
Часто поражаются мышца, напрягающая широкую фасцию, и полуперепончатая мышца
- Классическим примером является мышечная дистрофия Дюшена:
Двусторонняя симметричная псевдодистрофия мышц голени
• Морфология:
о Крупные мышцы с гладкими краями и нормальной формой
2. Рекомендации по визуализации:
• Лучший метод визуализации:
о При МРТ и КТ наблюдается изменение мышечной массы без нарушения архитектоники мышечных волокон
• Советы по протоколу исследования:
о Увеличение размеров легче всего выявляется на аксиальных срезах
о Включение в область исследования противоположной конечности может оказаться полезным
о На Т1 ВИ лучше всего определяется увеличение объема внутримышечной жировой клетчатки при псевдогипертрофии
о Для выявления отека используйте последовательности, чувствительные к жидкости
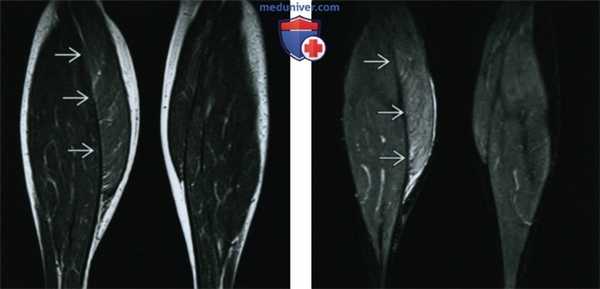
(Слева) МРТ Т1ВИ, корональный срез: при визуализации обеих нижних конечностей определяется диффузное увеличение размеров правой икроножной мышцы. На этой томограмме усилена интенсивность внутримышечного сигнала, обусловленная увеличением объема внутримышечной жировой ткани. Такая картина характерна для псевдогипертрофии.
(Справа) MPT STIR, корональный срез: у этого же пациента определяется повышение интенсивности внутримышечного сигнала в правой икроножной мышце. Такие отечные изменения наблюдаются как при истинной гипертрофии, так и при псевдогипертрофии.
3. КТ при денервационной гипертрофии:
• Увеличение размеров всей мышцы
• Отсутствие изменения контура или объемного образования с четкими контурами
• Сохранена нормальная внутренняя структура:
о Перистый рисунок внутримышечной жировой клетчатки не искажен
• При псевдогипертрофии увеличивается объем внутримышечной жировой ткани
о Нормальный перистый рисунок более выражен
4. МРТ при денервационной гипертрофии:
• Те же признаки, что описаны при КТ
• При псевдогипертрофии наблюдается увеличение интенсивности сигнала на Т1 ВИ
• ± внутримышечный отек: пятнистый или диффузный:
о Наблюдается как при псевдо-, так и при истинной гипертрофии
в) Дифференциальная диагностика денервационной гипертрофии:
1. Гипертрофия при избыточной нагрузке:
• Типичным примером являются спортсмены-тяжеловесы
• Определяется отек, вызванный отсроченной мышечной болью
• Обычно поражается более одной мышцы
2. Компенсаторная гипертрофия:
• Форма истинной гипертрофии, иная этиология
• Проведите диагностический поиск причины мышечных повреждений или недостаточности
• Например, гипертрофия мышцы, поднимающей лопатку, после обширной шейной диссекции
3. Отсроченная мышечная боль:
• Отсутствие увеличения размеров мышцы, объема внутримышечной жировой ткани
• Обычно поражается >1 мышцы
• Болезненность: возникает после нагрузки
4. Лимфома:
• Инфильтрация мышцы с искажением архитектоники
• Увеличение обычно является локальным
5. Идиопатическое доброкачественное увеличение жевательных мышц:
• Ограничено жевательными мышцами
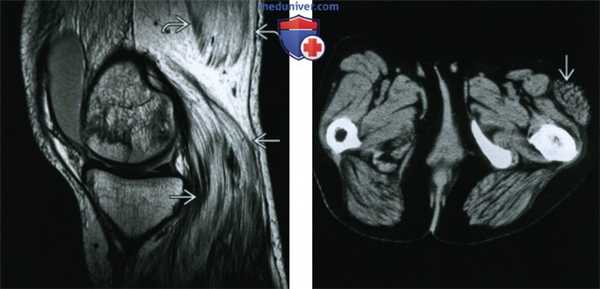
(Слева) МРТ, сагиттальный срез: исследование пациента с мышечной дистрофией. Обратите внимание на диффузное замещение икроножной и полуперепончатой мышц жировой тканью. Интересно, что эти мышцы не уменьшились в размерах и выглядят увеличенными. Эти изменения вносят вклад в увеличение икр, характерное для детей с этим заболеванием.
(Справа) КТ, аксиальный срез: определяется денервационная гипертрофия мышцы, напрягающей широкую фасцию бедра. Мышца увеличена за счет увеличения объема внутримышечной жировой ткани. Нарушения архитектоники ткани отсутствуют.
г) Патология:
1. Общая характеристика:
• Этиология:
о Частичное нарушение иннервации обусловливает избыточную стимуляцию оставшихся иннервированных мышечных волокон, размер которых увеличивается
о Механизм увеличения объема внутримышечной жировой ткани при псевдогипертрофии неизвестен
о Основные факторы:
- Поражение позвоночника, например грыжевое выпячивание межпозвонкового диска (наиболее часто); обычно на уровне S1
- Повреждение периферического нерва
- Мышечная дистрофия, особенно Дюшена
2. Микроскопия:
• Истинная гипертрофия: мелкие изогнутые мышечные волокна, нормальные волокна и гипертрофированные волокна:
о Поражаются волокна 1 и 2 типов
• Псевдогипертрофия: тот же спектр волокон, что и выше, в сочетании с увеличением объема жировой и других типов соединительной ткани между волокнами
д) Клинические особенности:
1. Проявления:
• Типичные признаки/симптомы:
о Безболезненное увеличение
• Другие признаки/симптомы:
о По данным ЭМГ подтверждается нарушение иннервации
2. Течение и прогноз:
• Сама по себе гипертрофия не имеет клинической значимости
• Клиническая значимость определяется выявленной причиной нарушения иннервации
3. Лечение:
• Направлено на основную причину нарушения иннервации
е) Список использованной литературы:
1. Evertsson К et al: р38 mitogen-activated protein kinase and mitogenactivated protein kinase-activated protein kinase 2 (MK2) signaling in atrophic and hypertrophic denervated mouse skeletal muscle. J Mol Signal. 9(1):2, 2014
Рентгенограмма, МРТ при синдромах Марфана и Элерса-Данлоса
а) Определения:
• Синдром Марфана (МФ): семейное заболевание, обусловленное пороком развития соединительной ткани с поражением опорно-двигательного аппарата, глаз и сосудов, но с вариабельной фенотипической экспрессией
• Синдром Элерса-Данлоса (ЭД): наследственное заболевание соединительной ткани с различными фенотипическими проявлениями (множество синдромов)
1. Непропорциональное удлинение конечностей (МФ, ЭД):
• Особенно кистей, стоп (арахнодактилия) в 89% случаев
2. Слабость связочного аппарата (МФ, ЭД):
• Патологическое искривление возможно в нескольких областях:
о Чаще возникает сгибательная деформация 5-го пальца (90°)
о Рекурвация коленного сустава, высокое стояние надколенника
• Реже нестабильность запястья
• Плоская стопа, вальгусная деформация большого пальца, молоткообразная деформация пальцев стопы
• Нестабильность суставов, вероятно обусловливающая хронические состояния:
о Повторяющаяся субклиническая травма
о Выпоты, гемартроз (ЭД>МФ)
о Ранний остеоартрит (ЭД>МФ)
• Вывихи суставов (наколенник, тазобедренный сустав, нижняя челюсть, ключица, пальцы) ЭД>МФ
• Протрузия вертлужной впадины
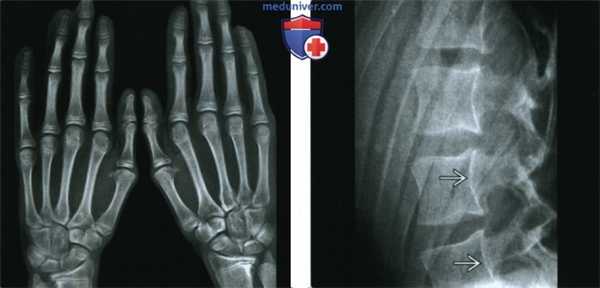
(Слева) Рентгенография кистей в ЗП проекции: определяется арахнодактилия при отсутствии других изменений. Наблюдается аномальный метакарпальный индекс.
(Справа) Рентгенография в боковой проекции, этот же пациент: определяется неровность задней поверхности тел позвонков. Плотность кости нормальная. На уровне позвонков L5-S1 был выявлен двусторонний спондилолизис с IV степенью спондилолистеза (изображение не представлено). Аномалии позвоночника в сочетании с арахнодактилией могут наблюдаться как при синдроме Марфана, так и при синдроме Элерса-Данлоса: в этом случае диагностирован синдром Марфана.
3. Мягкие ткани: различные проявления при МФ, ДМ:
• МФ: худощавость, атрофия мышц, скудная жировая клетчатка
• ЭД: подкожные кальцификации (некроз жировой ткани) в сочетании с повышенной частой гетеротопической оссификации
• При МРТ определяется слабость связочного аппарата, разрывы сухожилий, тендинопатия
4. Позвоночник (МФ, ЭД):
• Сколиоз (40-60%): картина схожа с идиопатическим сколиозом
• Неровность задней поверхности тел позвонков с эктазией твердой мозговой оболочки (63%):
о Также могут наблюдаться расширение отверстий, нарушение морфологии крестца
• Спондилолизис со спондилолистезом
• Подвывих атланто-аксиального сочленения (редко)
5. Грудная клетка (МФ, ЭД):
• Воронкообразная или килевидная деформация грудной клетки
6. Другие признаки:
• Плотность кости (МФ, ЭД): нормальная
• Эпифизиолиз головки бедренной кости (МФ, ЭД): ↑ частота встречаемости
в) Дифференциальная диагностика синдромов Марфана и Элерса-Данлоса:
1. Гомоцистинурия:
• Схожие признаки: непропорциональность длины конечностей, арахнодактилия и гиперподвижность суставов
• Клиническим признаком для дифференциального диагноза является задержка умственного развития
• Диффузная остеопения наблюдается при гомоцистеинурии, но не при других состояниях
• Большее число контрактур суставов
• Различный характер поражения глаз: двусторонний нижний вывих хрусталиков, возникающий в раннем детском возрасте
• Иной характер поражения сосудов: тромбоэмболия
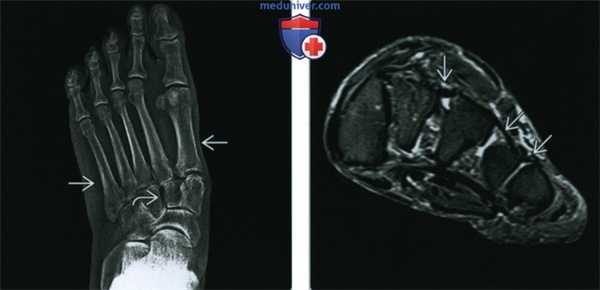
(Слева) Рентгенография в ПЗ проекции: плоская стопа, обусловленная болезнью Марфана. Наблюдается пронация переднего отдела стопы, определяемая по отклонению оснований плюсневых костей. Также имеется просвет между клиновидными костями, что говорит об ослаблении связок.
(Справа) МРТ Т2ВИ, режим подавления сигнала от жира, корональный срез: у этого же пациента определяется растяжение межклиновидных и межплюсневых связок В, что приводит к аномальному просвету между клиновидными и плюсневыми костями. На других изображениях (не представлены) определялись разрывы сухожилий, все это вносит вклад в формирование клинически плоской стопы, характерной для болезни Марфана.
г) Патология. Общая характеристика:
• Генетика:
о Синдром Марфана: обычно аутосомно-доминантный тип наследования; в 20-30% обусловлен спонтанными мутациями:
- Мутации в локусе (15q15-15q21) длинного плеча XV хромосомы (MFS1)
о ЭД: сложная классификационная система:
- Множество генетических дефектов, влияющих на синтез коллагена (не менее 19 фокусов минимум в 12 генах)
1. Проявления:
• Типичные признаки/симптомы:
о Синдром Марфана:
- Высокий рост, худощавость (> 95-го перцентиля)
- Непропорциональная длина конечностей относительно туловища):
Кисти, стопы > нижние конечности > верхние конечности
- Поражение сосудов:
Кистозный медионекроз с расслоением и разрывом аорты
Расширение проксимального отдела восходящей аорты → недостаточность аортального клапана и расширение венечных пазух
Медионекроз основной легочной артерии (менее часто)
Недостаточность аортального и митрального клапанов
- Поражение глаз:
Патологическое изменение подвешивающих связок → двусторонний вывих хрусталиков (в верхнем направлении) в 57% случаев
Также наблюдаются страбизм и отслоение сетчатки
о Диагностика синдрома Элерса-Данлоса основана на наличии клинической триады:
- Хрупкость кожных покровов:
Кожу можно приподнять с формированием высокой складки; со временем складки становятся постоянными; кожа легко рубцуется
- Гипермобильность суставов
- Хрупкость сосудов:
Желудочно-кишечные, кожные и бронхолегочные кровотечения
Спонтанное расслоение аорты или крупных сосудов, смерть от потери крови
- Встречается поражение глаз, но двусторонний вывих хрусталиков встречается менее часто, чем при МФ
2. Демография:
• Возраст:
о Симптомы часто не проявляются до детского возраста
• Эпидемиология:
о Синдром Марфана: 4-6 на 100000 новорожденных
3. Течение и прогноз:
• Средний возраст смерти при синдроме Марфана 28 лет; смерть вызвана сердечно-сосудистыми заболеваниями
4. Лечение:
• Устранение проблем, связанных с сердечно-сосудистой системой и органами зрения
• Реконструкция нестабильных слабых связок
е) Список использованной литературы:
1. Hammarstedt JE et al: Arthroscopic ligamentum teres reconstruction of the hip in Ehlers-Danlos syndrome: a case study. Hip Int. 0, 2015
1. Аббревиатура:
• Гипертрофия мышцы, поднимающей лопатку (МПЛ)
2. Определения:
• Повреждение ЧН XI ведет к денервационной атрофии ипсилатеральных трапециевидной и грудинно-ключично-сосцевидной мышц
• Функциональная гипертрофия МПЛ возникает в ответ на атрофию грудино-ключично-сосцевидной и трапециевидной мышц
1. Общая характеристика:
• Лучший диагностический критерий:
о Асимметричное увеличение МПЛ на фоне атрофии трапециевидной и грудино-ключично-сосцевидной мышц:
- Признаки шейной лимфодиссекции (отсутствие внутренней яремной вены, нарушение строения клетчаточных пространств, лежащих возле сонного влагалища, иногда отсутствие грудино-ключично-сосцевидной мышцы)
• Морфология:
о Мышца увеличена, контуры выпуклые
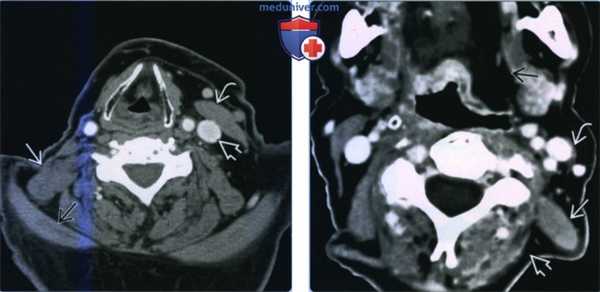
(Слева) КТ с КУ, аксиальная проекция, пациент, несколько месяцев назад перенесший радикальную шейную лимфодиссекцию. Справа определяется гипертрофия мышцы, поднимающей лопатку. Внутренняя яремная вена и грудино-ключично-сосцевидная мышца слева нормальные. Трапециевидная мышца атрофирована.
(Справа) КТ с КУ, аксиальная проекция. Параганглиома яремного отверстия (не показана) стала причиной гипертрофии мышцы, поднимающей лопатку, и атрофии трапециевидной и грудино-ключично-сосцевидной мышц. Также имеется атрофия языка с его жировой инфильтрацией.
2. Рентгенологические данные:
• Рентгенография:
о Рентгенограмма органов грудной клетки:
- Атрофия трапециевидной мышцы, увеличение тени от МПЛ
3. КТ при гипертрофии мышцы поднимающей лопатку:
• КТ с КУ:
о Хроническая стадия: гипетрофия МПЛ; плотность мышцы в пределах нормы
о Поиск причины:
- Наиболее распространенная - шейная лимфодиссекция с той же стороны:
Удаление внутренней яремной вены, грудино-ключично-сосцевидной мышцы и спинномозговой ветви добавочного нерва
Денервационная атрофия одноименной трапециевидной мышцы
- Редкие причины: опухоли яремного отверстия (параганглиома, шваннома, менингиома, метастазы):
Повреждение ЧН X: паралич голосовой складки стой же стороны
Повреждение ЧН XI: атрофия трапециевидной и грудино-ключично-сосцевидной мышцы с той же стороны
Повреждение ЧН XII: атрофия и жировая инфильтрация половины языка с той же стороны
4. МРТ при гипертрофии мышцы поднимающей лопатку:
• Т1ВИ:
о Увеличение МПЛ на фоне атрофии трапециевидной мышцы
о После проведенной радикальной шейной лимфодиссекции будут отсутствовать внутренняя яремная вена и грудино-ключично-сосцевидная мышца
• Т2ВИ:
о Острая стадия: возможен гиперинтенсивный сигнал
о Хроническая стадия: увеличение мышцы, сигнал нормальной интенсивности
• Т1ВИ с КУ:
о Подострая стадия: накопление контраста чуть интенсивнее, чем в норме
о Хроническая стадия: увеличение мышцы, контуры выпуклые
5. Рекомендации по визуализации:
• Лучший метод визуализации:
о Состояние после радикальной шейной лимфодиссекции
- МРТ выполняется в качестве контроля у пациентов с плоскоклеточным раком верхних отделов дыхательного и пищеварительного трактов
- Наиболее распространенным методом динамического наблюдения является КТ с контрастированием
о Опухоли основания черепа:
- При наличии нейропатии других черепных нервов (IX—XII) следует заподозрить опухоль основания черепа
- Оптимальный метод диагностики - КТ без КУ+МРТ FS с КУ
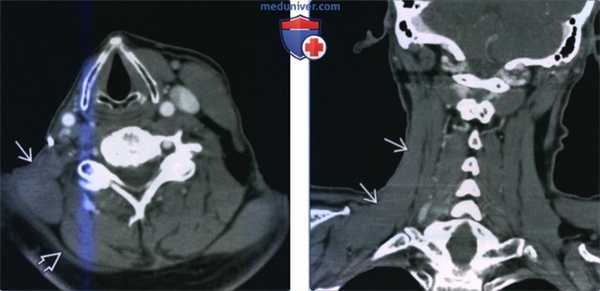
(Слева) КТ с КУ, аксиальная проекция. Гипертрофия правой мышцы, поднимающей лопатку. Обратите внимание, что при радикальной шейной лимфодиссекции правые грудино-ключично-сосцевидная мышца и внутренняя яремная вена были удалены. Трапециевидная мышца атрофирована вследствие повреждения добавочного нерва в ходе операции.
(Справа) КТ с КУ, сагиттальная проекция. Мышца, поднимающая лопатку, гипертрофирована на всем протяжении. Плотность мышцы нормальная.
в) Дифференциальная диагностика гипертрофии мышцы поднимающей лопатку:
1. Атрофия контрлатеральной МПЛ:
• Следствие денервации:
о Сдавливание корешков СЗ, С4 и/или С5 вследствие шейного спондилеза, поражения межпозвоночных дисков
2. Новообразование МПЛ:
• Воспалительные образования
• Доброкачественные опухоли: липома, шваннома, другие
• Злокачественные опухоли: инвазивный плоскоклеточный рак, саркома, другие
г) Патология. Общая характеристика:
• Этиология:
о Гипертрофия МПЛ возникает в ответ на атрофию грудино-ключично-сосцевидной и трапециевидной мышц
1. Проявления:
• Типичные признаки/симптомы:
о Пальпируемая «опухоль» в паравертебральном пространстве о Наличие в анамнезе шейной лимфодиссекции по поводу плоскоклеточного рака
• Другие признаки/симптомы:
о При опухолях основания черепа - денервационные изменения в области иннервации ЧН IX—XII
2. Демография:
• Эпидемиология:
о После консервативных вариантов шейных лимфодиссекций возникает реже
о Если ЧН XI в ходе лимфодиссекции был сохранен, гипертрофия не возникает
3. Лечение:
• Обнаружение данного «псевдозаболевания» позволяет избежать ненужной тонкоигольной биопсии
е) Диагностическая памятка:
1. Следует учесть:
• Если в анамнезе отсутствуют сведения об операциях на шее, причину паралича ЧН XI следует искать на уровне основания черепа или ствола мозга
2. Советы по интерпретации изображений:
• Отсутствие внутренней яремной вены и грудино-ключично-сосцевидной мышцы позволяет выявить истинную причину гипертрофии - наличие в анамнезе радикальной шейной лимфодиссекции
ж) Список использованной литературы:
1. Shpizner BA et al: Levator scapulae muscle asymmetry presenting as a palpable neck mass: CT evaluation. AJNR Am J Neuroradiol. 14(2):461-4, 1993
Лечение гипертрофии сердца
В России ежегодно умирает 1 млн 300 тыс. человек от болезней сердечно-сосудистой системы. При этом от 2 до 5 человек на 100 000 населения страдают от такого серьезного заболевания, как гипертрофия сердца. И примерно половина из них находится в возрасте от 20 до 35 лет. Больным ставится диагноз «гипертрофическая кардиомиопатия», сокращенно недуг обозначается как ГКМП. Это первичное поражение миокарда, при котором левый или правый желудочки увеличиваются в объеме. При этом медики разделяют ГКМП на симметричную и ассиметричную.
Гипертрофия левого желудочка
Это типичное заболевание среди гипертоников. При грамотном лечении гипертрофия левого желудочка сердца достаточно быстро перестает быть проблемой. Однако если пустить все на самотек, то летальный исход неизбежен. По статистике, 4 % случаев заканчиваются смертью. Опасность болезни в том, что гипертрофия левого желудочка сердца значительно ухудшает эластичность стенки.
Причины увеличения левого желудочка сердца:
- Гипертоническая болезнь вместе с гипертензией. Мышечные волокна миокрада деформируются из-за слишком высокой нагрузки на желудочек.
- Различные пороки сердца. Особенно часто причиной становится сужение аортального клапана.
- Атеросклероз аорты. В этом случае левый желудочек все время перегружен.
Проблема этой патологии в том, что лишь миокард становится больше. При этом сосуды и элементы проводящей системы не меняют свои размеры. Это постепенно приводит к тому, что развивается ишемия мышечных клеток. Сердечный ритм сбивается, а в левом желудочке скапливается много крови. Со временем это приводит к:
- сердечной недостаточности;
- блокадам;
- аритмии желудочков;
- инфаркту.
Гипертрофия правого желудочка
С этой части сердца и начинается малый круг кровообращения. По статистике врачей различных клиник, болезнь диагностируется обычно у новорожденных или детей постарше. При этом гипертрофия правого желудочка сердца является достаточно редким заболеванием. Оно может развиться также у:
В зависимости от размера желудочка болезнь разделяют на три этапа:
- Умеренное состояние. Правый желудочек может быть незначительно увеличен, но его масса равна левому.
- Среднее. Медики диагностируют изменения в размерах желудочка.
- Резко выраженное состояние. Желудочек значительно увеличивается, начинаются проблемы со здоровьем.
Причины, по которым развивается гипертрофия правого желудочка:
- бронхиальная астма;
- повышенное артериальное давление;
- легочная гипертензия;
- врожденные пороки сердца;
- сужение клапана легочной артерии.
Болезнь опасна тем, что могут быть затронуты легочные сосуды и артерии. Они теряют свою эластичность, что приводит к развитию склеротических процессов. Из-за этого недуга может развиться синдром Эйзенменгера, который особенно опасен для беременных женщин.
Признаки гипертрофии
Болезнь не сразу дает о себе знать определенными нарушениями в привычном образе жизни. Достаточно долго человек может вести себя как обычно. Поэтому так важно сразу распознать первые симптомы. Медики выделяют следующие признаки гипертрофии:
- одышка при обычной физической нагрузке и даже в покое;
- головокружения и обмороки (причем даже после приема пищи);
- приступы стенокардии во время физических нагрузок или стрессов;
- систолический шум;
- нарушение сердечного ритма.
Важно понимать, что гипертрофия сердца может вовсе не проявлять себя долгие годы. Иногда диагноз ставится уже посмертно, после вскрытия. Поэтому необходимо следить за состоянием здоровья и периодически обследоваться в медицинском центре.
Причины гипертрофии миокарда
Постепенно миокард может увеличиться в размерах, потерять эластичность. Это приведет или к серьезным проблемам со здоровьем, или даже к летальному исходу. Поэтому так важно знать, каковы причины гипертрофии миокарда. Медики обычно выделяют следующие факторы:
- постоянные чрезмерные физически нагрузки;
- приобретенные и врожденные пороки сердца;
- стрессы практически каждый день;
- артериальная гипертония;
- большой вес, ожирение;
- генетическая предрасположенность;
- проблемы с кровообращением.
Опытный врач при осмотре определит одну или несколько причин, а потом отправит на определенные обследования. Они позволят точно выяснить, что у больного гипертрофия сердца.
Диагностика заболевания
- эхокардиограмма для оценки работы сердца;
- анализ крови (необходимо знать количество холестерина, триглицеридов и др.);
- ЭКГ;
- стресс-тест;
- коронарная ангиография (необходимо оценить степень сужения артерий).
Как лечить гипертрофию сердца?
Как правило, болезнь удается купировать при помощи определенных лекарственных препаратов. Как лечить гипертрофию сердца, определяет только кардиолог. Он учитывает множество факторов:
- При отсутствии ярко выраженных симптомов достаточно принимать адреноблокаторы или блокаторы медленных кальциевых каналов.
- Если у больного умеренно выражены симптомы, то также показаны препараты, описанные выше. Как лечить гипертрофию левого желудочка сердца или правого, то есть дозировку, определяет только профессиональный кардиолог.
- При значительно выраженных симптомах могут дополнительно назначить диуретики.
- Если уже отмечены признаки обструктивной ГКМП, то необходимо срочно начинать профилактику инфекционного эндокардита.
Иногда требуется хирургическое вмешательство. Как можно лечить гипертрофию левого желудочка сердца таким способом, врач подробно расскажет на приеме. Обычно такая радикальная мера нужна тогда, когда симптомы выражены очень ярко, а лекарственные средства не дают должного эффекта.
К какому врачу обратиться?
Гипертрофия миокарда сердца и другие осложнения ГКМП не всегда диагностируются вовремя. В итоге лечение назначают тогда, когда недуг приводит к серьезным проблемам. Поэтому так важно знать, к какому врачу обратиться, чтобы вам была оказана всесторонняя помощь. В МХЦ сети «Открытая клиника» трудятся кардиологи с огромным опытом работы. Они определят признаки гипертрофии еще на первом осмотре. После этого врач выпишет направление на обследование, причем назначит лишь те процедуры, которые вам действительно необходимы.
После получения результатов КТ, МРТ, УЗИ, ЭКГ, анализа крови станет понятно, каким должно быть лечение гипертрофии сердца. После этого врач выпишет лекарственные препараты. Если возникнет вопрос о наблюдении и лечении в стационаре, то в МХЦ сети «Открытая клиника» вам будут предложены лучшие условия. Мы делаем все возможное, чтобы наши пациенты чувствовали себя комфортно в сложные периоды своей жизни.
Читайте также:
