Лабораторная диагностика отогенного сепсиса. Течение отогенного сепсиса
Добавил пользователь Евгений Кузнецов Обновлено: 29.01.2026
Лабораторная диагностика отогенного сепсиса. Течение отогенного сепсиса
В крови при отогенной пиемии в начале заболевания отмечается лейкоцитоз, редко превышающий, однако, 16 000 лейкоцитов (Я. С. Темкин), нейтрофилез, лимфопения, значительный сдвиг формулы белой крови влево, анэозинофилия и значительное ускорение РОЭ. По мере прогрессирования заболевания возникает и нарастает гипохромная анемия, анизоцитоз, пойкилоцитоз и полихромазия.
При чистых формах сепсиса нередко бывают нормальные цифры лейкоцитов и даже лейкопения, свидетельствующие об очень тяжелом течении. С. В. Байтерякова отмечала лейкопению у 10 из 13 тяжелобольных сепсисом и синустромбозом. Лейкопения сочеталась у них с резким сдвигом формулы крови влево, степень которого соответствовала тяжести процесса. При тяжелой интоксикации отмечалась также токсическая зернистость нейтрофилов.
Бактериологическое исследование крови, являясь одним из очень важных показателей сепсиса, все же не решаете абсолютной точностью диагностической задачи, особенно при отрицательных результатах посева. Наводнение крови бактериями происходит не непрерывно, а проникшие в ее ток микробы довольно быстро погибают. Поэтому посевы крови следует повторять многократно, соблюдая следующие правила: кровь брать в количестве не менее 10 мл во время подъема температуры и посев производить возможно быстрее.
Современные методы лечения привели к заметным изменениям клиники отогенного сепсиса и синустромбоза. Как упоминалось выше, значительно чаще сейчас стали встречаться афебрильные тромбозы и негнойные или невоспалительные осложнения, связанные с распространением процесса на вены мозга. В прежнее время они редко попадали под наблюдение клиницистов, так как стерилизация таких распространенных тромбов была недостижима, и больные обычно погибали от сепсиса, гнойных менингитов, энцефалитов и абсцессов мозга.
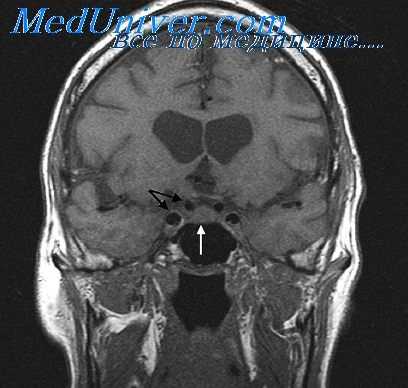
Довольно успешно излечивая эти грозные заболевания, но не устраняя связанных с тромбозом застойных явлений, антибиотики позволяют значительно чаще наблюдать теперь больных, у которых синустромбоз осложнился негнойным ограниченным энцефалитом, гидроцефалией и отеком мозга.
Применение современных антисептиков может также сопровождаться частичной стерилизацией тромба. В результате этого иногда еще до операции возникают длительные ремиссии, симулирующие излечение (Г. Н. Николаева). Под влиянием медикаментозной терапии изменился в известной мере и удельный вес отдельных симптомов. Наблюдая 60 больных, леченных до и после операции антибиотиками и сульфаниламидами, Г. Н. Николаева отметила следующие изменения симптоматики отогенного сепсиса:
1) значительно реже стали наблюдаться местные признаки осложнения — симптом Гризингера и болезненность по ходу яремной вены, что связано со сравнительно быстрой ликвидацией перифлебитических изменений;
2) температурная реакция, прослеживаемая с начала заболевания, остается и сейчас довольно типичным признаком сепсиса; однако антибиотики меняют характер кривой; высокие подъемы температуры наблюдаются редко и она быстро снижается до субфебрильного уровня, на котором может держаться, несмотря на применение пенициллина;
3) ознобы не являются теперь частым спутником септического осложнения;
4) в гемограммах, как правило, отмечается ускоренная РОЭ, эритропения и снижение гемоглобина; картина же белой крови стала менее характерной: количество лейкоцитов нередко остается нормальным;
5) наряду с этим внешний вид больных свидетельствует о тяжести заболевания: остается землистость или желтушность кожных покровов, сухой язык с налетом.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Отогенный сепсис
Отогенный сепсис – это синдромокомплекс, возникающий при системном распространении бактериальной микрофлоры из очага инфекции, находящегося в полости среднего или внутреннего уха. Клинические проявления включают в себя тяжелое общее состояние, гектическую лихорадку, чередование озноба с профузным потоотделением несколько раз в сутки, болезненность при пальпации позади сосцевидного отростка и по ходу кивательной мышцы. Диагностика основывается на данных анамнеза и физикального осмотра, результатах лабораторных тестов. Лечение заключается в нормализации гемодинамики, санации очага инфекции и рациональной антибактериальной терапии.
Общие сведения
Отогенный сепсис – одно из наименее распространенных осложнений в отоларингологии, возникающее в 2-4% от всех случаев поражения внутреннего или среднего уха. В тоже время, это состояние имеет самый высокий показатель летальности, который колеблется в широких пределах – от 5-21% при сохранении ясного сознания до 90% при пребывании пациента в состоянии комы. В среднем смертность составляет около 58%. Большинство больных с данным осложнением – лица с иммунодефицитом (от 50 до 75%). Патология с одинаковой частотой встречается у мужчин и женщин. Более чем в 85% случаев сепсис сочетается с другими отогенными осложнениями, чаще всего – с тромбозом синусов головного мозга.
Причины отогенного сепсиса
Заболевание является осложнением патологий среднего и внутреннего уха и возникает при попадании бактериальной флоры из инфекционного очага в общий кровоток. Чаще всего генерализация инфекционного процесса наблюдается на фоне острого гнойного среднего отита, мастоидита, хронического мезотимпанита и эпитимпанита, гнойного лабиринтита. В качестве возбудителей обычно выступают стафилококки и стрептококки, несколько реже – пневмококки и диплококки. В отдельных случаях болезнь вызывают протеи или синегнойная инфекция. Выделяют две группы факторов, увеличивающих риск развития септических осложнений:
- Иммунодефицитные состояния: гипогаммаглобулинемия, СПИД, аспления, лейкопения, онкогематологические заболевания. Снижение резистентности и нарушение реактивности организма обеспечивает быстрое развитие патологических изменений и бесконтрольное размножение патогенной микрофлоры.
- Морфологические особенности анатомических структур уха: дегисценция стенок барабанной полости, холестеатома, дополнительные лабиринтовые окна, незаращенная каменисто-чешуйчатая щель, большое количество складок и внутренних карманов крыши барабанной полости, ячеистая структура сосцевидного отростка облегчают проникновение инфекции за пределы внутреннего и среднего уха.
Патогенез
В основе патогенеза лежит проникновение бактерий и их токсинов в кровоток при гнойном расплавлении одной из стенок пораженной полости, происходящем из-за нарушения оттока экссудата, которое может быть обусловлено непроходимостью слуховой трубы или чрезмерной плотностью барабанной перепонки, затрудняющей ее перфорацию. При гнойном среднем отите основные пути распространения – верхняя стенка антрума, окно улитки и кольцевидная связка преддверия, при мастоидите – крыша пещеры среднего уха, площадка или верхушка сосцевидного отростка, при хронических мезо- и эпитимпаните – фистула в полукружном канале. При гнойном лабиринтите генерализация инфекции происходит через водопровод преддверия и падпаутинное пространство мостомозжечкового угла. Таким образом, бактерии попадают в среднюю черепную ямку, откуда проникают в сосуды и вместе с кровью распространяются по всему организму.
Классификация
В современной медицине принято выделять три основные клинические формы отогенного сепсиса. Все они представляют собой последовательные стадии развития патологических изменений в организме на фоне генерализации инфекции.
- Септицемия. Характеризуется проникновением патогенной микрофлоры в системный кровоток и развитием общего интоксикационного синдрома.
- Септикопиемия. В результате распространения инфекционных агентов по организму с током крови происходит формирование метастатических абсцессов в других тканях и органах.
- Бактериальный или септический шок. Возникает в результате массивного проникновения в систему кровообращения бактериальных токсинов, продуктов распада тканей и биогенных аминов. Септический шок проявляется критическим нарушением центральной и периферической гемодинамики, дисфункцией всех органов и систем.
Симптомы отогенного сепсиса
Первым признаком системного распространения инфекции является резкое ухудшение общего состояния на фоне длительного или тяжелого течения заболеваний уха. Наблюдается быстрый подъем температуры тела до 39,5-41,0 °C с последующим резким падением до 37,0-37,5 °C. Клинически это сопровождается ознобом и проливным потом. Типичная особенность у взрослых – возникновение подобных перепадов температуры 2-4 раза в сутки. У детей гипертермия имеет постоянный характер. Отмечается общее недомогание, одышка, тахикардия и головная боль, реже – тошнота и рвота. Кожа становится бледной, приобретает бурый землистый оттенок. Часто наблюдается желтушность склер, сухость языка и образование на нем белого налета.
Возможны боли в мышцах, суставах, в пояснице и области сердца. При тяжелой интоксикации выявляются признаки поражения нервной системы и нарушения сознания – бессонница, бред, сопорозное или коматозное состояние. При приеме антибиотиков признаки распространения инфекции могут быть «смазанными». Наряду с общими проявлениями обнаруживается очаговая симптоматика: вынужденное положение головы с наклоном в больную сторону, отечность и боль при пальпации мягких тканей за сосцевидным отростком (симптом Гризингера) и по боковой поверхности шеи вдоль переднего края кивательной мышцы (симптом Уайтинга).
Осложнения
Отогенный сепсис зачастую сопровождается развитием метастатических гнойных очагов в органах и тканях, куда патогенная микрофлора попадает гематогенным путем. Первое место по распространенности занимает поражение легких в виде двухсторонней очаговой пневмонии, которая при отсутствии срочной медицинской помощи приводит к смерти пациента. Нередко наблюдается поражение почек (пиелонефрит), сердца (эндокардит). Сепсис часто сочетается с отогенными внутричерепными осложнениями: гнойным менингитом, энцефалитом, тромбозом венозного синуса, абсцессами головного мозга или мозжечка.
Диагностика
Диагностика отогенного сепсиса осуществляется в сжатые сроки, поскольку пациенты зачастую находятся в тяжелом или критическом состоянии. При постановке диагноза важнейшую роль играет анамнез заболевания, в котором присутствуют острые или хронические заболевания уха. В диагностическую программу входят:
- Физикальное обследование. Помимо нарушения общего состояния определяется резкое снижение АД, специфические симптомы Уайтинга и Гризингера, которые являются признаками тромбоза внутренней яремной вены и сигмовидного синуса. При возможности отоларинголог проводит отоскопию для подтверждения отогенной этиологии сепсиса.
- Общий анализ крови. Методика позволяет выявить неспецифические признаки воспаления – высокий нейтрофильный лейкоцитоз и повышение СОЭ. О наличии сепсиса свидетельствует токсическая зернистость лейкоцитов, гипохромная анемия, дефицит альбуминов и снижение уровня общего белка.
- Бактериальный посев крови. Исследование дает возможность идентифицировать циркулирующего в системном кровотоке возбудителя. Используется для подтверждения диагноза и определения чувствительности высеянной микрофлоры к различным группам антибактериальных препаратов.
- Лучевые методы диагностики. По данным КТ височных костей может определяться деструкция сосцевидного отростка, исчезновение контуров пещеры среднего уха или наличие вместо нее узкого участка просветления с четкими границами, слияние антрума и аттика. При подозрении на синус-тромбоз выполняется синусография.
Отогенный сепсис дифференцируют с тромбоэмболией легочной артерии (ТЭЛА), острой почечной недостаточностью (ОПН) и тяжелой формой малярии. При ТЭЛА в анамнезе часто присутствует варикозное расширение вен, тромбофлебит, на рентгенограмме органов грудной клетки определяются симптомы острого легочного сердца и инфаркта легкого. ОПН характеризуется олигоанурией, нарастанием креатинина и мочевины в биохимическом анализе крови. При малярии лихорадка имеет цикличность в 3-4 дня, в ОАК и биохимическом исследовании крови выявляется острый гемолиз эритроцитов и признаки печеночной недостаточности.
Лечение отогенного сепсиса
Лечебная тактика заключается в ликвидации первичного очага и интенсивной антибактериальной терапии. В зависимости от основного заболевания, наличия осложнений и тяжести общего состояния применяются хирургические, медикаментозные и аппаратные методики.
- Хирургическое лечение. Его суть заключается в дренировании очага бактериальной инфекции. При необходимости осуществляется оперативное лечение внутричерепных осложнений. Выбор вмешательства определяется выявленными нарушениями.
- Антибиотикотерапия. Выбор лекарственных средств производится с учетом чувствительности возбудителя. Чаще всего применяются препараты из групп цефалоспоринов III-IV поколения, аминогликозиды, фторхинолоны и карбопенемы.
- Экстракорпоральная детоксикация. Может проводиться с использованием инфузионной терапии (переливание глюкозы, свежезамороженной плазмы и кровозамещающих препаратов, введение диуретиков) и аппаратными методами (плазмаферез, гемосорбция, гипербарическая оксигенация и др.).
- Патогенетическая и симптоматическая фармакотерапия. В разных клинических ситуациях могут вводиться десенсибилизирующие препараты, витамины группы В, сердечные гликозиды, обезболивающие, антикоагулянты и аналептики. При необходимости производится коррекция кислотно-щелочного состояния крови. На фоне выраженного иммунодефицита назначаются иммунокорректоры, антистафилококковая плазма, донорские иммуноглобулины.
Прогноз и профилактика
Отогенный сепсис – тяжелое заболевание, прогноз которого напрямую зависит от своевременности и рациональности оказания медицинской помощи. Патология почти всегда сопровождается образованием отдаленных абсцессов во внутренних органах. Чем больше и массивнее метастатические очаги инфекции – тем меньше шансов на благоприятный исход. К профилактическим мероприятиям относи тся ранняя диагностика и полноценное лечение заболеваний уха, соблюдение рекомендаций лечащего отоларинголога относительно антибактериальной терапии. Вторичная профилактика подразумевает коррекцию иммунодефицитных состояний и сопутствующих заболеваний, укрепление общих защитных сил организма и т. п.
Диагноз отогенного сепсиса. Дифференциация отогенного сепсиса
Отклонения от обычного ранее характера проявлений отогенного сепсиса стали теперь столь частыми, что говорить о типизме клинической картины в старом понимании не приходится. Это ставит перед современным отрлогом значительно более трудные, чем прежде, диагностические задачи.
Диагноз отогенного септического осложнения устанавливается легко в тех случаях, когда имеется выраженная картина местных и общих симптомов. Гектическая температура с ознобами или continua с картиной резкой интоксикации, высокий лейкоцитоз, нейтрофилез, сдвиг формулы влево и анэозинофилия позволяют в большинстве случаев остановиться на диагнозе септического состояния.
Одновременно существующий симптом Гризингера и болезненность при пальпации по ходу яремной вены заставляют связать это состояние с гнойным средним отитом, не предрешая, однако, вопроса о тромбическом или атромбическом характере первичного очага.
Выявление метастазов и получение культуры микробов из крови делают диагностику почти достоверной. Такая симптоматика иаблюдалась в большинстве случаев отогенного сепсиса и в досульфаниламидную эру. Применение антибиотиков заметно усложнило диагностику.

Поэтому тщательный анамнез, учитывающий характер первых общих симптомов осложнения, их соотношение по времени с появлением острого или обострения хронического отита и проводившееся ранее лечение, приобретает нередко для диагноза решающее значение.
Сопоставление этих данных с плохим самочувствием и общим состоянием больного и с повышенной температурой, пусть даже субфебрильной, но не исчезающей, несмотря на лечение антибиотиками, заставляет иногда заподозрить септическое осложнение. Проявления острого отита — мастоидита иногда настолько затушевываются антибиотиками, что в подозрительных случаях следует учитывать даже минимальные воспалительные изменения барабанной перепонки и костного слухового прохода и самые незначительные субъективные признаки (тяжесть в ухе, шум, особенно пульсирующий, длительное понижение слуха). В рентгенологической картине приходится больше внимания уделять затемнению клеток, чем симптомам костной деструкции (Розеивассер и Адельман).
Хронические гнойные эпитимпаниты, которым в настоящее время принадлежит ведущее место в развитии внутричерепных осложнений, легче поддаются учету. Однако и при них лечение антибиотиками иногда уничтожает специфический запах гноя и нередко быстро снимает наружные признаки поражения синуса.
Афебрильные синустромбозы удается, как правило, диагностировать лишь на операционном столе. При синустромбозах без выраженного септического состояния, ио сопровождающихся теми или иными общемозговыми или очаговыми симптомами, диагноз также чаще устанавливается во время операции. Положение облегчается тем, что такая симптоматика сама по себе служит показанием к производству вмешательства с обнажением твердой мозговой оболочки.
Затруднения при дифференциальном диагнозе иногда возникают при наличии гнойного среднего отита у больных брюшным тифом, малярией, бруцеллезом, милиарным туберкулезом, центральной пневмонией и др. Пенициллинотерапия, назначаемая с первых же дней лихорадочного заболевания, может усилить эти трудности, так как ведет к затушевыванию типичных для сепсиса клинической картины и изменений в белой крови. Использование всех дополнительных методов микробиологического, серологического и иммунологического исследований является, конечно, при этом обязательным. К сожалению, многие из них не обеспечивают ранней диагностики, так как становятся показательными в более поздние периоды болезни (например, реакция Видаля).
Трудности возникают иногда и при рожистом воспалении трепанационной раны, при котором покраснение кожи часто появляется несколько позднее, чем озноб и повышение температуры. Обильное выделение из раны и пышное разрастание отечных грануляций могут наблюдаться как при роже, так и при септическом осложнении. В результате перечисленных затруднений сейчас приходится несколько чаще, чем в досульфаниламидную эру, ставить диагноз отогенного синустромбоза во время операции.
Сепсис новорожденных
Сепсис новорожденных – генерализованная гнойно-септическая инфекция, характеризующаяся наличием первичного очага и циркуляцией инфекции в крови. Сепсис новорожденных проявляется признаками инфекционного токсикоза (температурной реакцией, вялостью, диспепсией, землистой окраской кожных покровов) и образованием гнойных метастатических очагов в различных органах (мозговых оболочках, легких, костях, печени и пр.). Диагноз сепсиса у новорожденных устанавливается на основании клинических критериев и выделения возбудителя при бактериологическом посеве крови. Лечение сепсиса новорожденных включает системную антибиотикотерапию, санацию первичного и метастатических гнойных очагов, посиндромную терапию.
Сепсис новорожденных – общий инфекционный процесс, обусловленный попаданием условно-патогенной и гноеродной микрофлоры из локальных очагов в кровяное русло и сопровождающийся тяжелыми системными проявлениями. По данным зарубежной педиатрии, частота сепсиса новорожденных составляет 0,1-0,8%; среди недоношенных и детей с перинатальной патологией, находящихся в ОРИТ, - 14%. Неонатальная смертность, обусловленная сепсисом новорожденных, высока и стабильна – около 30-40%. Развитию сепсиса способствуют недостаточная сформированность барьерных механизмов и иммунитета у новорожденных, пограничные состояния периода новорожденности, патологическое протекание перинатального периода, сложность ранней диагностики септических состояний.
Причины
В настоящее время доминирующее место (около 50%) среди возбудителей сепсиса новорожденных принадлежит грамположительной флоре (главным образом, стафилококкам, гемолитическому стрептококку группы А). Чуть реже (до 40% случаев) выявляется грамотрицательная микрофлора (кишечная палочка, синегнойная палочка, клебсиелла и др.); в 10% этиологическими агентами выступает смешанная флора (часто ассоциация стафилококка с грибами Candida).
Со стороны матери факторами, способствующими бактериальной контаминации новорожденного, выступают бактериальный вагиноз, кольпиты, эндометрит. Большое значение имеет степень и характер иммуносупрессии у новорожденного, которые могут быть связаны с неполноценным питанием или приемом лекарств беременной, наследственным иммунодефицитом или ВИЧ-инфекцией. В отдельных случаях причиной вспышек сепсиса новорожденных становится несоблюдение санитарного режима в родильных или детских отделениях.
По времени развития выделяют внутриутробный и постнатальный (ранний неонатальный и поздний неонатальный) сепсис новорожденных. Внутриутробный сепсис предполагает антенатальное или интранатальное инфицирование плода; при этом первичный гнойно-септический очаг располагается вне организма ребенка (чаще всего в его роли выступает плацентит, хорионит, хориоамнионит и т. д.). В случае постнатального сепсиса первичный гнойно-воспалительный очаг всегда располагается в организме самого новорожденного.
Ранний неонатальный сепсис новорожденных развивается в первые 4-ро суток жизни ребенка. Клинические течение заболевания обычно молниеносное, с быстрым развитием полиорганнной недостаточности, летальным исходом в 5-20% случаев. Поздний неонатальный сепсис новорожденных манифестирует на 5-й день и позднее. Характеризуется медленно прогрессирующим течением, возникновением вторичных септических очагов, 5-10%-ной летальностью.
Течение сепсиса новорожденных может быть молниеносным (3-7 дней), острым (до 4-8 недель), подострым (до 1,5-3 месяцев), затяжным (более 3 месяцев). С учетом локализации первичного септического очага и входных ворот различают: пупочный, кожный, легочный, ринофарингеальный, отогенный, риноконъюнктивальный, кишечный, урогенный, катетеризационный и др. виды сепсиса новорожденных. Сепсис новорожденных может протекать в форме септицемии или септикопиемии.
Симптомы сепсиса новорожденных
Септицемия или сепсис новорожденных без метастазов обычно развивается на фоне предшествующего мокнущего пупка, конъюнктивита, гнойничковой сыпи, опрелостей, стоматита. Предвестниками сепсиса новорожденных могут выступать вялость или беспокойство, снижение аппетита, обильные частые срыгивания, плохая прибавка в весе. В период разгара развивается температурная реакция (гипер- или гипотермия), отечный синдром или эксикоз, гипотрофия. Характерным признаком сепсиса новорожденных является грязновато-серый (землистый) оттенок кожных покровов, желтушность, мраморность кожи, сыпь.
Вследствие токсического поражения различных органов возникают гепатоспленомегалия, пневмопатия (тахипноэ, цианоз), кардиопатия (тахикардия или брадикардия, артериальная гипотензия), диспепсия, мочевой синдром (олигурия, анурия, ОПН), геморрагический синдром, надпочечниковая недостаточность. Чаще всего септицемия осложняется присоединением пневмонии, которая выступает как самостоятельное интеркуррентное заболевание.
Септикопиемия или сепсис новорожденных с гнойными метастазами характеризуется возникновением на фоне интоксикации вторичных очагов отсева в мозговых оболочках, легких, костях, печени, других органах. Чаще всего септикопиемия протекает с развитием гнойного менингита, абсцедирующей пневмонии, остеомиелита; реже – с формированием абсцесса печени, гнойного артрита, панофтальмита, медиастинита, флегмоны желудка или кишечника. В восстановительном периоде происходит санация пиемических очагов, стихание токсикоза, постепенное восстановление нарушенных функций.
Молниеносная форма сепсиса новорожденных протекает с развитием септического шока: стремительным ухудшением состояния ребенка, снижением температуры тела, брадикардией, кровоточивостью, отеком легких, острой почечной недостаточностью. Летальный исход при молниеносном течении сепсиса новорожденных наступает в течение 3-5 суток.
Диагностика сепсиса новорожденных
Диагноз сепсиса новорожденного может быть заподозрен неонатологом или педиатром на основании лихорадки свыше 3 дней или прогрессирующей гипотермии; гиперлейкоцитоза, сменяющегося лейкопенией; повышением содержания в крови маркеров инфекционного процесса (СРБ, интерлейкина-8, прокальцитонина).
Факт бактериемии при сепсисе новорожденных подтверждается путем посева крови на стерильность. Важное значение имеет выявление первичного гнойного очага и метастатических очагов, микробиологического исследование отделяемого из них (бактериологическое исследование мазка с конъюнктивы, мочи на микрофлору, соскоба/отделяемого с кожи на микрофлору, мазка из глотки, кала на дисбактериоз и т. п.).
Дифференциальная диагностика сепсиса новорожденных осуществляется с локализованными гнойно-воспалительными заболеваниями (пневмонией, медиастинитом, перитонитом, менингитом, энтероколитом), генерализованными вирусными инфекциями (цитомегалией, герпесом, энтеровирусной инфекцией) и микозами (кандидозом, аспергиллезом) и др. Для этого используются дополнительные лабораторные методы – ПЦР, ИФА, микроскопия.
Лечение сепсиса новорожденных
Терапия при сепсисе новорожденных проводится одновременно в нескольких направлениях и включает санацию септического и пиемических очагов, подавление циркуляции возбудителя в крови, коррекцию нарушенных функций.
Основу этиологического лечения сепсиса новорожденных составляет антибиотикотерапия: эмпирическая комбинированная до уточнения характера микрофлоры) и целенаправленная после получения антибиотикограммы. Противомикробные препараты вводятся внутривенно, в максимальных возрастных дозировках в течение 10-15 суток с последующей сменой. Чаще всего в клинической практике для лечения сепсиса новорожденных в различных сочетаниях используются цефалоспорины, аминогликозиды, аминопенициллины, карбапенемы и др.
С целью местного лечения гнойных очагов производится вскрытие фурункулов и абсцессов, перевязки с антибактериальными и ферментными препаратами; назначается УВЧ, СВЧ, электрофорез.
Патогенетическая терапия сепсиса новорожденных включает иммунокоррекцию (плазмаферез, гемосорбцию, введение иммуноглобулинов), проведение дезинтоксикационной терапии (внутривенной инфузии глюкозо-солевых растворов и свежезамороженной плазмы), адекватную кислородотерапию и т. д. При сепсисе новорожденных обязательно проводится мониторинг состояния жизненно-важных функций: АД, ЧСС, ЭКГ, КОС и газового состава крови, биохимических показателей (сахара крови, креатинина, электролитов), гематокрита.
В остром периоде сепсиса целесообразно пребывание новорожденных в кувезе, кормление материнским молоком, тщательный уход. В восстановительном периоде к лечению подключается гимнастика, массаж, лечебные ванны.
Прогноз и профилактика сепсиса новорожденных
Прогноз сепсиса новорожденных серьезный: летальность составляет от 30-40% до 60% среди глубоко недоношенных детей. У выздоровевших детей в отделенном периоде могут отмечаться частые ОРВИ, пиелонефрит, анемия, перинатальная энцефалопатия.
Профилактика сепсиса новорожденных включает выявление и санацию инфекций мочеполовой сферы у беременной, соблюдение противоэпидемических мероприятий медперсоналом родильных домов и отделений новорожденных, тщательный гигиенических уход за новорожденным, естественное вскармливание. Вопрос о сроках вакцинации новорожденных с сепсисом против туберкулеза и против гепатита В , проводимой в первые дни жизни, решается в индивидуальном порядке.
Сепсис
Сепсис - общая гнойная инфекция, развивающаяся вследствие проникновения и циркуляции в крови различных возбудителей и их токсинов. Клиническая картина сепсиса складывается из интоксикационного синдрома (лихорадки, ознобов, бледно-землистой окраски кожных покровов), тромбогеморрагического синдрома (кровоизлияний в кожу, слизистые, конъюнктиву), метастатического поражения тканей и органов (абсцессов различных локализаций, артритов, остеомиелитов и др.). Подтверждением сепсиса служит выделение возбудителя из культуры крови и локальных очагов инфекции. При сепсисе показано проведение массивной дезинтоксикационной, антибактериальной терапии, иммунотерапии; по показаниям – хирургическое удаление источника инфекции.
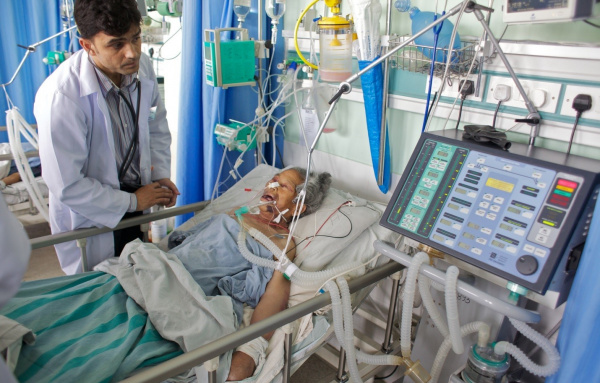
Сепсис (заражение крови) – вторичное инфекционное заболевание, вызванное попаданием патогенной флоры из первичного локального инфекционного очага в кровяное русло. Сегодня ежегодно в мире диагностируется от 750 до 1,5 млн. случаев сепсиса. По статистике, чаще всего сепсисом осложняются абдоминальные, легочные и урогенитальные инфекции, поэтому данная проблема наиболее актуальная для общей хирургии, пульмонологии, урологии, гинекологии. В рамках педиатрии изучаются проблемы, связанные с сепсисом новорожденных. Несмотря на использование современных антибактериальных и химиотерапевтических препаратов, летальность от сепсиса остается на стабильно высоком уровне – 30-50%.
Причины сепсиса
Важнейшими факторами, приводящими к срыву противоинфекционной резистентности и развитию сепсиса, выступают:
- со стороны макроорганизма - наличие септического очага, периодически или постоянно связанного с кровяным или лимфатическим руслом; нарушенная реактивность организма
- со стороны инфекционного возбудителя – качественные и количественные свойства (массивность, вирулентность, генерализация по крови или лимфе)
Ведущая этиологическая роль в развитии большинства случаев сепсиса принадлежит стафилококкам, стрептококкам, энтерококкам, менингококкам, грамотрицательной флоре (синегнойной палочке, кишечной палочке, протею, клебсиелле, энтеробактер), в меньшей степени - грибковым возбудителям (кандидам, аспергиллам, актиномицетам).
Выявление в крови полимикробных ассоциаций в 2,5 раза увеличивает уровень летальности больных сепсисом. Возбудители могут попадать в кровь из окружающей среды или заноситься из очагов первичной гнойной инфекции.
Велико значение внутрибольничной инфекции: ее росту способствует широкое применение инвазивных диагностических процедур, иммуносупрессивных лекарственных препаратов (глюкокортикоидов, цитостатиков). В условиях иммунодефицита, на фоне травмы, операционного стресса или острой кровопотери инфекция из хронических очагов беспрепятственно распространяется по организму, вызывая сепсис. Развитию сепсиса более подвержены недоношенные дети, больные, длительно находящиеся на ИВЛ, гемодиализе; онкологические, гематологические пациенты; больные сахарным диабетом, ВИЧ-инфекцией, первичными и вторичными иммунодефицитами.
Механизм развития сепсиса многоступенчатый и очень сложный. Из первичного инфекционного очага патогены и их токсины проникают в кровь или лимфу, обуславливая развитие бактериемии. Это вызывает активацию иммунной системы, которая реагирует выбросом эндогенных веществ (интерлейкинов, фактора некроза опухолей, простагландинов, фактора активации тромбоцитов, эндотелинов и др.), вызывающих повреждение эндотелия сосудистой стенки. В свою очередь, под воздействием медиаторов воспаления активизируется каскад коагуляции, что в конечном итоге приводит к возникновению ДВС-синдрома. Кроме этого, под влиянием высвобождающихся токсических кислородсодержащих продуктов (оксида азота, перекиси водорода, супероксидов) снижается перфузия, а также утилизация кислорода органами. Закономерным итогом при сепсисе является тканевая гипоксия и органная недостаточность.

Формы сепсиса классифицируются в зависимости от локализации первичного инфекционного очага. На основании этого признака различают первичный (криптогенный, эссенциальный, идиопатический) и вторичный сепсис. При первичном сепсисе входные ворота обнаружить не удается. Вторичный септический процесс подразделяется на:
- хирургический – развивается при заносе инфекции в кровь из послеоперационной раны
- акушерско-гинекологический – возникает после осложненных абортов и родов
- уросепсис – характеризуется наличием входных ворот в отделах мочеполового аппарата (пиелонефрит, цистит, простатит)
- кожный – источником инфекции служат гнойные заболевания кожи и поврежденные кожные покровы (фурункулы, абсцессы, ожоги, инфицированные раны и др.)
- перитонеальный (в т. ч. билиарный, кишечный) – с локализацией первичных очагов в брюшной полости
- плевро-легочный – развивается на фоне гнойных заболеваний легких (абсцедирующей пневмонии, эмпиемы плевры и др.)
- одонтогенный– обусловлен заболеваниями зубочелюстной системы (кариесом, корневыми гранулемами, апикальным периодонтитом, периоститом, околочелюстными флегмонами, остеомиелитом челюстей)
- тонзиллогенный – возникает на фоне тяжелых ангин, вызванных стрептококками или стафилококками
- риногенный – развивается вследствие распространения инфекции из полости носа и придаточных пазух, обычно при синуситах
- отогенный - связан с воспалительными заболеваниями уха, чаще гнойным средним отитом.
- пупочный– встречается при омфалите новорожденных
По времени возникновения сепсис подразделяется на ранний (возникает в течение 2-х недель с момента появления первичного септического очага) и поздний (возникает позднее двухнедельного срока). По темпам развития сепсис может быть молниеносным (с быстрым развитием септического шока и наступлением летального исхода в течение 1-2 суток), острым (длительностью 4 недели), подострым (3-4 месяца), рецидивирующим (продолжительностью до 6 месяцев с чередованием затуханий и обострений) и хроническим (продолжительностью более года).
Сепсис в своем развитии проходит три фазы: токсемии, септицемии и септикопиемии. Фаза токсемии характеризуется развитием системного воспалительного ответа вследствие начала распространения микробных экзотоксинов из первичного очага инфекции; в этой фазе бактериемия отсутствует. Септицемия знаменуется диссеминацией возбудителей, развитием множественных вторичных септических очагов в виде микротромбов в микроциркуляторном русле; наблюдается стойкая бактериемия. Для фазы септикопиемии характерно образование вторичных метастатических гнойных очагов в органах и костной системе.
Симптомы сепсиса
Симптоматика сепсиса крайне полиморфна, зависит от этиологической формы и течения заболевания. Основные проявления обусловлены общей интоксикацией, полиорганными нарушениями и локализацией метастазов.
Состояние больного сепсисом быстро утяжеляется. Кожные покровы приобретают бледновато-серый (иногда желтушный) цвет, черты лица заостряются. Могут возникать герпетические высыпания на губах, гнойнички или геморрагические высыпания на коже, кровоизлияния в конъюнктиву и слизистые оболочки. При остром течении сепсиса у больных быстро возникают пролежни, нарастает обезвоживание и истощение.
В условиях интоксикации и тканевой гипоксии при сепсисе развиваются полиорганные изменения различной степени тяжести. На фоне лихорадки отчетливо выражены признаки нарушения функций ЦНС, характеризующиеся заторможенностью или возбуждением, сонливостью или бессонницей, головными болями, инфекционными психозами и комой. Сердечно-сосудистые нарушения представлены артериальной гипотонией, ослаблением пульса, тахикардией, глухостью сердечных тонов. На этом этапе сепсис может осложниться токсическим миокардитом, кардиомиопатией, острой сердечно-сосудистой недостаточностью.
На происходящие в организме патологические процессы дыхательная система реагирует развитием тахипноэ, инфаркта легкого, респираторного дистресс-синдрома, дыхательной недостаточности. Со стороны органов ЖКТ отмечается анорексия, возникновение «септических поносов», чередующихся с запорами, гепатомегалии, токсического гепатита. Нарушение функции мочевыделительной системы при сепсисе выражается в развитии олигурии, азотемии, токсического нефрита, ОПН.
В первичном очаге инфекции при сепсисе также происходят характерные изменения. Заживление ран замедляется; грануляции становятся вялыми, бледными, кровоточащими. Дно раны покрывается грязно-сероватым налетом и участками некрозов. Отделяемое приобретает мутный цвет и зловонный запах.
Метастатические очаги при сепсисе могут выявляться в различных органах и тканях, что обусловливает наслоение дополнительной симптоматики, свойственной гнойно-септическому процессу данной локализации. Следствием заноса инфекции в легкие служит развитие пневмонии, гнойного плеврита, абсцессов и гангрены легкого. При метастазах в почки возникают пиелиты, паранефриты. Появление вторичных гнойных очагов в опорно-двигательной системе сопровождается явлениями остеомиелита и артрита. При поражении головного мозга отмечается возникновение церебральных абсцессов и гнойного менингита. Возможно наличие метастазов гнойной инфекции в сердце (перикардит, эндокардит), мышцах или подкожной жировой клетчатке (абсцессы мягких тканей), органах брюшной полости (абсцессы печени и др.).
Осложнения сепсиса
Основные осложнения сепсиса связаны с полиорганной недостаточностью (почечной, надпочечниковой, дыхательной, сердечно-сосудистой) и ДВС-синдромом (кровотечения, тромбоэмболии).
Тяжелейшей специфической формой сепсиса является септический (инфекционно-токсический, эндотоксический) шок. Он чаще развивается при сепсисе, вызванном стафилококком и грамотрицательной флорой. Предвестниками септического шока служат дезориентация больного, видимая одышка и нарушение сознания. Быстро нарастают расстройства кровообращения и тканевого обмена. Характерны акроцианоз на фоне бледных кожных покровов, тахипноэ, гипертермия, критическое падение АД, олигурия, учащение пульса до 120-160 уд. в минуту, аритмия. Летальность при развитии септического шока достигает 90%.

Диагностика сепсиса
Распознавание сепсиса основывается на клинических критериях (инфекционно-токсической симптоматике, наличии известного первичного очага и вторичных гнойных метастазов), а также лабораторных показателях (посев крови на стерильность).
Вместе с тем, следует учитывать, что кратковременная бактериемия возможна и при других инфекционных заболеваниях, а посевы крови при сепсисе (особенно на фоне проводимой антибиотикотерапии) в 20-30% случаев бывают отрицательными. Поэтому посев крови на аэробные и анаэробные бактерии необходимо проводить минимум трехкратно и желательно на высоте лихорадочного приступа. Также производится бакпосев содержимого гнойного очага. В качестве экспресс-метода выделения ДНК возбудителя сепсиса используется ПЦР. В периферической крови отмечается нарастание гипохромной анемии, ускорение СОЭ, лейкоцитоз со сдвигом влево.
Дифференцировать сепсис необходимо от лимфогранулематоза, лейкемии, брюшного тифа, паратифов А и В, бруцеллеза, туберкулеза, малярии и других заболеваний, сопровождающихся длительной лихорадкой.
Лечение сепсиса
Пациенты с сепсисом госпитализируются в отделение интенсивной терапии. Комплекс лечебных мероприятий включает в себя антибактериальную, дезинтоксикационную, симптоматическую терапию, иммунотерапию, устранение белковых и водно-электролитных нарушений, восстановление функций органов.
С целью устранения источника инфекции, поддерживающего течение сепсиса, проводится хирургическое лечение. Оно может заключаться во вскрытии и дренировании гнойного очага, выполнении некрэктомии, вскрытии гнойных карманов и внутрикостных гнойников, санации полостей (при абсцессе мягких тканей, флегмоне, остеомиелите, перитоните и др.). В некоторых случаях может потребоваться резекция или удаление органа вместе с гнойником (например, при абсцессе легкого или селезенки, карбункуле почки, пиосальпинксе, гнойном эндометрите и др.).
Борьба с микробной флорой предполагает назначение интенсивного курса антибиотикотерапии, проточное промывание дренажей, местное введение антисептиков и антибиотиков. До получения посева с антибиотикочувствительностью терапию начинают эмпирически; после верификации возбудителя при необходимости производится смена противомикробного препарата. При сепсисе для проведения эмпирической терапии обычно используются цефалоспорины, фторхинолоны, карбапенемы, различные комбинации препаратов. При кандидосепсисе этиотропное лечение проводится амфотерицином В, флуконазолом, каспофунгином. Антибиотикотерапия продолжается в течение 1-2 недель после нормализации температуры и двух отрицательных бакпосевов крови.
Дезинтоксикационная терапия при сепсисе проводится по общим принципам с использованием солевых и полиионных растворов, форсированного диуреза. С целью коррекции КОС используются электролитные инфузионные растворы; для восстановления белкового баланса вводятся аминокислотные смеси, альбумин, донорская плазма. Для борьбы с бактериемией при сепсисе широко используются процедуры экстракорпоральной детоксикации: плазмаферез, гемосорбция, гемофильтрация. При развитии почечной недостаточности применяется гемодиализ.
Иммунотерапия предполагает использование антистафилококковой плазмы и гамма-глобулина, переливание лейкоцитарной массы, назначение иммуностимуляторов. В качестве симптоматических средств используются сердечно-сосудистые препараты, анальгетики, антикоагулянты и др. Интенсивная медикаментозная терапия при сепсисе проводится до стойкого улучшения состояния больного и нормализации показателей гомеостаза.
Исход сепсиса определяется вирулентностью микрофлоры, общим состоянием организма, своевременностью и адекватностью проводимой терапии. К развитию осложнений и неблагоприятному прогнозу предрасположены больные пожилого возраста, с сопутствующими общими заболеваниями, иммунодефицитами. При различных видах сепсиса летальность составляет 15-50%. При развитии септического шока вероятность летального исхода крайне высока.
Профилактические меры в отношении сепсиса состоят в устранении очагов гнойной инфекции; правильном ведении ожогов, ран, локальных инфекционно-воспалительных процессов; соблюдении асептики и антисептики при выполнении лечебно-диагностических манипуляций и операций; предупреждении госпитальной инфекции; проведении вакцинации (против пневмококковой, менингококковой инфекции и др.).
Читайте также:
- Показания для артроскопического шва при массивных разрывах ротаторной манжеты плеча
- Ключично-черепной дизостоз (КЧД): атлас фотографий
- Вакцина против вируса Herpes Zoster
- Лучевая болезнь америция. Накопление и вывод из организма америция
- Последовательность миелинизации. Дифференциация головного мозга эмбриона
