Легионеллезная пневмония. Пневмония при туляремии и бруцеллезе
Добавил пользователь Morpheus Обновлено: 27.01.2026
3163. Возбудители легионеллеза представляют самостоятельный род и семейство микроорганизмов. Род Legionella образует генетически родственную таксономическую структуру, а семейство Legionellaceae состоит только из одного рода и принадлежит к g-подтипу протеобактерий.
3164. Известны более 50 видов легионелл, для 22 из которых доказана роль в инфекционной патологии человека. Более 90% случаев болезни ассоциированы с видом L. pneumophila. Среди других видов легионелл преимущественно заболевание вызывают при нарушениях клеточного иммунитета и (или) на коморбидном фоне виды L.micdadei, L.longbeuchae, L.dumoffii и L.bozemanii.
3165. Легионеллы представляют собой грамотрицательные палочки диаметром 0,5 - 0,7 мкм и длиной 2 - 5 мкм. В ряде случаев встречаются нитевидные формы длиной до 20 - 25 мкм. Не образуют эндоспор, микроцист и капсул, растут в аэробных условиях, подвижны за счет одного, двух или большего числа жгутиков. Микроорганизмы не ферментируют углеводы, разжижают желатин, не образуют уреазу, не восстанавливают нитраты, не растут на обычных питательных средах, что связано с потребностью возбудителя в L-цистеине и в растворимом пирофосфате железа (Fe++).
3166. Легионеллы устойчивы во внешней среде: в жидких средах при температуре 25 °C может сохраняться 112 календарных дней, при температуре 4 °C - 150 календарных дней. Легионеллы могут выживать в водопроводной воде до года, в дистиллированной - 2 - 4 месяца. Микроорганизмы быстро, за 1 мин., погибают под воздействием 70% спирта, 1% раствора формалина, 0,002% раствора фенола, в течение 10 мин. - в 3% растворе хлорамина.
3167. Кроме того, возбудители легионеллеза чувствительны к другим дезинфицирующим хлорактивным средствам, а также кислородсодержащим и средствам на основе катионных поверхностно-активных веществ, в частности четвертичным аммониевым соединениям, третичному алкиламину, полигуанидинам и глутаровому альдегиду.
3168. Легионеллы являются сапрофитами и широко распространены в природе. Обитают в пресноводных водоемах, где они паразитируют в водных амебах и других простейших. Размножение легионелл активно идет в теплой воде в диапазоне температур 20 - 45 °C, хотя их выделяют и из холодной воды. Условия для выживания легионелл в искусственных сооружениях более благоприятны, чем в естественных, что приводит к накоплению в них возбудителя в высоких концентрациях. Легионеллы активно колонизуют синтетические и резиновые поверхности водопроводного, промышленного, медицинского оборудования с образованием так называемых биопленок, в которых легионеллы значительно более устойчивы к действию дезинфицирующих веществ по сравнению с планктонными формами. При колонизации легионеллами искусственных водных систем, в том числе системы горячего и холодного водоснабжения, централизованные системы кондиционирования воздуха с водным охлаждением, градирни, вихревые бассейны и джакузи массового пользования в аквапарках и спортивно-восстановительных центрах, увлажнители воздуха, фонтаны, концентрация легионелл значительно возрастает, что представляет эпидемическую опасность.
3169. Легионеллы являются факультативными внутриклеточными паразитами. В организме человека они размножаются преимущественно в альвеолярных макрофагах, полиморфно-ядерных нейтрофилах и моноцитах крови.
3170. Легионеллез является сапронозной инфекцией, протекающей с поражением органов дыхания, часто в форме тяжелых пневмоний. Источниками при этом служат естественные и искусственные водоемы, различные системы водопользования, технические устройства с использованием воды, а также почва.
3171. Механизм передачи легионеллеза - аэрозольный, путь - воздушно-капельный. Факторами передачи инфекции являются мелкодисперсионный водный аэрозоль и вода, контаминированные легионеллами.
3172. Практически все крупные эпидемические вспышки и многие спорадические случаи легионеллеза связаны с распространением мелкодисперсного аэрозоля, содержащего легионеллы и генерируемого бытовыми, медицинскими или промышленными водными системами. Аспирация контаминированной водопроводной воды без образования аэрозоля считается альтернативным путем передачи инфекции. В последнее время он приобретает все большую актуальность. В тех случаях, когда температура воды в системах горячего водоснабжения не превышает 50 °C, создаются благоприятные условия для активного размножения возбудителя. В процессе водопользования, при наличии восприимчивых к легионеллезу лиц, происходит формирование эпидемических очагов с единичными или множественными случаями заболеваний.
3173. Проявлениями эпидемического процесса легионеллеза являются манифестные формы инфекции. Болезнь легионеров (легионеллезная пневмония) развивается у 5 - 10% лиц, подвергшихся действию факторов передачи инфекции, лихорадка Понтиак (острое респираторное заболевание) поражает 80 - 100% таких лиц.
3174. Инкубационный период зависит от клинической формы инфекции. Для клинического варианта легионеллеза, протекающего с преимущественным поражением легких, характерен инкубационный период 2 - 10 календарных дней. При форме в виде острой респираторной инфекции (лихорадка Понтиак) инкубационный период составляет от 5 часов до 3 календарных дней, при острой лихорадочной форме с экзантемой (лихорадка форта Брагг) - от нескольких часов до 10 календарных дней.
3175. Легионеллез выявляют преимущественно у людей среднего и пожилого возраста на фоне действия таких факторов риска, как курение, злоупотребление алкоголем, сопутствующие заболевания, в первую очередь, диабет и сердечно-сосудистые заболевания; иммуносупрессивная терапия, первичные и вторичные иммунодефициты. В то же время легионеллезная инфекция, включая тяжелые формы заболевания, может возникать и у ранее совершенно здоровых людей. У детей легионеллез выявляют редко, обычно на фоне сопутствующих заболеваний. Болезнь легионеров чаще поражает мужчин, чем женщин (соотношение заболевших составляет 2 - 3:1). Случаи легионеллеза выявляют круглогодично, но пик заболеваемости приходится на летние месяцы.
3176. Особенностью эпидемиологии легионеллезной инфекции является выделение трех основных групп заболеваний по характеру приобретения инфекции: внебольничный легионеллез (эпидемические вспышки и спорадические случаи), нозокомиальный легионеллез (инфекции, связанные с оказанием медицинской помощи) и легионеллез, связанный с поездками, путешествиями.). Носительство и персистенция легионелл не установлены.
Легионеллезная пневмония. Пневмония при туляремии и бруцеллезе
Легионеллезная пневмония. Пневмония при туляремии и бруцеллезе
Легионеллезная пневмония начинается остро с резкого озноба, высокой температуры - до 40°С и выше, выраженной интоксикацией, прострацией, слабости, атаксии. Симптомы поражения легких проявляются в период с 4-го по 7-й день болезни. Появляются одышка, кашель, вначале он непродуктивный, затем становится сильным, со слизистой мокротой, часто с кровью. Выслушиваются влажные хрипы и шум трения плевры (В.Е. Ноников). На рентгенограммах легких отмечаются инфильтраты, часто двусторонние. У некоторых пневмония носит мигрирующий характер. Инфильтраты могут быть интерстициальными, лобарными или пятнистыми. Иногда образуются полости и абсцессы, возможны пневмонит и альвеолит.
При вдыхании пыли, зараженной экскрементами и тушками павших грызунов, возможно развитие легочной формы туляремии. Продолжительность инкубационного периода от 3 до 7 дней. Заболевание начинается остро с озноба, повышения температуры, интоксикации, протекает в двух вариантах: с поражением верхних дыхательных путей по гриппоподобному или бронхитическому типу и с поражением легких в виде пневмонии - очаговой, диссеминированной, долевой. Для этого типа туляремии характерно увеличение лимфоузлов в корнях легких и поражение плевры. Течение заболевания изнуряющее: высокая лихорадка, сильный кашель, частая боль в грудной клетке (плевральная боль). Кровохарканье в отличие от чумы и сибирской язвы большая редкость. Выслушиваются влажные хрипы - крепитирующие и мелкопузырчатые.
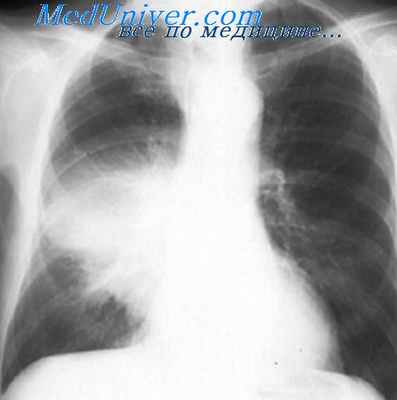
Решающее диагностическое значение имеют положительная внутрикожная аллергическая проба с тулярином (с 1-го дня болезни) и серологические сдвиги с конца 1-й недели болезни. В случаях ингаляции пыли и воздуха, содержащих споры сибиреязвенных бацилл, возможно развитие тяжелой геморрагической пневмонии, плеврита, медиастинита, менингита (сибиреязвенного сепсиса) с быстрым летальным исходом («болезнь тряпичников» старых авторов). Инкубационный период от нескольких часов до 8 дней. При экспериментальном аэрогенном заражении сибирской язвой в легких не наблюдается первичных специфических патологических изменений.
Изменения в их паренхиме развиваются на фоне последующего сепсиса, как и при кожной форме сибирской язвы у людей (П.Н Бургасов). Отличительной особенностью сибиреязвенной аэрогенной инфекции является развитие внутригрудного комплекса, включающего отек легких и средостения, геморрагическое воспаление в лимфоузлах (трахеобронхиальных, гилюсных, медиастинальных) и геморрагический плеврит. Г.П Руднев в качестве важного дифференциально-диагностического признака поражения легких при сибирской язве у людей отмечал быстрое свертывание крови в мокроте, тогда как по его же наблюдениям кровь в мокроте больного легочной чумой не свертывается. При аэрозольном заражении ботулиническим токсином в экспериментальных условиях развиваются геморрагические пневмонии.
При бруцеллезе в случаях пылевого пути заражения развивается специфическое поражение бронхов и легких. Отмечают высокую частоту бронхитов, плевритов (сухих и экссудативных), бронхоаденитов. Клиническое течение напоминает туберкулез, что является причиной частого нераспознавания легочных форм висцерального бруцеллеза, поэтому поражения легких при бруцеллезе в прошлом нередко фигурировали под названием псевдотуберкулезных форм (Г.П. Руднев). Диагностика бруцеллезных поражений легких затруднена тем, что при пылевом пути заражения они служат единственным клиническим проявлением болезни. Обычно у таких больных отсутствуют часто встречающиеся при бруцеллезе поражения локомоторного аппарата и гепатолиенальный синдром. В гемограмме возможен моноцитоз.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Туляремия
Существует 7 клинических синдромов, связанных с туляремией (см. таблицу Виды туляремии Виды туляремии ); клинические проявления могут варьировать в зависимости от типа экспозиции микроорганизма.
Возбудитель, F. tularensis, является маленькой, плеоморфной неподвижной неспорообразующей аэробной грамотрицательной бациллой, которая проникает в живой организм следующим образом:
Прием в пищу зараженной еды или воды
Укус зараженного членистоногого (клеща, мухи оленя, блохи)
Прямой контакт с зараженными тканями или материалом
Туляремия не передается от человека к человеку.
Микроорганизм может проникнуть через вроде бы цельный кожный покров, но может фактически попасть и через микротрещины.
Большинство случаев заболевания туляремией вызывают два типа F. tularensis:
Тип A: это более вирулентный серотип для людей, обычно встречается у кроликов, зайцев и грызунов в США и Канаде.
Тип В: обычно вызывает язвенно-железистую инфекцию в легкой форме и встречается у грызунов и в акваториях всего северного полушария, включая Северную Америку, Европу и Азию.
Обычно заражаются охотники, мясники, фермеры и обработчики меха. В зимние месяцы большинство случаев являются результатом контакта (особенно во время сдирания кожи) с зараженными дикими кроликами и зайцами. В летние месяцы инфекция обычно является следствием обработки шкур зараженных животных, или птиц, или укусов зараженных клещей, или других членистоногих. Изредка случаи являются результатом употребления термически необработанного мяса, зараженной воды или косьбы в эндемичных областях. На Западе США клещи, мухи оленя, мухи лошади и прямой контакт с зараженными животными также представляют собой источники инфекции. О случаях трансмиссии от человека к человеку не сообщалось. Лабораторные работники подвергаются особенно высокому риску, поскольку могут легко инфицироваться во время рутинной работы с зараженными образцами.
При диссеминированных случаях характерные очаговые некротические поражения на различных стадиях развития рассеяны по всему организму. Размером от 1 мм до 8 см в диаметре, имеют беловато-желтый цвет; внешне проявляются как первичные поражения на пальцах, глазах или в полоси рта и обычно появляются на лимфоузлах, селезенке, печени, почках и легких. При пневмонии некротические очаги появляются в легких. Хотя может быть и тяжелая системная интоксикация, никакие специфические токсины не обнаруживаются.
Симптомы и признаки туляремии
Начало туляремии внезапное, через 1–10 (обычно 2–4) дней после заражения, с головной болью, ознобом, тошнотой, рвотой, лихорадкой от 39,5 ° до 40° C и выраженной общей слабостью. Развиваются выраженная слабость, рецидивирующий озноб и проливные поты. Клинические проявления зависят в некоторой степени от типа заражения (см. таблицу Виды туляремии Виды туляремии ).
В пределах 24–48 часов на месте поражения (палец, рука, глаз, небо) появляется воспаленная папула, за исключением железистой или тифоидной туляремии. Папула быстро переходит в пустулу и превращается в язву с образованием чистого кратера язвы со скудным, тонким, бесцветным эксудатом. Язвы обычно одиночные на конечностях, но множественные во рту или глазах. Обычно поражен только один глаз. Региональные лимфоузлы увеличены, могут нагнаиваться и затем дренироваться. К 5-му дню часто развивается похожее на тиф состояние, у пациента может начаться нетипичная пневмония, иногда сопровождаемая делирием.
Пневмоническая туляремия может начаться после воздушно-капельного или гематогенного заражения другим типом туляремии; это развивается в 10–15% случаев язвенно-железистой туляремии и приблизительно в 50% случаев тифоидной туляремии. Хотя часто присутствуют признаки инфильтрации легочной ткани, ослабленное дыхание и непостоянные хрипы могут быть единственными физикальными проявлениями пневмонии при туляремии. Сухой, непродуктивный кашель связан с чувством жжения в ретростернальной области. Неспецифичная сыпь, похожая на розеолезную, может появиться на любой стадии болезни. Спленомегалия и периспленит также могут выявляться. При отсутствии лечения температура тела остается повышенной в течение 3–4 недель и постепенно снижается. Медиастинит, абсцесс легкого и менингит – редкие осложнения.
Диагностика туляремии
Серологическое исследование (в острой фазе и в период выздоровления) и полимеразная цепная реакция (ПЦР)
Диагноз устанавливается на основании данных о контактах с кроликами, зайцами или грызунами, или заражения от членистоногого переносчика, внезапном появлении симптомов, при наличии характерного первичного следа от укуса и регионарной лимфаденопатии.
У пациентов необходимо производить забор крови и образцов соответствующего клинического материала (например, из очагов поражений или мокроты) для последующего культивирования. Оно может давать отрицательные результаты, поэтому лаборатория должна быть уведомлена о подозрении на диагноз туляремии, для того чтобы можно было подобрать соответствующие селективные среды (и обеспечить необходимые меры безопасности при работе с этим возбудителем).
Титры антител в острой стадии и в период выздоровления должны быть исследованы с интервалом в 2 недели. Диагностическими являются 4-х кратное повышение титров или если один титр > 1:128. Сыворотка пациентов с бруцеллезом Бруцеллез Бруцеллез вызывается виды Brucella, грамотрицательной бактерией. Симптомы начинаются с острого фебрильного заболевания с несколькими локальными признаками или без них и могут прогрессировать. Прочитайте дополнительные сведения может перекрестно реагировать с антигенами F. tularensis, но обычно титры значительно ниже. Некоторые лаборатории используют флуоресцентный анализ антител или иммуногистохимическое окрашивание. ПЦР-тестирование может обеспечить быструю диагностику.
Часто имеется лейкоцитоз, но количество лейкоцитов крови может быть нормальным с увеличением только пропорции полиморфноядерных клеток.
Поскольку этот микроорганизм является высоко контагиозным, образцы и среды от пациентов с подозрением на наличие туляремии должны быть обработаны с чрезвычайной осторожностью и, если возможно, в лаборатории с оборудованием высокого уровня (уровень 3) биологической безопасности.
Прогноз при туляремии
Смертность приближается к нулю при лечении и составляет приблизительно 6% при отсутствии лечения случаев язвенно-железистой туляремии. Смертность выше при инфекции типа А и при тифоидной, септицемической и пневмонической туляремии; она достигает 33% при отсутствии лечения. Смерть обычно наступает при генерализованной инфекции, пневмонии, менингите или перитоните. Рецидивы могут произойти в случае неправильного лечения. У переболевших даже один раз приобретается иммунитет.
Лечение туляремии
Стрептомицин (плюс хлорамфеникол при менингите)
Предпочтительным препаратом является
Стрептомицин в дозе 1 г внутримышечно каждые 12 часов для взрослых и 15 мг/кг внутримышечно каждые 12 часов для детей в течение 7 - 10 дней при течении болезни от умеренной до тяжелой степени
Если есть доказательства менингита, добавляют хлорамфеникол по 12,5–25 мг/кг внутривенно каждые 6 часов или доксициклин 100 мг перорально 2 раза в день в течение 14–21 дня.
Альтернативы стрептомицину включают в себя следующее:
Гентамицин 1-2 мг/кг внутримышечно или внутривенно каждые 8 часов (при течении болезни от умеренной до тяжелой степени)
Доксициклин 100 мг перорально каждые 12 часов (при легком течении болезни)
Хлорамфеникол 12,5-25 мг/кг внутривенно каждые 6 часов (следует применять только для лечения менингита, так как в остальных случаях есть более эффективные и безопасные альтернативы)
Ципрофлоксацин 500 мг перорально каждые 12 часов (при легком течении болезни)
При массовом поражении, если парентеральное лечение невозможно, можно применять оральный доксициклин или ципрофлоксацин для взрослых и детей. Однако иногда при назначении всех этих лекарств наблюдаются рецидивы, и они не всегда предотвращают нагноение узла.
Постоянные влажные гипертонические повязки полезны при первичных поражениях кожи и могут уменьшить тяжесть воспаления лимфатических узлов и лимфаденита. Хирургический дренаж крупных абсцессов редко необходим, если терапия не отсрочена.
При глазной туляремии применение теплых солевых компрессов и использование темных очков дают некоторое облегчение. В тяжелых случаях 2% гоматоприм по 1–2 капли каждые 4 часа может облегчить симптоматику.
Интенсивная головная боль обычно снижается пероральными анальгетиками.
Профилактика туляремии
Попадая в эндемичные области, люди должны использовать защитную одежду от клещей и репелленты. Осмотр в поисках клещей должен проводиться после выхода из инфицированных клещами областей. Клещей следует удалять сразу же (см. боковую колонку ).
Контактируя с кроликами, зайцами и грызунами, особенно в эндемичных областях, люди должны носить защитную одежду, включая резиновые перчатки и маски, потому что возбудители могут быть у животного и в экскрементах насекомых, и на меху животного. Дикие птицы и дичь должны быть тщательно приготовлены перед употреблением в пищу.
Вода, которая может быть заражена, должна быть продезинфицирована перед использованием.
В настоящее время вакцины отсутствуют, хотя одна вакцина в данный момент находится на рассмотрении в Управлении по контролю за пищевыми продуктами и лекарственными средствами (FDA). После воздействия высокого риска (например, авария в лаборатории) рекомендуется антибиотикопрофилактика в течение 14 дней доксициклином или ципрофлоксацином.
Основные положения
F. tularensis является высококонтагиозным микроорганизмом; в США и Канаде главным резервуаром являются дикие кролики, заяйцы и грызуны.
Туляремией можно заразиться разными путями, в том числе через прямой контакт с инфицированными животными (особенно кроликами и зайцами) или птицами, через укусы инфицированных членистоногих, через случайный контакт с лабораторными образцами, или, реже, путем вдыхания инфекционного аэрозоля или приема в пищу зараженного мяса или воды.
У пациентов развивается лихорадка 39,5-40 ° С и другие системные симптомы (например, головная боль, озноб, тошнота, рвота, выраженная общая слабость) вместе со специфическими проявлениями, связанными с пораженным органом; кожные поражения и/или лимфаденит являются наиболее распространенными, также могут возникать пневмонии.
Диагноз устанавливают с помощью посевов крови и соответствующего клинического материала; также информативными могут быть определение антител в острый период и период выздоровления, полимеразная цепная реакция (ПЦР) и некоторые методы окрашивания.
Лечат стрептомицином (в комбинации с хлорамфениколом при менингите).
В эндемических районах следует принимать соответствующие меры предосторожности, в том числе стратегии защиты от клещей, использование защитной одежды при работе с кроликами, зайцами и грызунами, тщательное приготовление блюд из диких птиц и диких животных.
Авторское право © 2022 Merck & Co., Inc., Rahway, NJ, США и ее аффилированные лица. Все права сохранены.
Внебольничная пневмония, вызванная Legionella pneumophila («болезнь легионеров»): краткий обзор и клинические наблюдения
Ключевые слова
Об авторах
Федеральное государственное бюджетное учреждение Национальный исследовательский центр эпидемиологии и микробиологии имени почетного академика Н.Ф.Гамалеи
Россия
Конфликт интересов: not
Федеральное государственное бюджетное образовательное учреждение высшего образования «Первый Санкт-Петербургский государственный медицинский университет имени академика И.П. Павлова» Министерства здравоохранения Российской Федерации
Россия
Конфликт интересов: not
Федеральное государственное бюджетное образовательное учреждение дополнительного профессионального образования «Российская медицинская академия непрерывного профессионального образования» Министерства здравоохранения Российской Федерации
Россия
Тартаковский Игорь Семенович – доктор биологических наук, профессор, руководитель центра по легионеллезу.
123098 Москва ул. Гамалеи, 18; тел.: (499) 193-30-01
Конфликт интересов: нет
Федеральное государственное автономное образовательное учреждение высшего образования «Российский университет дружбы народов» (Медицинский институт)
Россия
Рачин Сергей Андреевич – студент VIкурса лечебного факультета.
Конфликт интересов: нет
Федеральное государственное автономное образовательное учреждение высшего образования «Российский университет дружбы народов» (Медицинский институт)
Россия
Конфликт интересов: not
Федеральное государственное автономное образовательное учреждение высшего образования «Российский университет дружбы народов» (Медицинский институт)
Россия
Хрулева Юлия Викторовна – ординатор кафедры внутренних болезней с курсом кардиологии и функциональной диагностики имени академика В.С.Моисеева.
117198, Москва, ул. Миклухо-Маклая, 6; тел.: (495) 434-53-00
Конфликт интересов: нет
Федеральное государственное автономное образовательное учреждение высшего образования «Российский университет дружбы народов» (Медицинский институт)
Россия
Бондарь Светлана Александровна – ординатор кафедры внутренних болезней с курсом кардиологии и функциональной диагностики имени академика В.С.Моисеева.
117198, Москва, ул. Миклухо-Маклая, 6; тел.: (495) 434-53-00
Конфликт интересов: нет
Список литературы
1. Diederen B.M.W. Legionella spp. and Legionnaires’ disease. J. Infect. 2008; 56 (1): 1–12. DOI: 10.1016/j.jinf.2007.09.010.
2. Тартаковский И.С., Синопальников А.И. Легионеллез: роль в инфекционной патологии человека. Клиническая микробиология и антимикробная химиотерапия. 2007; 3 (9): 219–233.
3. Тартаковский И.С., Груздева О.А. Легионеллез (болезнь легионеров, лихорадка Понтиак). В кн.: Брико Н.И., Онищенко Г.Г., Покровский В.И., ред. Руководство по эпидемиологии инфекционных болезней. М.: МИА; 2019. Т. 2: 477–495.
4. Тартаковский И.С., Груздева О.А., Галстян Г.М., Карпова Т.И. Профилактика, диагностика и лечение легионеллеза. М.: МДВ; 2013.
5. Joseph C., Ricketts C. The epidemiology of Legionnaires disease. In: Heuner K., Swanson M., eds. Legionella: Molecular Biology. Norfolk: Caster Akademic Press; 2008: 35–52.
7. Vergis E.N., Akbas E., Yu V.L. Legionella as a cause of severe pneumonia. Semin. Respir. Crit. Care Med. 2000; 21 (4): 295–304. DOI: 10.1055/s-2000-9862.
8. Zakharenkov I., Rachina S., Kozlov R. et al. Etiology and antibiotic resistance patterns in adults with severe community-acquired pneumonia in Russia. Eur. Respir. J. 2019; 54 (Suppl. 63): PA290.
9. Рачина С.А., Бобылев А.А. Атипичные возбудители внебольничной пневмонии: от эпидемиологии к особенностям диагностики и лечения. Практическая пульмонология. 2016; (2): 20–28.
10. Чучалин А.Г., Синопальников А.И., Козлов Р.С. и др. Российское респираторное общество (РРО), Межрегиональная ассоциация по клинической микробиологии и антимикробной химиотерапии (МАКМАХ). Клинические рекомендации по диагностике, лечению и профилактике тяжелой внебольничной пневмонии у взрослых. Пульмонология. 2014; (4): 13–48. DOI: 10.18093/0869-0189-2014-0-4-13-48.
12. Stout J.E., Yu V.L. Hospital-acquired Legionnairesʹ disease: new developments. Curr. Opin. Infect. Dis. 2003; 16 (4): 337–341. DOI: 10.1097/00001432-200308000-00005.
13. Тартаковский И.С., Груздева О.А., Габриэлян Н.И. Современное состояние проблемы нозокомиального легионеллеза. Вестник трансплантологии и искусственных органов 2010; 12 (4): 61–71.
14. Чучалин А.Г., Синопальников А.И., Тартаковский И.С. и др. Практические рекомендации по диагностике и лечению легионеллезной инфекции, вызываемой Legionella pneumophila серогруппы 1. Клиническая микробиология и антимикробная химиотерапия. 2009; 11 (1): 4–13.
15. Тартаковский И.С., Новокшонова И.В., Мариненко О.В. и др. Частота и уровень контаминации Legionella pneumophila потенциально опасных водных объектов в Московском регионе. Журнал микробиологии, эпидемиологии и иммунобиологии. 2010; (6): 21–26.
16. Груздева О.А., Тартаковский И.С. Организация профилактики легионеллеза. Здравоохранение Российской Федерации. 2011; (1): 26–28.
17. Груздева О.А., Тартаковский И.С., Карпова Т.И., Мариненко О.В. Особенности эпидемиологии и методы профилактики нозокомиального легионеллеза. Эпидемиология и вакцинопрофилактика. 2014; 1 (74): 19–23.
18. Mercante J.W., Winchell J.M. Current and emerging legionella diagnostic for laboratory and outbreak investigations. Clin. Microbiol. Rev. 2015; 28 (1): 95–133. DOI: 10.1128/CMR.00029-14.
19. Legionellosis – United States, 2000–2009. Am. J. Transplant. 2012; 12 (1): 250–253. DOI: 10.1111/j.1600-6143.2011.03938.x.
20. Рачина С.А., Козлов Р.С., Дехнич Н.Н. и др. Антибактериальная терапия тяжелой внебольничной пневмонии у взрослых: обзор рекомендаций и клинические примеры. Архив внутренней медицины. 2015; 3 (23): 63–74.
Азитромицин при лечении инфекций нижних отделов дыхательных путей
Для цитирования: Ноников В.Е., Константинова Т.Д., Макарова О.В., Евдокимова С.А. Азитромицин при лечении инфекций нижних отделов дыхательных путей. РМЖ. 2008;22:1482.
Эпидемиологическая ситуация в последние годы характеризуется возросшей этиологической значимостью таких возбудителей, как микоплазма и хламидии, распространенной сенсибилизацией населения к производным пенициллина и сульфаниламидам, значительным ростом резистентности многих микроорганизмов к наиболее часто применяющимся антибиотикам [1,2,5,6]. В немалой степени возрастание резистентности явилось следствием многолетнего шаблонного применения в амбулаторной практике ко–тримоксазола и полусинтетических тетрациклинов. В последние годы в поликлиниках шире стали применяться фторхинолоны – результатом стало формирование штаммов, устойчивых к этим препаратам.
Первый из макролидов – эритромицин был создан в 1952 г., но препараты этого ряда применялись редко до драматической вспышки легионеллезных пневмоний (80–е годы ХХ века), сопровождающейся 30% летальностью. Довольно быстро было установлено, что макролиды являются оптимальными препаратами для лечения инфекций, вызываемых внутриклеточными инфекционными агентами (легионеллой, микоплазмой, хламидиями), и это привело к широкому применению этой группы антибиотиков. Был создан ряд новых препаратов для перорального и парентерального применения, различающихся по показателям фармакокинетики и фармакодинамики.
Основу химической структуры макролидов [1,5] составляет макроциклическое лактонное кольцо. В зависимости от числа атомов углерода в лактонном кольце выделяют 14–членные (эритромицин, кларитромицин, рокситромицин), 15–членные (азитромицин) и 16–членные (джозамицин, мидекамицин, спирамицин) макролиды.
Азитромицин относится к подклассу азалидов, потому что один атом углерода в его кольце заменен атомом азота. Структурные особенности отдельных препаратов определяют различия в фармакокинетических характеристиках, переносимости, возможности лекарственных взаимодействий, а также некоторые особенности антимикробной активности. Азитромицин характеризуется уникальной клеточной кинетикой, быстрым и интенсивным проникновением в клетки и интерстициальные ткани, высокими уровнями распределения антибиотика в тканях и относительно низкими в крови.
Азитромицин хорошо подавляет (табл. 1) грамположительные (пневмококки, стрептококки, стафилококки) и грамотрицательные (моракселла, гемофильные палочки) микроорганизмы и внутриклеточные агенты (хламидии, микоплазму, легионеллу, уреаплазму). Другие макролиды (кроме кларитромицина), менее активны в отношении гемофильных палочек [5,6]. Если учесть, что в этиологической структуре внебольничных пневмоний лидирующие позиции занимают пневмококки, гемофильные палочки, микоплазма, хламидии, а обострения хронического бронхита (хронической обструктивной болезни легких), как правило, вызваны пневмококками, гемофильными палочками, моракселлой (реже – микоплазмой и хламидиями), становится ясно, что азитромицин нередко является предпочтительным антибиотиком для лечения пульмонологических больных.
В странах Западной и Южной Европы широкое применение макролидов привело к росту (до 30%) резистентности к ним пневмококков. Соответствующие показатели резистентности в нашей стране [1] по различным оценкам не превышают 4–8%. Особенности азитромицина определяются не только спектром действия, но и созданием высоких концентраций в легочной паренхиме и альвеолярных макрофагах. Сравнение концентраций, создаваемых в различных биосредах, показывает, что концентрации азитромицина в легочной паренхиме в 8–10 раз, а в альвеолярных макрофагах в 800 раз выше, чем в сыворотке крови. Таким образом, этот препарат должен быть высокоэффективен именно при лечении легочной патологии.
Азитромицин сохраняется в очаге инфекции в течение 4–5 и более дней в зависимости от дозы и тканевой структуры. Благодаря освобождению антибиотика из фагоцитов при их деструкции концентрация в очаге инфекции быстро возрастает [1,5]. Высокое внутриклеточное проникновение и накопление в клетках и инфицированных тканях обусловливает эффективность азитромицина, превышающую действие других антибиотиков, при инфекциях, вызываемых внутриклеточными патогенами, в том числе возбудителями опасных инфекционных заболеваний (бруцеллез, туляремия и др.).
Особенностью фармакодинамики макролидов является длительный постантибиотический эффект, вследствие которого при использовании антибиотика в минимальных ингибирующих концентрациях после его отмены действие антибиотика продолжается. В отношении азитромицина считается доказанным постантибиотический эффект продолжительностью до 90 часов, и это позволяет сократить продолжительность антибактериального лечения.
Аллергическая сенсибилизация к макролидам сравнительно редка. Среди побочных эффектов преобладают желудочно–кишечные проявления и, возможно, часть из них обусловлена способностью макролидов усиливать моторику кишечника. Побочные эффекты более часты при использовании эритромицина. Токсические и аллергические побочные эффекты при использовании азитромицина редки [1,4,5].
Азитромицин разрешен к медицинскому применению в нашей стране в нескольких лекарственных формах: капсулы по 0,25 г, таблетки по 0,5 г, порошок для суспензии 2,0 г, порошок для иньекций по 0,5 г. Таким образом, антибиотик может применяться перорально, внутривенно и в режиме ступенчатой терапии. Препарат удобен по режиму дозирования (вводится один раз в сутки). С учетом длительного постантибиотического эффекта азитромицина этот антибиотик часто применялся (и применяется) короткими 3–5 дневными курсами. Лекарственная форма – порошок для приготовления суспензии (2,0 г азитромицина) подразумевает лечение однократным приемом антибиотика.
Особенности фармакокинетики позволяют применять азитромицин один раз в сутки. Естественно, что препараты, применяемые один–два раза в сутки обладают большей комплаентностью и охотно используются больными. Существуют различные схемы перорального применения азитромицина. Наиболее распространенной при лечении легочных заболеваний является дозировка 500 мг в первые сутки лечения и 250 мг каждые 24 часа в последующие 4 дня. При такой схеме длительность лечения пневмонии 5 дней. Сроки лечения пневмоний, вызванных обычными бактериальными агентами (пневмококки, стрептококки, гемофильные палочки и др.), могут быть сокращены до трех дней, если ежесуточная доза составляет 500 мг. Продолжительность лечения пневмоний, вызванных микоплазмой и хламидиями – 14 дней, а легионеллезных пневмоний – 21 день.
Собственный опыт применения азитромицина на протяжении 15 лет основан на лечении этим антибиотиком более 1500 больных пневмониями, причем с высокой эффективностью применялись все описанные схемы пероральной терапии, ступенчатая терапия, лечение азитромицином в сочетании с b–лактамными антибиотиками.
По данным отделения пульмонологии Центральной клинической больницы в 1984 г. макролиды (применялся только эритромицин) составляли лишь 9% в структуре применявшихся антибиотиков. В 2004 г. частота их применения утроилась (27,3%), уступая только b–лактамным антибиотикам. Использовались 5 пероральных препаратов, из которых чаще всего (80%) применялся азитромицин. Значительная частота назначения макролидов объясняется подъемом заболеваемости хламидийной и микоплазменной инфекциями, а также широким использованием сочетаний макролидов с b–лактамными антибиотиками при невозможности этиологической расшифровки.
По данным микробиологических исследований мокроты в качестве ведущего этиологического агента инфекций органов дыхания по–прежнему доминирует (52,1%) пневмококк. Кроме пневмококка, из мокроты выделялись культуры зеленящего стрептококка, гемофильных палочек. Редко выявлялись грамотрицательные микроорганизмы и стафилококки. В последние годы значительно возросла частота микоплазменных и хламидийных инфекций, причем внутриклеточные агенты нередко являются причиной эпидемических очагов в семьях и коллективах.
Показаниями для назначения азитромицина являются [1,5] инфекции верхних дыхательных путей (тонзиллофарингит, острый средний отит, синусит), а также бронхиты и внебольничные пневмонии. Так называемые атипичные пневмонии [2–5] вызываются внутриклеточными агентами–вирусами, микоплазмой (50% всех случаев), хламидиями, легионеллой. Азитромицин является наилучшим антибиотиком для лечения большинства из них. Краткие отличия атипичных пневмоний [6] приведены в таблице 2. Инфекция часто передается от человека к человеку (в последние годы пришлось наблюдать несколько семейных и служебных вспышек микоплазменных и хламидийных пневмоний). Этиологический диагноз возможен путем выявления специфических антител класса IgM в сыворотке крови или сероконверсии (при исследовании парных сывороток).
Изучение клинических проявлений микоплазменных пневмоний показало, что характерен продромальный период в виде недомогания и респираторного синдрома, проявляющегося ринофарингитом, трахеобронхитом [2,3,6], реже отитом. Развитие пневмонии быстрое, иногда постепенное с появлением лихорадки или субфебрилитета [2,6]. Ознобы и одышка не характерны. Кашель, часто непродуктивный или с отделением слизистой мокроты, является доминирующим симптомом. У 30–50% больных типичным является пароксизмальный, непродуктивный, мучительный, коклюшеподобный кашель низкого тембра, иногда сопровождающийся затруднением вдоха [3]. Эти пароксизмы кашля нередко обусловлены развитием феномена трахео–бронхиальной дискинезии, при которой значительно возрастает подвижность pars membranacea трахеи и крупных бронхов. При аускультации выслушиваются сухие и/или локальные влажные хрипы. Крепитация и признаки уплотнения легочной ткани отсутствуют. Плевральный выпот развивается редко. Нередки внелегочные симптомы: миалгии (обычно боли в мышцах спины и бедер), обильная потливость, мышечная слабость, артралгии, поражения кожи и слизистых, желудочно–кишечные нарушения, головные боли, иногда бессонница.
При рентгенологическом исследовании выявляют типичную пневмоническую инфильтрацию легочной паренхимы (чаще очагового и многоочагового характера), однако у 20–25% больных определяются лишь интерстициальные изменения, а изредка на стандартных рентгенограммах (особенно выполненных в жестком режиме) патологии не отмечается. Поэтому в случаях, когда клинически пневмония не вызывает сомнений, а результаты рентгенографии не доказательны – может использоваться компьютерная рентгеновская томография, обеспечивающая подтверждение диагноза благодаря просмотру изображения в различных режимах и отсутствию для метода скрытых зон.
Феномен трахео–бронхиальной дискинезии выявляется при выполнении форсированных экспираторных легочных проб. Характерным является появление дополнительных «ступеней» на спирографической кривой. Более точно наличие этого синдрома может быть доказано при рентгеноскопии трахеи с кашлевой пробой.
Лейкоцитарная формула периферической крови обычно не изменена. Возможен небольшой лейкоцитоз или лейкопения. Изредка отмечают немотивированную анемию. Посевы крови стерильны, а мокроты неинформативны.
Для микоплазменных пневмоний характерна диссоциация некоторых клинических признаков: высокая лихорадка в сочетании с нормальной лейкоцитарной формулой и слизистой мокротой; низкий субфебрилитет с проливными потами и тяжелой астенизацией. Таким образом, микоплазменная пневмония имеет определенные клинические особенности, сопоставление которых с эпидемиологической ситуацией позволяет принять правильное решение о выборе антибактериального препарата.
При хламидийной инфекции [3,6] развитию пневмонии нередко предшествует респираторный синдром в виде недомогания и фарингита, протекающего с сухим кашлем при нормальной или субфебрильной температуре тела. Развитие пневмонии подострое с появлением ознобов и лихорадки. Кашель быстро становится продуктивным с отделением гнойной мокроты. При аускультации в ранние сроки выслушивают крепитацию, более стабильным признаком являются локальные влажные хрипы. При долевых пневмониях определяют укорочение перкуторного звука, бронхиальное дыхание, усиление бронхофонии. Хламидийные пневмонии могут осложняться плевритом, который проявляется характерными плевральными болями, шумом трения плевры. При плевральном выпоте перкуторно определяется тупость, а при выслушивании – резкое ослабление дыхания. Некоторые больные переносят высокую лихорадку относительно легко. У детей описано коклюшеподобное течение хламидийных пневмоний, что связано с нередким развитием трахеобронхиальной дискинезии, являющейся характерным признаком и при легочном хламидиозе у взрослых. Из внелегочных проявлений чаще (5%) встречаются синуситы, значительно реже – миокардиты и эндокардиты. Рентгенологические находки чрезвычайно вариабельны. Выявляют инфильтративные изменения в объеме одной и более долей, нередко инфильтрация носит интерстициальный характер. В типичных случаях лейкоцитарная формула не изменена, однако нередко отмечается лейкоцитоз с нейтрофильным сдвигом
Больная Х., 15 лет, госпитализирована в отделение пульмонологии на 7–й день болезни. В школе вспышка острой респираторной инфекции. В классе у 5 из 25 учеников диагностирована пневмония. У пациентки диагноз пневмонии установлен на 2–й день болезни. Начата терапия амоксициллином/клавуланатом по 2,0 г/сут. Лечение в течение 5 дней без эффекта. Все дни сохранялась лихорадка до 38–38,5°С. При поступлении состояние средней тяжести. Температура тела 38,5°С. Клинические и рентгенологические данные соответствуют правосторонней нижнедолевой пневмонии. В анализе крови умеренный лейкоцитоз без нейтрофильного сдвига в лейкоцитарной формуле. Назначен азитромицин перорально по 500 мг/сут. Через несколько часов после первого приема антибиотика температура тела нормализовалась. При обследовании в сыворотке крови обнаружены в высоких титрах антитела к хламидиям класса IgM. Азитромицин применялся 12 дней. Исход – выздоровление.
В данном клиническом наблюдении основой для правильной клинической оценки и выбора эффективного антибиотика (азитромицин) явились характерный эпидемиологический анамнез и отсутствие эффекта от 5–дневной терапии усиленным b–лактамным антибиотиком в эффективной дозе.
Кроме монотерапии азитромицином, этот антибиотик нередко назначается в сочетании с b–лактамными препаратами. Если пациент госпитализируется по поводу пневмонии средней тяжести или тяжелого течения, часто практикуется [1,3,5] тактика деэскалации, подразумевающая использование для исходной терапии сочетания антибиотиков и обычно это сочетание b–лактамного препарата (аминопенициллины, цефалоспорины, карбапенемы) с макролидом, который назначается исходя из возможности легионеллезной или хламидийной инфекции. В последующем, после уточнения диагноза один из препаратов отменяется.
Несколько лет назад на 4–й день болезни в наше отделение был госпитализирован пациент Н., 42 лет. При поступлении состояние тяжелое: температура тела 39,0°С, нестабильная гемодинамика, ЧД – 36 в 1 мин. Клинически и рентгенологически – двусторонняя многодолевая (инфильтрация 3–х долей) пневмония. Лейкоцитоз 22,0 с палочкоядерным сдвигом 30%. Назначена антибактериальная терапия: меропенем 4,0 г/сут. внутривенно в сочетании с азитромицином 500 мг/сут. перорально. Применены прессорные амины и глюкокортикостероиды внутривенно, использована оксигенотерапия. Показатели гемодинамики удалось стабилизировать в течение 4 часов и дальнейшее применение стероидов и прессорных аминов прекращено. Этиологически пневмония расшифрована, как легионеллезная (в сыворотке крови обнаружены антитела к легионелле в титре 1:1024). Длительность лечения азитромицином – 18 дней, меропенемом – 4 суток (препарат отменен после установления диагноза легионеллеза). Оксигенотерапия использовалась 7 дней. Исход – выздоровление.
Можно обоснованно полагать, что исход заболевания у наблюдавшегося пациента представлялся бы сомнительным, если бы эмпирическая антибактериальная терапия проводилась лишь меропенемом, а азитромицин назначался только после установления легионеллезной природы пневмонии.
Это наблюдение побудило нас проводить деэскалационную антибактериальную терапию (b–лактамный антибиотик + макролид) почти у половины больных пневмониями и во всех случаях лечения пневмоний тяжелого течения.
При тяжелом течении пневмонии антибиотики применяются внутривенно. При внутривенном использовании азитромицин дозируется по 500 мг каждые 24 часа.
Следует считаться с затратами на антибактериальную терапию, которые могут быть весьма значительными. В последние годы успешно применяется [1,3–5] так называемая ступенчатая терапия. При использовании азитромицина по этой методике лечение начинается с внутривенного применения антибиотика по 500 мг каждые 24 часа. По достижении клинического эффекта (обычно через 2–3 дня), когда антибактериальная терапия обеспечила улучшение состояния больного, сопровождающееся снижением или нормализацией температуры тела, уменьшением лейкоцитоза, возможен переход на пероральное применение азитромицина (если предполагается хорошая всасываемость) по 0,25–0,5/24 часа. При высокой эффективности подобной методики она отличается меньшей стоимостью не только вследствие различия цен на парентеральные и таблетированные препараты, но и за счет уменьшения расхода шприцев, капельниц, стерильных растворов. Такая терапия легче переносится пациентами и реже сопровождается побочными эффектами.
Внутривенное и ступенчатое применение азитромицина обычно используется при лечении пневмоний тяжелого течения. При лечении других бронхолегочных инфекций, как правило, можно ограничиться пероральной терапией.
Приведенные данные и собственный многолетний опыт свидетельствуют о том, что в настоящее время азитромицин занимает одну из основных позиций в лечении бронхолегочных инфекций.
Литература
1. Практическое руководство по антиинфекционной химиотерапии (Под ред. Л.С.Страчунского, Ю.Б.Белоусова, С.Н.Козлова) // Смоленск, МАКМАХ, 2007.– 464 с.
2. Ноников В.Е. Атипичные пневмонии: второе рождение макролидов //Новый медицинский журнал.–1995.–№ 1.–с.5–7
3. Ноников В.Е. Тактика антибактериальной химиотерапии пневмоний //РМЖ.–1997.–Том 5.–№ 24,– с.1568–1578
4. Ноников В.Е. Антибиотики–макролиды в пульмонологической практике // Атмосфера: пульмонология и аллергология.–2004.– № 2 (13).– с.24–26
5. Bartlett J. Pocket Book of Infectious Diseases Therapy //Lippincott Williams & Wilkins.–2005–6.– 349p.
6. Zackom H. Pulmonary Differential Diagnosis //W.B.Saunders.– 2000.– 885 p
Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Читайте также:
