Неонатальный судороги. Классификация
Добавил пользователь Алексей Ф. Обновлено: 27.01.2026
Эпилепсия — заболевание головного мозга, соответствующее любому из следующих состояний:
- Не менее двух неспровоцированных (или рефлекторных) эпилептических приступов с интервалом > 24 ч.
- Один неспровоцированный (или рефлекторный) эпилептический приступ и вероятность повторных приступов, соответствующая общему риску рецидива (³ 60 %) после двух неспровоцированных эпилептических приступов, в следующие 10 лет.
- Диагноз эпилептического синдрома.
Критерии разрешения эпилепсии включают достижение определенного возраста у пациентов с зависящим от возраста эпилептическим синдромом либо отсутствие эпилептических приступов в течение 10 лет у пациентов, не получавших противосудорожные препараты более 5 лет.
Классификация эпилепсии (Международная противоэпилептическая лига (ILAE) 2017 г. )
Классификация эпилепсии проводится после определения критериев диагностики эпилепсии (определение выше). Классификация проводится с использованием трехуровнего ранжирования — определение типа приступов, типа эпилепсии и синдрома эпилепсии. Нейроимиджинг, ЭЭГ и другие исследования, если они есть, помогают улучшить классификацию на всех трех уровнях. Где это возможно, следует установить диагноз на всех трех уровнях. Этиологию эпилепсии следует устанавливать с самого начала и на каждом этапе всего диагностического пути. Знание этиологии может способствовать оптимизации классификации и имеет важные лечебные последствия для пациента.
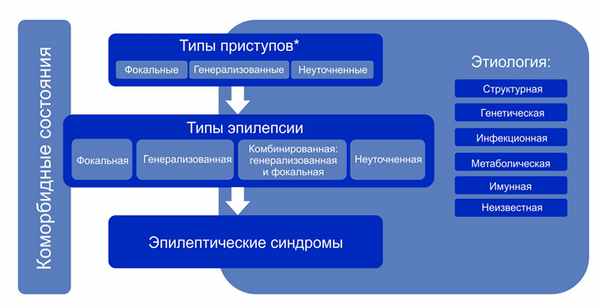
Структура Классификации эпилепсии ILAE 2017 г.
Примечание. * Оценивается по началу приступа.
Авакян Г. Н. Блинов Д. В. Лебедева А. В. Бурд С. Г. Авакян Г. Г. Классификация эпилепсии Международной Противоэпилептической Лиги: пересмотр и обновление 2017 года. Эпилепсия и пароксизмальные состояния. 2017; 9 (1): 6–25. DOI: 10.17749/2077–8333.2017.9. 1.006–025.
Алгоритм классификации эпилепсии:
- На первом этапе (уровне) определяют тип приступа: фокальный, генерализованный или с неизвестным началом.
- На втором этапе (уровне) устанавливают тип эпилепсии: фокальная, генерализованная или сочетанная фокальная и генерализованная, или неизвестная (unknown).
- На третьем этапе (уровне) определяют эпилептический синдром и коморбидность. Эпилептический синдром представляет собой совокупность характеристик, включая тип приступа, данные ЭЭГ и нейровизуализации, часто имеет возрастзависимый характер, провоцирующие факторы, хронозависимость и в ряде случаев определенный прогноз.
- На четвертом этапе (уровне) устанавливают этиологию эпилепсии: структурная, генетическая, инфекционная, метаболическая, иммунная или с неизвестной этиологией.
Генерализованная эпилепсия
Пациенты с генерализованной эпилепсией имеют генерализованные типы приступов и могут иметь типичные интериктальные и / или иктальные ЭЭГ паттерны, которые сопровождают генерализованные типы приступов (например, генерализованный спайк-волна). Сопутствуют семейная история генерализованных типов приступов или генерализованная эпилепсия.
Генетическая / идиопатическая генерализованная эпилепсия представляет собой эпилепсию с генерализованными приступами, ассоциированнами с генерализованными эпилептиформными паттернами ЭЭГ, такими как генерализованная спайк-волновая активность, которая, считается, имеет генетическую этиологию. Однако это не всегда означает, что эти эпилепсии унаследованы или могут передаваться потомству, поскольку генетическая этиология может быть спонтанной новой мутацией или наследование может быть сложным. Таким образом, термин «идиопатическая генерализованная эпилепсия» используется как синоним генетической генерализованной эпилепсии, и клиницист может выбрать, какой термин использовать, в зависимости от важности акцента на генетическом наследовании для конкретного пациента. Генетические / идиопатические генерализованные эпилепсии включают детскую абсансную эпилепсию, юношескую абсансную эпилепсию, юношескую миоклоническую эпилепсию, и эпилепсию с генерализованными тонико-клоническими приступами.
Фокальная эпилепсия
Пациенты с фокальной эпилепсией имеют фокальные типы приступов и могут иметь типичные интериктальные и / или иктальные ЭЭГ-паттерны, которые сопровождают фокальные типы приступов (такие как фокальные острые волны или фокальное интериктальное замедление). Нейроимиджинг демонстрирует фокальную структурную аномалию мозга и способствует установке диагноза, хотя пациенты с генетической этиологией и нормальной визуализацией могут также иметь фокальную эпилепсию. Фокальные эпилепсии могут быть унифокальными, мультифокальными или полушарными.
Сочетанная генерализованная и фокальная эпилепсия
Пациенты могут иметь как генерализованные, так и фокальные типы приступов, с интериктальными и / или иктальными ЭЭГ-паттернами, которые сопровождают оба типа приступов. Пациенты с синдромом Драве и синдромом Леннокс-Гасто могут иметь генерализованную и фокальную эпилепсию.
Неизвестная эпилепсия
Термин «неизвестный» используется для обозначения в случае, когда понимается, что у пациента есть эпилепсия, но невозможно определить, является ли она фокальной, генерализованной или комбинированной: фокальной и генерализованной. Это бывает при недостаточной информации для классификации эпилепсии, например, если ЭЭГ является нормальной / неинформативной.
Синдромы эпилепсии
В то время как концептуализация эпилепсий по их этиологии очень важна, эпилепсии также могут быть организованы (в соответствии с установленными достоверными общепринятыми клиническими и ЭЭГ — характеристиками) в эпилептические синдромы. Такие синдромы имеют типичный возраст начала приступа, специфические типы приступов и характеристики ЭЭГ и часто другие признаки, которые вместе взятые позволяют диагностировать конкретный эпилептический синдром. Идентификация синдрома эпилепсии полезна, так как она предоставляет информацию о том, какие основные этиологии следует учитывать и какие антиконвульсанты могут быть наиболее полезными. Некоторые эпилептические синдромы демонстрируют аггравацию приступов при определенных антиконвульсантах, чего можно избежать при ранней диагностике синдрома эпилепсии.
Эпилептические синдромы
Неонатальный и младенческий период:
- самокупирующиеся неонатальные приступы и самокупирующаяся семейная неонатальная эпилепсия;
- самокупирующаяся семейная и несемейная младенческая эпилепсия;
- ранняя миоклоническая энцефалопатия;
- синдром Отахара;
- синдром Веста;
- синдром Драве;
- миоклоническая эпилепсия младенчества, младенческая эпилепсия с мигрирующими фокальными приступами;
- миоклоническая энцефалопатия при непрогрессирующих заболеваниях;
- фебрильные приступы, фебрильные приступы плюс, генетическая эпилепсия с фебрильными приступами плюс.
Детский возраст:
- эпилепсия с миоклонически-атоническими (ранее – астатическими) приступами;
- синдром Леннокса–Гасто;
- фебрильные приступы, фебрильные приступы плюс;
- абсансная эпилепсия;
- эпилепсия с миоклоническими абсансами;
- детская затылочная эпилепсия с ранним дебютом (синдром Панайотопулоса);
- детская затылочная эпилепсия с поздним дебютом (синдром Гасто);
- фотосенситивная затылочная эпилепсия;
- самокупирующаяся эпилепсия с центрально-темпоральными спайками;
- атипичная эпилепсия с центрально-темпоральными спайками;
- эпилептическая энцефалопатия с продолженной пик-волновой активностью во время сна;
- синдром Ландау–Клеффнера;
- аутосомно-доминантная ночная лобная эпилепсия.
Подростковый и взрослый возраст:
- юношеская абсансная эпилепсия;
- юношеская миоклоническая эпилепсия;
- эпилепсия с изолированными генерализованными тонико-клоническими приступами;
- аутосомно-доминантная эпилепсия со слуховыми проявлениями;
- другие семейные височные эпилепсии.
Любой возраст:
- семейная фокальная эпилепсия с вариабельным фокусом;
- рефлекторные эпилепсии;
- прогрессирующие миоклонические эпилепсии.
Этиология эпилепсии
В последние годы значительно расширилось наше понимание основополагающих причин эпилепсии, подкрепленное достижениями в области современной нейровизуализации и генетического тестирования. Такая терминология, как «идиопатическая», «криптогенная» и «симптоматическая», больше не используется. Эпилепсии теперь описываются более точно конкретными основополагающими причинами.
Генетическая этиология
Понятие генетической эпилепсии заключается в том, что эпилепсия, насколько мы понимаем, является прямым результатом известного или предполагаемого генетического дефекта (ов), в котором судороги являются основным симптомом расстройства. Генетический дефект может возникать на хромосомном или молекулярном уровне. Важно подчеркнуть, что «генетический» не означает то же, что «унаследовано», поскольку мутации de novo не являются редкостью. Наличие генетической этиологии не исключает экзогенного влияния на возникновение эпилепсии.
Наиболее важные генетические причины эпилепсии, которые могут быть идентифицированы при клиническом тестировании:
Существует много способов, которыми генетические факторы могут способствовать развитию эпилепсии. Определенные генетические факторы, возможно, не были унаследованы и не могут быть переданы потомству. Вот некоторые важные генетические концепции, используемые на этом веб-сайте, и их определения:
- унаследованные аномалии генов, аутосомно-доминантное, аутосомно-рецессивное и менделевское наследование;
- приобретенные аномалии генов — de novo, спорадические, мозаицистические, зародышевые и соматические;
- полигенная / комплексная генетическая этиология.
Структурная этиология
Структурные эпилепсии определяются как имеющие выраженную структурную аномалию мозга, которая связана с существенно повышенным риском эпилепсии. Структурная аномалия мозга может быть приобретена (например, вследствие инсульта, травмы или инфекции) или может быть генетического происхождения; однако, как мы это понимаем в настоящее время, структурная аномалия мозга представляет собой отдельное нарушение, расположенное между приобретенным или генетическим дефектом и эпилепсией.
Нейроимиджинг
Магнитно-резонансная томография (МРТ) с использованием 1.5 Тесла аппарата является минимальным стандартным исследованием для исключения структурной аномалии. При этом исследовании важно выполнять протоколы, специфические для эпилепсии, которые позволяют тщательно изучать специфические приобретенные аномалии (например, склероз гиппокампа ) и тонкие пороки развития коры головного мозга, такие как фокальная дисплазия коры. Изображение с использованием 3 Тесла и использование передовых методов анализа программного обеспечения может помочь в выявлении структурных нарушений, не очевидных при обычной МРТ. Интериктальная и иктальная ЭЭГ вместе с дополнительными функциональными исследованиями нейровизуализации, такими как ПЭТ, ОФЭКТ и МЭГ, помогают внимательно изучить конкретную область мозга и идентифицировать тонкую аномалию. У детей младшего возраста в возрасте до 2 лет тонкие аномалии не могут быть выявлены из-за незаконченной миелинизации, и повторное исследование требуется в динамике.
Общие структурные аномалии мозга, связанные с эпилепсией:
- пороки развития коры головного мозга;
- сосудистые пороки развития;
- гиппокампальный склероз;
- гипоксически-ишемические структурные аномалии;
- травматическая повреждение мозга;
- опухоли;
- порэнцефалическая киста.
Метаболическая этиология
Метаболические эпилепсии определяются как имеющие определенное метаболическое нарушение, связанное с выраженным риском развития эпилепсии. Метаболические расстройства имеют генетическое происхождение; однако, как мы это понимаем в настоящее время, метаболические аномалии представляют собой отдельное нарушение, стоящее между генетическим дефектом и эпилепсией.
Важные метаболические эпилепсии:
- дефицит биотинидазы и голокарбоксилазы-синтазы;
- дефицит церебрального фолата;
- нарушения креатина;
- приступы при нарушении фолатного цикла;
- недостаточность транспортера глюкозы 1 (GLUT1);
- митохондриальные расстройства;
- пероксисомальные расстройства;
- пиридоксинзависимая эпилепсия.
Иммунная этиология
Иммунные эпилепсии определены как имеющие выраженную иммунную опосредованную этиологию с подтверждением воспаления центральной нервной системы, что, как было показано, связано с существенно повышенным риском развития эпилепсии.
Важные иммуноопосредованные эпилепсии:
- Синдром Расмуссена;
- Антителоопосредованная эпилепсия.
Инфекционная этиология
Наиболее распространенная этиология эпилепсии во всем мире является инфекционной, особенно в развивающихся странах. Инфекции в центральной нервной системе могут вызывать как острые симптоматические припадки (которые тесно связаны со сроками первичной инфекции), так и эпилепсией. Инфекционная этиология включает туберкулез, ВИЧ, церебральную малярию, нейроцистицеркоз, подострый склерозирующий панэнцефалит, церебральный токсоплазмоз. Эти инфекции иногда имеют структурный коррелят, однако основная причина эпилепсии определяется как инфекционный процесс. Инфекционная этиология может иметь специфические последствия лечения. Существуют также последствия для общественного здравоохранения, поскольку профилактика таких инфекций может снизить нагрузку на эпилепсию, особенно в развивающихся странах. Наиболее распространенные из таких инфекций следующие:
- бактериальный менингит или менингоэнцефалит;
- церебральная малярия;
- церебральный токсоплазмоз;
- цитомегаловирусная инфекция;
- ВИЧ;
- нейроцистицеркоз;
- туберкулез;
- вирусный энцефалит;
- подострый склерозирующий панэнцефалит;
- прочие инфекции (токсокариоз, шистосомоз, болезнь Лайма (нейроборрелиоз).
Неизвестная этиология
«Неизвестная» этиология должна рассматриваться нейтрально и обозначать, что природа основной причины возникновения эпилепсии пока неизвестна; это может быть фундаментальный генетический дефект или отдельное, пока еще установленное, нарушение.
Имитаторы эпилепсии
Существует ряд состояний, связанных с рецидивирующими пароксизмальными событиями, которые могут имитировать симптомы, и ошибочно диагностироваться как эпилепсия. Важно, чтобы эти расстройства учитывались при оценке пароксизмальных событий, так как частота ошибочных диагнозов при эпилепсии высока во всем мире. История заболевания и видеозапись приступов помогают установить правильный диагноз. Существуют некоторые состояния, при которых могут сосуществовать эпилептические и неэпилептические события.
Неонатальный судороги. Классификация
Неонатальный судороги. Классификация
Риск развития эпилептических приступов у новорожденных особенно высок, так как вероятность метаболических заболеваний, токсических поражений, нарушений структуры мозга и инфекций наиболее высока в периоде новорожденности по сравнению с другими возрастными периодами. Неонатальные судороги непохожи на эпилептические приступы у детей более старшего возраста и взрослых, так как генерализованные тонико-клонические приступы не развиваются на первом месяце жизни. Мозг новорожденных отличается незавершенностью ветвления аксонов и дендритов и процесса миелинизации, вследствие чего затруднено распространение эпилептиформных разрядов, приводящее к генерализованным приступам.
Выделяют по крайней мере пять типов эпилептических приступов, характерных для периода новорожденности.
Фокальные приступы представляют собой ритмичные сокращения мышечных групп, особенно мышц конечностей и лица. Эти приступы часто ассоциируются с локальным структурным поражением мозга, а также с инфекциями и субарахноидальным кровоизлиянием. Мультифокальные тонические приступы напоминают фокальные клонические судороги, однако отличаются вовлечением многих мышечных групп и часто возникают одновременно в нескольких группах мышц.
Тонические приступы характеризуются напряжением (ригидностью) конечностей и туловища и ассоциируются с фиксированной девиацией глаз. Миоклонические приступы представляют собой короткие фокальные или генерализованные подергивания мышц конечностей или туловища с тенденцией к вовлечению дистальных мышечных групп. Атипичные (стертые) неонатальные судороги включают жевательные движения, избыточное слюноотделение, изменение ритма дыхания (в том числе апноэ), моргание, нистагм, педалирующие движения (напоминающие езду на велосипеде) и изменения цвета кожных покровов.
Диагностика неонатальных судорог по клинической картине может быть затруднена, и в некоторых случаях двигательная активность новорожденных расценивается как проявления приступа, но ЭЭГ диагноз не подтверждает. Тем не менее выделено несколько клинических признаков, позволяющих отличить судороги от нормальной (неэпилептической) двигательной активности новорожденных.
Вегетативные нарушения, такие как тахикардия и повышение АД, часто ассоциируются с эпилептическими приступами, но нехарактерны для неэпилептических двигательных реакций новорожденных. Неэпилептическую двигательную активность новорожденных можно подавить, осторожно пытаясь ограничить движения ребенка, что невозможно при истинных приступах. Неэпилептические феномены активируются при сенсорной стимуляции, не оказывающей влияния на эпилептические приступы. Точное определение типа неонатальных судорог по классификации важно для правильного выбора антиэпилептической терапии.
Исследования с применением полиграфической записи ЭЭГ и видео-ЭЭГ-мониторинга вносят большой вклад в изучение особенностей неонатальных судорог и разработку медикаментозной терапии.
ЭЭГ классификация неонатальных судорог
Неонатальные судороги, при которых клинические проявления приступов сопровождаются эпилептиформными изменениями на ЭЭГ. К этой категории относятся приступы, клинические проявления которых сочетаются с эпи-лептиформной активностью на ЭЭГ и включают фокальные клонические, фокальные тонические и некоторые миоклонические приступы. Эпилептическая природа этих приступов не вызывает сомнения, и они хорошо отвечают на антиэпилептическую терапию.
Неонатальные судороги, клинические проявления которых не сочетаются с эпилептиформными изменениями на ЭЭГ. У новорожденных возможны клинические проявления неонатальных судорог без соответствующих им эпилептиформных изменений на ЭЭГ. Это характерно для всех генерализованных тонических приступов и атипичных судорог новорожденных, в некоторых случаях наблюдается и при миоклонических приступах. У новорожденных отмечается тенденция к угнетению ЦНС или развитию коматозного состояния как следствие гипоксически-ишемической энцефалопатии.
Вероятно, приступы этого типа могут представлять собой неэпилептические пароксизмы и не требуют антиэпилептической терапии (или терапия в данном случае может быть неэффективной).
Электрические эпилептические приступы при отсутствии клинических проявлений. Электрические эпилептические приступы (паттерн эпилептических приступов на ЭЭГ) в сочетании с выраженными нарушениями фонового ритма могут возникать у младенцев, находящихся в коматозном состоянии, не получающих антиконвульсанты. Кроме того, электрические эпилептические приступы (без клинических проявлений) могут сохраняться у пациентов с фокальными тоническими или клоническими приступами после начала приема антиконвульсантов.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Неонатальные судороги
Неонатальные судороги – синдром пароксизмальных мышечных сокращений, дебютирующий в первые 28 дней после рождения. Проявляется генерализованными или фокальными судорогами, сопровождающимися вегетативной симптоматикой, иногда с нарушением дыхания. На ЭЭГ наблюдается типичная картина эпилептического припадка, что в совокупности с анамнезом и клинической картиной подтверждает диагноз неонатальных судорог. Лечение комплексное. Проводится этиотропная терапия, обязательно назначение противосудорожных препаратов, может потребоваться ИВЛ. Прогноз чаще неблагоприятный.
Общие сведения
Неонатальные судороги фактически являются разновидностью симптоматической эпилепсии с привязкой к периоду новорожденности. Распространенность составляет от 1 до 16 случаев на 1000 новорожденных, патология чаще встречается у мальчиков. Играет роль степень доношенности ребенка, у недоношенных детей частота встречаемости выше, а течение более тяжелое. Неонатальные судороги занимают особое место в педиатрии, поскольку последствия судорожного синдрома необратимы, особенно если речь идет о ребенке в первый месяц жизни. Летальность составляет 15-40%, среди выживших детей высок процент инвалидизации. Нозология не до конца изучена, при современной базе знаний причины около 10% случаев патологии остаются невыясненными.
Причины и классификация неонатальных судорог
Мозг ребенка на момент рождения находится в незрелом состоянии, продолжают образовываться новые нейроны и межнейрональные связи. Этим обусловлена его высокая судорожная готовность. Как следствие, спектр причин, способных вызвать неонатальные судороги, очень широк. Чаще всего приступы провоцируются гипоксически-ишемической перинатальной энцефалопатией, которая является осложнением беременности и родов. Также судороги сопровождают травмы головного мозга с внутричерепными кровоизлияниями, опухоли головного мозга, внутриутробные инфекции и аномалии развития центральной нервной системы.
Неонатальные судороги могут быть связаны не только с церебральной патологией. Часто судорожный синдром обусловлен нарушениями метаболизма. Это могут быть наследственные патологии обмена конкретных витаминов, минералов и пр., в частности – пиридоксиновая зависимость, гипокальциемия, нарушения обмена мочевины, лизосомальные болезни накопления. Редко встречаются неонатальные судороги токсического генеза, когда у детей, рожденных от наркозависимых матерей, наблюдается своеобразный синдром отмены (неонатальный абстинентный синдром), проявляющийся судорожными припадками и другой симптоматикой. Подобная клиника характерна также в случае приема трициклических антидепрессантов и некоторых других препаратов во время беременности.
Клиническая классификация основана на типе судорожного синдрома. Выделяют тонические, клонические, миоклонические и атипичные судороги. Клиническая картина различается в зависимости от причины, но разные виды судорог могут наблюдаться под воздействием одного этиологического фактора. Также разделяют первичные (наследственные) и симптоматические неонатальные судороги. Лишь в 10% случаев судорожный синдром наблюдается изолированно. В МКБ-10 различают доброкачественные семейные неонатальные судороги и раннюю миоклоническую энцефалопатию, которая является злокачественным вариантом патологии. В остальных 90% случаев судорожный синдром сопровождается другой симптоматикой, специфичной для каждой конкретной нозологии.
Симптомы неонатальных судорог
Первые клинические проявления могут наблюдаться с момента рождения либо появиться спустя несколько дней и даже недель после периода благополучия или на фоне диагностированного заболевания. Время возникновения симптоматики зависит от основного диагноза. Тонические судороги чаще встречаются у недоношенных детей. Ребенок при этом запрокидывает голову, вытягивает руки вдоль туловища, характерно закатывание глазных яблок вверх, иногда отмечаются нарушения дыхания. Неонатальные судороги такого типа свидетельствуют о повреждении передних структур мозга и наблюдаются обычно в первые дни и часы жизни ребенка.
Чаще всего в клинической практике встречаются клонические и миоклонические неонатальные судороги, проявляющиеся генерализованными или локальными подергиваниями. Последний вариант характерен для травмы и кровоизлияния. Миоклонические неонатальные судороги развиваются практически при любом заболевании с клиникой судорожного синдрома. Редко встречаются атипичные проявления, выражающиеся в ритмичном подергивании глазных яблок, чмокании, вегетативных приступах. Отмечается цикличность возникновения симптоматики. Такой тип неонатальных судорог часто сопровождает негрубые аномалии развития головного мозга.
Диагностика неонатальных судорог
Постановка диагноза часто затруднена, поскольку неонатальные судороги могут быть обусловлены множеством разных причин, при этом судорожный синдром далеко не всегда занимает ведущее место в клинике. Большую роль играет выяснение анамнеза матери – учитываются имеющиеся соматические заболевания, семейный анамнез. Кроме того, педиатр выясняет особенности протекания беременности и родов. Возможно наличие диагностированной внутриутробной инфекции, родовой травмы новорожденных, недоношенности и т. д. Для разных заболеваний характерно начало судорог спустя различное время после рождения, и это также облегчает постановку конкретного диагноза.
Патологическая электрическая активность в головном мозге фиксируется при помощи ЭЭГ-исследования. Как правило, энцефалограмма обнаруживает комплексы «пик-волна» и медленные волны. Вне приступа наблюдается полное отсутствие патологических изменений на ЭЭГ либо незначительные изменения. Аномалии головного мозга и опухоли подтверждаются при помощи КТ и МРТ. Анализ спинномозговой жидкости пациентов с неонатальными судорогами позволяет выявить нарушения, характерные для внутриутробных инфекций, а также помогает в диагностике кровоизлияний. Метаболические синдромы и болезни накопления можно заподозрить по сопутствующим симптомам, диагноз подтверждается специфическими лабораторными тестами.
Лечение и прогноз неонатальных судорог
Лечение осуществляется в отделении интенсивной терапии, обязательно постоянное наблюдение и врачебный контроль, ребенку часто требуется респираторная поддержка. В терапии используются противосудорожные препараты. Такое лечение является симптоматическим, но его проведение жизненно необходимо, поскольку судорожный синдром сам по себе чрезвычайно опасен для жизни ребенка. Чем большее количество приступов переносит малыш, тем более тяжелый вред наносится его здоровью и тем хуже прогноз для дальнейшей жизни. Одновременно проводится этиотропная терапия: антибиотики и противовирусные препараты, оперативное лечение травм и опухолей, дегидратационная терапия, специфические препараты для лечения различных метаболических синдромов и др.
Прогноз чаще неблагоприятный. Исключение составляют доброкачественные семейные неонатальные судороги. Хорошо корректируется судорожный синдром, вызванный гипокальциемией. Любое другое заболевание, как правило, оказывает необратимое повреждающее действие на центральную нервную систему ребенка, что в дальнейшем приводит к нарушению социальной адаптации, отставанию в умственном развитии (ЗПР, олигофрения) и инвалидности. Высока смертность по причине неонатальных судорог, чаще летальные исходы наблюдаются у недоношенных детей, при массивных травмах и кровоизлияниях, грубых аномалиях развитиях и септических осложнениях. Предупредить неонатальные судороги можно только своевременной терапией основного заболевания.
Неонатальная эпилепсия
Неонатальные судороги – пароксизмальные состояния, проявляющиеся генерализованными или локальными мышечными сокращениями, вегетативно-висцеральными нарушениями, имитацией безусловных двигательных автоматизмов, сопровождающиеся специфическими изменениями на ЭЭГ в приступном периоде. Диагноз устанавливается на основании электроэнцефалографии; необходимо выявление причины судорог. Лечение зависит от этиологии заболевания.
Судороги выявляют у 1,4% доношенных детей и у 20% недоношенных Недоношенные младенцы Ребенок, родившийся до 37 недель беременности, считается недоношенным. Недоношенность определяется гестационным возрастом, в котором рождается ребенок. Раньше любой ребенок, родившийся с весом. Прочитайте дополнительные сведения . Судороги могут быть связаны с тяжелыми неонатальными проблемами и требовать немедленной оценки. Большинство судорог фокальные, вероятно потому, что генерализация эпилептической активности затруднена у новорожденных из-за отсутствия миелинизации и неполного формирования дендритов и синапсов в мозге.
У некоторых новорожденных, которым проводили электроэнцефалографию (ЭЭГ) для оценки судорог или других симптомов энцефалопатии (например, гипоактивности, сниженной реактивности) была выявлена субклиническая (бессимптомная) судорожная активность (≥ 20 секунд ритмической эпилептиформной электрической активности на ЭЭГ, но без клинических видимых судорожных проявлений). Когда субклиническая электрическая активность непрерывна и сохраняется в течение > 20 минут, ее определяют как электрический эпилептический статус.
Этиология неонатальных судорожных нарушений
Аномальные электрические разряды в центральной нервной системе (ЦНС) могут быть вызваны:
Первичными внутричерепными процессами (например, менингитом, ишемическим инсультом, энцефалитом, внутричерепными кровоизлияниями, опухолями, пороками развития)
Системными проблемами (например, гипоксией-ишемией, гипогликемией, гипокальциемией, гипонатриемией, другими нарушениями метаболизма)
По клиническим признакам судороги, развивающиеся в результате внутричерепного процесса, обычно не могут быть дифференцированы от судорог, возникающих в результате системных проблем (могут иметь как очаговые, так и генерализованные проявления).
Гипоксически-ишемическое поражение – наиболее распространенная причина возникновения судорог у новорожденных, возникающая до, во время или после родов (см. Краткий обзор перинатальных респираторных заболеваний Обзор перинатальных респираторных заболеваний (Overview of Perinatal Respiratory Disorders) Процесс родов сопровождается обширными физиологическими изменениями (см. также Легочная функция новорожденного (Neonatal Pulmonary Function)), которые иногда выявляют состояния, которые не представляли. Прочитайте дополнительные сведения ). Такие припадки могут быть очень серьезными и с трудом поддаются лечению, но они имеют тенденцию уменьшаться через 3–4 дня. Когда для лечения неонатальной гипоксии применяется терапевтическая гипотермия (обычно это охлаждение всего тела), судороги могут быть менее тяжелыми, но могут повторяться во время согревания.
Ишемический инсульт Ишемический инсульт Ишемический инсульт является внезапной неврологической недостаточностью, вызванной очаговой ишемией головного мозга с постоянным инфарктом мозга (например, положительные результаты при диффузионно-взвешенном. Прочитайте дополнительные сведения , вероятнее всего, может развиться у новорожденных с полицитемией Перинатальная полицитемия и синдром повышенной вязкости Полицитемия – аномальное увеличение эритроцитарной массы, определенное у новорожденных при венозном гематокрите ≥ 65%. Такое увеличение может привести к повышенной вязкости крови с осаждением. Прочитайте дополнительные сведения , тромбофилией вследствие генетического расстройства или тяжелой гипотензией, но может возникать и у новорожденных без каких-либо факторов риска. Инсульт обычно происходит в области средней мозговой артерии или, если связан с гипотензией, в дренируемых зонах. Судороги в результате инсульта, как правило, фокальные и могут привести к апноэ.
Неонатальные инфекции Обзор неонатальных инфекций (Overview of Neonatal Infections) Пути заражения неонатальной инфекцией: в утробе матери трансплацентарно, либо через разрыв околоплодных оболочек; в родовом канале во время родов (интранатально); из внешних источников после. Прочитайте дополнительные сведения , такие как менингит Бактериальный менингит новорожденных Бактериальный менингит новорожденных – это воспаление менингеальных оболочек, вызванное бактериальной инвазией. Признаки заболевания такие же, как и при сепсисе: раздражение центральной нервной. Прочитайте дополнительные сведения и сепсис Неонатальный сепсис Неонатальный сепсис является инвазивной инфекцией, как правило, бактериальной, развивающейся в неонатальном периоде. Симптомы сепсиса многообразны, неспецифичны и включают снижение спонтанной. Прочитайте дополнительные сведения , могут вызвать судороги; в таких случаях судороги, как правило, сопровождаются другими симптомами и признаками. Стрептококки группы B и грамотрицательные бактерии – распространенные возбудители таких инфекций у новорожденных. Энцефалит, вызванный цитомегаловирусом Врожденная и перинатальная цитомегаловирусная (ЦМВ) Цитомегаловирусная инфекция может быть приобретена пренатально или перинатально и является наиболее распространенной врожденной вирусной инфекцией. Признаками при рождении, если они присутствуют. Прочитайте дополнительные сведения , вирусом краснухи Врожденная краснуха Врожденная краснуха является вирусной инфекцией, передаваемой от матери ребенку во время беременности. Признаками этого заболевания являются множественные врожденные аномалии, которые могут. Прочитайте дополнительные сведения , Treponema pallidum Врожденный сифилис Врожденный сифилис является мультисистемной инфекцией, вызывается Treponema pallidum и передается плоду через плаценту. К ранним симптомам относят: поражения кожи, лимфатических узлов. Прочитайте дополнительные сведения Toxoplasma gondii. Проявления заболевания, если они имеют место, включают: недоношенность, задержку внутриутробного. Прочитайте дополнительные сведенияВнутричерепное кровоизлияние Кровоизлияния в головной мозг Стимуляция сокращения матки и родов иногда приводит к нанесению физических травм ребенку. Риск неонатальных травм в результате тяжелых или травматических родов снижается за счет увеличения использования. Прочитайте дополнительные сведения включая субарахноидальное Субарахноидальное кровоизлияние Стимуляция сокращения матки и родов иногда приводит к нанесению физических травм ребенку. Риск неонатальных травм в результате тяжелых или травматических родов снижается за счет увеличения использования. Прочитайте дополнительные сведения , может вызвать судороги. Внутрижелудочковое кровоизлияние, которое чаще всего возникает у недоношенных детей Недоношенные младенцы Ребенок, родившийся до 37 недель беременности, считается недоношенным. Недоношенность определяется гестационным возрастом, в котором рождается ребенок. Раньше любой ребенок, родившийся с весом. Прочитайте дополнительные сведения , является результатом кровотечения в герминальный матрикс (перивентрикулярную область, которая дает начало нейронам и глиальным клеткам во время развития).
Гипонатриемия Неонатальная гипонатриемия Гипонатриемия – концентрация натрия в сыворотке крови 135 мЭкв/л ( 135 ммоль/л). Значительная гипонатриемия может вызвать судороги или кому. Лечение состоит в осторожном замещении натрия внутривенным. Прочитайте дополнительные сведения может возникнуть в результате снижения концентрации натрия из-за разбавления (когда перорально или внутривенно вводится слишком много воды, особенно при гиповолемии, что, при достаточно серьезной ситуации, приводит к повышению уровня антидиуретического гормона [АДГ], несмотря на низкую осмолярность сыворотки [неосмотическое высвобождение АДГ]) или от потери натрия с калом или мочой.
Гипокальциемия Неонатальная гипокальциемия Гипокальциемия – это общая концентрация сывороточного кальция 8 мг/дл (2 ммоль/л) у доношенных новорожденных или 7 мг/дл (1,75 ммоль/л) у недоношенных детей. Ее также определяют, как уровень. Прочитайте дополнительные сведения (сывороточный уровень кальция 7,5 мг/дл [ 1,87 ммоль/л]) обычно сопровождается сывороточным уровнем фосфора > 3 мг/дл ( > 0,95 ммоль/л) и в иных случаях может проходить бессимптомно. Факторы риска развития гипокальциемии – недоношенность, интранатальная асфиксия, родовые травмы.
Гипомагнезиемия является редкой причиной судорог, которые могут возникнуть при уровне магния в сыворотке крови 1,4 мгЭкв/л ( 0,7 ммоль/л). Гипомагнезиемия часто сопутствует гипокальциемии и должна быть исключена у новорожденных с гипокальциемией, если судороги продолжаются после адекватной терапии кальцием.
Пороки развития ЦНС Обзор врожденных неврологических аномалий Врожденные аномалии мозга обычно вызывают тяжелые неврологические дефициты, а некоторые могут быть фатальными. Некоторые из наиболее серьезных неврологических аномалий (например, анэнцефалия. Прочитайте дополнительные сведения также могут вызывать судороги.
Неонатальные судороги могут быть семейными, а некоторые имеют генетические причины. Доброкачественные семейные неонатальные судороги являются калиевой каналопатией, которая наследуется по аутосомно-доминантному типу. Ранняя младенческая эпилептическая энцефалопатия (синдром Oтахара) - редкое заболевание, связанное с различными мутациями.
Симптомы и признаки неонатального судорожного расстройства
У новорожденных судороги обычно очаговые и с трудом отличаются от нормальной активности новорожденных, поскольку могут проявляться в виде жевания или движений, напоминающих езду на велосипеде. Общие проявления включают мигрирующие клонические подергивания конечностей, чередующиеся с гемисудорогами и примитивными подкорковыми приступами (которые вызывают остановку дыхания, жевательные движения, постоянные отклонения глаз или нистагмоидные движения и эпизодические изменения мышечного тонуса). Генерализованные тонико-клонические припадки редки.
Бессимптомная электроэнцефалографическая эпилептформная активность часто отмечается после гипоксически-ишемического инсульта (в том числе перинатальной асфиксии или инсульта), а также у новорожденных с инфекциями ЦНС, особенно после проведенного противоэпилептического лечения, которое скорее курирует только клинические проявления, а не электрическую судорожную активность.
Диагностика неонатальных судорожных нарушений
Лабораторные исследования (например, анализ крови на глюкозу, электролиты, анализ цереброспинальной жидкости (ЦСЖ), посев образцов мочи и крови; иногда генетические исследования)
Обычно визуализация головного мозга
Диагностическая оценка начинается со сбора подробного семейного анамнеза и физикального обследования.
Синдром повышенной нервно-рефлекторной возбудимости, проявляющийся в виде асинхронных движений в мышцах конечностей, следует отличать от истинных судорожных проявлений. Приступ повышенной нервно-рефлекторной возбудимости, как правило, носит стимул-индуцированный характер и может быть остановлен путем удерживания конечности; в отличие от него, судорожные припадки возникают спонтанно и двигательная активность сохраняется даже тогда, когда конечность удерживается на месте.
ЭЭГ-мониторинг имеет большое значение и время записи иногда нужно продлевать, особенно когда трудно определить наличие судорог у новорожденного. ЭЭГ также необходима для контроля ответа на лечение.
Запись видео-ЭЭГ должна охватывать периоды активного и спокойного сна и, следовательно, должна продолжаться ≥ 2 часов. Нормальная ЭЭГ с сохранными физиологическими паттернами различных стадий сна является хорошим прогностическим признаком; ЭЭГ с серьезными диффузными изменениями биоэлектрической активности головного мозга (например, диффузное уплощение биоэлектрического сигнала или паттерн «вспышка – подавление») прогностически неблагоприятна.
Прикроватная ЭЭГ с видеомониторингом в течение ≥ 24 часов может обнаружить продолжающиеся бессимптомные электрические судороги, в частности в течение нескольких первых дней после инсульта в ЦНС.
Лабораторные методы
Лабораторные исследования с целью диагностики основного заболевания должны быть проведены в экстренном порядке, тесты включают пульсоксиметрию, определение в сыворотке крови уровней глюкозы, натрия, калия, хлора, бикарбоната, кальция и магния и проведение люмбальной пункции для анализа СМЖ (определения количества и морфологии клеток, подсчета белка и глюкозы), а также бактериологического посева. Также следует получить результаты бакпосевов мочи и крови.
Потребность в других метаболических тестах (например, рН артериальной крови, уровень газов в крови, билирубин в сыворотке крови, амино- или органические кислоты в моче) или анализ на часто принимаемые наркотики (передаются новорожденным трансплацентарно или при грудном вскармливании) назначаются в зависимости от клинической ситуации.
Генетическое тестирование должно быть рассмотрено у детей с рецидивирующими или рефрактерными судорогами неопределенной этиологии.
Методы визуализации
Визаулизирующие исследования, как правило, проводятся, если причина не очевидна (например, изменение содержания глюкозы или электролитов). МРТ является более предпочтительным методом, но не всегда возможна; в таких случаях, выполняется КТ головы.
У очень ослабленных детей, которые не могут быть доставлены в радиологию, может быть сделано УЗИ исследование с помощью портативного аппарата; оно может обнаружить внутрижелудочковое, а не субарахноидальное кровоизлияние. МРТ или КТ проводится при стабильном состояние младенцев.
КТ головы может обнаружить внутричерепное кровотечение и некоторые пороки развития головного мозга. МРТ визуализирует мальформации более четко и может обнаружить ишемическую ткань в течение нескольких часов после появления.
Магнитно-резонансная спектроскопия может помочь определить степень ишемического повреждения или определить накопление определенных нейромедиаторов, связанных с основным метаболическим расстройством.
Прогноз при неонатальных судорожных нарушениях
Прогноз зависит от этиологии:
Около 50% новорожденных с судорогами вследствие гипоксически-ишемического поражения ЦНС имеют в дальнейшем нормальное психомоторное развитие.
Большинство новорожденных с судорогами вследствие субарахноидального кровоизлияния, гипокальциемии или гипонатриемии также имеют благоприятный прогноз.
Для пациентов с тяжелыми внутрижелудочковыми кровоизлияниями характерен более тяжелый прогноз.
Для идиопатических припадков или припадков вследствие пороков развития, раннее начало прогностически связывают с худшими показателями нервной системы.
Подозревается, но не доказано, что длительные или частые судорожные приступы у новорожденных могут вызвать большее повреждение, чем нарушения, вызванные основным расстройством. Однако, есть основания считать, что метаболический стресс, возникающий на фоне длительной патологической активности нервных клеток во время продолжительных судорог, может привести к дополнительному повреждению мозга. При таких повреждениях головного мозга, как гипоксия-ишемия, инсульт или инфекция, у новорожденных может возникнуть серия судорог, которые обычно исчезают через 3-4 дня и могут возникнуть снова через месяцы и годы при повреждениях головного мозга. Судороги вследствие других причин могут быть более стойкими в неонатальном периоде.
Лечение неонатальных судорожных нарушений
Лечение причины заболевания
Лечение неонатальных судорог прежде всего направлено на устранение основной причины заболевания.
Лечение причины заболевания
При низком содержании в сыворотке крови глюкозы вводят 10%-ный раствор декстрозы внутривенно по 2 мл/кг под контролем уровня глюкозы в сыворотке крови; по мере необходимости проводят дополнительные введения, но с осторожностью, чтобы не вызвать гиперликемию.
При гипокальциемии применяют 10%-ный кальций глюконат 1 мл/кг внутривенно (9 мг/кг элементарного кальция); повторные введения показаны при постоянных гипокальциемических судорогах. Скорость инфузии глюконата кальция не должна превышать 0,5 мл в минуту (50 мг в минуту); во время инфузии необходимо проводить непрерывный кардиомониторинг. Следует избегать избыточной экстравазации, поскольку это может вызвать шелушение кожи.
При гипомагниемии вводят 0,2 мл/кг (100 мг/кг) 50%-ного раствора сульфата магния внутримышечно.
Бактериальные инфекции следует лечить антибиотиками.
Герпетический энцефалит лечат ацикловиром.
Противоэпилептические препараты
Противоэпилептические препараты назначаются в случаях, если судороги не прекращаются вскоре после коррекции обратимых расстройств, таких как гипогликемия, гипокальциемия, гипомагниемия, гипонатриемия или гипернатриемия.
Фенобарбитал по-прежнему является наиболее широко используемым препаратом; нагрузочная доза составляет 15-20 мг/кг внутривенно. Если судороги продолжаются, каждые 15-30 минут может быть внутривенно введено 5-10 мг/кг до прекращения приступа или до максимальной дозы 40 мг/кг. Если судороги являются стойкими, поддерживающая терапия может быть начата через 24 часа по 1,5-2 мг/кг каждые 12 часов и увеличена до 2,5 мг/кг каждые 12 часов, основываясь на клиническом ответе или ЭЭГ, или на концентрации препаратов в сыворотке. Продолжают внутривенное введение фенобарбитала, особенно если приступы являются частыми или длительными. Когда ребенок стабилен, фенобарбитал может быть дан перорально 3-4 мг/кг 1 раз/день. Терапевтические уровни фенобарбитала в сыворотке крови составляют 20–40 мкг/мл (85–170 мкмоль/л), но иногда необходимы, хотя бы временно, более высокие уровни.
Леветирацетам используется для лечения судорог у новорожденных, потому что он менее сомногенный, чем фенобарбитал. Препарат вводят внутривенно в нагрузочной дозе 20-60 мг/кг со скоростью 2-5 мг/кг/минуту, затем терапию можно продолжить в дозе 10-30 мг/кг внутривенно каждые 12 часов. Терапевтические уровни для новорожденных четко не определены.
Лоразепам в дозе 0,1 мг/кг внутривенно можно использовать первоначально при продолжительных или резистентных судорогах и повторять введение с 5–10-минутными интервалами до 3 доз в течение 8 часов.
За новорожденными, которые получают противоэпилептические препараты внутривенно, необходимо тщательное наблюдение; большие дозы и комбинации препаратов, в частности лоразепама с фенобарбиталом, могут вызвать угнетение дыхания.
Оптимальная продолжительность поддерживающей терапии неизвестна для любого из противосудорожных препаратов и зависит от основной этиологии судорог и наличия факторов риска рецидива судорог.
Ключевые моменты
Неонатальные судороги обычно возникают как реакция на системное заболевание или поражение центральной нервной системе (например, гипоксию/ишемию, инсульт, кровоизлияния, инфекции, метаболические расстройства, структурные аномалии головного мозга).
Неонатальные судороги, как правило, очаговые и их трудно распознавать; общие проявления включают мигрирующие клонические судороги конечностей, жевательные движения, стойкие девиации глаз или нистагм и эпизодические изменения мышечного тонуса.
Электроэнцефалография является основным методом диагностики; для определения причины, как правило, проводятся лабораторные исследования и нейровизуализация.
Лечение ориентировано на устранение причины заболевания.
Авторское право © 2022 Merck & Co., Inc., Rahway, NJ, США и ее аффилированные лица. Все права сохранены.
Неонатальные судороги
Неонатальные судороги – пароксизмальные
состояния, возникающие в периоде
новорожденности и проявляющиеся
генерализованными или локальными
мышечными сокращениями, вегетативновисцеральными нарушениями или имитацией
безусловных двигательных автоматизмов,
сопровождающиеся специфическими
изменениями на ЭЭГ в приступный период по
типу пик-волны или медленноволновой
активности
Частота НС среди новорожденных 1,116/1000
Мальчики:девочки=1,3-1,8:1
Чем меньше гестационный возраст
ребенка – тем чаще НС (32-36 нед – 1,68%, 31 нед – 20%)
Симптоматические НС – 90%
Идиопатические НС – 10%
4. ИДИОПАТИЧЕСКИЕ НЕОНАТАЛЬНЫЕ СУДОРОГИ
ДОБРОКАЧЕСТВЕННЫЕ НЕОНАТАЛЬНЫЕ СУДОРОГИ
(СУДОРОГИ 5-ГО ДНЯ)
Возникают на фоне относительного благополучия
Возникают на 3-7 сутки (чаше на 5-е)
Неонатальный эпилептический статус генерализованных
мультифокальных клонических (реже очаговых
клонических) судорог
Продолжительность до 20 часов
Приступы апноэ до 1 мин
Иктальная ЭЭГ – острые θ-волны или альтернирующие
вспышки θ-волн
Резистентность к любой терапии
Купируются самостоятельно
Патогенез неизвестен (возможно нарушение обмена цинка)
Прогноз - благоприятный
5. ИДИОПАТИЧЕСКИЕ НЕОНАТАЛЬНЫЕ СУДОРОГИ
ДОБРОКАЧЕСТВЕННЫЕ СЕМЕЙНЫЕ НЕОНАТАЛЬНЫЕ
СУДОРОГИ
Доминантно-наследуемые НС
Возникают на фоне относительного благополучия
Возникают на 1-3 день
Клинически – простые или сложные моторные
автоматизмы, генерализованные или локальные
клонические судороги
Длятся от 5-7 дней до нескольких недель
ЭЭГ – в межприступном периоде нормальная, в момент
приступа – генерализованная или альтернирующая θактивность
Резистентность к терапии
Прогноз благоприятный в 85-90%
Эпилепсия в дальнейшем – 10-15%
СИМПТОМАТИЧЕСКИЕ НС
(ЭТИОЛОГИЯ)
Асфиксия (гипоксически-ишемическая
энцефалопатия)
Родовая травма (кровоизлияния, травматическая
дислокация)
Транзиторные метаболические нарушения
(глюкозы, электролитов, КЩР, билирубина,
токсемия матери, влияние медикаментов)
Наследственная патология обмена (аминокислот,
углеводов, липидов, мукополисахаридов,
электролитов, витаминов)
СИМПТОМАТИЧЕСКИЕ НС (ЭТИОЛОГИЯ)
Факоматозы (с.Штурге-Вебера, туберозный
склероз)
Врожденные аномалии развития мозга
(изолированные, при множественных уродствах и
хромосомных синдромах)
Внутриутробные инфекции
Вторичные токсико-метаболические и
гемодинамичские нарушения при врожденных и
наследственных заболеваниях внутренних
органов (сердца, легких, почек, печени,
эндокринных желез)
Объемные внутричерепные образования
(опухоли мозга, сосудистые аномалии, абсцессы,
гигромы)
8. РАБОЧАЯ КЛАССИФИКАЦИЯ НС (Brown, Minnis,1980)
-
ТОНИЧЕСКИЕ СУДОРОГИ
КЛОНИЧЕСКИЕ СУДОРОГИ
Фокальные
Мультифокальные
Генерализованные (билатеральные)
ФРАГМЕНТАРНЫЕ СУДОРОГИ
Моторные
Офтальмические
Отключение сознания
Апноэ (цианоз)
МИОКЛОНИЧЕСКИЕ СУДОРОГИ
9. ТОНИЧЕСКИЕ НЕОНАТАЛЬНЫЕ СУДОРОГИ
Возникают в остром периоде ГИЭ при
массивных кровоизлияниях, при врожденных
аномалиях мозга, токсической
билирубиновой энцефалопатии
Генерализованное тоническое напряжение
мышц туловища, шеи, конечностей по типу
децеребрационной ригидности
(разгибательная поза с запрокинутой назад
головой, разведенными руками, вытянутыми
напряженными ногами)
Длительность приступа до 1 мин
Апное, цианоз, гиперемия кожи
10. ТОНИЧЕСКИЕ НЕОНАТАЛЬНЫЕ СУДОРОГИ
ЭЭГ во время приступа –
медленноволновая активность
Дифференциальный диагноз – с
децеребрационной ригидностью
(сдавление среднего мозга при ВЧГ,
сочетание с глазодвигательными
симптомами и нарушением ритма
дыхания). Здесь нет изменений на ЭЭГ
и эффекта от ПСТ
11. КЛОНИЧЕСКИЕ НЕОНАТАЛЬНЫЕ СУДОРОГИ
Ритмичные мышечные подергивания 1-8 в 1 сек
Корковый генез
ЭЭГ иктальная – пик-волна, интериктальная –
может быть не изменена
ФОКАЛЬНЫЕ КЛОНИЧЕСКИЕ НЕОНАТАЛЬНЫЕ
СУДОРОГИ
Этиология – ГИЭ с фокальными инфарктами и
очаговыми кровоизлияниями, АВМ, абсцессы,
врожденные опухоли
Четкая локализация клоний, после приступапарез
Локальные изменения на ЭЭГ
12. КЛОНИЧЕСКИЕ НЕОНАТАЛЬНЫЕ СУДОРОГИ
МУЛЬТИФОКАЛЬНЫЕ КЛОНИЧЕСКИЕ НЕОНАТАЛЬНЫЕ
СУДОРОГИ
Диффузная судорожная активность коры (метаболические
нарушения, диффузные корковые дисплазии)
«Мигрирующий» характер судорог
ЭЭГ иктальная – диффузные МВ, отдельные пик-волны
ГЕНЕРАЛИЗОВАННЫЕ (БИЛАТЕРАЛЬНЫЕ) КЛОНИЧЕСКИЕ
НЕОНАТАЛЬНЫЕ СУДОРОГИ
В 95% трансформируются из фокальных
Симметричные судороги конечностей, потеря сознания,
нарушения ритма дыхания, цианоз, гиперсаливация
13. ФРАГМЕНТАРНЫЕ НЕОНАТАЛЬНЫЕ СУДОРОГИ (АТИПИЧНЫЕ, СТЕРТЫЕ)
Полиэтиологичность
Полиморфизм клиники
Сочетание различных типов
Могут трансформироваться из
тонических или клонических НС при
их активнос лечении
Диагностика – ЭЭГ-видомониторинг
(пик-волновые изменения во время
приступов
14. ФРАГМЕНТАРНЫЕ НЕОНАТАЛЬНЫЕ СУДОРОГИ (АТИПИЧНЫЕ, СТЕРТЫЕ)
АТИПИЧНЫЕ МОТОРНЫЕ НС
Клинически – имитация АШТР, «плавающие»
движения рук, педалирование, оперкулярные
пароксизмы
Может быть потеря сознания, апноэ, цианоз
ОФТАЛЬМИЧЕСКИЕ (ГЛАЗОДВИГАТЕЛЬНЫЕ) НС
Приступы горизонтального нистагма, движения
по типу «заходящего» или «восходящего» солнца
Может быть потеря сознания, апноэ, цианоз
15. ФРАГМЕНТАРНЫЕ НЕОНАТАЛЬНЫЕ СУДОРОГИ (АТИПИЧНЫЕ, СТЕРТЫЕ)
АТИПИЧНЫЕ НС
Кратковременно отключение
сознания – аналог абсанса у детей
старшего возраста?
ЭПИЛЕПТИЧЕСКИЕ НЕОНАТАЛЬНЫЕ
АПНОЭ
Частый и неблагоприятный вариант
12-13% - летальный исход
16. МИКЛОНИЧЕСКИЕ НЕОНАТАЛЬНЫЕ СУДОРОГИ
АКСИАЛЬНЫЕ МИОКЛОНИЧЕСКИЕ НС
Молниеносное сгибание головы, шеи
(кивки, клевки) 1-3 приступа в 1 сек
Могут сочетаться с вегетативновисцеральными нарушениями, мидриазом
МИОКЛОНИЧЕСКИЕ НС
Ритмичные симметричные сгибания
конечностей (чаще рук) 1 приступ в 1 сек
(имитация спонтанного р-са Моро)
17. МИКЛОНИЧЕСКИЕ НЕОНАТАЛЬНЫЕ СУДОРОГИ
СМЕШАННЫЕ МИОКЛОНИЧЕСКИЕ НС
Сочетание «клевков» с флексорным
сгибанием или разгибанием конечностей
При выраженных поражениях мозга
(тяжелые гипоксически-ишемические
поражения, с.Айкарди, микрополигирия,
болезни обмена)
Это переход к с.Отахара или с.Веста
ЭЭГ – в момент приступа и
интериктальная гипсаритмия
Выраженные нарушения нервнопсихического развития
Неблагоприятный прогноз
18. ДИФФЕРЕНЦИАЛЬНЫЙ ДИАГНОЗ НС
ФЕНОМЕНЫ ДЛЯ
ДИФФЕРЕНЦИРОВАНИЯ:
Вздрагивания
Р.Моро
Тремор подбородка и
конечностей
Дистонические эпизоды
Врожденный атетоз
Неонатальные
гиперкинезы
Экстензорные спазмы
Децеребрационная
ригидность
Доброкачественный
миоклонус
новорожденных
ОТЛИЧИТЕЛЬНЫЕ
ПРИЗНАКИ
НЕЭПИЛЕПТИЧЕСКИХ
СОСТОЯНИЙ:
Наличие провоцирующего
фактора
Нестереотипность
пароксизмов
Отсутствие
эпилептический изменений
на ЭЭГ
Отсутствие эффекта от
терапии АЭП
19. ТЕРАПИЯ НС
ЛЕЧЕНИЕ, НАПРАВЛЕННОЕ НА КОРРЕКЦИЮ
ВЫЯВЛЕННЫХ НАРУШЕНИЙ
Коррекция гипогликемии, гипокальциемии, введение
пиридоксина
АНТИЭПИЛЕПТИЧЕСКОЕ ЛЕЧЕНИЕ (2-4 нед)
Фенобарбитал – препарат выбора (кроме
миоклонических) начинать с 15-20 мг/кг/сут, на 2-3
сутки 6-8 мг/кг/сут, поддерживающая доза 1-2
мг/кг/сут
Дифенин (с 20 мг/кг, затем 4-6мг/кг/сут)
Гексамедин (15-20 мг/кг/сут, затем 5-15 мг/кг/сут)
20. ТЕРАПИЯ НС
АНТИЭПИЛЕПТИЧЕСКОЕ ЛЕЧЕНИЕ (2-4 нед)
Карбамазепин – при мультифокальных НС, с
фб (7-15 мг/кг/сут)
Клоназепам – при резистентных и
полиморфных (1-2 дня парентерально 0,10,2мг/кг, затем перорально 0,2-0,3 мг/кг
Нитразепам –при миоклонических,
фрагментарных НС, апное; с0,3-0,5 мг/кг до 1
мг/кг 3 раза в сутки
Депакин – при миоклоническихъ и
фрагментарных (10-30 мг/кг)
21. ПРОГНОЗ НС
Летальность 12,5-34,8%
2/3 летальных исходов – 1-й месяц
жизни, из них 44% - первые 36 часов,
70% - первые 72 часа жизни
70% - нормальное развитие
30% - нарушения развития
18% - эпилепсия и ДЦП
22. ПРОГНОЗ НС
ФАКТОРЫ ПЛОХОГО ПРОГНОЗА ДЛЯ ДЕТЕЙ С
НС:
Оценка по Апгар ниже 7 баллов
Необходимость в реанимации в первые
минуты жизни
Дебют приступов в 1-е сутки жизни
Продолжительность приступов более 30 мин
Тонический, миоклонический,полиморфный
характер приступов
Уплощенная ЭЭГ-кривая с
пароксизмальными изменениями в
межприступном периоде
23. ФЕБРИЛЬНЫЕ СУДОРОГИ
Фебрильные судороги - эпилептические
приступы, возникающие в раннем
детском возрасте (преимущественно от
1 до 5 лет) на фоне заболевания,
протекающего с лихорадкой и
отсутствием симптомов нейроинфекции
ФС – 85% всех судорожных состояний у детей
Распространенность среди детей до 5 лет 214/100
Соотношение мальчики/девочки=1,4/1
Преобладающий возрастной интервал 17-23
мес
85% - до 4 лет
26. ЧАСТОТА ВСТРЕЧАЕМОСТИ ФЕБРИЛЬНЫХ СУДОРОГ (%) В РАЗЛИЧНЫЕ ВОЗРАСТНЫЕ ПЕРИОДЫ (Berg, 1992; Murphy,1993)
27. ЭТИОЛОГИЯ И ПАТОГЕНЕЗ ФС
Генетическая предрасположенность
Перинатальная патология ЦНС
Патология беременности и родов (22%),
затяжные роды (21%), асфиксия (7,5%), тугое
обвитие пуповины (4,3%)
Метаболические нарушения (снижение
уровня ГАМК, повышение фолатов)
Гипертермия (при наследственной
отягощенности судорожный порог ниже)
Воздействие вирусов и токсинов на ЦНС
28. ПЕРИНАТАЛЬНЫЕ ФАКТОРЫ РИСКА ФЕБРИЛЬНЫХ СУДОРОГ В % (Nelson, Ellenberg, 1990)
ПРИЕМ АЭП
0,4
МАТЕРЬЮ
8,1
КУРЕНИЕ
МАТЕРИ
3,7
ЗАБОЛЕВАНИЯ
0,7
МАТЕРИ
СУДОРОГИ У
ОТЦА
8,0
1,6
СУДОРОГИ У
МАТЕРИ
8,4
3,0
0
2
8,9
4
6
8
10
12
14
29. НЕОНАТАЛЬНЫЕ ФАКТОРЫ РИСКА ФЕБРИЛЬНЫХ СУДОРОГ (Nelson, Ellenberg, 1990)
ВРОЖД.НАР-Я
0,1
ОБМЕНА
25
СЕПСИС 0,3
Р-ВА ДЫХАНИЯ 0,3
СЛАБЫЙ КРИК 1,2
МАКРОЦЕФАЛИЯ 0,8
0
13,1
9,8
7,4
7,3
5
10
15
20
25
30
30. КЛИНИЧЕСКИЕ ПЕРСПЕКТИВЫ ФС
Рецидив – 33% переносят 2 припадка,
9% - 3 припадка
Риск повторения удваивается при
наличии ФС у родственников 1 порядка
Развитие эпилепсии – 4%
Фебрильно-провоцируемый дебют
эпилепсии (ДАЭ, РЭ, ДМЭМ, ФС+)
Частые и длительные ФС формироуют
склероз гиппокампа!
31. ПРОСТЫЕ ФС
Составляют 80-90% случаев ФС
Единичный, короткий (до 15 мин),
генерализованный тонико-клонический
припадок
Предшествующее развитие нормальное
Изменений на ЭЭГ нет
Прогноз хороший
32. СЛОЖНЫЕ ФС
Встречаются реже (10-20%)
Длительность приступов может быть более
15-20 мин
Могут быть повторными в течение суток
Припадки могут быть парциальными
(гемиконвульсивными)
Может наблюдаться постприпадочный парез
Тодда или стойкие неврологические
нарушения
На ЭЭГ могут наблюдаться изменения
Риск трансформации в эпилепсию высокий
33. ФАКТОРЫ РИСКА ПОВТОРНЫХ ФС (Berg et al., 1992; Knudsen, 1996)
Дебют до 15 мес
Наличие ФС у родственников 1-й степени родства
Сложный характер первого эпизода ФС
Риск повторных ФС при отсутствии данных факторов
– 10%, при наличии 1 фактора 25%, при наличии 2
факторов 50%, при наличии 3 факторов 90-98%
РИСК ТРАНСФОРМАЦИИ ФС В ЭПИЛЕПСИЮ 2-10%
ФАКТОР
РИСК РАЗВИТИЯ
ЭПИЛЕПСИИ
НИЗКИЙ
РИСК РАЗВИТИЯ
ЭПИЛЕПСИИ
ВЫСОКИЙ
ВОЗРАСТ ДЕБЮТА ФС
1-5 ЛЕТ
ДО 1 ГОДА ИЛИ
СТАРШЕ 5 ЛЕТ
ДЛИТЕЛЬНОСТЬ ПРИСТУПОВ БОЛЕЕ
20 МИН
-
+
ПАРЦИАЛЬНЫЙ ХАРАКТЕР
ПРИСТУПОВ
-
+
ПОСТПРИПАДОЧНЫЕ СИМПТОМЫ
ВЫПАДЕНИЯ
-
+
ПОВТОРНЫЕ ПРИСТУПЫ НА
ПРОТЯЖЕНИИ ОДНОГО ЗАБОЛЕВАНИЯ
-
+
НЕВРОЛОГИЧЕСКИЕ НАРУШЕНИЯ ДО
РАЗВИТИЯ ФС
-
+
СЕМЕЙНЫЙ АНАМНЕЗ ЭПИЛЕПСИИ
-
+
+
СОХРАНЕНИЕ ИЗМЕНЕНИЙ НА ЭЭГ
БОЛЕЕ 7 ДНЕЙ
35. ФЕБРИЛЬНЫЙ ЭПИЛЕПТИЧЕСКИЙ СТАТУС
25% среди ЭС детского возраста
4% среди всех ФС
Длительность припадков более 30 мин
Наиболее часто – у девочек раннего возраста
при семейной отягощенности по ФС
Летальный исход – редко
Высок риск развития эпилепсии в
дальнейшем – 21%
36. ИЗМЕНЕНИЯ ЭЭГ У ПАЦИЕНТОВ С ФС
Изменения ЭЭГ неспецифичны (норма,
неспецифические изменения, пароксизмальные
изменения)
Пароксизмальные нарушения – чаше при сложных
ФС (фокальных, продолжительных – более 15 мин)
Частота пароксизмальных нарушения нарастает с
числом эпизодов ФС
Частота пароксизмальных нарушений нарастает с
возрастом
37. ИЗМЕНЕНИЯ ЭЭГ У ДЕТЕЙ С ФС (Sofijanov et al., 1992)
38. ЗАВИСИМОСТЬ ПАРОКСИЗМАЛЬНЫХ ИЗМЕНЕНИЙ ЭЭГ ОТ КОЛИЧЕСТВА ЭПИЗОДОВ ФС (Sofijanov et al., 1992)
39. ОБСЛЕДОВАНИЕ ДЕТЕЙ, ПЕРЕНЕСШИХ ФС
ЭЭГ (региональное или асимметричное замедление
БЭА может указывать на фокальную природу
припадка)
Эхо-ЭГ
Осмотр глазного дна
КТ – по показаниями (парциальный характер
припадков)
Осмотр инфекциониста – по показаниям (для
исключения нейроинфекции)
Люмбальная пункция - по показаниям (сложные ФС,
нарушение сознания, вялость, менингеальные
симптомы)
Консультация генетика – по показаниям (наличие
диспластического статуса, семейной отягощенности
по ФС, подозрение на патологию обмена веществ)
40. ОСНОВНЫЕ ПОДХОДЫ К ТЕРАПИИ ФС
Длительное назначение АЭП
Назначение АЭП короткими курсами во
время лихорадки
Интенсивная терапия во время
приступа
41. ДЛИТЕЛЬНОЕ НАЗНАЧЕНИЕ АЭП ПО ПОВОДУ ФС
Проводится при частых и тяжелых ФС, а также детям
с органическим поражением ЦНС
Фенобарбитал 2-3 мг/кг/сут, после 1-го припадка 2-3
мес, после повторного – 1 год
Альтернативный вариант – вальпроаты
Карбамазепин, дифенин, гекасмедин неэффективны
42. НАЗНАЧЕНИЕ КОРОТКИХ КУРСОВ ТЕРАПИИ АЭП ПО ПОВОДУ ФС
Фенобарбитал 2-3 мг/кг/сут в 2-3 приема
Диазепам (седукен) 0,5мг/кг (в/м или
ректально)
Дегидратация
Жаропонижающие
43. ПОКАЗАНИЯ К ГОСПИТАЛИЗАЦИИ ПО ПОВОДУ ФС
Первый приступ до 6 мес и после 5 лет
Длительность приступа более 15 мин
Подозрение на заболевание ЦНС (опухоль,
гематома, энцефалит)
Тяжелое общее состояние, обусловленное
инфекцией
Повторные ФС на протяжении одного
лихорадочного периода
44. АМБУЛАТОРНОЕ НАБЛЮДЕНИЕ РЕБЕНКА, ПЕРЕНЕСШЕГО ФС
Осмотр педиатра – 1 раз в 2 дня в течение всего
лихорадочного периода
Осмотр невропатолога – после приступа, через 2-3
дня, через месяц, затем 2 раза в год
ЭЭГ – после приступа, затем через год
Эхо-ЭГ – 1-2 раза в год
Вопрос о вакцинации решается индивидуально
Снатие наблюдения – через 2 года после приступа,
при отсутствии эпилептических знаков на ЭЭГ и
прогредиентности неврологических симптомов
Читайте также:
