Показания для имплантации кардиовертера-дефибриллятора (ИКД)
Добавил пользователь Дмитрий К. Обновлено: 27.01.2026
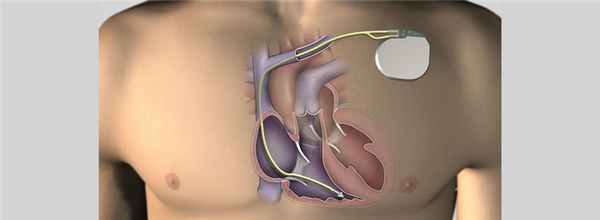
Имплантация кардиовертера-дефибриллятора (ИКД) — это высокотехнологичная малоинвазивная операция по устранению фатально угрожающих аритмий и предотвращения рисков остановки сердца. Кардиовертер-дефибриллятор представляет собой миниатюрный, непрерывно работающий сложный компьютер, имплантируемый в тело человека для контроля над его сердечной деятельностью. На сегодняшний день ИКД является единственной эффективной профилактической методикой при фатально угрожающих нарушениях ритма сердца (аритмиях).
При некоторых особенно опасных нарушениях ритма сердечных сокращений желудочки начинают сокращаться асинхронно, что ведет к остановке сердца и наступлению клинической смерти. Спасти человеку жизнь могут только экстренные реанимационные меры, принятые в течение первых минут. Установленный кардиовертер-дефибриллятор в этом случае распознает угрожающее состояние и исправляет нарушение ритма электроразрядом. По своей сути, ИКД — это экстренная помощь остановившемуся сердцу вне клиники.
Операция по имплантации прибора производится в условиях специально оборудованных рентгенохирургических операционных блоках эндоваскулярным доступом.
Преимущества ИКД в Центре хирургии «СМ-Клиника»
Многопрофильная помощь при лечении сердечно-сосудистых заболеваний по индивидуальным программам лечения, опытные врачи, в т.ч. экспертные специалисты по эндоваскулярной хирургии.
Инновационное оснащение операционных и диагностических кабинетов, высококачественные расходные материалы европейских производителей.
Малоинвазивные операционные методики, позволяющие в короткие сроки и с малой операционной травмой улучшить качество жизни пациента.
Показания к имплантации кардиовертера-дефибриллятора
- Эпизод остановки сердца вследствие желудочковой тахикардии (ЖТ) или фибрилляции желудочков (ФЖ), если он не был связан с временной или обратимой причиной.
- Внезапная остановка сердечной деятельности по причине сердечной патологии органического характера.
- Синкопе, причина которого не была установлена, если при электрофизиологическом исследовании сердца (ЭФИ) были выявлены значимые устойчивые ЖТ или ФЖ. При этом консервативная терапия должна быть признана неэффективной, не имеющей преимуществ или противопоказанной.
- ЖТ нестойкого характера, обусловленная коронарной патологией, перенесенным инфарктом миокарда, дисфункцией левого желудочка и некоторыми другими сердечно-сосудистыми нарушениями.
- Внезапная желудочковая тахикардия вне диагностированной органической болезни сердца, если применение других методов лечения невозможно.
Конечное решение о тактике лечения всегда принимает врач.
Подготовка к ИКД
Хирургическое вмешательство требует тщательного обследования пациента для минимизации рисков для его здоровья. В Центре хирургии предоперационное исследование включает:
- Лабораторную диагностику крови, включающую общие показатели, свертываемость, билирубин, наличие инфекций, группу и резус, Д-Димер и другие.
- Общий анализ мочи.
- Консультация сердечно-сосудистого хирурга.
- Электрокардиограмма.
- Рентгенография грудной клетки.
По индивидуальным показаниям могут потребоваться консультации у других узких специалистов и дополнительные аппаратные исследования.
Показания для имплантации кардиовертера-дефибриллятора (ИКД)


- НИО хирургии аорты, коронарных и периферических артерий
- НИО новых хирургических технологий
- НИО хирургической аритмологии
- НИО эндоваскулярной хирургии
- НИО сосудистой и гибридной хирургии
- НИО онкологии и радиотерапии
- НИО ангионеврологии и нейрохирургии
- НИО анестезиологии и реаниматологии
- НИО лучевой и инструментальной диагностики
- Состав совета по защите докторских и кандидатских диссертаций
- Требования к соискателям
- Соискатели
- Апелляции
- ГОСТ по оформлению диссертации и автореферата
- Контакты совета
- Генеральный директор Центра
- Руководство Центра
- Миссия
- История
- Мероприятия
- Фотопроекты
- Истории пациентов
- Нормативные документы
- Структура отдела
- Организационно-методическая работа с регионами
- Развитие телемедицинских технологий
- Кадровая политика и повышение квалификации
- Публичный отчет
- Устав и регистрационные документы
- Лицензии
- Публичный отчет
- Сведения о медицинских работниках
- План развития Центра
- Политика обработки персональных данных
- Охрана труда
- Политика в области охраны труда
- Противодействие коррупции
- Учетная политика
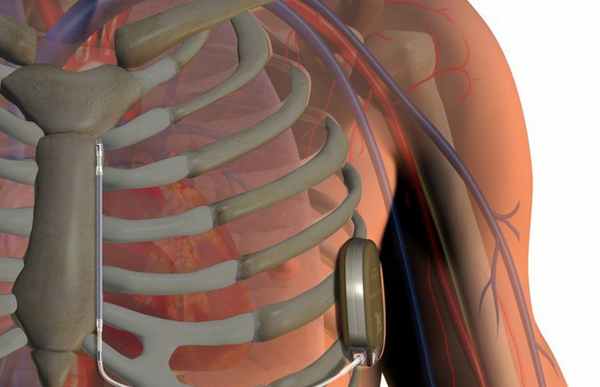
Имплантация прибора, предназначенного для устранения угрожающих жизни аритмий и предотвращения остановки сердца
Имплантируемый кардиовертер-дефибриллятор (ИКД) - прибор, предназначенный для устранения угрожающих жизни аритмий и предотвращения остановки сердца.
Имплантация прибора у взрослых проводится под местной анестезией, наркоз, как правило, применяется только у детей. Небольшой разрез делают под ключицей и через подключичную вену под рентген-контролем вводится электрод внутрь сердца. Наружный конец электрода соединяется с самим аппаратом, который погружается в подкожную жировую клетчатку в подключичной области. После чего разрез ушивают.
Через 1-2 дня после операции проводится программирование аппарата. Это безболезненная процедура, которая не требует повторного хирургического вмешательства.
Все ИКД нуждаются в замене. Частота замены зависит от типа устройства и скорости истощения батареи питания, на которую влияет частота возникновения опасных аритмий, потребность функционирования ИКД в качестве электрокардиостимулятора, дополнительные диагностические и лечебные функции, запрограммированные в ИКД.
Если опасная аритмия, требующая дефибриллирующих шоков, не возникает, аппарат может находиться в «ждущем» режиме в течение многих лет. ИКД заменяют, когда в нём еще достаточно энергии для устранения аритмий, которые могут возникнуть в период ожидания замены. Реимплантация ИКД обычно менее длительная процедура. Если электроды функционируют хорошо, их, не заменяя на новые, стыкуют с другим аппаратом.
Показания для имплантации кардиовертера-дефибриллятора (ИКД)
Эффективное лечение аритмии
Показания к имплантации ИКД
История применения ИКД в клинической практике насчитывает не более тридцати лет и сегодня эффективность современных устройств при ФЖ и ЖТ приближается к 100%.
В 1970 г. Michel Mirowski и Morton Mower, потрясенные внезапной смертью своего коллеги, предложили концепцию создания имплантируемого прибора, который мог бы автоматически проводить неотложную терапию в случае развития жизнеугрожающих желудочковых тахиаритмий. В 1980 г. Michel Mirowski осуществил первую в мире успешную операцию по имплантации кардиовертера-дефибриллятора молодой женщине с рецидивирующими эпизодами сердечного ареста вследствие фибрилляции желудочков. В последующем этот вид терапии стал одним из самых эффективных методов профилактики ВСС.
Современный ИКД представляет собой систему, состоящую из устройства, заключенного в небольшой титановый корпус и соединенных с ним одного или более электродов, расположенных в камерах сердца. ИКД имплантируется в левую или правую подключичную область под общей анестезией. В ходе операции после установки ИКД производится определение порога дефибрилляции. Аппарат содержит источник питания — литиево-серебрянно-ваннадиевую батарею, преобразователь напряжения, резисторы, конденсатор, микропроцессор и систему анализа сердечного ритма, высвобождения разряда, базу данных электрограмм аритмических событий. В клинической практике применяются желудочковые и предсердные электроды с пассивной и активной фиксацией для проведения кардиоверсии, дефибрилляции, антитахикардической, антибрадикардической электрокардиостимуляции. На сегодняшний день мы используем одно-, двух- камерные системы.
В основе детекции аритмий лежит анализ частоты собственного ритма, морфологии желудочкового сигнала, стабильность RR-интервала, соотношение характеристик предсердной и желудочковой активности (в двухкамерных системах). Указанные характеристики позволяют устройству дифференцировать желудочковые и наджелудочковые тахиаритмии.
В дефибрилляторах существуют так называемые зоны детекции быстрых и медленных ЖТ. В том случае, если частота аритмии попадает в первую зону, то происходит разряд дефибриллятора для купирования ФЖ или быстрой ЖТ. Во второй зоне возможно проведение различных видов антитахикардической желудочковой стимуляции для подавления аритмий. Параметры детекции и алгоритмы терапии для каждой зоны определяются в зависимости от характеристик ЖТ и устанавливатся с помощью программирующего устройства. При последующем наблюдении, в зависимости от клинической ситуации, проводимой медикаментозной терапии эти значения могут корригироваться.
Алгоритм терапии, осуществляемой устройством, устанавливается индивидуально, на основании переносимости больным клинической тахикардии. При гемодинамически незначимой, относительно медленной ЖТ могут быть эффективна антитахикардитическая стимуляция burst (стимуляция короткими пачками импульсов с частотой на 10-30% превышающей частоту тахикардии) или ramp (стимуляция импульсами с постепенно увеличивающейся частотой при которой каждый импульс укорачивает цикл стимуляции по сравнению с предыдущим), а при их неэффективности может быть использован режим кардиоверсии. При развитии ФЖ или быстрой ЖТ первым шагом в терапии сразу является дефибрилляция. При этом мощность разряда должна на 10 Дж превышать интраоперационный порог дефибрилляции с последующим пошаговым увеличением агрессивности терапии в виде нарастания мощности разряда до максимальных значений (30 Дж), а также изменением полярности в цепи дефибрилляции от корпуса ИКД к внутрисердечному электроду и наоборот.
Общий вид имплантируемого кардиовертера-дефибриллятора.
Общий вид имплантируемого кардиовертера-дефибриллятора.
Показания к имплантации ИКД.
Базируясь на результатов проведенных многоцентровых исследований, объединенная рабочая группа — Северо-Американское Общество Электрофизиологов/ Американский колледж Кардиологии/ Американская кардиологическая Ассоциация (NASPE/ACC/AHA) в 2002 году выработали показания к имплантации и рекомендации по клиническому ведению больных с кардиовертерами-дефибрилляторами. По-нашему мнению они являются приемлемыми и для Российской Федерации.
Класс I
1. Остановка сердца вследствие ЖТ/ФЖ, но не связанная с временной или обратимой причиной (уровень доказательств — А).
2. Спонтанная стойкая ЖТ, связанная с органическим заболеванием сердца (уровень доказательств — В).
3. Синкопе неустановленного происхождения в случаях, когда при ЭФИ индуцируются гемодинамически значимые стойкая ЖТ или ФЖ и лекарственная терапия неэффективна, непереносима или не имеет преимуществ (уровень доказательств — В).
4. Нестойкая ЖТ, обусловленная болезнью коронарных сосудов, перенесенным ИМ, дисфункцией левого желудочка и индуцируемой ФЖ или стойкой ЖТ при ЭФИ, которая не подавляется ААП I класса (уровень доказательств — А).
5. Спонтанная стойкая ЖТ у больных без органического заболевания сердца и которые не подлежат другим методам лечения (уровень доказательств — С).
Класс II а
Класс II b
1. Остановка сердца, вероятно, обусловленная ФЖ, но проведению электрофизиологического тестирования препятствуют другие медицинские обстоятельства (уровень доказательств — С).
2. Выраженные симптомы (например, синкопе), приписываемые стойким желудочковым тахиаритмиям у пациентов, ожидающих трансплантацию сердца (уровень доказательств — С).
3. Семейные или врожденные заболевания с высоким риском развития опасных для жизни желудочковых тахиаритмий, таких как синдром удлиненного интервала Q-T или гипертрофическая кардиомиопатия (уровень доказательств — В).
4. Нестойкая ЖТ у больных ИБС, перенесших ИМ, с дисфункцией левого желудочка, у которых при ЭФИ индуцируются стойкая ЖТ или ФЖ (уровень доказательств — В).
5. Повторные синкопальные состояния при наличии дисфункции левого желудочка и индуцируемой при ЭФИ желудочковой аритмии, когда другие причины синкопе исключены (уровень доказательств — С).
6. Синкопальные состояния неустановленной этиологии или необъяснимая внезапная сердечная смерть в семейном анамнезе в сочетании с типичной и атипичной БПНПГ и подъемом сегмента ST (синдром Бругада) (уровень доказательств — С).
7. Синкопальные состояния у больных с прогрессирующим сердечным заболеванием, у которых тщательное инвазивное и неинвазивное исследование не позволило выявить их причину (уровень доказательств — С).
Класс III
1. Синкопальные состояния неустановленного происхождения у больных без индуцируемой желудочковой тахиаритмий и без органического заболевания сердца (уровень доказательств — С).
2. Непрерывно рецидивирующие ЖТ или ФЖ (уровень доказательств — С).
3. ЖТ или ФЖ, обусловленные синдромом WPW, ЖТ с источником из выводного тракта правого желудочка, идиопатическая левожелудочковая тахикардия или фасцикулярная ЖТ, подлежащие хирургической или катетерной абляции (уровень доказательств — С).
4. ЖТ или ФЖ, связанные с временными или обратимыми расстройствами (например: ИМ, дисбаланс электролитов, действие лекарств, травма), когда коррекция нарушения считается осуществимой и, вероятно, значительно снизит риск рецидива аритмии (уровень доказательств — В).
5. Серьезные психические заболевания, которые могут обостряться при имплантации устройства или могут препятствовать проведению систематического катамнестического наблюдения (уровень доказательств — С).
6. Терминальное заболевание с предполагаемой продолжительностью жизни < 6 месяцев (уровень доказательств — С).
7. Больные ИБС с дисфункцией левого желудочка и широким комплексом QRS в отсутствие спонтанной или индуцируемой стойкой или нестойкой ЖТ, которым проводят операцию по шунтированию коронарных артерий (уровень доказательств — В).
8. ХСН IV ФК (NYHA), резистентная к лекарствам у больных, которые не являются кандидатами на пересадку сердца (уровень доказательств — С).
Имплантируемые кардиовертеры-дефибрилляторы (ИКД)
ИКД имплантируются подкожно или субпекторально, а введение электродов осуществляется трансвенозно в правый желудочек или иногда также в правое предсердие. Бивентрикулярная ИКД также имеет отведение в эпикард левого желудочка и имплантируется через коронарный синус венозной системы или с помощью торакотомии чтобы разрешить проведение ресинхронизирующей сердечной терапии Сердечная ресинхронизирующая терапия (СРТ) Необходимость в лечении аритмий зависит от симптомов и степени тяжести аритмии. Лечение направлено на причины заболевания. При необходимости проводится прямая антиаритмическая терапия, что включает. Прочитайте дополнительные сведения (РСТ) К ИКД относятся также полностью имплантированные подкожно ИКД, с электродами, расположенными не внутри сосудов, а непосредственно под кожей (П-ИКД), и портативные внешние дефибрилляторы для краткосрочного использования в виде электродного жилета.
ИКД-батарея в среднем рассчитана на 5–7 лет функционирования.
Показания для ИКД
Установка ИКД является предпочтительной для пациентов, у которых был
Эпизод ФЖ или гемодинамически значимая ЖТ, не связанные с обратимыми или транзиторными состояниями (например, электролитные нарушения, проаритмия на фоне антиаритмических препаратов, острый инфаркт миокарда)
ИКД также могут быть показаны пациентам с ЖТ или ФЖ, индуцированными во время пробы с физической нагрузкой, или пациентам с идио-патической ишемической кардиомиопатией Обзор кардиомиопатий (Overview of Cardiomyopathies) Кардиомиопатии – это первичные заболевания сердечной мышцы. Их надо отличать от структурных заболеваний сердца, таких как ишемическая болезнь сердца, патология клапанного аппарата, врожденные. Прочитайте дополнительные сведения и фракцией выброса ЛЖ < 35% и высоким риском развития ЖТ или ФЖ. Другие показания менее чёткие (см. таблицу Показания к имплантируемым кардиовертерам-дефибрилляторам [Indications for Implantable Cardioverter-Defibrillators] Показания для имплантации кардиовертеров- дефибрилляторов при желудочковых тахикардиях и фибрилляции желудочков ).
Такой подход позволяет продлить срок службы кардиовертера-дефибриллятора. Поскольку ИКД рекомендовано для лечения, а не для профилактики ЖТ и ФЖ, пациентам, склонным к этим аритмиям, может потребоваться прием антиаритмических препаратов Антиаритмические средства Необходимость в лечении аритмий зависит от симптомов и степени тяжести аритмии. Лечение направлено на причины заболевания. При необходимости проводится прямая антиаритмическая терапия, что включает. Прочитайте дополнительные сведения для уменьшения числа эпизодов аритмии и потребности в шоках.
ПОКАЗАНИЯ К ИМПЛАНТАЦИИ И ЭФФЕКТИВНОСТЬ ИСПОЛЬЗОВАНИЯ КАРДИОВЕРТЕРОВ-ДЕФИБРИЛЛЯТОРОВ У БОЛЬНЫХ С ДИЛАТАЦИОННОЙ КАРДИОМИОПАТИЕЙ
Ключевые слова
Об авторах
Первый Московский государственный медицинский университет имени И.М. Сеченова Министерства здравоохранения Российской Федерации (Сеченовский университет)
Россия
аспирант кафедры факультетской терапии № 1 лечебного факультета
119991, Российская Федерация, Москва, ул. Трубецкая, 8, стр. 2
Первый Московский государственный медицинский университет имени И.М. Сеченова Министерства здравоохранения Российской Федерации (Сеченовский университет)
Россия
д-р мед. наук, профессор кафедры факультетской терапии № 1 лечебного факультета
119991, Российская Федерация, Москва, ул. Трубецкая, 8, стр. 2
Первый Московский государственный медицинский университет имени И.М. Сеченова Министерства здравоохранения Российской Федерации (Сеченовский университет)
Россия
д-р мед. наук, профессор кафедры лучевой диагностики
119991, Российская Федерация, Москва, ул. Трубецкая, 8, стр. 2
Первый Московский государственный медицинский университет имени И.М. Сеченова Министерства здравоохранения Российской Федерации (Сеченовский университет)
Россия
д-р мед. наук, профессор кафедры патологической анатомии
119991, Российская Федерация, Москва, ул. Трубецкая, 8, стр. 2
д-р мед. наук, профессор, заведующая лабораторией медицинской генетики
119991, Российская Федерация, Москва, Абрикосовский пер., 2
Список литературы
1. Pasquale Losurdo, Davide Stolfo, Marco Merlo, Giulia Barbati, Marco Gobbo, Marta Gigli, et al. Early arrhythmic events in idiopathic dilated cardiomyopathy. JACC: Clinical Electrophysiology. 2016;2(5):535–543. DOI: 10.1016/j.jacep.2016.05.002.
2. Амосова Е.Н. Кардиомиопатии. Киев: Киев плюс; 1999:424
3. Беленков Ю.Н., Оганов Р.Г. Кардиология: нац. рук. М.: ГЭОТАР-Медиа; 2008:687
4. Благова О.В., Недоступ А.В., Коган Е.А., Седов В.П., Донников А.Е., Кадочникова В.В., и др. Дилатационная кардиомиопатия как клинический синдром: опыт нозологической диагностики с использованием биопсии и подходы к лечению. Терапевтический архив. 2011;83(9):41–48
5. Pinto Y.M., Elliott P.M., Arbustini E., Adler Y., Anastasakis A., Böhm M., et al. Proposal for a revised definition of dilated cardiomyopathy, hypokinetic non-dilated cardiomyopathy, and its implications for clinical practice: a position statement of the ESC working group on myocardial and pericardial diseases. Eur. Heart J. 2016 Jun. 14:37(23):1850–1858. DOI: 10.1093/eurheartj/ehv727.
6. Castelli G., Fornaro A., Ciaccheri M., Dolara A. Improving survival rates of patients with idiopathic dilated cardiomyopathy in Tuscany over 3 decades: impact of evidence-based management. Circ. Heart Fail. 2013;6(5):913–921. DOI: 10.1161/CIRCHEARTFAILURE.112.000120.
7. Morentin B., Audicana C. Population-based study of out-of-hospital sudden cardiovascular death: incidence and causes of death in middle-aged adults. Rev. Esp. Cardiol. 2011;64(1):28–34. DOI: 10.1016/j.recesp.2010.07.002.
8. Merlo M., Pivetta A., Pinamonti B. Long-term prognostic impact of therapeutic strategies in patients with idiopathic dilated cardiomyopathy: changing mortality over the last 30 years. Eur. J. Heart Fail. 2014;16(3):317–324. DOI: 10.1002/ejhf.16.
9. Elliott P., Charron P., Blanes J.R. European cardiomyopathy pilot registry: EURObservational research programme of the European Society of Cardiology. Eur. Heart J. 2016;37(2):164–173. DOI: 10.1093/eurheartj/ehv497.
10. Køber L., Thune J.J., Nielsen J.C. defibrillator implantation in patients with nonischemic systolic heart failure. N. Engl. J. Med. 2016;375(13):1221–1230. DOI: 10.1056/NEJMoa1608029.
11. Wolff G., Lin Y., Karathanos A. Implantable cardioverter/defibrillators for primary prevention in dilated cardiomyopathy post-DANISH: an updated meta-analysis and systematic review of randomized controlled trials. Clin. Res. Cardiol. 2017;106(7):501–513. DOI: 10.1007/s00392-017-1079-0.
12. Akel T., Lafferty J. Implantable cardioverter defibrillators for primary prevention in patients with nonischemic cardiomyopathy: A systematic review and meta-analysis. Cardiovasc. Ther. 2017;35(3):e12253. DOI: 10.1111/1755-5922.12253.
13. Cavalcanti R., Aboul-Hosn N., Morales G., Abdel-Latif A. Implantable cardioverter defibrillator for the primary prevention of sudden cardiac death in patients with nonischemic cardiomyopathy. Angiology. 2018;69(4):297–302. DOI: 10.1177/0003319717710851.
14. Schliamser J.E., Kadish A.H., Subacius H., Shalaby A., Schaechter A., Levine J., et al. Significance of follow-up left ventricular ejection fraction measurements in the Defibrillators in Non-Ischemic Cardiomyopathy Treatment Evaluation trial (DEFINITE). Heart Rhythm. 2013;10(6):838–846. DOI: 10.1016/j.hrthm.2013.02.017.
16. Goldberger J.J., Subačius H., Patel T. Sudden cardiac death risk stratification in patients with nonischemic dilated cardiomyopathy. J. Am. Coll. Cardiol. 2014;63(18):1879–1889. DOI: 10.1016/j.jacc.2013.12.021.
17. Grimm W., Timmesfeld N., Efimova E. Left ventricular function improvement after prophylactic implantable cardioverter-defibrillator implantation in patients with non-ischaemic dilated cardiomyopathy. Europace. 2013;15(11):1594–1600. DOI: 10.1093/europace/eut097.
18. Madhavan M., Waks J.W., Friedman P.A. Outcomes after implantable cardioverter-defibrillator generator replacement for primary prevention of sudden cardiac death. Circ. Arrhythm. Electrophysiol. 2016;9(3):e003283. DOI: 10.1161/CIRCEP.115.003283.
19. Arbustini E., Disertori M., Narula J. Primary prevention of sudden arrhythmic death in dilated cardiomyopathy: current guidelines and risk stratification. JACC Heart Fail. 2017;5(1):32–83. DOI: 10.1161/CIRCEP.115.003283.
20. Pavlicek V., Kindermann I., Wintrich J., Mahfoud F., Klingel K., Böhm M., et al. Ventricular arrhythmias and myocardial inflammation: Long-term follow-up of patients with suspected myocarditis. Int. J. Cardiol. 2019 Jan. 1;274:132–137. DOI: 10.1016/j.ijcard.2018.07.142.
21. Safak E., D’Ancona G., Schultheiss H.P., Kühl U., Kische S., Kaplan H., et al. Shocks after implantable cardioverter-defibrillator implantation in idiopathic cardiomyopathy patients: a myocardial biopsy study. Heart Vessels. 2018;33(2):205–211. DOI: 10.1007/s00380-017-1041-0.
22. Perazzolo Marra M., De Lazzari M., Zorzi A., Migliore F., Corrado D. Impact of the presence and amount of myocardial fibrosis by cardiac magnetic resonance on arrhythmic outcome and sudden cardiac death in nonischemic dilated cardiomyopathy. Heart Rhythm. 2014;11(5):856–863. DOI: 10.1016/j.hrthm.2014.01.014.
23. Halliday B., Gulati A., Ali A., Guha K., Newsome S., Arzanauskaite M., et al. Association between Midwall late gadolinium enhancement and sudden cardiac death in patients with dilated cardiomyopathy and mild and moderate left ventricular systolic dysfunction. Circulation. 2017;135(22):2106–2115. DOI: 10.1161/CIRCULATIONAHA.116.026910.
24. Di Marco A., Anguera I., Schmitt M. Late gadolinium enhancement and the risk for ventricular arrhythmias or sudden death in dilated cardiomyopathy: systematic review and meta-Analysis. JACC Heart Fail. 2017;5(1):28–38. DOI: 10.1016/j.jchf.2016.09.017.
Читайте также:
