Предраковые изменения шейки матки. Дисплазия шейки матки.
Добавил пользователь Валентин П. Обновлено: 29.01.2026
Предраковые заболевания шейки матки – ряд патологических состояний, которые при определенных условиях могут трансформироваться в рак шейки матки. К ним относятся дисплазия, лейкоплакия с атипией, эритроплакия, аденоматоз. У большинства женщин предраковые заболевания шейки матки протекают стерто; иногда могут сопровождаться водянистыми белями, контактными или межменструальными кровотечениями. Диагностируются на основании осмотра шейки матки в зеркалах, кольпоскопической картины, результатов онкоцитологии и биопсии, ВПЧ-типирования. В зависимости от характера и стадии предраковых изменений может осуществляться радиохирургическая, криогенная или лазерная деструкция патологического очага, конизация шейки матки или гистерэктомия.
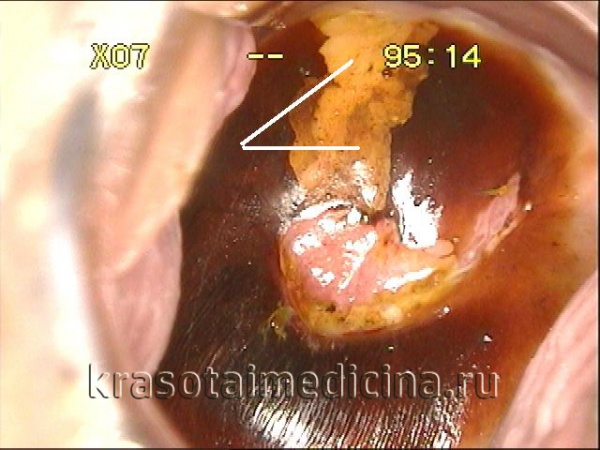
Общие сведения
Предраковые заболевание шейки матки – диспластические процессы в области влагалищной части шейки матки с высоким риском малигнизации. В гинекологии различают фоновые заболевания шейки матки (псевдоэрозия и истинная эрозия, полипы, простая лейкоплакия, эндометриоз, эктропион, папилломы, цервициты) и предраковые. Для фоновых патологий характерна нормоплазия эпителиальных клеток – их правильное деление, созревание, дифференцировка, отторжение.
Отличительной особенностью предраковых заболеваний шейки матки является то, что они протекают с дисплазией эпителия – его гиперпластической трансформацией, пролиферацией, нарушением дифференцировки, созревания и эксфолиации. Тем не менее, в отличие от рака шейки матки, все эти клеточные изменения ограничены пределами базальной мембраны. В большинстве случаев предраковые процессы развиваются в области фоновых заболеваний и нередко маскируются ими, что затрудняет своевременную диагностику. Средний возраст пациенток с предраком шейки матки составляет 30-35 лет.
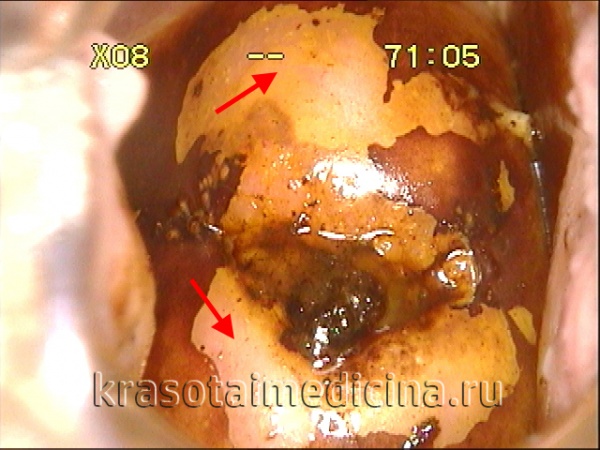
Причины предрака шейки матки
В настоящее время ключевой концепцией этиопатогенеза предраковых заболеваний шейки матки признана вирусная теория. Эпидемиологические исследования убедительно доказывают, что в развитии дисплазии ведущую роль играет папилломавирусная инфекция. В популяции женщин с тяжелой формой дисплазии шейки матки 85–95% являются ВПЧ-позитивными; у них, главным образом, обнаруживаются высокоонкогенные типы вируса — 16, 18 и 31. Попадая в организм при половых контактах, ВПЧ внедряется в клетки базального слоя эпителия. В инфицированной клетке вирус способен паразитировать в двух формах: доброкачественной, эписомальной и интрасомальной, стимулирующей опухолевый рост. Несмотря на то, что ВПЧ инфицирует базальные клетки, цитопатические эффекты возникают, в первую очередь, в клетках поверхностного слоя цервикального эпителия, где происходит вирусная репликация.
Возникновению предрака шейки матки способствует «содружество» ВПЧ, вируса простого герпеса II типа, хламидийной и цитомегаловирусной инфекций. Сочетание ВИЧ-инфекции и ВПЧ в разы повышает риск малигнизации. Важнейшим фактором, увеличивающим вероятность возникновения предраковых заболеваний шейки матки, является длительность персистенции вируса.
В меньшей степени, чем вирусные агенты, на риск развития фоновой и предраковой патологии шейки матки могут влиять и другие вероятные факторы риска. Так, ряд авторов ассоциирует цервикальную интраэпителиальную неоплазию (CIN) с курением. Доказано, что женщины, выкуривающие более 20 сигарет в день в течение 20 лет, имеют пятикратное повышение риска плоскоклеточной дисплазии. Содержащиеся в табачном дыме метаболиты проникают в цервикальную слизь и могут действовать и как самостоятельные канцерогены, и как факторы, активизирующие ВПЧ.
Установлена корреляция предраковых заболеваний шейки матки с длительным приемом эстроген-гестагенных оральных контрацептивов, особенно с повышенным гестагенным компонентом. Предраковыми заболеваниями шейки матки чаще страдают женщины, имеющие в анамнезе ранние роды, цервициты, травмы шейки матки при абортах и родах, нарушения гормональныго и иммунного гомеостаза. Среди других риск-факторов рассматриваются раннее (ранее 16 лет) начало половой жизни, частая смена половых партнеров, профессиональные вредности, отягощенный семейный анамнез по РШМ. Вместе с тем, ряд исследований показали, что длительный прием высоких доз витамина С и каротина может вызывать регресс интраэпителиальных цервикальных неоплазий.
Классификация цервикального предрака
Классификация предраковых заболеваний шейки матки претерпевала неоднократные пересмотры и уточнения. Одна из последних классификаций (1996 г.) выделяет доброкачественные фоновые изменения и собственно предрак. Согласно ей, к фоновым относятся дисгормональные (эктопия, эндометриоз, полипы), посттравматические (эктропион, рубцы, разрывы шейки матки), воспалительные (эрозия, цервицит) процессы.
Предраковые заболевания шейки матки, по данным кольпоцервикоскопического и гистологического исследования, делятся на несколько групп:
- Дисплазия (цервикальная интраэпителиальная неоплазия) - пролиферация атипического цервикального эпителия без изменения структуры стромального слоя и поверхностного эпителия. Включает в себя такие формы, как простая лейкоплакия, поля дисплазии, папиллярная и предопухолевая зона трансформации, предраковые полипы и кондиломы. Частота перерождения предрака шейки матки в рак колеблется в диапазоне 40-60%, зависит от вида патологии, ее локализации и длительности течения.
Различают легкую (CIN-I), умеренную (CIN-II) и тяжелую (CIN-III) дисплазию. При дисплазии легкой степени поражаются клетки глубоких - базального и парабазального – слоев (менее 1/3 толщины многослойного эпителия); атипичные клетки отсутствуют. Дисплазию умеренной степени характеризуют изменения 1/3-2/3 толщины эпителиального пласта; атипии не наблюдается. При тяжелой дисплазии на долю гиперплазированных клеток приходится более 2/3 толщи эпителиального слоя, встречаются клетки атипичной структуры.
- Лейкоплакия с атипией – морфологически характеризуется ороговением поверхностного эпителия, пролиферацией клеток базального слоя с явлениями атипизма, лимфоидной инфильтрацией подэпителиальной соединительной ткани. В 75% случаев дает начало инвазивному РШМ.
- Эритроплакия – предраковое заболевание шейки матки, протекающее с атрофией поверхностного и промежуточного слоем многослойного плоского эпителия; гиперплазией базального и парабазального слоев с наличием атипических клеток.
- Аденоматоз - атипическая гиперплазия желез эндоцервикса, напоминающая гиперплазию эндометрия. На фоне аденоматоза могут развиваться железистые формы рака.
Симптомы предраковых заболеваний шейки матки
Особенностью протекания предраковых заболеваний шейки матки является из бессимптомность или неспецифичность клинических проявлений. В основном данная группа патологий выявляется при проведении гинекологического осмотра и кольпоскопии с пробой Шиллера.
Дисплазия шейки матки не имеет самостоятельных симптомов. Лишь при присоединении вторичной инфекции может развиваться клиника вагинита или цервицита (бели, жжение, контактные кровянистые выделения). При изменениях, обусловленных гормональным дисбалансом, возможны нарушения менструльного цикла по типу мено- и метроррагий. Болевые ощущения отсутствуют.
Большинство женщин с лейкоплакией шейки матки считают себя практически здоровыми, лишь незначительная часть отмечает наличие обильных белей и контактных кровянистых выделений. Кольпоскопическая картина весьма патогномонична: участок лейкоплакии определяется в виде белесого перламутрового пятна. Дифференцировать простую и атипичную форму заболевания возможно только после гистологического изучения биоптата. Пациенток с эритроплакией могут беспокоить клейкие выделения желтоватого цвета. При кольпоскопии выявляются темно-красные участки с неровными границами, приподнятые над неизмененной слизистой.
Кондиломы шейки матки и аденоматозные полипы обнаруживаются, главным образом, при кольпоскопическом исследовании. При наличии в них вторичных изменений, вызванных изъязвлением, травматизацией и пр., возможно появление сукровичных выделений.
Диагностика предрака
Алгоритм диагностики предраковых заболеваний шейки матки разработан детально и включает в себя серию инструментальных и лабораторных исследований, позволяющих не только установить вид предрака, но и степень дисплазии.
При визуальном осмотре влагалищной порции шейки матки с помощью зеркал гинеколог оценивает форму наружного зева, окраску слизистой, характер секрета, видимые патологические процессы. В рамках гинекологического осмотра производится забор мазков с поверхности шейки матки для онкоцитологического исследования (ПАП-тест). При выявлении подозрительных участков шейки матки следующим этапом выполняется простая кольпоскопия, при необходимости – расширенное исследование с проведением медикаментозных проб (пробы Шиллера и др.). Каждой форме фоновых и предраковых заболеваний шейки матки соответствует своя кольпоскопическая картина, поэтому на данном этапе возможна дифференциальная диагностика патологий. Для выявления изменений эндоцервикса используется цервикоскопия.

Дальнейшая тактика обследования пациенток с подозрением на предраковые заболевания шейки матки предполагает осуществление прицельной биопсии шейки матки и выскабливания цервикального канала. На основании полученного гистологического заключения окончательно подтверждается или исключается предрак и определяется его форма. Дополнительная клинико-лабораторная диагностика может включать ПЦР исследование на ВПЧ с типированием, УЗИ малого таза, ОКТ шейки матки и др.
Лечение предраковых заболеваний шейки матки
Подход к лечению предраковых заболеваний шейки матки – дифференцированный и поэтапный. Целью терапии служит радикальное удаление патологически измененных тканей, устранение провоцирующих и сопутствующих факторов (лечение ВПЧ, иммунного и гормонального дисбаланса, воспалительных процессов). В соответствии с выявленными нарушениями назначается этиотропная противовоспалительная терапия (противовирусные, антибактериальные, иммуномодулирующие, интерферонстимулирующие, ферментные препараты). Проводится коррекция биоценоза влагалища, витаминотерапия, при необходимости – гормонотерапия.
Выбор способа хирургического лечения предраковых заболеваний шейки матки зависит от степени клеточной дисплазии. При CIN I-II, особенно у нерожавших пациенток, возможно щадящее физическое воздействие на патологические очаги: диатермокоагуляция, радиохирургическое лечение, лазерная вапоризация, криодеструкция. При CIN II-III показано радикальное хирургическое вмешательство в объеме эксцизии или конизации шейки матки, конусовидной ампутации или гистерэктомии (удаления матки). При полипах цервикального канала производится их удаление с РДВ.
После излечения предраковых заболеваний шейки матки контрольную кольпоцервикоскопию и онкоцитологию повторяют каждые 3 месяца на протяжении первого года и дважды в год в течение второго. Рецидивы редки, однако известно, что их процент выше у ВПЧ-инфицированных женщин. Профилактика предраковых заболеваний шейки матки предполагает широкий охват женского населения скрининговыми программами, вакцинацией против РШМ. Важную роль играет поведение самой женщины: использовании барьерной контрацепции при случайных контактах, отказ от курения, своевременное лечение фоновых заболеваний.
Дисплазия шейки матки
Под дисплазией шейки матки понимают атипические изменения эпителия в ее влагалищной части, относящиеся к предраковым процессам. На ранних стадиях своего развития дисплазия шейки матки является обратимым заболеванием, поэтому ее своевременное обнаружение и устранение является надежным способом профилактики онкологического риска. В отличие от эрозии, возникающей при механическом травмировании тканей, при дисплазии нарушения затрагивают клеточные структуры тканей, выстилающих шейку матки. Заболевание дисплазией шейки матки приходится, в основном, на возраст 25-35 лет и составляет 1,5 случая на 1000 женщин. Отсутствие явных клинических симптомов при дисплазии шейки матки на первый план в диагностике ставит инструментальные, клинические и лабораторные методики.
МКБ-10
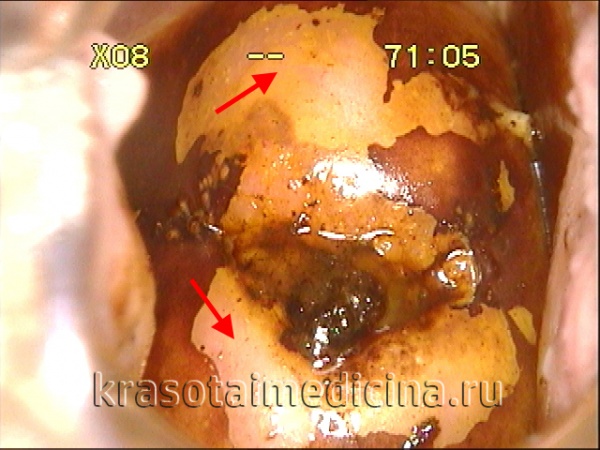
Под дисплазией шейки матки понимают атипические изменения эпителия в ее влагалищной части, относящиеся к предраковым процессам. На ранних стадиях своего развития дисплазия шейки матки является обратимым заболеванием, поэтому ее своевременное обнаружение и устранение является надежным способом профилактики онкологического риска.
В отличие от эрозии, возникающей при механическом травмировании тканей, при дисплазии нарушения затрагивают клеточные структуры тканей, выстилающих шейку матки. Заболевание дисплазией шейки матки приходится, в основном, на возраст 25-35 лет и составляет 1,5 случая на 1000 женщин. Для понимания, патологических процессов, происходящих при дисплазии шейки матки, необходимо составить представление об особенностях ее анатомо-физиологического строения.
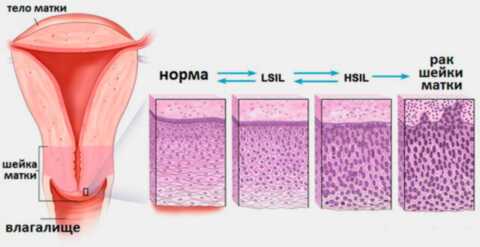
Виды дисплазии шейки матки
Нижний, узкий, цилиндрический отдел матки, частично расположенный в брюшной полости и частично вдающийся во влагалище (соответственно надвлагалищная и влагалищная часть), представляет собой шейку матки.
Влагалищную часть шейки матки обследуют при помощи влагалищных зеркал во время гинекологического осмотра. Внутри по шейке матки проходит узкий цервикальный (шеечный) канал длиной 1-1,5 см, один конец которого (наружный зев) открывается во влагалище, а другой (внутренний зев) – в полость матки, соединяя их.
Изнутри цервикальный канал выстлан слоем эпителиальных цилиндрических клеток и содержит шеечные железы, продуцирующие слизь. Слизистый секрет шеечного канала препятствует заносу микрофлоры из влагалища в матку. Эпителиальные цилиндрические клетки имеют ярко-красный цвет.
В зоне наружного маточного зева эпителиальные цилиндрические клетки шеечного канала переходят в многослойный плоский эпителий, покрывающий стенки влагалища, влагалищной части шейки матки и не имеющий желез. Плоский эпителий окрашен в бледно-розовый цвет и имеет многослойную структуру, состоящую из:
- базально-парабазального слоя - самого нижнего, глубокого слоя эпителия, образуемого базальными и парабазальными клетками. Базальный слой плоского эпителия граничит с нижерасположенными тканями (мышцами, сосудами, нервными окончаниями) и содержит молодые клетки, способные к размножению путем деления;
- промежуточного слоя;
- функционального (поверхностного) слоя.
В норме клетки базального слоя округлой формы, с одним крупным круглым ядром. Постепенно созревая и перемещаясь в промежуточный и поверхностный слои, форма базальных клеток уплощается, а ядро уменьшается в размере. Достигнув поверхностного слоя, клетки становятся уплощенными с очень маленьким ядром.
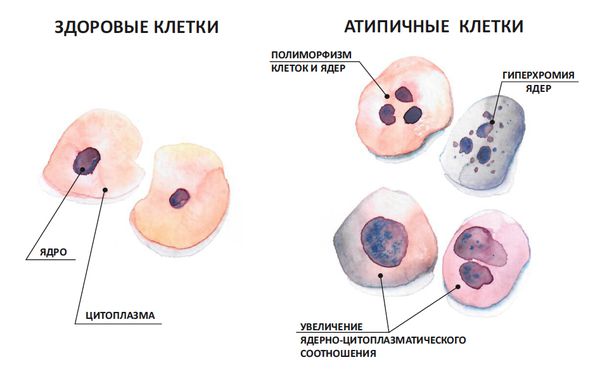
Дисплазия шейки матки характеризуется нарушениями в строении клеток и слоев плоского эпителия. Измененные эпителиальные клетки становятся атипичными – крупными, бесформенными, с множественными ядрами и исчезновением разделения эпителия на слои.
Дисплазия шейки матки может затрагивать различные слои клеток плоского эпителия. Выделяют 3 степени дисплазии шейки матки в зависимости от глубины патологического процесса. Чем больше слоев эпителия поражено, тем тяжелее степень дисплазии шейки матки. По международной классификации выделяют:
- Легкую дисплазию шейки матки (CIN I, дисплазия І) – изменения в строении клеток выражены слабо и затрагивают нижнюю треть многослойного плоского эпителия.
- Умеренную дисплазию шейки матки (CIN II, дисплазия ІІ) – изменения в строении клеток наблюдаются в нижней и средней трети толщи плоского эпителия.
- Тяжелую дисплазию шейки матки или неинвазивный рак (CIN III, дисплазия ІІІ) – патологические изменения встречаются во всей толще эпителиальных клеток, но не распространяются на сосуды, мышцы, нервные окончания, как при инвазивном раке шейки матки, затрагивающем эти структуры.
Причины дисплазии шейки матки
Наиболее часто развитие дисплазии шейки матки вызывают онкогенные типы вируса папилломы человека (ВПЧ-16 и ВПЧ-18). Эта причина выявляется у 95-98% пациенток с дисплазией шейки матки. При длительном нахождении в организме и клетках плоского эпителия (1-1,5 года), папилломавирусная инфекция вызывает изменения в строении клеток, т. е. дисплазию. Этому способствуют некоторые отягощающие фоновые факторы:
- иммунодефицит – подавление иммунной реактивности хроническими заболеваниями, стрессами, лекарственными препаратами, неправильным питанием и т. д.;
- табакокурение активное и пассивное – увеличивает вероятность развития дисплазии шейки матки в 4 раза;
- затяжные хронические воспаления половых органов;
- нарушения гормонального фона, вызванные менопаузой, беременностью, употреблением гормоносодержащих лекарств;
- ранняя половая жизнь и роды;
- травматические повреждения шейки матки.
Симптомы дисплазии шейки матки
Дисплазия шейки матки практически не дает самостоятельной клинической картины. Скрытое течение дисплазии наблюдается у 10% женщин. Гораздо чаще к дисплазии шейки матки присоединяется микробная инфекция, вызывающая патологические симптомы кольпита или цервицита: жжение или зуд, выделения из половых путей необычного цвета, консистенции или запаха, иногда с примесью крови (после использования тампонов, полового акта и т.д.). Болевые ощущения при дисплазии шейки матки практически всегда отсутствуют. Дисплазии шейки матки могут иметь длительное течение и самостоятельно регрессировать после соответствующего лечения воспалительных процессов. Однако, обычно процесс дисплазии шейки матки носит прогрессирующее течение.
Дисплазия шейки матки часто протекает вместе с такими заболеваниями, как остроконечные кондиломы влагалища, вульвы, заднего прохода, хламидиоз, гонорея.
Отсутствие явных клинических симптомов при дисплазии шейки матки на первый план в диагностике ставит инструментальные, клинические и лабораторные методики.
Диагностика дисплазии шейки матки
Схема диагностики дисплазии шейки матки состоит из:
- осмотра шейки матки при помощи влагалищных зеркал – с целью обнаружения видимых глазом, клинически выраженных форм дисплазии (изменение окраски слизистой, блеск вокруг наружного зева, пятна, разрастание эпителия и др.);
- кольпоскопии – осмотра шейки матки кольпоскопом – оптическим аппаратом, увеличивающим изображение более чем в 10 раз и одновременное проведение диагностических проб - обработки шейки матки раствором Люголя и уксусной кислоты;
- цитологического исследования ПАП-мазка – при дисплазии шейки матки исследование под микроскопом соскоба, полученного с разных участков, позволяет выявить атипичные клетки. Также с помощью ПАП-мазка обнаруживаются клетки-маркеры папилломавирусной инфекции, имеющие сморщенные ядра и ободок, являющиеся местом локализации вируса папилломы человека;
- гистологического исследования биоптата – фрагмента ткани, взятого в ходе биопсии шейки матки из зоны, подозрительной на дисплазию. Является наиболее информативным методом выявления дисплазии шейки матки;
- иммунологических ПЦР-методов – для выявления ВПЧ-инфекции, установления штаммов вируса и вирусной нагрузки (концентрации вируса папилломы в организме). Выявление наличия или отсутствия онкогенных типов ВПЧ позволяет определить выбор метода лечения и тактику ведения пациентки с дисплазией шейки матки.

Лечение дисплазии шейки матки
Выбор способа лечения дисплазии шейки матки определяется степенью дисплазии, возрастом женщины, размером зоны поражения, сопутствующими заболеваниями, намерениями пациентки сохранить детородную функцию. Ведущее место в лечении дисплазии шейки матки занимают:
- Иммуностимулирующая терапия (иммуномодуляторы, интерфероны и их индукторы) – показаны при обширных поражениях и течении дисплазии шейки матки, склонном к рецидивам.
- Методы хирургического вмешательства:
- деструкция (удаление) атипичного участка с помощью криотерапии (воздействия жидким азотом), электрокоагуляции, радиоволновой терапии, аргонового или углекислого лазера;
- оперативное удаление зоны дисплазии шейки матки (конизация) или всей шейки матки (ампутация).
При степени дисплазии І и ІІ, небольших размерах измененной зоны, молодом возрасте пациентки часто выбирается выжидательная тактика ввиду высокой вероятности самостоятельного регресса дисплазии шейки матки. Проведение повторных (каждые 3-4 месяца) цитологических исследований и получение двух положительных результатов, подтверждающих наличие дисплазии шейки матки, является показанием к решению вопроса о хирургическом лечении. Лечение дисплазии ІІІ проводят онкогинекологи, с использованием одного из хирургических способов (включая конусовидную ампутацию шейки матки).
Перед проведением любого из способов хирургического лечения дисплазии шейки матки назначается курс противовоспалительной терапии, направленной на санацию инфекционного очага. В результате этого нередко уменьшается степень дисплазии шейки матки или происходит ее полное устранение.
Реабилитация после лечения
После проведения хирургического лечения дисплазии шейки матки период реабилитации длится около 4 недель. В это время могут отмечаться:
- боли ноющего характера внизу живота на протяжении 3-5 дней (длительнее всего – после деструкции лазером);
- выделения из половых путей - обильные, иногда с запахом на протяжении 3-4 недель (длительнее всего - после проведения криодеструкции);
- обильное, длительное кровотечение из половых органов, интенсивные боли внизу живота, подъем температуры тела до 38 °С и выше – служат показаниями для немедленной медицинской консультации.
С целью скорейшего выздоровления, более быстрого заживления и предотвращения осложнений, необходимым является соблюдение полового покоя, исключение спринцеваний, подъема тяжестей, использования гигиенических тампонов и точное выполнение всех рекомендаций и назначений врача.
Наблюдение и профилактика дисплазии шейки матки
Первый контроль излеченности дисплазии шейки матки проводится спустя 3-4 месяца после хирургического лечения. Берутся цитологические мазки с последующими ежеквартальными повторами в течение года. Отрицательные результаты, показывающие отсутствие дисплазии шейки матки, позволяют в дальнейшем проводить обследование планово, при ежегодных диспансерных осмотрах.
Для профилактики дисплазии шейки матки и ее рецидивов рекомендуется:
- включение в рацион питания всех микроэлементов и витаминов, в особенности витаминов А, группы В, селена;
- своевременная санация всех очагов инфекций;
- отказ от табакокурения;
- применение барьерной контрацепции (при случайных половых контактах);
- регулярное наблюдение гинеколога (1-2 раза в год) с исследованием цитологического соскоба с шейки матки.
Перспективы лечения дисплазии шейки матки
Современная гинекология имеет эффективные методы диагностики и лечения дисплазии шейки матки, позволяющие избежать ее перерождения в рак. Раннее выявление дисплазии шейки матки, соответствующая диагностика и лечение, дальнейший регулярный врачебный контроль позволяют излечить практически любую стадию заболевания. После применения хирургических методик частота излеченности дисплазии шейки матки составляет 86-95%. Рецидивное течение дисплазии шейки матки наблюдается у 5-10% пациенток, перенесших хирургическое вмешательство, вследствие носительства папилломавируса человека или неполного иссечения патологического участка. При отсутствии лечения 30-50% дисплазий шейки матки перерождаются в инвазивный рак.
Предрак - симптомы и лечение
Что такое предрак? Причины возникновения, диагностику и методы лечения разберем в статье доктора Ефетова Сергея Константиновича, онколога со стажем в 14 лет.
Над статьей доктора Ефетова Сергея Константиновича работали литературный редактор Юлия Липовская , научный редактор Вячеслав Михайличенко и шеф-редактор Маргарита Тихонова

Определение болезни. Причины заболевания
Предрак (precancer) — это определённые изменения в клетках организма, которые увеличивают вероятность развития злокачественной опухоли.
Cинонимы: предопухолевое состояние, предраковое заболевание.
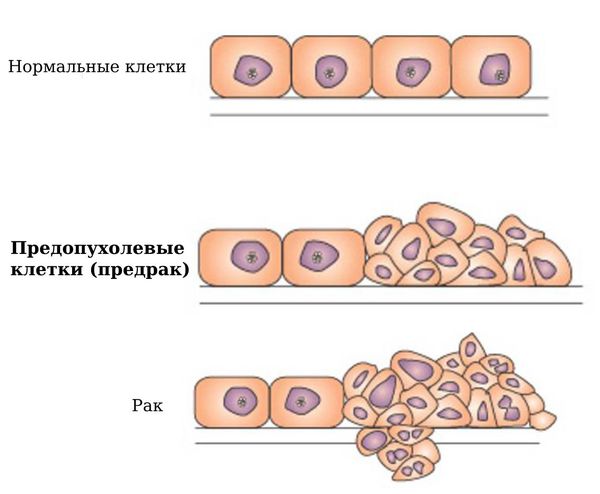
Предрак — это не онкологическое заболевание и не его начальная стадия. Предопухолевые клетки могут долго существовать без изменений, но при любом предраковом состоянии обязательно нужно лечиться или наблюдаться у врача, чтобы предотвратить развитие онкологического заболевания [1] [2] .
Чаще всего предраковые изменения появляются в клетках эпителия — слоя клеток, который выстилает поверхность (эпидермис) и полости тела, а также слизистые оболочки внутренних органов, желудочно-кишечного тракта, дыхательной системы и мочеполовых путей. Кроме этого, эпителий образует большинство желёз организма.
Какие состояния относят к предопухолевым
1. Заболевания желудочно-кишечного тракта:
- и эритроплакия полости рта. При лейкоплакии наблюдается повышенное ороговение слизистой оболочки рта, при эритроплакии слизистая оболочка истончается [3] .
- Пищевод Барретта. Это осложнение хронической гастроэзофагеальной рефлюксной болезни (ГЭРБ), при котором эпителий пищевода превращается в кишечный эпителий. Развивается примерно у 10 % пациентов с симптомами ГЭРБ. Появление таких атипичных клеток (отличных от нормальных) может привести к развитию рака пищевода[4] .
- . При этом заболевании изменяются и погибают клетки слизистой оболочки желудка, которые вырабатывают желудочный сок и соляную кислоту. В 80 % случаев атрофический гастрит вызван инфекцией Helicobacter pylori, в 5–10 % — реакцией иммунитета с отторжением клеток эпителия (аутоиммунный гастрит) [5][6] .
- Аутоиммунные воспалительные заболевания кишечника, например язвенный колит и болезнь Крона.
- Полипозы кишечника: спорадические, т. е. спонтанные, которые могут возникнуть у любого человека (одиночные, аденоматозные и ворсинчатые полипы толстой кишки), или наследственные, которые передаются от родителей и могут быть у других родственников (семейный аденоматозный полипоз, синдром Пейтца — Егерса ) [7][8][9][10] .
- Синдром Линча. Это н аследственное заболевание, которое приводит к развитию неполипозного рака толстой кишки [11] .
2. Заболевания дыхательной системы, например бронхиальная эпителиальная дисплазия (плоскоклеточная дисплазия, атипическая аденоматозная и диффузная идиопатическая нейроэндокринная гиперплазия). При этом состоянии изменяются клетки, которые выстилают поверхность бронхов. Бронхиальная эпителиальная дисплазия увеличивает вероятность развития рака лёгкого, чаще всего она возникает у курящих людей [12] [13] .
3. Заболевания кожи, например актинический (старческий, или солнечный) кератоз, кератоакантома, папилломатоз, диспластические невусы, пигментная ксеродерма [14] .
4. Заболевания половой системы:
Распределение предраковых состояний по полу и возрасту различны. Причины появления предраковых состояний тоже разнообразны, для каждого органа есть свои факторы риска и наиболее уязвимые группы людей.
Факторы риска
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы предрака
Предраковые состояния часто никак не проявляются или протекают с неспецифичными симптомами, т. е. такими, которые характерны одновременно для множества заболеваний, как доброкачественных, так и злокачественных. Кроме этого, симптомы зависят от органа, в котором появились изменённые клетки.
В полости рта:
- При лейкоплакии появляется налёт белого цвета, который сохраняется при чистке зубов, полоскании полости рта и после приёма пищи, при осмотре врач не может снять его шпателем. Термин «лейкоплакия» используется для тех образований, которые появляются в полости рта без очевидной причины.
![Белый налёт в полости рта при лейкоплакии [20, 21]](/pimg3/predrakovie-izmeneniya-sheyki-AEEABD.jpeg)
- Эритроплакия — б олее редкое и опасное состояние. Для него характерно появление красного пятна на слизистой оболочке. Поверхность такого пятна бархатистая, иногда с изъязвлениями. Если во рту появился белый налёт, покраснение или припухлость вокруг каймы губ, которые не проходят больше двух недель, нужно сразу обратиться к врачу-стоматологу [3] .
![Красное пятно в полости рта при эритроплакии [22]](/pimg3/predrakovie-izmeneniya-sheyki-E5CBAD.jpeg)
При пищеводе Барретта симптомы обычно такие же, как и при неосложнённой ГЭРБ. Может беспокоить изжога, тягостная, жгучая боль за грудиной, отрыжка, тошнота, кашель по утрам из-за попадания желудочного содержимого в глотку [4] .
При атрофическом гастрите часто ухудшается аппетит, появляется отрыжка тухлой пищей, тошнота и рвота, боли в животе, чувство тяжести после приёма пищи [6] .
Воспалительные заболевания кишечника, такие как язвенный колит и болезнь Крона, часто вызывают боль в животе и диарею, которая может чередоваться с запорами. Стул может быть с примесями крови и слизи, при осложнённом течении, например из-за присоединения инфекции, в кале появляется большое количество гноя, позывы на дефекация могут стать мучительными, схваткообразными и возникать несколько раз в день. Часто повышается температура, возникает слабость, боль в суставах, ухудшается аппетит, из-за этого снижается вес. Может беспокоить боль в правой подвздошной области, а при прощупывании живота иногда определяются объёмные образования — воспалительные инфильтраты (скопление в повреждённых тканях избытка жидкости и клеток крови) [18] . Однако такой набор жалоб или каждая жалоба в отдельности могут возникать и при других заболеваниях [9] .
При полипозах кишечника и синдроме Линча может не быть никаких жалоб, иногда появляются симптомы, характерные для многих заболеваний желудочно-кишечного тракта: боли в животе, вздутие, запоры или диарея. Также могут беспокоить вялость, слабость, головокружение и утомляемость, связанные с анемией из-за небольшой, но постоянной потери крови. Если после дефекации на туалетной бумаге или стенках унитаза появилась кровь, нужно как можно скорее обратиться к врачу. Он назначит исследование толстого кишечника — колоноскопию, чтобы выявить источник кровотечения [9] .
При дисплазии шейки матки обычно ничего не беспокоит, но иногда появляются маточные кровотечения, необычные кровянистые или другие выделения, нехарактерные для определённого периода менструального цикла, менопаузы или постменопаузы [15] .
Проявления предраковых состояний кожи также неспецифичны. Должны насторожить: любые подозрительные высыпания; незаживающие раны и изъязвления; родинки или пигментные пятна, которые изменили форму, цвет или размер; выделение жидкости на родинках. При появлении этих признаков нужно немедленно обратиться к врачу для обследования.
При актиническом кератозе появляются небольшие (менее 1 см в диаметре) желто-коричневые, красные или телесные образования с грубой, похожей на наждачную бумагу, поверхностью. Могут наблюдаться выросты, которые получили название «кожный рог». Чаще поражаются открытые участки кожи (лицо, руки, тыльная сторона кистей), иногда изменения появляются на губах (актинический хейлит) [14] .
![Образование на коже при актиническом кератозе [23]](/pimg3/predrakovie-izmeneniya-sheyki-CB542A.jpeg)
Патогенез предрака
Как выглядят нормальные эпителиальные клетки
Эпителиальные клетки тесно прилежат друг к другу и в один или несколько слоёв покрывают многие органы, отделяя их от внешней среды (эпителий кожи, полости носа, бронхов) или от внутренней (эпителий пищевода, желудка, кишечника). Есть несколько типов эпителиальных клеток, и они выполняют множество жизненно важных функций: эпителий кожи защищает организм от бактерий и загрязнений, эпителий органов ЖКТ позволяет усваиваться питательным веществам и жидкости [14] .
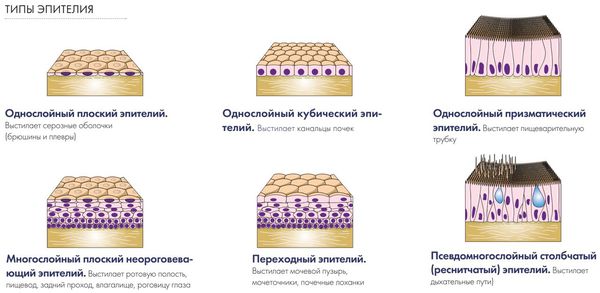
Почему появляются изменённые клетки
Эпителиальные клетки довольно быстро обновляются и делятся. Этот процесс регулируется генами, в них заложены своеобразные инструкции, которые помогают клетке правильно работать и делиться в необходимом количестве. Под воздействием различных факторов в генах может возникнуть поломка — мутация, ошибка в инструкции. Из-за этого строение эпителиальной клетки меняется, она перестаёт быть похожей на обычные, здоровые клетки организма, т. е. становится атипичной:
- клеточные ядра, отвечающие за жизнедеятельность и размножение клеток, увеличиваются;
- слои изменённых клеток лежат неровно, неупорядоченно, нарушается постепенный рост по направлению к поверхности эпителия.
Для этого процесса используют термин «дисплазия», что буквально означает нарушение роста [2] [8] [14] . Диспластические клетки не являются злокачественными, они не могут прорастать в окружающие органы и ткани и не распространяются по организму, но в них уже есть изменения.
Классификация и стадии развития предрака
Классификация предраковых заболеваний по частоте перехода в рак:
- Облигатные — рак возникает примерно в 80–95 % случаев. К ним относится семейный аденоматозный полипоз кишечника, синдром Линча, пигментная ксеродерма, актинический хейлит и др. Такие заболевания требуют не только тщательного наблюдения, но и лечения.
- Факультативные предраковые заболевания — рак развивается не более чем в 5–10 % случаев [1] . К ним относится пищевод Барретта, язвенный колит, актинический кератит, атрофический гастрит, атипическая протоковая гиперплазия, атипическая гиперплазия предстательной железы.
Чтобы определить степень дисплазии клеток, используется классификация GRADE. Она помогает предположить, как будет протекать заболевание, и определить тактику лечения. Для этого в ходе гистологического исследования ткани врач-патоморфолог определяет свойства клеток (например, число поделившихся клеток и разнообразие их формы), которые типичны для злокачественной опухоли, затем подсчитывает сумму баллов. Эта сумма сверяется со шкалой злокачественности опухоли. Например, для оценки рака предстательной железы используется шкала Глисона:
- 2–6 баллов по Глисону — низкая степень злокачественности. Клетки новообразования очень похожи на нормальные (их называют хорошо дифференцированными) и растут медленно.
- 7 баллов — промежуточная степень. Клетки не похожи на нормальные (умеренно дифференцированные) и растут быстрее, чем обычно.
- 8–10 баллов — высокая степень. Клетки сильно отличаются от нормальных (малодифференцированные или недифференцированные) и быстро растут .
Осложнения предрака
Осложнение предракового состояния — развитие онкологического заболевания. Несмотря на то, что предопухолевые клетки могут длительно существовать без изменений, при любом предраке обязательно нужно регулярно проходить обследования или лечиться с последующим наблюдением. Это поможет предотвратить развитие онкозаболевания [19] .
Врач может заподозрить предопухолевое состояние, тщательно расспросив пациента об истории его жизни и болезни. Доктор может спросить:
- Были ли случаи онкологических заболеваний в семье.
- Какие есть хронические заболевания.
- Проходит ли пациент скрининговые обследования, которые рекомендованы по возрасту. Скрининговыми называют исследования, помогающие выявить болезни, когда они ещё не вызывают симптомов.
Чтобы выявить предраковые состояния желудочно-кишечного тракта (пищевод Барретта, атрофический гастрит, аденоматозный полипоз желудка), проводится гастроскопия [4] [5] .
При подозрении на воспалительные заболевания кишечника (язвенный колит и болезнь Крона), полипозы кишечника или синдром Линча необходима колоноскопия.
При подозрении на бронхиальную эпителиальную дисплазию проводится бронхоскопия.
Чтобы обнаружить изменённые клетки шейки матки, используется ПАП-тест. Это скрининговое исследование мазка с шейки матки, окрашенного по Папаниколау. Его нужно делать всем женщинам 25–65 лет каждые три года. Чтобы уточнить диагноз, проводится кольпоскопия — визуальное исследование шейки матки с помощью специального увеличительного прибора.
![ПАП-тест [24]](/pimg3/predrakovie-izmeneniya-sheyki-293C3.jpeg)
Однако точно поставить диагноз предрака или самого онкологического заболевания можно только после гистологического исследования врачом-патоморфологом. Для этого в ходе биопсии берут кусочек изменённой ткани.
Как проводят биопсию
В зависимости от органа, в котором находятся изменённые клетки, биопсию выполняют по-разному. Чтобы взять образец кожи и слизистых оболочек полости рта, требуется небольшая операция под местной анестезией.
Образец ткани некоторых внутренних органов можно взять только при эндоскопическом исследовании: гастроскопии, колоноскопии, бронхоскопии или кольпоскопии.
Когда образец получен, врач внимательно изучает строение кусочка ткани под микроскопом. Никакие другие методы не позволяют точно определить предрак или онкологическое заболевание. Именно результат гистологического исследования, т. е. заключение врача-патоморфолога, определяет план ведения и лечения пациента.
Лечение предрака
Лечение каждого случая предрака прежде всего зависит от степени дисплазии (изменения клеток) и от того, в каком органе есть предопухолевые изменения [15] . Например, при атрофическом гастрите, который вызван инфекцией Helicobacter pylori, проводится антибактериальная терапия. При актиническом кератозе — операция по удалению изменённого участка кожи. При воспалительных заболеваниях кишечника, синдроме Линча, семейном аденоматозном полипозе может потребоваться профилактическая операция, которая существенно снижает риск возникновения колоректального рака.
Тактику лечения определяет команда специалистов, в которую входят онкологи, хирурги и другие врачи, занимающиеся лечением заболеваний конкретного органа: маммологи, дерматологи, гинекологи, колопроктологи и др.
Прогноз. Профилактика
Дисплазия не всегда превращается в злокачественную опухоль. Умеренная дисплазия затрагивает не все слои эпителия и может быть обратимой, если устранить причину повреждения клеток [8] . Однако вероятность рака при дисплазии увеличивается по сравнению с обычными клетками.
Прогноз некоторых предраковых состояний выглядит следующим образом:
- Большинство аденокарцином пищевода связано с пищеводом Барретта, но развивается эта злокачественная опухоль не очень часто: при низкой степени дисплазии — у 0,5 % больных в год, при дисплазии высокой степени — у 6 % пациентов в год [25] .
- У пациентов с синдромом Линча вероятность заболеть колоректальным раком составляет 70–80 %.
- При семейном аденоматозном полипозе, для которого характерны множественные полипы в толстой кишке, к 40 годам может развиться карцинома [17] .
В то же время современные методы наблюдения и лечения пациентов с предраковыми заболеваниями существенно снижают риск развития онкологического заболевания или позволяют выявить его на ранней стадии, что значительно улучшает прогноз.
Профилактика предрака
- Проводить самообследование: еженедельно осматривать кожу после гигиенических процедур, осматривать полость рта, женщинам обследовать молочные железы через 7–10 дней после окончания каждой менструации.
- Посещать стоматолога не реже, чем раз в полгода, для осмотра полости рта.
- Проходить диспансеризацию и ежегодный осмотр у терапевта.
- Меньше бывать на солнце, отказаться от посещения солярия, использовать солнцезащитный крем.
- Отказаться от курения и жевательного табака.
- Лечить хеликобактерную инфекцию и вакцинироваться от ВПЧ, это снизит риск развития рака желудка и шейки матки.
Также необходимо делать скрининговые обследования, показанные в определённом возрасте:
Дисплазия шейки матки - симптомы и лечение
Что такое дисплазия шейки матки? Причины возникновения, диагностику и методы лечения разберем в статье доктора Игнатенко Татьяны Алексеевны, гинеколога со стажем в 14 лет.
Над статьей доктора Игнатенко Татьяны Алексеевны работали литературный редактор Елена Бережная , научный редактор Сергей Федосов
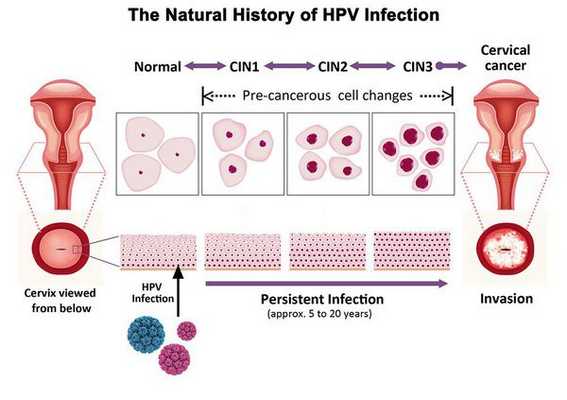
Дисплазия шейки матки, или цервикальная интраэпителиальная неоплазия (ЦИН), или Cervical Intraepithelial neoplasia (CIN) — это патологический процесс, при котором в толще клеток, покрывающих шейку матки, появляются клетки с различной степенью атипии (неправильного строения, размера, формы).
Причины дисплазии шейки матки
Папилломавирусная инфекция (ВПЧ) — основная причина дисплазии и рака шейки матки. К болезни приводит длительное персистирование именно ВПЧ высокого канцерогенного риска. У женщин с риском развития цервикальной неоплазии распространенность онкогенных типов ВПЧ чрезвычайно велика. ВПЧ становится причиной CIN 2-3 и рака шейки матки в 91,8% и 94,5% случаев соответственно. [1]
К факторам риска дисплазии шейки матки относится длительный приём контрацептивов и курение. Выявлена связь между пассивным курением среди некурящих и повышенным риском возникновения CIN 1. [3]
Другие факторы риска — раннее начало половой жизни, большое число и частая смена половых партнеров, употребление алкоголя, сопутствующие половые инфекции, много беременностей и родов. Риск цервикальной CIN 2 особенно высок у женщин, которые до этого имели опыт пересадки органов, у них выявлена ВИЧ-инфекция или они принимают иммунодепрессанты. [2]
Дисплазия шейки матки, как правило, имеет бессимптомное течение, поэтому пациентки не предъявляют никаких специфических жалоб.
Патогенез дисплазии шейки матки
Критический фактор развития цервикальной интраэпителиальной неоплазии — инфицирование вирусом папилломы человека. Во многих случаях цервикальная интраэпителиальная неоплазия легкой степени отражает временную реакцию организма на папиломавирусную инфекцию и без лечения исчезает в течение полугода-года наблюдения. При цервикальной интраэпителиальной неоплазии умеренной и тяжелой степени высока вероятность встраивания вируса папилломы человека в клеточный геном. Инфицированные клетки начинают продуцировать вирусные белки E6 и Е7, которые продлевают жизнь клетки, сохраняя ее способность к неограниченному делению. Неизбежно формирующиеся на этом фоне мутации клеток ведут к формированию предрака (дисплазии) и рака шейки матки, влагалища и вульвы.
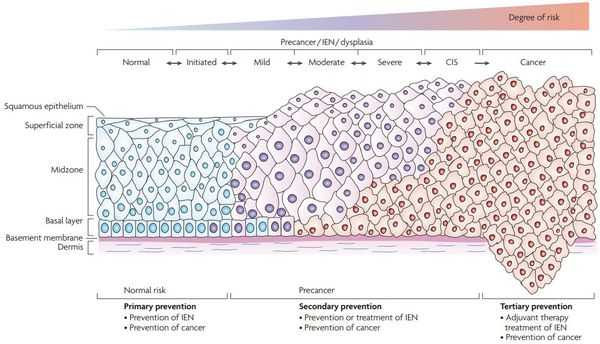
Онкогенные белки ВПЧ (Е6, Е7) взаимодействуют с регуляторными белками клеток шейки матки, приводя к повышению активности онкомаркера p16INK4A, что свидетельствует о неконтролируемом размножении клеток шейки матки. Таким образом, сверхэкспрессия p16INK4A, определяемая в материале шейки матки, который получают при биопсии, является биомаркером интеграции вируса папилломы человека высокого риска в геном и трансформации эпителиальных клеток под действием вируса, что делает эту информацию полезной при оценке прогноза развития предраковых и злокачественных поражений, связанных с инфицированием генитального тракта вирусом папилломы человека. [5]
Классификация и стадии развития дисплазии шейки матки
Для постановки цитологического диагноза (по результатам цитологического исследования соскобов шейки матки и цервикального канала с окрашиванием по Папаниколау (Рар-тест) или жидкостной цитологии) используется классификация Бетесда (The Bethesda System, 2014), основанная на термине SIL (Squamous Intraepithelial Lesion) – плоскоклеточное интраэпителиальное поражение. [10]
Выделяют три вида результатов соскобов с поверхности шейки матки (экзоцервикса):
- нормальные мазки, без изменений клеток шейки матки (NILM, Negative for intraepithelial lesion or malignancy);
- «непонятные» мазки без определенного значения, по которым нельзя определить характер поражения, однако они при этом не являются нормой (ASC-US, Atypical Squamous Cells of Undetermined Significance) или, что хуже, ASC-H, Atypical squamous cells cannot exclude HSIL, обнаружение атипичных клеток плоского эпителия, не исключающее SIL высокой степени);
- предраки низкой (LSIL, Low Grade Squamous Intraepithelial Lesion) и высокой (HSIL, High Grade Squamous Intraepithelial Lesion) степени.
Классификация Папаниколау
- 1-й класс — нормальная цитологическая картина (отрицательный результат);
- 2-й класс — изменение морфологии клеток, которое обусловлено воспалением во влагалище и (или) шейке матки;
- 3-й класс — единичные клетки с аномалией ядер и цитоплазмы (подозрение на злокачественное новообразование);
- 4-й класс — отдельные клетки с явными признаками озлокачествления;
- 5-й класс — много типично раковых клеток (злокачественное новообразование).
Существуют также гистологические классификации для оценки материала, полученного при биопсии.
По классификации R. M. Richart (1968) в зависимости от глубины поражения поверхностного клеточного слоя выделяют три степени дисплазии шейки матки:
- ЦИН 1 (дисплазия слабой степени) — признаки папилломавирусной инфекции (койлоцитоз и дискератоз). Поражение до 1/3 толщины клеточного пласта;
- ЦИН 2 (дисплазия средней степени) — поражена 1/2 толщины клеточного слоя;
- ЦИН 3 (дисплазия тяжелой степени) — поражение более 2/3 клеточного слоя. [8]
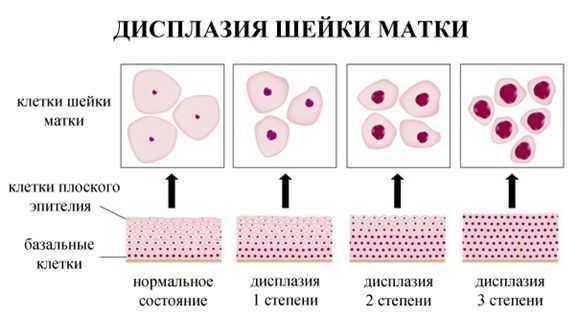
В приведенной ниже таблице даны соотношения классификаций предраковых поражений шейки матки. [9]
| Система Папаниколау | Описательная система ВОЗ | CIN | Терминологи- ческая система Бетесда (ТСБ) |
|---|---|---|---|
| Класс 1 (норма) | Отсутствие злокачественных клеток | Отсутствие неопластических изменений | Норма |
| Класс 2 (метаплазия эпителия, воспалительный тип) | Атипия, связанная с воспалением | Реактивные изменения клеток ASC: ASC - US, ASC - H | |
| Класс 3 ("дискариоз") | Слабая дисплазия | CIN 1 койлоцитоз | LSIL |
| Умеренная дисплазия | CIN 2 | HSIL | |
| Тяжелая дисплазия | CIN 3 | ||
| Класс 4 (клетки, подозрительные на рак или карцинома in situ | Карцинома in situ | ||
| Класс 5 (рак) | Инвазивная карцинома | Карцинома | Карцинома |
Осложнения дисплазии шейки матки
Последствия дисплазии шейки матки
Основное и самое опасное осложнение цервикальной интраэпителиальной неоплазии заключается в развитии рака шейки матки, любой случай развития которого — результат упущенных возможностей диагностики и лечения дисплазии шейки матки. [7]
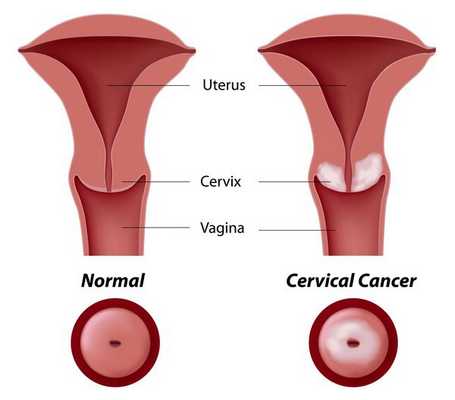
Проводились длительные, систематические исследования риска рака шейки матки у женщин с диагнозом цервикальной интраэпителиальной неоплазии 3 степени (CIN3) по сравнению с женщинами, у которых были нормальные цитологические результаты. Согласно полученным данным, долгосрочный относительный риск развития рака шейки матки зависит от различных гистологических типов CIN3 и выше всего он для аденокарциномы in situ. Даже через 25 и более лет после конизации (хирургического иссечения патологических тканей шейки матки) риск злокачественного перерождения клеток был значительным. [4]
Для ранней диагностики предраковых поражений шейки матки во многих странах мира существует система цервикального скрининга.
Методы диагностики дисплазии шейки матки
В России система цервикального скрининга включает последовательность действий:
- Цитологическое исследование: РАР-тест;
- ВПЧ-тестирование: в США и странах Евросоюза ВПЧ-тест применяется для первичного скрининга рака шейки матки (РШМ). В России его использование вариативно: при первичном скрининге в сочетании с РАР-тестом, в качестве самостоятельного теста, при ведении пациенток с неясными результатами РАР-теста (ASCUS) и для наблюдения паценток после лечения HSIL;
- Кольпоскопия: показаниями к исследованию являются положительные результаты РАР-теста (класс 2-5). Метод основан на осмотре шейки матки при помощи увеличивающих оптических систем и проведения диагностических проб с растворами уксусной кислоты и йода (Люголя). С помощью кольпоскопии определяют локализацию поражения, его размер, выбирают участок для проведения биопсии, определяют тактику лечения.
При кольпоскопии должна быть тщательно оценена зона трансформации (переходная зона стыка двух видов покровного эпителия шейки матки).
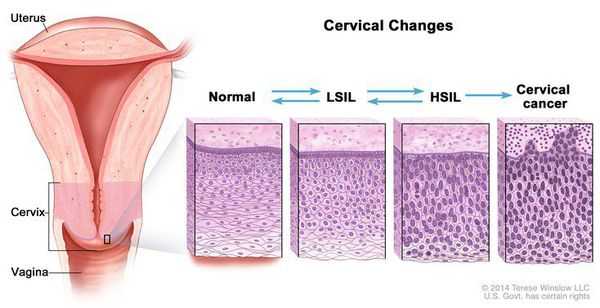
Влагалищная часть шейки матки (экзоцервикс) покрыта многослойным плоским эпителием. В канале шейки матки (цервикальном канале, эндоцервиксе) — цилиндрический эпителий. Место перехода цилиндрического эпителия цервикального канала в многослойный плоский эпителий поверхности шейки матки носит название зоны трансформации. Эта область имеет большое клиническое значение, поскольку именно в ней возникает более 80% случаев дисплазии и рака шейки матки.
- Зона трансформации 1 типа — переходная зона видна полностью. Это самый оптимальный и прогностически «благоприятный» вариант кольпоскопического заключения.
- Зона трансформации 2 типа — переходная зона частично скрыта в канале шейки матки. Адекватно оценить такую картину сложно, так как наиболее измененные участки могут быть не видны и пропущены.
- Зона трансформации 3 типа — переходная зона находится глубоко в канале шейки матки и оценить её кольпоскопически невозможно. Кольпоскопия в этом случае считается неинформативной, поскольку глубина залегания патологического очага остается неизвестной.
- Биопсия: прицельная или расширенная биопсия (конизация) всегда должна выполняться под контролем кольпоскопии. Выбор метода биопсии зависит от типа поражения, возраста пациентки и зоны трансформации. Важной информацией, которую дает биопсия, является возможность иммуногистохимического определения маркера ранней диагностики дисплазии с высокой степенью риска озлокачествления: p16INK4a.
Динамическому наблюдению подлежат молодые пациентки (до 35 лет) с LSIL (ВПЧ, ЦИН 1, ЦИН 2, если при биопсии не обнаружен белок р16, являющийся признаком проникновения ВПЧ высокого риска в геном и трансформации опухолевых клеток под действием вируса). Наблюдать возможно пациенток только с 1 и 2 кольпоскопическим типом зоны трансформации.
Контрольные осмотры, цитологическое и ВПЧ-тестирование показаны через 6 и 12 месяцев после первичного обнаружения патологии.
Хирургическое лечение дисплазии
При выявлении HSIL (ЦИН 2 c обнаружением белка р16 при биопсии, ЦИН 3) неизбежно хирургическое лечение в виде абляции («прижигания») или эксцизии (удаления) поврежденной ткани. Для абляции используют электро-/радио-, крио- и лазерные воздействия. Эксцизия возможна электро-/радиоволновая или ножевая.
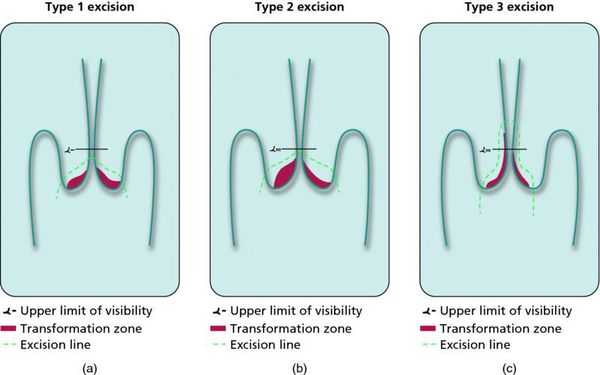
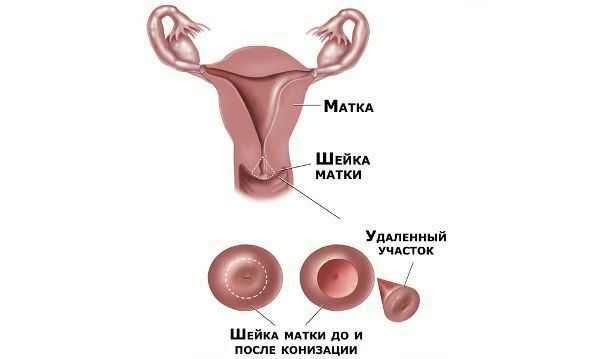
Немаловажно, что при выявлении по кольпоскопии 3 типа зоны трансформации на фоне положительного РАР-теста гинеколог обязан провести выскабливание слизистой канала шейки матки и/или широкую эксцизионную биопсию (конизацию шейки матки) для исключения опухолевого процесса, потенциально располагающегося вне зоны кольпоскопического обзора. Немаловажно наблюдение после операции через 6 и 12 месяцев с выполнением цитологического соскоба и ВПЧ-теста.
Следует отметить, что процедура хирургического иссечения патологических тканей на шейке матки увеличивает риск преждевременных родов. А сама по себе цервикальная интраэпителиальная неоплазия первой степени на течении беременности и родов никак не отражается и зачастую опасности не представляет. [12]
Средний возраст женщин, когда может потребоваться хирургическая коррекция цервикальной внутриэпителиальной неоплазии — около 30 лет. Хирургическое лечение нередко ассоциировано с неблагоприятным течением последующей беременности. Частота и тяжесть неблагоприятных осложнений возрастают с увеличением глубины иссекаемых тканей. [13]
Реабилитация после хирургического лечения
В течение месяца после операции следует воздержаться от спринцеваний, половых контактов и не пользоваться тампонами. На 2–3 недели исключают тяжёлые физические нагрузки и тепловые процедуры. Незначительные сукровичные выделения, усиливающиеся иногда до менструальноподобных, в течение 10–20 дней после операции — это нормальное явление.
При реабилитации после хирургического лечения шейки матки эффективны препараты, содержащие антисептик и стимулятор регенерации эпителия.
После лечения возможен рецидив, поэтому необходимо пожизненное наблюдение: цитологический мазок через 6 и 12 месяцев после операции, затем раз в год в течение 10 лет, далее раз в 3 года.
Планировать беременность после операции на шейке матки можно не ранее, чем через 3–6 месяцев. Эти сроки будут зависеть от глубины эксцизии или конизации и длины шейки матки [9] .
Лечение дисплазии при беременности
В большинстве случаев лечение должно быть отложено на послеродовый период. При беременности на фоне дисплазии шейки матки каждые три месяца проводится кольпоскопический и цитологический контроль. При выявлении рака шейки матки пациентку консультирует онкогинеколог. Доктор подбирает тактику лечения, может потребоваться прервать беременность по онкологическим показаниям [9] .
Дополнительными факторами риска прогрессирования ПВИ с формированием предраковой патологии являются:
- курение;
- длительное использование гормональных контрацептивов;
- многократные травматичные роды;
- ВИЧ-инфекция.
- У пациенток с ЦИН часто обнаруживают вирус простого герпеса 2 типа, цитомегаловирусную инфекцию, хламидийную урогенитальную инфекцию, бактериальный вагиноз, ассоциированный с резким снижением или отсутствием вагинальной лактофлоры, повышенным ростом во влагалище Gardnerella vaginalis и Atopobium vaginae, повышение концентрации в бакпосеве грибов рода Candida, Mycoplasma hominis.
Устранение и профилактика данных факторов способны снизить вероятность развития предраковой патологии шейки матки.
Рак шейки матки поражает преимущественно женщин репродуктивного возраста. Скрининг является важной стратегией вторичной профилактики. Длительный процесс канцерогенной трансформации от появления в организме вируса папилломы человека (ВПЧ) до инвазивного рака дает широкие возможности для выявления заболевания на стадии, когда лечение высокоэффективно. Подходящими скрининговыми тестами в мире признаны цитологическое исследование, визуальный осмотр после применения уксусной кислоты и тесты на выявление ВПЧ. Всемирная организация здравоохранения рекомендует проводить скрининг женщин по крайней мере один раз в жизни в возрасте от 30 до 49 лет. [14]
Согласно приказу Министерства здравоохранения РФ от 03.02.2015. N36ан "Об утверждении порядка проведения диспансеризации определенных групп взрослого населения", осмотр со взятием мазка (соскоба) с поверхности шейки матки и цервикального канала на цитологическое исследование производится 1 раза в 3 года для женщин в возрасте от 21 года до 69 лет включительно.
Читайте также:
