Рентгенография при трахеопищеводном свище.
Добавил пользователь Владимир З. Обновлено: 27.01.2026
Не уверены в правильности поставленного вам диагноза? Прочь сомнения! Приходите в «МедикСити» и бесплатно проконсультируйтесь у н.
Консультация проктолога - 50%!
По направлению врачей эндоскописта (после колоноскопии), гастроэнтеролога или гинеколога «МедикСити» консультация врача-прокт.
Скидки для друзей из социальных сетей!
Эта акция - для наших друзей в "Одноклассниках", "ВКонтакте", "Яндекс.Дзене", YouTube и Telegram! Если вы являетесь другом или подписчиком стр.
Для жителей районов Савеловский, Беговой, Аэропорт, Хорошевский
В этом месяце жителям районов Савеловский, Беговой, Аэропорт, Хорошевский» предоставляется скидка 5% на ВСЕ мед.
Абдуллаев Рустам Казимович
Врач-колопроктолог, общий хирург
Пак Алексей Геннадиевич
Сазонов Виктор Васильевич
Мы в Telegram и "Одноклассниках"
Эпителиальный копчиковый ход
15 минут
Нет боли
Анестезия не требуется
Подготовка не требуется
Не требуется
Сохраняется
Нет ограничений
Фистулография — это вид рентгенологического исследования свищевых ходов (или фистул) с применением контрастного вещества.
Свищом, или фистулой, называются патологическое соединение (ход) между различными органами или тканями (например, пузырно-прямокишечный свищ - между мочевым пузырем и прямой кишкой; ректовагинальный – между прямой кишкой и влагалищем; уретроректальный – между уретрой и прямой кишкой и др.).
В проктологии фистулографию используют для выявления и дифференциальной диагностики при заболеваниях аноректальной и крестцово-копчиковой областей при обнаружении на коже свищей.
Метод фистулографии очень эффективен для определения направления, протяженности, разветвлений свищевого хода, выявления образовавшихся по его ходу полостей и взаимоотношений с соседними органами.
Историческая справка
Первую фистулографию свища произвел Рейх в 1918 году. В свищ желчного пузыря он ввел раствор вазелина с бариевой пастой. В 1922 году Тенней и Патерсон в Америке и Карно и Блямутье во Франции заполнили барием общий желчный проток, введенный во время операции через дренаж. Эти первые опыты доказали, что с помощью фистулографии можно исследовать природу свища, его топографию и состояние желчных путей.
Чаще всего свищи образуются как следствие определенных заболеваний. Так, основные причины заболевания свищом прямой кишки – это острый парапроктит, болезнь Крона, СПИД, сифилис и онкологические заболевания.
Как проводится фистулография свища
Фистулография может проводиться как до операции, так и во время нее, или даже после оперативного вмешательства. Перед началом исследования проводятся рентгенограммы в двух перпендикулярных проекциях.
Фистулографию можно совмещать с другими исследованиями: цистографией, абцессографией, уретрографией или эндоскопическими методиками: ректороманоскопией и другими. Обычно ее проводит врач-рентгенолог в присутствии хирурга.
Перед фистулографией посредством шприца удаляют содержимое свищевого канала, промывают его. Пациентов, страдающих аллергией, перед началом процедуры фистулографии необходимо обследовать на наличие аллергии на йод.
Во время фистулографии во внешнее свищевое отверстие вставляют иглу или катетер и вводят рентгеноконтрастное вещество. Это масляные или водные соединения йода (уротраст, омнипак, верографин, йодолипол, пропилйодон) или взвесь бария.
Объем вводимого вещества зависит от размера и глубины свища (главное правило: пространство должно быть заполнено доверху). Затем заполненное отверстие плотно прикрывают шариком из марли, заклеивают медицинским клеем или лейкопластырем и готовят несколько рентгенологических снимков в различных проекциях. После проведения фистулографии контрастное вещество удаляют, или оно вытекает самостоятельно. Иногда фистулографию делают под анестезией.
После проведения фистулографии свища возможно небольшое повышение температуры и некоторая болезненность в районе свища.
Диагностика
С помощью фистулографии можно:
- измерить длину свищевого канала;
- понять направление свищевого канала;
- определить конфигурацию свищевого хода;
- увидеть наличие разветвлений свища;
- определить локализацию внутреннего свищевого отверстия;
- обнаружить связь с полыми органами (кишкой, мочевым пузырем, влагалищем, уретрой);
- выявить наличие гноя в свищевом канале;
- увидеть, есть или нет инородное тело, определить взаимоотношение с ним;
- найти источник свища - секвестр, абсцесс;
- выявить наличие связей между свищевыми каналами.
Информация, выявленная во время обследования, крайне важна для определения плана дальнейшего лечения.
Показания для фистулографии свища
Фистулография может применяться при следующих видах свищей:
- кишечном;
- пищеводном;
- мочепузырном;
- бронхопульмональном.
Противопоказания
Не следует проводить фистулографию в следующих случаях:
- острое воспаление в зоне свища;
- кровотечение из свищевого хода;
- беременность.
При проведении фистулографии возможно попадание контрастного вещества в расположенную рядом полость. Это осложнение может появиться, если вводить смесь при особенно высоком давлении. Чтобы этого не случилось, старайтесь проходить исследование в хорошо зарекомендовавших себя медицинских клиниках у настоящих профессионалов! В нашей клинике фистулографию проводят опытные специалисты высокой квалификации. При необходимости процедуру можно провести с применением внутривенной анестезии.
Рентгенография при трахеопищеводном свище.
Первый Московский государственный медицинский университет им. И.М. Сеченова, Москва, Россия
Российский научный центр хирургии им. акад. Б.В. Петровского, РАМН, Москва
Первый Московский государственный медицинский университет им. И.М. Сеченова, Москва, Россия
Российский научный центр хирургии им. акад. Б.В. Петровского РАМН, Москва
Транстрахеальный доступ при мультифокальном трахеопищеводном свище
Журнал: Хирургия. Журнал им. Н.И. Пирогова. 2013;(7): 55‑57
Паршин В.Д., Вишневская Г.А., Паршин В.В., Шарипжанова Р.Д. Транстрахеальный доступ при мультифокальном трахеопищеводном свище. Хирургия. Журнал им. Н.И. Пирогова. 2013;(7):55‑57.
Parshin VD, Vishnevskaia GA, Parshin VV, Sharipzhanova RD. The transtracheal access by multifocal tracheoesophageal fistula. Pirogov Russian Journal of Surgery = Khirurgiya. Zurnal im. N.I. Pirogova. 2013;(7):55‑57. (In Russ.).
Первый Московский государственный медицинский университет им. И.М. Сеченова, Москва, Россия
Первый Московский государственный медицинский университет им. И.М. Сеченова, Москва, Россия
Российский научный центр хирургии им. акад. Б.В. Петровского, РАМН, Москва
Первый Московский государственный медицинский университет им. И.М. Сеченова, Москва, Россия
Российский научный центр хирургии им. акад. Б.В. Петровского РАМН, Москва
Хирургия трахеопищеводного свища (ТПС) в настоящее время остается уделом ограниченного круга специализированных медицинских учреждений. Это связано не только с редкостью данного заболевания, но и со сложностью лечения подобных больных. Результаты этого лечения в руках опытных специалистов представляются вполне приемлемыми. Разработанные в последние десятилетия лечебная тактика и хирургические приемы позволили практически полностью отказаться от паллиативных вариантов лечения, излечивать больных за одну операцию, даже при ТПС в сочетании со стенозом трахеи. Осложненные формы ТПС, обусловленные рубцовым процессом в трахее или пищеводе, а также дегенеративными изменениями пищеводной стенки из-за ее чрезмерного постоянного расширения воздухом, существенно затрудняют лечение. Эти состояния являются основными причинами рецидива свища, неоправданного удаления пищевода, требующего последующей сложной реконструкции пищеварительного тракта, а также других осложнений, в том числе двустороннего паралича гортани.
Истончение стенки пищевода при больших размерах ТПС, массивном поступлении воздуха в пищеварительный тракт существенно затрудняет операцию. Во время операции пищевод легко травмируется при его мобилизации. Дефект пищевода трудно ушить, особенно когда он был увеличен в результате операционной травмы. В этих ситуациях актуальность приобретает адекватный доступ к свищу. В большинстве наблюдений к ТПС удается подойти через трахеопищеводную борозду, наиболее часто с левой стороны. Манипуляции в этой зоне всегда опасны из-за возможности повреждения нижнего возвратного гортанного нерва, особенно слева. Травма данного нерва с одной стороны не приводит к нарушению дыхания и глотания. Двусторонний приводящий паралич голосовых складок в послеоперационном периоде является грозным осложнением. Возникает потребность в трахеостомии для обеспечения дыхания пациента. Длительное нахождение инородного тела (трахеостомической трубки) в области недавно наложенных швов трахеи является основной причиной рецидива ТПС в ближайшем послеоперационном периоде. Кроме того, стеноз гортани, обусловленный приводящим параличом, в дальнейшем потребует нескольких операций со сложной функциональной реабилитацией. При двустороннем повреждении нижних гортанных возвратных нервов возможно возникновение и отводящего паралича без нарушения дыхания. Это не должно обнадеживать хирурга. Данная ситуация имеет временный характер. В дальнейшем возникнет приводящий паралич и появится клиническая картина стридора. Предрасполагающими факторами для двустороннего повреждения нижних возвратных гортанных нервов являются ТПС больших размеров с вовлечением в патологический процесс всей ширины мембранозной стенки трахеи. Чрезмерно большой диаметр пищевода обусловливает технические трудности выделения свища, смещение органов средостения в латеральных направлениях.
Для хирургического доступа в зависимости от локализации ТПС производят цервикотомию, стернотомию либо правостороннюю боковую торакотомию. Однако у некоторых больных приходится избирать нетрадиционный доступ. Примером подобной ситуации является следующее клиническое наблюдение.
Больная К., 19 лет, поступила в отделение хирургии легких и средостения с жалобами на кашель с выделением слизистой мокроты, поперхивание при приеме пищи, одышку при физической нагрузке. С детского возраста состояла на учете у педиатра по поводу врожденной аномалии развития легких. В 1994 г. ей выполнили нижнюю лобэктомию слева с резекцией язычковых сегментов по поводу бронхоэктазов. В период с 1994 по 2007 г. возникали частые обострения воспалительного процесса в легких, по поводу чего неоднократно лечилась в стационаре по месту жительства. При обследовании высказывалось предположение о наличии ТПС, однако при ФЭГДС диагноз не был подтвержден. В 2007 г. состояние больной ухудшилось, усилился кашель, увеличилось количество слизисто-гнойной мокроты. При повторной операции выполнена верхняя лобэктомия слева по типу пневмонэктомии. В сентябре 2011 г. больная вновь отметила ухудшение состояния, прогрессирование одышки, появление кашля с мокротой гнойного характера, поперхивание при приеме пищи. При обследовании по месту жительства был диагностирован ТПС.
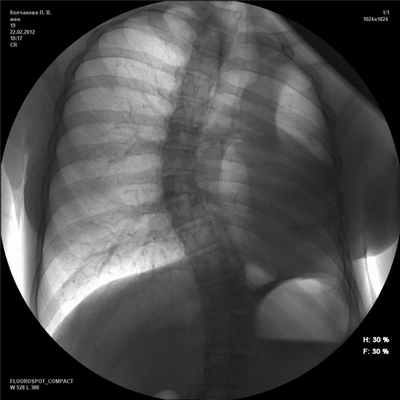
При поступлении общее состояние больной относительно удовлетворительное. Подкожный жировой слой плохо развит. Аускультативно справа выслушивалось жесткое дыхание, хрипов не было. Тоны сердца ясные и ритмичные. Пульс 75 в 1 мин, удовлетворительного наполнения и напряжения. АД 110/70 мм рт.ст. Язык чистый. Живот мягкий, безболезненный. При полипозиционной рентгеноскопии и рентгенографии органов грудной клетки левая половина грудной клетки деформирована и затемнена (рис. 1). Рисунок 1. Рентгенограмма грудной клетки в прямой проекции. Смещение органов средостения влево, легочная грыжа, искривление позвоночника. Отсутствие левого легкого после пневмонэктомии. Тень средостения определялась слева от средней линии. Правое легочное поле было прозрачное, без очаговых и инфильтративных теней. В переднем средостении определялась легочная грыжа. При приеме водорастворимого контрастного вещества в положении больной на правом боку отмечался заброс препарата в трахею на уровне ключиц. Диаметр свищевого хода 5 мм.
При компьютерной томографии (рис. 2) Рисунок 2. Компьютерные томограммы. В шейно-грудном отделе трахеи трахеопищеводный свищ, резкое расширение пищевода, стенка которого истончена (а). Рисунок 2. Компьютерные томограммы. Органы средостения смещены влево после пневмонэктомии (б). диагностирован фиброторакс слева после пневмонэктомии, средостение значительно смещено влево. Определялось трахеопищеводное соустье. На значительном протяжении стенка между трахеей и пищеводом была крайне истончена.
При эндоскопическом исследовании голосовые складки подвижны. Слизистая трахеи и бронхов незначительно отечна и гиперемирована. Культя левого главного бронха была длиной около 3 см без видимых дефектов. В мембранозной части трахеи на расстоянии приблизительно 6 см от голосовых складок и 5 см от карины трахеи имеется отверстие размером 3×5 мм с гладкими краями. Через него эндоскоп свободно проходит в просвет пищевода. Последний не изменен, слизистая гладкая, розовая, блестящая. На расстоянии 20 см от резцов по передней стенке определяется свищевое отверстие диаметром около 3-4 мм, слизистая краев отверстия гладкая, розовая.
Таким образом, диагностирован ТПС с локализацией его устья в шейно-грудном отделе. Неблагоприятными моментами для хирургического лечения были смещение трахеи и пищевода вместе с органами средостения влево, резкое увеличение размеров пищевода с истончением его стенки в результате большого сброса воздуха из дыхательного пути через ТПС, тонкая прослойка тканей между трахеей и пищеводом, что повышало риск их повреждения при выделении соустья. От правосторонней боковой торакотомии отказались из-за высокого расположения ТПС, смещения средостения влево, необходимости выполнения операции через плевральную полость единственного легкого, что могло повлечь нарушение газообмена, а в послеоперационном периоде развитие пневмонии травматического генеза. Подойти к трахее и пищеводу через стернотомию для разделения свища было также затруднительно, так как пришлось бы значительно ротировать трахею для доступа к ее мембранозной стенке. Увеличенный и истонченный пищевод при этом могли легко травмировать. Кроме того, имелся крайне высокий риск повреждения нижних гортанных возвратных нервов. С учетом всего изложенного выше было принято решение в качестве нетрадиционного доступа избрать стернотомию с последующим поперечным пересечением трахеи и мобилизацией пищевода с разобщением свища.
01.03.12 - операция. Произведена цервикотомия по нижней кожной складке, частичная продольно-поперечная стернотомия до уровня третьего межреберья. В рану прилежала большая легочная грыжа. При ее отделении и смещении содержимого в правую плевральную полость медиастинальная плевра была повреждена и произошел пневмоторакс справа. При дальнейшей ревизии установлено, что структуры средостения несколько смещены влево. Выделены и взяты на держалки левая плечеголовная вена и артериальный брахицефальный ствол. Остро и тупо мобилизованы трахея и грудной отдел пищевода, которые были интимно спаяны друг с другом. Стенка пищевода резко истончена, его диаметр превышал размеры трахеи и соответствовал диаметру позвонков, к которым он был интимно припаян. С учетом сложившейся ситуации разделение трахеи и пищевода через трахеопищеводную борозду было сопряжено с риском повреждения пищевода, увеличением размеров свища, повреждением возвратных нервов. В связи с этим принято решение пересечь трахею в поперечном направлении с последующим отделением мембранозной стенки под визуальным контролем. Трахея взята на держалку. С помощью трансиллюминации установлен уровень ТПС. Трахея поперечно пересечена с оставлением участка мембранозной стенки у устья ТПС (рис. 3, а, б). Рисунок 3. Этапы операции. а — трахея пересечена с оставлением участка мембранозной стенки вокруг свища. Рисунок 3. Этапы операции. б — определяется 2 трахеопищеводных свища. В них введен зажим.
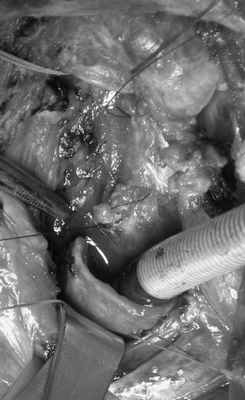
Краниальная культя трахеи отделена от пищевода острым путем. При этом диагностировано второе устье ТПС, которое располагалось на 2-3 см краниальнее первого. Оно было хорошо эпителизировано, без признаков воспаления. В этой зоне трахея и пищевод разделены аналогичным способом с оставлением участка мембранозной стенки трахеи вокруг устья свища. Оба свища ушиты двухрядным швом: первый - с использованием участка мембранозной части трахеи, второй - мышечной оболочки пищевода с погружением в нее первого шва (рис. 3, в). Рисунок 3. Этапы операции. в — дефекты пищевода ушиты двухрядным швом. Интубационная трубка через операционную рану установлена в каудальном отделе трахеи по типу шунт—дыхание.
Для наложения швов использована викриловая нить 3/0 на атравматической игле. После ушивания дефектов пищевода выкроен лоскут из мышц шеи, который отсечен в его краниальной части и ротирован в средостение путем фиксации к передней стенке пищевода отдельными узловыми швами для изоляции его швов. Ввиду образовавшихся дефектов в мембранозной стенке трахеи выполнена ее циркулярная резекция на протяжении около 3,5 см. Целостность дыхательного пути восстановленна с помощью межтрахеального анастомоза по типу конец в конец (рис. 3, г, д). Рисунок 3. Этапы операции. г — целостность мембранозной стенки восстановлена обвивным швом. Рисунок 3. Этапы операции. д — окончательный вид трахеального анастомоза. Мембранозная стенка ушита обвивным викриловым швом, хрящевая - узловыми викриловыми швами. Трахеальный анастомоз изолирован от брахицефального артериального ствола участком вилочковой железы на ножке. Правая плевральная полость дренирована двумя дренажами, средостение - одним дренажем. Грудина фиксирована узловыми стальными швами. После послойного ушивания раны голова больной фиксирована в положении приведения к передней стенке грудной клетки с помощью двух кожных швов.
Послеоперационный период протекал без осложнений. Питание через рот восстановлено на 5-е сутки. Дыхание полностью компенсировано. По данным эндоскопии, трахеальный анастомоз зажил первичным натяжением без признаков стенозирования.
Таким образом, индивидуальный подход в выборе тактики лечения больной с длительно существующим мультифокальным ТПС на фоне дегенеративных изменений пищевода, связанных с его перераздуванием воздухом, после левосторонней пневмонэктомии и смещением органов средостения, позволил выполнить радикальную органосохраняющую операцию с хорошим результатом. Прецизионный транстрахеальный доступ к пищеводу в области локализации ТПС дал возможность минимизировать риск повреждения истонченного пищевода и нижних возвратных гортанных нервов, обеспечить надежное ушивание дефекта пищевода за счет участка мембранозной стенки трахеи и хорошую изоляцию пищеводных швов мышечным лоскутом на питающей ножке. Восстановление целостности дыхательного пути с помощью формирования межтрахеального анастомоза конец в конец в условиях отсутствия натяжения тканей и при соответствующем опыте оперирующего хирурга надежно и минимально рискованно. Представляется, что подобный транстрахеальный доступ также показан при сочетании ТПС и стеноза трахеи, когда патологическое соустье располагается на уровне стенозированного фрагмента дыхательного пути. В таких ситуациях резекция суженного отдела трахеи позволяет подойти к пищеводу спереди, хорошо визуализировать и ушить свищевое отверстие, тем самым излечить больного от сочетанных заболеваний за одну операцию. Приведенное наблюдение показывает, что хирургическое лечение трахеопищеводного свища требует серьезного практического опыта и неклассического мышления оперирующего хирурга.
Трахеопищеводный свищ ( Трахеоэзофагеальная фистула )
Трахеопищеводный свищ – это патологическое соустье, соединяющее просвет дыхательного горла с пищеводом. Может являться аномалией развития или приобретенной патологией. Трахеопищеводный свищ проявляется приступами кашля во время приема пищи, которые сопровождаются удушьем, цианозом, выделением пенистой мокроты с кусочками пищи. Часто развивается аспирационная пневмония. Подтверждающая диагностика проводится с помощью эндоскопических методов (эзофагоскопии, трахеобронхоскопии), рентгенографии пищевода. Лечение исключительно оперативное – закрытие трахеопищеводного свища, нередко с одномоментной трахеопластикой, циркулярной резекцией трахеи, эзофагопластикой.
МКБ-10
Общие сведения
Причины
Врожденный трахеопищеводный свищ образуется к 4-6-й неделе эмбриогенеза при неполном разделении первичной кишки и дыхательной трубки. При рождении дети с данной аномалией обычно имеют массу тела менее 2500 г.
Природа происхождения приобретенных трахеоэзофагеальных фистул может быть различной. Чаще всего с такой патологией приходится сталкиваться онкологам, а сами свищи возникают в результате далеко зашедшего рака пищевода или трахеи, лимфом, лимфогранулематоза. Второй по распространенности причиной служат травмы пищеварительной и дыхательной трубки (в том числе их ятрогенные повреждения), полученные при проведении эзофагоскопии, бужировании пищевода, перфорации пищевода или трахеи инородными телами, вследствие химических ожогов пищевода, при закрытых и проникающих ранениях шеи и груди. Возможно непреднамеренное повреждение трахеи и пищевода при операционных вмешательствах в этой области.
В анестезиолого-реанимационной практике отмечены случаи образования пролежней от трахеостомической или интубационной трубки, приводящие к формированию трахеопищеводного свища. К числу редких причин относят перфорацию дивертикула пищевода в трахею. Трахеопищеводный свищ может явиться осложнением неспецифической бактериальной инфекции (эмпиемы плевры, абсцесса легкого, гнойного медиастинита) или специфических воспалительных процессов (туберкулеза внутригрудных лимфатических узлов, сифилиса, актиномикоза).
Классификация
По своему происхождению трахеопищеводные свищи могут быть врожденными или приобретенными в процессе жизни. Различают 5 типов врожденных трахеопищеводных свищей, обозначаемых римскими знаками:
По наличию/отсутствию клапанного механизма трахеопищеводные свищи подразделяются на клапанные и бесклапанные. При единственном дефекте говорят об изолированном свище, при сочетании с другими патологическими процессами трахеи или пищевода – о сочетанном. Клиническое течение трахеопищеводных свищей может быть неосложненным, гладким или осложненным различными состояниями (аспирационной пневмонией, нутритивной недостаточностью и кахексией, бактериальной деструкцией легких, пневмогенным сепсисом и т. д.).
Симптомы трахеопищеводного свища
Клиническая картина, ее выраженность и особенности зависят от времени возникновения, размеров, типа, направления хода свища. Большинство детей с данной аномалией рождаются недоношенными, а доношенные новорожденные имеют признаки внутриутробной гипотрофии. Во время гестации у беременных отмечается многоводие.
Признаки врожденного трахеопищеводного свища с атрезией пищевода появляются уже через несколько часов после рождения. Возникает кашель, приступы удушья, вздутие живота. Во время первого же кормления диагноз становится очевиден. Каждый глоток молока или воды сопровождается приступом кашля, выделением пенистой слизи из носа и рта ребенка. Дыхание затрудняется, развивается резкий цианоз и аритмия, в легких выслушиваются обильные крупнопузырчатые хрипы. Рано присоединяется аспирационная пневмония и ателектазы легких. Состояние ребенка прогрессивно ухудшается.
Наиболее выражены перечисленные признаки при широком и коротком трахеопищеводном свище. При наличии узкого и длинного свищевого хода аномалия долгое время нередко остается нераспознанной. Изредка при кормлении возникает поперхивание и несильный кашель, однако изменение позы кормления избавляет ребенка от приступов, поэтому родители не придает этому факту должного значения. Такие дети страдают частыми пневмониями.
У 40% новорожденных с трахеопищеводным свищом выявляются сопутствующие врожденные пороки сердца, аномалии развития кишечника и мочевыводящих путей. В литературе описан синдром VATER, включающий в себя аномалии развития позвоночника (клиновидные позвонки), атрезию заднего прохода, трахеопищеводный свищ, гипоплазию лучевой кости и дисплазию почек.
Приобретенный трахеопищеводный свищ манифестирует кашлем, удушьем, цианозом, связанными с приемом пищи. В откашливаемом секрете можно обнаружить кусочки еды. При клапанной трахеоэзофагеальной фистуле кашель может отсутствовать. Нередко у больных отмечаются боли в груди и эпигастрии, кровохарканье, рвота с примесью крови, одышка, нарушение фонации, снижение массы тела. Во всех случаях трахеопищеводный свищ сопровождается периодическими подъемами температуры, рецидивирующими легочными инфекциями.
Диагностика
При подозрении на трахеопищеводный свищ пациент нуждается в консультации торакального хирурга, гастроэнтеролога, детского хирурга, эндоскописта, рентгенолога. На первичном этапе используется зондирования пищевода с помощью резинового катетера: если продвижению катетера мешает сопротивление слепого конца пищевода, а при введении в катетер жидкости, окрашенной метиленовым синим, она при кашле выделяется через рот или нос, вероятность трахеопищеводного свища оценивается как очень высокая.
Лучевое исследование включает выполнение рентгеноскопии и рентгенографии легких, эзофагографии, МСКТ грудной клетки. Контрастное исследование пищевода проводят очень осторожно, используя водорастворимые или масляные вещества, которые вводятся через зонд (применение сульфата бария в этих случаях недопустимо). Трахеопищеводный свищ требует проведения тщательной дифференциальной диагностики с изолированной атрезией и стенозом пищевода, гастроэзофагеальным рефлюксом, ахалазией кардии, дисфагией различного генеза.
Эндоскопическая диагностика трахеопищеводного свища остается основной. Для лучшей визуализации патологического соустья и получения максимальной информации о его особенностях, выполняется эзофагоскопия и трахеобронхоскопия. При критическом стенозе трахеи диагностическая трахеоскопия может быть трансформирована в лечебную процедуру путем эндоскопического восстановления просвета трахеи или стентирования стенозированного участка.
Лечение трахеопищеводного свища
Лечение проводится хирургическим путем, консервативная терапия малоперспективна и используется только на этапе подготовки к оперативному вмешательству. С целью удаления скапливающегося секрета производится установка катетера в слепо заканчивающийся конец пищевода, выполняются санационные бронхоскопии. В рамках лечения аспирационной пневмонии назначается оксигенотерапия, антибактериальная и инфузионная терапия, УВЧ на грудную клетку. Для предотвращения попадания пищи в трахеобронхиальное дерево полностью прекращается кормление через рот, осуществляется гастростомия, нутритивная поддержка, витаминотерапия.
Варианты радикального хирургического устранения трахеопищеводного свища могут быть различны. Операция обычно производится из шейного доступа или заднебоковой торакотомии. Длинный свищевой ход выделяют и пересекают между двумя наложенными лигатурами. Дефекты в стенках пищевода и трахеи ушивают погружными швами. При коротком и широком свищевом ходе трахею отсекают от пищевода, после чего на оба дефекта накладывают непрерывный двухрядный шов. Для закрытия дефекта могут использоваться аутоткани (сальник или стенка желудка).
В тех случаях, когда трахеопищеводный свищ сочетается со стенозом трахеи либо атрезией пищевода, производится разобщение свища с одномоментной циркулярной резекцией или пластикой трахеи и/или одномоментной пластикой пищевода. Если имеется большой диастаз между проксимальным и дистальным сегментами пищевода, не позволяющий наложить анастомоз «конец-в конец», верхний отдел пищевода выводят на шею, свищ разобщают и на этом операцию заканчивают.
В межоперационный период питание больного осуществляют через гастростому. На втором этапе производят пластику пищевода желудочным или тонкокишечным трансплантатом. При трахеопищеводных свищах, обусловленных распадом раковой опухоли, ограничиваются паллиативной гастростомией. В послеоперационном периоде продолжается активная противопневмоническая терапия. В первые сутки осуществляется парентеральное питание, затем – кормление через зонд, который оставляют на 7-10 суток.
Прогноз
Из послеоперационных осложнений возможны стенозы в области пищеводных анастомозов, которые подлежат бужированию, и рецидивы свища, требующие повторной операции. Летальность при оперативном лечении трахеопищеводного свища составляет 10-15% и связана, главным образом, с исходно тяжелым состоянием пациента. В то же время при отказе от операции показатели летальности возрастают до 80-90%.
Трахеопищеводные свищи. Симптомы и лечение трахеопищеводных свищей
Пищеводная и дыхательная трубки, формирующиеся из одного начала, при каком либо нарушении во время внутриутробного периода могут иметь между собой патологические соединения — это свищи.
Причины трахеопищеводного свища
Причина трахеопищеводного свища – аномальное деление первичной кишки на дыхательную и пищеводную трубки и приводит к появлению свища. Обычное расположение свища идет на уровне 1 -го грудного позвонка.
2. Симптомы трахеопищеводного свища
Трахеопищеводный свищ имеет следующие симптомы:
- Кашель во время употребления пищи;
- Цианоз (синюшный окрас тканей при недостатке кислорода);
- При большом размере свища возможно развитие пневмонии.
3. Диагностика свища
Диагностика свища проводится при помощи бронхоскопии. Это эндоскопический метод, при котором вводят контрастное вещество, обнаруживающее аномальное изменение между трахеей и пищеводом (свищ).
Также в постановке диагноза существенно помогает рентгенография, т.к. на полученном снимке отсутствует газовый пузырь желудка.
4. Лечение трахеопищеводного свища
Лечение трахеопищеводного свища заключается в установлении многоходового санационного катетера в слепо заканчивающийся проксимальный конец пищевода. Это необходимо для ликвидации скапливающегося секрета. Пищеводный анастомоз накладывают в конец из правого торакотомического доступа. В случае если расстояние между дистальным и проксимальным концами велико, то проксимальный выводят в виде стомы в шею или перевязывают, после чего делают гастростомию.
Заболевания- Cтенозы трахеи и крупных бронхов различной этиологии (рубцовые, опухолевые,экспираторные)
- Респираторно-органные свищи (трахеопищеводный, бронхопищеводный и другие)
- Доброкачественные новообразования легких и средостения (гамартомы, невриномы,бронхогенные и энтерогенные кисты и другие)
- Эхинококкоз легких
- Хилоторакс, кисты грудного протока
- Метастатическое поражение легких
- Опухоли плевры
- Трахея
- Грудная клетка
- Средостение
- Легкие
- Бронхи
Если вы обнаружили у себя подобные симптомы, возможно, это сигнал заболевания, поэтому рекомендуем проконсультироваться с нашим специалистом.
Диагностика- Рентгенография органов грудной клетки
- МСКТ органов грудной клетки
- Сцинтиграфия легких
- ПЭТ-КТ (позитронно-эмиссионная томография)
- Бронхоскопия
- Консультация врача торакального хирурга, профессор - 10000 р.
- Рентгенография органов грудной клетки на базе ЛПУ-партнера - от 2000 р.
- МСКТ органов грудной клетки на базе ЛПУ-партнера - от 6000 р.
- Сцинтиграфия легких на базе ЛПУ-партнера - 8000 р.
- ПЭТ-КТ (позитронно-эмиссионная томография) на базе ЛПУ-партнера - от 35000 р.
Мы стараемся оперативно обновлять данные по ценам, но, во избежание недоразумений, просьба уточнять цены в клинике.
Данный прайс-лист не является офертой. Медицинские услуги предоставляются на основании договора.
АТРЕЗИЯ ПИЩЕВОДА
Атрезия пищевода — порок развития, при котором проксимальный и дистальный концы пищевода не сообщаются между собой.
Пороки развития пищевода встречаются с частотой 1:3 000 – 1:5 000 новорожденных, наиболее частый вариант порока – сочетание атрезии с трахеопищеводным свищем.
Атрезия пищевода в более чем половине случаев (63-72%) сочетается с другими пороками развития.
- врожденные пороки сердца
- пороки развития ЖКТ
- пороки развития трахеобронхиального дерева.
- деформации костно-мышечной системы: позвоночного столба, ребер, конечностей.
- хромосомные аномалии: около 3% пациентов с атрезией пищевода и трахеопищеводным свищем имеют хромосомные аномалии – трисомии (18,13,21 пары хромосом).
Наиболее известные синдромы, которые встречаются при атрезии пищевода – это VACTER и CHARGE-синдромы.
В 1973 г Quan и Smith впервые описали VATER-ассоциацию, которая состоит из комбинации аномалий включающих пороки развития позвоночника (vertebral), аноректальной области (anorectal), трахеопищеводный свищ (tracheoesophageal) и пороки развития почек (renal).
Позднее этот синдром включил пороки развития сердца (cardiac) и конечностей (limb).
CHARGE-синдром (колобома, пороки сердца, атрезия хоан, задержка роста, генитальная гипоплазия, аномалии ушной раковины);
Диагноз атрезии пищевода устанавливается чаще всего в родзале, когда невозможна постановка назогастрального зонда при первичном осмотре. Ребенок не может проглотить слюну, в связи с чем, отмечается повышенная саливация, слюна пенится и отходит через рот и нос.
При подозрении на атрезию пищевода ребенка ни в коем случае нельзя кормить, так как невозможность проглатывания молока приводит к развитию аспирационной пневмонии!
Пренатальная эхографическая диагностика атрезии пищевода основывается, как правило, только на косвенных признаках порока, начиная с 18 недель беременности:
- многоводие, связанное с невозможностью проглатывания плодом амниотической жидкости, вследствие непроходимости пищевода.
- отсутствие эхографического изображения желудка или маленьких его размеров при динамическом ультразвуковом наблюдении (чаще при изолированной форме атрезии пищевода).
- в некоторых случаях может выявляться расширение глотки и проксимального конца пищевода.
Чувствительность эхографии в диагностике атрезии пищевода при комбинированном использовании эхографических признаков (многоводие, отсутствие эхотени желудка) не превышает 42%.
Основной диагностический признак атрезии пищевода при рождении ребенка – невозможность постановки желудочного зонда.
Далее обязательно проводится рентгенологическое обследование для подтверждения диагноза. На обзорном снимке грудной и брюшной полостей начало зонда определяется в слепом конце пищевода, далее наличие газа в желудочно-кишечном тракте позволяет дифференцировать свищевые формы атрезии пищевода. Отсутствие газа в желудке при обзорной рентгенографии чаще всего связано с отсутствием сочетания атрезии пищевода со свищем в трахею.
Новорожденные дети с установленным диагнозом атрезии пищевода нуждаются в проведении срочного оперативного лечения.
Операцией выбора является наложение прямого анастомоза между двумя концами пищевода.
В нашем отделении данная операция проводится малоинвазивным эндоскопическим методом – через минимальные проколы (3мм) в правой половине грудной клетки выявляются атрезированные концы пищевода и сшиваются между собой.
В случае невозможности одномоментного сшивания пищевода мы используем процедуру по поэтапному вытяжению пищевода по Foker, так же выполняемую эндоскопическим методом. По этой методике концы пищевода в состоянии максимального натяжения фиксируются к грудной стенке, тем самым получаю импульс к росту. В результате концы пищевода следующим этапом сшиваются между собой.
Приоритетным направлением в хирургии пищевода в нашем отделении является реконструкция собственного пищевода, что в последующем избавляет детей от необходимости замещать пищевод другими отделами кишки.
В ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии имени академика В.И. Кулакова» Минздрава России Вы получаете уникальную возможность получить БЕСПЛАТНО оперативное стационарное лечение по квотам на высоко-технологическую медицинскую помощь (ВМП по ОМС).
Читайте также:
