Соматосенсорная обратная связь. Стимуляция спинальных мотонейронов
Добавил пользователь Евгений Кузнецов Обновлено: 28.01.2026
Методика применяется для лечения различного рода патологических состояний сопровождающихся выраженными болями в ногах, в спине, в промежности, спастичности в нижних конечностях. Также применяется для лечения эректильной дисфункции, нарушения функции тазовых органов. Методика заключается в установке на поверхность спинного мозга электродов, к которым подаются стимулы от стимулятора, вшиваемого под кожу. Перед окончательной имплантацией стимулятора проводится тестовая стимуляция, когда электроды выводятся наружу и подключаются к внешнему стимулятору, для подбора параметров стимуляции, оценки эффективности в каждом конкретном случае.
CТИМУЛЯЦИЯ СПИННОГО МОЗГА - (SPINAL CORD STIMULATION - SCS)
Метод лечения хронического болевого синдрома, спастики, нарушения функции тазовых органов.
Эффект достигается при помощи электрических импульсов, которые доставляются электродами, имплантированными в эпидуральное пространство.
- Электрические импульсы активируют тормозящие боль нейроны в заднем роге спинного мозга, в результате чего чувство боли уменьшается;
- Стимуляция также вызывает парестезию (ощущение мягкой приятной вибрации) в зоне, откуда происходит боль, и ее округе;
- Применение SCS считается успешным, если удалось достичь более чем 50%-ного уменьшения боли по визульно-аналоговой шкале;
- Однако 30%-ное уменьшение боли также является клинически значимым
- Ежегодно более 15 000 пациентам во всем мире имплантируются нейростимуляторы для лечения хронической невропатической боли;
Электроды соединяются с нейростимулятором, который имплантируется подкожно.
На сегодняшний день консервативные методы лечения не всегда обеспечивают достаточное обезболивание.
- Фармакотерапия, как правило, является первым и главным методом лечения, однако;
- Более 50% пациентов остаются недовольными фармакотерапией, независимо от применяемого лекарства.
- Многие лекарства вызывают различные побочные эффекты.
Невропатическая боль (НБ) может быть фармакорезистентной (лекарства не приносят желаемого облегчения или вызывают непереносимые побочные эффекты).
Нейростимуляция является альтернативным методом лечения пациентов с НБ, в случае если традиционные консервативные методы лечения не приносят желаемого результата.
ТЕСТОВАЯ НЕЙРОСТИМУЛЯЦИЯ (ТН)
ТН предполагает имплантацию электрода, который является частью системы для проведения теста. Введение электрода осуществляется под местной анестезией. Благодаря ТН уже на операционном столе удается получить анальгетический (обезболивающий) эффект, а также с большей долей вероятности прогнозировать эффективность нейростимуляции еще до имплантации всей системы.
Тестовый период в течение 7-10 дней проводится в амбулаторных условиях, приближенных к повседневным, для лучшей оценки больным динамики болевого синдрома и влияния его на повседневную активность. В тестовом периоде проводится подбор оптимальных параметров электростимуляции.
Если по результатам ТН удалось достичь 50% - го снижения боли по Визуально-аналоговой шкале (шкала оценки интенсивности боли), то пациенту может быть имплантирована система нейростимуляции полностью. В случае же неудачи, встанет вопрос о переходе на следующую ступень.
Отдельно следует отметить, что при некоторых болевых синдромах, например при травматическом отрыве корешков нервного сплетения пациентам производятся хирургические вмешательства, например DREZ-операция. При грыже межпозвоночного диска - соответствующее иссечение грыжи. А при онкологических болях - хордотомия.
Обязательное условие: Перед установкой нейростимулирующей системы проводится тестовая стимуляция (см. выше), при которая позволяет врачу убедиться в эффективности методики.
КОМПОНЕНТЫ SCS-СИСТЕМЫ КОМПАНИИ MEDTRONIC
Система для неиростимуляции состоит из трех базовых имплантируемых компонентов, которые могут использоваться унилатерально или билатерально:
- Нейростимулятор
- Удлиннитель
- Чрезкожный цилиндрический или хирургический электрод
Нейростимулятор, или имплантируемый генератор импульсов.
Нейростимулятор представляет собой изолированное устройство, похожее на кардиостимулятор, состоящее из батареи и электроники. Он имплантируется подкожно, и вырабатывает электрические импульсы, необходимые для унилатеральной или билатеральной стимуляции. Эти импульсы проводятся по удлиннителям и электродам в спинной мозг.
Удлиннитель
Удлиннитель - это тонкий изолированный провод. Удлиннители имплантируют подкожно, соединяя электрод с нейростимулятором.
Электрод представляет собой тонкий изолированный четырехжильный провод с четырьмя, восемью или 16-ю контактами на кончике. Электрод имплантируется в эпидуральное пространство, чтобы проводить туда электрический ток, осущевляющий нейростимуляцию. Оптимальное положение электрода всегда находится в корреляции с зоной боли пациента. Для стимуляции спинного мозга электроды имплантируются в эпидуральное пространство (между позвонком с твердой мозговой оболочкой), при этом контакты электродов находятся достаточно близко к заднему рогу спинного мозга, чтобы осуществлять стимуляцию толстых миелиновых нервных волокон.
Неимплантируемые компоненты системы
К неимплантируемым компонентам системы относятся пульт пациента и программатор врача, которые используются для управления нейростимулятором.
Программатор врача N'Vision. Используется для программирования нейростимуляторов. Параметры импульсов, вырабатываемых нейростимулятором, могут быть неинвазивно изменены при помощи программатора врача. Программатор передает настройки нейростимулятору дистанционно при помощи радиочастотной связи.
Пульт пациента. Пульт пациента-это портативное устройство, которое позволяет пациенту самостоятельно включать и выключать нейростимулятор,когда это необходимо, а также проверять уровень заряда батареи нейростимулятора.
Соматосенсорная обратная связь. Стимуляция спинальных мотонейронов
Удержание тела от действия силы тяжести. Ретикулярная система головного мозга
а) Удержание тела от действия силы тяжести — роль ретикулярных и вестибулярных ядер. На рисунке ниже показана локализация ретикулярных и вестибулярных ядер в стволе мозга.
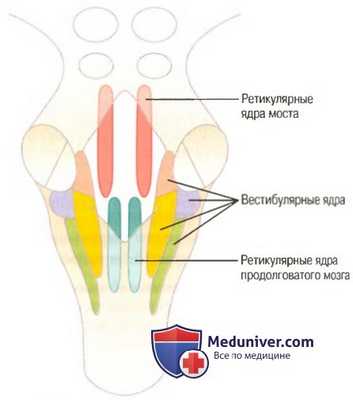
Локализация ретикулярных и вестибулярных ядер в стволе мозга
б) Возбудительно-тормозной антагонизм между ретикулярными ядрами моста и продолговатого мозга. Ретикулярные ядра подразделяют на две основные группы:
(1) ретикулярные ядра моста, расположенные несколько сзади и латерально в области моста и распространяющиеся в средний мозг;
(2) ретикулярные ядра продолговатого мозга, которые идут вдоль всего продолговатого мозга и лежат впереди и медиально, у средней линии.
Эти две группы ядер — в основном функциональные антагонисты, при этом ядра моста антигравитационные мышцы возбуждают, а ядра продолговатого мозга их расслабляют.
в) Ретикулярная система моста. Ретикулярные ядра моста посылают возбуждающие сигналы к спинному мозгу по ретикулоспиналъному тракту моста, идущему вдоль переднего столба спинного мозга, как показано на рисунке ниже.
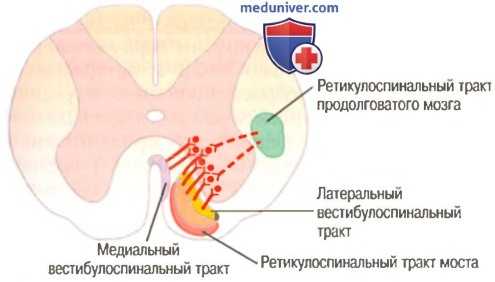
Вестибулоспинальные и ретикулоспинальные тракты, нисходящие в спинной мозг для возбуждения (сплошные линии) и торможения (пунктирные линии) передних мотонейронов, иннервирующих мускулатуру оси тела
Волокна этого пути заканчиваются на медиальных передних мотонейронах, иннервирующих осевые мышцы тела, которые помогают противостоять действию силы тяжести, т.е. мышцы, выпрямляющие позвоночник, и мышцы-разгибатели конечностей.
Ретикулярные ядра моста имеют высокую степень естественной возбудимости. Кроме того, они получают мощные возбуждающие сигналы от вестибулярных ядер, а также от глубоких ядер мозжечка. Следовательно, при отсутствии противодействия ретикулярной системы продолговатого мозга ретикулярная возбуждающая система моста вызывает такое мощное возбуждение антигравитационных мышц тела, что четвероногое животное, если ему придать вертикальное положение, может «стоять», противодействуя силе тяжести, без каких-либо сигналов от вышележащих уровней головного мозга.
г) Ретикулярная система продолговатого мозга. Ретикулярные ядра продолговатого мозга проводят тормозные сигналы к тем же антигравитационным передним мотонейронам по другому пути — ретикулоспинальному тракту продолговатого мозга, который расположен в боковом столбе спинного мозга, как показано на рисунке выше. Ретикулярные ядра продолговатого мозга получают мощные входные коллатерали от:
(1) кортикоспинального тракта;
(2) руброспинального тракта;
(3) других моторных путей.
В норме они активируют тормозную ретикулярную систему продолговатого мозга, уравновешивая возбудительные влияния ретикулярной системы моста, и при нормальных условиях мышцы тела имеют нормальный тонус.
Однако некоторые сигналы от вышерасположенных областей головного мозга могут затормозить систему продолговатого мозга при необходимости возбуждения мостовой системы для обеспечения вертикального положения тела. В других случаях возбуждение ретикулярной системы продолговатого мозга может тормозить антигравитационные мышцы в некоторых частях тела, чтобы позволить этим частям тела выполнить специфические двигательные функции.
Возбуждающие и тормозные ретикулярные ядра составляют регулируемую систему, которая управляется моторными сигналами от коры большого мозга и других областей, чтобы обеспечить необходимые тонические сокращения мышц для противодействия силе тяжести при стоянии и, когда требуется, тормозить соответствующие группы мышц для выполнения других двигательных функций.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
а) Соматосенсорная обратная связь с моторной корой помогает контролировать точность мышечных сокращений. Когда сигналы от моторной коры вызывают сокращение мышц, соматосенсорные сигналы от активированных регионов возвращаются к нейронам моторной коры, инициирующим действие. Большинство этих соматосенсорных сигналов возникают в:
(1) мышечных веретенах;
(2) сухожильных органах мышечных сухожилий;
(3) тактильных рецепторах кожи над мышцей.
Эти соматические сигналы через положительную обратную связь часто вызывают усиление мышечных сокращений следующим образом.
В случае мышечных веретен, если интрафузальные мышечные волокна веретен сокращаются сильнее, чем крупные волокна скелетных мышц, центральные части веретен растягиваются и, следовательно, возбуждаются. Затем сигналы от этих веретен быстро возвращаются к пирамидным клеткам моторной коры, сообщая им, что крупные мышечные волокна сокращаются недостаточно сильно. Пирамидные клетки сильнее возбуждают мышцы, помогая им «догнать» сокращение мышечных веретен.
В случае тактильных рецепторов, если при мышечном сокращении кожа придавливается к объекту, например при обхватывании пальцами сжимаемого в кулаке предмета, сигналы от кожных рецепторов могут, если это необходимо, вызвать дальнейшее возбуждение мышц и, следовательно, усиление сжимающего действия кисти.
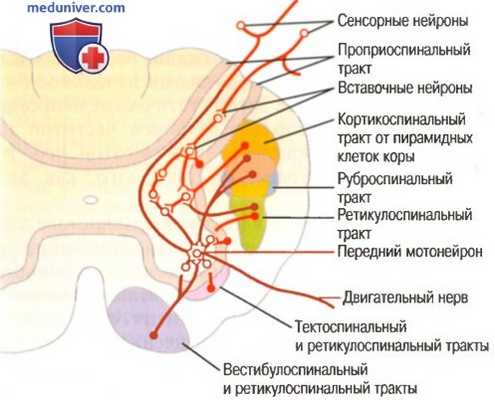
Конвергенция различных двигательных регуляторных путей на передних мотонейронах
б) Стимуляция спинальных мотонейронов. На рисунке выше показано поперечное сечение спинного мозга, демонстрирующее:
(1) множество моторных и сенсомоторных регулирующих трактов, входящих в этот сегмент спинного мозга;
(2) типичный передний мотонейрон в середине серого вещества переднего рога.
Кортикоспинальный и руброспинальный тракты лежат в задней части боковых столбов белого вещества. Эти волокна заканчиваются в основном на вставочных нейронах промежуточной области серого вещества спинного мозга.
В области шейного утолщения спинного мозга, где представлены нейроны, иннервирующие мышцы кисти и пальцы, большое число кортикоспинальных и руброспинальных волокон заканчиваются непосредственно на передних мотонейронах, таким образом обеспечивая прямой путь от головного мозга для активации мышечных сокращений. Это согласуется с тем фактом, что первичная моторная кора имеет очень высокую степень представительства для тонкой регуляции движений кистей, пальцев, и особенно — больших пальцев рук.
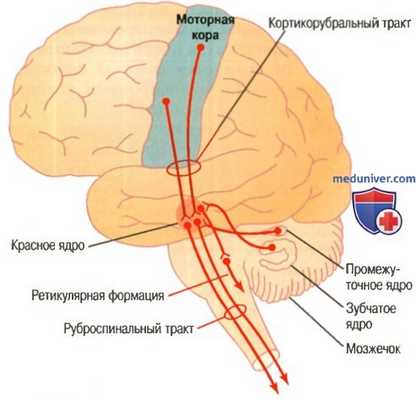
Кортикоруброспинальный путь двигательного контроля; показана также связь этого пути с мозжечком
в) Двигательные акты, возбуждаемые центрами спинного мозга. Спинной мозг может обеспечить некоторые специфические рефлекторные двигательные акты в ответ на стимуляцию сенсорных нервов. Многие из этих движений также важны при возбуждении передних мотонейронов спинного мозга сигналами из головного мозга. Например, рефлекс на растяжение осуществляется постоянно. Он помогает сглаживать любые осцилляции мышечных сокращений, инициируемых головным мозгом.
Вероятно, этот рефлекс обеспечивает также, по крайней мере частично, движущую силу, необходимую для вызова мышечных сокращений, если интрафузальные волокна мышечных веретен сокращаются сильнее, чем крупные волокна скелетных мышц. При этом возбуждается рефлекторное «самоусиление» стимуляции мышц в дополнение к их центральной стимуляции кортикоспинальными волокнами.
Кроме того, когда сигналы из головного мозга возбуждают мышцу, обычно нет необходимости посылать одновременно тормозные сигналы, расслабляющие мышцу-антагонист. Это достигается с помощью контура реципрокной иннервации, который всегда присутствует в спинном мозге для координации деятельности антагонистических пар мышц.
Наконец, командными сигналами из головного мозга могут активироваться любые другие рефлекторные механизмы спинного мозга, например рефлексы отдергивания, шагания на месте и ходьбы, чесания и поддержания позы. Таким образом, простые управляющие сигналы головного мозга могут инициировать много нормальных двигательных актов, особенно для таких функций, как ходьба и принятие телом различных поз.
Экстрапирамидная двигательная система. Нейроны двигательной системы
Термин «экстрапирамидная двигательная система» широко используют в клинических кругах для обозначения всех отделов головного мозга, которые участвуют в двигательном контроле, но не являются частью прямой кортикоспинальной пирамидной системы. Сюда входят пути через базальные ганглии, ретикулярную формацию ствола мозга, вестибулярные ядра и часто — через красные ядра.
Это всеобъемлющая и многообразная группа областей нервной системы, контролирующих двигательные функции, что так называемой экстрапирамидной системе как целостной системе трудно приписать специфические нейрофизиологические функции. По этой причине термин «экстрапирамидная двигательная система» все реже используют как в клинике, так и в физиологии.

а) Возбуждение двигательных областей спинного мозга первичной моторной корой и красным ядром. Нейроны моторной коры организованы в вертикальные колонки. В отдельных статьях на сайте (просим вас пользоваться формой поиска выше) указывалось, что клетки соматосенсорной и зрительной коры организованы в вертикальные колонки. Клетки моторной коры также собраны в вертикальные колонки, диаметр которых составляет долю миллиметра; одна колонка включает тысячи нейронов.
Каждая колонка клеток функционирует как единое целое, обычно стимулируя группу мышц-синергистов, а иногда лишь одну мышцу. Кроме того, как и вся кора большого мозга, колонка имеет 6 отдельных слоев клеток. Все пирамидные клетки, дающие начало кортикоспинальным волокнам, лежат в 5 слое клеток от поверхности коры, а сигналы входят в колонку через 2-4 слои; 6 слой дает начало основной части волокон, которые связывают колонку с другими регионами самой коры большого мозга.
б) Функция каждой колонки нейронов. Нейроны каждой колонки действуют как интегративная система обработки данных, использующая информацию от множества источников, на основании которой формируется ответ на «выходе» из колонки. Кроме того, каждая колонка может функционировать как усилительная система, стимулируя одновременно большое число пирамидных волокон, связанных с одной мышцей или с мышцами-синергистами.
Это важно, поскольку стимуляция одиночной пирамидной клетки редко может возбудить мышцу. Обычно для вызова сокращения определенной мышцы нужно, чтобы одновременно или в быстрой последовательности возбудились 50-100 пирамидных клеток.

в) Динамические и статические сигналы, передаваемые пирамидными нейронами. Если для запуска быстрого сокращения к мышце посылается сильный сигнал, то дальнейшее длительное поддержание сокращения может обеспечить гораздо более слабый продолжительный сигнал. Это обычный характер возбуждения, обеспечивающий мышечные сокращения.
Для этого каждая колонка клеток возбуждает две популяции пирамидных нейронов, одну из которых называют динамическими нейронами, а другую — статическими нейронами. В течение короткого периода в начале сокращения интенсивно возбуждаются динамические нейроны, вызывая начальное быстрое разбитие силы. Затем статические нейроны возбуждаются с гораздо меньшей частотой и, продолжая возбуждаться с этой частотой, поддерживают силу сокращения так долго, как это необходимо.
Нейроны красного ядра имеют подобные динамические и статические характеристики, за исключением того, что в красном ядре больше процент динамических нейронов, а в первичной моторной коре больше процент статических нейронов. Возможно, это объясняется тем, что красное ядро тесно связано с мозжечком, а мозжечок играет важную роль в быстрой инициации мышечного сокращения.
Введение в проблему регуляции мышечного тонуса. Спастичность.
Функция поддержания мышечного тонуса обеспечивается по принципу обратной связи на различных уровнях регуляции организма Периферическая регуляция осуществляется с участием гамма-петли, в состав которой входят супраспинальные моторные пути, вставочные нейроны, нисходящая ретикулярная система, альфа- и гамма-нейроны.
Существует два типа гамма-волокон в передних рогах спинного мозга. Гамма-1-волокна обеспечивают поддержание динамического мышечного тонуса, т.е. тонуса, необходимого для реализации процесса движения. Гамма-2-волокна регулируют статическую иннервацию мышц, т.е. осанку, позу человека. Центральная регуляция функций гамма-петли осуществляется ретикулярной формацией через ретикулоспинальные пути. Основная роль в поддержании и изменении мышечного тонуса отводится функциональному состоянию сегментарной дуги рефлекса растяжения (миотатического, или проприоцептивного рефлекса). Рассмотрим его подробнее.
Рецепторным элементом его является инкапсулированное мышечное веретено. Каждая мышца содержит большое количество этих рецепторов. Мышечное веретено состоит из интрафузальных мышечных волокон (тонких) и ядерной сумки, оплетенной спиралевидной сетью тонких нервных волокон, представляющих собой первичные чувствительные окончания (анулоспинальная нить). На некоторых интрафузальных волокнах имеются также и вторичные, гроздевидные чувствительные окончания. При растяжении интрафузальных мышечных волокон первичные чувствительные окончания усиливают исходящую из них импульсацию, которая через быстропроводящие гамма-1-волокна проводится к альфа-большим мотонейронам спинного мозга. Оттуда, через также быстропроводящие альфа-1-эфферентные волокна, импульс идет к экстрафузальным белым мышечным волокнам, которые обеспечивают быстрое (фазическое) сокращение мышцы. От вторичных чувствительных окончаний, реагирующих на тонус мышцы, афферентная импульсация проводится по тонким гамма-2-волокнам через систему вставочных нейронов к альфа-малым мотонейронам, которые иннервируют тонические экстрафузальные мышечные волокна (красные), обеспечивающие поддержание тонуса и позы.
Интрафузальные волокна иннервируются гамма-нейронами передних рогов спинного мозга. Возбуждение гамма-нейронов, передаваясь по гамма-волокнам к мышечному веретену, сопровождается сокращением полярных отделов интрафузальных волокон и растяжением их экваториальной части, при этом изменяется исходная чувствительность рецепторов к растяжению (происходит снижение порога возбудимости рецепторов растяжения, и усиливается тоническое напряжение мышцы).
Гамма-нейроны находятся под влиянием центральных (супрасегментарных) воздействий, передающихся по волокнам, которые идут от мотонейронов оральных отделов головного мозга в составе пирамидного, ретикулоспинального, вестибулоспинального трактов.
При этом если роль пирамидной системы заключается преимущественно в регуляции фазических (т.е. быстрых, целенаправленных) компонентов произвольных движений, то экстрапирамидная система обеспечивает их плавность, т.е. преимущественно регулирует тоническую иннервацию мышечного аппарата. Так, по мнению J. Noth (1991), спастичность развивается после супраспинального или спинального поражения нисходящих двигательных систем при обязательном вовлечении в процесс кортикоспинального тракта [2] .
В регуляции мышечного тонуса принимают участие и тормозные механизмы, без которых невозможно реципрокное взаимодействие мышц-антагонистов, а значит, невозможно и совершение целенаправленных движений. Они реализуются с помощью рецепторов Гольджи, расположенных в сухожилиях мышц, и вставочных клеток Реншоу, находящихся в передних рогах спинного мозга. Сухожильные рецепторы Гольджи при растяжении или значительном напряжении мышцы посылают афферентные импульсы по быстропроводящим волокнам 1б-типа в спинной мозг и оказывают тормозящее воздействие на мотонейроны передних рогов. Вставочные клетки Реншоу активизируются через коллатерали при возбуждении альфа-мотонейронов, и действуют по принципу отрицательной обратной связи, способствуя торможению их активности. Таким образом, нейрогенные механизмы регуляции мышечного тонуса многообразны и сложны.
При поражении пирамидного пути растормаживается гамма-петля, и любое раздражение путем растяжения мышцы приводит к постоянному патологическому повышению мышечного тонуса. При этом поражение центрального мотонейрона приводит к снижению тормозных влияний на мотонейроны в целом, что повышает их возбудимость, а так же на вставочные нейроны спинного мозга, что способствует увеличению числа импульсов, достигающих альфа-мотонейронов в ответ на растяжение мышцы [4].
В качестве других причин спастичности можно указать структурные изменения на уровне сегментарного аппарата спинного мозга, возникающие вследствие поражения центрального мотонейрона: укорочение дендритов альфа-мотонейронов и коллатеральный спрауттинг (разрастание) афферентных волокон, входящих в состав задних корешков.
Возникают так же и вторичные изменения в мышцах, сухожилиях и суставах. Поэтому страдают механико-эластические характеристики мышечной и соединительной ткани, которые определяют мышечный тонус, что еще больше усиливает двигательные расстройства.
В настоящее время повышение мышечного тонуса рассматривается как комбинированное поражение пирамидных и экстрапирамидных структур центральной нервной системы, в частности кортикоретикулярного и вестибулоспинального трактов. При этом среди волокон, контролирующих активность системы «гамма-нейрон – мышечное веретено», в большей степени обычно страдают ингибирующие волокна, тогда как активирующие сохраняют свое влияние на мышечные веретена.
Следствием этого является спастичность мышц, гиперрефлексия, появление патологических рефлексов, а также первоочередная утрата наиболее тонких произвольных движений [5].
Наиболее значимым компонентом мышечного спазма является боль. Болевая импульсация активирует альфа- и гамма-мотонейроны передних рогов, что усиливает спастическое сокращение мышцы, иннервируемой данным сегментом спинного мозга. В то же время, мышечный спазм, возникающий при сенсомоторном рефлексе, усиливает стимуляцию ноцицепторов мышцы. Так, по механизму отрицательной обратной связи формируется замкнутый порочный круг: спазм – боль – спазм – боль [3].
Помимо этого, в спазмированных мышцах развивается локальная ишемия, так как алгогенные химические вещества (брадикинин, простагландины, серотонин, лейкотриены и др.) оказывают выраженное действие на сосуды, вызывая вазогенный отек тканей. В этих условиях происходит высвобождение субстанции «Р» из терминалей чувствительных волокон типа «С», а также выделение вазоактивных аминов и усиление микроциркуляторных нарушений.
Интерес представляют также данные о центральных холинергических механизмах регуляции мышечного тонуса. Показано, что клетки Реншоу активируются ацетилхолином как через коллатерали мотонейрона, так и через ретикулоспинальную систему.
M.Schieppati и соавт., (1989) установили, что фармакологическая активация центральных холинергических систем значительно снижает возбудимость альфа-мотонейронов путем повышения активности клеток Реншоу.
В последние годы исследователи регуляции мышечного тонуса придают огромное значение роли нисходящих адренергических супраспинальных путей, начинающихся в области голубого пятна. Анатомически эти образования тесно связаны со спинальными структурами, особенно с передними рогами спинного мозга. Норадреналин, высвобождаемый с терминалей бульбоспинальных волокон, активизирует адренорецепторы, располагающиеся во вставочных нейронах, первичных афферентных терминалях и мотонейронах и воздействует одновременно на альфа- и бета-адренорецепторы в спинном мозге (D.Jones et al., 1982). К ядерным образованиям ретикулярной формации ствола подходят многочисленные аксоны болевой чувствительности. На основе информации, поступающей в ретикулярную формацию ствола головного мозга, выстраиваются соматические и висцеральные рефлексы. От ядерных образований ретикулярной формации формируются связи с таламусом, гипоталамусом, базальными ядрами и лимбической системой, которые обеспечивают реализацию нейроэндокринных и аффективных проявлений боли, что особенно важно при хронических болевых синдромах [2].
В итоге формирующийся порочный круг включает в себя мышечный спазм, боль, локальную ишемию, дегенеративные изменения, которые самоподдерживают друг друга, усиливая первопричину патологических изменений.
Следует учитывать, что чем больше компонентов этого порочного круга становятся мишенями при лечении, тем выше вероятность его успеха. Поэтому современными требованиями к миорелаксирующей терапии являются: мощность миорелаксирующего действия, его селективность, наличие противосудорожного и антиклонического эффектов, мощность анальгетического действия, а так же безопасность и наличие широкого терапевтического диапазона доз препарата.
Согласно современным представлениям, большинство миорелаксантов воздействуют на трансмиттеры или нейромодуляторы ЦНС. Воздействие может включать супрессию возбуждающих медиаторов (аспартат и глутамат) и/или усиление тормозных процессов (ГАМК, глицин). Далее
Читайте также:
- Примеры флюоресцентной ангиографии астроцитарной гамартомы сетчатки
- Гемангиоперицитома глазницы: признаки, гистология, лечение, прогноз
- Случай лечения рецидивирующего хронического цистита, ассоциированого с Escherichia coli
- Объективное исследование селезенки. Топография (расположение) селезенки
- Методы лечения карциноида и их эффективность
