Спонтанный бактериальный перитонит
Добавил пользователь Валентин П. Обновлено: 27.01.2026
Аннотация научной статьи по клинической медицине, автор научной работы — Лазебник Л. Б., Винницкая Е. В., Дроздов В. Н., Осипов Г. А., Петраков А. В.
Представлены результаты собственных исследований в сопоставлении с данными литературы по во- просам этиологии, патогенеза и диагностики спонтанного бактериального перитонита (СБП) при цир- розе печени (ЦП), осложненном асцитом. На основе полученных данных предложена дефиниция СБП. Выделены критерии ранней диагностики СБП на основе клинических проявлений бактериального перитонита, системного воспалительного ответа, результатов исследования асцитической жидкости (АЖ) с применением газовой хроматографии - масс-спектрометрии (ГХ-МС). В соответствии с пред- ложенными критериями разработана схема диагностики, лечения и профилактики СПБ. Приведены данные по эффективности терапии и профилактики СБП. Обозначены возможные основные перспек- тивные направления в лечении СБП при циррозе печени .
Похожие темы научных работ по клинической медицине , автор научной работы — Лазебник Л. Б., Винницкая Е. В., Дроздов В. Н., Осипов Г. А., Петраков А. В.
Конкурс по специальности «Гепатология», VIII съезд НОГР (первая премия спонтанный бактериальный перитонит: новые подходы к диагностике при алкогольном циррозе печени
Текст научной работы на тему «Спонтанный бактериальный перитонит: научно-практические достижения и перспективы»
№02/2011 ЭКСПЕРИМЕНТАЛЬНАЯ И КЛИНИЧЕСКАЯ
СПОНТАННЫЙ БАКТЕРИАЛЬНЫЙ ПЕРИТОНИТ: 5 НАУЧНО-ПРАКТИЧЕСКИЕ ДОСТИЖЕНИЯ И ПЕРСПЕКТИВЫ
1 ЛазебникЛ.Б.1, Винницкая Е.В.1, Дроздов В.Н.1, Осипов Г.А.2, Петраков А.В.1
£ 1 ГУ Центральный научно-исследовательский институт гастроэнтерологии ДЗ г. Москвы
s 2 Научный центр сердечно-сосудистой хирургии им. А. Н. Бакулева РАМН
* Винницкая Елена Владимирована
| 111123, Москва, ш. Энтузиастов, д. 86
Представлены результаты собственных исследований в сопоставлении с данными литературы по вопросам этиологии, патогенеза и диагностики спонтанного бактериального перитонита (СБП) при циррозе печени (ЦП), осложненном асцитом. На основе полученных данных предложена дефиниция СБП. Выделены критерии ранней диагностики СБП на основе клинических проявлений бактериального перитонита, системного воспалительного ответа, результатов исследования асцитической жидкости (АЖ) с применением газовой хроматографии — масс-спектрометрии (ГХ-МС). В соответствии с предложенными критериями разработана схема диагностики, лечения и профилактики СПБ. Приведены данные по эффективности терапии и профилактики СБП. Обозначены возможные основные перспективные направления в лечении СБП при циррозе печени.
Ключевые слова: спонтанный бактериальный перитонит; цирроз печени; системная воспалительная реакция; сепсис; патогенез; критерии диагностики; лечение; профилактика.
We presented the results of our research in comparison with the literature on the etiology, pathogenesis and diagnosis of spontaneous bacterial peritonitis (SBP) at liver cirrhosis (LC), complicated by ascites. Based on these data, was proposed a classification of SBP. Were identified criteria for early diagnosis of SBP on the basis of clinical manifestations of bacterial peritonitis, systemic inflammatory response, results of studies of ascitic fluid (AF) using gas chromatography — mass spectrometry (GC-MS). In accordance with the proposed criteria was proposed a scheme for the diagnosis, treatment and prevention of STDs. Presents data on the effectiveness of therapy and prevention of SBP. Denote the potential major long-term trends in the treatment of SBP in cirrhosis. Keywords: spontaneous bacterial peritonitis; cirrhosis; systemic inflammatory response; sepsis; pathogenesis; diagnostic criteria; treatment; prevention.
Спонтанный бактериальный перитонит — прогностически тяжелое полиэтиологическое осложнение декомпенсированного цирроза печени, развивающееся в результате транслокации кишечной флоры, на фоне портальной гипертензии и избыточного бактериального роста, характеризующееся воспалением брюшины и контаминацией асцитической жидкости, синдромом системной воспалительной реакции (ССВР) с последующим развитием сепсиса и полиорганной недостаточности. Основной отличительной характеристикой СБП является воспаление висцеральной и париетальной брюшины без нарушения целостности внутренних органов и тяжелых воспалительных процессов брюшной
полости и малого таза, не требующее хирургического вмешательства [1].
Данные по частоте этого осложнения ЦП противоречивы: по различным наблюдениям, СБП составляет от 8 до 31% общего числа больных ЦП, наблюдающихся стационарно 5.
В 1960-е годы, когда СБП впервые был описан Гарольдом Конном [1], летальность при этом осложнении составляла около 90%. Отсутствие правильной диагностики, своевременной и адекватной терапии приводило к неоправданно высокой смертности. В последующие годы смертность от СБП в условиях стационара снизилась, по данным разных авторов, до 20-38% [3; 5; 7].
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ СПБ
В основе патогенетических механизмов СБП
лежит теория бактериальной транслокации. Суть этого явления заключается в проникновении жизнеспособных бактерий (представителей резидентной флоры) через эпителиальный барьер желудочно-кишечного тракта в экстраинтестиналь-ные, обычно стерильные, ткани макроорганизма, например мезентериальные лимфоузлы, селезенку, где часть из них подвергается лизису макрофагами, часть — через воротную вену попадает в печеночные синусы и лизируется макрофагами печени [8]. Наряду с бактериями во внутреннюю среду проникают эндотоксины и частицы микробных клеток. В патогенезе СБП, как и любого другого инфекционного процесса, ведущую роль играет взаимодействие трех факторов: болезнетворных качеств микроба, количества микробов и защитных механизмов организма.
РОЛЬ ПАТОГЕННОСТИ МИКРООРГАНИЗМОВ
Особое значение в развитии болезни имеют факторы патогенности и вирулентности аэробных и анаэробных микроорганизмов. Резидентную флору относят к слабопатогенной. Для процессов, вызываемых нормальной микрофлорой, характерны или отклонения от типичной клинической картины заболевания, или трудности при определении нозологической формы, к которой его можно отнести. Это положение в особенности применимо к СБП.
Этиологическая структура. В литературе имеются описания СБП, вызванные почти всеми известными бактериями. Согласно многочисленным клиническим микробиологическим исследованиям, наиболее часто при СБП в АЖ выявляются следующие микроорганизмы: Escherichia coli (по данным ряда авторов, до 70% случаев), несколько реже — Streptococci, Staphylococci, реже — Klebsiella oxytoca, Salmonella enteritidis, Enterococcus faecium, Acinectobacter anitratus. Описаны единичные случаи заболевания туберкулезной и грибковой (Cryptococcus neoformans) этиологии.
РОЛЬ КОЛИЧЕСТВА МИКРОБОВ (ИЗБЫТОЧНОГО БАКТЕРИАЛЬНОГО РОСТА)
Количество микроорганизмов, необходимых для развития заболевания, называют «критическим числом». В медицинской практике данные о «критическом числе» как при клинически выраженных проявлениях, так и при невыраженных инфекциях отсутствуют. Доказана прямая зависимость уровня транслокации бактерий от уровня их популяции в кишечнике. С этой точки зрения особенно велика роль синдрома избыточного бактериального роста при ЦП.
При декомпенсированном ЦП класса В и С по Child-Pugh возникает целый ряд взаимосвязанных механизмов, нарушающих нормальные функции организма и способствующих бактериальной кишечной транслокации и развитию СБП. Это портальная гипертензия, асцит, повышение внутри-брюшного давления, замедление пассажа содержимого по кишечнику, синдром избыточного бактериального роста, снижение белково-синтетической функции печени, белковое голодание, снижение общей иммунореактивности, энтеральной недостаточности, эндотоксемии, а также локальные изменения слизистой кишки в виде нарушения микроциркуляции и проницаемости [4; 9; 10].
Важную роль в развитии СБП играет вну-трибрюшная гипертензия (ВБГ), которая возрастает при декомпенсации ЦП за счет портальной гипертензии и асцита, с одной стороны, и развития синдрома избыточного бактериального роста — с другой. Увеличение ВБГ замедляет кровоток по нижней полой вене и уменьшает венозный возврат, способствует снижению лимфооттока по грудному лимфатическому протоку, замедлению обратного всасывания АЖ.
Наличие ЦП, класса В и С по СЫЫ-Р^^ с нарушением функции печени, сопровождается как снижением белково-синтетической функции, так и нарушением функции ретикуло-эндотелиальной системы, что приводит к снижению способности к образованию антител и формированию вторичного иммунодефицита.
Доказано, что активированные микроорганизмами нейтрофилы, моноциты, макрофаги и клетки эндотелия продуцируют провоспалительные медиаторы — цитокины (ЦК), кинины, метаболиты арахидоновой кислоты, фактор активации тромбоцитов и оксид азота, которые инициируют и поддерживают воспалительную реакцию, вызывают вторичное выделение аналогичных медиаторов с повреждением эндотелия и снижением органной перфузии и доставки кислорода. В этих условиях печень вместо синтеза альбумина, который и так резко снижен при декомпенсированном ЦП, начинает продуцировать белки острой фазы, такие как гли-копротенины, а1-антитрипсин, С-реактивный белок, церулоплазмин, факторы свертывания, компоненты комплемента, ферритин — вещества, которые, обладая различным действием, способствуют усилению процессов свертывания, воспаления, нарушению метаболизма [4; 9-11].
Кроме того, при СБП в итоге происходит снижение функции нейтрофилов, нарушение синтеза лейкотриена, супероксидного аниона, тромбоци-тактивирующего фактора.
Контроль за реализацией иммунной и воспалительной реактивности осуществляется системой
Спонтанный бактериальный перитонит
Е.В. ВИННИЦКАЯ, старший научный сотрудник отделения хронических заболеваний печени Центрального научно-исследовательского института гастроэнтерологии Департамента здравоохранения г. Москвы, доктор медицинских наук
Грозное последствие цирроза
Спонтанный бактериальный перитонит (СБП) остается часто встречающимся, но редко диагностируемым осложнением цирроза печени (ЦП). Уточню, что СБП— это прогностически тяжелое осложнение декомпенсированного ЦП. Оно развивается в результате бактериальной транслокации на фоне снижения резистентности организма, избыточного бактериального роста. СБП проявляется контаминацией асцитической жидкости и воспалением брюшины. Частота этого грозного осложнения за последние годы колеблется в пределах от 10 до 37% среди стационарных больных ЦП, осложненным асцитом.
В 1960 годы летальность при этом осложнении составляла около 90%. Отсутствие понимания, правильной диагностики, своевременной и адекватной терапии приводило к неоправданно высокой смертности. В последующие годы смертность от СБП в условиях стационара снизилась до 20—38%.
По своей сути спонтанный бактериальный перитонит — это частная форма первичного асцита-перитонита. Этот термин отражает острое или хроническое воспаление брюшины у больного с асцитом и инфицированием асцитической жидкости, сопровождающееся местными и общими симптомами и нарушением жизненно важных функций организма.
Бактерии проникают через барьер
В основе патогенетических механизмов СБП лежит теория бактериальной транслокации. Суть этого явления заключается в проникновении жизнеспособных бактерий через эпителиальный барьер ЖКТ в экстраинтестинальные ткани организма, например мезентериальные лимфоузлы, селезенку. Там часть из них подвергается лизису макрофагами, часть — через воротную вену попадает в печеночные синусы и лизируется макрофагами печени.
Особое значение в развитии болезни играют факторы патогенности и вирулентности микроорганизмов. К ним относят: факторы адгезии и колонизации, факторы инвазии, факторы, препятствующие фагоцитозу, ферменты «защиты и агрессии» бактерий, а также эндотоксины. Наиболее часто при СБП в асцитической жидкости выявляются следующие микроорганизмы: Escherichia сoli, несколько реже — Streptococci, Staphylococci, реже — Klebsiella oxytoca, Salmonella enteritidis, Enterococcus faecium, Acinectobacter anitratus.
При декомпенсированном ЦП классов В и С по Child-Pugh возникает целый ряд взаимосвязанных механизмов, нарушающих нормальные функции организма, способствующих бактериальной кишечной транслокации и развитию СБП. Это портальная гипертензия, асцит, повышение внутрибрюшного давления, замедление пассажа содержимого по кишечнику, синдром избыточного бактериального роста, снижение белково-синтетической функции печени, белковое голодание, снижение общей иммунореактивности, энтеральной недостаточности, эндотоксемии, а также локальные изменения слизистой кишки в виде нарушения микроциркуляции и проницаемости.
Важную роль в развитии СБП имеет внутрибрюшная гипертензия (ВБГ), которая возрастает при декомпенсации ЦП за счет портальной гипертензии и асцита, с одной стороны, и развития синдрома избыточного бактериального роста— с другой. Увеличение ВБГ замедляет кровоток по нижней полой вене и уменьшает венозный возврат, способствует снижению лимфооттока по грудному лимфатическому протоку, замедляет всасывание асцитической жидкости. Транслокация бактерий формируется по прошествии 3 часов после повышения внутрибрюшного давления до 15 мм рт. ст. А транслокация бактерий при внутрибрюшном давлении > 25 мм рт. ст. развивается в течение часа.
Наличие ЦП классов В и С по Child-Pugh с нарушением функции печени, сопровождается снижением как белково-синтетической функции, так и нарушением функции ретикуло-эндотелиальной системы, что приводит к снижению способности образования антител и формированию вторичного иммунодефицита.
Доказано, что активированные микроорганизмами нейтрофилы, моноциты, макрофаги и клетки эндотелия продуцируют провоспалительные медиаторы — цитокины, кинины, метаболиты арахидоновой кислоты, фактор активации тромбоцитов и оксид азота, которые инициируют и поддерживают воспалительную реакцию, вызывают вторичное выделение аналогичных медиаторов с повреждением эндотелия и снижением органной перфузии и доставки кислорода. В этих условиях печень вместо синтеза альбумина, который и так резко снижен при декомпенсированном ЦП, начинает продуцировать белки острой фазы, такие как гликопротеины, ?1-антитрипсин, С-реактивный белок, церулоплазмин, факторы свертывания, компоненты комплемента, ферритин — вещества, которые, обладая различным действием, способствуют усилению процессов свертывания, воспаления, нарушению метаболизма.
Кроме того, при СБП в итоге происходит снижение функции нейтрофилов, нарушение синтеза лейкотриена, супероксидного аниона, тромбоцитоактивирующего фактора.
Контроль за реализацией иммунной и воспалительной реактивности осуществляется системой цитокинов. Именно баланс взаимоотношений между про- и антивоспалительными медиаторами, при физиологических условиях, способствует созданию условий для уничтожения патогенов и поддержания гомеостаза. При нарушении баланса цитокиновой системы превалируют деструктивные эффекты медиаторов воспаления. Концентрация отдельных провоспалительных цитокинов в крови в норме обычно не превышает 5—20 пкг/мл, может возрастать в 5—10 и более раз, все это приводит к нарушению проницаемости и функции эндотелия капилляров, запуску синдрома ДВC (диссеминированное внутрисосудистое свертывание крови), формированию отдаленных очагов системного воспаления.
Осложнение распознается с трудом
СБП представляет трудно разрешимую диагностическую задачу для клинициста и является одним из наиболее тяжелых и трудно распознаваемых осложнений декомпенсированного ЦП.
Очень редко заболевание дебютирует картиной септического шока, проявляющегося снижением АД ниже 90 мм рт. ст., тахикардией более 100 ударов в 1 мин, олигурией менее 20 мл в 1 час. Многие авторы подразделяют симптомы СБП на местные (боль в животе, рвота, диарея, признаки пареза кишечника) и системные проявления инфекции: лихорадка (повышение температуры выше 37,4 ?С), лейкоцитоз (повышение числа лейкоцитов выше 10 х 109 кл/л), а также энцефалопатия, быстро нарастающая печеночная недостаточность, гепаторенальный синдром. Почечная недостаточность является одним из наиболее грозных осложнений, в значительной степени определяющих прогноз. В связи с этим любое клиническое ухудшение у больного ЦП, осложненным отечно-асцитическим синдромом, может являться следствием СБП.
Диагностика СБП многие годы основывалась на выявлении микроорганизмов в асцитической жидкости с использованием посева на специальные среды. В литературе широко обсуждался вопрос о целесообразности и безопасности диагностического парацентеза при отсутствии подозрений на СБП. До настоящего времени обязательным в диагностике СБП считается исследование асцитической жидкости с проведением подсчета числа полиморфноядерных лейкоцитов (ПЯЛ), определение содержания белка, концентрации альбумина, посева асцитической жидкости на культуральные среды.
Перед диагностическим парацентезом, как правило, проводится УЗИ, при котором в асцитической жидкости могут быть визуализированы нити фибрина, взвесь. При бактериальном перитоните вне зависимости от этиологии увеличивается количество и калибр взвешенных частиц, выявляются множественные нити фибрина, свободно колеблющиеся в асцитической жидкости в такт дыхательным движениям.
«Золотым стандартом» диагностики СБП считается способ определения возбудителей инфекционного процесса с использованием посева асцитической жидкости на питательные среды для выявления роста микроорганизмов с последующей идентификацией в чистой культуре. Бесспорным достоинством метода является его абсолютная специфичность. Однако чувствительность культурального метода не превышает 25—42%, естественно, что отрицательные результаты посева не могут гарантировать отсутствия бактериемии.
В общепринятой клинической практике диагностика СБП основывается на количественном определении содержания нейтрофилов в асцитической жидкости и результатах культурального метода. В соответствии с международными рекомендациями достаточным для постановки диагноза СБП является количество ПЯЛ, равное 250 кл/мм?.
В зависимости от числа нейтрофилов и идентификации возбудителей инфекции выделяют 3 формы проявления СБП:
I — классический, полный вариант СБП. Асцитическая жидкость содержит более 250 ПЯЛ на мм?, дает рост культуры при высевании. Такое сочетание определяет назначение антибактериальной терапии.
II — культуро-негативный нейтрофильный асцит, когда асцитическая жидкость содержит более 250 ПЯЛ на мм?, не дает ростa культуры при высевании. Это состояние также требует обязательного проведения антибактериальной терапии.
III — культуропозитивный асцит с низким содержанием нейтрофилов. Асцитическая жидкость содержит менее 250 ПЯЛ на мм?, дает рост культуры при высевании.
Однако пока остается неясным, какова правильная тактика по отношению к той группе больных, где имеет место клиническая картина СБП, но отсутствует нейтрофилез в асцитической жидкости, а посев жидкости и крови не дает роста, поскольку совершенно очевидно, что такие больные вызывают тревогу у врачей и требуют особой клинической настороженности. Низкая чувствительность метода культивирования асцитической жидкости на средах не позволяет исключить и так называемый IV вариант течения СБП — ложнокультуронегативный с низким содержанием нейтрофилов и наличием клинической картины СБП.
Амилаза и липаза — важные критерии
Дифференциальная диагностика СБП основана на исключении перитонита вторичного генеза, определении основного заболевания, вызвавшего асцит, исключении асцита смешанного генеза, определении наличия инфицированности асцитической жидкости. Наиболее часто у больных с декомпенсированным ЦП проводится дифференциальный диагноз между СБП и вторичными перитонитами, среди которых наиболее часто встречается панкреатит, а также туберкулез. Во многом это связано с тем, что большая часть больных СБП страдает ЦП алкогольной этиологии, хроническим панкреатитом, туберкулезом.
Инфекционные осложнения с поражением поджелудочной железы и забрюшинного пространства развиваются у 40—70% больных панкреонекрозом. Особенно трудна диагностика панкреонекроза у больных с ЦП алкогольной этиологии с транзиторным асцитом, продолжающих злоупотребление алкоголем, когда нарастание асцита может ошибочно расцениваться как проявление отечно-асцитического синдрома. Основными клинико-морфологическими формами панкреатической инфекции являются инфицированный панкреонекроз и панкреатогенный абсцесс, нагноение псевдокисты поджелудочной железы.
Важными диагностическими критериями является повышение уровня амилазы и липазы в асцитической жидкости. В качестве критерия инфицированности применяется определение С-реактивного белка, прокальциотонина.
Во всех случаях необходима оценка клинической картины заболевания, с учетом причин, которые могут вызвать перитонит у больных и без асцита. Число нейтрофилов в асцитической жидкости, как правило, в этих случаях превышает 500 кл/мм3. Наиболее характерным является повышение уровня лактатдегидрогеназы >225 mU/L, общего белка >1 г/дл, снижения глюкозы до 50 мг/дл. По данным УЗИ при вторичном перитоните значительно чаще, чем при СБП, выявляются множественные нити фибрина. Решающее значение в этих случаях имеет лапароскопия.
В дифференциальной диагностике первичного и вторичного бактериальных перитонитов всегда стоит вопрос о целесообразности проведения диагностической лапаротомии или лапароскопии. Хорошо известно, что при ЦП с осложненным течением внутрибрюшные хирургические вмешательства часто имеют неблагоприятный исход. Оперативное вмешательство, даже малоинвазивное, целесообразно только при подозрении на ургентную патологию, поскольку может осложнять течение СБП, приводить к острой печеночной недостаточности.
Международный клуб асцита рекомендует
В соответствии с Рекомендациями Международного клуба асцита подходы к лечению больного с СБП при ЦП могут быть представлены следующим образом. Необходимы, во-первых, антибактериальная терапия, во-вторых, парацентез с возмещением объема плазмы альбумином, в-третьих, лечение и профилактика осложнений.
Антибактериальную эмпирическую терапию проводят цефалоспоринами III поколения (цефотаксим, цефтизоксим, цефтазидим, цефоницид). Наиболее хорошо изученный и часто применяемый препарат из этой группы цефотаксим назначается каждые 12 часов в течение 5 дней в/в, минимальная разовая доза 2 г. Амоксициллин/клавунат калия по эффективности сравним с цефотаксимом, применяется в/в 1,2 г каждые 6 часов в течение 5—7 дней.
Точка зрения на выбор антибиотиков первой линии на сегодняшний день неоднозначна, что связано с ростом резистентности микроорганизмов к антибиотикам. Больным неосложненным СБП (при отсутствии шока, илеуса, гастроинтестинального кровотечения, выраженной печеночной энцефалопатии или повышения сывороточного креатинина более 3 мг/дл), не получавшим ранее профилактически фторхинолоны, может быть рекомендован офлоксацин внутрь в дозе не менее 400 мг каждые 12?часов. Есть исследования, указывающие, что по эффективности применение таблетированного ципрофлоксацина по 500 мг каждые 12 часов не уступает по эффективности цефотаксиму и цефтриксону и даже превосходит их по эффективности в лечении СБП.
В соответствии с международными рекомендациями эффективность проведения адекватной антибактериальной терапии достигает 90%, и она оценивается по снижению содержания ПЯЛ менее 250 кл/мм3 в асцитической жидкости, по исчезновению местных и системных проявлений инфекции.
Оптимальным критерием эффективности считается снижение числа ПЯЛ в асцитической жидкости через два дня от начала антибактериальной терапии по сравнению с исходными показателями. В связи с этим в ходе терапии рекомендуется проводить хотя бы один повторный парацентез через 48 часов от начала терапии. Критериями же неэффективности считается ухудшение состояния в течение первых часов антибактериальной терапии, а также снижение числа ПЯЛ в асцитической жидкости менее чем на 25%.
При отсутствии эффекта от антибактериальной терапии рекомендуется смена антибиотика с учетом чувствительности микрофлоры или эмпирически при отрицательных результатах посева, а также необходимо проведение более тщательной дифференциальной диагностики с вторичным перитонитом.Парацентез с возмещением объема плазмы альбумином рекомендуется к применению при лечении рефрактерных асцитов. Взгляд на эффективность и безопасность этой методики у пациентов с СБП остается спорным.
Непреложной истиной является необходимость проведения мероприятий, направленных на предупреждение и лечение осложнений ЦП, являющихся факторами риска СБП, первичную профилактику СБП.
В настоящее время большие рандомизированные исследования показали высокую эффективность непрерывной профилактики СБП с применением фторхинолонов у больных ЦП, перенесших СБП. В соответствии с Международными рекомендациями профилактика возвратного бактериального перитонита проводится непрерывно норфлоксацином по 400 мг/сут. В связи с низкой выживаемостью после первого эпизода спонтанного перитонита, которая в течение первого года составляет 30—50%, а в течение второго всего 25—30%, рекомендуется рассматривать таких пациентов в качестве кандидатов на трансплантацию печени.
Спонтанный бактериальный перитонит при циррозе является распространенным осложнением, характеризуется высокой смертностью, поздней выявляемостью. Существующие методы диагностики являются либо недостаточно чувствительными, либо обладают низкой специфичностью, сложны в практическом применении, длительны по срокам выполнения. Все это делает актуальными проблемы поиска и разработки новых методов диагностики, лечения и профилактики подобного заболевания.
В связи с расширением представлений о патогенезе спонтанного бактериального перитонита, позволяющим оценить роль избыточного бактериального роста, процессов микробной транслокации, обоснован интерес гепатологов к бактериальным препаратам пробиотикам и эубиотикам в аспекте лечения этого заболевания.
«Золотым стандартом» диагностики СБП считается способ определения возбудителей инфекционного процесса с использованием посева асцитической жидкости на питательные среды для выявления роста микроорганизмов с последующей идентификацией в чистой культуре. Бесспорным достоинством метода является его абсолютная специфичность.
Диагностика вторичного бактериального перитонита требует срочного хирургического вмешательства.
Спонтанный бактериальный перитонит (СБП)
СБП представляет собой инфицирование асцитической жидкости без наличия очевидного источника. Клинические проявления могут включать в себя лихорадку, слабость, симптомы, сопряженные с наличием асцита, и усиление печеночной недостаточности. Диагноз основывается на результатх исследования асцитической жидкости. Лечение проводится цефотаксимом или другим антибиотиком.
СБП особенно часто встречается при асците, вызванным цирозом печени Цирроз печени Цирроз – финальная стадия печеночного фиброза, который приводит распространенному нарушению печеночной архитектоники. Цирроз характеризуется образованием узлов регенерации, окруженных плотной. Прочитайте дополнительные сведения . Эта инфекция может привести к серьезным осложнениям или смерти. Чаще всего СБП вызывается грамнегативными бактериями Escherichia coli и Klebsiella pneumoniae и грамположительными бактериями Streptococcus pneumoniae, обычно в патологический процесс вовлечен только один микроорганизм.
Симптомы и признаки СБП
Признаки СБП могут включать лихорадку, энцефалопатию, ухудшение степени печеночной недостаточности и необъяснимое общее ухудшение в состоянии пациента. Перитонеальные знаки (например, напряженность брюшной стенки и симптом Щеткина), как правило, имеются, но могут быть выражены слабее из-за наличия асцитической жидкости.
Диагностика СБП
Клиническая диагностика СБП может быть затруднена; она требует весомого клинического обоснования и свободного применения диагностического парацентеза, включающего посев культуры. Помещение асцитической жидкости в емкость с культурой перед инкубацией повышает чувствительность метода почти до 70%. Количество полиморфноядерных лейкоцитов (PMNs) > 250 клеток/мкл (0,25 х 10 9 /л) является диагностическим показателем СБП. Количество ПМЯ - это общее количество лейкоцитов в жидкости, полученной при асците Асцит Асцит – это наличие свободной жидкости в брюшной полости. Наиболее частой причиной асцита служит портальная гипертензия. Симптомы обычно обусловлены растяжением брюшной полости. Диагноз основывается. Прочитайте дополнительные сведения на процент нейтрофилов. Также показаны исследования культуры крови. Так как СБП обычно возникает от одного микроорганизма, обнаружение смешанной флоры в асцитической жидкости предполагает перфорирование органа брюшной полости или заражение образца.
Лечение СБП
Цефотаксим или другие антибиотики
Альбумин для предотвращения гепаторенальный синдром
Если диагностирован СБП, антибиотик, например, цефтриаксон или цефотаксим назначается в дозе 2 г внутривенно через каждые 4–8 часов (пока ожидаются результаты окраски по Граму и посева на культурные среды) в течение как минимум 5 дней, пока анализ асцитической жидкости не покажет 250 полиморфоядерных лейкоцитов/мкл. Антибиотики увеличивают шанс выживания. Так как СБП рецидивирует в течение года почти у 70% пациентов, показано профилактическое назначение антибиотиков; хинолонов (например, норфлоксацина 400 мг/день), что широко используется в клинической практике.
Профилактическое назначение антибиотиков пациентам с асцитом и кровотечением из варикозно расширенных вен пищевода снижает риск развития СБП.
Авторское право © 2022 Merck & Co., Inc., Rahway, NJ, США и ее аффилированные лица. Все права сохранены.
Спонтанный бактериальный перитонит
Спонтанный бактериальный перитонит (англ. spontaneous bacterial peritonitis, SBP) — воспаление брюшной полости (перитонит) бактериальной природы при отсутствии очевидного источника инфекции. Спонтанный бактериальный перитонит происходит почти исключительно у пациентов с портальной гипертензией (повышение давления в системе воротной вены), и, чаще всего, как осложнение цирроза печени. Спонтанный бактериальный перитонит также встречается у пациентов с нефротическим синдромом.
Диагноз устанавливается на основе исследования взятой из брюшной полости жидкости (называемой асцитической). Если асцитическая жидкость содержит бактерии или более 250 клеток в мм 3 нейтрофильных гранулоцитов (тип белых кровяных клеток), то инфекция подтверждается.
Спонтанный бактериальный перитонит является наиболее частым инфекционным осложнением цирроза. Его выявляют у 8–32% больных. Общая смертность в течение первого года после первого эпизода спонтанного бактериального перитонита достигает 61–78%, что в немалой степени обусловлено преимущественным развитием данного осложнения на фоне декомпенсированного цирроза с высоким риском летального исхода от прогрессирующей печеночной недостаточности или кровотечения. В то же время адекватные профилактические и лечебные мероприятия позволяют ликвидировать непосредственную угрозу жизни у большинства больных (А.О. Буеверов).
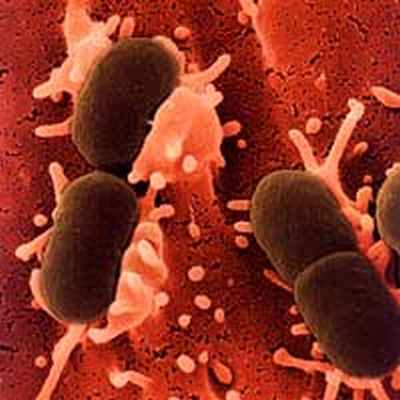 |
| Кишечная палочка (Escherichia coli) — наиболее частый возбудитель спонтанного бактериального перитонита |
Больному назначают антибиотик из группы цефалоспоринов 3-го поколения цефотаксим по 2 г 2 раза в сутки в течение 7 дней и вводят настои альбумина.
Лечение антибиотиками при спонтанном бактериальном перитоните у людей с прогрессирующим заболеванием печени
Найти наилучший доступный антибиотик для спонтанного бактериального перитонита (накопление жидкости в животе (брюшной полости), инфицированной бактериями) у людей с прогрессирующим заболеванием печени (цирроз печени или поздняя стадия рубцевания печени с осложнениями). Патологическое накопление жидкости у людей с циррозом печени называют асцитом. Иногда эта жидкость может быть инфицирована бактериями, без очевидного источника инфекции. Это называют "спонтанным бактериальным перитонитом". Основным методом лечения при спонтанном бактериальном перитоните являются антибиотики, но неясно, какой антибиотик лучше всего подходит для его лечения. Авторы собрали и проанализировали все подходящие исследования для ответа на этот вопрос и нашли 12 рандомизированных клинических испытаний (участники получали лечение, основанное на методе, похожем на «подбрасывание монеты», это гарантирует, что люди, которые получают различное лечение, схожи во всех аспектах, кроме лечения, таким образом любые различия между результатами лечения могут быть отнесены скорее к лечению, чем к различиям между типами людей, которые получали лечение). При анализе данных авторы использовали стандартные Кокрейновские методы, которые позволяют сравнивать два вида лечения одновременно. Авторы также использовали прогрессивные методы, которые позволяют сравнивать множество вариантов лечения одновременно (так называемый «сетевой мета-анализ» или «множественные сравнения видов лечения»). Цель обзора состоит в том, чтобы собрать надежные доказательства об относительной пользе и вреде различных видов антибиотиков.
Дата поиска литературы
Ноябрь 2018 года.
Ключевая информация
Ни одно из исследований не было проведено без недочетов, и из-за очень низкой определенности в результатах авторы не могут предположить, какой антибиотик, назначаемый отдельно или в комбинации, для устранения бактерий из живота, лучше или хуже других антибиотиков при лечении спонтанного бактериального перитонита.
Источник финансирования был неясен в 10 исследованиях; промышленные организации финансировали два исследования.
Что было изучено в этом обзоре?
В этом обзоре изучали людей разного пола, возраста и происхождения, с прогрессирующим заболеванием печени различной этиологии, у которых развился спонтанный бактериальный перитонит. Людям назначали различные антибиотики при лечении спонтанного бактериального перитонита. Авторы исключили исследования с участниками, перенесшими трансплантацию печени, и бактериальным перитонитом вследствие других причин. Возраст участников, когда это сообщалось, колебался от 42 до 60 лет. Число женщин, когда это сообщалось, варьировало от 18 до 42 из 100. Назначаемые группы антибиотиков представляли собой цефалоспорины, пенициллины и хинолоны. Авторы обзора планировали собрать и проанализировать данные о смертности, качестве жизни, серьезных и несерьезных осложнениях, времени до трансплантации печени (замена больной печени здоровой), времени до исчезновения спонтанного бактериального перитонита и исчезновения симптомов.
Каковы основные результаты этого обзора?
12 исследований включали небольшое число участников (1278 участников). Данные исследований были скудными; данные для анализа были получены из 10 исследований с 893 участниками. Период наблюдения в испытаниях варьировал от одной недели до трех месяцев. Этот обзор показывает следующее.
- Из 13 различных антибиотиков, сравниваемых в клинических испытаниях, цефтриаксон и цефотаксим для внутривенного введения использовали наиболее часто.
- Тип антибиотика, возможно, не влияет на число или процент людей с серьезными осложнениями или с любыми осложнениями; число (любых) осложнений на человека; процент людей, перенесших трансплантацию печени; или тех, кто выздоровел от спонтанного бактериального перитонита по данным лабораторных тестов или других осложнений цирроза печени.
- Двадцать пять из каждых 100 человек умерли в течение трех месяцев, и 75 из каждых 100 человек выздоровели от спонтанного бактериального перитонита.
- Ни в одном из испытаний не сообщали о качестве жизни, связанном со здоровьем, числе серьезных неблагоприятных событий или симптоматическом восстановлении после спонтанного бактериального перитонита.
- У нас очень низкая уверенность в общих результатах. Могут ли некоторые антибиотики привести к значимой или менее значимой пользе или вреду по сравнению с другими, когда их назначают людям с прогрессирующим заболеванием печени и спонтанным бактериальным перитонитом, остается неясным.
- Нам необходимы данные из клинических испытаний надлежащего дизайна и качества, чтобы выявить лучший антибиотик при спонтанном бактериальном перитоните.
Читайте также:
