Тактика при хронической эмпиеме плевры. Лечение бронхиальных свищей
Добавил пользователь Cypher Обновлено: 07.01.2026
Заболевание пищевода, сопровождающееся воспалением его слизистой оболочки.
Диагностика:
- эзофагогастродуоденоскопия;
- эзофагогастродуоденоскопия с биопсией.
Тромбозы и эмболии артерий - внезапная закупорка магистральных сосудов. Мгновенное прекращение доставки крови к органу приводит к гибели органа и запускает механизмы, приводящие к гибели всего организма. Тромбозом магистральной артерии называется образование тромба на измененной стенке артерии с закупоркой просвета сосуда. Основной причиной тромбоза является атеросклероз при котором изменение сосудистой стенки ведет к турбуленции крови, склеиванию эритроцитов и тромбоцитов и оседанию их на стенке. Эмболия это перенос током крови организованного тромба из другой области (сердца или аорты) в другой сосуд и закупоркой его.
Наиболее часто эмболии случаются при болезнях сердца (инфаркт миокарда, мерцательная аритмия, инфекционное поражение сердечных клапанов) и при расширении крупных сосудов - аневризмах. При попадании его в мозговые сосуды развивается инсульт, в кишечник - мезентериальный тромбоз, в руку или ногу - гангрена. При тромбозе или эмболии, нормальное кровоснабжение в бассейне закупоренного сосуда внезапно прекращается и развивается патологическое состояние называемое острой ишемией. При ишемии кислородный голод приводит к прекращению функционирования, а в последующем, и гибели тканей пораженного органа. Выключение функции начинается с нервной ткани. При этом вначале происходит ее раздражение, что приводит к сильной боли, затем прекращается проведение нервного импульса - исчезает чувствительность, конечность "деревенеет". В итоге развивается паралич мышц - активные движения прекращаются.После гибели нервной ткани наступает умирание мышечной ткани. Этот процесс сопровождается окоченением отдельных мышц и их групп с развитием тугоподвижности суставов, а в последующем и невозможности согнуть конечность ни в одном суставе.
Подобное состояние называется мышечной контрактурой. Наиболее жизнеспособна кожа. Нередко приходилось наблюдать полную гибель мышц, тогда как кожа внешне остаётся не измененной. Полная мышечная контрактура свидетельствует о гибели конечности и необходимости срочной ее ампутации с целью спасения жизни, так как всасывание продуктов мышечного распада приводит к необратимому отравлению организма с нарушением функции всех жизненно-важных органов. Процесс развития острой ишемии достаточно быстрый, но на определенных этапах обратимый. Если орган или конечность утратили свою функцию, но еще не погибли, то восстановление кровообращения дает шанс полного их восстановления. В поздние сроки восстановление может быть неполным, потеря времени лишает всякой надежды.
Срок, отпущенный острой ишемией для существования конечности, зависит от многих факторов. При тромбозе гибель конечности наступает не сразу и не всегда, так как сосуд был изначально сужен атеросклеротической бляшкой, а конечность привыкла вести "полуголодное" существование. Развивались окольные пути кровоснабжения. Однако изменение условий кровоснабжения углубляет дефицит кислорода и постепенно приводит к умиранию органа.
При тромбозах в зависимости от объема и жизненной важности органа есть 2-5 дней для спасения. При эмболиях нарушение кровоснабжения наступает мгновенно, что приводит к резкому спазму артерий и выключению коллатерального кровообращения. Отсутствие доставки кислорода к органу или конечности запускает механизмы острой ишемии. При эмболиях лучшие результаты лечения для восстановлении кровотока в головном мозге минуты, внутренних органах от 30 минут до 1 часа, конечностях до 6 часов, от начала заболевания. До 12 часов можно спасти только 60% конечностей, после 24 часов лишь 20 %. Боль при недостаточности крови возникает в начале болезни. При эмболии боль сильнее и напоминает удар и бывает очень сильной. При тромбозах болевые ощущения менее выражены и часто характеризуются "нога затекла, онемела". Постепенно болевые ощущения затихают, что связано с гибелью нервных окончаний. Второй основной признак - изменение окраски кожных покровов и резкое снижение температуры конечности. Она становится "ледяной" на ощупь. При эмболии чаще вначале кожа резко бледнеет, затем по мере уменьшения боли начинает синеть, становится "мраморной". Следующим этапом исчезает чувствительность. При этом сохраняется чувство тупой боли, но покалывание иглой, прикосновение горячим и холодным не ощущается. Вслед за исчезновением чувствительности исчезают и движения. Пораженная конечность не воспринимается, как своя, но пассивные движения еще возможны. Этот этап является последним, когда еще можно восстановить функцию конечности. В дальнейшем развивается отек мышц, частичная и полная мышечная контрактура.
От скорости обращения больного к сосудистому хирургу зависит исход лечения. Ни в коем случае нельзя согревать больную конечность. В стационаре при эмболии в ближайшие часы сделают экстренную операцию по извлечению тромбов (эмболэктомию). При тромбозе часто есть несколько дней для обследования. Производятся операции шунтирования или протезирования закупоренного участка сосуда. Для исключения таких состояний любые боли или неприятные ощущения в конечностях должны стать поводом к обращению за консультацией сосудистому хирургу.
Эмпиема плевры – воспаление плевральных листков с накоплением гноя между ними. По характеру возбудителя воспаления различают специфическую (туберкулезную, актиномикотическую) и неспецифическую эмпиему плевры. Среди возбудителей неспецифической эмпиемы плевры превалируют стафилококки, стрептококки, протей, синегнойная палочка, кишечная палочка, которые преимущественно находятся в ассоциации с неклостридиальной анаэробной микрофлорой (более чем в 50% случаев): фузобактериями, бактероидами, пептококками, пептострептококками.
Различают первичную и вторичную эмпиему плевры. На практике чаще встречается вторичная, которая является осложнением какого-либо другого гнойного воспаления – пневмонии, абсцесса или гангрены легкого, остеомиелита ребер, медиастинального лимфаденита. При первичной эмпиеме плевры инфекция попадает в плевральную полость при травме груди, резекции легких, реже гематогенно при сепсисе.
Классификация эмпием плевры.
По клиническому течению:
- острые (до 3 месяцев);
- хронические (свыше 3 месяцев).
По наличию деструкции легкого:
- эмпиема без деструкции легкого (простая);
- эмпиема с деструкцией легкого;
- пиопневмоторакc.
- Закрытые.
- Открытые:
- с бронхоплевральным свищем;
- с плеврокожным свищем;
- с бронхоплевральнокожным свищем;
- с решетчатым легким;
- с другим полым органом.
- ограниченные (чаще осумкованные спайками);
- субтотальные;
- тотальные.
Клиническая картина.
Клинические проявления острой эмпиемы зависят от распространенности гнойного процесса, вирулентности микрофлоры, степени деструкции легочной ткани, реактивности больного, а также от своевременности и полноценности проводимого лечения (Рис. 2.3.). В большинстве случаев заболевание протекает на фоне дыхательной и сердечно-сосудистой недостаточности, которые обусловлены полным или частичным спадением легкого, смещением средостения, сдавлением крупных сосудов и нарастающей эндогенной интоксикацией.
При объективном обследовании отмечается бледность кожи и слизистых оболочек, тахикардия, одышка. Грудная клетка на стороне поражения становится бочкообразной со сглаженными межреберьями. Перкуторно отмечается притупление легочного звука в нижних отделах и коробочный звук выше горизонтальной линии жидкости. Аускультативно – резкое ослабление или отсутствие дыхательных шумов. При закрытой эмпиеме, при отсутствии воздуха в плевральной полости и сращений, верхняя граница тупости соответствует линии Эллиаса-Дамуазо, а над зоной тупости отмечается тимпанический звук (признак Шкоды).
Диагностика.
Рентгенологически на стороне эмпиемы определяется интенсивное затенение, смещение средостения в здоровую сторону. При пиопневмотораксе верхняя граница жидкости становятся горизонтальной. Над уровнем жидкости определяется воздушная полость. В зависимости от степени коллапса легкого различают ограниченный, субтотальный и тотальный пиопневмоторакс. При ограниченных эмпиемах плевры для уточнения формы, размеров, наличия бронхиальных свищей проводят плеврографию – введение водорастворимых контрастных веществ в полость эмпиемы с помощью пункции или через фистулу при наличии плеврокожного свища.
В последние годы в диагностике острых и хронических эмпием плевры все большее распространение получает ультразвуковое исследование, особенно при осумкованных, ограниченных эмпиемах, когда скопления жидкости маскируются массивными плевральными швартами и оказываются недоступными для рентгенологического распознавания. В ряде случаев при отграниченной гнойной полости возможно выполнение пункции и дренирования ее под контролем ультразвука. В трудных для диагностики ситуациях в первую очередь для выявления деструкции в легком используют компьютерную томографию.
Одним из обязательных этапов диагностики эмпиемы плевры является диагностическая пункция плевральной полости. Она позволяет окончательно установить этиологическую причину накопления выпота в плевральной полости – геморрагический при раке легкого, гной при туберкулезе, актиномикозе, неспецифической эмпиеме. Цитологическое, биохимическое и бактериологическое исследования содержимого плевральной полости является обязательным.
Лечение эмпиемы плевры включает:
1. Полноценную аспирацию гноя и санацию плевральной полости, которые при ограниченных эмпиемах достигаются регулярными пункциями, аспирациями гноя, промываниями полости эмпиемы антисептиками и введением антибиотиков; при открытых, тотальных и субтотальных эмпиемах – дренированием и промыванием полости эмпиемы.
2. Мероприятия, направленные на скорейшее расправление легкого (дренирование с активной аспирацией, при наличии бронхиального свища – с временной окклюзией бронха, или дренирование по Бюлау).
3. Массивную антибактериальную терапию (цефалоспорины III-IV поколения, фторхинолоны, карбапенемы).
6. Общеукрепляющую терапию, направленную на восстановление функций жизненно важных органов и систем.
Возможны следующие основные варианты санации плевральной полости: пассивное дренирование с фракционным лаважем; постоянная активная аспирация с фракционным лаважем или непрерывное промывание полости. Однако наиболее эффективным приемом лечения острой эмпиемы плевры является фракционный лаваж или непрерывное промывание полости в сочетании с активной аспирацией. Точку для пункции или дренирования полости плевры определяют на основании многоосевой рентгеноскопии. Сроки нахождения дренажной трубки в плевральной полости во многом зависят от быстроты расправления легкого и прекращения отделения гноя, но в среднем составляют 2-3 недели.
При лечении эмпиемы плевры отсасывают по возможности весь экссудат. При наличии густого гноя, пленок фибрина или казеозных масс применяют протеолитические ферменты, способствующие разжижению вязкого гноя, лизису напластований фибрина на плевральных листках и потенцирующему действию антибиотиков. Наряду с ферментами в полость плевры вводят растворы антибиотиков, которые подбирают с учетом характера и чувствительности выделенной из экссудата микрофлоры. У больных с острым гнойным плевритом такое лечение обычно уже через 2-3 недели приводит к прекращению накопления экссудата в плевральной полости, улучшению общего состояния, ликвидации явлений интоксикации и в конечном итоге к выздоровлению.
Если не удается добиться облитерации полости и расправления легкого, формируется хроническая эмпиема плевры. В этих случаях единственно эффективным методом лечения является оперативное вмешательство – плеврэктомия с декортикацией легкого, а при наличии деструкции в легком, бронхоэктазов – резекция легкого.
Тактика при хронической эмпиеме плевры. Лечение бронхиальных свищей
Кафедра фтизиатрии и торакальной хирургии ФППОВ Первого Московского государственного медицинского университета им. И.М. Сеченова
Кафедра фтизиопульмонологии и торакальной хирургии им. М.И. Перельмана ГБОУ ВПО "Первый МГМУ им. И.М. Сеченова" Минздрава России, Москва, Россия
Кафедра фтизиопульмонологии и торакальной хирургии им. М.И. Перельмана ГБОУ ВПО "Первый МГМУ им. И.М. Сеченова" Минздрава России, Москва, Россия
Кафедра фтизиопульмонологии и торакальной хирургии им. М.И. Перельмана ФГАОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России, Москва, Россия
Кафедра фтизиопульмонологии и торакальной хирургии им. М.И. Перельмана ГБОУ ВПО "Первый МГМУ им. И.М. Сеченова" Минздрава России, Москва, Россия
Кафедра фтизиопульмонологии и торакальной хирургии им. М.И. Перельмана ФГАОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России, Москва, Россия
Кафедра фтизиопульмонологии и торакальной хирургии им. М.И. Перельмана ФГАОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России, Москва, Россия
Хирургическое лечение туберкулезной эмпиемы плевры у детей
Журнал: Хирургия. Журнал им. Н.И. Пирогова. 2019;(8): 22‑28
Кафедра фтизиатрии и торакальной хирургии ФППОВ Первого Московского государственного медицинского университета им. И.М. Сеченова
Собственный опыт и данные литературы свидетельствуют о том, что, если неспецифическую эмпиему в большинстве случаев можно излечить дренированием и местной санацией полости эмпиемы, то излечение туберкулезной эмпиемы часто требует больших торакальных операций. Цель исследования — изучить результаты оперативного лечения туберкулезной эмпиемы плевры у детей в зависимости от стадии процесса. Материал и методы. Приведен опыт диагностики и хирургического лечения туберкулезной эмпиемы плевры у 82 больных в возрасте от 4 до 17 лет. Показаны различия в клинике и рентгенологической картине разных стадий туберкулезной эмпиемы. Рассмотрены виды оперативных вмешательств на каждой стадии процесса. Результаты. У 72 пациентов с III стадией эмпиемы выполнено 76 операций. У 2 (2,6%) пациентов возникли послеоперационные осложнения (замедленное расправление легкого), успешно ликвидированные при помощи торакоцентеза с дренированием плевральной полости. Послеоперационная летальность отсутствует. Выводы. Комплексное лечение туберкулезной эмпиемы плевры со своевременным применением хирургических методов позволяет добиться клинического излечения у всех детей и подростков, однако тяжесть операции, количество послеоперационных осложнений и срок лечения напрямую зависят от стадии болезни. К сожалению, почти у 90% пациентов, направленных на хирургическое лечение, регистрируется III стадия эмпиемы, когда возможности малоинвазивной хирургии ограничены и приходится прибегать к обширным, травматичным операциям.
Кафедра фтизиатрии и торакальной хирургии ФППОВ Первого Московского государственного медицинского университета им. И.М. Сеченова
Кафедра фтизиопульмонологии и торакальной хирургии им. М.И. Перельмана ГБОУ ВПО "Первый МГМУ им. И.М. Сеченова" Минздрава России, Москва, Россия
Кафедра фтизиопульмонологии и торакальной хирургии им. М.И. Перельмана ГБОУ ВПО "Первый МГМУ им. И.М. Сеченова" Минздрава России, Москва, Россия
Кафедра фтизиопульмонологии и торакальной хирургии им. М.И. Перельмана ФГАОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России, Москва, Россия
Кафедра фтизиопульмонологии и торакальной хирургии им. М.И. Перельмана ГБОУ ВПО "Первый МГМУ им. И.М. Сеченова" Минздрава России, Москва, Россия
Кафедра фтизиопульмонологии и торакальной хирургии им. М.И. Перельмана ФГАОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России, Москва, Россия
Кафедра фтизиопульмонологии и торакальной хирургии им. М.И. Перельмана ФГАОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России, Москва, Россия
Для эмпиемы плевры туберкулезной этиологии характерно скопление гнойного экссудата в плевральной полости. Основными клиническими проявлениями туберкулезной эмпиемы плевры являются невыраженная симптоматика, более высокая чем у неспецифической эмпиемы резистентность к консервативному лечению с использованием дренирования плевральной полости и склонность к хроническому течению [1—13]. По срокам течения заболевания туберкулезную эмпиему плевры подразделяют на острую (срок болезни до 2 мес) и хроническую (>2 мес), выделяя отдельно туберкулезный плеврит [5, 11—13].
Яркая клиническая картина эмпиемы при туберкулезе появляется, как правило, в случае присоединения вторичной неспецифической микрофлоры, что случается чаще всего при появлении бронхиального свища. Если неспецифическую эмпиему в 85—90% случаев можно вылечить дренированием и местной санацией полости эмпиемы, то для излечения туберкулезной эмпиемы гораздо чаще приходится прибегать к большим торакальным операциям [5, 6, 8, 11—16].
Эмпиема плевры туберкулезной этиологии — абсолютное показание к хирургическому лечению. Такие пациенты обязательно должны проходить лечение в хирургическом торакальном отделении. Хирургическое лечение этих больных начинают с дренирования плевральной полости, что можно выполнить разными способами (торакоцентез с использованием троакара, дренирование полости эмпиемы по проводнику, плевростомия, видеоторакоскопическая (ВТС) санация плевральной полости с дренированием) [12, 13].
Виды операций, применяемые при этом заболевании, в значительной степени зависят от стадии процесса, определить которую помогает в первую очередь компьютерная томография органов грудной клетки. Лечению туберкулезных эмпием у взрослых посвящено множество работ [3—5, 11, 12, 14, 16—18], однако в течение последнего десятилетия мы не нашли ни одной публикации о хирургическом лечении туберкулезной эмпиемы у детей.
Лечение неспецифической эмпиемы плевры у детей активно обсуждается в мировой литературе. Для того чтобы подчеркнуть ряд особенностей туберкулезной эмпиемы и сделать результаты исследования сравнимыми с современными работами о лечении неспецифической эмпиемы у детей, мы использовали классификацию Американского торакального общества (American Thoracic Society): I стадия соответствует экссудативной фазе воспаления, II — фибринозно-гнойной фазе, III — фазе организации с формированием остаточной полости и фиксированного легкого.
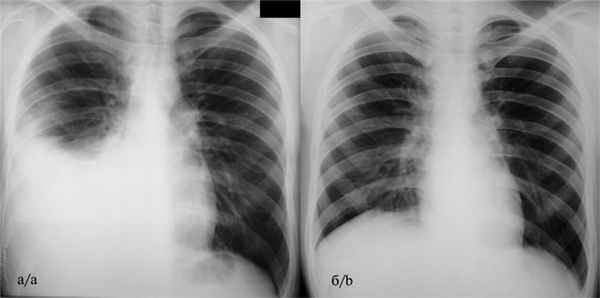
Рентгенологически I стадия эмпиемы характеризуется синдромом гидроторакса с формированием классической косовосходящей линии Соколова—Эллиса—Дамуазо (рис. 1, а). Рис. 1. Обзорная рентгенограмма органов грудной клетки больной А. до (а — правосторонний гидроторакс с формированием линии Соколова—Эллиса—Дамуазо) и через 1 мес (б — явления правостороннего гидроторакса полностью купированы без остаточных изменений) после видеоторакоскопической плеврэктомии.
На этой стадии туберкулезной эмпиемы мы отдаем предпочтение ранней ВТС-санации полости эмпиемы, что позволяет наиболее эффективно и быстро ликвидировать симптомы интоксикации и уменьшить риск развития хронической эмпиемы. Во время этой операции выполняют следующие этапы: 1) эвакуация серозно-гнойного экссудата; 2) вскрытие отдельных затеков и осумкований; 3) удаление наложений фибрина с висцеральной и костальной плевры; 4) частичную париетальную плеврэктомию в области наиболее выраженных воспалительных изменений для гистологической верификации процесса и ускорения резорбции экссудата из плевральной полости; 5) дренирование полости эмпиемы для дальнейшего удаления экссудата, местной антибактериальной терапии и противотуберкулезной химиотерапии.
Преимущества операции туберкулезной эмпиемы плевры в I стадии: морфологическая верификация диагноза в сомнительных случаях; выявление микобактерии туберкулеза (МБТ) и определение чувствительности к противотуберкулезным препаратам; ускорение рассасывания экссудата, быстрое купирование клинических проявлений, уменьшение сроков лечения; профилактика формирования грубых плевральных рубцов с потерей функции легкого (см. рис. 1, б).
Во II стадии неспецифической эмпиемы хирургическое, ВТС-лечение или с видеоподдержкой является общепризнанным стандартом [4, 5, 11—13, 17—19]. В научном мире пока нет соглашения по оптимальной методике лечения эмпиемы плевры II стадии у детей. Судя по данным литературы, неспецифическую эмпиему плевры II стадии можно лечить с почти 80% вероятностью выздоровления дренированием плевральной полости, с 84% вероятностью выздоровления фибринолитиками и почти со 100% вероятностью выздоровления торакоскопическим методом. Однако описанная для лечения эмпиемы плевры тактика, да и сама классификация American Thoracic Society, по сути объединяющая плеврит и эмпиему, применительно к процессу туберкулезной этиологии, по нашему мнению, не совсем адекватно отражает происходящее. Так, если неспецифическая эмпиема I стадии у детей, в большинстве случаев через несколько дней под влиянием консервативной терапии ликвидируется, то туберкулезный плеврит при консервативном лечении сохраняется по большей части всего несколько месяцев и гораздо чаще переходит во II и III стадию.
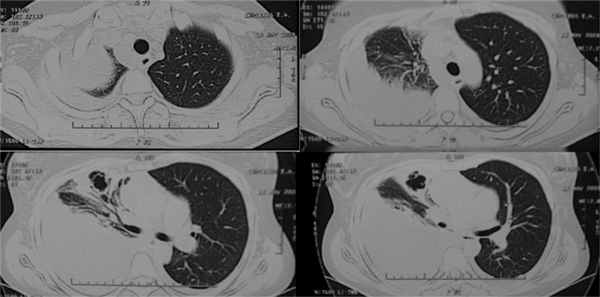
Во II стадии туберкулезной эмпиемы изменяются состав и консистенция плеврального выпота. Если в начале этой фазы выпот довольно жидкий, фибрина еще мало, а спайки нежные и эластичные, то можно довольно легко достичь полного расправления легкого и соответственно выздоровления путем активного дренирования плевральной полости. Если процесс зашел далеко и фибринозно-гнойное содержимое плевральной полости начало организовываться, появилось утолщение плевры и легкое не расправлено, то шансы на выздоровление путем местной санации плевральной полости невысоки (рис. 2). Рис. 2. Компьютерные томограммы органов грудной клетки пациента во II стадии туберкулезной эмпиемы. Отмечается утолщение париетальной плевры, сгущение экссудата, пневмофиброз в легком.
Во II стадии туберкулезной эмпиемы при наличии бронхиальной фистулы во время видеоторакоскопии можно герметизировать легочный дефект разными способами — электрокоагуляцией, аргоноплазменной коагуляцией, ушить легочный дефект, заклеить фистулу тахокомбом или биологическим клеем, установить в бронх бронхоблокатор, дренирующий полость легочной деструкции. Последующее за санационной видеоторакоскопией с частичной плеврэктомией местное лечение позволяет у большинства пациентов с острой эмпиемой плевры II стадии ликвидировать или уменьшить воспаление. Однако у части пациентов, особенно часто при наличии бронхиальной фистулы, формируется хроническая эмпиема, требующая радикальных операций. Пытаться вылечить хроническую туберкулезную эмпиему консервативно или методами местной санации обычно бесперспективно. В хирургическом лечении хронической туберкулезной эмпиемы III стадии выполняют более радикальные вмешательства — плеврэктомию с декортикацией легкого, плеврэктомию с резекцией легкого, плевропневмонэктомию, торакомиопластику, этапные операции с применением окклюзии бронхиального свища.
Приводим клиническое наблюдение выполнения видеоассистированной (ВАТС) плеврэктомии с декортикацией легкого.
Больная Г., 10 лет, заболела остро 29.09.07. Заболевание началось с жалоб на сухой кашель, фебрильную температуру тела, выраженную одышку в покое. В поликлинике по месту жительства выполнена обзорная рентгенограмма грудной клетки, выявлен тотальный гидроторакс слева с выраженным смещением средостения вправо.
Срочная госпитализация в отделение реанимации районной больницы, где выполнены пункция и дренирование плевральной полости слева с эвакуацией 1000 мл серозно-гнойного экссудата (атипичные клетки и кислотоустойчивые микобактерии в экссудате отсутствовали). Состояние пациентки улучшилось, нормализовалась температура тела. Плевральный дренаж удален через 10 дней после операции. В дальнейшем, несмотря на антибиотикотерапию, в левой плевральной полости сформировалась осумкованная эмпиема объемом до 200 мл. Заподозрена туберкулезная этиология процесса, 13.11.07 больную направили на лечение в детское туберкулезное отделение с диагнозом «хроническая туберкулезная эмпиема плевры слева».
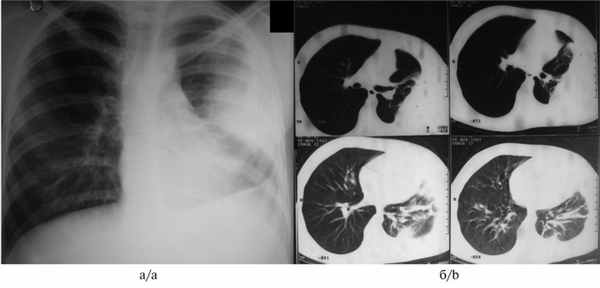
При поступлении предъявляла жалобы на общую слабость, снижение аппетита, одышку при физической нагрузке, повышение температуры до 37,8 °С. При обзорной рентгенографии легких (рис. 3, а) Рис. 3. Данные обследования больной Г. до операции. а — обзорная рентгенограмма органов грудной клетки (слева определяется субтотальная туберкулезная эмпиема плевры); б — компьютерные томограммы органов грудной клетки (в левой плевральной полости заднекостально располагается массивное осумкование густой жидкости). 20.11.07 выполнена ВАТС-плеврэктомия слева с декортикацией легкого (хирург Д.Б. Гиллер). слева определяется осумкованная эмпиема плевры. На компьютерных томограммах (см. рис. 3, б) в задних отделах левой плевральной полости массивное осумкование с выраженным уменьшением объема левого гемиторакса.
При исследовании функции легких установлено умеренное снижение вентиляционной способности легких по смешанному типу (жизненная емкость легких 79%, объем форсированного выдоха за 1-ю секунду 69%).
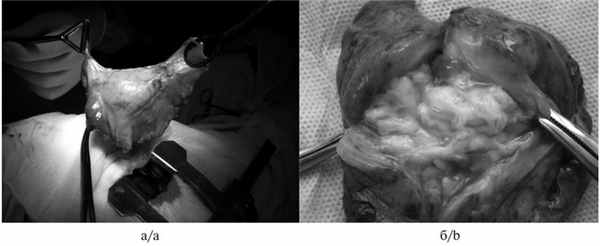
Из боковой миниторакотомии (6 см) в пятом межреберье под ВТС-контролем легкое выделено в экстрафасциальном и поднадкостничном слое до медиастинальной поверхности и интраплеврально в проекции средостения. Эмпиемный мешок размером 15×12×5 см по боковой и заднекостальной поверхности легкого с затеком в междолевую борозду. Его наружная стенка резко утолщена до 0,5 см (рис. 4, а). Рис. 4. Интраоперационные фотографии больной Г. а — мешок эмпиемы удален целиком без его вскрытия; б — в полости эмпиемного мешка казеозные массы.
Длительность операции составила 190 мин, интраоперационная кровопотеря — 80 мл. Удаленный препарат представлял собой субтотальную эмпиему, на разрезе определялся густой казеоз (см. рис. 4, б).
Гистологическое исследование: хроническая эмпиема плевры туберкулезной этиологии. В послеоперационном периоде без осложнений.
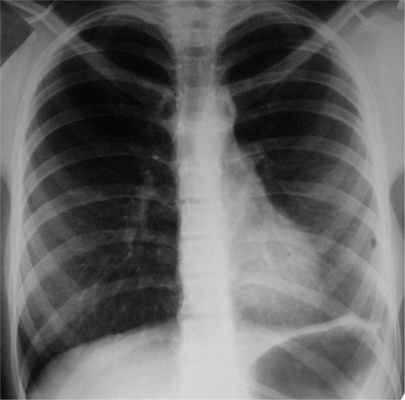
При обследовании через 3 года после операции самочувствие хорошее, физическое развитие соответствует возрасту. Одышки нет, занимается спортивной гимнастикой. Деформации грудной клетки и сколиоза, наблюдавшихся перед операцией, нет. При исследовании функции легких вентиляционная способность легких нормализовалась (жизненная емкость легких 102%, объем форсированного выдоха за 1-ю секунду 105%). Обострений туберкулеза за 3 года не было, в мокроте при всех исследованиях МБТ не обнаружены. При обзорной рентгенографии (рис. 5) Рис. 5. Обзорная рентгенограмма органов грудной клетки больной Г. через 3 года после ВАТС-плеврэктомии с декортикацией левого легкого по поводу хронической туберкулезной эмпиемы плевры. Легкие хорошо пневматизированы, признаков обострения туберкулеза нет. легкие хорошо пневматизированы, признаков обострения туберкулеза нет.
В ряде случаев гнойные осумкования туберкулезной эмпиемы могут быть следствием неизлеченного до конца туберкулезного плеврита и протекать малосимптомно в течение многих лет. При этом довольно часто изменения ошибочно трактуются рентгенологом как плевральные наложения вследствие перенесенного плеврита или искусственного пневмоторакса, и лишь появление туберкулезного натечника в мягких тканях грудной клетки или бронхоплеврального свища выявляет хронически протекающий воспалительный процесс. На обзорной рентгенограмме при этом часто не видно грубых патологических изменений, и небольшие утолщения париетальной плевры трактуются как «плеврокостальные наложения» после перенесенного туберкулезного плеврита.
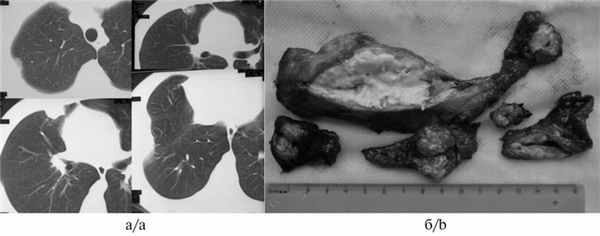
Для уточнения локализации и характера патологического процесса в этом случае помогает компьютерная томография (рис. 6, а). Рис. 6. Результаты обследования и лечения больной В., 17 лет, через 1 год после перенесенного плеврита. а — компьютерные томограммы органов грудной клетки (видны осумкования в правой плевральной полости); б — фотография операционного препарата (удаленный эмпиематозный мешок, на его разрезе жидкий казеоз). На компьютерных томограммах видны утолщения плевры и осумкования различной плотности.
Несмотря на ограниченный характер рентгенологических изменений и частое отсутствие клинических проявлений, в операционном препарате видна картина хронической туберкулезной эмпиемы с жидким казеозом и резким утолщением плевры (см. рис. 6, б).
Материал и методы
Проанализированы истории болезней 82 детей и подростков в возрасте от 4 до 17 лет, оперированных нами в 1984—2017 гг. По поводу туберкулезной эмпиемы I и II стадии оперированы 10 подростков, им выполнены ВТС-плеврэктомии с частичной декортикацией легкого. В 5 случаях до операции этиология эмпиемы не установлена, и операция носила лечебно-диагностический характер. Во всех этих случаях гистологическое исследование позволило верифицировать диагноз туберкулеза, у одного пациента методом ПЦР удалось выявить МБТ с сохраненной чувствительностью ко всем противотуберкулезным препаратам.

По поводу туберкулезной эмпиемы III стадии 72 пациентам выполнили 76 операций (см. таблицу). Операции по поводу туберкулезной эмпиемы плевры III стадии у детей В 37 (48,7%) случаях произведена ВТС- или ВАТС-плеврэктомия с декортикацией легкого.
У 2 (3%) подростков после резекции легкого с плеврэктомией и декортикацией по поводу III стадии туберкулезной эмпиемы возникли послеоперационные осложнения (замедленное расправление легкого), которые успешно ликвидировали с помощью торакоцентеза и дренирования плевральной полости. Послеоперационной летальности не было.
Таким образом, комплексное лечение туберкулезной эмпиемы плевры у детей и подростков со своевременным применением хирургических методов позволяет добиться клинического излечения у всех пациентов. Однако тяжесть операции, количество послеоперационных осложнений и срок лечения напрямую зависят от стадии процесса, при которой больной направлен на хирургическое лечение. К сожалению, почти 90% пациентов поступают к нам в III стадии эмпиемы, когда возможности малоинвазивной хирургии ограничены и приходится прибегать к обширным травматичным операциям.
Авторы заявляют об отсутствии конфликта интересов.
T he authors de clare no conflict of interest.
Сведения об авторах
Тактика при хронической эмпиеме плевры. Лечение бронхиальных свищей
Тактика при хронической эмпиеме плевры. Лечение бронхиальных свищей
Анализ специальной литературы по данному разделу дает основание сегодня сделать вывод, что эти обширные, травматичные, чаще повторные операции, дают малый клинический эффект. Они приводят к инвалидизации. Ряд операций при хронических бронхо-плевральных фистулах и эмпиеме, такие, как реампутация культи главного бронха технически сложны и опасны ранением культей легочных сосудов. Малую эффективность названных выше операций, по-видимому, следует объяснить тем, что все они производятся в зоне инфицированных тканей, в гнойной плевральной полости.
Мы наблюдали больных, у которых неоднократными операциями был использован реберный каркас и все возможный группы мышц, а бронхиальный свищ и эмпиема сохранялись. Нам кажется, что эффективность подобных операций у некоторых больных является просто удачей. Сегодня можно утверждать, что этот путь борьбы с бронхиальными свищами и эмпиемой после операции пульмонэктомии не имеет будущего в торакальной хирургии.
В нашей клинике, руководимой заслуженным деятелем науки, лауреатом Ленинской премии академиком АМН СССР Л. К. Богушем, с 1968 г. впервые в клинической практике тачала применяться новая хирургическая тактика для одномоментной ликвидации хронических бронхоплевральных свищей и эмпиемы плевральной полости из трансстернального трансперикардиального или трансмедиастинально-перикардиального доступа. К настоящему времени эта операция произведена у 12 больных.
Минимальное время с момента возникновения бронхо-плеврального свища и эмпиемы до операции трансперикардиалыюй окклюзии главного бронха 3 месяца, максимальное—8 лет. У 9 из 12 больных имелись выраженные туберкулезные изменил в единственном легком, а у 3 кавернозный туберкулез. Больные к моменту операции (кроме ребенка 9 лет) являлись инвалидами I группы и нуждались в хирургическом стационаре.

Все больные с выраженной клиникой специфической и гнойной интоксикации, у всех был резко выражен дефицит веса, всех их беспокоил кашель с мокротой гнойного характера, одышка, усиливающаяся при физической нагрузке, большая часть из них (в зависимости от диаметра свища в бронхе) в постели занимала вынужденное положение, т. к. поворот на здоровую сторону сразу вызывал приступообразный кашель. У 6 больных была выражена афония. Все больные нуждались в ежедневных или частых пункциях и промываниях плевральной полости с эвакуацией гнойного экссудата.
Исследование мокроты выявило рост пневмококка, патогенного и апатогенного стафилококка, гемолитического стафилококка у 5 больных, синегнойной палочки, грибов типа.
У 7 больных в мокроте определялись БК. Микобактерии выявлены в экссудате из плевральной полости у 2-х больных, у 4-х больных выявлены грибки типа Aspergillus и Candida, у 8 больных щри исследовании экссудата получена смешанная флора (патогенный стафилококк, пневмококк, негемолитический и гемолитический стрептококк и др.).
У всех больных этой группы имелась выраженная легочно-сердечная недостаточность, изменения со стороны других органов и систем, характерные для больных, страдающих длительной инфекцией. Трансперикардиальный доступ был применен у 3-х больных с нетуберкулезной патологией.
Операция была произведена у 6 больных справа и у 6 больных слева.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Перспективные направления в изучении патогенеза эмпиемы плевры
Острая неспецифическая эмпиема плевры (ОНЭП) является одной из наиболее тяжелых из всех существующих гнойных патологий. Несмотря на положительные результаты лечения больных эмпиемами плевры (ЭП), на сегодняшний день остается необходимость совершенствования тактики лечения и методов ее прогнозирования. Перспективным в этом отношении является дальнейшее изучение патологической анатомии ОНЭП и определение гистологических критериев острого и хронического гнойного плеврита, плеврогенного пневмосклероза, поскольку морфологические характеристики играют важную роль в определении прогноза и выборе оптимальной тактики лечения. Однако в клинической практике полноценное гистологическое исследование висцеральной плевры и легкого затруднительно, т. к. любое повреждение пораженного легкого грозит формированием бронхиального свища. Между тем макроскопические характеристики плевральной полости и гистологические изменения в висцеральной плевре и легком взаимосвязаны. Углубленное исследование этой взаимосвязи и доказательство морфологической идентичности патоморфологических изменений в париетальной плевре и висцеральной плевре и легком при ЭП позволит повысить диагностическую эффективность торакоскопии и разработать методику торакоскопической экспресс"диагностики гистологических изменений, а также обозначить принципиально новые пути совершенствования подходов в лечении ЭП. При этом актуален поиск оптимальных для гистологической экспресс"диагностики молекулярных медиаторов плеврального фиброза. Выявленные закономерности могут помочь и в разработке новых методов лечения и профилактики плеврогенного пневмосклероза. В статье дается обзор современных представлений об основных механизмах ремоделирования внеклеточного матрикса при плевральном фиброзе и вызывающих его факторах. Анализ этих процессов может определять новые механизмы ремоделирования внеклеточного матрикса и путей его устранения при плеврогенном пневмосклерозе, а также использовать определение выявленных «ключевых посредников» плеврального фиброза в экспресс"диагностике стадий ОНЭП
Ключевые слова
Об авторах
ГБОУ ВПО «Пермский государственный медицинский университет им. акад. Е.А.Вагнера» Минздрава России: 614990, Пермь, Петропавловская, 26
Россия
д. м. н., главный научный сотрудник отдела морфологических и патофизиологических исследований ЦНИЛ, заведующая курсом клинической лабораторной диагностики, доцент кафедры микробиологии, вирусологии с курсом КЛД ГБОУ ВПО «Пермский государственный медицинский университет им. акад. Е.А.Вагнера» Минздрава России; тел.: (342) 2171031
заведующий Первым химиотерапевтическим отделением ГБУЗ ПК «Пермский краевой онкологический диспансер»; тел.: (342) 2201657
ГБОУ ВПО «Пермский государственный медицинский университет им. акад. Е.А.Вагнера» Минздрава России: 614990, Пермь, Петропавловская, 26
Россия
д. м. н., доцент кафедры нормальной, топографической и клинической анатомии, оперативной хирургии ГБОУ ВПО «Пермский государственный медицинский университет им. акад. Е.А.Вагнера» Минздрава России; тел.: (342) 2171031
Список литературы
1. Макаров В.В. Современные аспекты санации плевральной полости у больных с острой эмпиемой плевры. Буковинский медицинский вестник. 2008; 12 (3): 39–41. /Makarov V.V. Current aspects of pleural draining in acute empyema. Bukovinskiy meditsinskiy vestnik 2008; 12 (3): 39–41 (in Russian).
2. Дударев А.А., Сухоруков А.М., Большаков В.Н. и др. Оценка гемостазиологических сдвигов у больных с острой неспецифической эмпиемой плевры. В кн.: Материалы III Съезда хирургов Сибири и Дальнего Востока. Томск; 2009: 86–87. / Dudarev A.A., Sukhorukov A.M., Bol'shakov V.N. et al. Haemostatic change in patients with acute non"specific empyema. In: Proceedings of the 3rd Congress of Surgeons of Syberia and the Far East. Tomsk; 2009: 86–87 (in Russian).
3. Никольский В.И., Логинов С.Н., Баженов М.С., Семисаженов О.А. Динамическая торакоскопия с применением торакопорта в лечении больных с неспецифической эмпиемой плевры. Известия высших учебных заведений. Поволжский регион. 2010; 4 (16): 99–107. / Nikol'skiy V.I., Loginov S.N., Bazhenov M.S., Semisazhenov O.A. Dynamic thoracoscopy in patients with acute non-specific empyema using thoracoport. Izvestiya vysshikh uchebnykh zavedeniy. Povolzhskiy region. 2010; 4 (16): 99–107 (in Russian).
4. Lee S.F., Lawrence D., Booth H. et al. Thoracic empyema: current opinions in medical and surgical management. Curr. Opin. Pulm. Med. 2010; 16 (3): 194–200.
5. Черкасов В.А., Хусейн Х.С. Лечение больных эмпиемой плевры. Пермский медицинский журнал. 2009; 26 (2): 15–19. / Cherkasov V.A., Khuseyn Kh.S. Treatment of patients with empyema. Permskiy meditsinskiy zhurnal 2009; 26 (2): 15–19 (in Russian).
6. Проценко А.В. Выбор способа торакопластики при бронхиальном свище и эмпиеме плевры после пульмонэктомии. Анналы хирургии. 2009; 2: 40–42. / Protsenko A.V. A choice of thoracoplastics method in post"pneumonectomy bronchial fistula and empyema. Annaly khirurgii 2009; 2: 40–42 (in Russian).
7. Dudarev А.А., Sukhorukov А.М., Bolshakov V.N. et al. Use of thoracoscopy in local treatment of nonspecific pleural empyema. Bull. Intern. Sci. Surg. Ass. 2010; 5 (1): 11–12.
8. Cheah Y.L., Ng T., Shah K. et al. Video"assisted Thoracoscopic Surgery (VATS) drainage of salmonella enteritidis empyema and needle"localization for retrieval of a dropped gallstone. Surg. Laparosc. Endosc. Percutan. Tech. 2010; 20 (4): 265–268.
9. Лукомский Г.И. Неспецифические эмпиемы плевры. М.: Медицина; 1976. / Lukomskiy G.I. Non"specific empyema. Moscow: Meditsina; 1976 (in Russian).
11. Olgac G., Fazlioglu M., Kutlu C.A. VATS decortication in patients with stage 3 empyema. Thorac. Cardiovasc. Surg. 2005; 53 (5): 318–320.
12. Vyhnánek F., Fanta J., Jirava D., Ocadlík M. Contemporary approach to treatment of the posttraumatic empyema of the thorax. Rozhl. Chir. 2006; 85 (1): 4–8.
14. Andrews N.C., Parker E.F., Shaw R.R. et al. Management of nontuberculous empyema. Am. Rev. Respir. Dis. 1962; 85: 935–936.
16. Light R.W. Parapneumonic effusions and empyema. Proc. Am. Thorac. Soc. 2006; 3 (1): 75–80.
17. Порханов В.А., Коровин А.Я. Новые возможности лечения постпневмонэктомической острой эмпиемы плевры со свищами главных бронхов: В кн.: Материалы III Конгресса ассоциации хирургов им. Н.И.Пирогова. М.; 2001: 122–124. / Porkhanov V.A., Korovin A.Ya. Novel approaches to treatment of acute post"pneumonectomy empyema and bronchial fistula of the main bronchus. In: Proceedings of the 3rd Congress of N.I.Pirogov Association of Surgeons. Moscow; 2001: 122–124 (in Russian).
18. Decologne N., Kolb M., Margetts P.J. et al. TGF"β1 induces progressive pleural scarring and subpleural fibrosis. J. Immunol. 2007; 179 (9): 6043– 6051.
19. Owens S., Jeffers A., Boren J. et al. Mesomesenchymal transition of pleural mesothelial cells is PI3K and NF"κB dependent. Am. J. Physiol. Lung Cell. Mol. Physiol. 2015; 308 (12): 1265–1273.
20. Heldin C."H., Miyazono K., Dijke P. TGF"b signalling from cell membrane to nucleus through SMAD proteins. Nature. 1997; 390: 465–471.
21. Chena L."J., Yeb H., Zhanga Q. et al. Bleomycin induced epithelial"mesenchymal transition (EMT) in pleural mesothelial cells. Toxicol. Appl. Pharmacol. 2015; 283 (2): 75–82.
22. Mutsaers S.E., Birnie K., Lansley S. et al. Mesothelial cells in tissue repair and fibrosis. Front. Pharmacol. 2015; 6: 113.
23. Lee Y.C., Malkerneker D., Devin C.J. et al. Comparing transforming growth factor β"2 and fibronectin as pleurodesing agents. Respirology. 2001; 6: 281–286.
24. Lee Y.C., Lane K.B., Zoia O. et al. Transforming growth factor"b induces collagen synthesis without inducing IL"8 production in mesothelial cells. Eur. J. Respir. 2003; 22: 197–202.
26. Qing"qing Z., Geng"Yun S. Transforming growth factor"β and pleural fibrosis. Intern. J. Respir. 2009; 29 (10): 609–612.
27. Leask A. Signaling in fibrosis: targeting the TGF beta, endothelin"1 and CCN2 axis in scleroderma. Front. Biosci. 2009; 1: 115–122.
28. Итмезех А. Механизмы формирования пневмосклероза при хроническом эндотоксикозе (экспериментальное исследование): Дисс. … канд. мед. наук. Волгоград; 2006. / Itmezekh A. Mechanisms of the lung tissue fibrosis in chronic endotoxicosis: Diss. Volgograd; 2006 (in Russian).
29. Xaubet A., Marin"Arguedas A., Lario S. et al. Transforming growth factor"beta1 gene polymorphisms are associated with disease progression in idiopathic pulmonary fibrosis. Am. J. Respir. Crit. Care Med. 2003; 168: 431–435.
30. Lawson W.E., Crossno P.F., Polosukhin V.V. et al. Endoplasmic reticulum stress in alveolar epithelial cells is prominent in IPF: association with altered surfactant protein processing and herpesvirus infection. Am. J. Physiol. Lung Cell. Mol. Physiol. 2008; 294: 1119–1126.
31. Datta A., Scotton C.J., Chambers R.C. Novel therapeutic approaches for pulmonary fibrosis Pulmonary fibrosis. Br. J. Pharmacol. 2011; 163: 141– 172.
32. Moore B.B., Murray L., Das A. et al. The role of CCL12 in the recruitment of fibrocytes and lung fibrosis. Am. J. Respir. Cell. Mol. Biol. 2006; 35: 175–181.
33. Mehrad B., Burdick M.D., Strieter R.M. Fibrocyte CXCR4 regulation as a therapeutic target in pulmonary fibrosis. Int. J. Biochem. Cell. Biol. 2009; 41: 1708–1718.
35. Scotton C.J., Chambers R.C. Molecular targets in pulmonary fibrosis: the myofibroblast in focus. Chest. 2007;132: 1311–1321.
36. Moodley Y.P., Scaffidi A.K., Misso N.L. et al. Fibroblasts isolated from normal lungs and those with idiopathic pulmonary fibrosis differ in interleukin"6/gp130"mediated cell signaling and proliferation. Am. J. Pathol. 2003; 163: 345–354.
37. Moodley Y.P., Caterina P., Scaffidi A.K. et al. Comparison of the morphological and biochemical changes in normal human lung fibroblasts and fibroblasts derived from lungs of patients with idiopathic pulmonary fibrosis during FasLinduced apoptosis. J. Pathol. 2004; 202: 486–495.
38. Kogan E., Тuong V., Demoura S. Mechanism of bronchoalveolar duct junction (BADJ) remodeling in idiopathic pulmonary fibrosis (IPF) as base for new pathogenetic therapy. Eur. Respir. J. 2008; 32 (Suppl. 52): 3489.
39. Tuong V., Demoura S., Kogan E. Markers of cell proliferation, apoptosis and angiogenesis in remodeling of bronchoalveolar duct junctions. Polish Histochemichal et Cytological Society. Folia Histochemica et Cytobiologica.
41. Scotton C.J., Krupiczojc M.A., Konigshoff M. et al. Increased local expression of coagulation factor X contributes to the fibrotic response in human and murine lung injury. J. Clin. Invest. 2009; 119: 2550–2563.
42. Scotton C.J., Chambers R.C. Pulmonary fibrosis. Br. J. Pharmacol. 2011; 163: 141–172.
43. Sun Z."M., Li F."Y., Wang L. et al. Expression of fibroblast specific protein"1 in pleural tuberculosis and its clinical biological significance. World J. Surg. Oncol. 2014; 12: 151.
44. Miles S.E., Sandrini A., Johnson A.R., Yates D.H. Clinical consequences of asbestos"related diffuse pleural thickening: A review. J. Occup. Med. Toxicol. 2008; 3: 1–10.
45. Huang S.X.L., Jaurand M."C., Kamp D.W. et al. Role of Mutagenicity in asbestos fiber"induced carcinogenicity and other diseases. J. Toxicol. Environment. Health. Part B. Crit. Rev. 2011; 14 (1–4): 179–245.
46. Broaddus V.C., Everitt J.I., Black B., Kane A.B. Non"neoplastic and neoplastic pleural endpoints following fiber exposure. J. Toxicol. Environ. Health. Part B. Crit. Rev. 2011; 14 (1–4): 153–178.
47. Sasse S.A., Jadus M.R., Kukes G.D. Pleural fluid transforming growth factor"β1 correlates with pleural fibrosis in experimental empyema. Am. J. Respir. Crit. Care Med. 2003; 168: 700–705.
48. Papaioannou A.I., Kostikas K., Kollia P., Gourgoulianis K.I. Clinical implications for vascular endothelial growth factor in the lung: friend or foe? Respir. Res. 2006; 7: 128.
49. Compernolle V., Brusselmans K., Acker T. et al. Loss of HIF"2alpha and inhibition of VEGF impair fetal lung maturation, whereas treatment with VEGF prevents fatal respiratory distress in premature mice. Nat. Med. 2002; 8 (7): 702–710.
50. Kazi A.S., Lotfi S., Goncharova E.A. et al. Vascular endothelial growth factor"induced secretion of fibronectin is ERK dependent. Am. J. Physiol. Lung Cell. Mol. Physiol. 2004; 286 (3): 539–545.
51. Mura M., dos Santos C.C., Stewart D., Liu M. Vascular endothelial growth factor and related molecules in acute lung injury. J. Appl. Physiol. 2004; 97 (5): 1605–1617.
52. Grove C.S., Lee Y.C. Vascular endothelial growth factor: the key mediator in pleural effusion formation. Curr. Opin. Pulm. Med. 2002; 8 (4): 294–301.
53. Mohammed K.A., Nasreen N., Hardwick J. et al. Bacterial induction of pleural mesothelial monolayer barrier dysfunction. Am. J. Physiol. Lung Cell. Mol. Physiol. 2001; 281 (1): 119–125.
54. Humadi H.Y.A. Matrix Metalloproteinases and TIMPs Expression in Pleural Effusion of Different Origins. Thesis submitted for fulfillment of Master Degree in Pulmonology. Faculty of Medicine Cairo University; 2012.
55. Oikonomidi S., Kostikas K., Kalomenidis I. et al. Matrix metalloproteinase levels in the differentiation of parapneumonic pleural effusions. Respiration. 2010; 80: 285–291.
56. El Margoushya N.M., Khaleel A.T. Metalloproteinase and tissue inhibitor of metalloproteinase in tuberculosis and malignant pleural effusion. Egypt. J. Chest Dis. Tub. 2013; 62 (2): 235–240.
57. Yamashita C.M., Dolgonos L., Zemans R.L. et al. Matrix metalloproteinase 3 is a mediator of pulmonary fibrosis. Am. J. Pathol. 2011; 179( 4): 1733–1745.
58. Kim J.Y., Choeng H.C., Ahn C. Cho S."H. Early and late changes of MMP"2 and MMP"9 in bleomycin"induced pulmonary fibrosis. Yonsei Med. J. 2009; 50 (1): 68–77.
59. Sheen P., O’Kane C.M., Chaudhary K. et al. High MMP"9 activity characterises pleural tuberculosis correlating with granuloma formation. Eur. Respir. J. 2009; 33 (1): 134–141.
Тактика при хронической эмпиеме плевры. Лечение бронхиальных свищей
Свищ пищевода – это появление соединения между пищеводом и окружающими его органами и тканями. Наиболее часто свищи формируются между пищеводом и трахеей, бронхами (пищеводно-трахеальные и пищеводно-бронхиальные), либо с плеврой и средостением (пищеводно-плевральные и пищеводно-медиастинальные).
Приобретенные свищи пищевода являются тяжелым заболеванием и требуют в своем лечении комплексного и персонифицированного подхода.
Причины появления свищей
Частой причиной развития приобретенных свищей являются гнойно-воспалительные осложнения после операций на пищеводе, легких и средостении.
Другими причинами могут служить:
- прорастание злокачественной опухоли,
- перфорация дивертикула пищевода и пептической язвы пищевода,
- туберкулез,
- абсцесс легкого,
- актиномикоз,
- перфорация при эзофагоскопии и бужировании пищевода,
- открытые и закрытые повреждения шеи, груди и живота.
Известны свищи опухолевого происхождения, травматические, а также свищи, возникающие при специфическом и неспецифическом воспалении.
Наиболее часто образуются свищи при злокачественных опухолях. Как правило, они возникают при распаде раковой опухоли пищевода, прорастающей в трахею и бронхи.
Чем опасны свищи
При формирования свищей пищевода возникает контакт внутренней среды организма с внешней. Бактерии извне проникают внутрь, запуская инфекционный процесс в грудной клетке. Это может приводить к развитию пневмонии, эмпиемы плевры, медиастинита.
Свищи пищевода являются относительно редким заболеванием, и настороженность врачей в плане их выявления снижена, что приводит к поздней диагностике, неправильной тактике лечения, несвоевременной специализированной помощи и нередко – к летальному исходу.
Виды свищей
Свищ пищевода может возникать в любом его отделе. Различают наружные и внутренние свищи пищевода в зависимости от того, куда именно происходит «открытие» свища.
- Наружные свищи открываются непосредственно в окружающую среду, на кожу (например, наружный свищ в шейном отделе).
- Внутренние свищи сообщаются, соответственно, с внутренними органами.
В результате появления «соединения» или канала между пищеводом и внешней или внутренней средой происходит поступление содержимого пищевода (съеденной пищи и слюны) в соответствующий орган или полость.
Наиболее тяжело протекающими являются пищеводно-респираторные свищи, при которых происходит попадание содержимого пищевода в легкие через трахеобронхиальное дерево. Это приводит к развитию хронического аспирационного синдрома и, зачастую, к рецидивирующей аспирационной пневмонии.
Симптомы
Симптоматика свищей пищевода зависит от его локализации, длительности заболевания, характера свища, размера, степени вовлечения окружающих структур.
Клинические проявления свищей пищевода значительно варьируют и во многом зависят от основного заболевания/состояния, которое привело к формированию свища у данного пациента.
К пищеводным симптомам при свищах относятся:
- затруднение при проглатывании пищи (дисфагия),
- боли при проглатывании,
- срыгивание съеденной пищей.
При наружном свище на коже отмечается появление свищевого хода (отверстия), из которого поступает содержимое, обычно, гноевидного характера с развитием воспалительных изменений в области свища.
Более сложным является диагностика внутренних свищей.
У большинства пациентов развиваются гнойно-вопалительные осложнения со стороны респираторной системы:
- гнойный бронхит,
- пневмония,
- бронхообструктивный синдром,
- абсцесс и гангрена легких,
- сепсис.
При отсутствии связи с трахеобронхиальным деревом такой яркой клинической картины может не быть. Заподозрить развитие пищеводного свища возможно по неспецифическим симптомам. К ним относятся:
- повышение температуры тела (от субфебрильных цифр до лихорадки),
- немотивированная слабость,
- одышка,
- снижение массы тела,
- серый или цианотичный оттенок кожных покровов.
Диагностика
Диагностика свищей пищевода должна носить комплексный характер.
- Обязательным является проведение рентгенографии и рентгеноскопии пищевода с водорастворимым контрастным веществом (барий использовать не рекомендуется, рисунок 1, 2).
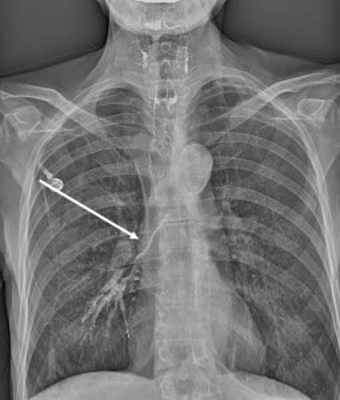
Рисунок 1. Пищеводно-респираторный свищ при рентгенографии/рентгеноскопии пищевода
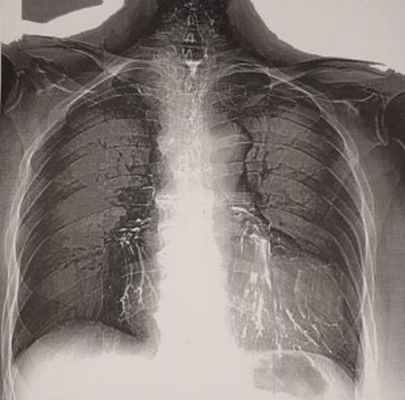
Рисунок 2. Остатки бария сульфата в бронхах у пациентки с пищеводно-бронхиальными свищами
- Эзофагогастродуоденоскопия для оценки состояния пищевода и верхних отделов желудочно-кишечного-тракта.
- Фибробронхоскопия для оценки состояния трахеобронхиального дерева и возможной верификации зоны свища.
- Сочетанная фибробронхоскопия и эзофагоскопия в том числе с применением красителей (метиленового синего).
- Мультиспиральная компьютерная томография шеи, органов грудной клетки и/или брюшной полости для обнаружения зоны свища, скоплений жидкости, оценки степени поражения легочной паренхимы, плевральной полости и средостения (рисунок 3).
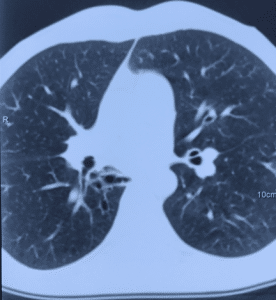
Рисунок 3. Вторичные бронхоэктазы и пневмофиброз нижней доли правого легкого у пациента с пищеводно-бронхиальным свищом и тотальной ожоговой стриктурой пищевода.
Лечение свища пищевода
Лечение может быть консервативным и хирургическим.
Первой задачей является исключение поступления пищи и жидкости в пищевод, что достигается за счет отказа от перорального питания (через рот). Для обеспечения питания пациента в этом случае может быть применено:
- парентеральное питание,
- назоинтестинальный зонд с установкой последнего за связку Трейтца,
- формирование гастростомы или энтеростомы.
С целью предотвращения рефлюкса содержимого желудка в пищевод в отдельных случаях может быть рекомендовано проведение фундопликации.
Обязательным является проведение нутритивной поддержки и антибактериальной терапии. В зависимости от тяжести состояния больного и вовлечения органов грудной клетки и брюшной полости в инфекционный процесс может быть проведено дренирование скоплений жидкости в области свища.
При бесперспективности консервативного лечения, прогрессировании признаков инфекционного процесса показано проведение радикального хирургического лечения.
Хирургический доступ зависит от локализации свища (на шее, в грудной клетке, в брюшной полости).
В зависимости от состояния болезни, операция может проводиться с сохранением или удалением пищевода.
При возможности выполнения органосохраняющей операции:
- Свищевой ход выделяют и иссекают.
- Дефекты стенки пищевода и другого органа поочередно ушивают.
- Линию швов дополнительно укрепляют местными тканями (плеврой, перикардом, мышцей, диафрагмой, сальником и т.п.).
В большинстве случаев при запущенных состояниях: хирургическое лечение может закончиться удалением пищевода с формированием эзофагостомы (для дренирования слюны) и гастро-энтеростомы для обеспечения энтерального питания.
После стабилизации состояния пациента, купирования инфекционного процесса, стабилизации массы тела пациенту будет предложено проведение реконструктивного вмешательства на пищеводе, которое включает проведение загрудинной пластики пищевода (рисунок 4).
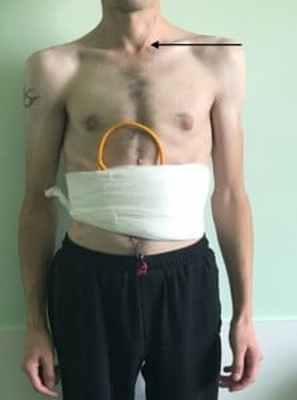
Рисунок 4. Пациент с этапным лечение пищеводно-бронхиального свища на фоне тотальной ожоговой стриктуры пищевода и ожоговым стенозом желудка. 1-м этапом пациенту была выполнена эзофагогастрэктмоия с формиованием эзофагостомы м энтеростомы для питания, лобэктомия нижней доли правого легкого. Через 3 месяца пациент поступил для проведения реконструктивного вмешательства на пищеводе. Стрелкой указана эзофагостома на шее (согласие пациента на публикацию фото получено).
Лечение в отделении торакоабдоминальной хирургии и онкологии
Приобретенные свищи пищевода являются грозным потенциально жизне-угрожающим заболеванием!
При подозрении на возникновение свища необходимо консультация в специализированном хирургическом отделении, имеющем опыт лечения пациентов со свищами пищевода и реконструктивных вмешательств.
Целесообразным представляется проведение этапного лечения данного заболевания. Положительный результат лечения можно получить при своевременной диагностике этой патологии, правильном планировании лечения и выполнения хирургического вмешательства в высокоспециализированном хирургическом стационаре.
Наше отделение имеет большой опыт лечения пациентов с приобретенными свищами различной локализации, как с проведение консервативного лечения, так и различных вариантов хирургических вмешательств (органосохраняющих, эзофагэктомии с последующим реконструктивным вмешательством и т.д.).
Лечение в отделении проводится по программам ОМС, ДМС, ВМП, а также на коммерческой основе.
Читайте, как попасть на лечение в отделение торакоабдоминальной хирургии и онкологии РНЦХ.
Для записи на консультацию позвоните по телефонам:
Отправьте заявку на консультацию, заполнив форму на нашем сайте и прикрепив необходимые документы.
Читайте также:
