Тимомы. Эпидемиология и строение тимом
Добавил пользователь Skiper Обновлено: 27.01.2026
В вилочковой железе развивается целый ряд разнообразных по строению и гистогенезу новообразований, большинство которых ранее обозначались термином – тимомы. В настоящее время термин «тимома» относится только к опухолям, развивающимся из эпителия паренхимы вилочковой железы, а все многообразие опухолей вилочковой железы подразделяется на две большие группы: органоспецифические, гистогенез которых связан с ее эпителиальным компонентом, и органонеспецифические. К последним относятся лимфомы, новообразования нейроэндокринного генеза, мякотные (фибромы, липомы, варианты сарком), нейрогенные и герминогенные опухоли, а также тератомы (рис. 77).
I. Органоспецифические опухоли вилочковой железы.
1. Тимомы. Наиболее часто встречающиеся опухоли средостения, составляющие 10-20% всех его новообразований. Для них типична локализация в верхнем отделе переднего средостения (рис. 78), хотя неоднократно описаны тимомы и в других его отделах, что обусловлено аберрантной локализацией тимоцитов.
Это своеобразные опухоли, к которым не применимы привычные понятия злокачественности и доброкачественности. Все они могут быть инвазивными или неинвазивными, причем эта важнейшая онкологическая характеристика определяется не морфологом, а хирургом во время операции.
Рис. 77. Классификация опухолей вилочковой железы.
Примерно в 2/3 наблюдений опухоли представляют собой солитарный узел, расположенный в нижних отделах или в центре долей вилочковой железы, но у 1/3 больных наблюдается мультицентрический рост опухоли, в основном в виде двух, реже – трех узлов, причем в разных участках органа.
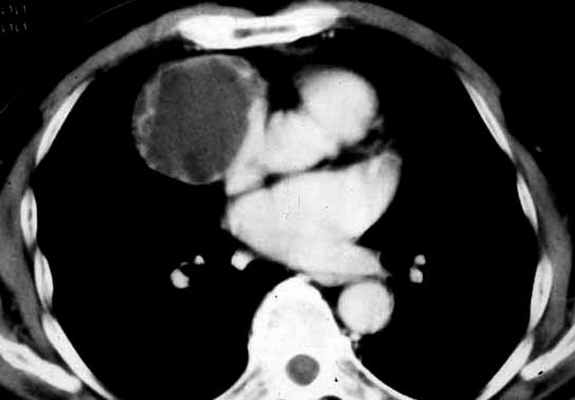
Рис. 78. Тимома передне-верхнего отдела средостения в виде округлой солитарной опухоли, примыкающей к грудине. Компьютерная томография.
В преобладающем большинстве случаев тимома представляет собой образование округлой или овальной формы (рис. 78), ограниченное фиброзной капсулой неравномерной толщины. Полностью инкапсулированная тимома имеет гладкую или слегка бугристую поверхность. Капсула часто содержит макроскопически заметные
участки кальцификации. Величина узлов варьирует от микроскопических до 20 см, а в случаях с выраженным инвазивным ростом опухоль может занимать все средостение, вес опухоли в большинстве случаев варьирует в пределах 150-300 г.
Консистенция опухолей от мягкой до плотно-эластичной. Небольшие инкапсулированные узлы имеют как правило более плотную консистенцию, в отдельных случаях хрящевидную.
Вид тимом на разрезе различный, ткань опухоли серо-розового цвета, с мелкими кистами, плотными серыми прослойками, реже – слоистая, или с очагами бурого, желтого или черного цвета (рис. 79).
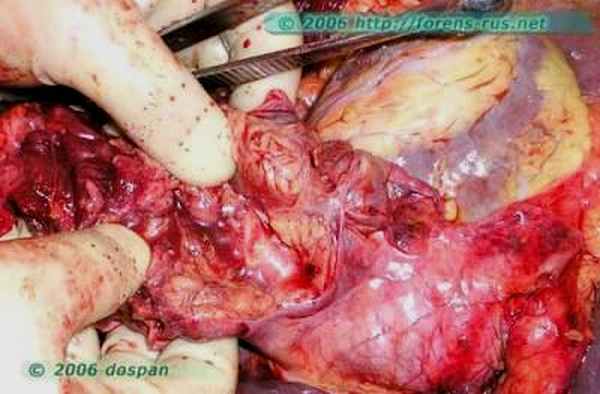
Рис. 79. Внешний вид тимомы на разрезе
Фиброзные прослойки, разделяющие основной узел на узлы и дольки различной величины, являются одним из самых характерных макроскопических признаков тимомы. Не менее характерным признаком является наличие кистозных полостей, чаще небольших размеров. Эти полости заполнены бесцветной или слегка желтоватой жидкостью. В крупных тимомах кистообразование связано с дистрофическими изменениями, в таких кистах могут обнаруживаться свертки крови или детрит различного происхождения. В подобных случаях также часто обнаруживаются очаги кальцификации.
В отдельных случаях целостность фиброзной капсулы тимомы может нарушаться, в тех участках, где капсула отсутствует, опухоль интимно спаяна с прилежащими тканями за счет инвазивного роста новообразования. Характер роста опухоли оказывает существенное влияние на прогноз, так как даже хорошо дифференцированные тимомы, инфильтрирующие капсулу, склонны к рецидивированию и иногда к внутриторакальному метастазированию.
По классификации, предложенной Monden Y. (1984), различают четыре стадии инвазии тимом:
1) полностью инкапсулированная опухоль без инвазии капсулы;
2) инвазия элементов опухоли в капсулу, окружающую жировую клетчатку и/или медиастинальную плевру;
3) инвазия элементов опухоли в прилежащие органы: легкое, перикард, крупные сосуды;
4) плевральная или перикардиальная дессиминация опухоли, интраторакальные органные метастазы.
Более поздняя классификация Американского ракового общества объединяет две последние степени инвазии в одну. Инвазивные тимомы (рис. 80) могут давать лимфогенное метастазирование, после удаления нередко рецидивируют в средостении, реже дают метастазы в других анатомических областях, причем обычно в мягких тканях. Еще реже наблюдается гематогенная диссеминация по паренхиматозным органам и костям скелета.
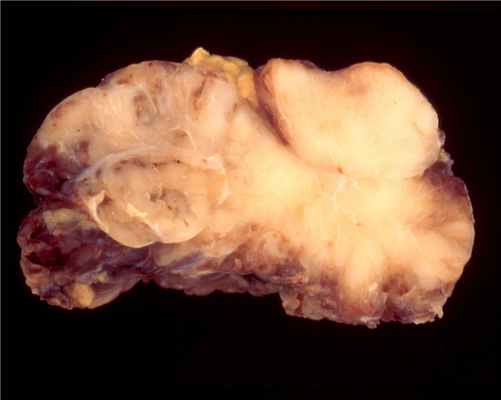
Рис. 80. Внешний вид инвазивной тимомы.
По морфологической структуре тимомы классифицируются как.
а) с кортикально-клеточной дифференцировкой;
б) с медуллярно-клеточной дифференцировкой.
а) с кортикально-клеточной дифференцировкой,
б) с медуллярно-клеточной дифференцировкой.
3. Смешанноклеточные (из светлых и темных клеток)
Данная классификация основана на следующих критериях:
тимомой является опухоль вилочковой железы, состоящая из двух компонентов: эпителиального (опухолевые клетки без или с минимальной атипией) и
лимфоидного (не подвергающиеся опухолевой трансформации, обычные для вилочковой железы Т-лимфоциты на разных этапах созревания);
варианты тимом выделяются на основании светооптического и/или ультраструктурного сходства эпителиальных клеток с кортикальными или медуллярными эпителиальными клетками неизмененной вилочковой железы;
учитывается гормональная активность тимом, косвенным признаком которой является состояние сохранившейся ткани вилочковой железы;
используются результаты клинико-морфологического анализа, выявившего связь между выделенными вариантами тимом, их клиническим проявлением и степенью злокачественности.
Светлоклеточные тимомы составляют около 60% (50% инвазивные). Смешанноклеточные тимомы 38% (50% инвазивные). Темноклеточные тимомы составляют лишь 2% наблюдений, а инвазии среди них не наблюдалось.
Исходя из гистогенеза эпителиальных клеток опухоли, выделяют кортикальноклеточные, медуллярноклеточные и смешанноклеточные тимомы. Медуллярноклеточные тимомы в большинстве своем являются доброкачественными и могут быть причиной иммунных дефицитов с гипогамма-глобулинемией, гипопластической анемией. Кортикальноклеточные тимомы отличаются агрессивным течением, сопровождаются развитием аутоиммунных заболеваний, прежде всего миастении.
На основании последней гистологической классификации, предложенной ВОЗ в 1999 году, тимомы подразделяют на тип А и В на основании их гистологической и иммунофенотипической близости к клеткам кортикального или медуллярного слоев тимуса. В классификации ВОЗ разработанные гистологические типы обозначены буквенными индексами:
тип А медулярноклеточная тимома,
тип АВ смешанноклеточная тимома,
тип В1 – тимома преимущественного кортикального типа,
тип В2 – кортикальноклеточная тимома,
тип В3 высокодифференцированная карцинома,
тип С соответствует недифференцированным карциномам.
Преимущество новой классификации состоит в том, что выделенные варианты строения тимом сильно коррелируют с прогнозом заболевания, что помогает выбрать правильную тактику лечения. Так, например B2 и B3 опухоли отличаются агрессивным течением, инвазивностью и высокой вероятностью рецидивов при сравнении с опухолями типов A, AB и B1. Последние отличаются доброкачественным течением, протекают бессимптомно и сочетаются с иммунным дефицитом. Кроме этого, тимомам типов A, AB и B1 свойственна полная резектабельность, в отличие от типов B2 и B3.
По клинической симптоматике можно выделить три группы больных:
1) с бессимптомно протекающей тимомой;
2) с наличием клинических признаков синдрома сдавления соседних органов;
3) с сопутствующими синдромами или с сочетанием синдрома сдавления и сопутствующих синдромов.
Другая важнейшая клиническая характеристика тимом их возможная связь с миастеническим синдромом, в зависимости от чего их делят на миастенические и немиастенические. Этот признак имеет первостепенное прогностическое значение: если больные с инвазивными немиастеническими тимомами гибнут в основном от рецидивной опухолевой инвазии, то пациенты с миастеническими тимомами от прогрессирования миастенической симптоматики.
Сопутствующие синдромы в виде аутоиммунных заболеваний сопровождают 40% опухолей тимуса. Наиболее часто наблюдается генерализованная миастения, реже – другие аутоиммунные заболевания, в частности системная красная волчанка, дерматомиозит, системная склеродермия, идиопатическая болезнь Аддисона, диффузный токсический зоб, гемолитическая анемия. Частота опухолей вилочковой железы у больных генерализованной миастенией составляет 10-20%. Несомненно, что развитие заболевания в большинстве случаев связано с опухолями вилочковой железы. На это указывает их необычайно высокая частота при генерализованной миастении, повышение титра аутоантител к антигенам мышечных клеток и ацетилхолиновым рецепторам у больных с тимомами, даже без клинических проявлений заболевания, положительный эффект операции тимэктом. Иногда генерализованная миастения может развиваться при неопухолевом поражении вилочковой железы, а опухоль возникнуть уже в ходе болезни.
Генерализованная миастения (Myasthenia gravis) – органонеспецифическое аутоиммунное заболевание из группы антительных болезней рецепторов, клинически проявляющееся слабостью и патологической утомляемостью разных групп поперечно-полосатых мышц. Частота генерализованной миастении в популяции составляет 0,1 на 1000 человек, соотношение мужчин и женщин 1:2, средний возраст 30-40 лет. Патогенез генерализованной миастении связан с аутоантителами к ацетилхолиновым рецепторам – гетерогенной группой поликлональных аутоантител классов IgG, реже IgM или IgA, способных блокировать, повреждать или ускорять деградацию ацетилхолиновых рецепторов постсинаптической мембраны нервно-мышечных синапсов поперечно-полосатых мышц, что нарушает нервно-мышечную передачу.
Патологические изменения в вилочковой железе, согласно литературным данным, при генерализованной миастении отмечаются у 90-100% больных. Сопоставление результатов детального морфологического исследования вилочковой железы с клинико-иммунологическими показателями позволили выделить две формы генерализованной миастении при неопухолевом поражении этого органа:
1-я форма генерализованной миастении характеризуется гиперпродукцией тимических гормонов, гиперплазией или возрастной нормой объема истинной паренхимы вилочковой железы, чаще встречается у детей и женщин;
2-я форма – дефицитом тимических гормонов и атрофией истинной паренхимы вилочковой железы, встречается главным образом у взрослых больных.
Симптоматология миастении многообразна и выраженность миастенических расстройств различна у каждого индивидуума. Общим и классическим симптомом для всех больных является мышечная слабость и патологическая утомляемость, которая приводит к псевдопаралитическому состоянию отдельных мышечных групп либо мускулатуры в целом. Специфическая особенность утомления характеризуется исчезновением ее после отдыха и введения антихолинэстеразных препаратов. Наиболее частым начальным проявление миастении является птоз, диплопия, ограничение подвижности глазных яблок. Поражение мимической мускулатуры проявляется амимией либо гипомимией. Нередко встречается слабость жевательных мышц и отвисание нижней челюсти. Наиболее патогномоничными для миастении являются бульбарные нарушения – расстройства фонации, артикуляции, акта глотания. При тяжелых формах миастении и в терминальных стадиях поражается дыхательная мускулатура, что приводит к асфиксии. Со стороны опорно-двигательного аппарата описаны нарушения походки, выраженная мышечная слабость в конечностях, которая затрудняет обычные для больного процедуры.
Удаление тимуса ведет к частичной или полной ремиссии Myasthenia gravis, подтвержденной уменьшением или прекращением медикаментозной терапии у 60-80% пациентов.
2. Рак вилочковой железы. К органоспецифическим опухолям также относится рак вилочковой железы. В группу раков вилочковой железы входят опухоли из эпителиальных клеток, потерявшие признаки органоспецифичности. Все эти новообразования характеризуются обычными признаками злокачественности: выраженной анаплазией клеток, их полиморфизмом, большим количеством митозов. Большинство из них отличаются быстрым ростом, прорастают в окружающие органы, дают имплантанты по плевре и перикарду, метастазируют. В вилочковой железе встречаются различные варианты плоскоклеточного рака, аденокарциномы, недифференцированного рака и др.
Выделяют следующие разновидности раков вилочковой железы: 1) плоскоклеточный, 2) веретеноклеточный, 3) недифференцированный (анапластический), 4) лимфоэпителиальный, 5) светлоклеточный и 6) мукоэпидермальный.
Наиболее часто встречающейся разновидностью рака вилочковой железы является плоскоклеточный рак. Как и в других органах, следует различать: 1) высоко, 2) умеренно и 3) малодифференцированные варианты плоскоклеточного рака вилочковой железы. Высоко дифференцированный плоскоклеточный рак также обозначается как эпидермоидная тимома. Основанием для такого выделения является некоторое отличие клинического течения: имеются наблюдения длительного существования эпидермоидных тимом в виде солитарного узла с незначительными темпами роста. Строма плоскоклеточных раков, как правило, хорошо развита. Пласты опухолевых клеток окружены прослойками различной ширины, образованными либо рыхловолокнистой соединительной тканью, инфильтрированной различного типа лейкоцитами, либо гиалинизированной фиброзной тканью.
Тимомы. Эпидемиология и строение тимом
Тимомы. Эпидемиология и строение тимом
Тимомы — новообразования зобной железы — не представляют исключительной редкости, однако до сих пор эти опухоли не достаточно изучены, как не изучена и функция зобной железы. Зобная железа — thymus — может быть названа лимфатическим органом, хорошо развитым в детском возрасте. Ее инволюция происходит в период полового созревания (12—14 лет), но рудиментарные остатки железы сохраняются и во взрослом состоянии человека.
Обычно зобная железа располагается в нижнем отделе шеи и верхнепереднем средостении и состоит из двух долей — правой и левой, соединяющихся между собой с помощью небольшого слоя клетчатки. Шейная часть железы несколько выступает над рукояткой грудины и во время вдоха погружается в средостение. Спереди своей правой долей она прилежит к грудине, сзади соприкасается с трахеей, правой безымянной и внутренней яремной венами, основанием правой общей сонной и правой подключичной артерий, правым блуждающим нервом. Позади левой доли железы лежат левая безымянная и нижняя щитовидная вены, левая подключичная и левая общая сонная артерия, а также левый блуждающий нерв.
Нижняя часть зобной железы лежит на аорте, перикарде. Боковые поверхности обеих ее долей прикрываются плевральными мешками в их медиастинальных отделах. Кровоснабжение thymus происходит за счет аа. mammaria interna aa. thyreoidea inferior — ветвей a. anonyma и от аа. pericardiaco-phrenicae. Иннервируют железу ветви блуждающих и симпатических нервов.
При гистологическом исследовании зобной железы в ее массе определяются два слоя — корковый и мозговой. Корковое вещество железы имеет аденоидную структуру с рассеянными лимфоцитами (тимоциты). Мозговое вещество по своему строению сходно с корковым, но в нем определяется много клеток со светлыми ядрами и меньше лимфоцитов. В нем, кроме того, располагаются так называемые гассаловы тельца, имеющие округлую или несколько удлиненную форму, с крупными клетками в центре. Эти клетки нередко характеризуются признаками дегенерации. Гассаловы тельца находят в зобной железе 3-месячного зародыша, а затем в процессе созревания организма они гибнут. Функция этих телец недостаточно известна, но им приписывают секреторные влияния (они гибнут при секреции — «гипокринные железы»). До сих пор еще роль зобной железы в гормональной системе человека выявлена крайне недостаточно, однако многие приписывают ей значение органа роста и питания (Г. П. Сахаров, 1929).
В начале XIX столетия существовало мнение, что большинство опухолей средостения происходит из зобной железы. После того как заболевания органов грудной полости стали диагностироваться чаще и точнее (введение рентгенологических методов исследования), это мнение было отвергнуто и в настоящее время установлено, что тимомы среди новообразований средостения наблюдаются лишь в 5—10% случаев.
В 1954 г. Дивиш опубликовал свою монографию об опухолях и кистах средостения, в которой большое внимание уделено тимомам. Автор собрал из литературы 510 наблюдений медиастинальных опухолей, в числе которых было 53 тимомы (10%). В настоящее время это количество нужно увеличить до 210 (оперированные больные). В специализированных торакальных клиниках данные новообразования выявляются чаще. Так, например, Эффлер и Мак Кормак (Effler, McCormac, 1956) сообщили о 26 случаях тимом. При тщательном изучении гистологических препаратов опухоли в дальнейшем из этого числа было исключено 7 случаев, когда не было картины истинной тимомы (дермоиды, метастазы семиномы, гипертрофия зобной железы).
Наибольшим числом наблюдений располагает клиника Мейо, где произведено 45 операций по поводу тимом [Зейболд, Мак Дональд, Кледжет, Гуд (McDonald, Clagett, Good и др., 1950)].
В отечественной литературе успешная операция при тимоме впервые описана нами в 1954 г. По данным мировой литературы, тимомы чаще имеют злокачественный характер, однако наши наблюдения этого не подтверждают.
В 1911 г. С. М. Рубашов собрал в мировой литературе 69 случаев злокачественных тимом, а Д. Г. Александровский к 1929 г. опубликовал 154 аналогичных наблюдения. Больные в основном не были оперированы.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Тимома
При этом заболевании метастазы в основном распространяются в грудной клетке: плевре (оболочка, плотно облегающая легкие и стенку грудной полости), перикарде (наружная соединительнотканная оболочка сердца), диафрагме, которые случаются редко, но в некоторых случаях случаются рецидивы спустя более 10 лет после хирургического лечения.
На долю данного заболевания приходится 20–25 % от всех опухолей средостения. Пик заболеваемости находится между 35 и 70 годами.
По системе Всемирной Организации Здравоохранения выделяют шесть типов тимом: А, АВ, В1, В2, В3, С. По мере прогрессирования от А к С отмечается ухудшение прогноза, снижение выживаемости.
В 30 % случаев заболевание протекает бессимптомно, и часто случайно обнаруживаются при рентгенографическом исследовании. Около 40 % пациентов предъявляют жалобы на болевой синдром в области грудной клетки, кашель, связанные с локальным воздействием опухоли. Главной особенностью этой опухоли является связь с аутоиммунной патологией, иммунодефицит и аутоиммунные реакции организма. Самым частым и тяжелым проявлением аутоиммунных нарушений является миастенический синдром (заболевание нервной и мышечной системы, которое характеризуется слабостью и патологической утомляемостью поперечно-полосатых мышц), а также в редких случаях анемией. Часто тимомы сочетаются с другими иммунными расстройствами, такими как лейкойз, лимфома, ревматоидный артрит.
Пациенты с тимомами имеют повышенный риск развития дополнительных злокачественных новообразований различных локализаций.
Мультиспиральная компьютерная томография (МСКТ) с контрастированием.
Рентгенограмма органов грудной клетки.
Магнитно-резонансная томография (МРТ).
Позитронно-эмиссионная томография, совмещенной с КТ (ПЭТ-КТ).
Тонкоигольная аспирационная биопсия (ТАБ) –метод морфологической верификации новообразований средостения.
Неоадъювантная терапия по схеме CAP (циклофосфамид, доксорубицин, цисплатин.
- Лучевая терапия СОД 50 Гр.
- Хирургические методы лечения, включающие в себя малоинвазивные торакоскопические операции на вилочковой железе.
Клинический случай пациента МКНЦ.
Мужчина 38 лет обратился в МКНЦ с жалобами на слабость в руках. Первые симптомы появились еще в 2017 году, но после ухудшения состояния в 2018 году он обратился в наш Центр. При обследовании специалистами МКНЦ пациенту был установлен диагноз неврит лицевого нерва. Была проведена необходимая терапия, которая временно дала положительный эффект.
В марте 2019 года у пациента появились трудности с дыханием и глотанием, поэтому он был госпитализирован с подозрением на ангионевротический отек. После осмотра ЛОР-врачом ангионевротический отек исключен, а неврологом установлен диагноз: миастения прогрессирующая форма, бульбарный тип. При дообследовании в МКНЦ проведены УЗИ и КТ и выявлено опухолевое образование тимуса.
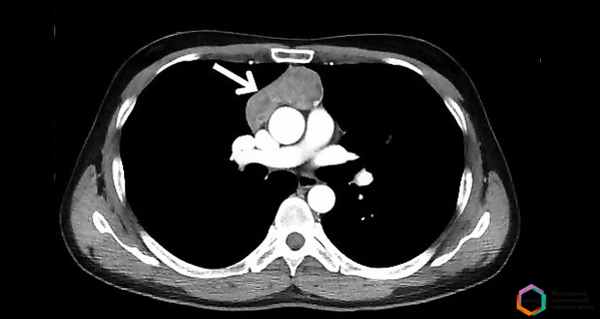
Пациенту была проведена консервативная терапия, после чего он был госпитализирован для проведения торакоскопической тимомэктомии.
Пациенту выполнено торакоскопическое удаление опухоли тимуса, удалённый материал отправлен на плановое патоморфологическое исследование.
Данный гистологический тип тимомы отличается наилучшим прогнозом в случае радикальной операции. Специалисты нашего Центра назначили пациенту оптимальное лечение, направленное на снижение рисков развития рецидивов данного заболевания и улучшение качества жизни. Пациент выписан, на данный момент чувствует себя хорошо, жалоб не имеет.
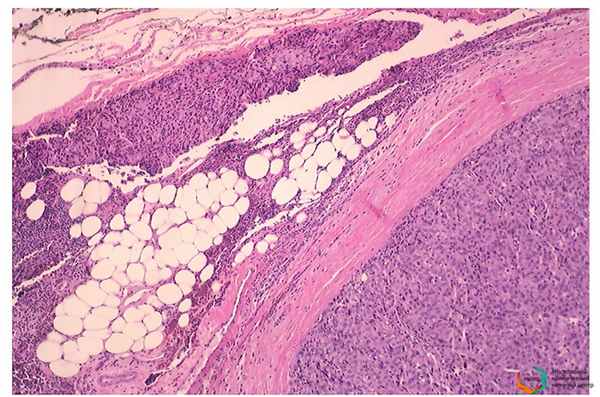
Эта патология является редкой, частота встречаемости заболевания 0,13% на 100 000 населения. С этим связана трудность обследования для достоверной постановки диагноза, что требует от пациента своевременного обращения в высоко специализированные медицинские учреждения.
Новообразования средостения (часть 2)
Стенограмма второй части видеолекции профессора Игоря Евгеньевича Тюрина о новообразованиях средостения из цикла передач Лучевая диагностика для терапевтов.
Игорь Евгеньевич Тюрин, профессор, доктор медицинских наук:
- Другая распространенная проблема этой же области (я ее показываю специально, чтобы было понятно, насколько иногда непросто для врача-рентгенолога определить, о чем идет речь в этой ситуации) – тератома.
Чаще эти опухоли встречаются у более молодых пациентов. Большинству из них меньше 30-ти лет, в отличие от тимом. Большинство пациентов имеют явные клинические симптомы. Это опухоли, растущие и приводящие к сдавлению или оттеснению анатомических структур в грудной полости.
Тем не менее, большинство из них доброкачественные. Это один из наиболее частых вариантов герменогенных опухолей. Лучевые признаки обычно точно там же, где и располагаются тимомы, перед восходящей аортой. Четко очерченное округлое образование. Но, в отличие от тимомы как мягкотканого образования, иногда жировые включения, костные фрагменты, иногда даже фрагменты зубов – то, что позволяет рентгенологу сформулировать, предположить правильный диагноз.
Хотя если этого нет, то на обзорных снимках очень сложно сказать, что это такое. Такое же овальное патологическое образование в переднем средостении. Контрастированный пищевод, который проходит по задней поверхности сердца и вдоль задней стенки трахеи.
Но сказать на основании обзорной рентгенограммы, что это такое, может быть крайне сложно. Любое патологическое образование. Почему мы говорим, что это термоидное образование, герменогенная опухоль. Внутри мы видим включение жировой клетчатки, кистозные включения, множественные перегородки.
Расположение точно такое же – переднее средостение, средний этаж. Но достаточно характерная картина, которая позволяет говорить о том, что это такое и предпринимать соответствующее лечение.
Еще один очень важный признак, который позволяет нам иногда правильно характеризовать характер патологического образования в средостении – это взаимосвязь с другими анатомическими структурами. Классикой жанра здесь является внутригрудной зоб. Он чаще возникает у женщин. Чаще это патология у людей старше 40 – 45 лет. Достаточно частые по статистике образования.
Несмотря на очень большие размеры, оно длительное время может протекать бессимптомно. Важно, что почти всегда мы можем наблюдать связь со щитовидной железой. Это образование располагается в области верхней апертуры. Может быть в переднем или заднем средостении. Как правило, оттесняет и суживает трахею, что на рентгеновских снимках создает очень характерную типичную картину.
Если вы посмотрите на обзорный снимок в прямой проекции, то сразу же будет видно, насколько изменилась конфигурация воздушного столба в трахее на уровне грудино-ключичных расчленений и выше в области верхней апертуры. Трахея оттеснена по дуге вправо и практически достигает контура средостения и несколько сужена.
Почему? Ответ на этот вопрос в компьютерно-томографическом исследовании. Два огромных узла, один из которых располагается на шее. Второй в переднем средостении. Оба гиперваскулярны, неоднородной структуры. Это типичная картина огромных размеров внутригрудного зоба, который занимает переднюю часть средостения.
Еще одна особенность патологических образований, когда мы говорим об их локализации. Лимфомы, если говорить о преимущественной локализации этих патологических образований, часто занимают тот же средний этаж переднего средостения, что и тимомы и герменогенные опухоли. Но очень часто по характеру клинического течения, по дополнительным признакам они отличаются.
Здесь самое главное – системные поражения. Это поражения многих групп лимфатических узлов, в том числе и периферических лимфатических узлов, с чего начинается обследование такого пациента. Патология возникает либо в молодом возрасте 20-ти лет, либо старше 50-ти лет.
Это патологическое состояние разделяется на две большие группы. Сейчас это болезнь Ходжкина и злокачественные неходжкинские лимфомы (ЗНЛ). Последние чаще встречаются у людей более старшего возраста. По количеству они значительно чаще встречаются.
Но если говорить о патологии средостения, то там болезнь Ходжкина занимает первое место по частоте. Проявления одинаковые. Мы редко можем предположить нозологическую принадлежность, гистологическую форму, тип патологического процесса. Но когда мы видим отдельные увеличенные лимфатические узлы в переднем средостении или когда это сочетается с увеличением периферических лимфатических узлов, с характерной клинической симптоматикой, тогда предположение врача-рентгенолога становится более понятным и очевидным.
Расширение тени средостения на обзорном снимке влево в области аорто-пульмонального окна, в области талии сердца и при томографическом исследовании прекрасно виден конгламерат увеличенных лимфатических узлов, которые располагаются в переднем средостении. Объемные образования, которые состоят из множества лимфатических узлов, отличают такой процесс от обычных опухолей средостений.
С другой стороны, эти лимфатические узлы могут вырастать в патологическое образование, которое совершенно неотличимо ни от каких других опухолей средостений, с признаками инвазии, с вовлечением в грудной стенке, со сдавлением крупных сосудов, со стеснением и сужением трахеи главных бронхов.
В этой ситуации требуется морфологическая верификация, чтобы ответить на вопрос: что это за патологический процесс.
В качестве иллюстрации: почему рентгенологи предпочитают разделять средостения на различные части, отделы. Патология заднего средостения, которая совершенно отличается по нозологии от того, что мы видим в передней части средостения, потому что здесь может встречаться внутригрудной зоб.
Но все-таки это территория, где чаще возникают нейрогенные опухоли, где обычно локализуются бронхо- и энтерогенные кисты, могут увеличиваться лимфатические узлы при лимфомах, но очень редко, где возникают значительные аневризмы аорты в области дуги нисходящей части. Классикой жанра здесь являются нейрогенные опухоли. Иногда совсем маленькие, они случайно выявляются при рентгеновском исследовании.
Небольшое патологическое образование, которое по форме напоминает нисходящую часть аорты в поперечном сечении. Бессимптомное течение. Обычно 3-я или 4-я декады жизни, округлая форма, четкие контуры, тканевая плотность. Очень часто кальцификация, кисты. Самое главное – абсолютно типичная локализация в большинстве случаев в реберно-позвоночном углу.
В этом случае, даже если у нас есть обычное компьютерно-томографическое исследование, без всякого контрастирования, информации, локализация в заднем средостении, которая четко определяется по обзорным снимкам, проекция патологического образования на тень позвонков, которая позволяет нам говорить, что это образование находится в реберном позвоночном углу.
Подтверждение этому томографическое исследование со всеми типичными характерными признаками. По компьютерной томографии мы хорошо видим, что это образование не внедряется в позвоночный канал. В этом случае можно не выполнять МРТ.
В тех случаях, когда эти опухоли (что, к счастью, бывает редко) озлокачествляются и приобретают крупные размеры, тогда судить о природе, источнике чрезвычайно сложно. Это злокачественная нейрогенная опухоль, которая привела к оттеснению средостения в противоположную сторону – в сторону правого легкого с накоплением жидкости в правой половине плевральной полости.
Огромных размеров патологическое образование, оттесняющее аорту впереди в сторону сердца, занимающее практически всю левую половину грудной полости, оттесняющее селезенку, почку и диафрагму вниз. Это злокачественная нейрогенная опухоль. Но сказать о том, что эта опухоль исходит из нервных образований, при томографическом исследовании очень сложно и не всегда возможно.
Почему мы не можем сегодня ограничиваться только этими данными, только локализацией. Конечно, возможные ошибки. Различные опухоли могут располагаться в одном и том же отделе средостения. Мы это видели на примере средней части переднего средостения.
С другой стороны, одинаковые опухоли могут располагаться в совершенно различных отделах средостения. Классикой в этом случае являются нейрогенные опухоли, которые могут встречаться не только в заднем, но и в переднем, центральном средостении.
Здесь важен еще один вид анализа при лучевом исследовании. Это структура патологического образования. То, что мы очень плохо можем различить на обычных обзорных рентгенограммах, на линейных томограммах. Мы всегда говорим о том, что подозрение на патологическое образование в средостении есть прямое показание к выполнению компьютерной томографии или магнитного резонанса.
В зависимости от того, что мы обнаруживаем в этом случае (скопление жидкости, жира или необычные реакции на контрастное вещество, его избыточное накопление или обызвествления), мы можем более глубоко и более точно оценить характер этих образований.
Жиросодержащие образования (мы сегодня уже говорили о герменогенных опухолях и тератомах), которые отличаются от всех остальных образований тем, что содержат заключения жира. Другим таким же примером являются грыжи диафрагмы, которые очень часто вызывают затруднения при обычном рентгенологическом исследовании. Избытки жира скапливаются в области реберных диафрагмальных синусов, в области сердца или позвоночника.
В этом случае возникает предположение, нет ли здесь патологического образования, опухоли, которая требует хирургического лечения. Если этот вопрос нельзя решить на основании рентгеновского исследования, то томографическое исследование четко показывает скопление чаще всего жировой клетчатки.
Никаких сомнений в том, что здесь нет злокачественной опухоли и вообще опухоли, не остается. На этом процесс диагностики заканчивается.
Грыжи различаются по локализации, по характеру. Это описано в большинстве руководств и учебников. Я не буду на этом сейчас останавливаться. Другим примером такой же дифференциальной диагностики является кистозное образование, очень частое, особенно у детей.
Речь идет в том числе о врожденных кистах. Это примерно 20% всех патологических образований средостений. Каким образом их можно отличить от солидных опухолей той же локализации. По денситометрическим характеристикам.
Наиболее частые бронхогенные кисты, которые локализуются в паратрахеальной правой области или около бифуркации трахеи. Как правило, имеют плотность жидкости, если у них не возникает или не накапливается растворимый кальций. Тогда плотность может повышаться и в существенно большей степени.
Типичная локализация расположения патологического образования в правой паратрахеальной области. Контрастированная верхняя полая вена в том и другом случае смещены впереди. Само патологическое образование прилежит к правой стенке трахеи. Типичная локализация.
Очень часто такие пациенты выявляются при первом же флюорографическом исследовании. У них определяется расширение тени средостения вправо. Это может интерпретироваться как проявление увеличения лимфатических узлов. Нередко – как проявление туберкулезного поражения лимфатических узлов. Вследствие этого начинается лечение без томографического исследования.
Выполнение томографии здесь позволяет сразу же исключить какие-то воспалительные патологические процессы.
Про обызвествления мы уже говорили. Это внутригрудной зоб, тератомы, лимфатические узлы.
В заключение на чем бы мне хотелось остановиться сейчас – это мягкотканые образования, которые в некоторых случаях имеют либо обычную, либо не совсем обычную реакцию на введение контрастного препарата.
Обычное усиление, обычная реакция – так же как реагируют тканевые структуры – наблюдаются при тимомах, невриномах, герминогенных опухолях, мезенхимальных опухолях (фибромы, миомы и так далее), при злокачественных лимфомах. Здесь нет никакой специфики.
Локализация этих патологических образований в сочетании с другими признаками иногда позволяет предположить правильный диагноз. То, что имеет важное значение – в некоторых случаях мы видим обызвествления или повышенную плотность при первичном исследовании. Это характеризует, например, внутригрудной зоб или свежие гематомы.
Самое интересное – это необычная реакция на введение контрастного вещества. Она наблюдается в виде исключительно высокого повышения плотности патологического образования. Такие изменения мы наблюдаем у больных с внутригрудным зобом, при опухолях паращитовидных желез, при болезни Кастлмана, при некоторых формах карциноидных образований средостений.
Это характерная картина, которая должна подлежать интерпретации. Мы опять возвращаемся к опухолям, исходящим из щитовидной железы, которые через верхнюю апертуру спускаются вниз в область грудной полости средостения. Типичные, это хорошо видно, характерные проявления этого патологического образования с оттеснением средостения и локализацией его в области верхней апертуры.
Насколько повышает плотность это патологическое образование. Оно практически соответствует по плотности сосудистым структурам средостения, контрастированию крови в сосудах и камерах сердца. Это характерно для тканей щитовидной железы.
Другой пример. Болезнь Кастельмана. Здесь специально оставлены денситометрические показатели. Средняя плотность образования, которое располагается между типичных образований, между восходящей и нисходящей аортой и оттесняет трахею сзади и справа, составляет почти 140 или 150 единиц (неразборчиво, 15:07).
Практически так же как контрастированная кровь. Очень немногие патологические образования средостения реагируют таким образом на введение контрастного вещества. В этом случае сочетание точной локализации и реакции на контрастный препарат позволяют предположить правильный диагноз.
Но, с другой стороны, в некоторых случаях, особенно когда речь идет о мезенхимальных опухолях, как в данном случае – ангиомиосаркоме, мы видим избыточную васкуляризацию таких патологических образований, все признаки злокачественного процесса. Но сделать здесь какое-либо морфологическое заключение очень сложно. Это может быть сделано только на основании гистологического исследования самого патологического образования.
Подводя итог сегодняшнему разговору о томографическом исследовании, вообще о лучевом исследовании при патологии средостения и при новообразованиях средостения, хочу еще раз подчеркнуть, что первичные выявления – это выявления с помощью рентгеновских исследований, рентгенографии в прямой и боковой проекции.
В качестве уточняющих методов чаще всего это компьютерная томография. Обычно с внутривенным контрастированием, чтобы мы могли точно разграничить образования на две большие части. По их локализации в средостении и по реакции на введение контрастного вещества.
В этом случае мы можем четко определить и локализацию изменений и взаимоотношения с прилежащими структурами. Нередко поставить и нозологический диагноз.
Тимома
Тимомы — опухоли, которые развиваются из эпителиальных клеток вилочковой железы (тимуса). Этот орган находится в грудной клетке, в области, которая называется передним средостением, в нем происходит созревание и «обучение» иммунных . Тимус функционирует у детей, достигает максимального размера у подростков, а затем постепенно исчезает — происходит его инволюция.


Тимомы могут возникать в любом возрасте, чаще всего у людей 40–60 лет.
Типы тимомы
Термин «тимома» собирательный, он объединяет довольно много разных эпителиальных опухолей. Существуют злокачественные тимомы (иногда их называют раком тимуса) и доброкачественные, причем, четкой границы между ними не существует. Степень злокачественности определяется способностью опухоли прорастать в окружающие ткани.
Чаще всего — примерно в 90% случаев — тимомы возникают в переднем средостении. В 5–10% случаев их обнаруживают в области шеи, в среднем и заднем средостении. Считается, что такое нехарактерное расположение опухоли связано с добавочными дольками тимуса.
Помимо эпителиальных опухолей, в тимусе встречаются новообразования из лимфоидной ткани. Они называются лимфомами. Очень редко в вилочковой железе развиваются нейроэндокринные опухоли.
Почему развивается заболевание?
Причины и факторы риска опухолей вилочковой железы на данный момент изучены недостаточно.
Известно, что 30–40% людей с тимомами параллельно заболевают миастенией гравис — патологией, при которой иммунная система разрушает рецепторы на поверхности поперечнополосатых мышц, в результате чего возникает их слабость, повышенная утомляемость. В 5% случаев тимомы ассоциированы с такими состояниями, как дерматомиозит, истинная эритроцитарная аплазия, синдром Кушинга, системная красная волчанка, синдром неадекватной секреции антидиуретического гормона.
Позаботьтесь о себе, запишитесь на консультацию сейчас
Стадии и типы заболевания
При стадировании инвазивных тимом можно руководствоваться общепринятой международной классификацией TNM. Буквы в этой аббревиатуре, соответственно, обозначают состояние первичной опухоли, наличие очагов поражения в регионарных лимфатических узлах и отдаленных метастазов:
Не удается оценить первичную опухоль.
Первичная опухоль не обнаруживается.
- Опухоль распространяется только на жировую клетчатку, окружающую вилочковую железу (T1a).
- Опухоль проросла в плевру — тонкую оболочку из соединительной ткани, выстилающую изнутри грудную полость и покрывающую легкие (T1b).
Опухоль прорастает в окружающую жировую клетчатку и околосердечную сумку (перикард).
Опухоль прорастает в соседние ткани и органы: легкие, кровеносные сосуды легких, диафрагмальный нерв.
Опухоль прорастает в трахею, пищевод, крупные кровеносные сосуды.
Не удается оценить состояние регионарных лимфоузлов.
Опухолевые очаги в регионарных лимфатических узлах отсутствуют.
Опухолевые очаги в близлежащих лимфатических узлах.
Опухолевые очаги в лимфоузлах в области шеи или внутри грудной полости.
Отдаленные метастазы не обнаружены.
Многие онкологи используют классификацию Masaoka/Koga, она считается наиболее удобной и предусматривает деление всех опухолей вилочковой железы на 4 стадии:
Опухоль находится в пределах тимуса, не прорастает его капсулу.
Опухоль прорастает капсулу органа и распространяется в окружающую жировую клетчатку:
- Прорастание капсулы видно только под микроскопом (IA).
- Прорастание капсулы видно невооруженным глазом (IB).
Опухоль прорастает в соседние органы:
- Вторгается в крупные кровеносные сосуды (IIIA).
- Не вторгается в крупные кровеносные сосуды (IIIB).
- Очаги в лимфатических узлах ().
- Отдаленные метастазы (M1).
Специальная система классификации была разработана в 2004 году экспертами Всемирной Организации Здравоохранения. Она подразумевает деление тимом на шесть типов, в зависимости от гистологического строения:
Веретеноклеточные, или медуллярные, тимомы. Отличаются хорошим прогнозом. Практически все пациенты, у которых установлен такой диагноз, живут 15 лет и дольше.
Смешанные тимомы. Под микроскопом внешний вид опухолевой ткани напоминает тимому B, но в нем присутствуют лимфоциты.
Такие тимомы называют богатыми лимфоцитами, лимфоцитарными, преимущественно кортикальными, органоидными. В них, как следует из названия, много лимфоцитов. Также отличаются хорошим прогнозом. Примерно 90% пациентов остаются живы в течение 20 лет и дольше, после того как у них установлен такой диагноз.
Кортикальная тимома. Напоминает тип B1, в ней также содержится много лимфоцитов, но эпителиальные клетки сильнее отличаются от нормальных. Прогноз выживаемости с момента установления диагноза составляет 60%.
Эти тимомы известны как эпителиальные, атипические, сквамоидные, высокодифференцированный рак тимуса. В опухоли обнаруживаются измененные эпителиальные клетки и небольшое количество лимфоцитов. Прогноз выживаемости — 20%.
Наиболее агрессивная разновидность опухолей вилочковой железы. Клетки в опухолевой ткани совсем не похожи на нормальные, это типичные раковые клетки. Прогноз выживаемости при таких новообразованиях наименее благоприятный. В течение 5 лет выживают 35% пациентов, в течение 10 лет — 28%.
Симптомы
Не все пациенты с опухолями вилочковой железы испытывают симптомы. У 30–50% больных нет жалоб. Возможные проявления тимом:
- Боль, чувство давления в груди.
- Упорный хронический кашель.
- Мышечная слабость.
- Повышенная утомляемость.
- Частые инфекционные заболевания.
- Затруднение глотания.
- Отек руки, лица.
- Опущение век, двоение в глазах.
- Головокружения.
- Снижение уровня эритроцитов и гемоглобина в крови.
Симптомы тимом неспецифичны. Они могут встречаться при многих других заболеваниях. Точный диагноз сможет установить только врач после осмотра и обследования.
Мы вам перезвоним
Методы диагностики
Большинство тимом можно обнаружить с помощью обычной рентгенографии. Опухоль выглядит как тень с ровными краями в верхней половине грудной клетки. Она частично перекрывает тень от сердца, находится преимущественно справа или слева.
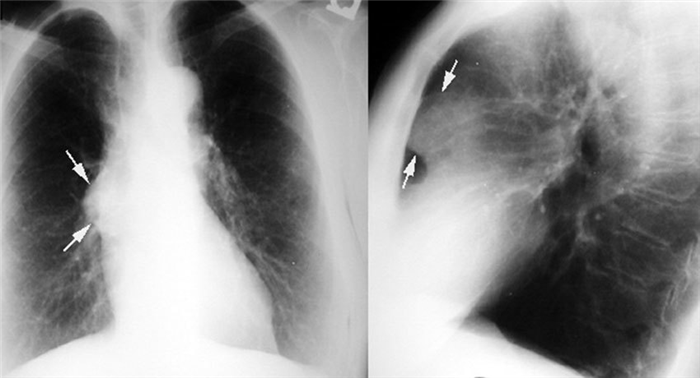
Компьютерная томография помогает уточнить размеры и локализацию тимомы, выявить небольшую опухоль, которая не обнаруживается во время рентгенографии. Увеличение тимуса на снимках, полученных с помощью КТ, также чаще всего свидетельствует о том, что в вилочковой железе присутствует тимома.
Компьютерная томография предпочтительна у пациентов с миастенией. Наиболее информативны снимки, выполненные с внутривенным контрастированием. Они помогают оценить расположение тимомы по отношению к крупным кровеносным сосудам, ее кровоснабжение, правильно спланировать операцию.
Кроме того, врач может назначить для диагностики тимомы МРТ. Это исследование также может быть проведено с контрастом. УЗИ помогает обнаружить очаги в лимфатических узлах.
Зачастую ценную диагностическую информацию позволяет получить . Во время этого исследования в организм вводят специальный радиофармпрепарат, который накапливается в опухолевых клетках и делает очаги видимыми на снимках.
Для подтверждения диагноза выполняют биопсию:
- Тонкоигольная биопсия выполняется с помощью пункции (прокола) специальной иглой. Ее выполняют под местным обезболиванием, под контролем компьютерной томографии.
- Фрагмент опухолевой ткани можно получить во время торакоскопии — эндоскопического исследования плевральной полости с помощью инструмента с миниатюрной видеокамерой, введенного через прокол.
В международной клинике Медика24 применяется современное диагностическое оборудование. Наши врачи в максимально короткие сроки установят точный диагноз и определят оптимальную тактику лечения.
Получить заочную консультацию врача
Лечение тимомы
Основной метод лечения опухолей вилочковой железы — хирургический. Операция может быть выполнена открытым способом (через разрез) или торакоскопически (через прокол в грудной стенке). Врач выбирает вид вмешательства в зависимости от размеров опухоли, ее распространения в соседние структуры и других факторов.
Если опухоль находится в пределах тимуса (стадия I по Masaoka/Koga), помимо удаления тимомы обычно не требуется никакого дополнительного лечения. Если новообразование прорастает в соседние органы, распространяется в лимфатические узлы, после операции назначают химиотерапию, или лучевую терапию, или их сочетание (химиолучевая терапия). Иногда эти виды лечения применяют до хирургического вмешательства, чтобы уменьшить размеры образований и упростить их удаление. Неоадъювантная и адъювантная терапия помогают снизить риск рецидива.
Если опухоль невозможно удалить, например, очень сильного прорастания в соседние структуры, наличия множества метастазов, лечение тимомы проводят химиопрепаратами и/или лучевой терапией.
Обратитесь за помощью к профессионалам в международной клинике Медика24. Наши врачи выполняют хирургические вмешательства любой сложности, проводят лечение тимом и других новообразований противоопухолевыми препаратами последних поколений в соответствии с современными международными рекомендациями.
Прогноз выживаемости
Обычно в онкологии прогноз оценивают по показателю пятилетней выживаемости — проценту пациентов, которые остаются в живых в течение пяти лет после установления диагноза. При тимомах часто используют показатель десятилетней выживаемости, потому что эти опухоли обладают высокой склонностью к рецидивированию даже спустя много лет:
| Стадия по Masaoka/Koga | Пятилетняя выживаемость / Десятилетняя выживаемость |
| I | 90% / 80% |
| II | 90% / 80% |
| III | 60% / 30% |
| IV |
*По данным Мемориального онкологического центра имени Слоуна — Кеттеринга (Memorial Sloan Kettering, США).
Прогноз при тимоме хуже, если пациент испытывает симптомы, потому что при этом обычно опухоль отличается высокой степенью злокачественности. Тем не менее, как правило, на любой стадии и при любом типе тимом пациенту можно помочь. Если опухоль не удается удалить хирургически, медикаментозное лечение и лучевая терапия способны замедлить прогрессирование заболевания, продлить жизнь больного и уменьшить симптомы. Приходите на прием к врачу в международной клинике Медика24, мы обязательно постараемся помочь.
Читайте также:
