Ушивание стенки трахеи при трахеопищеводном свище.
Добавил пользователь Skiper Обновлено: 29.01.2026
Изобретение относится к области медицины, а именно к хирургии, и может быть использовано при лечении трахеопищеводных свищей неопухолевого генеза.
Наиболее близким к предлагаемому (прототипом) является способ радикальной операции по поводу свища пищевода и дыхательных путей, включающий выделение, иссечение или рассечение свищевого хода, раздельное ушивание отверстий трахеи и пищевода [2]. Недостатки способа связаны с риском несостоятельности швов на пищеводе и трахее в ранние сроки после операции с развитием медиастинита или рецидива свища. К этому предрасполагает неизбежное инфицирование области вмешательства в результате вскрытия просвета трахеи и пищевода, нарушение кровоснабжения разобщенных трахеи и пищевода, техническая сложность ушивания образующихся дефектов, а также неравномерная компрессия тканей по линии шва, проникновение швов через слизистую оболочку в просвет трахеи и пищевода, что нарушает биологическую герметичность шва и условия для первичного заживления. Кроме того, вследствие выраженных воспалительных изменений в области шва существует риск развития стеноза трахеи и пищевода в отдаленном периоде. Для предупреждения несостоятельности швов на трахее и пищеводе в дополнение к способу рекомендовано разобщение линии швов этих органов путем ротирования пищевода вокруг своей оси или укрытие швов ауто-, ксено- или аллотрансплантатом и их обязательное подшивание по линии шва и вокруг них. В качестве пластического укрывающего материала применяются мышечный лоскут на питающей ножке (лоскут грудино-щитовидной, грудино-подъязычной, большой грудной, межреберных, грудино-ключично-сосцевидной мышцы, лоскут диафрагмы и др.) [2, 3, 4], бычий перикард, политетрафторэтилен («Gore-Тех») [5].
Новая техническая задача - упрощение действий хирурга и сокращение продолжительности операции, повышение ее состоятельности.
Отсутствие в мировой литературе и в патентно-информационных источниках решений со сходной совокупностью существенных признаков свидетельствует о соответствии предложения авторами критериям «новизна» и «изобретательский уровень». Изобретение иллюстрируется схемами выполнения конкретных приемов и примерами отдельных операций в эксперименте.
На иллюстрациях представлено:
Фиг.1. Формирование и перемещение лоскута большого сальника на питающей ножке в грудную полость: 1 - лоскут большого сальника со свободным краем U-образной формы, 2 - тракционные лигатуры, 3 - трахея, 4 - пищевод, 5 - диафрагма.
Фиг.2. Подведение при помощи двух лигатур жирового лоскута на питающей ножке со свободным краем U-образной формы к свищу: 2 - тракционные лигатуры, 6 - трахеопищеводный свищ.
Фиг.3. Фиксирование лигатурами жирового лоскута на уровне свища. Схема поперечного среза на уровне свища.
Фиг.4. Установка компрессионной клипсы (7). Схема поперечного среза на уровне свища.
Фиг.5. Вид клипсы, укрытого жировым лоскутом трахеопищеводного свища, дренажа: 7 - бранши клипсы, 8 - дренажная трубка.
Проверочным тестом достижимости технического результата является экспериментальная апробация предлагаемого способа хирургического лечения трахеопищеводных свищей неопухолевого генеза, смоделированных на 8 беспородных собаках массой тела 10-16 кг. Эксперименты на животных выполнены в отделе экспериментальной хирургии Центральной научно-исследовательской лаборатории СибГМУ. Исследование проводили согласно этическим принципам, изложенным в "Европейской конвенции по защите позвоночных животных, используемых для экспериментальных и других научных целей", все манипуляции и выведение животных из опытов проводили под общей анестезией. В послеоперационном периоде проводилось клиническое наблюдение, рентгенологический, эндоскопический контроль, гистологическое исследование препаратов.
Пример 1 (беспородная собака массой тела 16 кг с предварительно сформированным трахеопищеводным свищом на уровне шеи). После обработки операционного поля йодом и спиртом под общей анестезией с управляемым дыханием выполнили цервикотомию, осуществили доступ к сформированному трахеопищеводному свищу, разделили трахею и пищевод на уровне свища, выделили свищ, сформировали лоскут из жировой клетчатки переднего средостения на питающей ножке со свободным краем U-образной формы. После формирования лоскута необходимой длины его прошили за свободные края двумя обвивными лигатурами и тракцией за них подвели лоскут в боковое пространство между трахеей и пищеводом на уровне трахеопищеводного свища (фиг.2), осуществили укрытие свищевого хода и фиксацию лоскута, связывая лигатуры между собой (фиг.3), свободные концы лигатур срезали. Развели бранши предварительно охлажденной клипсы из никелида титана с эффектом памяти формы и сверхэластичности, выполненной в виде двухвитковой продолговатой проволочной спирали, сомкнутой по всей длине, с симметричным расположением свободных концов проволоки у первого конца спирали, причем обе ветви каждого витка спирали на преобладающей длине в сторону второго конца спирали спрямлены и сближены до взаимного касания для образования линейных бранш [5], прикрепленной дистальным концом к тракционной нити, и установили клипсу на жировой лоскут в проекции свищевого хода (фиг.4). После нагревания от окружающих тканей и смыкания бранш клипсы произошло пережатие свища и фиксация лоскута жировой клетчатки. Свободный конец тракционной нити провели наружу через просвет дренажной трубки (фиг.5). Установили дренажную трубку к области вмешательства и вывели через отдельный разрез на шею. Операционную рану послойно ушили. Удаление клипсы произвели через 8 суток после оперативного вмешательства тракцией за нить. Дренажную трубку удалили через сутки после извлечения клипсы.
Пример 2 (беспородная собака массой тела 14 кг с предварительно сформированным трахеопищеводным свищом на уровне шеи). После обработки операционного поля йодом и спиртом под общей анестезией с управляемым дыханием выполнили цервикотомию, осуществили доступ к сформированному трахеопищеводному свищу, разделили трахею и пищевод на уровне свища, выделили свищ. Выполнили лапаротомию, сформировали дефект в диафрагме и лоскут большого сальника на питающей ножке со свободным краем U-образной формы (фиг.1). После формирования лоскута необходимой длины его прошили за свободные края двумя обвивными лигатурами и тракцией за них через сформированное отверстие в диафрагме, переместили в переднее средостение и далее на шею, уложили лоскут в боковое пространство между трахеей и пищеводом на уровне трахеопищеводного свища (фиг.2), осуществили укрытие свищевого хода и фиксацию лоскута, связывая лигатуры между собой (фиг.3), свободные концы лигатур срезали. Развели бранши предварительно охлажденной клипсы из никелида титана с эффектом памяти формы и сверхэластичности, выполненной в виде двухвитковой продолговатой проволочной спирали, сомкнутой по всей длине, с симметричным расположением свободных концов проволоки у первого конца спирали, причем обе ветви каждого витка спирали на преобладающей длине в сторону второго конца спирали спрямлены и сближены до взаимного касания для образования линейных бранш [5], прикрепленной дистальным концом к тракционной нити, и установили клипсу на лоскут жировой клетчатки в проекции свищевого хода (фиг.4). После нагревания от окружающих тканей и смыкания бранш клипсы произошло пережатие свища и фиксация лоскута жировой клетчатки. Свободный конец тракционной нити провели наружу через просвет дренажной трубки (фиг.5). Установили дренажную трубку к области вмешательства и вывели через отдельный разрез на шею. Операционные раны послойно ушили. Удаление клипсы произвели через 10 суток после оперативного вмешательства тракцией за нить. Дренажную трубку удалили через сутки после извлечения клипсы.
Результаты экспериментальной апробации подтверждают работоспособность предлагаемого способа и достижимость технического результата. Готовность операции к клиническому применению свидетельствует о соответствии предложения критерию «промышленно применимо».
Таким образом, предлагаемый способ позволяет упростить и сократить продолжительность операции, повысить ее состоятельность.
1. Пат. 2202961, МПК 7 А61В 17/00. Способ хирургического лечения приобретенных трахеопищеводных свищей / М.Б.Скворцов, Е.В.Нечаев, В.В.Дроков. №2000116538; Заявлено 21.06.2000; Опубл. 27.04.2003, Бюл. №18, Приоритет 21.06.2000 (Россия). 6 с.
2. Трахео-бронхиальная хирургия / Б.В.Петровский, М.И.Перельман, Н.С.Королева. М.: 1978. - С.254-257.
3. Sokolov V.V., Bagirov M.M. Reconstructive surgery for combined tracheoesophageal injuries and their sequelae // Eur. J.Cardiothorac. Surg. 2001; 20: 1025-1029.
4. Bardini R., Radicchi V., Parimbelli P. et al. Repair of a recurrent bening tracheoesophageal fistula with a Gore-tex membrane // Ann. Thorac. Surg. 2003; 76: 304-6.
5. Пат. 2285468, МПК 7 A61B 17/11, A61B 17/122. Клипса для анастомоза полых органов / Г.Ц.Дамбаев, В.Э.Гюнтер, М.М.Соловьев и др. №2005103056; Заявлено 07.02.2005; Опубл. 20.10.2006, Бюл. №29, Приоритет 07.02.2005 (Россия). 8 с.
Публикации в СМИ
Врождённый трахеопищеводный свищ — отсутствующий в норме канал, выстланный грануляционной тканью или эпителием и соединяющий просвет пищевода с просветом трахеи; аномалия развития.
Классификация • Свищевой ход короткий и широкий (наблюдают чаще всего) • Свищевой ход узкий и длинный • Пищевод и трахея на протяжении имеют одну общую стенку • Пищевод и трахея на протяжении сливаются и представляют из себя одну трубку.
Клиническая картина. Клинические симптомы проявляются в большинстве случаев после первых кормлений, интенсивность их зависит от варианта порока развития • Широкий и короткий свищ — кормление новорождённого почти всегда сопровождается приступом кашля, цианозом, пенистыми выделениями изо рта. Быстро развивается аспирационная пневмония. После еды количество влажных крупнопузырчатых хрипов в лёгких увеличивается. Кормление ребёнка в вертикальном положении уменьшает возможность затекания молока через свищевой ход в трахею, и кашель возникает реже, не сопровождаясь цианозом • Узкий и длинный свищевой ход не проявляется в период новорождённости. При кормлении изредка возникают несильные приступы кашля. Родители обычно не придают им значения, т.к. кормление ребёнка в определённом положении избавляет его от приступов. Новорождённые часто болеют пневмонией • Большое соустье проявляется при первом кормлении. Каждый глоток жидкости вызывает приступ кашля. Нарушение дыхания бывает продолжительным, сопровождается резким цианозом. Общее состояние прогрессивно ухудшается из-за тяжёлой пневмонии и ателектазов лёгких.
Специальные методы исследования • Рентгенологическое исследование • Эзофагоскопия. При введении эзофагоскопа и осмотре пищевода свищевой ход становится заметным по выделяющимся из него в такт дыхания мелким пузырькам воздуха. Узкий и длинный свищ обычно при эзофагоскопии не виден • Трахеобронхоскопия. На глубине 7–8 см, обычно выше бифуркации трахеи на 2–3 см по заднеправой её поверхности, обнаруживают щелевидный дефект. Бронхоскопия облегчается при введении в пищевод 1% р-ра метиленового синего. Появление р-ра метиленового синего в трахее подтверждат диагноз.
ЛЕЧЕНИЕ. Единственный метод лечения — хирургический.
Предоперационная подготовка начинается сразу после выявления трахеопищеводного свища • Полностью исключают кормление через рот, вводят желудочный зонд, удаляемый после каждого кормления • С первого дня начинают активное противопневмоническое лечение (антибиотики, оксигенотерапия, УВЧ на грудную клетку, внутривенное введение препаратов крови, плазмы, витаминов и т. д.).
Способы оперативного лечения • При наличии длинного свищевого хода последний выделяют, перевязывают двумя лигатурами и пересекают между ними. На пищевод и трахею накладывают один ряд погружных швов • При широкой и короткой фистуле пищевод отсекают от трахеи и оба отверстия закрывают двухрядным непрерывным швом, причём пищевод ушивают в поперечном направлении • При ликвидации трахеопищеводного свища, при котором оба органа имеют на некотором протяжении общую стенку (обычно 0,5–0,7 см), пищевод пересекают в двух местах. Образовавшееся на трахее отверстие ушивают, а затем восстанавливают непрерывность пищевода путём создания анастомоза конец в конец.
Послеоперационное ведение • Активная противопневмоническая терапия • Первые 10–12 ч — парентеральное питание, затем кормление через тонкий зонд, оставленный после операции. Зонд удаляют на 6–7 сут, после создания анастомоза кормление через зонд проводят в течение 9–10 дней • В случае выявления сужения в области ликвидированного свища следует провести курс бужирования не раньше чем через месяц после хирургического вмешательства.
Прогноз благоприятный в случае своевременного выполнения оперативного лечения.
МКБ-10 • Q39.2 Врождённый трахеально-пищеводный свищ без атрезии
Код вставки на сайт
Cвищ трахеопищеводный врождённый
Врождённый трахеопищеводный свищ — отсутствующий в норме канал, выстланный грануляционной тканью или эпителием и соединяющий просвет пищевода с просветом трахеи; аномалия развития.
Классификация • Свищевой ход короткий и широкий (наблюдают чаще всего) • Свищевой ход узкий и длинный • Пищевод и трахея на протяжении имеют одну общую стенку • Пищевод и трахея на протяжении сливаются и представляют из себя одну трубку.
Клиническая картина. Клинические симптомы проявляются в большинстве случаев после первых кормлений, интенсивность их зависит от варианта порока развития • Широкий и короткий свищ — кормление новорождённого почти всегда сопровождается приступом кашля, цианозом, пенистыми выделениями изо рта. Быстро развивается аспирационная пневмония. После еды количество влажных крупнопузырчатых хрипов в лёгких увеличивается. Кормление ребёнка в вертикальном положении уменьшает возможность затекания молока через свищевой ход в трахею, и кашель возникает реже, не сопровождаясь цианозом • Узкий и длинный свищевой ход не проявляется в период новорождённости. При кормлении изредка возникают несильные приступы кашля. Родители обычно не придают им значения, т.к. кормление ребёнка в определённом положении избавляет его от приступов. Новорождённые часто болеют пневмонией • Большое соустье проявляется при первом кормлении. Каждый глоток жидкости вызывает приступ кашля. Нарушение дыхания бывает продолжительным, сопровождается резким цианозом. Общее состояние прогрессивно ухудшается из-за тяжёлой пневмонии и ателектазов лёгких.
Специальные методы исследования • Рентгенологическое исследование • Эзофагоскопия. При введении эзофагоскопа и осмотре пищевода свищевой ход становится заметным по выделяющимся из него в такт дыхания мелким пузырькам воздуха. Узкий и длинный свищ обычно при эзофагоскопии не виден • Трахеобронхоскопия. На глубине 7–8 см, обычно выше бифуркации трахеи на 2–3 см по заднеправой её поверхности, обнаруживают щелевидный дефект. Бронхоскопия облегчается при введении в пищевод 1% р-ра метиленового синего. Появление р-ра метиленового синего в трахее подтверждат диагноз.
ЛЕЧЕНИЕ. Единственный метод лечения — хирургический.
Предоперационная подготовка начинается сразу после выявления трахеопищеводного свища • Полностью исключают кормление через рот, вводят желудочный зонд, удаляемый после каждого кормления • С первого дня начинают активное противопневмоническое лечение (антибиотики, оксигенотерапия, УВЧ на грудную клетку, внутривенное введение препаратов крови, плазмы, витаминов и т. д.).
Способы оперативного лечения • При наличии длинного свищевого хода последний выделяют, перевязывают двумя лигатурами и пересекают между ними. На пищевод и трахею накладывают один ряд погружных швов • При широкой и короткой фистуле пищевод отсекают от трахеи и оба отверстия закрывают двухрядным непрерывным швом, причём пищевод ушивают в поперечном направлении • При ликвидации трахеопищеводного свища, при котором оба органа имеют на некотором протяжении общую стенку (обычно 0,5–0,7 см), пищевод пересекают в двух местах. Образовавшееся на трахее отверстие ушивают, а затем восстанавливают непрерывность пищевода путём создания анастомоза конец в конец.
Послеоперационное ведение • Активная противопневмоническая терапия • Первые 10–12 ч — парентеральное питание, затем кормление через тонкий зонд, оставленный после операции. Зонд удаляют на 6–7 сут, после создания анастомоза кормление через зонд проводят в течение 9–10 дней • В случае выявления сужения в области ликвидированного свища следует провести курс бужирования не раньше чем через месяц после хирургического вмешательства.
Прогноз благоприятный в случае своевременного выполнения оперативного лечения.
МКБ-10 • Q39.2 Врождённый трахеально-пищеводный свищ без атрезии
Стенозы трахеи
Трахея представляет собой трубку, которая связывает гортань с бронхами. Основной ее функцией является проведение воздуха в легкие и из легких. У взрослых трахея начинается на уровне 6-7 шейных позвонков и оканчивается на уровне тел 4-5 грудных позвонков делением на два главных бронха. Длина трахеи 10-13 см, ширина – 1,5 – 2,5 см.
Различают шейную и грудную части трахеи, граница между которыми соответствует яремной вырезке грудины спереди и второму грудному позвонку сзади. В грудном отделе трахеи выделяют три части: верхнегрудную, среднегрудную и надбифуркационную. Длина шейной части трахеи примерно 5 см, что соответствует 6-8 хрящевым кольцам. При разгибании шеи длина шейной части трахеи, как и число хрящей, существенно увеличивается. Начальные кольца трахеи располагаются на глубине 1,5-2см, на уровне яремной вырезкой - на глубине 4-6 см.
Спереди и с боков начальный отдел трахеи прикрыт щитовидной железой. Ниже железы спереди трахеи располагается претрахеальное клетчаточное пространство, в котором в грудной полости находится вилочковая железа. Кзади и несколько слева от трахеи лежит пищевод. В трахеопищеводной борозде слева на передней стенке пищевода проходит левый возвратный нерв. Правый возвратный нерв проходит позади трахеи на правой боковой стенке пищевода. В средостении спереди трахеи на уровне 1 ребра проходит левая плечеголовная вена. Позади нее трахею примерно посередине пересекает плечеголовной ствол, который проходит косо слева направо, непосредственно примыкая к ее передней стенке. Справа от грудной части трахеи располагаются верхняя полая вена, непарная вена и правая плечеголовная вена. К бифуркации трахеи прилежит дуга аорты и левая общая сонная артерия. Кровоснабжение шейного отдела трахеи осуществляется преимущественно ветвями нижних щитовидных артерий, надбифуркационный отдел трахеи и главные бронхи кровоснабжаются бронхиальными артериями. Кроме того, источниками кровоснабжения трахеи являются также ветви подключичной, внутренней грудной и плечеголовной артерий. Сосуды входят в трахею по боковым стенкам несколько кпереди от трахеопищеводной борозды. Венозный отток осуществляется преимущественно через вены щитовидной железы.
История хирургии трахеи
Вмешательства на трахее известны давно. Их выполняли еще за 3500 лет до нашей эры в Древнем Египте и за 2000 лет в Индии. Старейшей и наиболее распространенной в настоящее время операцией на трахее является трахеостомия. О разрезах дыхательного горла при травме, сопровождающейся обструкцией дыхательных путей сообщалось еще за 1500 лет до нашей эры. Beatrous описал, как Александр Македонский кончиком своего меча выполнил трахеостомию солдату. Galen и Aretaeus во втором-третьем веках нашей эры также описывали эту операцию. В это время трахею именовали бурной артерией или трахеальной артерией, считая, что по ней проходит не только воздух, но и кровь. Имена хирургов, возможно выполнявших трахеостомию, не известны. До 19 века многие считали это вмешательство бесперспективным и вредным. Goodall в 1934 году провел исследование, при котором установил, что до 19 века было выполнено только 28 успешных трахеотомий. Сдерживало применение метода плохое знание анатомии и неудовлетворительные результаты. В связи с высокой смертностью до 18 века при удушье, вызванном обструкцией верхних дыхательных путей, чаще применяли кровопускание.
Первая успешная трахеотомия, по мнению Goodall, была выполнена в 1546 итальянским врачом A.M.Brasavola больному, которому цирюльник, вскрыл глоточный абсцесс, но из-за развившейся в дальнейшем обструкции верхних дыхательных путей отказался что-либо делать. В 1610 году M.A.Severino из Неаполя применял трахеостомию при эпидемии дифтерии, используя вертикальный разрез по Fabrizio d Aquapendente (16 век), который также предложил трахеостомическую трубку и вертикальный разрез на шее, но сам не выполнял операцию. Первую успешную операцию удаления инородного тела из трахеи выполнил N.Habicot в 1620 году. У 14-летнего мальчика, проглотившего во время игры 9 кусочков золота, завернутых в материю, наступила асфиксия из-за обтурации трахеи куском материи. Он выполнил трахеотомию, перевел кусок материи в пищевод и переместил сверток с золотом в желудок, который в дальнейшем вышел обычным путем. В своей работе «Вопросы хирургии» в 17 веке N.Habicot демонстрировал необходимый для этого инструментарий. Операция была названа им бронхотомией.
Термин «трахеостомия» впервые применил T.Fienus в 1625 году. В 1714 году G.Detharding предложил трахеотомию для спасения утопленников. В Национальной галерее в Лондоне есть картина, соответствующая этому периоду. На берегу реки лежит женщина с раной на шее в положении на боку. Считалось, что в этой позиции вода может вытечь из легких.
 |
| Рис.5. Картина Piero di Cosima в Национальной Галерее в Лондоне. |
Первые резекции шейного отдела трахеи с анастомозом конец в конец выполнили на собаках Gluck и Zeller в 1881 году. Первую резекцию трахеи по поводу посттравматического стеноза шейного отдела трахеи успешно осуществил в 1886 году Kuster. В начале двадцатого века Nowakowski и Levit применяли для закрытия дефектов трахеи кожу, широкую фасцию бедра.
Циркулярная резекция трахеи наиболее долго из других вмешательств в торакальной хирургии внедрялась в практику, что было связано как с ее сложностью, так и с редкой необходимостью ее выполнения. Интерес к реконструктивным операциям на трахее возник в середине двадцатого века. Sanger во время Второй мировой войны и Griffith в 1949 году выполнили реконструктивные операции на бронхах и грудной части трахее. Одной из первых была публикация R.Belsey в 1950 году о резекции внутригрудной части трахеи. Belcher в 1950 году и Mathey в 1951 году осуществили анастомоз главных бронхов после случайного пересечения. J.Mathey в 1951 году впервые выполнил резекцию бифуркации трахеи. Увеличение в последние десятилетия числа больных с рубцовыми стенозами трахеи способствовало широкому внедрению реконструктивных операций на трахее в практику. Большое значение в становлении современной трахеальной хирургии имели работы хирургов, обладающих наибольшим опытом операций на трахее. Это работы J.Mathey, H.Eschapasse, F.G.Pearson, H.C.Grillo и в нашей стране М.И.Перельмана.
Стеноз трахеи
Стеноз трахеи может быть вызван рубцовыми изменениями стенки трахеи, сдавлением ее извне при опухолях средостения, новообразованиях щитовидной железы, аномалийными сосудами средостения и врожденной дезорганизацией тканей стенки трахеи, например при экспираторном стенозе.
Рубцовый стеноз трахеи характеризуется замещением нормальной стенки трахеи рубцовой тканью. Причиной ее появления является повреждение стенки трахеи с последующим развитием гнойно-некротического процесса обычно в месте давления манжеты интубационной трубки на стенку трахеи в процессе длительной искусственной вентиляции легких. Существенное значение в развитии стеноза имеет воспалительный процесс в области трахеостомы, давление конца трахеостомической трубки на стенку трахеи или рубцевание вследствие механического повреждения трахеи. Как правило, стеноз развивается в области трахеостомического отверстия или в области расположения манжеты трахеостомической трубки.
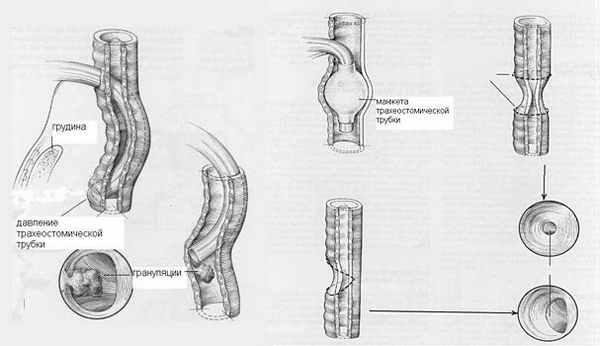 |
| Рис.6. Механизм формирования стеноза трахеи (Взято из W.W.Montgomery «Surgery of the laryngs, trachea, esophagus and neck», 2002). |
В крайне редких случаях причину стеноза трахеи установить не удается. Подобный стеноз носит название идиопатического. Как правило, им страдают женщины среднего возраста. Плотный келоидный рубец захватывает преимущественно адвентицию верхней трети трахеи, имеет протяженность 1-3 см.
В последние годы отмечается рост числа больных с рубцовыми стенозами трахеи. Благодаря достижением реаниматологии, длительной искусственной вентиляции легких стало возможным спасение больных, которые считались ранее безнадежными. Однако у многих из них через некоторое время развивается картина рубцового стеноза трахеи. По данным Корбера 1999г. стенозирование просвета трахеи после трахеостомии достигает 51%. Law 1993г. сообщил о 67% повреждений трахеи после трахеостомии. Морфологические изменения различны – от повреждения эпителия с образованием эрозий до трансмурального некроза стенки. Симптомы стеноза трахеи могут развиться через неделю или несколько месяцев после экстубации, но у 80% пациентов они появляются в течение первых 3 месяцев.
Профилактика – минимальная травма при трахеостомии, строгое соблюдение принципов асептики при любых манипуляциях на трахее, каждые 2 часа снижение давления в манжетке трахеостомической трубки, перемещение трубки по длине, замена трубки каждые 2 дня, антибиотикопрофилактика с учетом чувствительности микрофлоры.
- По этиологии: постинтубационный, посттрахеостомический, посттравматический, идиопатический.
- По локализации: гортань (с поражением подскладочного отдела, голосовых складок), шейный отдел трахеи, верхнегрудной, среднегрудной, надбифуркационный отделы трахеи, комбинированные поражения.
- По степени сужения: 1 степень (просвет сужен на 1\3 диаметра дыхательного пути), 2 степень (от 1\3 до 2\3 диаметра), 3 степень (более 2\3 диаметра).
- По распространенности: ограниченный (до 2 см), протяженный (более 2 см).
- По анатомической форме поражения: переднебоковые стенки, циркулярное сужение, атрезия.
- По состоянию стенок трахеи: с трахеомаляцией, без трахеомаляции.
- По наличию трахеостомы: с трахеостомой, без трахеостомы.
Данные анамнеза и появление одышки позволяют заподозрить стеноз трахеи. Одышка носит приступообразный характер, усиливается при небольшой физической нагрузке, уменьшается после откашливания вязкой мокроты. При прогрессирования стеноза отмечается шумное, слышное на расстоянии дыхание. Основными методами подтверждения стеноза и оценки степени сужения являются бронхоскопия и компьютерная томография.
В лечении больных с рубцовыми стенозами трахеи принимают участие не только торакальные хирургии, но и отоларингологи, эндоскописты. Наибольший опыт лечения больных с данной патологией накоплен в РНЦХ им. Б.В.Петровского. Радикальным методом лечения больных с рубцовым стенозом трахеи является циркулярная резекция трахеи, однако она возможна, как правило, при ограниченных стенозах. Консервативное лечение применяют только в начальный период формирования стеноза или как паллиативное лечение при невозможности оперативного вмешательства. Оно заключается в антибиотикотерапии, аэрозольтерапии, применении стероидных и нестероидных противовоспалительных препаратов. Нормальный просвет трахеи восстанавливают с помощью ригидной бронхоскопии, удаляя избыточные грануляции или рассекая суженный участок трахеи с помощью электрокоагуляции, лазерного воздействия. Данное вмешательство можно выполнять не более 3-4 раз. Для сохранения адекватного просвета трахеи осуществляют стентирование ее на срок 4-6 месяцев. После удаления стента добиться сохранения стойкого просвета трахеи удается не более чем у трети больных. Бужирование стеноза трахеи тубусом ригидного бронхоскопа различного диаметра или дилатационным бронхоскопом применяется также при угрозе асфиксии в качестве экстренного паллиативного вмешательства.
При обширных поражениях трахеи выполнить ее резекцию не представляется возможным. В подобных случаях возможна трансплантация трахеи. В 2006 году в РНЦХ была выполнена успешная трансплантация трахеи больному с субтотальным рубцовым стенозом трахеи. Кровоснабжение трахеи осуществляется через сосуды щитовидной железы.
Трахеопищеводные свищи
Наиболее часто трахеопищеводные свищи возникают у больных раком пищевода при распаде опухоли, прорастающей в трахею. Другими причинами являются ранения пищевода и трахеи, перфорация пищевода при его бужировании по поводу рубцовых стриктур, пролежень от трахеостомической и интубационной трубок при длительной искусственной вентиляции легких.
Частота трахеопищеводных свищей не превышает 0,5% среди больных, которым проводилась длительная искусственная вентиляция легких. Как правило, трахеопищеводные свищи у этой группы больных возникают от избыточного давления манжетки интубационной трубки или давления дистального конца трахеостомической трубки на заднюю стенку трахеи при наличии в пищеводе зонда для энтерального питания, что приводит к ее ишемии, некрозу и образованию соустья между пищеводом и трахеей. Часто трахеопищеводные свищи сочетаются со стенозом трахеи, что существенно осложняет лечение таких больных. Заброс пищи в трахею приводит к гнойному трахеобронхиту с последующим развитием абсцедирующей пневмонии, что значительно ухудшает прогноз заболевания. Питание у такого рода больных через рот исключается. Адекватное питание больного обеспечивается через энтеральный зонд или гастростому. Учитывая, что консервативное лечение больных с трахеопищеводными свищами малоэффективно, единственным радикальным способом ликвидации свища неопухолевой природы является оперативное вмешательство.
Клиническая диагностика трахеопищеводных свищей, как правило, не вызывает трудностей. Проявляются они приступообразным кашлем, который возникает во время приема пищи. Однако уточнение их локализации при рентгенологическом исследовании с барием и эзофагоскопии вызывает существенные трудности, особенно при небольших размерах свища. Более информативным оказывается трахеоскопия, при которой удается определить размеры свища, расстояние от голосовых связок и карины. Кроме того, значительную помощь в выявлении трахеопищеводных свищей оказывает также компьютерная томография.
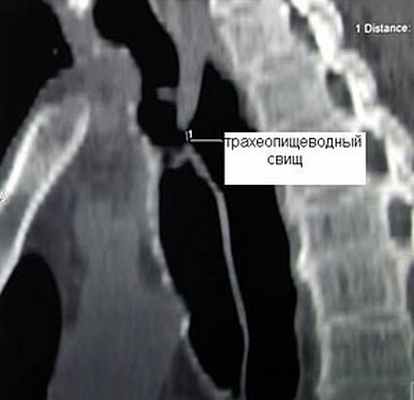 Рис.9. Компьютерная томограмма больного с трахеопищеводным свищом. | 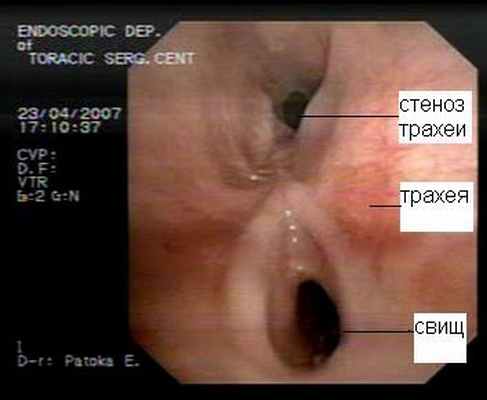 Рис. 10. Трахеоскопия больного с трахеопищеводным свищом, осложненным стенозом трахеи. |
Радикальным методом лечения трахеопищеводных свищей является разъединение пищевода и трахеи с ушиванием дефектов в них и интерпозицией мышц между ними, обычно участка грудиноключичнососцевидной мышцы.
Резекция трахеи
Радикальной операцией, позволяющей удалить стенозированный участок трахеи или опухоль, является циркулярная резекция трахеи. До недавнего времени считалось, что можно безопасно резецировать 2 см трахеи. При необходимости резекции большего участка трахеи для его замещения применяли кожу, перикард, другие ткани, а также различные протезы. Показанием к циркулярной резекции трахеи по поводу стеноза является ограниченный рубцовый стеноз. Важной задачей предоперационной подготовки является адекватное восстановление просвета дыхательного пути с целью устранения гипоксии. Для решения этой задачи выполняют бужирование трахеи жестким бронхоскопом с оставлением больного на сутки на продленной искусственной вентиляции легких через интубационную трубку.
Нецелесообразно выполнять резекцию трахеи при наличии трахеостомы. Ее необходимо предварительно ликвидировать путем эндопротезирования трахеи и ушивания дефекта за 2-3 недели до радикальной операции.
Стентирование трахеи
Различные эндоскопические методы расширения просвета трахеи широко применяются при стенозах доброкачественной и злокачественной природы. Бужирование стенозированного участка трахеи, скусывание опухоли или грануляций, лазерная резекция, фотодинамическая терапия и другие эндоскопические методы позволяют добиться быстрого, однако кратковременного восстановления просвета трахеи. Для предупреждения повторного сужения трахеи применяется ее стентирование. Этот метод является паллиативным методом лечения больных со стенозом трахеи и применяется при невозможности выполнения резекции трахеи или как этап в подготовке больного к радикальной операции. Стентирование возможно также при сужениях анастомозов после трансплантации легкого и циркулярных резекций. Наиболее часто показания для стентирования возникают при нерезектабельных злокачественных опухолях трахеи и крупных бронхов, крупных метастазах в лимфоузлы средостения, вызывающих обструкцию верхних дыхательных путей с выраженной дыхательной недостаточностью.
 Трахеальный стент. |  Трахеальный стент в просвете трахеи. |
© 2022 ФГБУ «НМХЦ им. Н.И. Пирогова» Минздрава России. Использование материалов сайта полностью или частично без письменного разрешения строго запрещено.
Treatment of esophagus damage caused by foreign bodies in children
The paper assesses in the expert way intensive care in two children with esophagus damage caused by foreign bodies, complicated with mediastinitis and tracheoesophageal fistula. Shortcomings of intensive care and anesthesia that in 1st case promoted adverse outcome and prolonged hospitalization in the 2nd case have been discussed. The author concluded, that in these patients the choice of anesthetic and surgical tactics were of the most importance, as well as proper antibacterial agents, detoxification, respiratory and nutritional support; specifications of every case should have been taken into account.
Keywords: esophagus, damage, mediastinitis, tracheoesophageal fistula, respiratory support, intensive care, expert assessment.
Механические повреждения пищевода относятся к наиболее тяжелым травмам, нередко заканчивающимся летальным исходом. Частота повреждений пищевода при попадании инородных тел варьирует в больших пределах от 30 до 77% [1, 3, 10]. У детей повреждения пищевода наблюдаются сравнительно редко, возникая главным образом в связи с химическими ожогами или перфорацией стенки органа (инородными телами, инструментами). Чаще всего инородные тела пищевода возникают у детей до двухлетнего возраста [2, 6, 8]. Летальность при инородных телах пищевода на протяжении десятилетий остается стабильной около 1% [6,9]. Однако в наиболее тяжелых случаях при возникновении глубоких перфораций, осложненных медиастинитом, плевритом летальность возрастает до 40–45% [1,9]. Причиной неблагоприятных исходов в большинстве случаев являются септические осложнения, но это могут быть и недостатки в проведении анестезиологического пособия, примером чему является следующее клиническое наблюдение.
Больной Н., 1,5 лет, находился на лечении в хирургическом отделении детской больницы с 13.08. по 14.10., в том числе с 24.08.по 9.09. – в ОРИТ. Диагноз: Инородное тело в/3 пищевода (элемент питания), длительно стоящее. Осложнения: Фибринозный эзофагит. Трахео-пищеводный свищ. Сопутствующие: Обструктивный бронхит. Анемия средней степени.
10.08. ребенок проглотил батарейку круглой формы. При первичном обращении по месту жительства рентгенография грудной клетки и брюшной полости не сделана. 13.08. направлен в ЛОР-отделение. Рентгенологически диагностировано инородное тело гортани. При эзофагоскопии – инородное тело верхней трети пищевода. Пролежень пищевода. Извлечь батарейку не удалось, из-за опасности перфорации пищевода. Переведен для дальнейшего лечения в детскую хирургическую клинику, где при поступлении выполнена экстренная фиброэзофагогастродуоденоскопия (ФЭГДС). Инородное тело (батарейка «таблетка» 20×2мм) в в/3 пищевода, плотно фиксировано, вокруг фибрин, отечная слизистая, остатки пищи. Инородное тело удалено.
Состояние оставалось тяжелым, фебрильная температура. Ребенка кормили, поили, рвоты не было. При кормлении отмечалось поперхивание. С 23.08. отрицательная динамика – нарастала одышка, акроцианоз. Назначен голод, парентеральное питания, смена антибиотиков. Установлен КПВ слева, назогастральный зонд. Состояние стабилизировалось. 24.08. на R-скопии диагностирован трахеопищеводный свищ. Переведен в ОРИТ. 27.08. наложена гастростомия по Кадеру. В дальнейшем проводилось зондовое питание. Состояние ближе к средней тяжести, объем кормления по гастростоме доведен до 50 мл×6 р/день. 9.09. переведен в хирургическое отделение, где энтеральное кормление через гастростому доведено до 150мл×6 р/день. Был 3-дневный эпизод гипертермии до 39°С. 28.09. выписывается на амбулаторное лечение с рекомендацией явиться на плановую операцию через 10–14 дней. Однако 29.09. вновь госпитализируется в хирургическое отделение в связи с резким усилением кашля, сопровождавшегося отхождением значительного количества слизистой мокроты и позывами на рвоту. Подготовлен для радикального оперативного вмешательства – устранения трахеопищеводного свища. 14.10. под эндотрахеальным комбинированным наркозом (атаралгезия + эпидуральная анестезия) выполнена операция – заднее-боковая правосторонняя торакомедиастинотомия. В ходе операции в момент попытки ушить верхний дефект пищевода у ребенка наступила «внезапная» остановка кровообращения. Реанимационные мероприятия, в течение 30 мин оказались безуспешными. Констатирована биологическая смерть.
Диагноз основной: Инородное тело пищевода (электробатарейка).
Осложнения: Химический ожог верхней трети пищевода. Фибринозный эзофагит. Некроз стенки пищевода и трахеи на фоне отграниченного медиастинита. Сформировавшийся широкий трахео-бронхиальный свищ. Правосторонняя очагово-сливная аспирационная пневмония. Состояние после наложения гастростомы от 27.08. Состояние после внеплевральной торако-медиастинотомии от 14.10. Разделение трахео-пищеводного свища. Ушивание дефекта стенки трахеи и попытки ушивания дефекта в пищеводе. ОССН IIIст. Отек головного мозга. Вклинение продолговатого мозга? Тромбоэмболия легочной артерии?
Патологоанат. диагноз основной: Инородное тело пищевода (электробатарейка).
Осложнения: Химический ожог пищевода в верхней трети. Фибринозный эзофагит. Очаговый некроз стенки пищевода и трахеи с формированием широкого трахео-пищеводного свища, отграниченного медиастинита. Состояние после наложения гастростомы от 27.08. Катаральный трахеобронхит с признаками хронизации процесса. Двусторонняя очаговая лейкоцитарно-десквамативная пневмония. Акцидентальная трансформация тимуса 3–4 фазы. Состояние после внеплевральной торако-медиастинотомии; разделения трахео-пищеводного свища; ушивания дефекта стенки трахеи и попытки ушивания дефекта в пищеводе от 14.10. Отек головного мозга с формированием борозды вклинения нижних миндалин мозжечка в большое затылочное отверстие. Мелкие кровоизлияния в эпидуральную клетчатку позвоночного канала, в мягкую мозговую оболочку. Жидкая кровь в полостях сердца. Венозное полнокровие внутренних органов. Дистрофические изменения в паренхиматозных органах.
Сопутствующие осложнения. ОРВИ – десквамативный бронхит.
Патологоанатомический эпикриз. 14.10. во время проведения радикального оперативного устранения трахеопищеводного свища у больного развились острая сердечно-сосудистая недостаточность (ОССН), отек головного мозга, которые привели к смерти во время операции.
Комментарий. В данном случае непосредственной причиной остановки кровообращения у больного Н. во время оперативного вмешательства была, вероятнее всего, не первичная ОССН, а гиповентиляция легких во время ИВЛ при проведении эндотрахеального наркоза. Операция продолжалась длительно, около 4 часов. Продолжительное время проводились обработка и ушивание свища трахеи, который был достаточно большого размера. Во время этой манипуляции, закономерно увеличившей размер отверстия в трахее, разгерметизация дыхательного контура стала более значительной по сравнению с исходной ситуацией, когда происходило раздувание пищевода при проведении ИВЛ. Результатом стал сброс воздуха на вдохе, уменьшение дыхательного объема и развитие вентиляционной или гиперкапнической дыхательной недостаточности. Для вентиляционной ДН характерной является гиперкапния, которая в данном случае и привела к отеку головного мозга и к вклинению головного мозга [4, 5, 7].. Имела место и гипоксия, вынудившая перейти на 100% ингаляцию кислорода и отключить закись азота, хотя по пульсоксиметрии она не диагностировалась. 100% кислород в дальнейшем мог поддерживать достаточную оксигенацию. Такую ситуацию следовало прогнозировать и предпринять меры к ее предупреждению. Можно было на время разгерметизации применить или однолегочную вентиляцию, или высокочастотную ИВЛ, или, в крайнем случае, увеличить дыхательный объем.
Следующий пример успешного лечения подобной патологии.
Больной С., 1,5 лет находился на лечении в хирургическом отделении детской больницы с 20.05. по 24.05. по поводу язвенного эзофагита, стадия заживления. Состояние после удаления инородного тела пищевода. Поступил в стационар с жалобами на затруднение глотания плотной пищи, рвоту после еды. Мама не исключала возможность проглатывания инородного тела. 20.05. выполнена эзофогоскопия. В обл. в/з пищевода обнаружено инородное тело – монета, которая удалена. При контрольном осмотре на боковых стенках пищевода, на расстоянии 15 см от резцов обнаружены линейные дефекты слизистой протяженностью до 1,5 см. Дно дефекта выполнено фибрином грязно-серого цвета. 24.05. – при контрольной ФЭГДС выявлены те же дефекты слизистой, покрытых желтым фибрином. Заключение: Язвенный эзофагит, стадия заживления. Состояние после удаления инородного тела пищевода. Проводилось лечение, назначены: стол 16, амикацин, жирогормональная смесь. 24.05. пациент выписан на амбулаторное лечение под наблюдение хирурга по месту жительства с рекомендацией контрольной ФЭГДС через 1 месяц, которая не была выполнена.
22.08. к ребенку была вызвана бригада СМП по поводу отравления лекарством (феназепамом). Со слов мамы он съел неизвестное количество таблеток. При осмотре ребенок вялый, сонлив. Произведено промывание желудка «до чистых вод». Во время промывания ребенок стал кричать, появилось возбуждение, в связи с чем он был доставлен в приемное отделение хирургического стационара. Состояние при поступлении тяжелое, возбужден, ЧСС – 160 в мин, АД – 120/80 мм рт. ст., ЧД – 30 в мин. Госпитализирован в палату интенсивной терапии (ПИТ) соматического отделения, где вскоре обнаружена подкожная эмфизема в области груди, распространяющаяся на шею. При УЗ-сканировании в средостении обнаружен воздух. Переведен в отделение реанимации и интенсивной терапии (ОРИТ) с диагнозом: Пневмомедиастинум. На ФЭГДС выявлен разрыв пищевода в в/з длиной 2 см (от резцов 8–10 см) шириной 1см, покрытый слизью. Признаков продолжающегося кровотечения нет. На R-грамме от 22.08. выраженная подкожная эмфизема в области шеи. Пневмомедиастинум. Назначена антибактериальная терапия, инфузионная, форсированный диурез, дробное введение жидкости через зонд. В связи со стабилизацией состояния, уменьшением подкожной эмфиземы 24.08. больной переведен в ПИТ с рекомендацией дробного питания с 26.08. через зонд и парентерального питания. Состояние ребенка оценивалось как средней тяжести. Лихорадка до фебрильных цифр. 25.05. в нарушение рекомендаций был удален желудочный зонд и начато кормление через рот. 27.08 консультирован хирургом. На контрольной R-грамме – пневмогидроторакс справа. Снова переведен в ОРИТ. 27.08. произведена плевральная пункция, получено 65 мл прозрачного желтого экссудата. Рентгенкартина перфорации пищевода, медиастинита, плеврита справа. На ФЭГДС от 28.08. – разрыв пищевода в в/з. 28.08. установлен торакоцентез справа.
В связи с отрицательной динамикой и отсутствием эффекта от консервативной терапии 29.08. выполнена операция – шейная медиастинотомия справа, ушивание разрыва пищевода, дренирование средостения. 30.08. отмечено выделение из средостения гнойного выпота. С 31.08. начали поить ребенка через зонд. 2.09. удалена торакоцентезная трубка. С 4.09. назначено зондовое питание. 11.09. на ФЭГДС обнаружена несостоятельность швов на пищеводе. На R-грамме – положительная динамика в легких и средостении. Сформировался пищеводный свищ, который к 25.09. закрылся, что установлено при контрольной R-графии и ФЭГДС. Помимо хирургического вмешательства больной получал лечение: респираторную поддержку, до 3.09. находился на ИВЛ, 10.09. был экстубирован, проводилась рациональная антибактериальная терапия, инфузионная корригирующая терапия, трансфузия эритромассы, питание комбинированное – зондовое и парентеральное, общеметаболические препараты, симптоматическое лечение. Результатом явилось выздоровление. 4.10. пациент выписан домой под наблюдение педиатра и хирурга. На ФЭГДС от 6.11. патологии не выявлено.
Комментарий. Несмотря на благополучный исход, было проведено экспертное исследование, так как мама обратилась с жалобой на некачественное оказание медицинской помощи врачом СМП. По ее мнению действия врача, осуществлявшего промывание желудка, явились причиной этого тяжелого осложнения. В данном случае, действительно, имеем пример тяжелого осложнения, казалось бы, простой манипуляции промывания желудка. Однако вины врача СМП в возникновении перфорации пищевода нет, причем в данном случае речь должна идти не о перфорации, а о разрыве пищевода. Промывание желудка, которое было проведено по абсолютным показаниям, вернее, введение зонда в желудок, естественно, сопровождалось рвотными движениями, а, следовательно, повышением внутрипищеводного давления. Это, видимо, и привело к разрыву пищевода в месте его дефекта, возможно истончения стенки, которое образовалось в результате бывшего пролежня (язвенного процесса), вызванного пребыванием инородного тела. Повреждение пищевода зондом не могло произойти и потому, что манипуляция по описанию была выполнена без технических трудностей. Что является очевидным, так это недостаточное внимание к ребенку со стороны родителей, по недосмотру которых ребенок в течение 2 месяцев глотает монету, а затем лекарственные препараты. Обращает на себя внимание и то, что и в медицинской карте, которая была заведена при поступлении в хирургический стационар, в анамнестических данных отсутствуют сведения об эпизоде с проглатыванием монеты, что помогло бы правильно трактовать клиническую ситуацию. Поэтому можно полагать, что они не были известны и врачу СМП. Таким образом, можно считать, что основным недостатком оказания помощи пациенту С. явилось раннее извлечение желудочного зонда в палате интенсивной терапии, что привело к усилению воспалительного процесса в средостении и необходимости проведения операции. Возможно, раннее наложение гастростомы, как то рекомендуют многие авторы [2, 8, 10] в таких случаях, могло предотвратить обострение процесса в средостении, однако избранная тактика была сознательной и базировалась на быстром улучшении и стабилизации состояния больного сразу после поступления в стационар. Осложнение, которое развилось у больного относится к разряду тяжелых, сопровождающихся высокой летальностью. В данном случае, очевидно, только профессионализм врачей, оказывавших помощь, помог больному остаться в живых. Тот дефект лечения, который был допущен, а именно раннее извлечение зонда, послужил причиной удлинения сроков лечения больного и, к счастью, не отразился на результатах лечения.
Приведенные клинические наблюдения свидетельствуют о крайней тяжести механических повреждений пищевода, особенно, проникающих в средостение с последующим развитием медиастинита, плеврита, пневмомедиастинума, трахео-пищеводного свища, что сопровождается возникновением жизнеугрожающих синдромов, требующих проведения интенсивной терапии, а в ряде случаев и хирургического вмешательства. Важнейшими проблемами в лечении подобных больных являются выбор хирургической тактики, а также адекватная антибактериальная, дезинтоксикационная терапия, респираторная и нутритивная поддержка с учетом конкретной клинической ситуации. Следует помнить и о высоком анестезиологическом риске при выполнении операций по поводу повреждения пищевода, что в определенных случаях требует применения специальных методик проведения анестезиологического пособия.
Литература
1. Абакумов М.М., Погодина А.Н. Механические повреждения пищевода. Материалы 2-ой международной конференции по торакальной хирургии, посвященной 40-летию профильных отделений РНЦХ РАМН. М.: 2003; 323–330.
2. Баиров Г.А. Срочная хирургия детей. Руководство для врачей. СПб.: Питер. 1997; 462.
3. Бастрыгин A.B., Супрунов А.Д., Махотин A.A., Савенко А.Ю., Гандуров С.Г., Сова В.В. Эндоскопическое удаление инородных тел пищевода. 3 международная конференция по торакальной хирургии: Материалы конференции. М.: 2005; 264–266.
4. Зильбер А.П. Дыхательная недостаточность: Руководство для врачей. М.: Медицина, 1989; 480.
5. Интенсивная терапия : национальное руководство : в 2 т. / Под ред. Б.Р.Гельфанда, А.И.Салтанова. М.: ГЭОТАР-Медиа, 2009; I.
6. Окунев H.A. Инородные тела и травматические повреждения пищевода у детей. Клинико-экспериментальные аспекты современной медицины: Материалы научн. конф. Саранск, 1999; 42: 47–48.
7. Осложнения при анестезии / Под ред. Ф.К.Оркина, Л.Х.Купера. Пер. с англ., М., Медицина.1985; 2.
8. Сотников С.И. Инородные тела пищевода у детей. Материалы межобластной конференции. Орел, 1999; 4: 448–449.
9. Харитонов, Дмитрий Анатольевич Профилактика и лечение осложнений инородных тел пищевода. Дисс. Канд. Астрахань. 2005; 131.
10. Kerschner J.E., Beste D.J., Conley S.F., Kenna M.A., Lee D. Mediastinitis associated with foreign body erosion of the esophagus in children. Int-J-Pediatr-Otorhinolaryngol. 2001; 59: 2: 89–97.
Ушивание стенки трахеи при трахеопищеводном свище.
Государственное бюджетное учреждение здравоохранения
Тюменской области "Областная клиническая больница №1"
Нам доверяют самое ценное!
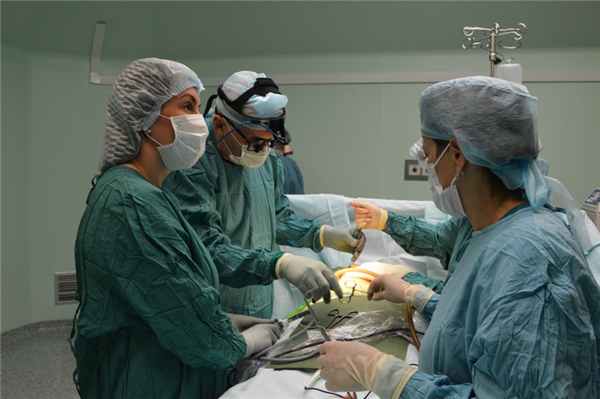
К врачам «ОКБ № 1» за помощью едут со всей страны! Торакальные хирурги провели сложнейшую операцию на трахее жительнице Свердловской области.
К врачам «ОКБ № 1» за помощью едут со всей страны! Торакальные хирурги провели сложнейшую операцию на трахее жительнице Свердловской области.
30 Марта 2018
Центр торакальной хирургии «Областной клинической больницы № 1» Тюменской области является одним из ведущих в Российской Федерации с широким спектром лечебных и диагностических хирургических вмешательств. Специалисты - торкальные хирурги Центра успешно оперируют пациентов с заболеваниями органов грудной клетки как «открытым» способом, так и «миниинвазивно» - с применением видеоторакоскопической техники.
В январе 2018 года за помощью к тюменским специалистам обратилась жительница Свердловской области по поводу ухудшения состояния своей матери на фоне трахеопищеводного свища. Восстановительные операции на трахее и пищеводе относятся к категории сложных вмешательств и только несколько клиник нашей страны владеют этой технологией. Специалисты «ОКБ № 1» и медицинской организации Свердловской области на онлайн консилиуме определили показания к хирургическому лечению и 80- летняя пациентка была оперативно доставлена в Тюмень.
Реконструктивную операцию с использованием современного эндоскопического оборудования выполнил Игорь Аркадьевич Бродер, торакальный хирург, заместитель главного врача «ОКБ № 1» по медицинской части. Во время операции необходимо тщательно, не повредив стенки, разделить трахею и пищевод, а затем восстановить их целостность. Важно для профилактики рецидива свища места пластики трахеи и пищевода укрепить мышечным лоскутом на сосудистой ножке. Также важно не допустить ранения сосудов, идентифицировать и сохранить возвратный нерв, обеспечивающий функционирование дыхательной системы, речевого аппарата и акта глотания. Кроме этого, важным является обеспечить стабильное состояние больного во время операции, учитывая возраст и сопутствующую патологию, организовать раннюю послеоперационную реабилитацию. Благодаря опыту многопрофильной бригады врачей операция прошла успешно!
«В декабре прошлого года, у мамы после трахеостомы ухудшилось состояние. Она не могла ни есть, ни дышать нормально. Человек просто тихонько умирал. Врачи нашей больницы подсказали обратиться в Тюмень. Я очень благодарна хирургам и всем врачам «ОКБ № 1» за то, что спасли мою маму, за внимание и отношение к ней!», - написала дочь.
«Трахеопищеводные свищи – это довольно редкая патология. Лечение их исключительно хирургическое, поскольку консервативная тактика абсолютно бесперспективна. Проведение реконструктивных операций на трахее и пищеводе возможно только в многопрофильной клинике, обладающей современным оборудованием, в составе которой есть опытная команда торакальных хирургов, анестезиологов-реаниматологов, диагностов. Именно такой клиникой является «Областная клиническая больница № 1», - рассказал Сергей Евгеньевич Ярцев, главный врач ГБУЗ ТО «ОКБ № 1».
Читайте также:
