Врожденная дисфункция коры надпочечников. Кора надпочечников и функция сердца.
Добавил пользователь Владимир З. Обновлено: 30.01.2026
Врожденная дисфункция коры надпочечников. Кора надпочечников и функция сердца.
Термин врожденная дисфункция коры надпочечников объединяет группу нарушений надпочечникового стероидогенеза, наследуемых по аутосомно-рецессивному типу, в основе которых лежит дефицит транспортного белка или одной из пяти ферментных систем, необходимых для синтеза кортизола. Недостаточность процессов 21-гидроксилирования, помимо нарушения синтеза кортизола и альдостерона, ведет к гиперсекреции адренокортикотропного гормона (АКТГ), гиперплазии коры надпочечников и избыточной продукции гормонов — предшественников прогестерона и 17-гидроксипрогестерона. Последние являются субстратом для избыточного синтеза андрогенов. Так как надпочечники плода начинают функционировать с 12-й недели гестации, повышенный уровень андрогенов наблюдается уже внутриутробно, вызывая вирилизацию гениталий. Кроме того, анаболическое влияние андрогенов приводит к увеличению мышечной массы; одним из клинических проявлений такого эффекта является развитие врожденной симметричной гипертрофии миокарда.
Частота. Наиболее часто встречается недостаточность 21-гидроксилазы (21-ОН). Установлено, что частота дефицита 21-ОН в Европе и Америке варьирует от 1:5000 до 1:13000.
Клиническая симптоматика врожденной дисфункции коры надпочечников. Заболевание сопровождается дефицитом глюко- и минералокортикоидов на фоне избытка андрогенов. Основными клиническими формами заболевания являются простая (вирильная), сольтеряющая и атипичная. В период новорожденности наиболее часто развивается синдром «потери соли» на фоне гермафродитного строения гениталий у девочек и в большинстве случаев нормального строения наружных половых органов у мальчиков. Гормональная недостаточность проявляется срыгиваниями, рвотой, частым жидким стулом, потерей массы тела, мышечной гипотонией, эксикозом, снижением артериального давления, малым сердечным выбросом. Вероятно развитие кардиомиопатии в виде симметричной гипертрофии миокарда.
Диагностика врожденной дисфункции коры надпочечников. Диагностическим критерием недостаточности 21-ОН является повышение базального уровня 17-ОНР (надпочечникового стероида, накапливающегося из-за имеющегося энзимного блока) более 4 нг/мл. Используются также иммуногенетические и молекулярно-генетические методы выявления мутантных генов. Лабораторная оценка уровня 17-ОНР может использоваться для проведения скрининга новорожденных.
Эхокардиография выявляет симметричную гипертрофию миокарда; возможны нарушения систолической и диастолической функций желудочков.

Лабораторные данные указывают на гипонатриемию, гиперкалиемию, гипохлоремию, декомпенсированный метаболический ацидоз. Имеет место повышенная экскреция нейтральных 17-кетостероидов с мочой.
Для правильного определения пола ребенка в план обследования необходимо также включать цитогенетическое исследование и ультразвуковое исследование внутренних гениталий.
Лечение врожденной дисфункции коры надпочечников.
Комплексная терапия врожденной дисфункции коры надпочечников проводится эндокринологом и кардиологом. С целью супрессии синтеза андрогенов назначают глюкокортикоиды 2 раза в день: гидрокортизон 15—20 мг/м2, преднизолон 4-5 мг/м2, дексаметазон 0,5-0,75 мг/м2. По мере стабилизации состояния возможен перевод ребенка с парентерального приема гидрокортизона на пероральный (кортеф). Критерием адекватности терапии глюкокортикоидами является отсутствие симптомов глюкокортикоидной недостаточности и уровень 17-ОНР ниже 2 нг/мл.
При сольтеряющей форме терапия глюкокортикоидами дополняется минералокортикоидами. В настоящее время основным является пероральный препарат флюдрокортизон (кортинефф), доза которого устанавливается строго индивидуально. Критериями адекватности терапии являются отсутствие клинических симптомов минералокортико-идной недостаточности, а также нормальные показатели артериального давления, ренина плазмы и электролитов крови. В большинстве случаев препарат назначают в начальной дозе 300 мкг/сут с постепенным снижением до 50—175 мкг/сут и распределяют равномерно на 2— 3 приема. Следует иметь в виду, что в случае неадекватного подбора дозы кортинеффа у ребенка повышается артериальное давление, что способствует прогрессированию гипертрофии миокарда левого желудочка и формированию фибросклеротических процессов в сердечной мышце.
При необходимости проводят симптоматическую терапию артериальной гипертензии диуретиками (фуросемид, триампур). Калийсберегающие диуретики (верошпирон), а также ИАПФ противопоказаны.
В острый период заболевания используют также инфузионную терапию для коррекции водного и электролитного баланса.
В процессе лечения необходим систематический контроль артериального давления, показателей натрия и калия в сыворотке крови, ЭКГ и ЭхоКГ (контроль за толщиной миокарда, его систолической и диастолическои функцией, степенью обструкции выводных отделов желудочков). В большинстве случаев на фоне адекватно подобранной терапии основного заболевания наблюдается замедление и постепенный регресс изменений со стороны сердечно-сосудистой системы.
Феминизирующая пластика наружных гениталий у девочек должна быть произведена не позднее двухлетнего возраста.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Врожденная вирилизирующая гиперплазия коры надпочечников: причины и механизмы развития
Заболевание обусловлено врожденным дефектом биосинтеза кортикостероидов, приводящим к избыточной продукции андрогенов.
Этиология заболевания обусловлена врожденным генетически обусловленным дефектом ферментативных систем, принимающих участие в нормальном биосинтезе коры надпочечников. Это положение находит подтверждение в семейном характере проявления заболевания и наличии некоторых элементов нарушения биосинтеза кортикостероидов у родственников больных. Патогенез заболевания обусловлен недостатком ферментов (3b-дегидрогеназы, 21-гидроксилазы и 11-гидроксилазы), участвующих в биосинтезе кортикостероидов. Считают, что основную роль играет недостаток 21-гидроксилазы, что препятствует образованию кортизола в достаточных количествах. Недостаток кортизола приводит к растормажи-ваниго гипоталамо-гипофизарной системы и увеличению продукции АКТГ.
Усиление биосинтеза стероидных гормонов при этом идет по пути избыточного образования андрогенов и соответственного увеличения выделения с мочой их метаболитов (17-кетостероидов). Вместе с этим избыточная стимуляция функции коры надпочечников может приводить к поступлению в кровь дезоксикортикостерона и, возможно, некоторых стероидов, не продуцируемых надпочечниками в нормальных условиях. Избыточный синтез андрогенов приводит к неправильному формированию половых органов, т. е. возникает диссоциация между генотипом и фенотипом при развитии организма.
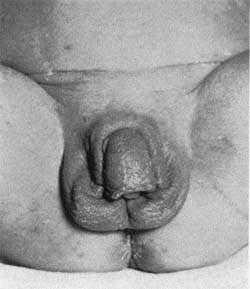
Обычно у детей с женским генотипическим полом появляются аномалии развития женских половых органов (гипертрофия клитора, недоразвитие влагалища, образование урогенитального синуса), которые являются результатом внутриутробной нормальной эволюции мюллеровых протоков. Ненормальное развитие половых органов часто при рождении таких детей значительно затрудняет определение истинного пола. Усиленная продукции андрогенов после рождения приводит к дальнейшей вирилизации организма (чрезмерное развитие мускулатуры, гипертрихоз, акне, огрубение голоса, нарушение или отсутствие менструаций).
Гиперплазия коры надпочечников у лиц с генетическим мужским полом вызывает преждевременное половое созревание у мальчиков; вначале ускоряется рост, увеличивается половой член, появляются вторичные половые признаки, появляются эрекции, половое влечение, но сперматогенез отсутствует.
В тех случаях, когда наступает недостаток 11-гидроксилазы, биосинтез кортикостероидов идет по пути образования избыточного количества минералокортикоидов. Недостаток Зр-дегидрогеназы и 21-гидроксилазы приводит к резкому снижению биосинтеза минералокортикоидов и возникновению солетеряющего синдрома в результате потери организмом натрия и хлоридов, при задержке калия. Если блокада биосинтеза кортикостероидов наступает на уровне образования прегненолона, то дети погибают от острой недостаточности коры надпочечников.
Патологическая анатомия. Анатомически обнаруживается гиперплазия надпочечников с увеличением их веса до 60—80 г. Гиперплазия диффузная и узелковая наблюдается в сетчатой зоне, пучковая и клубочковая интактны или гипоплазированы. Обращает на себя внимание несоответствие наружных половых органов, имитирующих мужские, и наличие яичников — женский псевдогермафродитизм.
Врожденная дисфункция коры надпочечников
Адреногенитальный синдром Hадпочечники секретируют кортикостероиды, которые по биологическим свойствам можно разделить на 4 группы: глюкокортикоиды, минералокортикоиды, андрогены и эстрогены. Синтез кортизола в надпочечниках плода под вли
 |
| Адреногенитальный синдром |
Hадпочечники секретируют кортикостероиды, которые по биологическим свойствам можно разделить на 4 группы: глюкокортикоиды, минералокортикоиды, андрогены и эстрогены.
Синтез кортизола в надпочечниках плода под влиянием адренокортикотропного гормона (АКТГ) начинается рано, в связи с этим дефект ферментных систем приводит к вирилизации до рождения ребенка. Так как к этому сроку формирование внутренних половых органов заканчивается, вирилизация затрагивает наружные половые органы.
Из различных ферментных дефектов недостаточность 21-гидроксилазы встречается наиболее часто и протекает в виде двух клинических форм: вирильного и сольтеряющего синдромов.
Вирильная форма связана с частичной недостаточностью 21-гидроксилазы. Как правило, при этом наблюдается компенсация функции коры надпочечников в результате повышенной секреции АКТГ, то есть уровень кортизола определяется на нижней границе нормы. Компенсаторное выделение АКТГ приводит к образованию значительного количества андрогенов, прогестерона, 17-гидроксипрогестерона, которые угнетают сользадерживающую активность на уровне канальцев почек, что ведет к значительному увеличению продукции альдостерона. У девочек с вирильной формой с рождения имеются признаки ложного гермафродитизма. Клитор гипертрофирован, напоминает по строению половой член, имеющий единое мочеполовое отверстие — урогенитальный синус, открывающийся у корня клитора, мошонкообразные большие половые губы.
| Врожденная дисфункция коры надпочечников является наследственным заболеванием, характеризующимся нарушением синтеза кортикостероидов, в основном кортизола, в результате дефицита ферментных систем коры надпочечников с одновременной избыточной продукцией андрогенов в надпочечниках |
У мальчиков с рождения отмечается увеличение полового члена, кожа мошонки морщинистая, выражена пигментация шва полового члена, кожи мошонки, передней линии живота, ареолы сосков.
В постнатальном периоде продолжается избыточная секреция андрогенов, усиливаются явления вирилизации. Дети быстрее растут, имеют развитую мускулатуру. Вначале больные обгоняют в росте сверстников, в дальнейшем же, после 9-10 лет, в связи с закрытием зон роста остаются низкорослыми. В возрасте 2–4 лет появляется преждевременное оволосение на лобке, подмышках, туловище, лице. У некоторых мальчиков значительно увеличивается половой член и появляются эрекции. Телосложение девочек мускулинного типа. В пубертатный период менструации не наступают, молочные железы не развиваются, так как повышенная секреция андрогенов надпочечниками по принципу обратной связи тормозит образование и выделение гонадотропинов. У мальчиков по этой причине угнетается развитие яичек — они остаются маленькими.
При сольтеряющей форме дефицит 21-гидроксилазы более глубокий, поэтому наряду с дефицитом образования кортизола происходит резкое снижение биосинтеза альдостерона. Если при вирильной форме потеря натрия, обусловленная избыточной продукцией прогестерона, 17-гидроксипрогестерона, компенсируется избыточной секрецией альдостерона, то при сольтеряющей форме снижено образование альдостерона. Результатом такого комбинированного действия является развитие клинической картины по типу острой надпочечниковой недостаточности.
| Заболевание наследуется по аутосомно-рецессивному типу и проявляется в гомозиготном состоянии. Распространенность составляет в среднем 1:4000-5000, а гетерозиготное носительство — 1:35-40 человек |
У новорожденных при этом синдроме резко выражены симптомы вирилизации, особенно у детей женского пола — полное заращение половой щели и появление мошоночноподобного образования. На 5–10-й день наступает быстрое ухудшение состояния, связанное с частой рвотой, жидким стулом. Развивается дегидратация, ребенок становится вялым, снижается масса тела. В сыворотке крови нарастает уровень кальция и снижается содержание натрия и хлора.
Гипертоническая форма дисфункции коры надпочечников, связанная с дефицитом 11b-гидроксилазы, встречается реже. В клинической картине, помимо признаков андрогенизации в раннем возрасте, характерно повышение артериального давления. При этой патологии отсутствует гиперплазия юкстагломерулярного аппарата почки и уровень ренина в плазме не повышен.
Дифференциальный диагноз врожденной дисфункции коры надпочечников у девочек первых лет жизни следует проводить с дисгенезией гонад, анорхизмом, истинным гермафродитизмом; у мальчиков — с преждевременным половым развитием различного генеза, в том числе с опухолью яичка, с андрогенпродуцирующей опухолью надпочечника (андростерома). Сольтеряющую форму у новорожденных дифференцируют с пилороспазмом и пилоростенозом.
У девочек старшего возраста при подозрении на врожденную дисфункцию коры надпочечников требуется исключить такие заболевания, как андрогенпродуцирующая опухоль яичника, стромальный текоматоз, поликистоз яичников.
Наиболее приемлемым средством заместительной терапии является преднизолон, который в течение длительного срока сохраняет достаточную концентрацию и обладает некоторым минералокортикоидным действием. Суточная доза его подбирается индивидуально и колеблется в зависимости от возраста: от 1,5–3 мг (для детей младше 3 лет) до 5 мг для детей старшего возраста. Реже применяют преднизолон, кортизон, дексаметазон. Соответственно суточному физиологическому ритму 17-гидроксипрогестерона принимать преднизолон рекомендуется рано утром, в 6-7 часов (причем в это время следует принять 2/3–1/2 дозы) и поздно вечером (23–24 часа). Глюкокортикоиды больные должны получать постоянно, так как отмена препарата ведет к декомпенсации заболевания.
При лечении больных с сольтеряющей формой врожденной дисфункции коры надпочечников к кортикостероидам добавляют минералкортикоиды. Это либо масляный раствор дезоксикортикостерона ацетата (ДОКА), либо таблетированный препарат кортинеф (0,1 мг), который в 5–10 раз активнее первого. Препараты назначаются в течение 1–2 недель ежедневно (ДОКА по 1–2 мл, кортинеф по 1 таб.) с последующим постепенным снижением дозы до оптимальной. Возможно поддерживающую терапию проводить через каждые 1–2 дня. У некоторых больных дефицит минералкортикоидов можно компенсировать добавлением в пищу поваренной соли. Обязательный контроль за весом, артериальным давлением, калием, натрием, ЭКГ.
Начальные дозы кортикостероидов должны быть в два раза выше физиологических.
При адекватном лечении у детей уменьшается мышечная гипертрофия, перераспределяется подкожножировая клетчатка, половое оволосение не прогрессирует. Если лечение начинают до закрытия ядер окостенения, то увеличивается темп роста. В случаях же поздней терапии эти дети так и остаются низкорослыми.
Гипертоническая форма заболевания лечится аналогично вирильной.
При присоединении интеркуррентных заболеваний дозу глюкокортикоидов увеличивают в 1,5–2 раза.
В случае развития острого криза недостаточности коры надпочечников показано внутривенное капельное введение жидкости (физиологический раствор и 5%-ный раствор глюкозы 100-200 мл/кг массы тела в сутки) в 4 приема, ДОКА 2–3 мг/кг массы тела в сутки. В последующие дни доза глюкокортикоидов быстро снижается и больной переводится на пероральный прием преднизолона.
Важное место в лечении врожденной дисфункции коры надпочечников занимает психотерапия, особенно в случае необходимости перемены пола ребенка.
Большинство девочек с этим заболеванием нуждается в проведении феминизирующей пластики наружных гениталий, удалении клитора и формировании малых половых губ после вскрытия урогенитального синуса. Коррекцию наружных гениталий рекомендуется проводить через год после назначения кортикостероидной терапии.
Недостаточность коры надпочечников у детей: причины, диагностика, лечение
Врождённая гиперплазия надпочечников является наиболее распространённой неятрогенной причиной недостаточной секреции кортизола и минералокортикоидов.
Первичная недостаточность коры надпочечников (известная как болезнь Аддисона) редко встречается среди детей. Она может возникать в результате:
• аутоиммунного процесса — иногда в связи с другими аутоиммунными эндокринными заболеваниями, например, с сахарным диабетом, гипотиреозом, гипопаратиреозом;
• кровоизлияния / инфаркта — неонатальная, менингококковая септицемия (обычно смертельный исход);
• адренолейкодистрофии — редкого нейродегенеративного заболевания;
• туберкулёза — в настоящее время редко.
Недостаточность надпочечников может быть также вторичной по отношению к гипопитуитаризму вследствие гипоталамо-гипофизарного заболевания или гипоталамо-гипофизарно-надпочечниковой супрессии вследствие длительной глюкокортикоидной терапии.
Клинические проявления недостаточности коры надпочечников у детей
У младенцев клинические симптомы проявляются внезапно в сопровождении с кризом с потерей солей, гипотензией и/или гипогликемией.
Дегидратация может возникать после гастроэнтеритоподобного заболевания, после которого ребёнок выздоравливает до следующего эпизода. У детей старшего возраста клинические проявления обычно начинаются с хронического нарушения здоровья и пигментации.
Особенности надпочечниковой корковой недостаточности
• Острая недостаточность коры надпочечников у детей:
- Гипонатриемия.
- Гиперкалиемия.
- Гипогликемия.
- Дегидратация.
- Гипотензия.
- Циркуляторный коллапс.
• Хроническая недостаточность коры надпочечников у детей:
- Рвота.
- Сонливость.
- Коричневая пигментация (дёсны, шрамы, складки кожи).
- Нарушение развития.
Диагностика недостаточности коры надпочечников у детей
Она проводится путём установления гипонатриемии и гиперкалиемии, часто сопровождаемых метаболическим ацидозом и гипогликемией. Уровень кортизола в плазме низкий, а концентрация АКТГ — высокая (если нет гипопитуитаризма).
По данным теста АКТГ (Синактен) концентрация кортизола в плазме остаётся низкой как при первичной надпочечниковой недостаточности, так и при длительно существующей гипофизарной / гипоталамической Аддисоновой болезни.
Нормальные результаты исключают недостаточность коры надпочечников.
Ведение детей с недостаточностью коры надпочечников
Надпочечниковый криз требует экстренного лечения внутривенной инфузией солевых растворов, глюкозы и гидрокортизона. Долгосрочное ведение пациентов состоит в заместительной терапии глюкокортикоидами и минералокортикоидами.
Требуется увеличение дозы глюкокортикоидов в три или пять раз в периоды болезни или при хирургическом вмешательстве. Все дети с риском надпочечникового криза должны носить браслет «MedicAlert».
Недостаточность коры надпочечников:
• Обычно связана с глюкокортикоидной терапией, врождённой гиперплазией надпочечников или, в редких случаях, болезнью Аддисона.
• Может приводить к надпочечниковому кризу, требующему неотложной терапии.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Надпочечниковая недостаточность
Надпочечниковая недостаточность – заболевание, возникающее вследствие недостаточной гормональной секреции коры надпочечников (первичная) или регулирующей их гипоталамо-гипофизарной системы (вторичная надпочечниковая недостаточность). Проявляется характерной бронзовой пигментацией кожных покровов и слизистых оболочек, резкой слабостью, рвотой, поносами, склонностью к обморокам. Ведет к расстройству водно-электролитного обмена и нарушению сердечной деятельности. Лечение надпочечниковой недостаточности включает устранение ее причин, заместительную терапию кортикостероидными препаратами, симптоматическую терапию.
Общие сведения
Надпочечниковая недостаточность – заболевание, возникающее вследствие недостаточной гормональной секреции коры надпочечников (первичная) или регулирующей их гипоталамо-гипофизарной системы (вторичная надпочечниковая недостаточность). Проявляется характерной бронзовой пигментацией кожных покровов и слизистых оболочек, резкой слабостью, рвотой, поносами, склонностью к обморокам. Ведет к расстройству водно-электролитного обмена и нарушению сердечной деятельности. Крайним проявлением надпочечниковой недостаточности является надпочечниковый криз.
Корковое вещество надпочечников вырабатывает глюкокортикостероидные (кортизол и кортикостерон) и минералокортикоидные (альдостерон) гормоны, регулирующие основные виды обмена в тканях (белковый, углеводный, водно-солевой) и адаптационные процессы организма. Секреторная регуляция деятельности коры надпочечников осуществляется гипофизом и гипоталамусом посредством секреции гормонов АКТГ и кортиколиберина.
Надпочечниковая недостаточность объединяет различные этиологические и патогенетические варианты гипокортицизма - состояния, развивающегося в результате гипофункции коры надпочечников и дефицита вырабатываемых ею гормонов.
Причины
Первичная надпочечниковая недостаточность развивается при поражении 85-90% ткани надпочечников.
В 98% случаев причиной первичного гипокортицизма служит идиопатическая (аутоиммунная) атрофия коркового слоя надпочечников. При этом по неизвестным причинам в организме образуются аутоиммунные антитела к ферменту 21-гидроксилазе, разрушающие здоровые ткани и клетки надпочечников. Также у 60% пациентов с первичной идиопатической формой надпочечниковой недостаточности отмечаются аутоиммунные поражения других органов, чаще – аутоиммунный тиреоидит. Туберкулезное поражение надпочечников встречается у 1-2% пациентов и в большинстве случаев сочетается с туберкулезом легких.
Редкое генетическое заболевание – адренолейкодистрофия служит причиной первичной надпочечниковой недостаточности в 1-2% случаев. В результате генетического дефекта Х-хромосомы возникает недостаток фермента, расщепляющего жирные кислоты. Преимущественное накопление жирных кислот в тканях нервной системы и коры надпочечников вызывает их дистрофические изменения.
Крайне редко к развитию первичной надпочечниковой недостаточности приводят коагулопатии, опухолевые метастазы в надпочечники (чаще из легкого или молочной железы), двусторонний инфаркт надпочечников, ВИЧ-ассоциированные инфекции, двустороннее удаление надпочечника.
Предрасполагают к развитию атрофии коры надпочечников тяжелые нагноительные заболевания, сифилис, грибковые поражения и амилоидоз надпочечников, злокачественные опухоли, пороки сердца, использование некоторых лекарственных препаратов (антикоагулянтов, блокаторов стероидгенеза, кетоконазола, хлодитана, спиронолактона, барбитуратов) и т. д.
Вторичная надпочечниковая недостаточность вызывается деструктивными или опухолевыми процессами гипоталамо-гипофизарной области, приводящими к нарушению кортикотропной функции, в результате:
- опухолей гипоталамуса и гипофиза: краниофарингиомы, аденомы и др.;
- сосудистых заболеваний: кровоизлияния в гипоталамус или гипофиз, аневризма сонной артерии;
- гранулематозных процессов в области гипоталамуса или гипофиза: сифилис, саркоидоз, гранулематозный или аутоиммунный гипофизит;
- деструктивнотравматических вмешательств: лучевая терапия гипоталамуса и гипофиза, операции, длительное лечение глюкокортикоидами и т. д.
Первичный гипокортицизм сопровождается снижением секреции гормонов коры надпочечников (кортизола и альдоатерона), что приводит к нарушению обмена веществ и баланса воды и солей в организме. При дефиците альдостерона развивается прогрессирующее обезвоживание, обусловленное потерей натрия и задержкой калия (гиперкалиемия) в организме. Водно-электролитные расстройства вызывают нарушения со стороны пищеварительной и сердечно-сосудистой систем.
Уменьшение уровня кортизола снижает синтез гликогена, приводя к развитию гипогликемии. В условиях дефицита кортизола гипофиз начинает повышенно вырабатывать АКТГ и меланоцитостимулирующий гормон, вызывающий усиление пигментации кожи и слизистых. Различные физиологические стрессы (травмы, инфекции, декомпенсация сопутствующих заболеваний) вызывают прогрессирование первичной надпочечниковой недостаточности.
Вторичный гипокортицизм характеризуется только дефицитом кортизола (в результате недостатка АКТГ) и сохранением продукции альдостерона. Поэтому вторичная надпочечниковая недостаточность, по сравнению с первичной, протекает относительно легко.
Классификация
Недостаточность коры надпочечников может носить острое и хроническое течение.
Острая форма надпочечниковой недостаточности проявляется развитием тяжелого состояния - аддисонического криза, обычно представляющего собой декомпенсацию хронической формы заболевания. Течение хронической формы надпочечниковой недостаточности может быть компенсированным, субкомпенсированным или декомпенсированный.
Согласно начальному нарушению гормональной функции хроническую надпочечниковую недостаточность разделяют на первичную и центральную (вторичную и третичную).
- Первичная недостаточность коры надпочечников (1-НН, первичный гипокортицизм, аддисонова или бронзовая болезнь) развивается в результате двустороннего поражения самих надпочечников, встречается более чем в 90% случаев, не зависимо от пола, чаще в зрелом и пожилом возрасте.
- Вторичная и третичная надпочечниковая недостаточность встречаются гораздо реже и возникают вследствие недостатка секреции АКТГ гипофизом или кортиколиберина гипоталамусом, приводящих к атрофии коры надпочечников.
Симптомы надпочечниковой недостаточности
Ведущим критерием первичной хронической надпочечниковой недостаточности является гиперпигментация кожных покровов и слизистых оболочек, интенсивность которой зависит от давности и тяжести гипокортицизма. Вначале более темную окраску приобретают открытые участки тела, подверженные солнечному облучению, - кожа лица, шеи, рук, а также участки, имеющие в норме более темную пигментацию, - ареолы сосков, наружные половые органы, мошонка, промежность, подмышечные области. Характерным признаком является гиперпигментация ладонных складок, заметная на фоне более светлой кожи, потемнение участков кожи, в большей степени соприкасающихся с одеждой. Цвет кожи варьирует от легкого оттенка загара, бронзового, дымчатого, грязной кожи до диффузно-темного. Пигментация слизистых оболочек (внутренней поверхности щек, языка, неба, десен, влагалища, прямой кишки) синевато-черной окраски.
Реже встречается надпочечниковая недостаточность с мало выраженной гиперпигментацией - «белый аддисонизм». Нередко на фоне участков гиперпигментации у пациентов обнаруживаются беспигментные светлые пятна – витилиго, размером от мелких до крупных, неправильной формы, выделяющиеся на более темной коже. Витилиго встречается исключительно при аутоиммунном первичном хроническом гипокортицизме.
У пациентов с хронической надпочечниковой недостаточностью снижается масса тела от умеренного похудания (на 3-5 кг) до значительной гипотрофии (на 15-25 кг). Отмечаются астения, раздражительность, депрессия, слабость, вялость, вплоть до потери трудоспособности, снижение полового влечения. Наблюдается ортостатическая (при резком изменении положения тела) артериальная гипотензия, обморочные состояния, вызываемые психологическими потрясениями и стрессами. Если до развития надпочечниковой недостаточности у пациента в анамнезе присутствовала артериальная гипертензия, АД может быть в пределах нормы. Практически всегда развиваются расстройства пищеварения - тошнота, понижение аппетита, рвота, боль в эпигастрии, жидкий стул или запоры, анорексия.
На биохимическом уровне происходит нарушение белкового (снижение синтеза белка), углеводного (снижение уровня глюкозы натощак и плоская сахарная кривая после глюкозной нагрузки), водно-солевого (гипонатриемия, гиперкалиемия) обменов. У пациентов отмечается выраженное пристрастие к употреблению соленой пищи, вплоть до употребления чистой соли, связанное с нарастающей потерей солей натрия.
Вторичная надпочечниковая недостаточность протекает без гиперпигментации и явлений недостаточности альдостерона (артериальной гипотонии, пристрастия к соленому, диспепсии). Для нее характерны неспецифические симптомы: явления общей слабости и приступов гипогликемии, развивающихся через несколько часов после еды.
Осложнения
Наиболее грозным осложнением хронического гипокортицизма при не проводимом или неправильном лечении является надпочечниковый (аддисонический) криз – резкая декомпенсация хронической надпочечниковой недостаточности с развитием коматозного состояния. Аддисонический криз характеризуется резчайшей слабостью (вплоть до состояния прострации), падением артериального давления (вплоть до коллапса и потери сознания), неукротимой рвотой и жидким стулом с быстрым нарастанием обезвоживания организма, запахом ацетона изо рта, клоническими судорогами, сердечной недостаточностью, еще большей пигментацией кожных покровов.
Острая надпочечниковая недостаточность (аддисонический криз) по преобладанию симптомов может протекать в трех клинических формах:
- сердечно-сосудистой, при которой доминируют нарушения кровообращения: бледность кожи, акроцианоз, похолодание конечностей, тахикардия, артериальная гипотония, нитевидный пульс, коллапс, анурия;
- желудочно-кишечной, напоминающей по симптоматике признаки пищевой токсикоинфекции или клинику острого живота. Возникают спастические боли в животе, тошнота с неукротимой рвотой, жидкий стул с кровью, метеоризм.
- нервно-психической, с преобладанием головной боли, менингеальных симптомов, судорог, очаговой симптоматики, бреда, заторможенности, ступора.
Аддисонический криз трудно поддается купированию и может вызвать гибель пациента.
Диагностика
Диагностику надпочечниковой недостаточности начинают с оценки анамнеза, жалоб, физикальных данных, выяснения причины гипокортицизма. Проводят УЗИ надпочечников. О первичной надпочечниковой недостаточности туберкулезного генеза свидетельствует наличие кальцинатов или очагов туберкулеза в надпочечниках; при аутоиммунной природе гипокортицизма в крови присутствуют аутоантитела к надпочечниковому антигену21-гидроксилазе. Дополнительно для выявления причин первичной надпочечниковой недостаточности может потребоваться МРТ или КТ надпочечников. С целью установления причин вторичной недостаточности коры надпочечник КТ и МРТ головного мозга.
При первичной и вторичной надпочечниковой недостаточности наблюдается снижение в крови кортизола и уменьшение суточного выделения свободного кортизола и 17-ОКС с мочой. Для первичного гипокортицизма характерно повышение концентрации АКТГ, для вторичного – его уменьшение. При сомнительных данных за надпочечниковую недостаточность проводят стимуляционный тест с АКТГ, определяя содержание кортизола в крови через полчаса и час после введения адренокортикотропного гормона. Повышение уровня кортизола менее чем на 550 нмоль/л (20 мкг/дл) свидетельствует о недостаточности надпочечников.
Для подтверждения вторичной недостаточности коры надпочечников применяют пробу инсулиновой гипогликемии, вызывающей в норме значительный выброс АКТГ и последующее повышение секреции кортизола. При первичной надпочечниковой недостаточности в крови определяются гипонатриемия, гиперкалиемия, лимфоцитоз, эозинофилия и лейкопения.
Лечение надпочечниковой недостаточности
Современная эндокринология обладает эффективными методами лечения надпочечниковой недостаточности. Выбор метода лечения зависит прежде всего от причины возникновения заболевания и преследует две цели: ликвидацию причины надпочечниковой недостаточности и замещение гормонального дефицита.
Устранение причины надпочечниковой недостаточности включает медикаментозное лечение туберкулеза, грибковых заболеваний, сифилиса; противоопухолевую лучевую терапию на область гипоталамуса и гипофиза; оперативное удаление опухолей, аневризм. Однако при наличии необратимых процессов в надпочечниках, гипокортицизм сохраняется и требует пожизненного проведения заместительной терапии гормонами коры надпочечников.
Лечение первичной надпочечниковой недостаточности проводят глюкокортикоидными и минералокортикоидными препаратами. При легких проявлениях гипокортицизма назначаются кортизон или гидрокортизон, при более выраженных - комбинация преднизолона, кортизона ацетата или гидрокортизон с минералокортикоидами (дезоксикортикостерона триметилацетат, ДОКСА - дезоксикортикостерона ацетат). Эффективность терапии оценивается по показателям артериального давления, постепенному регрессу гиперпигментации, прибавке массы тела, улучшению самочувствия, исчезновению диспепсии, анорексии, мышечной слабости и т. д.
Гормональная терапия у пациентов с вторичной надпочечниковой недостаточностью проводится только глюкокортикоидами, т. к. секреция альдостерона сохранена. При различных стрессовых факторах (травмах, операциях, инфекциях и др.) дозы кортикостероидов увеличивают в 3-5 раз, при беременности незначительное увеличение дозы гормонов возможно лишь во втором триместре.
Назначение анаболических стероидов (нандролон) при хронической надпочечниковой недостаточности показано и мужчинам, и женщинам курсами до 3-х раз в год. Пациентам с гипокортицизмом рекомендовано соблюдение диеты, обогащенной белком, углеводами, жирами, солями натрия, витаминами В и С, но с ограничением солей калия. Для купирование явлений аддисонического криза проводят:
- регидратационную терапию изотоническим раствором NaCl в объеме 1,5-2,5 л в сутки в сочетании с 20 % р-ром глюкозы;
- внутривенную заместительную терапию гидрокортизоном или преднизолоном с постепенным снижением дозы по мере стихания явлений острой надпочечниковой недостаточности;
- симптоматическую терапию заболеваний, приведших к декомпенсации хронической надпочечниковой недостаточности (чаще антибактериальную терапию инфекций).
Прогноз и профилактика
В случае своевременного назначения адекватной гормонально-заместительной терапии течение надпочечниковой недостаточности относительно благоприятное. Прогноз у пациентов с хроническим гипокортицизмом во многом определяется профилактикой и лечением надпочечниковых кризов. При сопутствующих заболеванию инфекциях, травмах, хирургических операциях, стрессах, желудочно-кишечных расстройствах необходимо немедленное увеличение дозы назначенного гормона.
Необходимо активное выявление и постановка на диспансерный учет у эндокринолога пациентов с надпочечниковой недостаточностью и лиц группы риска (длительно принимающих кортикостероиды при различных хронических заболеваниях).
Читайте также:
- Остеохондропатия бугристости большеберцовой кости - болезнь Осгуда-Шлаттера. Деформирующий артроз колена
- Отравление амриноном и его побочные эффекты
- Лучевая болезнь америция. Накопление и вывод из организма америция
- Стерильность альвеол. Инородные тела альвеол
- Методы обследования гонадной стромальной опухоли яичка
