Аномалии развития сердца, аорты и легочного ствола плода. Допплерография аномалий сердца плода
Добавил пользователь Евгений Кузнецов Обновлено: 01.02.2026
Основные пороки сердца у плода формируются в 1 триместре беременности на сроке 12-14 недель. Это может быть реакция на внешние факторы либо генетические проблемы. К этому сроку происходит формирование сердечной мышцы плода, поэтому будущей матери необходимо пройти УЗИ обследование на выявление патологий органа.

Во внутриутробном развитии пороки сердца возникают как реакция организма на нарушение плацентарного кровообращения либо воздействие канцерогенных веществ (формальдегиды, никотин, токсические вещества).
Аномалии положения сердца плода
Среди аномалий расположения сердца выделяют эктопию сердца (размещение вне грудной клетки). К таким патологиям относят декстрокардию (смещение сердца в правую сторону относительно нормального положения) и мезокардию (расположение сердца не с левой стороны грудины, а по срединной линии тела).
Эктопия сердца у плода возникает на сроке 14-18 дней с момента зачатия мезадерма начинает развиваться неправильно, что вызывает неправильное срастание брюшной стенки. У плода либо отсутствует диафрагма вообще, либо нет диафрагмального сегмента перикарда.
Из-за отверстия в стенке между правым и левым желудочком слышны интракардиальные шумы. Также у плода эктопия сердца нередко сопровождается другими аномалиями — гидроцефалией, энцефалоцеле и пр.
Надо сказать, что существует высокая вероятность ошибочного диагноза по установки положения сердца. При тазовом предлежании плода на УЗИ сердца визуализируется справа, хотя на самом деле оно располагается в положенном месте.
В 71% случаев эктопия сердца вызывается плевральным выпотом, кистозным аденоматозным пороком развития лёгкого, диафрагмальной грыжей.
Различают четыре вида эктопии:
- абдоминальная (сердце находится в брюшине);
- грудная (сердце выходит наружу через дефекты грудины);
- торакоабдоминальная (пентада Кантрелла — сложнейшая патология, имеющая комплекс отклонений от нормы);
- шейная (сердце смещается в область сердца).
Грудная эктопия встречается в 55-60% случаев, торакоабдоминальная — в 38%, шейная — почти в 3%. Выживаемость составляет около 10%. В большинстве случаев при эктопии младенец либо рождается мёртвым, либо умирает сразу после рождения.
Патология сопровождается смещением других внутренних органов, которые не защищены от механических повреждений и подвержены инфекциям и вирусам больше обычного.
Врождённые дефекты сердца
Пять наиболее встречаемых дефектов — это тетрада Фалло, дефект межжелудочковой перегородки, транспозиция магистральных сосудов, коарктация аорты, гипоплазия левых камер.
Оптимальным сроком для проведения ультразвуковой диагностики сердца плода считается период 24-26 недель беременности. Именно в это время анатомические структуры сердца максимально визуализируются, а на более ранних сроках можно увидеть только явные и глобальные пороки сердца.
Наиболее информативен ультразвуковой осмотр 4-камерного среза сердца. После которого при любом отклонении от нормы женщина отправляется на более детальное обследование плода с использованием допплеровской эхокардиографии. Также проводится кариотипирование, потому что в 30% случаев аномалии являются результатом хромосомных нарушений.
Что выявляет УЗИ
В нашей клинике используется современное 4D оборудование, имеющее допплеровский режим. С его помощью можно получить изображение 3-х главных сосудов — верхней полой вены, лёгочного ствола и восходящей аорты. Во время обследования выявляется не только расположение сосудов, но и их диаметр и другие параметры.
На экране монитора будут видны следующие патологии плода:
- Уменьшение диаметра аорты при расширении лёгочного ствола можно говорить об гипоплазии (недоразвитости) левых отделов сердца малыша, отвечающих за начало кровообращения;
- Уменьшение ствола лёгочной артерии в размерах при сохранении в норме диаметров аорты и верхней полой вены указывает на стеноз (сужение) лёгочной артерии. У плода выявляются только выраженные формы;
- Маленький диаметр аорты при нормальном 4-камерном строении сердца является следствием коарктации аорты (сужение аорты сердца в определённом сегменте);
- Визуализация 2 сосудов вместо 3 может быть следствием соединения сосудов в общий артериальный ствол;
- Смещение аорты вперёд или правее лёгочной артерии наблюдается при транспозиции магистральных сосудов;
- Диаметр аорты расширен, но при этом сужен диаметр лёгочной артерии, а аорта смещена вперёд. Это может является тетрадой Фалло (очень тяжёлая сочетанная аномалия сердца). Проблема включает в себя стеноз или гипертрофию выходного отдела правого желудочка, дефект межжелудочковой перегородки, декстропозицию аорты (отхождение в правую сторону). Диагностика плода крайне затруднительна, поэтому на помощь приходит допплеровский режим, помогающий визуализировать поток крови в аорту из обоих желудочков;
- Гипоплазия (недоразвитость) правых камер сердца определяется по уменьшению их размеров относительно левых камер. Эта патология сопровождается обычно дисплазией (провисанием или выбуханием) митрального клапана;
- Общий предсердно-желудочковый канал виден как дефект перегородки сердца с расщеплением атриовентрикулярного клапана;
- Гипопластический синдром левых отделов сердца проявляется в виде недоразвития желудочка и митрального и аортального клапанов;
- Единственный желудочек также не является нормой, потому что их должно быть два и они хорошо просматриваются в четырёхкамерном срезе;
- При недоразвитости трёхстворчатого клапана кровь из правого предсердия не попадает в левое, что хорошо видно при допплеровском исследовании;
- Со 2 триместра фиброэластоз эндокарда визуализируется как утолщение миокарда и ухудшении его сокращения;
- Недоразвитие миокарда одного из желудочков (аномалия Уля) заметна на 2 триместре.
Какие патологии сердца у плода сложно выявить на скрининговом УЗИ
Трудности в диагностике заболеваний сердца на УЗИ вызывают следующие патологии органа:
- дефект межпредсердной перегородки;
- дефект межжелудочковой перегородки;
- транспозиция главных артерий.
При подозрении на их наличие, пациентка должна регулярно наблюдаться и соблюдать все рекомендации гинеколога.
Допплерометрия плода выявляет патологии кровотока при беременности
Доплерометрия при беременности - это современный метод диагностики при помощи ультразвука, позволяющий объективно и полноценно исследовать кровообращение плода, плаценты и матки. По состоянию кровеносной системы можно оценить состояние плода, скорость его развития — не страдает ли малыш от недостатка кислорода, а также возможные патологические изменения. Допплерометрия плода — единственная методика, способная показать точное нахождение патологии сосудов (в матке, пуповине или плаценте).
Зачем и когда проводить допплерометрию при беременности
Сегодня заболевания сосудов — одна из наиболее распространенных проблем в медицинской практике. Своевременная диагностика позволяет выявить такие патологии еще на ранней стадии развития, а вместе с тем и многие факторы, способные вызвать развитие нарушений кровообращения.
Ценность процедуры заключается в её высокой информативности, благодаря чему врач способен выявить не только уже развившуюся патологию, но и практически незаметные доклинические симптомы болезни. Процедура назначается после полного формирования плаценты — не ранее 18 недель, чаще на 32-34 неделе в качестве плановой проверки.
При наличии даже незначительных подозрений на нарушения развития плода - УЗИ с доплером проводят на любом сроке. Доплер делают в комплексе со скрининговым УЗИ , при этом по ощущениям для беременной женщины процедура ничем не отличается от классического УЗ-обследования.
Суть метода
Этот способ изучения кровеносной системы основан на применении эффекта Доплера.
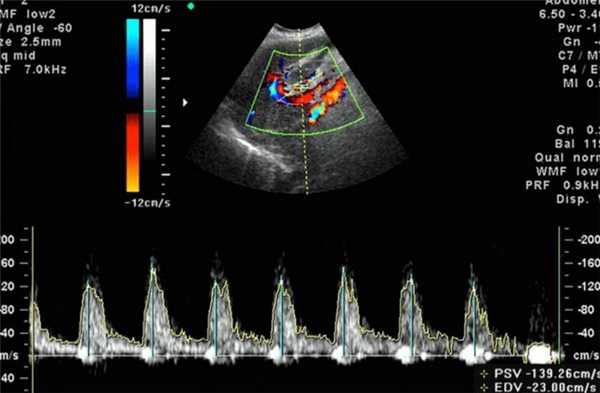
Для обследования используется такой же ультразвук, как и при обыкновенном ультразвуковом исследовании. Отличие заключается в особом датчике, работающем на основе допплеровского эффекта, и интерпретации полученных данных. При исследовании фиксируются ультразвуковые волны, отраженные не от статичных тканей, а от подвижных объектов - клеток крови, в результате чего частота отраженных лучей сильно изменяется в сравнении с изучаемыми. Аппарат обрабатывает полученные данные и создает двухмерное цветное изображение. Благодаря этому возможно оценить скорость и направление кровотока, анатомию и проходимость сосудов.
Длительность допплерографии составляет 20 - 40 минут. Она не имеет ни противопоказаний, ни осложнений, ни негативного воздействия на организм. Исследование совершенно безболезненное и безопасное.
Показания
Гинекологи рекомендуют проходить обследование с доплером 1-2 раза во время беременности вместе с плановыми УЗИ . Если же есть проблемы, доппплер плода нужно сделать в ближайшие сроки. В основном допплерометрия назначается при несоответствии размеров плода гестационному возрасту. Также процедура проводится в следующих случаях:
- осложнения в вынашивании ребенка;
- фетоплацентарная недостаточность;
- у матери присутствуют хронические и тяжелые заболевания (сахарный диабет, гипертония, анемия, системные заболевания);
- резус-конфликт беременной и ребенка;
- многоплодная беременность;
- неиммунная водянка плода;
- неправильное положение плода в матке;
- преждевременное созревание плаценты;
- обвитие шеи ребенка пуповиной, подозрение на гипоксию;
- выраженное маловодие / многоводие;
- гестоз (поздний токсикоз, сопровождающийся ухудшением работы почек, сосудов и мозга — появляется белок в моче, повышается давление);
- травмы живота у беременной;
- хромосомные патологии младенца;
- плод шевелится меньше обычного или шевеления не ощущаются вовсе;
- неудовлетворительные результаты кардиотокографии;
- осложнения в вынашивании предыдущей беременности (преждевременные роды, выкидыш и т.д.).
Также УЗИ плода с доплером нужно пройти в случаях, если матери нет 20 лет или ей более 35 лет.
Что выявляет допплерометрия плода
Допплер помогает своевременно выявить гипоксию плода и избежать проблемы еще до того, как ребёнку будет угрожать опасность, или же свести негативные последствия к минимуму. С его помощью врач может узнать причины обвития пуповиной и увидеть сколько раз и насколько туго обвита шея младенца. Без этой жизненно необходимой информации специалисты не смогут выбрать правильную тактику родов, что ставит под угрозу здоровье и жизнь ребенка.
Также с помощью доплера можно увидеть:
- состояние и ритм работы сердца плода в состоянии покоя и движения;
- состояние сердечных клапанов основных кровеносных сосудов, артерий и вен;
- скорость и объем кровотока периферийной кровеносной системы;
- кровообращение в пуповине и плаценте;
- состояние кровеносной системы, сердца и почек беременной.
Полученная информация позволяет врачу оценить:
- проходимость и состояние сосудистого русла, наличие отклонений, блокирующих кровоток плода;
- насыщение кровью и питательными веществами всех тканей ребенка;
- проходимость и состояние пуповины, обвитие шеи младенца;
- эффективность работы плаценты;
- состояние и работа кровеносной системы женщины в период беременности.
Подготовка и особенности проведения УЗИ плода с доплером
Процедура не требует никаких подготовительных мер: ни рацион питания, ни наполненность мочевого пузыря и желудка не оказывают влияния на результаты обследования. Единственная рекомендация — сделать перерыв в еде на пару часов до обследования.
Беременной нужно взять с собой следующее: направление и результаты прошлых анализов и обследований (УЗИ, КТГ, ЭКГ), обменную карту беременной. Бумажные салфетки и одноразовую пеленку или полотенце не нужны — в нашей клинике все предоставляется бесплатно.
Методика проведения допплерометрии аналогична трансабдоминальному УЗИ. Женщина ложится на кушетку спиной и оголяет живот. Врач наносит на исследуемый участок специальный гель для лучшей проходимости ультразвуковых волн и затем водит по нему датчиком, параллельно исследуя полученные данные на мониторе. Интерпретация результатов выдается женщине в тот же день.
Доплерометрию при беременности можно проводить несколькими способами:
- Ультразвуковой допплер - применяется для оценки направления, интенсивности, характера кровотока в сосудах.
- Дуплексное исследование - отличается от предыдущего метода большей точностью и информативностью. Применяется для оценки кровотока сосудов и их анатомии.
- Цветное картирование - состояние даже мельчайших сосудов и их проходимость кодируется цветом.
Расшифровка результатов допплерометрии плода
Оценка состояния кровоснабжения с помощью допплера формируется на основе следующих показателей:
- Систоло-диастолическое отношение - отношение максимальной и минимальной скорости кровотока;
- Индекс резистентности - отношение разницы максимальной и минимальной скорости кровотока к максимальной в период сжатия;
- Пульсационный индекс - отношение разницы максимальной и минимальной скорости кровотока к средней скорости за полный цикл сердца.
Допплерометрия плода: норма по неделям и прогноз при отклонениях
Чтобы расшифровка результатов прошла правильно и все отклонения были выявлены, необходимо сравнить полученные данные с нормативными значениями с учетом гестационного срока.
Порок развития сердца у плода при беременности: методы определения и тактика действий
Термин «врожденный порок сердца» — причина для серьезного беспокойства родителей. Ситуация осложняется, если этот диагноз был поставлен еще до рождения малыша.
Если в семье уже рождались дети с ВПС, или возраст женщины более 35 лет, следует особенно тщательно планировать беременность. Нужно вести здоровый образ жизни, убедиться в отсутствии инфекций или излечить имеющиеся отклонения.
Конечно, полностью минимизировать риски заболевания не удастся. Здесь совет только один: вовремя проходить все обязательные скрининги и другие обследования, показанные при беременности.
Причины и механизм развития пороков сердца
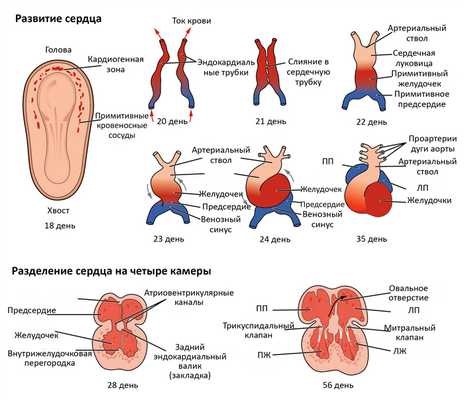
Сердце формируется одним из первых из всех органов эмбриона. Уже в первом триместре оно начинает свою работу. Порок сердца при беременности у плода является чаще всего результатом наследственных факторов, болезней женщины, расплатой за вредный образ жизни будущей матери. Реже формирование ВПС связано с другими аномалиями развития эмбриона, например, с синдромом Дауна.
Женщины с высоким риском: кто подвержен опасности?
- перенесших выкидыши, мертворождения;
- возрастом старше 35 лет;
- куривших во время беременности;
- живущих в районах с неблагополучной экологией;
- переболевших на ранних сроках беременности краснухой;
- употреблявших во время беременности аспирин, сульфаниламидные препараты, антибиотики;
- имеющих тяжелый семейный анамнез по порокам сердца.
Врожденный порок сердца - дефект, находящийся в структуре сердца. По статистике, десять детей из тысячи будут иметь диагноз ВПС в своих медицинских картах. И число их будет расти, в основном по причине повышения доступности и эффективности диагностических методик. Сейчас диагноз можно поставить не дожидаясь рождения малыша, с помощью стандартных аналитических систем на различных сроках внутриутробного развития.
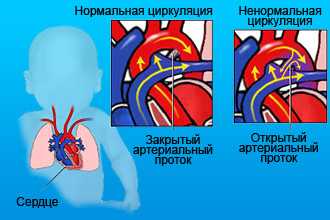
Пороки сердца отличаются разнообразием семиотики. Врачи-кардиологи делят их на «бледные» и «синие». Для первых характерна бледность кожи. К ним относятся в основном дефекты сердечных перегородок. При «синих» кожа приобретает синюшный оттенок. Связано это с тем, что в крови недостаточно кислорода. К «синему» типу пороков относятся более тяжелые состояния: болезнь Фалло, транспозиция магистральных сосудов и другие.
К комбинированным принято относить патологии клапанов сердца. Они вызываются недоразвитием створок, а также их склеиванием, как правило, из-за перенесенной матерью при беременности вирусной инфекции.
Самый важный период в развитии сердца — с четырнадцатого по шестидесятый день от зачатия. Именно тогда сердце разделится перегородками и станет четырехкамерным, из общего артериального ствола выделится аорта и легочная артерия, образуется желудочек, сформируются клапаны.
Если в любой из этих важных для развития эмбриона дней беременный организм столкнется с угрозой, вполне возможны последствия в виде формирования дефекта в сердечно-сосудистой системе.
Как правило, о многих пороках сердца будущие родители узнают на первом скрининге, то есть, начиная с 12 недели беременности. Если аномалия слишком тяжела, после ряда уточняющих обследований матери будет предложено прервать беременность. Если ВПС будущего ребенка совместим с жизнью, у родителей будет время подготовиться к неизбежной после его рождения операции на сердце.
В некоторых регионах России уже сейчас проводятся внутриутробные операции на сердце, позволяющие малышу родиться полностью здоровым.
Клинические проявления во время беременности
Как правило, беременность плодом с ВПС для женщины мало чем отличается от типичного варианта. Диагноз становится очевидным лишь при проведении УЗИ плода и его сердца, допплерографии или КТГ.
Плод, как правило, страдает от гипоксии и отличается отставанием в развитии. Возможно назначение беременной лекарственных средств, облегчающих работу сердца плода. Но о полной компенсации состояния речь, как правило, речь не идет.
Главная задача матери, вынашивающей ребенка с дефектом развития сердца, — максимально продлить срок беременности в динамике состояния плода.
Диагностика и детализация состояния плода
Основной показатель нормального развития плода - его сердечный ритм.
- 110-130 ударов до восьмой недели беременности;
- 175-185 до конца первого триместра;
- 145-160 до родов.
На пороки развития сердечно-сосудистой системы плода указывают:
- брадикардия или тахикардия;
- различные временные интервалы между ударами;
- приглушенные звуки сердцебиения - признак кислородного голодания плода.

Порок сердца у плода на УЗИ становится очевидным в случае визуализации дефекта камер органа. ЧСС будущего ребенка можно посчитать уже в первом триместре беременности на рутинном обследовании при помощи акушерского стетоскопа. Более полную информацию о работе сердца плода даст КТГ, которое назначается после 32 недели беременности. Оценив его результаты, акушеры определяют параметры состояния малыша.
Основные заключения анализа показателей состояния плода:
Это доступные и для пациентки, и для врача методики обследования. Они не требуют особой подготовки и не занимают много времени.
Но лидером в исследованиях гемодинамических процессов в сердце и сосудах плода считается доплер-эхокардиография.Этот метод оценивает три основных показателя -направление, скорость и характер кровотока. Процедура такова:на животе беременной устанавливается датчик УЗИ. На экран передается цветное изображение. Красным обозначается течение крови, которая двигается в сторону датчика.Синий цвет указывает на объем крови, идущий в обратном направлении. Максимальная интенсивность того или иного цвета обозначает повышенную гемодинамику.
Чрезвычайно ценную информацию о сердце и самом плоде дает ЭХО-КГ. Исследование может назначаться на любом сроке беременности, но, как правило, выполняется начиная с 12 недели после получения настораживающих показаний первого скрининга.
Это исследование определит:
- направление и скорость кровотока в сосудах;
- проходимость кровяного русла;
- соотношение объемов входящей и выходящей из сердца плода крови;
- ЧСС.
Лучше всего проводить процедуру на сроке от 18 до 24 недели, так как именно в этот срок обеспечивается максимальный визуальный эффект.
Исследования, проведенные ранее этого времени, не будут достаточно объективными из-за малых размеров сердца. К концу беременности ЭХО-КГ плода редко используется из-за большого объема живота, затрудняющего визуализацию органа.
К решению вопросов, касающихся результатов исследования плода с ВПС, привлекается детский кардиолог и кардиохирург.
Тактика ведения беременной

Акушерская тактика ведения беременной, которая вынашивает плод с ВПС представляет собой постановку вопроса об амнио- или кордоцентезе после тщательного эхокардиографического исследования. Их цель — получить материал для проведения хромосомного анализа. Если дефект выявится у нежизнеспособного эмбриона, беременной будет предложен аборт. Срок при этом не имеет никакого значения, особенно если порок сердца будет сочетаться с генетическими аномалиями.
Если ВПС совместим с жизнью, беременная будет до конца срока находится под усиленным наблюдением акушеров. По истечению сорока недель ей будет предложено госпитализироваться для родов в специализированный перинатальный центр. Как правило, у подобного плода показано родоразрешение при помощи кесарева сечения.
После родов малыш будет переведен для обследования, лечения и возможной хирургической операции в кардиологическое отделение детской больницы.
Выводы
Любой порок развития плода, выявленный при беременности, — это всегда сложная проблема и для будущей матери и для обеспечивающих ее течение врачей. Аномалия сердца — не исключение. Сейчас существует множество достоверных методик, позволяющих на ранних сроках опровергнуть или подтвердить диагноз ВПС, оценить состояние, сделать предположение о его жизнеспособности. Почти все они широко применяются и доступны пациенткам.
Для подготовки материала использовались следующие источники информации.
Коарктация аорты у плода. Точность и ошибки диагностики
ФГБУ "Научный центр акушерства, гинекологии и перинатологии им. В.И. Кулакова" Минсоцразвития РФ, Москва.

УЗИ аппарат RS85
Революционные изменения в экспертной диагностике. Безупречное качество изображения, молниеносная скорость работы, новое поколение технологий визуализации и количественного анализа данных УЗ-сканирования.
Распределение диагностики ВПС в зависимости от нозологической формы значительно варьирует. Определенные ВПС пренатальная диагностика позволяет выявить в 90% случаев. Цифры статистики неумолимо показывают низкий процент выявления ВПС (30%) по результатам скринингового исследования. В специализированных учреждениях частота выявления ВПС выше и достигает 54% [1, 2].
Точность ультразвуковой диагностики патологии плода за последние годы многократно подвергается критике со стороны акушеров-гинекологов и в большей степени педиатров. Порой клинические признаки интересуют специалистов значительно меньше, чем данные ультразвукового антенатального исследования плода.
В этой работе представлен анализ возможностей ультразвукового пренатального исследования при коарктации аорты. В работе учтены данные, имеющиеся в публикациях отечественных и зарубежных авторов, а также материал отделения функциональной диагностики Центра.
Латинский термин "сoarctatius" означает "суженный, стиснутый". Впервые его описал J.F. Meckel в 1750 году. Коарктация аорты - это патологическое сужение ее просвета, которое может возникнуть в любом месте по всей ее длине. Частота порока составляет 6,3%, по данным клинических наблюдений из выборки в 2000 случаев [3], и 8,4% по результатам патологоанатомического материала [4].
У детей первого года жизни коарктация аорты занимает четвертое место cреди ВПС. Как правило, она развивается дистальнее места ответвления левой подключичной артерии вблизи артериального протока (ductus arteriosus). В зависимости от локализации сужения аорты относительно артериального протока различают два классических типа коарктации: предуктальную и постдуктальную [5].
При наличии сужения аорты клиническая картина может нарастать как шквал после закрытия артериального протока. В течение первого года погибают 56% пациентов. В основном смертельный исход бывает вызван сочетанием коарктации с другими аномалиями сердца. Изолированная форма в первые недели и дни жизни также характеризуется высоким процентом смертности (34%). Если этот период дети переживают, то продолжительность жизни в среднем составляет 30-50 лет. Причиной смерти у новорожденных является сердечно-легочная недостаточность. При артериальной высокой гипертензии, как исключение, может быть кровоизлияние в мозг.
В ФГБУ "Научный центр акушерства, гинекологии и перинатологии им. В.И. Кулакова " Минсоцразвития РФ за двухлетний период (2010-2011) родились 27 детей с аномалиями аорты, от незначительного сужения до полного перерыва. В 15 наблюдениях в отделении функциональной диагностики диагноз был поставлен антенатально. Это были беременные, обратившиеся в поздние сроки от 35 до 39 нед гестации. Во всех наблюдениях патология аорты сочеталась с гипоплазией левого желудочка. Диагноз был подтвержден во всех случаях. В изолированном виде коарктация аорты за этот период была диагностирована в 6 наблюдениях. В 3 из них диагноз был поставлен антенатально, в 2 - сужение было выявлено у новорожденных на 3-5-е сутки после закрытия артериального протока. В одном случае после рождения был поставлен диагноз кинкинг аорты. Таким образом, наши данные свидетельствуют о сложности и невысоком проценте выявления изолированной коарктации аорты. Лишь в тех наблюдениях, когда имеются выраженные гемодинамические нарушения, приводящие к значительным анатомическим изменениям в виде гипоплазии левого желудочка, диспропорции желудочков сердца, увеличения диаметра легочной артерии диагноз с большой достоверностью может быть поставлен антенатально.
Первые работы по диагностике коарктации аорты у плода относятся к 1984 г. [6, 7]. По данным литературы, трансвагинальный доступ в 12-15 нед гестации позволяет диагностировать коарктацию аорты в 21,4% случаев [1]. При трансабдоминальном доступе частота выявления коарктации аорты увеличивается: в 16-30 нед она составляет 43%, после 30 нед, по мере прогрессирования гемодинамических нарушений, не превышает 54% [8].
Согласно результатам скринингового ультразвукового обследования 20 248 плодов при сроках 19-22 нед беременности в крупном регионе Германии (1990-1994) пренатальный диагноз коарктации аорты не был установлен ни в одном из 7 случаев. Аналогичные данные были получены в Норвегии, даже в специализированном центре пренатальной диагностики. Согласно данным мультицентрового анализа, проведенного в 12 европейских странах, точный пренатальный диагноз изолированной коарктации аорты в конце 90-х гг. был установлен только в 9 (15,8%) из 57 случаев [9]. Средний срок обнаружения изолированной коарктации составил 22 нед, при этом 7 из 9 случаев было выявлено до 24 нед. При сочетании коарктации аорты с экстракардиальными пороками и хромосомными аномалиями точность ее пренатальной диагностики была существенно выше за счет выраженности гемодинамических нарушений и расширенного эхокардиографического исследования плода и составила 52%.
По данным института сердечно-сосудистой хирургии им. А.Н. Бакулева, точность диагностики не превышает 27%. Как правило, патология наиболее часто отмечается при сочетании коарктации аорты с другими кардиальными аномалиями [10].
Таким образом, обобщая статистические данные материала Центра, публикации ведущих специалистов России и зарубежных коллег, можно отметить очень низкий процент диагностики коарктации аорты у плода.
В чем же причина столь низкого процента выявления коарктации аорты антенатально?
Существует несколько факторов, затрудняющих диагностику коарктации аорты антенатально.
Первая причина не диагностированной коарктации аорты это морфогенез патологии и теория первичного нарушения развития дуги аорты. Теория была предложена в 1828 г. [11]. Автор считает, что данная патология связана с недостаточным соединением 4 и 6 дуги аорты с нисходящим ее отделом. Поэтому перешеек - это место, где наиболее часто локализуется участок сужения [12], так как оба отдела образуются из разных эмбриональных зачатков. В норме область перешейка аорты равна 2/3 диаметра восходящего отдела аорты (рис. 1).
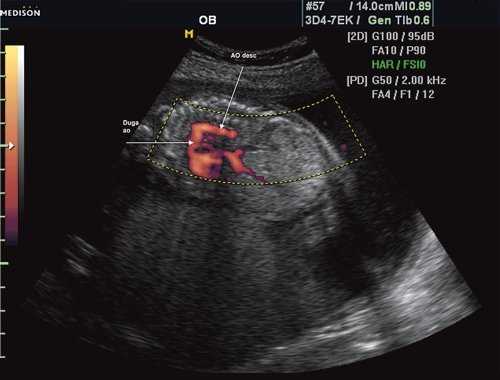
Рис. 1. Восходящий отдел, дуга и нисходящий отдел аорты плода в режиме энергетического допплера в норме.
Согласно "теории дуктальной ткани" коарктация аорты возникает в результате миграции гладких мышечных клеток протока в предуктальную аорту, с последующей констрикцией и сужением просвета аорты [4]. При формировании коарктации аорты в области перешейка сохраняется сужение различной протяженности и формы (рис. 2, 3). Наиболее часто это проявляется в виде локальной перетяжки, выше или ниже которой диаметр аорты сохраняется в норме.
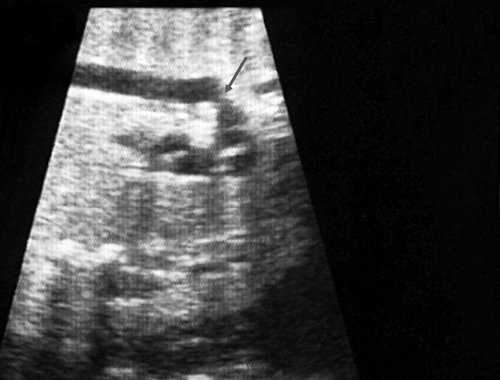
Рис. 2. Ультразвуковое исследование восходящего отдела, дуги и нисходящего отдела аорты. Стрелкой указано место сужения.
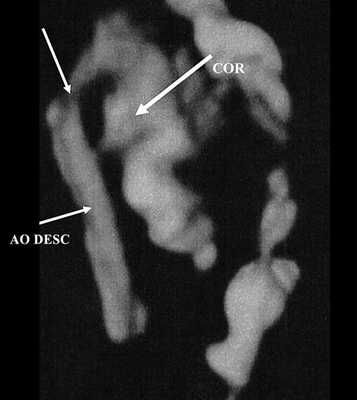
Рис. 3. Трехмерное изображение сердца и аорты плода в 16 нед беременности. Стрелкой указано место сужения аорты. AO DESC - нисходящий отдел аорты, COR - сердце.
Следовательно, оценка сужения аорты в типичном месте как признак развивающейся патологии не всегда представляется возможной в ранние сроки беременности. Поскольку речь идет о предуктальной коарктации аорты (сужение аорты локализовано проксимальнее протока), то, очевидно, что в период внутриутробной жизни в более поздние сроки отмечается снижение кровотока через левые отделы сердца и перешеек аорты и развивается гипоплазия левого желудочка и аорты. Это и способствует более позднему проявлению патологии и возможности ее ультразвуковой диагностики.
Вторая причина, затрудняющая диагностику коарктации аорты - это теория постнатального развития. У плода перешеек аорты узкий и после рождения и закрытия артериального протока он должен в норме расшириться для обеспечения адекватного кровотока в нисходящий отдел аорты. Таким образом, имеющееся физиологическое сужение перешейка аорты не позволяет предположить формирование коарктации аорты после рождения.
Постдуктальная коарктация развивается уже после рождения и практически всегда представляет собой изолированный дефект. Эта аномалия, вероятнее всего, является результатом разрастания мышечной ткани артериального протока в аорту плода. Когда же проток после рождения сужается, эктопическая ткань внутри аорты также сжимается, перекрывая, как тампоном, просвет сосуда по всей его окружности. В отличие от предуктальной коарктации в данном случае гипоплазия аорты не развивается. Закрытие артериального протока у некоторых детей приводит к наличию сужения аорты и развитию коарктации через 2-3 нед после рождения [13].
Третья причина не диагностированной коарктации аорты состоит в особенностях внутрисердечной гемодинамики у плода. Кровообращение плода, так же, как и взрослого, подчиняется ряду основных закономерностей физического и биологического воздействия. Поток крови движется из зоны высокого давления в область низкого давления. При выраженном потоке размеры увеличиваются, при уменьшении объема потока уменьшаются. Так, гипоплазия левого желудочка и коарктация аорты часто сопутствуют порокам со сниженным выбросом крови в аорту (стеноз аорты, дефект межжелудочковой перегородки) и практически не встречаются при пороках с большим объемом потока через аорту (при тетраде Фалло).
Исходя из особенностей внутрисердечной гемодинамики плода, для диагностики коарктации аорты были предложены косвенные признаки патологии в антенатальном периоде: дилатация правого желудочка и его гипертрофия (см. рис. 3), дилатация легочной артерии [6, 7, 14]. Авторы считают, что это достоверные признаки и встречаются они достаточно часто (в 18 из 24 случаев верифицированных диагнозов коарктации аорты). Поэтому была предложена оценка индексов отношения полости правого желудочка к левому (в норме - 1,1) и легочной артерии к аорте (у здоровых - 1,2). Исходя из увеличения этих параметров, можно предположить наличие затрудненного выброса в аорту или гипоплазию дуги аорты. Тем не менее, по данным предложивших эти косвенные признаки авторов, такие изменения выявляются только в 30% наблюдений (рис. 4).
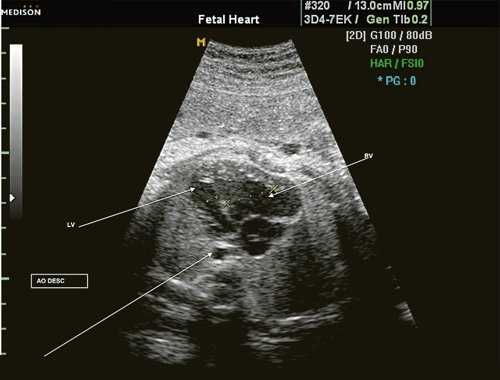
Рис. 4. Диспропорция размеров желудочков сердца при коарктации аорты. RV - правый желудочек; LV - левый желудочек; AO DESC - поперечное сечение нисходящего отдела аорты.
Во второй половине 90-х гг. было опубликовано несколько работ, посвященных изучению диагностической ценности увеличения правого желудочка и уменьшения левого желудочка при коарктации аорты. Авторы, опубликовавшие эти результаты [2], считают, что чем раньше проводится исследование (от 14-16 до 25 нед гестации), тем оно информативнее для диагностики коарктации аорты. Доказательством могут служить данные, полученные D. Brown и соавт. [15]. В представленных исследованиях коарктация аорты отмечена у 8 (62%) из 13 плодов с диспропорцией размеров желудочков до 34 нед и только у 6 (21%) из 29 плодов после 34 нед беременности. Несмотря на то, что более половины случаев коарктации аорты сопровождается диспропорцией размеров желудочков, что достаточно легко выявляется при изучении четырехкамерного среза сердца плода, во многих исследованиях в Норвегии она не была диагностирована, даже при обязательном скрининговом изучении размеров сердца до 18 нед беременности [9].
Такие прoтиворечивые результаты можно объяснить гемодинамической теорией [16, 17]. Внутриутробно в восходящий отдел аорты поступает 50% суммарного выброса крови, в нисходящую - 65%, а через перешеек аорты всего лишь 25%. Исходя из уменьшенного объема кровотока возникает его физиологическое сужение, которое усугубляется лишь после рождения.
Допплеркардиография, позволяющая оценить кровоток, информативна лишь при выраженном сужении аорты [18]. При этом возникает обратная зависимость максимальной скорости кровотока в восходящем и нисходящем отделах аорты. В норме скорость в восходящем отделе немного преобладает над скоростью нисходящего отдела.
При перерыве дуги аорты отмечается ретроградный кровоток заполнения участка дуги аорты после перерыва через открытый артериальный проток и отсутствие прямого кровотока на уровне перерыва.
И, наконец, последняя причина не диагностированной коарктации аорты заключается в частоте сочетания с другими аномалиями сердца. Изолированная коарктация аорты составляет всего лишь 15-18%. По данным M. Campell и P. Polani [19], процент сочетания коарктации аорты с кардиальными аномалиями колеблется от 13 до 18%. Наиболее часто (85%) коарктация аорты сочетается с двустворчатым аортальным клапаном [20], нередко сочетается с фиброэластозом эндомиокарда, распространяющимся на выходной тракт левого желудочка и на межжелудочковую перегородку. Возможно, при коарктации аорты аномальное отхождение правой подключичной артерии или обеих подключичных артерий от нисходящей аорты, дистальней коарктации (5%).
Наличие сопутствующей кардиальной патологии может нивелировать типичные для коарктации гемодинамические изменения со стороны сердца плода, на которые обязательно обращает внимание специалист при ультразвуковом исследовании.
Существует еще и понятие как псевдокоарктация, или "кинкинг" аорты - деформация аорты, аналогичная классической коарктации, но препятствие кровотоку незначительное, так как имеется простое удлинение и извилистость аорты (рис. 5).
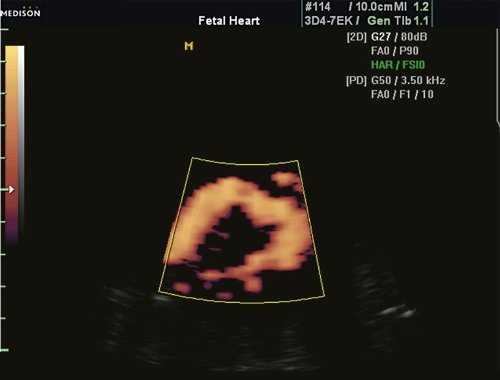
Рис. 5. Кинкинг аорты у плода в 34 нед беременности. Исследование в энергетическом режиме.
Итак, становится очевидным, что практически ни один из ультразвуковых признаков в антенатальном периоде не имеет высокой степени диагностической точности.
Известно, что диагноз данного порока сердца опирается на прямой признак - визуализацию места сужения аорты, и, возможно, расширение проксимального отдела аорты. Однако четко визуализировать участок сужения аорты у плода достаточно трудно и удается только в единичных наблюдениях. Порок можно увидеть лишь тогда, когда имеется уменьшение диаметра перешейка аорты более чем на 1/3 по сравнению с нормой для каждого срока беременности (см. рис. 2, 3).
Ключом к пренатальной диагностике коарктации аорты является комплексный учет данных, получаемых как при изучении четырехкамерного среза сердца (дилатация правого желудочка, гипоплазия левого желудочка), так и при оценке самих главных артерий. При наличии коарктации диаметр аорты в среднем в 2 раза меньше диаметра дилатированной легочной артерии. Поэтому для диагностики коарктации аорты следует использовать визуализацию самой аорты, что наиболее целесообразно при скрининговой оценке среза через три сосуда. Помощь в диагностике может оказать измерение диаметра артериального протока, который при коарктации аорты широкий.
Окончательный диагноз коарктации аорты устанавливается при использовании среза через дугу аорты, так как чаще всего сужение аорты отмечается в области ее перешейка - на уровне впадения артериального протока. Следует отметить, что сужение может охватывать большой участок аорты вплоть до тубулярной гипоплазии. Нормальный переход дуги аорты в артериальный проток в норме гладкий и плавный. Кроме того, при исследовании аорты по длинной оси наиболее надежным признаком следует считать гипоплазию поперечной части дуги аорты. Как один из косвенных признаков коарктации аорты можно использовать извилистость дуги аорты при изучении ее по длинной оси [2].
Важное дополнительное значение имеет допплерэхокардиографическое исследование, которое при коарктации орты позволяет выявить ускорение и турбулентный характер кровотока в аорте. Однако в антенатальном периоде этот признак может не проявиться [2]. Более надежно выявление левоправого шунта через овальное окно. Предполагается, что этот шунт является компенсаторным механизмом, обеспечивающим уменьшение потока крови в левый желудочек и аорту. G. Sharland и соавт. [18] отметили левоправый шунт через овальное окно у 7 из 12 плодов с коарктацией аорты. У оставшихся 5 плодов обнаруживалось как левоправое, так и праволевое направления потоков крови через овальное окно.
В случаях резко выраженных анатомических изменений аорты и функции левого желудочка с увеличением постнагрузки может наблюдаться сердечная недостаточность [21]. Нарушения гемодинамики и сердечная недостаточность характеризуются антенатально наличием выпота в перикарде, уменьшением сердечного выброса с уменьшением размеров левого желудочка [22].
После рождения и закрытия артериального протока весь поток крови поступает в восходящий отдел аорты и перешеек расширяется до нормального уровня. После рождения, когда проток перекрывается, коарктация аорты приводит к серьезными клиническим проявлениям.
Итак, анализ возможностей и ошибок ультразвуковой диагностики коарктации аорты в пренатальном периоде показывает насколько проблематично поставить диагноз во всех случаях данного порока сердца у плода. К сожалению, все эхокардиографические антенатальные признаки патологии не обеспечивают высокий процент диагностики.
Хочется надеяться, что развитие новых технологий и накопление позитивного и анализ негативного опыта позволят в будущем повысить процент диагностики такого сложного порока сердца с высокой неонатальной смертностью.
Литература
Возможности эхокардиографии плода в I триместре беременности (11-14 недель)
Московский областной НИИ акушерства и гинекологии (МОНИИАГ), Россия.
Гомельский областной медико-генетический центр с консультацией "Брак и семья", Гомель, Беларусь.
УЗИ сканер RS80
Эталон новых стандартов! Беспрецедентная четкость, разрешение, сверхбыстрая обработка данных, а также исчерпывающий набор современных ультразвуковых технологий для решения самых сложных задач диагностики.
Введение
Актуальность темы пренатальной диагностики врожденных пороков сердца (ВПС) понятна всем врачам, которые связаны с пренатальной диагностикой, неонатологией, педиатрией, кардиологией, генетикой. ВПС являются одной из ведущих причин перинатальной смертности и регистрируются с частотой 4-13 на 1000 живорожденных [1]. В связи с тем, что профилактические мероприятия по предупреждению ВПС не имеют должного успеха, представляется актуальной и необходимой их пренатальная ультразвуковая диагностика.
- Семьи, имеющие ребенка с ВПС.
- Семьи с ВПС у одного или обоих супругов.
- Женщин, страдающих сахарным диабетом, системными заболеваниями соединительной ткани, гипотиреозом.
- Беременных с тератогенной экспозицией в ранние сроки беременности (герпес ранее 6-7-й недели) [2].
Однако параллельно другими учеными эти группы риска отвергались, потому что большинство ВПС встречались у плодов и детей, матери которых не входили ни в одну из предложенных групп риска. Единственными разумными критериями так называемого селективного отбора были признаны беременные, попавшие в группу риска после проведения скрининга I триместра и беременные с подозрением на ВПС при ультразвуковом исследовании (УЗИ) плода [3].
Неоспоримо, что оптимальными сроками беременности для исследования сердца плода являются 20-22 недели, однако большинство летальных и клинически значимых пороков сердца могут быть диагностированы в конце I триместра беременности. Позволим себе процитировать слова главы Fetal Medicine Foundation Кипраса Николаидеса, высказанные им на страницах сайта FMF (www.fetalmedicine.com): "Специалист ультразвуковой диагностики с 12 недели беременности должен заверить большинство родителей, что у их ребенка нет крупных врожденных пороков сердца. В случае крупных врожденных пороков сердца их раннее выявление может привести к постановке правильного диагноза или хотя бы вызвать подозрение для осуществления ультразвукового мониторинга".
Главная цель пренатальной диагностики сформулирована специалистами пренатальной диагностики всего мира - это обеспечение женщины максимально возможной информацией о пороке как можно раньше. Мы должны дать право женщине и семье в целом решать вопрос о пролонгировании беременности с грубыми пороками развития у плода [4].
С каждым годом все большее количество публикаций посвящается диагностике ВПС в ранние сроки - в I триместре беременности 6. Практически ни один из выпусков журнала ISUOG (Ultrasound In Obstetrics and Gynecology, или "белого" журнала, как его называют специалисты) не обходит своим вниманием тему ранней диагностики врожденных пороков развития.
На самом знаменитом сайте в мире пренатальной диагностики www.thefetus.net (Philippe Jeanty, USA) опубликовано уже более 30 случаев находок ВПС в I триместре беременности. Однако в отечественной периодике встречаются лишь единичные работы по этой теме. Все они пренадлежат "перу" специалистов пренатальной диагностики Российской ассоциации врачей ультразвуковой диагностики в перинатологии и гинекологии, хотя для многих специалистов как раньше, так и сейчас осмотр сердца плода в сроки 11-14 недель заключается лишь в констатации числа сердечных сокращений.
Цель эхокардиографии в I триместре беременности состоит в выявлении летальных и клинически значимых ВПС. Это исследование не ставит целью выявление стенозов и гипоплазий выносящих трактов, диагностику мелких дефектов перегородок, патологий дуги аорты и артериального протока. Многие из этих пороков не только технически невозможно заподозрить в I триместре, манифестируют они после 30-й недели беременности, т.е. их диагностика является прерогативой исследования III триместра.
Точность пренатальной диагностики ВПС во все сроки беременности варьирует в широком диапазоне. Причинами этого могут быть разный опыт специалистов, ожирение беременной, частота использованных ультразвуковых трансдьюсеров и класс ультразвукового аппарата, перенесенные ранее абдоминальные операции, срок беременности, количество околоплодных вод и положение плода. Однако заметим, что многие из этих факторов теряют свою актуальность именно при проведении трансвагинальной эхокардиографии в I триместре беременности. Своевременная диагностика ВПС позволяет идентифицировать плоды высокого риска по генетическим синдромам, что имеет важное значение при проведении пренатального консультирования и оказывает существенное влияние на акушерскую тактику.
Результаты
С 2006 по 2011 г. пренатально в I триместре беременности были выявлены 125 ВПС. Из них 68 (55%) ВПС сочетались с различными хромосомными аномалиями (ХА) плода, 30 (24%) входили в состав различных множественных врожденных пороков развития (МВПР), 27 (21%) ВПС были изолированными.
При эхокардиографии изучались четырехкамерный срез сердца плода (рис. 1) и срез через три сосуда (рис. 2). УЗИ проводилось трансабдоминальным датчиком, лишь при необходимости (затрудненная визуализация) использовался внутриполостной датчик. Четырехкамерный срез сердца плода при ультразвуковом сканировании трансабдоминальным датчиком визуализировался в 85% случаев, срез через сосуды - в 73%, при использовании трансвагинального датчика эти цифры существенно возрастали до 100 и 91% соответственно. Оптимизация пренатальной диагностики ВПС может быть достигнута путем строгого соблюдения основных методических правил. При оценке четырехкамерного среза плода необходимо оценить нормальное расположение сердца плода, исключив его эктопию (рис. 3), положение оси сердца плода, что не представляет никаких трудностей, нормальные пропорции и размеры камер сердца, движение створок атриовентрикулярных клапанов должно быть свободным, септальная створка трикуспидального клапана должна располагаться ближе к верхушке сердца (рис. 4). При оценке среза через три сосуда необходимо оценить взаиморасположение сосудов и их диаметр.
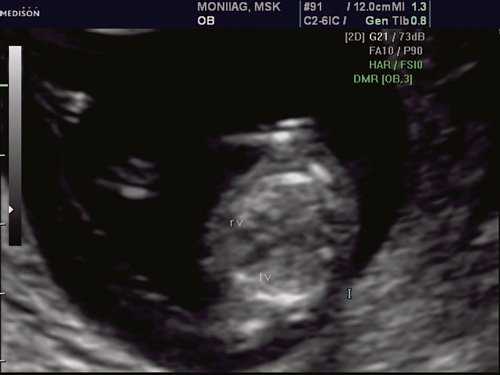
Рис. 1. Беременность 12 недель. Четырехкамерный срез сердца плода. Отчетливо видны камеры сердца.
Читайте также:
- Рекомендации по анализу рентгенограммы запястья в ЗП проекции
- Техника, этапы операции реконструкции латеральных связок голеностопного сустава с использованием аутосухожилия подошвенной мышцы
- Профессиональные заболевания уха. Особенности профессиональных заболеваний уха
- Гастроэнтерит, вызванный E. coli
- Синдром Гирке (Gierke)
