Дифференциальная диагностика воспалительных и инфекционных заболеваний толстой кишки
Добавил пользователь Владимир З. Обновлено: 28.01.2026
Для цитирования: Фадеева Н.А., Артыкова Г.Б., Филимонов А.Ю. и др. Трудности дифференциальной диагностики воспалительных заболеваний кишечника. Эффективная фармакотерапия. 2022; 18 (14): 58-64.
- Аннотация
- Статья
- Ссылки
- Английский вариант
Представлен клинический случай осложненного течения болезни Крона (БК) у пациентки пожилого возраста. В статье отражены особенности диагностики, тактики консервативного и хирургического лечения БК, а также своевременной диагностики колоректального рака у пациента с БК пожилого возраста.
- КЛЮЧЕВЫЕ СЛОВА: болезнь Крона, воспалительные заболевания кишечника, биологическая терапия, устекинумаб, ведолизумаб, колоректальный рак
Представлен клинический случай осложненного течения болезни Крона (БК) у пациентки пожилого возраста. В статье отражены особенности диагностики, тактики консервативного и хирургического лечения БК, а также своевременной диагностики колоректального рака у пациента с БК пожилого возраста.
Рис. 1. Компьютерная томография с контрастированием: выраженное утолщение стенок ободочной кишки в области установленных стентов
Болезнь Крона (БК) и язвенный колит (ЯК) относятся к хроническим аутоиммунным воспалительным заболеваниям кишечника (ВЗК), имеющим волнообразный характер течения. Длительное время ВЗК были наиболее распространены среди лиц молодого возраста, однако со временем стало возрастать число заболеваний среди пожилых людей. Согласно данным мировой литературы, около 25-35% пациентов с ВЗК старше 60 лет, из них 15% - это пациенты с впервые установленным диагнозом позднее 60 лет и 20% - пациенты с ВЗК, диагностированным в молодом возрасте, перешедшие в статус пожилых пациентов [1, 2].
Известно, что БК может поражать любой участок желудочно-кишечного тракта от ротовой полости до перианальных областей, но зачастую затрагивает терминальный отдел подвздошной кишки. Пожилые пациенты с БК имеют нетипичные проявления болезни: характерна локализация БК в толстой кишке, реже - в терминальном отделе подвздошной кишки; клинически этих больных чаще беспокоят ректальные кровотечения, реже - боли в животе, лихорадка, снижение массы тела [3].
В связи с разнообразием клиники, коморбидностью, полипрагмазией у пациентов с ВЗК пожилого возраста необходимо помнить о дифференциальном диагнозе, в первую очередь со злокачественными новообразованиями, ишемическим колитом, колитом на фоне приема нестероидных противовоспалительных препаратов, клостридиальной инфекцией [4].
В течение первых 10 лет от дебюта БК у половины пациентов с БК в любом возрасте необходимо хирургическое лечение в связи с осложненным течением заболевания. Однако оперативное лечение не приводит к полному излечению от БК [5, 19].
Пожилые пациенты с ВЗК имеют более высокий риск хирургического вмешательства при постановке диагноза или вскоре после него, в то время как долгосрочная частота операций аналогична другим возрастным группам.
По данным клинических наблюдений в специализированных центрах и рандомизированных клинических исследований, спустя год после операции частота эндоскопического рецидива БК по шкале Rutgeerts достигает 75% [6].
Таким образом, пациентам с БК в зависимости от сочетания факторов риска, а также эффективности ранее проводившейся терапии показано назначение или продолжение длительной противорецидивной терапии через четыре недели после хирургического лечения [7].
Клиническое наблюдение
Больная Д., 70 лет, поступила в гастроэнтерологическое отделение Московского клинического научного центра (МКНЦ) им. А.С. Логинова в июне 2021 г.
Из анамнеза известно, что в феврале 2021 г. на фоне полного благополучия пациентка впервые отметила появление спастических болей в животе, а также учащение стула до трех раз в сутки. В марте 2021 г. амбулаторно по месту жительства в Клинико-диагностическом центре № 6 выполнена колоноскопия (КС) с осмотром ободочной кишки до нисходящего отдела, по данным которой выявлены дивертикулез толстой кишки, полиповидное образование сигмовидной кишки (тип 0-1р). В описании протокола эндоскопического исследования данных за воспалительные изменения слизистой оболочки толстой кишки не было. Однако в заключении патоморфологического исследования биоптатов толстой кишки получено следующее описание: очаговая гиперплазия слизистой оболочки толстой кишки с фокусами неоплазии тяжелой степени на фоне активного колита с косвенными признаками эрозирования. В связи с этим больная была направлена к онкологу по месту жительства для дообследования. Выполнена магнитно-резонансная томография органов брюшной полости - изменения сигмовидной кишки следует дифференцировать с крупным полипом и аденомой.
31 марта 2021 г. на фоне резкого ухудшения состояния - появления режущих болей в нижних отделах живота, учащения стула до 10 раз в сутки с примесью крови - бригадой скорой медицинской помощи больная была госпитализирована в хирургическое отделение Городской клинической больницы (ГКБ) им. В.В. Вересаева г. Москвы. По результатам проведенного обследования (компьютерная томография (КТ) органов брюшной полости с внутривенным контрастированием, КС) выявлены стриктуры поперечной и нисходящей ободочной кишки, эрозивный колит. Согласно медицинской документации, в отделении хирургии проводили консервативную терапию - без эффекта, в связи с чем 3 апреля 2021 г. проведено эндоскопическое стентирование поперечной и нисходящей ободочной кишки. При морфологическом исследовании биоптатов толстой кишки выявлен хронический эрозивный колит высокой степени активности. После эндоскопического стентирования ободочной кишки больная выписана на амбулаторное лечение под наблюдение онколога, хирурга, колопроктолога по месту жительства.
13 апреля 2021 г. амбулаторно в ГКБ № 62 по результатам колоноскопии картина соответствовала язвенному колиту, субтотальное поражение, высокой степени активности; эндоскопическая картина подозрительна в отношении новообразования ободочной кишки на фоне язвенного колита. При морфологическом исследовании выявлен хронический колит высокой степени активности; опухолевого роста не обнаружено.
Пациентке впервые назначена местная терапия свечами с месалазином 1 г в сутки с кратковременным положительным эффектом.
Однако 17 мая 2021 г. в связи сохраняющимся болевым синдромом пациентка самостоятельно обратилась в консультативно-диагностическое отделение МКНЦ им. А.С. Логинова, где была осмотрена колопроктологом и направлена на госпитализацию в гастроэнтерологическое отделение для уточнения диагноза и коррекции терапии.
По данным лабораторных исследований, в общем анализе крови отмечено снижение уровня гемоглобина (Нb) до 117 г/л, увеличение СОЭ до 68 мм/ч, повышение С-реактивного белка до 10 мг/л; в биохимическом анализе крови - снижение уровня железа до 7,2 ммоль/л, умеренная белково-энергетическая недостаточность (гипопротеинемия до 58 г/л и гипоальбуминемия до 33 г/л). Сданы анализы крови на онкомаркеры: отмечено повышение раково-эмбрионального антигена до 9 нг/мл (норма 0-5,0 Ед/мл), СА-19-9 до 37,3 Ед/мл (норма 0-30 Ед/мл).
По данным УЗИ органов брюшной полости и кишечника выявлены признаки функционирующих стентов ободочной кишки (поперечной-ободочной, нисходящей ободочной), умеренно выраженных воспалительных изменений стенки поперечно-ободочной и нисходящей ободочной кишки.
При КТ-энтерографии с внутривенным контрастированием в области установленных стентов отмечалось выраженное утолщение стенок толстой кишки, что соответствовало воспалительным изменениям (рис. 1).
При КС эндоскоп проведен в купол слепой кишки, на осмотренных участках слизистой ободочной кишки признаки сегментарного активного воспаления с эрозированием, наиболее соответствующего болезни Крона, слизистая прямой кишки и терминального отдела подвздошной кишки не изменена, состояние после стентирования непокрытыми нитиноловыми стентами поперечной и нисходящей ободочной кишки с признаками изъязвления в области стентов, прорастание стентов грануляционной тканью с сохранением просвета кишки, эпителиальные образования слепой, восходящей и сигмовидной кишки с признаками аденом (рис. 2).
По результатам морфологического исследования биопсийного материала, взятого при КС, получены данные о хронических воспалительных изменениях стенок толстой кишки в пораженных отделах, а также диагностирована тубулярная аденома высокой степени активности с признаками стромальной инвазии, аденома с низкой степенью дисплазии. Однако дифференцировать воспалительное заболевание кишечника по данным гистологического исследования не представлялось возможным (рис. 3).
С учетом тяжелого течения заболевания, выявленной при морфологическом исследовании дисплазии проведен общебольничный консилиум в составе ведущих специалистов МКНЦ им. А.С. Логинова, сформулирован клинический диагноз: «Недифференцированный колит, впервые выявленный, тяжелой степени, высокой активности». Принято решение о проведении на первом этапе хирургического лечения.
23 июня 2021 г. выполнено оперативное вмешательство в объеме субтотальной колэктомии с формированием концевой илеостомы. Интраоперационно: свободной жидкости в брюшной полости не выявлено. Печень, желудок, тонкая кишка гладкие, блестящие, без патологических изменений. Ободочная кишка отечная, местами дилатирована, истончена. В области нисходящей ободочной, а также поперечно-ободочной кишок визуализированы максимально уплотненные, отечные участки, в которых пальпаторно определяются металлические стенты. Терминальный отдел подвздошной кишки без признаков воспаления или отека (рис. 4).
По данным морфологического исследования операционного материала визуализированы участки трансмурального воспаления с формированием щелевидных язв и эпителиоидно-клеточных гранулем с гигантскими многоядерными клетками. Отмечалась также гиперплазия нейронов межмышечных нервных ганглиев и встречались участки пилорической метаплазии. Комплекс этих морфологических изменений позволил верифицировать у пациентки болезнь Крона. Кроме того, в операционном материале были выявлены гистологические признаки низкодифференцированной слизистой аденокарциномы с прорастанием в мышечный слой до адвентиции (рис. 5).
Таким образом, согласно результатам гистологического исследования операционного материала, впервые установлен диагноз: «Болезнь Крона в форме колита, впервые выявленная, тяжелой степени, высокой активности, осложненная формированием стриктур ободочной кишки от 04.2021». Операции: субтотальная колэктомия с формированием концевой илеостомы от 23.06.2021. Рак поперечной ободочной кишки рT2N0M0 G2.
Пациентка консультирована онкологом - полихимиотерапевтическое лечение в настоящее время не показано, рекомендовано наблюдение онколога по месту жительства.
В послеоперационном периоде была проведена терапия препаратами 5-аминосалициловой кислоты 4 г в сутки; антибактериальная терапия; коррекция водно-электролитных, метаболических нарушений; назначены препараты железа, превентивная антикоагулянтная терапия. Пациентка выписана под наблюдение онколога, гастроэнтеролога, хирурга по месту жительства. Рекомендовано контрольное обследование через 6 месяцев.
Согласно мировым клиническим исследованиям, второй пик заболеваемости ВЗК приходится на пожилой возраст (60-74 года) [8].
С учетом нетипичного течения заболевания в пожилом возрасте, сопутствующих заболеваний, повышенного риска хирургических осложнений пациентам данной группы показано мультидисциплинарное ведение с участием специалистов: гастроэнтеролога, колопроктолога, нутрициолога, ревматолога, фтизиатра, кардиолога.
Все пациенты с ВЗК нуждаются в скрининге колоректального рака (КРР) [9]. Само начало ВЗК в пожилом возрасте не связано с дополнительным повышенным риском КРР, хотя время между началом ВЗК и диагнозом КРР у пожилых пациентов, по-видимому, короче. Таким образом, следует проводить скрининг КРР пациентов с ВЗК в пожилом возрасте как можно раньше. По результатам морфологического исследования биоптатов толстой кишки у пациентки Д. выявлена дисплазия низкой и высокой степени в нескольких фрагментах, лабораторно - незначительное повышение онкомаркеров, а также имелся высокий риск хирургических осложнений (перфорация) в связи с ранее установленными стентами. Таким образом, принято решение на первом этапе о проведении хирургического лечения с последующим гистологическим исследованием операционного материала для уточнения диагноза.
В ГКБ им. В.В. Вересаева при выявлении сужений в области поперечной и нисходящей ободочной кишки врачами принято решение об эндоскопической установке самораскрывающихся стентов. Однако с учетом наличия у пациентки воспалительного заболевания кишечника, согласно рекомендациям Европейской организации по изучению язвенного колита и болезни Крона (European Crohn's and Colitis Organization - ECCO), установка стентов нецелесообразна [10, 11]. Установка колоректального стента может быть произведена при злокачественных новообразованиях толстой кишки как с паллиативной целью, так и для предоперационной подготовки [12].
Согласно результатам гистологического исследования биоптатов слизистой оболочки толстой кишки, при КС дифференцировать ЯК и БК не представлялось возможным. По морфологическому исследованию операционного материала в связи с наличием участков трансмурального воспаления и формированием глубоких щелевидных язв и эпителиоидно-клеточных гранулем с гигантскими многоядерными клетками был выставлен диагноз «болезнь Крона в форме колита».
Данное клиническое наблюдение демонстрирует трудности дифференциальной диагностики осложненного течения БК толстой кишки у пожилого пациента. У каждого пациента с БК независимо от возраста необходимо учитывать риски послеоперационных рецидивов, к которым, по данным российских клинических рекомендаций, относятся: курение, пенетрирующий фенотип, перианальные поражения, предшествующие резекции кишки, резекция протяженного сегмента тонкой кишки (более 50 см), раннее начало заболевания [13, 14]. В зависимости от количества и сочетания факторов риска пациенты должны быть стратифицированы в группы риска. Больные, имеющие два и более факторов, относятся к группе высокого риска послеоперационного рецидива. У пациентки Д. определен низкий риск рецидива БК, однако по жизненным показаниям ей рекомендована длительная противорецидивная терапия.
Терапия, применяемая в более молодых возрастных группах, подходит и пожилым пациентам, но должное внимание необходимо уделять также побочным эффектам и лекарственным взаимодействиям. Сложности ведения пациентов пожилого возраста с ВЗК заключаются в коморбидности, полипрагмазии, ограничениях в возможности назначения длительной иммуносупрессивной терапии. Так, при назначении иммуносупрессоров из группы тиопуринов повышается риск развития онкологических заболеваний и панцитопении. По данным метаанализа А. Kandiel и соавт., риск лимфомы у пациентов с ВЗК, получавших азатиоприн и 6-меркаптопурин, был увеличен в четыре раза [15]. Иммуносупрессивная терапия, особенно в сочетании с другими лекарствами, и пожилой возраст связаны с повышенным риском оппортунистических инфекций, включая туберкулез [16, 17]. В многоцентровом клиническом исследовании пожилые пациенты имели более высокий риск инфекций, злокачественных новообразований и смертности по сравнению с молодой группой при использовании генно-инженерных биологических препаратов (ГИБП) из группы ингибиторов фактора некроза опухоли (ФНО) альфа - инфликсимаба и адалимумаба [18]. Таким образом, пациентке Д. в связи с пожилым возрастом, наличием в анамнезе онкологического заболевания (аденокарцинома толстой кишки) крайне нежелательно назначение иммуносупрессивной терапии тиопуринами, ГИБП из группы анти-ФНО-альфа.
В качестве противорецидивной терапии пациентке Д. наиболее предпочтительно применение ГИБП с благоприятным профилем безопасности - ингибитора ИЛ-12/ИЛ-23 (устекинумаба) или блокатора интегринов альфа-4-бета-7 (ведолизумаба) [20, 21].
Ведолизумаб - гуманизированное моноклональное антитело класса IgG-1, селективно блокирует взаимодействие α4-β7-интегрина с молекулами клеточной адгезии слизистой оболочки адрессином-1 (MAdCAM-1).
В отличие от ведолизумаба молекула устекинумаба имеет уникальный механизм действия класса ингибиторов ИЛ-12/23, обусловленный блокированием ключевых регуляторных цитокинов, обеспечивает эффективность системного и безопасность селективного биологического препарата [22]. Профиль безопасности устекинумаба в отношении риска возникновения инфекций, в том числе туберкулеза, и малигнизации сопоставим с плацебо и препаратами селективного механизма действия и остается благоприятным на протяжении длительного времени [23, 24].
При выборе между устекинумабом и ведолизумабом представляется важным отметить, что устекинумаб ингибирует путь активации как Th1-клеток, так и Th17-клеток, прерывая внутриклеточную и нижележащую передачу сигналов ИЛ-12 и ИЛ-23, и, как следствие, эффективен как при ранней болезни Крона, так и на поздних стадиях заболевания. Ведолизумаб ингибирует только путь активации Th1-клеток, поэтому может быть эффективен преимущественно в ранней фазе БК (6-10 недель) [25].
Следовательно, устекинумаб представляется более предпочтительным в данной клинической ситуации.
Таким образом, приведенное клиническое наблюдение демонстрирует осложненное течение БК с поражением толстой кишки в пожилом возрасте. Необходимо помнить, что специфического маркера ВЗК не существует - диагноз устанавливается на основании анализа совокупности данных (клинических, эндоскопических, рентгенологических и морфологических). Своевременная диагностика ВЗК обеспечивает лучшие результаты лечения, снижает риск развития колоректального рака и хирургических осложнений.
Дифференциальная диагностика воспалительных и инфекционных заболеваний толстой кишки
предоставляем актуальную медицинскую информацию от ведущих специалистов, помогая врачам в ежедневной работе
Для цитирования: Воспалительные заболевания кишечника. Проблемы дифференциальной диагностики и лечения. РМЖ. 2006;3:154.
В группу ВЗК объединены два заболевания - болезнь Крона и неспецифический язвенный колит (НЯК). Для этих заболеваний характерны различная распространенность патологического процесса в ЖКТ, разная глубина поражения слизистой оболочки кишки, определенные морфологические признаки, а также различное течение и прогноз. Несмотря на это некоторые сходные особенности, такие как общность патогенетических механизмов развития этих заболеваний, и вследствие этого единые подходы к лечению, а также сходные клинические проявления позволяют объединять эти два заболевания в одну группу.
Эпидемиология НЯК и болезни Крона очень схожи. При обоих заболеваниях наиболее низкая распространенность наблюдается в африканских и азиатских странах. Частота язвенного колита в России составляет 20 на100 000 населения (из них около 10% - дети), а болезни Крона 3,5 на 100 000 (20-25% дети). В США распространенность НЯК у детей в возрасте 10 - 19 лет составляет 2 на 100 000 населения. Распространенность в Великобритании и Швеции возросла вдвое, достигнув 16,6 на 100 000.
Этиология и патогенез ВЗК до настоящего времени до конца не определены. При ВЗК возникает иммунопатологический процесс в слизистой оболочке ЖКТ, при БК в любом его отделе и при неспецифическом язвенном колите только в толстой кишке. В качестве триггеров обсуждается роль некоторых вирусов, бактерий. В настоящее время доказана роль CARD15/NOD2 гена в предрасположенности к развитию БК. При этом показано, что активизация CARD15, возникающая под воздействием компонентов бактериальной стенки, вызывает активацию провоспалительных молекул.
Диагностика ВЗК очень сложна. В среднем на установление диагноза уходит около 5 лет. Диагноз ВЗК основывается на клинических данных и данных обязательных обследований, включающих рентгенологическое, эндоскопическое и гистологическое исследования.
Одним из важных этапов дифференциальной диагностики является исключение кишечных инфекций, паразитов. Обычные кишечные инфекции могут вызывать сходные клинические симптомы (диарея, боли в животе, кровь в стуле), внекишечные проявления (реактивный артрит, узловатая эритема), а также в ряде случаев сходные эндоскопические и гистологические изменения (отек и воспаление слизистой, крипт абсцессы, крипт язвы).
Наиболее часто ВЗК приходится дифференцировать с иерсиниозами, вызываемыми Yersinia Enterocolitica и Yersinia pseudotuberculosis. Иерсиниозы протекают с болями в животе, диарейным синдромом, в ряде случаев наблюдается артралгии, нодозная эритема. У некоторых больных боли в животе локализуются в правой подвздошной области, и наблюдается аппендицитоподобный синдром, обусловленный терминальным илеитом, мезаденитом. При эндоскопическом исследовании выявляются афтоидные и продольные язвы в терминальном отделе подвздошной кишки, слепой и восходящей ободочной кишке. В некоторых случаях иерсиниоз приобретает хроническое течение, имитируя развитие ВЗК. При дифференциальной диагностике используют бактериологический и серологический методы. Возбудитель иерсиниоза выделяется из кала, мочи, крови, гноя, операционного материала. Решающее значение в диагностике имеет нарастание титра антител.
Кампилобатерная инфекция вызывается Campylobacter jejuni и Campylobacter fetus. При кампилобактерной инфекции часто развивается энтерит, энтероколит, сопровождающийся диареей, болями в животе, повышением температуры тела, рвотой. Стул часто с прожилками крови, иногда содержит свежую кровь. Возможно развитие реактивного артрита. Эндоскопическая картина слизистой оболочки прямой и сигмовидной кишки, при кампилобактерной диарее может быть практически такой же, как и при неспецифическом язвенном колите и при болезни Крона.
Диагностика основана на выделении кампилобактеров из фекалий больного, а также на определении в крови специфических антител в диагностических титрах.
Salmonella обладает выраженной инвазивностью и цитотоксичностью к эпителию кишечника, но может проникать и внутрь эпителиоцитов в собственную пластинку слизистой оболочки. Нередко отмечаются глубокие воспалительные изменения, доходящие до подслизистого слоя. Эндоскопические изменения при сальмонеллезном колите трудно отличить от таковых при НЯК, но при сальмонеллезе часто наблюдается терминальный илеит. В диагностике помогает выделение сальмонеллы из кала, мочи, желчи и нарастание титра антител в крови.
Шигеллез. Симптомами шигеллеза являются, боли в животе, лихорадка, диарея, тенезмы с выделением слизи, крови. При эндоскопическом исследовании больных шигеллезом выявляются выраженное поражение ректосигмоидного отдела толстой кишки и различное по интенсивности поражение проксимальных отделов толстой кишки. Эндоскопическая картина приблизительно в 15% случаев при инфицировании Shigella поражается вся толстая кишка. В некоторых случаях, как правило, у ослабленных детей инфицирование Shigella вызывает затяжное течение заболевания. Шигеллез иногда развивается как суперинфекция при БК.
Escherichia coli. Взаимоотношения E.coli и БК сложные. Кишечную инфекцию, вызываемую штаммом O157:H7 E.coli, крайне трудно отличить клинически и эндоскопически от БК. Дифференциальная диагностика проводится с помощью бактерилогического метода. Однако при иммуногистохимическом исследовании биоптатов кишечника больных с БК на поверхности эпителия, в язвах, крипт абсцессах, в собственной пластинке слизистой в макрофагах часто обнаруживаются E.coli. E.coli часто выделяется из операционного материала от больных БК, кроме того, у больных БК часто выявляются высокие титры антител к различным штаммам E.coli (скорее всего, это связано с развитием суперинфекции).
К более редким патогенам, вызывающим сходную картину заболевания, относятся Entamoeba histolytica, Chlamidia trahomatis, Aeromonas hydrophilia, Blastocystis hominis, Mycobacterium avium intracellulare.
Entamoeba histolytica может вызывать острый амебный колит, напоминающий БК. Однако в ряде случаев у больных БК может происходить суперинфицирование дизентерийной амебой. При этом исследование стула и биоптатов, а также серологические методы могут быть отрицательными. У больных, получающих стероидную терапию, возможно развитие фульминантного колита, связанного с суперинфекцией. В связи с этим некоторыми исследователями считается целесообразным назначать больным БК, получающим стероидную терапию, антибактериальные препараты (например, метранидазол).
Aeromonas hydrophila может вызывать развитие диареи с примесью крови в стуле. Последняя в тяжелых случаях может продолжаться до нескольких недель. При этом во время эндоскопического исследования выявляется хронический сегментарный колит, напоминающий БК. Дифференциальная терапия проводится с помощью бактериологического метода.
Blastocystis hominis в ряде случаев может вызывать терминальный илеит. Основными клиническими проявлениеми бластоцистоза являются диарея и боли в животе. Заболевание развивается как по типу простого энтерита, так и в виде энтероколита или колита.
БК нужно также дифференцировать с абдоминальной формой туберкулеза, такими заболеваниями, как гистоплазмоз, криптококкоз, актиномикоз, базидиоболомикоз.
Цитомегаловирусная инфекция (ЦМВ) у иммунокомпрометированных больных может вызывать поражения кишечника, напоминающие ВЗК. Поражения кишечника часто наблюдаются при врожденной ЦМВ инфекции. Однако чаще ЦМВ наблюдается как оппортунистическая инфекция у больных с НЯК и БК, причем при НЯК цитомегаловирус выявляется чаще, чем при БК.
Большие сложности возникают при дифференцировании БК и неспецифического язвенного колита. Известно, что при БК поражается любой отдел пищеварительного тракта, при НЯК только толстая кишка. Для НЯК характерно поражение прямой кишки. Перианальные поражения, свищи, стриктуры характерны для БК. Рецидив после удаления пораженного сегмента толстой кишки при НЯК встречается крайне редко, тогда как при БК процесс прогрессирует, часто наблюдается рецидив заболевания. Однако основными критериями диагностики являются гистологические изменения. При БК воспалительный процесс начинается в подслизистом слое и распространяется на все слои кишечной стенки, (в отличие от НЯК, при котором воспалительные изменения ограничиваются только слизистой оболочкой). Специфическим гистологическим признаком при БК является формирование эпителиоидных гранулем, состоящих из эпителиоидных и гигантских многоядерных клеток. Однако гранулемы встречаются только в 40-60% случаев. Для ВЗК характерна лимфоплазмоцитарная инфильтрация. Присоединяющееся изъязвление эпителия сопровождается инфильтрацией нейтрофилами. Неравномерная плотность инфильтрата собственной пластинки слизистой оболочки также является характерной для БК. Лимфоидные фолликулы нагнаиваются и изъязвляются. При БК язвы чаще бывают глубокие и узкие, могут проникать до субсерозного слоя и окружающей клетчатки, с формированием свищей и спаек с соседними органами.
В последние годы были выявлены специфические маркеры ВЗК. У больных с НЯК в 70% случаев в крови определяются антинейтрофильные цитоплазматические антитела (рANCA). У больных БК - антитела к грибам Saccharomyces cerevisiae (ASCA).
Неясность этиологии ВЗК обусловливает отсутствие этиотропной терапии. Поэтому в настоящее время проводится патогенетическая и симптоматическая терапия этих заболеваний. Основными целями лечения служат достижение и продление ремиссии заболевания, снижение риска развития осложнений, а также улучшение качества жизни пациентов, страдающих ВЗК.
На сегодняшний день основными классами препаратов, использующимися при лечении ВЗК, являются препараты 5-аминосалициловой кислоты (5-АСК), глюкокортикоиды и цитостатики. В последние годы активно разрабатывается молекулярная терапия, включающая препараты, содержащие антитела к ФНО-a, рекомбинантные гуманизированные антитела к а4-интегрину, антиCD3 моноклональные антитела, ИЛ-10, ИЛ-11. Однако многие из этих препаратов пока ограничены в применении, в связи с тем, что некоторые из них до настоящего времени находятся на стадии клинических испытаний, другие имеют высокую стоимость.
При низкой активности заболевания и для поддержания ремиссии применяют препараты, содержащие месалазин (5-АСК). С чем связана эффективность месалазина, до конца не изучено. Однако установлено, что месалазин способен ингибировать циклооксигеназу и подавлять таким образом продукцию простагландинов. Установлено также, что месалазин подавляет липооксигеназный путь метаболизма арахидоновой кислоты активированных нейтрофилов, ингибирует образование цитокинов (ИЛ-1, ИЛ-6), подавляет рецепторы ИЛ-2. Кроме того, показано, что месалазин стимулирует апоптоз клеток колоректального рака, подавляет митоген-активированную протеинкиназу и уменьшает пролиферацию колоректальной слизистой оболочки у больных со спорадическими полипами. Первым препаратом этой группы был сульфасалазин. Сульфасалазин состоит из двух компонентов - сульфапиридина и месалазина. Сульфапиридин играет роль транспортного агента для месалазина. Расщепление сульфасалазина с высвобождением месалазина происходит только в толстой кишке под действием микрофлоры. Рекомендуемая доза сульфасалазина у детей - 50 мг/кг массы тела, ее можно повысить до 80 мг/кг. Неактивный сульфапиридин не обладает терапевтической активностью, а напротив вызывает ряд побочных эффектов, поэтому предпочтительнее использовать препараты, содержащие только месалазин.
Первый чистый препарат месалазина (Салофальк) был создан в 1984 году, в форме ректальных свечей. В настоящее время Салофальк производится в таблетках, гранулах, свечах, клизмах. Таблетки и гранулы, содержащие месалазин, покрыты кишечнорастворимой оболочкой, которая препятствует высвобождению препарата при рН менее 6,0. В отличие от таблеток, гранулы имеют несколько слоев. Внешняя оболочка, содержащая скользящее вещество (любрикант), облегчает проглатывание и транзит гранул. Кишечнорастворимая пленочная оболочка из эудрагита L обеспечивает высвобождение месалазина в дистальных отделах тонкой кишки. Внутреннее ядро на основе полимерной матрицы обеспечивает пролонгированное высвобождение действующего вещества. Салофальк в таблетках выпускается в дозе 250мг и 500мг, салофальк в гранулах - 500мг и 1000 мг. Рекомендуемая доза у взрослых при активных формах НЯК - 1,5-3 г в сутки, при активной форме БК - 3-4,5 г в сутки. Для профилактики рецидивов ВЗК Салофальк назначается в дозе 1,5 г в сутки. У детей рекомендованная доза Салофалька при активной форме ВЗК - 20 мг на 1 кг массы тела, при необходимости доза может быть повышена до 50 мг/кг. Наличие гранул Салофалька в 1000 мг уменьшает общее число приемов препарата. Преимущество гранул Салофалька перед таблетками состоит также в том, что маленькие размеры гранул не позволяют им задерживаться в желудке, гранулы могут приниматься независимо от приема пищи.
При дистальном колите месалазин (Салофальк) можно применять местно через прямую кишку в свечах (1-2 г/сут) и в виде клизм (2 г ежедневно или 4 г через день).
У больных ВЗК при относительно легком течении и для поддержания ремиссии возможна монотерапия препаратами 5-АСК. При тяжелых и распространенных формах заболевания, при недостаточной эффективности от лечения месалазином следует дополнять кортикостероиды. У пациентов БК, имеющих длительный анамнез заболевания с продолжительной кортикостероидной терапией при предыдущих обострениях, лечение 5-АСК неэффективно.
До настоящего времени кортикостероидная терапия является наиболее эффективным методом лечения острых форм БК. Глюкокортикоиды эффективны при любой локализации процесса. Преднизолон назначают в стандартной дозе 1-2 мг/кг в сутки с постепенным уменьшением и отменой в течение 3-4 месяцев. Пероральный прием глюкокортикоидов приводит к развитию таких побочных эффектов, как диабет, гипертензия, остеопороз и повышенная восприимчивость к инфекциям, а также косметические дефекты. В настоящее время широко используется топический кортикостероид - будесонид (Буденофальк). Буденофальк обладает в пять раз большей активностью, чем преднизолон, а 90% всосавшегося Буденофалька быстро инактивируется в печени, благодаря чему побочные глюкокортикоидные эффекты сводятся к минимуму. Доза будесонида для перорального применения составляет 9 мг в сутки, для поддерживающей терапии 3 и 6 мг через день. В индукции ремиссии Будесонид (буденофальк) лишь на 13% менее эффективен, чем системные кортикостероиды, при этом не вызывает характерных для стероидов побочных эффектов. При тяжелом поражении дистальных отделов толстой кишки применяются традиционные глюкокортикоиды в виде клизм или пены, будесонид в клизмах. Отмена будесонида, как и традиционных форм глюкокортикоидов должна проводиться постепенно. Исследования показали, что применение будесонида (буденофальк) при БК, как и других кортикостероидов в качестве поддерживающей терапии во время ремиссии, удлиняет ремиссию, но не предотвращает появление рецидива.
В случае если длительная кортикостероидная терапия не приводит к ремиссии или в случае возникновения резистентности или непереносимости, в терапии используют иммуносупрессанты. Механизм их действия включает супрессию функции лимфоцитов (преимущественно Т-клеток). При ВЗК используются азатиоприн или его метаболит 6-меркаптопурин. Суточная доза у взрослых составляет 2-3 мг /кг, у детей 1-2 мг/кг. У детей поддерживающая доза назначается в течение 2 лет после последнего рецидива. При НЯК, рефрактерном к лечению кортикостероидами, применяют метотрексат, циклоспорин. Метотрексат обладает выраженной гепатотоксичностью. Применение метортрексата возможно только с подросткового возраста в дозе 25 мг внутримышечно один раз в неделю или перорально 5 мг через день. При стероидорезистентных формах НЯК применяют также циклоспорин в дозе 2 мг/кг. Эффективность циклоспорина при БК очень низкая. В случае развития бактериальных инфекций применяют антибактериальные препараты - ципрофлоксацин, метронидазол. При отсутствии эффекта от консервативного лечения, а также при возникновении осложнений проводится хирургическое лечение.
Имеются данные о повышенном риске развития рака толстой кишки в случае возникновения НЯК в детском и юношеском возрасте, при тотальном колите, а также при продолжительности заболевания более 10 лет. Клинические исследования показали, что регулярный прием месалазина (Салофалька) снижает риск развития рака у больных НЯК.
Колит - симптомы и лечение
Что такое колит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Куракина Александра Анатольевича, проктолога со стажем в 11 лет.
Над статьей доктора Куракина Александра Анатольевича работали литературный редактор Елена Бережная , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Колит (лат. colitis, от греч. kolon (толстый кишечник) и itis (воспаление) — собирательное понятие, включающее большую группу заболеваний с одним общим признаком: воспалением толстого кишечника.
Основные признаки колита: частый жидкий стул с кровью, боль в животе и высокая температура.
Колиты встречаются в практике гастроэнтерологов, инфекционистов, терапевтов, колопроктологов, хирургов и других специалистов.
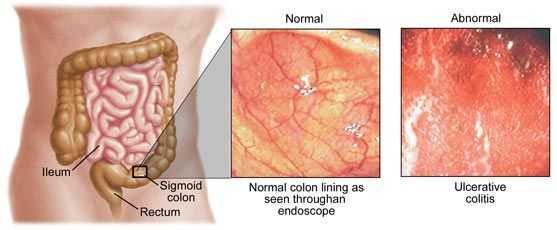
Этиология колита
Основные формы колитов можно описать только по отдельности, в зависимости от этиологического фактора. Размеры статьи не позволяют коснуться всех видов колита. Рассмотрим только основные из них.
Инфекционный колит — это заболевание кишечника, возникающее из-за активизации условно-патогенных микроорганизмов в кишечнике или попадания новых болезнетворных микробов из внешней среды. [1]
Инфекционный колит имеет очень широкое распространение: нет человека, ни разу не переносившего данное заболевание. Количество заболевших увеличивается в жаркий период, когда создаются благоприятные условия для распространения инфекции. Поэтому чаще болеют люди в регионах с жарким климатом (Африка, Юго-Восточная и Средняя Азия). Заболевание чаще встречается в детском возрасте, особенно у детей, посещающих учебные заведения (детские сады, школы и т. д.). Гастроэнтерологи и проктологи могут встречать в практике больных с данной патологией, но она не является профильной. Лечат заболевание обычно инфекционисты.
Причины инфекционного колита:
- бактерии (шигеллы, эшерихии, сальмонеллы, клостридии, иерсинии, брюшнотифозная палочка, кампилобактерии, протей, стафилококки);
- вирусы (аденовирус, энтеровирус, ротавирус);
- простейшие (амебы, лямблии и др.);
- возбудители туберкулеза и сифилиса;
- грибки (кандида, актиномицеты). Возникновение грибкового колита свидетельствует о снижении иммунитета и часто проявляется у лиц, страдающих СПИДом, получающих химиотерапию, стероидные гормоны;
- дисбактериоз.
Формы инфекционного колита:
- катаральная;
- фиброзная;
- катарально-геморрагическая;
- флегмонозная;
- флегмонозно-гангренозная;
- некротическая.
Воспалительные явления могут иметь стадийный характер, а могут сразу иметь картину запущенного воспаления. Его выраженность напрямую зависит от характера инфекции. Некротическое и флегмонозно-гангренозное воспаление встречается при клостридиальной инфекции. Катарально-геморрагическое — при дизентерии. Катаральное воспаление встречается чаще при вирусных заболеваниях. [2]
Ишемический колит — воспаление стенки толстого кишечника, возникающее из-за нарушения процессов кровобращения. Существует хроническое и острое нарушение кровообращения. [3]
Причиной нарушения кровообращения является полное прекращение или критическое снижение притока крови к толстой кишке, вследствие чего возникает воспаление. При тяжёлом течении может приводить к некрозу стенки кишечника. Причиной закупорки сосудов могут быть тромбы, но чаще всего к сужению просвета сосуда приводят атеросклеротические бляшки. Поэтому болезнь чаще проявляется у лиц пожилого возраста. Около 79% больных ишемическим колитом старше 48 лет. [4] Частота встречаемости не имеет связи с половой принадлежностью и регионом. Впервые открыт в 1966 году. Ишемический колит является профильным заболеванием для колопроктологов, но им также занимаются общие хирурги и гастроэнтерологи. [5]
Причины ишемического колита:
- сосудов;
- закупорка брыжеечных сосудов вследствие эмболии или тромбоэмболии (в результате аллергических реакций, травм, осложнений операций, системного васкулита, ДВС-синдрома);
- снижение давления крови может приводить к нарушению питания стенки кишки.
Закупорка просвета сосуда приводит к ишемии стенки кишки, а как следствие — к некрозу и далее перфорации. [6]
Объём поражения зависит от размера питающей артерии, длительности закупорки. Если закупорка сосуда происходит постепенно (при образовании атеросклеротических бляшек в сосудах), то говорят о хроническом нарушении кровообращения, что в свою очередь приводит к стриктурам.
При критических состояниях и снижении давления крови (например, анафилактический шок, ДВС-синдром и т.д.), происходит централизация кровообращения, при этом резко снижается приток крови к кишечнику, что приводит к ишемии и некрозу.
При атеросклерозе чаще страдает сигмовидная и поперечная ободочная кишка. Воспаление начинается со слизистой оболочки, затем переходит на все слои. [7]
По характеру поражения выделяют:
- транзиторную форму (когда ишемические процессы обратимы);
- стенозирующую (когда формируются стриктуры);
- гангренозную (когда образуются язвы с дальнейшим развитием некроза, поражение носит необратимый характер). [8]
Лучевой колит — образуется в результате ионизирующего воздействия на стенку толстого кишечника.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы колита
Симптомы острого и хронического колита: боль в животе, кровь в кале, диарея, высокая температура, слабость, слизь и кровь в стуле, спазмы.
Симптомы язвенного колита: к перечисленным выше признакам добавляются боли в анусе и анемия.
Боли при колите кишечника:
Инфекционный колит
Клиника инфекционного колита напрямую зависит от возбудителя.
Для любого инфекционного колита независимо от этиологии характерно:
- начало заболевания, как правило, имеет острый характер;
- жидкий частый стул с примесью слизи в кале;
- боли локализуются чаще в левом подреберье, но могут также распространяться по всем отделам живота;
- боль имеет периодический, спазматический характер;
- высокая температура;
- чувство слабости, недомогания;
- сухость кожных покровов и слизистых;
- белый налет на корне языка;
- рвота как первый симптом колита кишечника (если в воспалительный процесс вовлечен желудок).
Для первичной оценки этиологии инфекционного колита оценивают характер дефекации, объём и особенности каловых масс.
- при дезентерии стул очень частый, малыми порциями (до 20 раз за день) со слизью и прожилками алой крови (ректальный «плевок»);
- при амебиазе кал имеет вид малинового желе;
- при сальмонеллезе кал напоминает болотную тину, имеет неприятный запах;
- при псевдомембранозном колите (вызыванном клостридиями) частый жидкий стул с запахом гнили.
Ишемический колит
Симптоматика очень вариабельна, характерно быстрое прогрессирование.
- болезненные ощущения в животе;
- кровь и слизь в стуле;
- неустойчивый, частый стул;
- выраженные боли в околопупочной и левой подвздошной области;
- при ректальном осмотре можно заметить кал с кровью, слизью или гноем;
- при хронической форме боли имеют низкую интенсивность, обычно возникают после еды;
- при длительной хронической ишемии появляются стриктуры в толстой кишке, которые в дальнейшем могут быть следствием непроходимости или малигнизации (раковому перерождению).
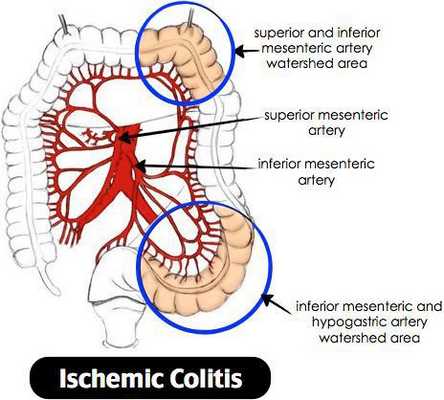
Лучевой колит
Обычно колит формируется у лиц, перенёсших курс лучевой терапии по поводу новообразований, локализующихся в области малого таза или брюшной полости. [12]
- большую чувствительность к излучению имеет тонкий кишечник, формируется лучевой энтерит, который клинически проявляется нарушением абсорбции в тонком кишечнике;
- повреждению кишечника свойствен избирательный характер, обычно воспаление локализуется в прямой и сигмовидной кишке, при этом клиника сопоставима с клиникой язвенного и ишемического колита. При воздействии больших доз радиации клиника развивается не сразу, проявляется обильным, жидким стулом, при этом нарушается всасывание в толстом кишечнике. [13]
Патогенез колита
Толстый кишечник очень восприимчив к ионизирующему излучению. [10] Лучевой колит возникает при воздействии малых доз облучения: происходит атрофия слизистой оболочки (сразу после облучения).
- Усиливаются процессы деления клеток, уменьшается длина ворсинок.
- Активизируются воспалительные процессы с нейтрофильной реакцией. Чаще всего эти процессы локализуются в прямой и сигмовидной кишке.
- При воздействии больших доз (более 40 Гр.) воспалительные процессы могут возникать спустя длительное время после облучения (до нескольких лет), в данной ситуации происходит воспаление мелких сосудов кишечника, что приводит к ишемизации кишечника. Развиваются язвы и стриктуры. Могут поражаться все отделы толстого и тонкого кишечника. [11]
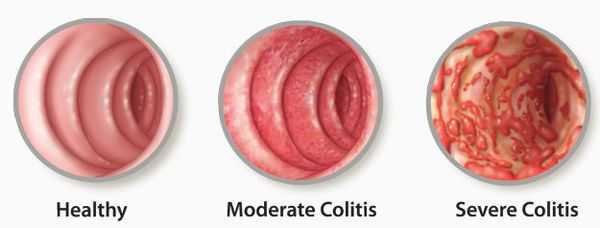
Классификация и стадии развития колита
По течению:
По этиологии:
- язвенный колит кишечника и болезнь Крона (воспалительные заболевания кишечника с неизвестной этиологией);
- инфекционный (этиологический фактор бактериальный, вирусный, грибковый, паразитарный);
- ишемический (развивается вследствие снижения притока крови к толстой кишке);
- спастический (из-за неправильного питания нарушается моторика толстого кишечника и возникают спазмы);
- токсический (при применении нестероидных противовоспалительных препаратов);
- лучевой (при поражении радиацией).
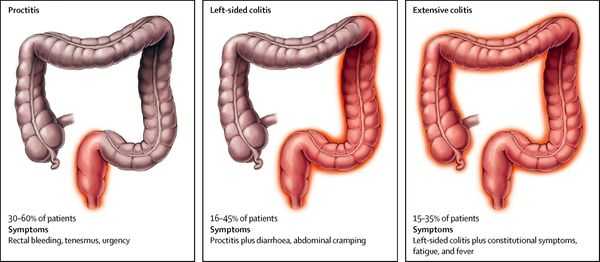
По локализации:
| Вид колита | Локализация |
|---|---|
| проктит | воспаление прямой кишки |
| панколит | тотальное поражение кишечника |
| тифлит | воспаление слепой кишки |
| трансверзит | воспаление поперечной ободочной кишки |
| сигмоидит | воспаление сигмовидной кишки |
| диффузный колит кишечника | охватывает два и более отдела кишечника |
Поражение кишечной стенки подразделяют на три вида:
- катаральный колит кишечника — слабое воспаление, слизистая краснеет, и возникает отёк;
- эрозивный колит кишечника — появляются эрозии;
- атрофический колит кишечника — слизистая атрофируется.
Осложнения колита
- сильное кровотечение;
- перфорация толстой кишки;
- сильное обезвоживание; ;
- воспаление кожи, суставов и глаз;
- повышенный риск рака толстой кишки;
- токсичный мегаколон;
- повышенный риск образования тромбов в венах и артериях [15] .
Диагностика колита
Инфекционный колит:
- Лабораторные методы:
- анализ кала на вирусы, бактерии, паразиты (позволяет точно поставить диагноз);
- серологическое исследование (определяют антитела к вирусам, паразитам);
- анализ крови на стерильность (при подозрении на сепсис);
- общеклинический анализ крови (высокое СОЭ, увеличение количества лимфоцитов при вирусной этиологии).
- Инструментальные методы:
- ректороманоскопия используется как дополнительный метод для дифференциальной диагностики;
- ультразвуковое исследование используется для исключения осложнений.
Ишемический колит:
- Ректороманоскопия дает возможность оценить состояние слизистой оболочки. При осмотре можно отметить наличие точечных кровоизлияний, сглаженность сосудистого рисунка, бледность слизистой. При обнаружении данных признаков показано взятие биопсии.
- Ирригоскопия — самое необходимое исследование. Обнаруживается симптом пальцевых вдавливаний. Признаки дефектов слизистой свидетельствуют о наличии язв, сужения просвета при стриктурах.
- Колоноскопия показана для уточнения распространенности воспаления, также показана биопсия в области измененного участка.
- Ангиография позволяет определить степень сужения сосуда и его локализацию. [9]
- Злокачественные новообразования. Опухоли развиваются достаточно длительное время, в течении многих лет.
- Инфекционный колит. Преобладают симптомы общей интоксикации (слабость, лихорадка и т.д.). Кроме того, имеет место эпидемический анамнез.
- Язвенный колит и болезнь Крона. Для них характерно достаточно медленное прогрессирование. Проявляются обычно в раннем возрасте.
Лучевой колит:
- При сборе анамнеза учитывают наличие факта облучения ионизирующей радиацией.
- Ректороманоскопия и колоноскопия с биопсией позволяют выявить воспаление слизистой оболочки толстого кишечника. При лучевом энтерите воспаление сочетается с атрофией слизистой. Крипты становятся менее глубокими, уменьшается длина ворсинок. При лучевом колите на слизистой обнаруживают язвы, стриктуры. [14]
- Энтерит лучевого генеза следует дифференцировать с болезнями тонкой кишки, при которых страдает функция всасывания (целиакия), при данных заболеваниях происходит атрофия по гиперрегенераторному типу, а при лучевом поражении преобладают гипорегенераторные процессы слизистой.
- Радиационные поражения толстого кишечника дифференцируют с язвенным колитом, болезнью Крона, новообразованиями толстого кишечника. [15]
Лечение колита
- антибактериальные, противогрибковые средства с учетом чувствительности микроорганизмов. Предпочтение отдают таблетированным формам препаратов;
- восполнение потерянной жидкости и минералов: растворами для приема внутрь (Регидрон и др.), внутривенное введение (раствор Рингера, Трисоль и др.);
- прием сорбентов;
- пробиотики и пребиотики;
- ферменты (креон, фестал);
- симптоматическая терапия (противовоспалительные средства, спазмолитики и др.)
- консервативное лечение колита (щадящая диета, препараты, смягчающие стул, лекарства для улучшения кровотока, дезагреганты, витаминные препараты, дезинтоксикационное лечение, восполнение баланса электролитов и жидкости, гемотрансфузии (при показаниях), антибактериальные препараты);
- оперативное лечение колита.
Показаниями для срочного хирургического лечения служат:
- перфорация, толстокишечная непроходимость. В таком случае удаляется участок кишки, с последующей санацией и дренированием брюшной полости.
- плановое оперативное лечение колита кишечника показано больным в случае сужения (стриктуры) толстого кишечника без явлений острой кишечной непроходимости.
Терапия лучевого колита схожа с терапией язвенного колита и болезни Крона:
- лекарства, содержащие 5-аминосалициловую кислоту (месалазин, салофальк);
- антибактериальная терапия.
Может быть полезно вести дневник питания, чтобы отслеживать, что вы едите, а также свои чувства. Если вы обнаружите, что некоторые продукты вызывают обострение ваших симптомов, вы можете попробовать их устранить.
Диетотерапия
Убедительных доказательств того, что неправильное питание приводит к воспалению кишечника, нет. Но оно может усугубить симптомы болезни, особенно при обострении. Поэтому полезно вести дневник питания и отслеживать свои реакции на определённые продукты.
- есть меньше молочных продуктов — у пациента может быть непереносимость лактозы, т. е. организм не переваривает молочный сахар;
- есть небольшими порциями по 5-6 раз в день;
- пить больше жидкости — предпочтительнее вода; алкоголь и напитки, содержащие кофеин, стимулируют кишечник и могут усилить симптомы болезни [15] .
Прогноз. Профилактика
На сегодняшний день хорошо известны причины возникновения инфекционного колита, разработаны современные методики лечения. Поэтому при неосложненном течении и вовремя начатой терапии удается достигнуть полного выздоровления. Менее благоприятный прогноз у лиц с явлениями иммунодефицита и ослабленной иммунной системой (например, у людей пожилого возраста). Прогноз благоприятный.
Основными методами профилактики являются:
- гигиенические мероприятия (тщательное мытье рук);
- использование только свежих продуктов, чистой воды;
- уделение особого внимания термической обработке пищи.
При транзиторной форме ишемического колита прогноз благоприятный. При гангренозной форме — зависит от вовремя поставленного диагноза и проведенного лечения.
Так как ишемический колит является осложнением других болезней, то для его профилактики необходимо:
- своевременное лечение сопутствующих заболеваний;
- сбалансированное питание.
Лучевой колит приводит к постоянным, необратимым изменениям кишечной стенки, поэтому прогноз неблагоприятный.
При радиационном колите могут появляться язвы и стриктуры на слизистой оболочке толстого кишечника, что может привести к кишечной непроходимости. В таком случае необходимо хирургическое лечение, от своевременности которого зависит прогноз. При правильном и вовремя проведенном лечении прогноз благоприятный. Специальных методов профилактики лучевого колита не существует.
Читайте также:
