Дисметаболические полиневропатии. Боли при диабете. Лечение болей при диабете.
Добавил пользователь Дмитрий К. Обновлено: 28.01.2026
Одним из наиболее частых осложнений сахарного диабета (СД) является диабетическая полиневропатия (ДПН), приводящая к снижению качества жизни, инвалидизации и смерти больных [1,2]. При стаже СД более 25 лет ДПН развивается примерно у 50% пациентов [3].
Механизм развития полиневропатии при сахарном диабете
Несмотря на большие достижения в понимании патогенеза поражения периферических нервов при СД в последние годы, до настоящего времени не разработано метода лечения, который стал бы “золотым стандартом” эффективности терапии ДПН.
Лечение ДПН может быть направлено на ликвидацию ее проявлений и замедление прогрессирования поражения нервов (в том случае, если используется патогенетическая терапия) или только на борьбу с проявлениями ДПН, например, болевым синдромом, если применяется симптоматическая терапия.
Современная терапия ДПН
Компенсация сахарного диабета
Гипергликемия запускает каскад метаболических и сосудистых нарушений, вызывающих развитие ДПН. В связи с этим первоочередной задачей должно быть снижение уровня сахара до величин, близких к норме. Многолетние исследования показали, что интенсивная терапия СД с поддержанием уровня сахара, близким к нормогликемии, значительно снижает вероятность развития ДПН [4,5]. Процент возникновения ДПН был выше в группе с традиционным ведением СД по сравнению с группой, получавшей интенсивную терапию. Вместе с тем и при интенсивной терапии СД у части больных развивалась ДПН. Это, скорее всего, свидетельствует о том, что даже незначительные и кратковременные колебания сахара крови могут приводить к развитию ДПН, и подчеркивает необходимость дополнительной терапии ДПН, в том числе, возможно, профилактической.
Антиоксиданты
При гипергликемии множество процессов - аутоокисление глюкозы, усиленное образование конечных продуктов избыточного гликирования белков (AGEs), активация перекисного окисления липидов, NO-синтазы приводит к избыточному образованию свободных радикалов - молекул, как правило, содержащих атом кислорода с непарными электронами и обладающих повышенной реагентной способностью. Свободные радикалы нарушают деятельность клеточных структур, в первую очередь эндотелия, вызывая эндоневральную гипоксию и приводя к развитию ДПН. Активность собственной антиоксидантной системы организма (“ловушки” свободных радикалов - ферменты супероксиддисмутаза, каталаза, глутатиона и другие) при СД снижена, что, возможно, связано с генетическими факторами [6,7]. Это приводит к формированию феномена оксидантного стресса - нарушению баланса анти- и прооксидантных систем в пользу последних [8]. В условиях оксидантного стресса угнетается синтез оксида азота (NO) - основного регулятора расслабления сосудистой стенки, и активируется ядерный фактор (NF-kB), инициирующий выделение субстанций, которые ухудшают кровоток, например, эндотелина-1 [9,10]. В настоящее время роль оксидантного стресса в развитии ДПН считается одной из ведущих. Логичным поэтому является применение препаратов, обладающих антиоксидантным действием.
Первое место среди антиоксидантов и вообще препаратов, использующихся для патогенетического лечения ДПН, сегодня занимает a-липоевая (тиоктовая) кислота (ТК), естественный липофильный антиоксидант. Возможности ТК уменьшать окислительный стресс при СД доказана в ряде исследований [11]. В экспериментах показано, что важным достоинством ТК является ее влияние не только на уменьшение проявлений оксидантного стресса, т.е. на сосудистый компонент, но и на увеличение содержания в нерве нейротрофических факторов, к примеру, фактора роста нерва. На клиническом материале показано, что введение ТК нормализует сниженное при СД содержание NO и увеличивает синтез защитных пептидов группы теплового шока [12].
Первое применение ТК в клинике для лечения ДПН проведено в 1959 г. Результаты исследования ALADIN, опубликованные в 1995 г, показали, что при внутривенном введении ТК имеется дозозависимое уменьшение клинических проявлений ДПН (боль, онемение, жжение, парестезии), эффект плацебо и дозы 100 мг не отличаются друг от друга, а дозы 600 и 1200 мг достоверно уменьшают проявления ДПН. К настоящему времени выполнено еще несколько исследований с применением внутривенного (600 мг) или перорального введения (от 600 до 1800 мг) ТК. При лечении ТК отмечено уменьшение основных клинических проявлений ДПН, улучшение функционального состояния соматических и вегетативных нервов, а также уменьшение перекисного окисления липидов в крови и мембранах эритроцитов [13, 14]. Результаты исследования ORPIL позволили сделать вывод о том, что клиническая эффективность 1800 мг ТК при пероральном приеме аналогична эффекту внутривенного введения 600 мг, что совпадает с данными о том, что уровень содержания ТК в плазме при этих двух формах приема одинаков. Сейчас в США и России выполняются исследования NATAN и Sydney, результаты которых позволят дать окончательную оценку эффективности лечения ТК. Необходимо отметить, что современные исследования эффективности внутривенного введения ТК (рандомизированные двойные слепые плацебо-контролируемые исследования), результаты которых приведены выше, выполнены с применением препарата “Тиоктацид”.
Оптимальным считается назначение в начале лечения внутривенного капельного введения Тиоктацида (600 мг на 200 мл физиологического раствора) в течение 3 недель (15 капельниц) с последующим приемом 600 мг препарата в виде таблеток (один раз в день за 30-40 минут до еды) в течение 1-2 месяцев.
Известно, что ТК имеет еще одно важное свойство - она улучшает утилизацию глюкозы, уменьшая инсулинорезистентность. В связи с этим представляет интерес сахароснижающий препарат, созданный на основе Тиоктацида, который проходит в настоящее время клинические испытания. Можно ожидать, что этот препарат, помимо сахароснижающего эффекта, будет обладать протекторным эффектом в отношении ДПН, что позволит использовать его как для профилактики, так и для лечения ДПН. Некоторые из современных сахароснижающих препаратов, например, троглитазон также обладают корригирующим действием на механизмы развития ДПН, однако их клиническая эффективность в этом отношении пока не доказана.
Из других антиоксидантов привлекает к себе внимание экстракт листьев гингко билоба. В нашем исследовании, проведенном в 2000 г, при лечении 58 больных СД в течение 3 месяцев суточной дозой 120 мг получено достоверное снижение выраженности ДПН и улучшение ЭМГ-показателей. Этот антиоксидант является препаратом выбора при лечении больных СД пожилого возраста (после 70 лет).
Витаминотерапия
При СД наблюдается уменьшение содержания в крови и тканях аскорбиновой кислоты и токоферола, входящих в систему антиоксидантной защиты организма. В эксперименте применение этих витаминов уменьшало проявления ДПН, но убедительных данных об их клинической эффективности на сегодняшний день не получено.
Терапию витаминами группы В, строго говоря, нельзя отнести к патогенетической терапии ДПН, поскольку не показано снижение содержания витаминов этой группы при СД в крови или тканях ни в эксперименте, ни у больных СД. Мы сочли нужным внести их в этот раздел по следующим причинам: во-первых, они способны оказывать действие на механизмы развития ДПН, например, усиливая нейротрофическую защиту нерва и способность нерва к регенерации, а во-вторых, доказана их клиническая эффективность при лечении болей при ДПН, и они широко используются с этой целью в некоторых странах, включая Россию, Германию и Японию.
Клиническая эффективность водорастворимых форм витаминов группы В относительно невысока вследствие низкой биодоступности. Качественным прорывом в применении витаминотерапии для лечения ДПН стало создание жирорастворимых форм витамина В1 - аллитиаминов, из которых наиболее высокой биодоступностью обладает бенфотиамин. По сравнению с водорастворимыми формами витамина B1 бенфотиамин значительно быстрее абсорбируется и дольше сохраняет высокую концентрацию в крови и клетках. Проведено несколько рандомизированных двойных слепых плацебо-контролируемых исследований эффективности бенфотиамина или его комбинаций с витаминами В6 и B12, показавших достоверное уменьшение болей и парестезии, снижение порога вибрационной чувствительности и улучшение ЭМГ-показателей функционального состояния нерва [15]. Важным достоинством бенфотиамина является возможность его применения у детей с СД, так как препарат принимается перорально и значительно менее токсичен по сравнению с водорастворимыми формами. Лечение бенфотиамином в дозе 100 мг или 150 мг проводится в течение 3-6 месяцев с суточной дозой 200-300 мг.
Лечение болевого синдрома
Лечение боли при ДПН часто представляет собой серьезную проблему. Главным условием успешной терапии таких больных является установление строгого контроля СД. Зачастую снижение уровня сахара в крови до показателей нормы приводит к регрессу болевого синдрома. Даже в тех случаях, когда появление болевого синдрома связано с резким снижением уровня гликемии на фоне установления или усиления контроля СД, уменьшать сахароснижающую терапию нет необходимости. В тех случаях, когда развитие болевой невропатии связано с острой потерей веса, установление контроля гликемии приводит не только к уменьшению болей, но и к восстановлению массы тела.
Частое наличие депрессии у пациентов, страдающих хронической болевой диабетической невропатией, дало повод использовать трициклические аитидепрессанты (ТЦА) в качестве монотерапии или в комбинации с транквилизаторами. Клинические исследования доказали эффективность лечения ТЦА болевых форм ДПН. Показано дозозависимое действие ТЦА в отношении жгучих и стреляющих болей как у пациентов с депрессией, так и без нее, хотя эффективность лечения у больных с ассоциированной депрессией оказалась выше [16]. Наибольший обезболивающий эффект наблюдался при применении амитриптилина в дозе 150 мг на ночь. Возможный механизм действия ТЦА заключается в угнетении обратного захвата норадреналина в синапсах центральной антиноцицептивной системы.
Успешное применение антиконвульсантов (карбамазепина) в лечении тригеминальной невралгии послужило основанием для их использования при болевых формах ДПН. Механизм действия этой группы препаратов, а также антиаритмических средств (лидокаина и мексилетина) заключается в стабилизации мембран нейронов за счет блокады натриевых каналов. При лечении антиаритмическими средствами побочные эффекты были выражены значительно меньше, чем у антиконвульсантов. Лидокаин в виде медленных внутривенных инфузий (30 минут) в дозе 5 мг/кг эффективно уменьшает боль при ДПН [17]. Антиноцицептивный эффект пероральной формы мексилетина в дозе 450-600 мг/сут. был доказан в ряде двойных слепых плацебо-контролируемых исследований [18]. По шкале общей оценки боли улучшение оказалось незначительным, но межгрупповой анализ показал достоверное снижение стреляющих, жгучих болей, покалывания и чувства жара.
Местное применение капсаицина (алкалоида жгучего перца) в виде кожных мазей и кремов оказалось эффективным в лечении жгучих поверхностных и колющих болей, не вызывая при этом серьезных побочных эффектов [19]. Однако некоторые пациенты были вынуждены прервать терапию в самом начале из-за того, что не могли переносить усиление жжения, которое обычно возникает в первую неделю лечения, а затем регрессирует.
Антагонисты возбуждающих Н-метил-Д-аспартатных (НМДА) рецепторов эффективно устраняют проявления невропатической боли в экспериментальных моделях, но серьезные нейропсихотропные эффекты такого препарата, как кетамин, ограничивают его применение в клинической практике. Декстрометорфан, также блокатор НМДА рецепторов, имеет более широкий диапазон терапевтических возможностей и меньше побочных эффектов, что делает возможным его клиническое использование. Эффективность таблетированной формы декстрометорфана в средней дозе 380 мг/сут. при болевой форме ДПН доказана в ходе рандомизированного двойного слепого плацебо-контролируемого исследования [20].
Применяются различные физиотерапевтические методы лечения боли при ДПН, такие как чрескожная электронейростимуляция и аккупунктура, но их эффективность не доказана. Применение электростимуляции задних рогов спинного мозга путем имплантации электродов эффективно в 80% случаев, когда болевой синдром не купируется стандартной фармакотерапией [21]. Необходимо проявлять осторожность в выборе физиотерапевтических средств лечения, т.к. нарушения чувствительности и вегетативные расстройства при ДПН предрасполагают к образованию ожогов и язв.
Все вышеперечисленные группы препаратов с различной эффективностью уменьшают болевой синдром, не устраняя при этом первопричину - вызванное гипергликемией поражение нервов. Общим принципом лечения болей при ДПН должно быть назначение базовой патогенетической терапии с подключением дополнительного симптоматического лечения.
Лечение отдельных форм автономных нарушений
Ортостатическая гипотония (ОГ) встречается у 1-3% больных СД. При легких формах ОГ рекомендуется медленное вставание, отказ от физических нагрузок, отмена гипотензивных лекарственных средств, сон на кровати с приподнятым головным краем, диета с высоким содержанием натрия (поваренной соли), бинтование ног эластичными бинтами. При тяжелых случаях ОГ, приводящих к инвалидизации больного, применяется специальный сдавливающий комбинезон (противоперегрузочный костюм летчика) и фармакотерапия. Наиболее эффективным является назначение минералокортикоида 9-a-флудрокортизона в дозе 0,1-1 мг/сут. В качестве дополнительной терапии при неэффективности 9-a-флудрокортизона или в качестве монотерапии при невозможности его назначениями применяют эфедрин, клонидин, йохимбин. Кофеин и ингибиторы простагландинсинтазы (индометацин, напроксен, ибупрофен) относят к дополнительным препаратам, не используемым в качестве монотерапии.
Пищевое потоотделение. Сильное потоотделение во время и сразу после еды локализуется в области головы, лица, шеи и грудной клетки, иммитирует гипогликемию и нарушает комфортность жизни больного. Предложен препарат - гликопирролат, обладающий антимускариновым эффектом, для местной обработки кожи, который значительно уменьшает потливость в этих случаях [22].
Гастропарез. В первую очередь необходимы диетические рекомендации, тщательное пережевывание, употребление жидкой или гомогенизированной пищи. Могут оказать эффект препараты, повышающие моторику кишечника: цизаприд - агонист серотониновых рецепторов; эритромицин - антибиотик группы макролидов, являющийся одновременно холиномиметиком и агонистом рецепторов к мотилину; метоклопрамид - антагонист дофамина, обладающий холинергическим действием за счет активации 5НТ3- и 5НТ4-серотониновых рецепторов; домперидон - периферический антагонист дофаминовых рецепторов, подобный метоклопрамиду по структуре и механизму действия, но с меньшим числом побочных эффектов. Для уменьшения таких симптомов, как тошнота и рвота, сопровождающих гастропарез, используются ТЦА (амитриптилин 10-25 мг дважды в сутки), агонисты опиоидных рецепторов - федотозин, антагонисты серотонина - ондасетрон и гранисетрон. Хирургическое лечение (антрэктомия, ваготомия, гастрэктомия, создание анастомозов и пилоропластика) обычно малоэффективно, за исключением трансплантации поджелудочной железы.
Диабетическая диарея. Медикаментозная терапия включает в себя прежде всего препараты, угнетающие перистальтику кишечника: лоперамид, верапамил, октреотид. К развитию диареи может привести уменьшение абсорбции жидкости слизистой кишечника под влиянием снижения a2-адренергических влияний. Именно на наличии a2-адреномиметических свойств и основывается терапевтический эффект клонидина при диарее у больных СД. Клонидин восстанавливает нормальную реабсорбцию жидкости слизистой кишечника и снижает избыточные парасимпатические влияния на его перистальтику. С этой же целью применяются кодеин и дифеноксилат - опиаты, повышающие реабсорбцию жидкости в кишечнике. Гипокалиемия, часто возникающая при диабетической нефропатии, может приводить к снижению перистальтики кишечника. Заместительная терапия препаратами калия у таких больных позволяет эффективно снизить выраженность желудочно-кишечных расстройств.
Эректильная дисфункция. При эректильной дисфункции около 50% пациентов имеют отклонения в психологическом статусе. Именно поэтому ведущее место в лечении таких пациентов занимает психотерапия. К органическим причинам нарушения эрекции относятся вегетативная невропатия и сосудистая патология. Если имеются легкие нарушения, лекарственная терапия может быть эффективна. Прежде всего следует проанализировать и при необходимости заменить получаемую больным терапию. Известно, что препараты для лечения артериальной гипертонии и антидепрессанты могут вызывать нарушения эрекции. Тразодон, являясь a-адреноблокатором, восстанавливает эрекцию при приеме в дозе от 50 до 150 мг/сут. Назначение гормональных средств (тестостерона) оправдано для пациентов с гипогонадизмом для повышения либидо и улучшения эрекции. Йохимбин, пресинаптический a2-адреноблокатор, уменьшает отток крови от пещеристой ткани и, возможно, имеет центральный эффект в виде повышения либидо. К препаратам разового применения, вызывающим эрекцию “по мере надобности”, относится ингибитор циклической гуанозинмонофосфатфосфодиэстеразы (цГМФ) 5-го типа - силденафил. Из нефармакологических методов используются вакуумные устройства, инъекции вазоактивных препаратов (папаверина) в кавернозные тела, внутриуретральное введение простагландина E1 (PGE-1) и протезирование. Нарушение эякуляции может проявляться слабостью выброса семени или ретроградной эякуляцией (вследствие слабости сфинктера мочевого пузыря). Применение симпатомиметиков позволяет восстановить эякуляцию. Обычно используются эфедрин и имипрамин за 60 минут до полового акта.
Диабетическая цистопатия, характеризующаяся нарушением опорожнения мочевого пузыря требует изменения поведения больных. Необходимо предпринимать попытки осуществить акт мочеиспускания каждые 4 часа, независимо от того, имеется позыв на мочеиспускание или нет. Из фармакологических препаратов для улучшения опорожнения мочевого пузыря используются a-адреноблокаторы, а также холинергический агонист бетаникол. При выраженных нарушениях подключают регулярную асептическую катетеризацию мочевого пузыря каждые 4-6 часов с обучением самого больного этой процедуре.
Несмотря на наличие широкого арсенала средств, с успехом использующихся для терапии ДПН, лечение большинства форм вегетативных нарушений до сих пор остается симптоматическим. Это объясняется практически полной необратимостью поражения вегетативных волокон на фоне применяющейся в настоящее время патогенетической терапии, что подчеркивает особое значение раннего выявления и профилактического патогенетического лечения вегетативных расстройств при СД. При выявлении вегетативных нарушений на ранних стадиях необходимо назначать патогенетическую терапию, сочетая ее при необходимости с дополнительным симптоматическим лечением в зависимости от формы автономных нарушений.
Полинейропатия - симптомы и лечение
Что такое полинейропатия? Причины возникновения, диагностику и методы лечения разберем в статье доктора Богдановой Евгении Павловны, нейрофизиолога со стажем в 10 лет.
Над статьей доктора Богдановой Евгении Павловны работали литературный редактор Вера Васина , научный редактор Наталья Пахтусова и шеф-редактор Маргарита Тихонова

Определение болезни. Причины заболевания
Полинейропатия (Polyneuropathy) — это группа заболеваний периферической нервной системы, при которых повреждаются периферические нервные волокна, входящие в состав различных нервов. Полинейропатия может быть вызвана множеством причин, но проявляется общими симптомами: слабостью в руках и ногах, онемением, покалыванием и жжением в кистях и стопах.

Полиневропатия и полинейропатия — это разные варианты написания одного и того же термина.
Как часто встречается полинейропатия
Полинейропатией страдает около 2,4 % населения, заболевание чаще встречается среди пожилых людей [6] .
Причины полинейропатии
Выделяют первичные и вторичные полинейропатии. Первичные полинейропатии — это наследственные формы, которые могут сочетаться с поражением других органов и отделов нервной системы. К наследственным полинейропатиям относятся транстиретиновая семейная амилоидная полинейропатия, болезнь Фабри, порфирийная полинейропатия, болезнь Рефсума.
Вторичные полинейропатии встречаются гораздо чаще. В зависимости от причинного фактора их можно разделить на несколько видов:
- Инфекционные и инфекционно-аллергические (с известным и неизвестным возбудителем, аллергические). В эту группу входит синдром Гийена — Барре.
- Токсические: медикаментозные, при хронических бытовых и производственных интоксикациях (ртутью, свинцом, литием), при токсикоинфекциях (ботулизм, дифтерия, столбняк), алкогольные. Медикаментозные полинейропатии могут развиться при приёме Амиодарона, Колхицина, Хлоракина, Хлорамфеникола, Дапсона, Дисульфирама, Этамбутола, Этионамида, Глутетимида, статинов, Изониазида, Гидралазина, Фенитоина, Никотинамида, препаратов золота. Чаще всего полинейропатия развивается при длительном применении больших доз этих лекарств. Также к ней может привести приём нуклеозидов — препаратов для лечения ВИЧ-инфекции. Полинейропатия может возникать на фоне химиотерапии — примерно через месяц после начала применения Цисплатина, если доза превышает 400 мг/м 2 ; при терапии Винкристином и Винбластином — нередко в первые два месяца лечения, если суммарная доза препаратов превышает 30-50 мг [8] . В редких случаях полинейропатию вызывает Интерферон-альфа, используемый при гепатите С и опухолях.
- При воздействии физических факторов: холода, вибрации, радиации, хронических компрессиях (из-за утолщения оболочек вокруг нерва при системных болезнях соединительной ткани) и т. д.
- Сосудистые: при системных заболеваниях соединительной ткани, специфических и неспецифических васкулитах, атеросклерозе.
- Метаболические: при болезнях обмена веществ, дефиците витаминов (алиментарные), эндокринных заболеваниях (например, при сахарном диабете), болезнях печени и почек. Полинейропатия может быть первым проявлением сахарного диабета, чаще всего 2-го типа.
- Паранеопластические (при злокачественных новообразованиях).
Около 20-30 % аксональных полинейропатий, т. е. возникших из-за повреждения длинных отростков нервов, являются идиопатическими: их причину не удаётся выявить, несмотря на полную диагностику [7] . Иногда поиск причины полинейропатии может затянуться на месяцы. Это связано с многообразием провоцирующих факторов и трудностями при сборе анамнеза: пациенты не всегда честно рассказывают о вредных привычках и часто не знают, чем болели родственники.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы полинейропатии
Клиническая картина полинейропатий типична и проявляется следующими симптомами:
- Двигательные нарушения. При заболевании развиваются периферические парезы — снижается мышечная сила и тонус, атрофируются мышцы, угнетаются или исчезают рефлексы. Постепенно слабеют и уменьшаются в размерах мышцы рук и ног, чаще в стопах, голенях и кистях. Пациенты быстро устают при ходьбе, подъёме по лестнице и занятиях спортом, не могут встать на носки и пятки, взять и удержать тяжёлые предметы, чувствуют неловкость в руках, отмечают шаткость при ходьбе.
- Чувствительные нарушения. Страдают глубокие (суставно-мышечное чувство, вибрационная чувствительность) и поверхностные виды чувствительности (чаще — болевая чувствительность). Чувствительные нарушения проявляются следующими симптомами:
- Снижается или исчезает чувствительность к боли и температуре, преимущественно в стопах, голенях и кистях. Немеют руки и ноги, пациенты не различают горячую и холодную воду, могут поранить ногу, наступить на что-то острое и не заметить этого, так как не чувствуют боли.
- Нейропатическая боль — пациенты описывают болевые ощущения по-разному: колющие, кинжальные, жгучие, ноющие, как от удара электрическим током. Боль может сочетаться с нарушением болевой и температурной чувствительности, аллодинией (боль возникает из-за прикосновения к коже) и гипералгезией (слабый раздражитель вызывает сильную боль). Нейропатическая боль часто начинается со стоп, но пациент, как правило, не может указать точно, где болит, и лишь примерно показывает область боли. Боль может быть постоянной или периодической, возникать самопроизвольно или в ответ на прикосновение.
- Из-за нарушения глубоких видов чувствительности развивается сенситивная атаксия: пациент неустойчив, вынужден при ходьбе всегда смотреть под ноги, так как не чувствует поверхность под ногами. К глубоким видам чувствительности относится ощущение вибрации и суставно-мышечное чувство — понимание положения своего тела в пространстве. При ходьбе по твёрдой поверхности у больного возникает ощущение мягкого ковра под ногами. Особенно сложно передвигаться в темноте, когда невозможно смотреть под ноги. В таких случаях пациенты часто падают.
- Трофические нарушения. Истончается кожа и изменяется её окраска, утолщаются ногтевые пластины. Эти изменения связаны с тем, что периферические нервы не только обеспечивают движения мышц, но и питают мышцы и кожу.
При поражении периферических отделов вегетативной нервной системы нарушается работа внутренних органов. Эти нарушения сопровождаются следующими симптомами:
- ортостатическая гипотензия — давление снижается при перемене положения тела, например когда человек сидел или лежал, а потом резко встал ; в покое;
- ригидный пульс, т. е. исчезновение его физиологической нерегулярности;
- пониженное потоотделение;
- нарушение тонуса мочевого пузыря и недержание мочи;
- запоры и диарея; [3][6] .
Патогенез полинейропатии
Периферической называют ту часть нервной системы, которая не входит в центральную нервную систему, т. е. нервы за пределами головного и спинного мозга.

Периферическую нервную систему образуют длинные отростки нервных клеток, тела которых залегают в спинном мозге, стволе головного мозга, спинномозговых и вегетативных узлах. Эти длинные отростки называют аксонами. Аксоны получают питание из тела нервных клеток [11] .
Выделяют два типа нервных волокон: тонкие ( безмиелиновые ) и толстые ( миелиновые ). Миелин окружает аксон прерывистой электроизолирующей оболочкой, благодаря чему возбуждение передаётся быстрее. Этому способствуют перехваты Ранвье — периодические участки, не покрытые миелином.

Полинейропатии делят на два основных класса:
- аксонопатии, или аксональные полинейропатии, — повреждён непосредственно сам аксон;
- миелинопатии, или демиелинизирующие полинейропатии, — поражена миелиновая оболочка аксона.
Зачастую при поражении миелиновой оболочки позже повреждается и сам аксон, а при первичном повреждении аксона со временем разрушается и миелиновая оболочка.
Классификация и стадии развития полинейропатии
Формы полинейропатии в зависимости от причины:
- инфекционные и инфекционно-аллергические;
- токсические;
- от воздействия физических факторов;
- метаболические;
- паранеопластические.
По течению полинейропатии могут быть:
- острыми — развиваются от нескольких дней до четырёх недель;
- подострыми — симптомы усиливаются в течение 4-8 недель;
- хроническими — развиваются в течение нескольких месяцев или лет.
По патоморфологическим признакам выделяют аксонопатии и миелинопатии.
По преобладанию симптомов выделяют:
- сенсомоторные полинейропатии (в равной степени присутствуют чувствительные и двигательные нарушения);
- преимущественно моторные;
- преимущественно сенсорные;
- преимущественно вегетативно-трофические (с нарушением работы внутренних органов).
В чистом виде они встречаются редко, чаще развивается сочетанное поражение двух или трёх видов нервных волокон [6] .
Осложнения полинейропатии
К ослож нениям полинейропатии можно отнести атрофию мышц и утрату движений в конечностях, тревожные и депрессивные расстройства из-за боли при сенсорных полинейропатиях.
Также на фоне полинейропатии могут возникать ожоги, повреждения кожи из-за нарушения чувствительности и частые падения, которые приводят к травмам [15] .
Диагностика полинейропатии
Сбор анамнеза
При диагностике полинейропатии важно выяснить, на что жалуется пациент, какой образ жизни он ведёт и какими болезнями страдают его близкие родственники.
На приёме доктор спрашивает:
- о наличии хронических и онкологических болезней, а также уточняет, проводилась ли химиотерапия;
- о вредных привычках и профессиональных факторах, например работе с тяжёлыми металлами и фосфорорганическими соединениями;
- о схожих симптомах у родственников, например слабости и онемении в ногах и руках, — эти нарушения могут указывать на наследственную полинейропатию.
Нужно обязательно рассказать доктору о вредных привычках, в том числе о злоупотреблении алкоголем, а также о том, что предшествовало развитию полинейропатии, например инфекция, боль в животе, голодание и т. д.
Неврологический осмотр
Доктор осматривает кожу, ощупывает мышцы, измеряет окружность рук и ног, оценивает сухожильные, надкостничные рефлексы и чувствительность.
Сухожильные рефлексы проверяют с помощью лёгкого удара неврологическим молоточком по сухожилию мышцы:
- при ударе по ахиллову сухожилию стопа сгибается в области подошвы;
- при ударе по сухожилию четырёхглавой мышцы бедра разгибается голень (проверка коленного рефлекса);
- при ударе по шиловидному отростку лучевой кости рука сгибается в локте и поворачивается кисть (проверка надкостничного рефлекса).
Если рефлексы выпадают, описанные движения не происходят.
Чтобы оценить походку, силу мышц рук и ног, доктор просит пациента встать на носки и пятки, сесть на корточки и встать, лёжа потянуть стопы на себя и от себя, согнуть и разогнуть ноги в коленях, сжать кулаки, согнуть и разогнуть руки в локтях и т. д.
Нарушение разных видов чувствительности определяют различными методами:
- для оценки температурной чувствительности к коже прикасаются пробирками с тёплой и холодной водой;
- болевую чувствительность проверяют с помощью лёгкого покалывания заострённой деревянной палочкой;
- вибрационную чувствительность исследуют с помощью камертона;
- при оценке суставно-мышечного чувства пациент закрывает глаза, доктор шевелит пальцами его рук и ног, пациент описывает свои ощущения.
Определить интенсивность боли можно с помощью специальных шкал, например DN4 и визуальной аналоговой шкалы (ВАШ). Принцип ВАШ состоит в том, что пациенту предлагают оценить силу боли по 10-балльной шкале, где 0 — это отсутствие боли, а 10 — самая сильная боль, какую он испытывал в жизни. С помощью этой шкалы можно оценить эффективность лечения, сравнив интенсивность боли до него и после.
Лабораторная диагностика
Лабораторная диагностика позволяет установить причину полинейропатии.
К основным лабораторным методам относятся:
- Общий анализ крови, определение концентрации витамина В12, анализ крови и мочи на содержание тяжёлых металлов, проба Уотсона — Шварца (специфическое исследование мочи при подозрении на порфирию).
- Биохимический анализ крови (глюкоза, гликированный гемоглобин, показатели работы печени, почек).
- Исследование антител к ганглиозидам — информативный метод при моторной мультифокальной и хронической воспалительной демиелинизирующей полинейропатии, синдроме Гийена — Барре и других аутоиммунных невропатиях. Однако повышенный титр антител к GM1-ганглиозидам выявляют у 5 % здоровых людей, зачастую у пожилых пациентов [6] .
- Антитела к ассоциированному с миелином гликопротеину (анти-MAG антитела) — определяются при парапротеинемической полинейропатии и ряде других аутоиммунных полинейропатий.
- Исследование спинномозговой жидкости — проводится при подозрении на демиелинизирующие полинейропатии. Повышенное содержание белка в ликворе может указывать на синдром Гийена — Барре, хроническую воспалительную демиелинизирующую полинейропатию. Реже небольшое повышение встречается при диабетической полинейропатии. Избыток клеток в ликворе может указывать на полинейропатию при ВИЧ-инфекции и болезни Лайма[8] .
- Молекулярно-генетический анализ — назначают при подозрении на наследственные мотосенсорные полинейропатии [6] . При анализе берут кровь из вены и отправляют в лабораторию.
Инструментальная диагностика
- Стимуляционная электронейромиография (ЭНМГ) — основной метод диагностики полинейропатии, при котором определяется скорость проведения импульса по двигательным и чувствительным нервам. Позволяет подтвердить полинейропатию, определить её тип (аксонопатия или миелинопатия).
- Игольчатая электромиография с оценкой состояния мышц рук и ног — проводится, если результаты стимуляционной ЭНМГ сомнительны: например, пограничные между нормой и патологией, или требуется дифференциальная диагностика между полинейропатией и поражением мышц (миопатией) [1][2][6] .
- Ультразвуковое исследование нервов (УЗИ) — позволяет определить, на каком именно участке повреждены нервы.
- Биопсия нервов — при полинейропатии проводится редко, целесообразна при подозрении на васкулит и амилоидную полинейропатию. Чаще всего для биопсии выбирают икроножный нерв [6] .

Лечение полинейропатии
Чтобы вылечить полинейропатию, нужно выявить и устранить причину болезни, а также подавить механизмы её развития.
Методы лечения полинейропатии зависят от основного заболевания:
- при сахарном диабете — подбирают диету и терапию, которая снижает уровень глюкозы;
- при дефиците витаминов — дают рекомендации по питанию и назначают витамины;
- при аутоиммунных воспалительных полинейропатиях — применяют плазмаферез и внутривенно вводят иммуноглобулин [14] .
Чтобы уменьшить нейропатическую боль, применяют:
- медикаментозное лечение — антидепрессанты и антиконвульсанты (препараты для лечения эпилепсии);
- немедикаментозное лечение — психотерапия, методы с биологической обратной связью.
Нестероидные противовоспалительные препараты (НПВС) при нейропатической боли неэффективны [6] [8] .
В терапии диабетической полинейропатии широко применяют препараты тиоктовой кислоты — антиоксиданта, защищающего клетки от повреждения [13] .
Помимо медикаментозного лечения, проводится физическая реабилитация: лечебная физкультура, массаж, методы с биологической обратной связью, физиотерапия (электромиостимуляция) и т. п.
Эффективного лечения наследственных полинейропатий пока не существует [6] . При болезни Рефсума основной метод лечения — это диетотерапия, также может применяться плазмаферез . Пациенту нужно ограничить поступление фитановой кислоты, есть меньше зелёных овощей, говядины, рыбы (тунца, пикши и трески).
Прогноз. Профилактика
Прогноз зависит от течения основного заболевания и своевременного и правильного лечения. Также влияет тип полинейропатии: при миелинопатиях прогноз благоприятнее, чем при аксонопатиях [8] .
Наследственные полинейропатии, как правило, неуклонно прогрессируют, но благодаря их медленному развитию пациенты адаптируются и обслуживают себя самостоятельно до поздних стадий болезни.
Прогноз токсических полинейропатий относительно благоприятный при прекращении интоксикации, например если пациент откажется от алкоголя.
При диабетической полинейропатии с адекватной терапией прогноз тоже относительно благоприятный. Без лечения заболевание прогрессирует, а невропатическая боль снижает качество жизни: пациенты не могут нормально спать и работать [6] [8] .
Профилактика полинейропатии
Профилактика заключается в своевременной диагностике и лечении соматических заболеваний, нарушений обмена веществ, а также отказе от алкоголя. Пациентам с хроническими заболеваниями необходимо регулярно посещать лечащего врача и выполнять его рекомендации. При подозрении на полинейропатию доктор направит больного на электронейромиографию [5] [7] .
Людям, занятым на вредном производстве, необходимо регулярно посещать профпатолога. Обычно такие консультации входят в ежегодный профилактический медицинский осмотр.
Пациентам, чьи родственники страдают наследственными формами полинейропатии, желательно обратиться к медицинскому генетику, чтобы определить свой риск развития болезни.
Дисметаболические полиневропатии. Боли при диабете. Лечение болей при диабете.
В 2007 году экспертами по боли сформулировано новое определение невропатической боли, согласно которому она вызывается первичным повреждением или болезнью соматосенсорной системы. В основе невропатической боли лежит патологическая активация путей проведения боли, что может быть связано с повреждением нервной системы на уровне периферических нервов, сплетений и задних корешков (периферическая невропатическая боль) или спинного и головного мозга (центральная невропатическая боль). Исследования, проведенные в различных странах, показали, что невропатическая боль наблюдается у 6-8% популяции и связана с хроническими болевыми синдромами, женским полом, пожилым возрастом больных и невысоким уровнем социального положения, которые могут рассматриваться как факторы риска. Невропатическая боль, обусловленная широким спектром повреждений и заболеваний, ассоциируется с большей интенсивностью болевого синдрома и частым обращением за медицинской помощью. При наличии невропатической боли снижается качество жизни больных, их социальная адаптация и трудоспособность, а во многих случаях невропатическая боль плохо поддается лечению. Это свидетельствует о высокой социальной и медико-экономической значимости проблемы диагностики и лечения невропатической боли.
Литература
1. Болевые синдромы в неврологической практике. Под редакцией А.М.Вейна - М. - 2001
2. Bone M, Critchley P, Buggy D.J. Gabapentin in postamputation limb pain: a randomized, double-blind, placebo-controlled, cross-over study // Reg Anesth Pain Med - 2002 - Vol.27 - P. 481-486.
3. Кукушкин М.,Л., Хитров Н.К. Общая патология боли // М. - 2004 - 144 стр.
4. Cohen H.W., Gibson G., Alderman M.H. Excess risk of myocardial infarction in patients treated with antidepressant medication. Association with use of tricyclic agents // Am J Med - 2000 - Vol.108 - P.2-8.
5. Backonja M. Anticonvulsants and antiarrhythmics in the treatment of neuropathic pain syndromes // In Neuropathic Pain: Pathophysiology and Treatment. Ed. Hansson P.T. - Seatle, IASP Press - 2001 - P.185-201.
6. Rose M.A., Kam P.C.A. Gabapentin: pharmacology and ist use in pain management // Anaesthesia - 2002 - Vol.57 - P.451-462.
7. McLean M.J., Morell M.J., Willmore L.J. et al. Safety and tolerability of gabapentin as adjunctive therapy in a large, multicenter study // Epilepsia - 1999 - Vol.40 - P. 965-972.
8. Bakonja M. Gabapentin monotherapy for the symptomatic treatment of painfuk neuropathy: a multicenter, double-blind, placebo-controlled trial in patients with diabetes mellitus // Epilepsia - 1999 - Vol.40 (Suppl.6) - P.57-59.
9. Singh D., Kennedy D. The use of gabapentin for the treatment of postherpetic neuralgia // Clin Ther - 2003 - Vol.25 - P.852-889.
10. Cheshire W. Defining the role for gabapentin in the treatment of trigeminal neuralgia: a retrospective study // J.Pain - 2002 - Vol.3 - P.137-142.
11. Solaro C., Ucelli A., Inglese M. et al. Gabapentin is effective in treating paroxysmal symptoms in multiple sclerosis // Neurology - 1998 - Vol.50 (Suppl.4) - P.A147.
12. Attal N., Cruccu G., Haanpaa M. et al. EFNS guidelines on pharmacological treatment of neuropathic pain // European Journal of Neurology - 2006 - Vol.13 - P.1153-1169.
13. Rosenstock J., Tuchman M., LaMoreaux L. et al. Pregabalin for the treatment of painful diabetic peripheral neuropathy/ A double-blind placebo-controlled trial // Pain - 2004 - Vol.110 - P.628-638.
14. Sabatowski R., Galevz R., Cherry D.A. et al. Pregabalin redused pain and improves sleep and mood disturbances in patients with post-herpetic neuralgia. Results of a randomized, placebo-controlled clinical trial // Pain - 2004 - Vol.109 - P. 26-35.
15. Яхно Н.Н., Кукушкин М.Л., Давыдов О.С. и другие. Результаты Российского эпидемиологического исследования распространенности невропатической боли, ее причин и характеристик в популяции амбулаторных больных, обратившихся к врачу неврологу // Боль - 2008 - №3 - стр.24-32.
16. Данилов А.Б., Давыдов О.С. Нейропатическая боль // Из-во Боргес, Москва - 2007 - стр.32-55.
17. Chan A.W., MacFarlane I.A., Bowsher D.R. et al. Chronic pain in patients with diabetes mellitus : comparison with non-diabetic population // Pain Clinic - 1990 - №3 - P.147-159.
18. Новиков А.В., Солоха О.А. Невропатическая боль: Обозрение по материалам журнала “The Lancet” (май-июнь 1999) // Неврологический Журнал - 2000- №1 - С.56-61.
19. Besson J. The neurobiology of pain // Lancet - 1999 - Vol.353 - P.1610-1615.
20. Sorensen L., Siddall P.J., Trenell M.I. et al. Differences in metabolites in pain-processing brain regions in patients with diabetes and painful neuropathy // Diabetes Care - 2008 - Vol.31 - P.980-981.
21. Stacey B.R., Dworkin R.H., Murphy K. et al. Pregabalin in the treatment of refractory neuropathic pain: results of a 15-month open-label trial // Pain Med - 2008 Mar 11.
22. Jann M.W., Slade J.H. Antidepressant agents for the treatment of chronic pain and depression // Pharmacotherapy - 2007 - Vol.27 -P.1571-1587.
23. Методические рекомендации по диагностике и лечению невропатической боли. Под редакцией академика РАМН Н.Н.Яхно //Москва, издательство РАМН - 2008 - 32 стр.
Диабетическая нейропатия (дистальная симметричная полинейропатия)
Диабетическая нейропатия - повреждение нервов, обусловленное диабетом, клинически очевидное или субклиническое, при отсутствии другой возможной этиологии (WHO) [1]. Наиболее изученной и распространенной формой диабетической нейропатии является дистальная симметричная полинейропатия. ДСПН - наличие симптомов дисфункции дистальных отделов периферических нервов у пациентов с сахарным диабетом после исключения других причин [2].
Код(ы) МКБ-10:
| МКБ-10 | |
| Код | Название |
| G63.2* | Диабетическая полинейропатия (E10-E14+ с общим четвертым знаком.4) |
Дата разработки/пересмотра протокола: 2017 год.
Сокращения, используемые в протоколе:
| GPP | Good Point Practice (Надлежащая клиническая практика) |
| WHO | World Health Organization (Всемирная организация здравоохранения) |
| ВАШ | визуальная аналоговая шкала |
| ДАН | диабетическая автономная нейропатия |
| ДМН | диабетическая мононейропатия |
| ДН | диабетическая полинейропатия |
| ДПН | диабетическая полинейропатия |
| ДСПН | диабетическая сенсомоторная полинейропатия |
| МКБ 10 | международная классификация болезней 10-го пересмотра |
| НС | нервная система |
| РКИ | рандомизированные клинические исследования |
| СД I | сахарный диабет I типа |
| СД 2 | сахарный диабет II типа |
| ЭНМГ | Электронейромиография |
Пользователи протокола: неврологи, эндокринологи, врачи общей практики.
Категория пациентов: взрослые.
Шкала уровня доказательности:
Таблица 1 - Шкала уровней доказательности
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты которых могут быть распространены на соответствующую популяцию. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или Высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+). Результаты которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию. |
| D | Описание серии случаев или неконтролируемое исследование или мнение экспертов. |
| GРP | Надлежащая клиническая практика. |

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 800 RUB / 4500 KZT / 27 BYN - 1 рабочее место в месяц

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место - 800 RUB / 4500 KZT / 27 BYN в месяц
Мне интересно! Свяжитесь со мной
Классификация
Согласно классификации Американской ассоциации диабета от 2016 [2]:
Диффузные нейропатии
Диабетическая сенсомоторная полинейропатия:
· преимущественно мелких волокон;
· преимущественно крупных волокон;
· смешанные (мелких и крупных волокон) - наиболее частые.
Автономная нейропатия
Кардиоваскулярная
· брадикардия;
· тахикардия в покое;
· ортостатическая гипотензия;
· внезапная смерть (злокачественная аритмия).
Гастроинтестинальная:
· диабетический гастропарез (гастропатия);
· диабетическая энтеропатия (диарея);
· толстокишечная гипомоторика (запоры).
Урогенитальная:
· диабетическая цистопатия (нейрогенный мочевой пузырь);
· эректильная дисфункция;
· женская половая дисфункция.
Судомоторная дисфункция:
· дистальный гипогидроз/ангидроз;
· «вкусовая» потливость (связанная с приемом пищи);
· отсутствие предвестников гипогликемии;
· аномальная функция зрачка.
Мононейропатия (атипичные формы):
· изолированные нейропатии черепно-мозговых или периферических нервов;
· множественные мононейропатии.
Радикулопатия/полирадикулопатия (атипичные формы):
· радикулоплексусная нейропатия (пояснично-крестцовая полирадикулопатия, проксимальная моторная амиотрофия);
· грудная радикулопатия.
Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ
Диагностические критерии 9
Жалобы:
· онемение кончиков пальцев ног, стоп;
· парэстезии;
· жжение в пальцах ног, подошвах, икрах;
· боли в пальцах ног, подошвах, икрах;
· слабость в нижних конечностях;
· крампи;
· симметричная дистальная локализация неврологических симптомов.
Анамнез:
· наличие СД1 или СД2;
· появление и постепенное нарастание выраженности вышеперечисленных жалоб, коррелирующих с тяжестью и длительностью СД;
· характерно усиление симптоматики в ночное время;
· перенесенные длительно незаживающие язвенные дефекты в стопах;
· перенесенные порезы и др. травматические повреждения в стопах, не сопровождающиеся болевыми ощущениями
Физикальное обследование:
Общий неврологический осмотр:
· исследование тактильной чувствительности на конечностях с помощью стандартного микрофиламента (10 г) (80);
· исследование болевой чувствительности на конечностях с помощью неврологической иглы, одноразовой зубочистки/зубчатого колеса (Pin-wheel);
· исследование температурной чувствительности на конечностях с помощью термического наконечника (Tip-term), поочередного прикосновения пробирок с водой различной температуры (20°С и 40°С);
· исследование вибрационной чувствительности с помощью градуированного камертона 128 Гц или биотензиометра;
· исследование мышечно-суставного чувства;
· исследование коленных и ахилловых рефлексов;
· исследование силы мышц;
· исследование статики и походки с открытыми и закрытыми глазами;
· исследование координационных проб (пальце-носовой и пяточно-коленной) с открытыми и закрытыми глазами.
Все исследования чувствительности проводятся симметрично с обеих сторон по направлению от дистального отдела проксимально.
Клинически значимы следующие признаки:
· снижение/отсутствие болевой, температурной чувствительности в дистальных отделах нижних конечностей;
· аллодиния (синдром, при котором человек чувствует боль от факторов, которые обычно боли не вызывают, например, механическая/тактильная аллодиния, когдаболь возникает от прикосновений) в дистальных отделах нижних конечностей;
· гиперэстезия(повышенная чувствительность к раздражителям) в дистальных отделах нижних конечностей;
· снижение/отсутствие вибрационной чувствительности и мышечно-суставного чувства в дистальных отделах нижних конечностей;
· снижение/выпадение ахилловых и коленных рефлексов;
· снижение силы мышц в дистальных отделах конечностей;
· нарушение координации при закрытых глазах (сенситивная атаксия).
Лабораторные исследования: смотрите клинический протокол СД1 и СД2 у взрослых.
Инструментальные исследования:
Стимуляционная ЭНМГ нижних конечностей с оценкой скорости проведения по моторным и сенсорным волокнам, не менее 2-х нервов с каждой стороны (снижена у больных сахарным диабетом до 35-40 м/сек при норме 50-65м/сек, наиболее выражена в дистальных отделах нижних конечностей) (УД-B) [3].
Проведение данного исследования является самым объективным для динамического наблюдения, оценки эффективности проводимой терапии [2,11-13].
Дуплексное сканирование сосудов нижних конечностей (при подозрении на диабетическую ангиопатию) покажет толщину артериальной стенки, стеноз просвета артерий нижних конечностей, наличие атеросклеротических бляшек, степень кальцификации, снижение эластичности артериальной стенки [1].
Рентгенография стопы в 2-х проекциях (при подозрении на нейроостеоартропатию Шарко)выявляет деформацию, деструкцию костей, суставов; в более поздних стадиях - фрагментации суставов с ремоделированием кости, возникающим компенсаторно с целью восстановить устойчивость костей и суставов, при этом кости фиксируются в новом положении [1].
Показания для консультации специалистов:
· консультация ангиохирурга - с целью исключения/диагностирования диабетической ангиопатии, синдрома диабетической стопы;
· консультация хирурга-ортопеда - с целью исключения/диагностирования нейроостеоартропатии Шарко;
· консультация хирурга - при язвенном дефекте стопы с/без инфицированием/-я;
· консультация эндокринолога - при нестабильной гликемии, усугубляющей течение ДСПН;
· консультация кардиолога;
Согласно консенсусу, принятому в Сан-Антонио (1988, 1992 гг.), для диагноза ДСПН необходимы как минимум наличие одного симптома и одного изменения, выявленного при электродиагностических исследованиях [21,22].
Проведение скрининга на ДСПН
Таблица 2 - Категории пациентов для проведения скрининга на ДСПН [2]
| Категории пациентов для проведения скрининга | Уровень доказательности |
| все пациенты с впервые выявленным СД2 | В |
| пациенты с СД1 через 5 лет после постановки диагноза | В |
| пациенты на «Д» учёте без ранее диагностированной ДСПН | В |
| пациенты с нарушенной толерантностью к углеводам | В |
Диагностический алгоритм:
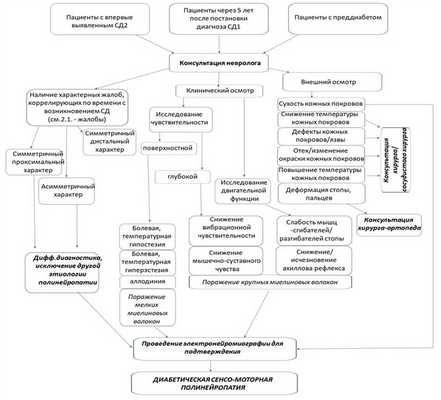
Рисунок 1. Алгоритм диагностики ДСПН [14,15]
Дифференциальный диагноз
Дифференциальный диагноз и обоснование дополнительных исследований
ДСПН является диагнозом-исключением. Наличие сахарного диабета и признаков полинейропатии не означает автоматически наличие диабетической полинейропатии. Для постановки окончательного диагноза требуется тщательная дифференциальная диагностика [2].
Таблица 3 - Дифференциальная диагностика ДСПН [2,14,15]
| Диагноз | Обоснование для дифференциальной диагностики | Обследование | Критерии исключения диагноза |
| Алкогольная ПН | Признаки полинейропатии, не укладывающиеся в рамки ДПНП* | Биохимический анализ крови. УЗИ ОБП. | Анамнестические данные. Наличие алкогольной дистрофии печени, других проявлений со стороны НС: алкогольная энцефалопатия, алкогольная миелопатия, алкогольная полирадикулонейропатия |
| ПН при аутоиммунных заболеваниях | Признаки полинейропатии, не укладывающиеся в рамки ДПНП* | Иммунологические исследования крови. | Аутоиммунные заболевания в анамнезе. Клинико-лабораторные признаки данных заболеваний. |
| ПН при дефиците витамина В12 | Признаки полинейропатии, не укладывающиеся в рамки ДПНП* | Определение уровня В12 в крови. | Низкая концентрация витамина В12 в сыворотке. Возможно сочетание с макроцитарной мегалобластной анемией. |
| ПН при других метаболических нарушениях (гипотиреоз, гипертиреоз, ожирение) | Признаки полинейропатии, не укладывающиеся в рамки ДПНП* | Анализ крови на гормоны щитовидной железы. УЗИ щитовидной железы | Анамнестические данные. Клинико-лабораторно-инструментальные признаки данных заболеваний. |
| Паранеопластические синдромы | Признаки полинейропатии, не укладывающиеся в рамки ДПНП* | В соответствии с КП онкологических заболеваний. | Анамнестические данные. Результаты инструментальных исследований, указывающие на наличие онкопроцесса. |
| Воспалительные демиелинизирующие ПН (поствакцинальные, после перенесенной острой инфекции) | Признаки полинейропатии, не укладывающиеся в рамки ДПНП* | ЭНМГ. Анализ ликвора. Биопсия n.suralis | Анамнестические данные. Специфические данные на ЭНМГ. Обнаружение белка в ликворе. Специфические изменения биопсии n.suralis |
| Наследственные ПН | Признаки полинейропатии, не укладывающиеся в рамки ДПНП* | Исследования в лабораториях молекулярно-генетического профиля. ЭНМГ | Анамнестические данные. Семейный анамнез. Клинико-лабораторные признаки того или иного наследственного заболевания. |
| ПН при экзогенных интоксикациях (свинец, мышьяк, фосфор и др.) | Признаки полинейропатии, не укладывающиеся в рамки ДПНП* | Анализы крови и мочи на наличие токсических веществ. | Анамнестические данные. Клинико-лабораторные признаки той или иной интоксикации. |
| ПН при эндогенных интоксикациях (хроническая печеночная недостаточность, хроническая почечная недостаточность) | Признаки полинейропатии, не укладывающиеся в рамки ДПНП* | Биохимические анализы крови и мочи. УЗИ и\или МРТ ОБП и почек | Анамнестические данные. Клинико-лабораторно-инструментальные признаки хронической печеночной недостаточности или хронической почечной недостаточности. |
| ПН при инфекциях (сифилис, лепра, ВИЧ, бруцеллез, герпес, дифтерия и др.) | Признаки полинейропатии, не укладывающиеся в рамки ДПНП* | Анализ крови (ИФА, ПЦР и др.) на наличие определенных инфекций. | Анамнестические данные. Клинико-лабораторные признаки той или иной инфекции |
*несимметричная/преимущественно моторная/локализованная в верхних конечностях/остро развившаяся полинейропатия
Читайте также:
- УЗИ при солидном образовании поджелудочной железы
- Внутренняя поверхность грудной клетки. Топография плевры
- Железистый рак молочной железы: лечение аденокарциномы, классификация рака груди
- Лечение множественного рака толстой кишки. Прогноз при раке толстой кишки
- Базальноклеточный рак. Особенности базальноклеточного рака.
