Доступ и ход операции ревизии общего желчного протока
Добавил пользователь Евгений Кузнецов Обновлено: 01.02.2026
В настоящее время существует несколько технологий выполнения холецистэктомии.
Лапароскопическая технология выполнения холецистэктомии
Является «золотым стандартом» в лечении хронического холецистита и опцией выбора при лечении острого холецистита. Ее выполняют с помощью специального инструментария через 3-4 прокола в брюшной стенке диаметром 5-10 мм. В эти проколы вводят специальные трубки (троакары), в брюшную полость с помощью инсуффлятора (насоса) вводят углекислый газ — накладывают пневмоперитонеум. Введенный газ создает пространство для работы инструментов.
Через троакары с помощью видеокамеры и специальных зажимов и электродов выделяют анатомические элементы желчного пузыря — пузырную артерию и пузырный проток, накладывают на них специальные металлические скобки (клипсы) и пересекают. Современные видеосистемы предоставляют отличное качество изображения и визуализации структур, намного превосходящие таковые при открытых операциях. Желчный пузырь отделяют от печени и удаляют через один из проколов брюшной стенки.
Преимущества лапароскопической холецистэктомии
- минимальная травма брюшной стенки;
- практически отсутствующий болевой синдром;
- быстрый период восстановления после операции;
- краткое пребывание в стационаре (1-2 дня);
- быстрое восстановление сил и возвращение к повседневной деятельности и работе.
Миниинвазивная открытая технология выполнения холецистэктомии
К сожалению, в 1-5% случаев выполнить холецистэктомию из лапароскопического доступа невозможно. Чаще всего это обусловлено анатомическими аномалиями желчных путей, выраженным воспалительным или спаечным процессом, развитием интраоперационных осложнений. В таких случаях выполняют переход на открытую операцию (конверсия), чаще всего на малоинвазивную, или, реже на традиционную открытую операцию.
Миниинвазивную открытую холецистэктомию используют с 70-х годов прошлого века с целью минимизации травмы брюшной стенки. Желчный пузырь удаляют из разреза в правом подреберье длиной 3-7 см.
Преимуществами ее являются: значительно меньшая травма передней брюшной стенки, чем при открытой холецистэктомии; возможность выполнения вмешательства у пациентов, перенесших ранее операции на брюшной полости; прямой визуальный контроль и применение традиционных приемов хирургической диссекции тканей, что позволяют относительно безопасно манипулировать в условиях выраженного инфильтрата.
Малоинвазивная открытая холецистэктомия показана в тех случаях, когда в связи с сопутствующими заболеваниями наложение пневмоперитонеума и, следовательно, лапароскопическая операция, противопоказаны.
В настоящий момент наиболее распространенными технологиями малоинвазивной открытой холецистэктомии является операция с использованием набора инструментов «Лига-7» (Россия) и операция из подреберного мннидоступа.
При любом варианте холецистэктомии из минидоступа сроки пребывания больных в стационаре как правило длиннее, чем при лапароскопии, и составляют 3-5 дней. Срок послеоперационной реабилитации тоже более длительный.
Традиционная открытая технология выполнения холецистэктомии
Традиционную открытую холецистэктомию выполняют из верхней срединной лапаротомии или косых подреберных разрезов типа доступов Кохера и Федорова, которые обеспечивают широкий доступ к желчному пузырю, внепеченочным желчным протокам, печени, поджелудочной железе, двенадцатиперстной кишке. При таких доступах выполнимы все методы интраоперационной ревизии внепеченочных желчных протоков, включая измерение их ширины, зондирование протоков, интраоперационную холангиографию, интраоперационное ультразвуковое исследование, холедохотомию с интраоперационной холедохоскопией и пр.
В настоящее время холецистэктомию из широкого лапаротомного доступа чаще всего выполняют у больных с острым холециститом, который осложнен распространенным перитонитом, либо при сложных формах патологии желчных протоков.
Недостатками ее являются: значительная травма структур передней брюшной стенки, значительное число ранних и поздних раневых осложнений (в частности, послеоперационных вентральных грыж); операционная травма средней тяжести, ведущая к развитию послеоперационного пареза кишечника, нарушениям функции внешнего дыхания, ограничению физической активности больного; существенный косметический дефект; длительный период посленаркозной и послеоперационной реабилитации и нетрудоспособности.
Трансвагинальная (или трансгастральная) NOTES холецистэктомия
Наиболее новой и малоизученной является трансвагинальная/трансгастральная холецистэктомия по технологии NOTES (Natural Orifice Transluminal Endoscopic Surgery, или эндоскопическая хирургия через естественные отверстия). Преимуществами ее является то, что на брюшной стенке не остается рубцов, все доступы осуществляются с помощью гибких эндоскопов через естественные отверстия (влагалище или рот). Первая в мире такая операция выполнена в апреле 2007 года в Европейском институте телехирургии в Страсбурге под руководством профессора J. Marescaux. В данный момент такая технология лишь происходит клиническую апробацию эффективности и безопасности, и поэтому не рекомендована для широкого клинического применения.
Какой метод оперативного вмешательства выбрать?
Принципиально во всех технологиях отличным является только доступ. При любом способе холецистэктомии хирургическим путем выделяют, пересекают и перевязывают или клиппируют пузырный проток и пузырную артерию, отделяют желчный пузырь от печени, обрабатывают ложе желчного пузыря, извлекают желчный пузырь из брюшной полости, при необходимости дренируют брюшную полость.
Однозначного ответа на него не существует, необходим выбор оптимальной технологии для каждого индивидуального пациента в зависимости от особенностей его заболевания, сопутствующей патологии, общего состояния здоровья.
Наиболее общими рекомендациями являются: при хроническом холецистите и полипах желчного пузыря методом выбора является лапароскопическая холецистэктомия, при остром процессе — лапароскопическая или малоинвазивная открытая, при развитии перитонита (гнойного воспаления брюшины) — открытая. У больных, которым лапароскопия противопоказана из-за сопутствующей патологии или перенесенных операций на брюшной полости — методом выбора является холецистэктомия из минидоступа. При патологии желчевыводящих путей возможно использование разных технологий холецистэктомии в комбинации с эндоскопической санацией желчных протоков.
Выбор технологии оперативного вмешательства осуществляется совместно хирургом, анестезиологом и пациентом.
Доступ и ход операции ревизии общего желчного протока
Холедохолитотомия — это операция по удалению камней из общего жёлчного протока через разрез. Основным показанием к операции является заболевание холедохолитиаз.
Операция проводится при неэффективности или невозможности проведения эндоскопического лечения при холедохолитиазе.
Необходимым условием при выполнении данной операции является проведение интраоперационной холангиографии через пузырный проток под рентгенологическим контролем для исключения «немых» камней в холедохе.
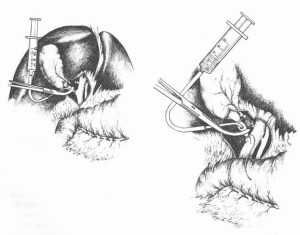
Интраоперационная холангиография
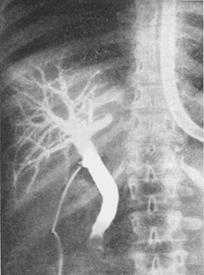
Конкремент в дистальный отделе холедохе
Методика операции
Методика холедохолитотомии включает доступ к общему желчному протоку в печёночно-двенадцатиперстной связке, при этом необходимо четко визуализировать место слияния общего печеночного протока и пузырного протока, провести ревизию всех отделов холедоха. На фоне холедохолитиаза общий желчный проток обычно расширен, что облегчает проведение манипуляций на нем. При этом следует помнить, что проток тонкостенный, за ним может располагаться воротная вена. Опасным является непреднамеренное ранение задней стенки холедоха или вены при проведении холедохотомии.
Для выполнения разреза стенку холедоха берут на две держалки с последующим вскрытием стенки между ними в продольном направлении, что позволяет контролировать длину разреза. Нити необходимо накладывать и подтягивать, чтобы приподнять переднюю стенку протока и избежать ранения задней. Разрез общего жёлчного протока необходимо проводить непосредственно у двенадцатиперстной кишки (ДПК) как можно дистальный, чтобы сократить длину слепого ретродуоденального «мешка» в случае формирования холедохоеюноанастомоза.
После вскрытия просвета проводят удаление конкрементов с обязательным зондированием протока мягкими пластиковыми бужами. Зондирование протока следует проводить только эластичными Буэми, которые могут искривляться и принимать форму протока. Применение жестких металлических бужей или форсированное зондирование протока может привести к ранению его или ДПК, формированию ложного хода с последующим развитием гнойно-воспалительного процесса. Зонд должен свободно проходить в ДПК, не встречая препятствий.
Дренирование
Наиболее частым вариантом окончания операции на общем желчном протоке является его дренирование. Как правило, применяем Т-образный дренаж Кера, который достаточно прочно фиксируется в протоке, а его удаление в дальнейшем не сопровождается осложнениями.
Дренаж типа Кера
Наиболее часто срезаем верхнюю часть дренажа в виде узкой полоски на всем протяжении горизонтальной ветви, что способствует более легкому его удалению в дальнейшем. Дистальный Бранка, идущая в направлении ДПК не должна быть длинен 2-3 см, а проксимальная - не должна перекрывать бифуркацию общего печеночного протока. После окончания введения дренажной трубки в неё вводят физиологический раствор и проверяют, достаточно ли герметично стоит дренаж, нет ли подтекание между стенкой дренажа и протока.
Глухой шов на общий желчный проток можно наложить при ПОЛНОЙ уверенности в его хорошей проходимости и при минимально травматический манипуляциях на нем (например, после лёгкого удаления одиночного невклиненного камня). Как и большинство хирургов, мы редко прибегаем к такому завершению операции, поскольку намного безопаснее произвести временное дренирование, если проток был вскрыт и проводилась его инструментальная ревизия. Кроме того, возможно выполнение глухого шва при выполнении дренирования через пузырный проток (дренаж Холстеда-Пиковского).
Дренирование по Холстеду-Пиковскому
Если нет уверенности, что удалены все камни из общего жёлчного протока, обнаружены множественные камни во внутрипеченочных протоках, операцию следует закончить формированием билиодигестивного анастомоза (на выключенной по Ру петле тонкой кишки длиной не менее 80 см).
Холедохолитотомия в отделении торако — абдоминальной хирургии и онкологии РНЦХ
Операция по удалению камней из желчного протока — не редкий случай в нашей врачебной практике. В отделении есть все необходимое для получения высопрофессиональной медицинской помощи — опытные врачи, новейшее современное оборудование. Комфортные условия пребывания и отзывчивый персонал помогут быстро восстановиться после операции.
Лечение в нашем отделении проводится в рамках программ ОМС, ДМС, ВМП, а также на коммерческой основе. Ознакомьтесь, как попасть на лечение в отделение торако-абдоминальной хирургии и онкологии РНЦХ им. акад. Петровскаого.
Для записи на консультацию позвоните по телефонам:
Отправьте заявку на консультацию, заполнив форму на нашем сайте и прикрепив необходимые документы.
Центральная городская клиническая больница, г. Великий Новгород
Центральная городская клиническая больница, Великий Новгород, Россия
Лапароэндоскопические вмешательства на общем желчном протоке у больных холецистохоледохолитиазом и холангитом
Журнал: Эндоскопическая хирургия. 2019;25(2): 12‑16
Цель исследования — оценить возможности применения лапароэндоскопических вмешательств на общем желчном протоке у больных холецистохоледохолитиазом и холангитом. Материал и методы. У 51 больного (43 женщины и 8 мужчин) в возрасте от 30 до 92 лет использован лапароскопический метод хирургического вмешательства на общем желчном протоке с фиброхоледохоскопическим контролем. Результаты. Лапароэндоскопические вмешательства на общем желчном протоке удалось успешно выполнить у 39 (76,5%) больных. У 6 (11,8%) больных произведен переход на открытое вмешательство на гепатикохоледохе. У 6 (11,8%) больных после проведения интраоперационной холангиографии выявлены противопоказания к лапароэндоскопическим манипуляциям на внепеченочных желчных путях. Этим пациентам было выполнено лапароскопическое дренирование общего желчного протока по Холстеду—Пиковскому с последующей успешной эндоскопической папиллосфинктеротомией. Послеоперационные осложнения выявлены у 7 (13,7%) больных, летальный исход произошел у 1 (2,0%) пациентки. Заключение. Полученный опыт лапароэндоскопических вмешательств на общем желчном протоке у больных с холедохолитиазом и холангитом показывает их хорошую выполнимость; метод нуждается в дальнейшей четкой отработке показаний и противопоказаний, совершенствовании и может использоваться при литэкстракции.
Желчнокаменная болезнь — одно из распространенных заболеваний и встречается у 8—13% населения развитых стран. У 15—33% больных, наряду с камнями желчного пузыря, заболевание осложняется холедехолитиазом [1]. При хирургическом лечении калькулезного холецистита в настоящее время в подавляющем большинстве случаев используется лапароскопическая холецистэктомия [2]. В лечении холецистохоледохолитиаза, как правило, используется двухэтапный подход: вначале проводится санация внепеченочных желчных протоков с использованием эндоскопической ретроградной холангиопанкреатографии (ЭРХПГ) и эндоскопической папиллосфинктеротомии (ЭПСТ), затем выполняется лапароскопическая холецистэктомия [3].
В последние годы получают распространение одномоментные лапароскопические вмешательства по удалению желчного пузыря и литэкстракции из желчных протоков под контролем интраоперационной холангиографии и холедохоскопии [4—7]. Однако количество наблюдений невелико, нередко возникают технические трудности, обусловливающие переход на открытый доступ, недостаточно изучены непосредственные и отдаленные результаты одномоментных вмешательств, что требует дальнейшего изучения этой проблемы.
Цель исследования — оценить возможности применения лапароэндоскопических вмешательств на общем желчном протоке у больных холецистохоледохолитиазом и холангитом.
Материал и методы
За период с 2007 по 2017 г. оперированы 2270 больных острым холециститом в возрасте от 18 лет до 100 лет, среди них лапароскопическая холецистэктомия выполнена у 1965 (86,6%). Сочетание острого холецистита с подозрением на конкременты или наличием камней во внепеченочных желчных протоках выявлено у 305 (13,4%) больных.
В течение последних трех лет при подозрении на холедохолитиаз или явных признаках холедохолитиаза и холангита у 51 больного мы использовали лапароскопический метод хирургического вмешательства на общем желчном протоке. К лапароскопическим вмешательствам при наличии камней во внепеченочных желчных путях прибегали в тех случаях, когда попытка ЭРХПГ и ЭПСТ была неэффективна либо когда не было технической возможности их выполнения.
В описываемой группе женщин было 43, мужчин — 8, возраст больных варьировал от 30 до 92 лет, составляя в среднем 58,2±3,4 года. У 49 больных имелись камни в желчном пузыре, у 2 — ранее желчный пузырь был удален. Основными проявлениями холедохолитиаза были желтуха и холангит, которые отмечены у 43 (84,3%) больных.
Всем поступившим пациентам было проведено комплексное обследование, включая клинико-лабораторную, эндоскопическую и ультразвуковую (УЗИ) диагностику. При УЗИ расширение гепатикохоледоха до 1,2—2,0 см с наличием в нем конкрементов отмечено у 36 больных, у остальных — расширение общего желчного протока не превышало 8—12 мм, при этом только у 6 больных имелись ультрасонографические признаки холедохолитиаза.
Данные дооперационного УЗИ позволили уточнить диаметр пузырного, печеночного и общего желчного протоков, размеры, количество и локализацию конкрементов, а также особенности вариантов строения внепеченочных желчевыводящих путей, что учитывалось при выполнении операции.
Лапароскопическое вмешательство выполняли после получения информированного согласия пациента, под эндотрахеальным наркозом с использованием мышечных релаксантов. В работе использовали видеолапароскопическую стойку фирмы «Karl Storz» (Германия), 5 мм фиброхоледохоскоп фирмы «Pentax» (Япония), эндохирургический инструментарий фирмы «ППП» (Казань, Россия). С профилактической целью, во время хирургического вмешательства, вводили внутривенно антибиотики из группы цефалоспоринов в дозе не менее 1 г. Хирургическая бригада состояла из трех человек. Оперирующий хирург располагался слева от пациента, ассистент — справа, операционная сестра — слева от хирурга.
При выполнении эндовидеохирургического вмешательства на внепеченочных желчных протоках использовали 5 троакаров: первый, 10 мм, вводили на 1 см ниже пупка для лапароскопа, второй, 10 мм, — на 2—3 см ниже мечевидного отростка и несколько правее срединной линии, третий, 5 мм, — на 4—5 см ниже правой реберной дуги по среднеключичной линии, четвертый, 5 мм, — на уровне пупка по переднеподмышечной линии и пятый, 10 мм, — по левой среднеключичной линии на середине расстояния между пупком и мечевидным отростком. Через эпигастральный троакар вводили фиброхоледохоскоп для интраоперационной холангиоскопии и литэкстрации, а пятый троакар использовали для введения иглодержателя.
Операцию начинали с выделения пузырного протока и гепатикохоледоха. Проводили мобилизацию пузырного протока до места впадения в общий печеночный проток и далее обнажали переднюю стенку супрадуоденальной части общего желчного протока. На пузырный проток, тотчас ниже шейки желчного пузыря, накладывали клипсу, ниже ее надсекали пузырный проток и вводили через него катетер, через который проводили холангиографию водорастворимым контрастом.
Показаниями к лапароэндоскопическим вмешательствам на гепатикохоледохе были расширение общего желчного протока более 8 мм и наличие в нем конкрементов. Использовали доступы через пузырный проток и переднюю стенку общего желчного протока. У 3 больных, при широком пузырном протоке и наличии конкрементов менее 5 мм, через второй троакар и надрез стенки пузырного протока в общий желчный проток вводили фиброхоледохоскоп. Для удаления конкрементов использовали корзинку Дормиа, которую проводили через рабочий канал холедохоскопа под контролем видеомонитора. Корзинку проводили в обход конкремента в дистальном направлении, раскрывали ее и, проводя тракцию кверху, захва-тывали конкремент и медленно вместе с холедохоскопом извлекали из просвета желчных путей. После литэкстракции проводили контрольную холангиографию, пересекали пузырный проток и осуществляли через его культю дренирование общего желчного протока по Холстеду—Пиковскому.
У остальных больных ревизия общего желчного протока проводилась через холедохотомический доступ. Показаниями для вскрытия просвета общего желчного протока были узкий пузырный проток и невозможность введения через его просвет холедохоскопа, а также наличие конкрементов диаметром более 5 мм.
Лапароскопическую холедохотомию проводили, рассекая переднюю стенку общего желчного протока лезвием остроконечного скальпеля, взятого в зажим, на протяжении 1,0—1,5 см. При необходимости разрез удлиняли, используя эндоножницы. В ряде случаев отмечалось небольшое кровотечение из сосудов стенки гепатикохоледоха, которое останавливали прижатием микротупфером и точечной коагуляцией. Лит-экстракцию проводили корзинкой Дормиа под контролем видеофиброхоледохоскопа. После извлечения конкрементов проводили осмотр дистальной части общего желчного протока, затем холедохоскоп вводили в проксимальном направлении и осматривали общий печеночный проток, долевые и сегментарные печеночные протоки. По завершении холедохоскопической ревизии в просвет гепатикохоледоха вводили Т-образный дренаж и ушивали холедохотомическое отверстие непрерывным швом монофиламентной нитью на атравматической игле.
После проведения лапароэндоскопических вмешательств на внепеченочных желчных путях и дренирования гепатикохоледоха удаляли желчный пузырь. Такая последовательность в проведении этапов операции была обусловлена тем, что при использовании тракции за желчный пузырь в краниальном направлении создается хорошая экспозиция подпеченочного пространства и гепатодуоденальной связки, обеспечивающая комфортные условия для манипуляций на общем желчном протоке.
После мобилизации желчного пузыря и его удаления через 3-й троакар выводили холедохостомический дренаж и через него выполняли контрольную фистулохолангиографию. Через четвертый троакар дренировали подпеченочное пространство.
Результаты и обсуждение
Лапароэндоскопические вмешательства на общем желчном протоке удалось успешно выполнить у 39 (76,5%) больных. Следует отметить, что техника удаления камней из желчных протоков имела индивидуальные особенности и выполнялась различными способами. При наличии механической желтухи, гнойного холангита после вскрытия просвета гепатикохоледоха, обычно под напором отходили гнойная мутная желчь, сладжи и нередко крупные конкременты, которые иногда пальпировались через стенку общего желчного протока. В ряде случаев приходилось дополнительно увеличивать размеры холедохотомического отверстия, используя эндоножницы и «выдаивать» конкремент, поочередно сжимая гепатикохоледох диссектором и зажимом выше и ниже места положения камня.
Извлечению подвижных конкрементов также помогало промывание общего желчного протока через введенный в его просвет полихлорвиниловый катетер. Катетер вводили в дистальном направлении, общий печеночный проток пережимали зажимом выше холедохотомического отверстиия и под напором вводили физиологический раствор. Вместе с промывными водами отходили конкременты, сладжи, фибринные пленки.
Для извлечения конкрементов, которые не отходили самостоятельно, использовали корзинку Дормиа и фиброхоледохоскоп, подключенный к видеокамере и монитору. Мелкие камни вымывали под давлением струи физиологического раствора через катетер, введенный в просвет гепатикохоледоха. Во время фиброхоледохоскопии вначале осматривали дистальный отдел общего желчного протока, оценивали состояние слизистой оболочки, состояние большого дуоденального сосочка и его проходимость. При визуализиации камней через рабочий канал холедохоскопа вводили корзинку Дормиа, с помощью которой захватывали и извлекали оставшиеся конкременты. При необходимости процедуру повторяли. После удаления конкрементов из дистальной части общего желчного протока фиброхоледохоскоп вводили в проксимальном направлении и осуществляли тщательную ревизию общего печеночного, долевых и сегментарных желчных протоков и при обнаружении в них конкрементов извлекали их корзинкой Дормиа. После литэкстракции извлеченные конкременты погружали в контейнер и удаляли из брюшной полости.
После лапароэндоскопической холедехолитотомии у 36 больных операция была завершена дренированием общего желчного протока по Керу и у 3 больных — по Холстеду—Пиковскому, через культю пузырного протока.
У 6 (11,8%) больных вследствие технических трудностей, обусловленных вклинением камней в терминальном отделе общего желчного протока и невозможностью лапароэндоскопической литэкстракции, произведен переход на открытое вмешательство на гепатикохоледохе.
У 6 (11,8%) больных после проведения интраоперационной холангиографии выявлены мелкие камни в гепатикохоледохе (1—3 мм), при этом диаметр общего желчного протока был менее 8 мм, что послужило противопоказанием к лапароэндоскопическим манипуляциям на внепеченочных желчных путях. У этих пациентов выполнено лапароскопическое дренирование общего желчного протока по Холстеду—Пиковскому, а в последующем — эндоскопическая ретроградная папиллосфинктеротомия с хорошим результатом.
У 49 больных с камнями желчного пузыря лапароскопические вмешательства на гепатикохоледохе завершены холецистэктомией. Продолжительность лапароскопических операций варьировала от 90 до 205 мин, составив в среднем 130,0±25,0 мин.
Послеоперационные осложнения выявлены у 7 (13,7%) больных. Наиболее частым осложнением было желчеистечение вследствие недостаточной герметичности швов холедехотомического отверстия, которое наблюдалось у 6 пациентов. В 3 случаях оно прекратилось самостоятельно через 5—6 дней, у 3 больных осуществлена релапароскопия, дополнительное наложение швов на холедохотомическое отверстие.
Летальный исход отмечен в одном случае (2%). У больной 92 лет в связи с наличием неудалимого вклиненного в большом дуоденальном сосочке конкремента был осуществлен переход на открытый доступ и наложен холедоходуоденоанастомоз. Смерть наступила от острой сердечно-сосудистой недостаточности.
Максимальный послеоперационный период пребывания в стационаре составил 24 дня, минимальный — 8 дней, в среднем — 11,6±1,9 дня. Средняя продолжительность стационарного лечения составила 12,6±0,7 дня.
Заключение
Таким образом, полученный опыт лапароэндоскопических вмешательств на общем желчном протоке у больных с холедохолитиазом и холангитом показывает их хорошую выполнимость; метод нуждается в дальнейшей четкой отработке показаний и противопоказаний, совершенствовании и может использоваться при литэкстракции.
Авторы заявляют об отсутствии конфликта интересов.
The authors declare no conflicts of interest.
Сведения об авторах
1 Доложено на I съезде хирургов Центрального административного округа, Рязань, 27—29 сентября 2017 г.
В связи с развитием эндоскопии в 80-х годах прошлого века эндоскопическая ретроградная холангиопанкреатикография (ЭРХПГ) и эндоскопическая папиллосфинктеротомия (ЭПСТ) выступили на первый план и серьезно потеснили трансдуоденальную папиллосфинктеропластику и ХДА. ЭПСТ стала широко применяться в качестве первичного лечения постхолецистэктомического холедохолитиаза и стриктур [3].
С широким распространением лапароскопии начался период миниинвазивного двухмоментного лечения холецистолитиаза, сочетанного с холедохолитиазом и дистальными стриктурами ОЖП. Эта двухмоментная стратегия, заключающаяся в коррекции патологических изменений ОЖП эндоскопическим методом, а желчного пузыря - лапароскопическим методом, в настоящее время применяется в большинстве клиник как стандартный метод лечения [1, 9, 10].
Вместе с тем двухэтапная стратегия имеет и много недостатков. Во-первых, у 5-15% больных ЭПСТ бывает невыполнимой или неудачной вследствие выраженных стриктур, вклиненных камней, отека, операций на желудке, пилоростеноза, беспокойства больного. В таких ситуациях возникает необходимость хирургического вмешательства. Во-вторых, хотя ЭПСТ и является миниинвазивной процедурой, в 10% наблюдений после ее выполнения отмечаются осложнения, в частности острый панкреатит, перфорация двенадцатиперстной кишки и рестенозы. В-третьих, двухэтапный метод увеличивает длительность лечения: например, после выполнения предоперационной ЭПСТ необходимо выждать как минимум 1-2 дня до выполнения лапароскопии.
В связи с этим в последние годы возрос интерес к миниинвазивным и одномоментным вмешательствам. В частности, одновременно с выполнением лапароскопической холецистэктомии производятся холедохотомия [20], дренирование ОЖП через пузырный проток [7, 19, 24, 25] или Т-образной трубкой [19], интраоперационная ЭПСТ [11], стентирование [13] и ХДА [6-8, 12, 14, 16-18, 21-23]. Хотя из этих методов более привлекательными кажутся одномоментные лапароскопическая холецистэктомия и эндоскопическая сфинктеротомия (техника «рандеву»), в ситуациях, когда выполнение ЭПСТ невозможно, возникает потребность в помощи «старого друга» - ХДА. Однако, по данным литературы, большого опыта выполнения ХДА лапароскопическим методом нет. Поиск по базе данных Medline указывает на 11 исследований по всему миру, всего 117 операций лапароскопического формирования ХДА [6, 8, 12, 14, 16-18, 21-23]. В этой статье мы представляем наш опыт выполнения лапароскопического ХДА и его результаты.
Материал и методы
Показаниями к формированию ХДА были дистальная стриктура ОЖП и его расширение. Последняя у 9 больных была диагностирована до операции с помощью магнитно-резонансной холангиографии (МРХГ), у 15 - при интраоперационнной холангиографии.
У 21 больного дистальная стриктура ОЖП сочеталась с камнями в нем и в желчном пузыре: у 2 - в протоке, у 12 - в желчном пузыре, у 7 - в протоке и желчном пузыре. У 2 больных была обнаружена бескаменная постхолецистэктомическая стриктура. В 1 наблюдении ХДА был наложен в связи с периампулярной опухолью, результаты лечения не включены в данное исследование. У 4 больных предоперационная ЭРХПГ оказалась безуспешной, у 2 больных был констатирован рецидив стриктуры после ЭПСТ. Постхолецистэктомическая стриктура была обнаружена у 3 больных (у 1 с камнем ОЖП, у 2 без камней).
Предоперационное обследование больных осуществляли по стандартному протоколу: общеклинические исследования, УЗИ, определение функционального состояния печени и показателей холестаза, МРХГ. Лапароскопическое формирование ХДА производили с помощью 5 троакаров: 4 троакара размещали в стандартных для холецистэктомии точках, 5-й троакар - по правой параректальной линии на уровне пупка, его использовали для тракции двенадцатиперстной кишки и постоянной аспирации. После ревизии брюшной полости и ворот печени проводили диссекцию в области треугольника Кало с клипированием пузырной артерии и выделением пузырного протока. Чреспузырным катетером производили холангиографию для уточнения патологических изменений ОЖП. Ширина протока более 1 см, отсутствие пассажа контрастного вещества в кишечник, отсутствие перистальтики ампулы на фоне ее сужения при наблюдении в динамике расценивали как показания к наложению ХДА. После продольного вскрытия супрадуоденальной части ОЖП на протяжении 2 см камни вымывали либо удаляли, используя корзинку. В последнее время для ревизии ОЖП рутинно применяли холедохоскопию. ХДА длиной 2 см накладывали бок в бок отдельными швами нитью викрил 4/0 или PDS. Операцию завершали холецистэктомией и дренированием области вокруг анастомоза.
Спустя 1, 3, 6 и 12 мес больных обследовали: УЗИ, функциональные печеночные пробы, эндоскопия через 6-12 мес для ревизии состояния анастомоза. Отдаленные результаты лечения оценивали как отличные (нормальные данные клинического, лабораторного, ультразвукового и эндоскопического исследований), хорошие (нет признаков, связанных с перенесенной операцией, есть небольшие жалобы со стороны желудочно-кишечного тракта), плохие (есть жалобы, при обследовании выявляется рефлюкс), очень плохие (жалобы сохраняются, повторно выявляются камни или стриктура, необходимо повторное вмешательство).
Результаты и обсуждение

Лапароскопические холецистэктомия и холедоходуоденостомия выполнены 21 больному, только наложение ХДА - 3 (табл. 2). Продолжительность операции составила в среднем 128±36 мин (от 90 до 205 мин). Конверсий доступа не было. Продолжительность госпитализации составила 4,5 дня (от 3 до 9 дней, не включены наблюдения, в которых имели место серьезные осложнения). Летальных исходов на было. Повторные боли после приема пищи в течение 3 мес отмечались у 1 больного, рефлюкс-гастрит - у 1, признаки холангита - у 2 больных. Эти осложнения были купированы консервативным лечением.
Несостоятельность анастомоза наблюдалась у 2-х больных. У одного их них было выделение 30-70 мл желчной жидкости по подпеченочному дренажу в течение первых 2 дней, прекратившееся спонтанно. У другого больного (большая несостоятельность) с первого дня отмечались признаки перитонита и сепсиса, при УЗИ обнаружена жидкость в брюшной полости. Через 36 ч произведена повторная лапароскопия, во время которой обнаружен дефект 1 / 3 анастомоза, установлена Т-образная трубка в области анастомоза. У этого больного в последующие дни развилась флегмона правой стенки живота, произведены лампасные разрезы. Больной был выписан через 28 дней в стабильном состоянии, Т-образная трубка удалена через 45 дней.
Спустя 6-12 мес 18 больным было произведено эндоскопическое исследование: у 4 анастомоз не визуализировался, у 14 отмечен функционирующий анастомоз диаметром 6-10 мм.
Показатели холестаза через 6 мес увеличились у 2 больных, через 1 год - у 1 больного.
Таким образом, после 23 лапароскопических операций наложения ХДА по поводу доброкачественных стриктур ОЖП осложнения наблюдались у 2 (8,7%) больных, отличный и хороший результы отмечены у 82,7% больных, плохой - у 3 (13%), очень плохой результат - у 1 (4,3%) больного, летальных исходов не было.
В период до применения эндоскопии ХДА широко использовался как один из способов билиарного шунтирования у больных с камнями ОЖП, его дистальными стриктурами, злокачественными обструктивными сужениями и расширением. С появлением и широким внедрением ЭРХПГ эндоскопическая сфинктеротомия стала стандартным методом лечения при камнях и дистальных сужениях ОЖП [10]. В частности, при сочетании камней желчного пузыря и холедохолитиаза или стриктуры наибольшее распространение получило двухэтапное вмешательство, заключающееся в пред- или послеоперационной ЭРХПГ + ЭПСТ и ранее открытой, а в последние годы лапароскопической холецистэктомии. В настоящее время этот подход принимается как метод выбора начального лечения при постхолецистэктомических стриктурах и камнях и является успешным у 80-95% больных [3]. Однако такое положение, при котором нецелесообразно проводить ЭРХПГ (протяженные стриктуры, вклиненные камни, сложности канюляции, беспокойство больного), имеется опасность осложнений (перфорация, панкреатит), или необходимость двухэтапного лечения при сопутствующих камнях желчного пузыря, создает предпосылки для поиска альтернативных методов лечения. В последние годы возрос интерес к одномоментным лапароскопическим вмешательствам при холецистолитиазе и стриктурах ОЖП.
В связи с этим появилась тенденция использования методов одномоментной лапароскопической холецистэктомии и эндоскопической сфинктеротомии (техника «рандеву») и наложению ХДА [11, 14, 22].
Несмотря на то что ХДА считается технически простой операцией, дающей хорошие ранние результаты, существует обеспокоенность такими осложнениям, как рефлюкс-холангит, рефлюкс-гастрит, проблема дистальной культи. Однако в нерандомизированном исследовании [5] была показана необоснованность этой обеспокоенности. Поскольку большой опыт лапароскопического формирования ХДА отсутствует, нет возможности высказать новые идеи относительно ценности этого метода. Согласно нашим данным, отдаленные результаты лапароскопического наложения ХДА могут расцениваться как удовлетворительные, хотя сама операция не обходится без осложнений. В частности, выраженность холангита, рефлюкс-гастрита, холедохолитиаза не очень высока, и в 82,7% наблюдений удается получить отличные и хорошие результаты. Эти показатели близки к таковым при двухэтапном лечении. Коме того, возможность лапароскопического наложения ХДА, если нельзя выполнить ЭПСТ, доказывает право этого метода на существование.
Таким образом, операция лапароскопического наложения холедоходуоденоанастомоза, выполняемая опытными хирургами отобранным больным, дает хорошие отдаленные результаты и может служить альтернативой эндоскопической папиллосфинктеротомии.
Хирургия малых доступов - понятие более широкое, чем лапароскопическая хирургия, и подразумевает получение информации о месте приложения лечебного воздействия любым способом - рентгенологическим, с помощью ультразвукового исследования (УЗИ) или компьютерной томографии (КТ), через минидоступ, видеоэндоскопически [6].
В результате пациенту оказывается хирургическое пособие, вызывающее минимальные болевые ощущения, дающее возможность быстрого восстановления активности и трудоспособности, требующее кратковременного пребывания в стационаре. Хирургия малых доступов характеризуется широкими показаниями, мультидисциплинарным подходом, необходимостью специальных навыков и специфического оборудования [7].
По мнению ряда авторов, положительными моментами холецистэктомии из минидоступа являются:
1) отсутствие пневмоперитонеума;
2) аналогичные стандартному способу оперирования технические приемы;
3) отсутствие проблемы перфорации воспалительно-измененной стенки желчного пузыря эндозажимами;
4) возможность выполнения холецистотомии и полного опорожнения желчного пузыря;
5) полное отграничение операционного поля от свободной брюшной полости;
6) отсутствие проблем с удалением препарата из брюшной полости;
7) сохранение возможности выполнения малотравматичной операции при наличии пузырно-дуоденального и пузырно-ободочного свищей;
8) близкая к стандартной техника ревизии и санации общего желчного протока, возможность применения любого способа завершения холедохотомии (первичного шва, наружного или внутреннего дренирования).
По данным П.С. Ветшева и соавт. [2], одним из достоинств холецистэктомии из минидоступа считают возможность непосредственного визуального контроля за ходом операции. Это обстоятельство, по мнению авторов, можно использовать для обучения начинающих хирургов, первоначально овладевших навыками традиционной холецистэктомии, лапароскопической методике оперирования.
Уже длительное время при заболеваниях желчного пузыря лапароскопическая холецистэктомия является операцией выбора во всем мире [3]. По травматичности лапароскопическая холецистэктомия и холецистэктомия из минидоступа сопоставимы, имеют значительные преимущества перед холецистэктомией из традиционного доступа.
В нашей работе мы также не ставили целью доказать, что минилапаротомия имеет лучшие результаты по сравнению с лапароскопической холецистэктомией. Проанализировав данные литературы, результаты собственых исследований, мы пришли к выводу, что достоверных различий в травматичности и частоте развития осложнений при лапароскопической холецистэктомии и холецистэктомии из минидоступа нет.
Проведен анализ результатов хирургического лечения 207 больных с желчнокаменной болезнью (ЖКБ), в том числе с осложненными формами, находившихся на стационарном лечении в Республиканской клинической больнице Нальчика.
Распределение больных в зависимости от возраста представлено в табл. 1. Чаще желчнокаменной болезнью болеют женщины в возрасте от 31 года до 50 лет.
Больные были разделены на 3 группы. В 1-ю группу вошли 110 больных, которым произведена холецистэктомия из верхнесрединного доступа и доступа Кохера. Среди больных было 25 (22,7%) мужчин и 85 (77,3%) женщин. Во 2-ю группу включены 50 больных, которым выполнена видеолапароскопическая холецистэктомия. Среди больных было 17 (34%) мужчин и 33 (66%) женщины. 3-ю (основную) группу составили 47 больных, которым произведена холецистэктомия из предложенного нами минидоступа. Это принципиально отличающийся от описываемых в литературе минидоступ для выполнения холецистэктомии. Среди больных этой группы было 16 (34%) мужчин и 31 (66%) женщина.
Все больные обследованы клинически и лабораторно. На основании УЗИ был поставлен диагноз желчнокаменной болезни.
Практически у всех больных (n=201, или 97,1%) выявлен сопутствующий панкреатит, часто наблюдалось ожирение разных степеней (n=186, или 89,8%), что важно отметить, говоря о минидоступе, ИБС была у 51 (24,6%), язвенная болезнь двенадцатиперстной кишки (ДПК) - у 47 (22%) больных. Диагноз панкреатита ставили на основании данных УЗИ. В случае клинической картины острого панкреатита, гиперамилаземии, при наличии в анамнезе частых приступов опоясывающих болей и болей в левом подреберье, эпизодов пожелтения кожного покрова проводилась КТ и интраоперационная холангиография (без расширения операционного доступа). Реже встречались ИБС и язвенная болезнь ДПК. Распределение больных в зависимости от ожирения представлено в табл. 2. Использованная классификация ожирения приведена в табл. 3.
При сравнении клинических групп по возрасту и степени ожирения выявлено, что 2-я и 3-я группы в процентном соотношении практически сопоставимы, в 1-й клинической группе преобладали больные старше 40 лет и с ожирением III-IV степени. По другим сопутствующим заболеваниям данные клинические группы почти равнозначны.
Описание метода
Параллельно и ниже реберной дуги справа, отступив несколько сантиметров от срединной линии, максимально близко к выбранным до операции при УЗИ точкам выполняли разрез кожи и подкожной клетчатки длиной 3-5 см (рис. 1, а). Рисунок 1. Интраоперационные фотографии. а - разрез кожи. После вскрытия таким же по направлению разрезом влагалища прямой мышцы выделяли медиальную ее треть. Выделение осуществляли от белой линии живота путем отделения указательным пальцем от задней стенки влагалища прямой мышцы. Мышцы пересекали электроножом либо на зажимах. Верхние надчревные артерии вену сдвигали в сторону. При соблюдении всех моментов хорошо открывается зона оперативного воздействия с сохранением крепкого каркаса брюшного пресса (рис. 1, б). Рисунок 1. Интраоперационные фотографии. б - сохраненная часть прямой мышцы. К рассекаемым задней стенке влагалища и брюшине подшивали простыни.

В брюшную полость вводили крючок с осветителем (рис. 2), Рисунок 2. Крючок с осветителем. который чаще используется для отведения правой доли печени.
Зону желчного пузыря и гепатодуоденальной связки отграничивали хирургическими салфетками с длинными «хвостами». Вводили их в брюшную полость полностью и помещали между узкими зеркалами (количеством до 3), как при традиционной холецистэктомии: влево - под левую долю печени, влево и вниз - для отведения желудка и большого сальника, вправо и вниз - для отведения печеночного угла ободочной кишки и петель тонкой кишки.
Холецистэктомия из минидоступа отличается от традиционной холецистэктомии необходимостью дистанционного оперирования (из-за невозможности ввести руку в брюшную полость). При затягивании узлов использовали палочку В.В. Виноградова, а оттягивание желчного пузыря осуществляли мягким длинным зажимом, введенным через контрапертуру, через которую в последующем проводили дренажную трубку. Контрапертуру длиной 1 см выполняли несколько ниже основного разреза, принимая во внимание необходимость создания удобств для манипуляции на желчном пузыре. Поперечный доступ, выполняемый с учетом локализации гепатикохоледоха и желчного пузыря, и использование перечисленных выше приемов позволяют оперировать под хорошим визуальным контролем.
Кровотечения, соскальзывания лигатур с пузырных артерий и вен в послеоперационном периоде не отмечалось.
Наиболее близкой к предлагаемой методике является холецистэктомия из минидоступа с использованием комплекта инструментов Мини-ассистент по М.И. Прудкову (Руководство по хирургии желчных путей, под редакцией Э.И. Гальперина, П.С. Ветшева, с. 176).
Данная операция предусматривает малый разрез брюшной стенки и создание зоны в брюшной полости, доступной адекватному осмотру и манипулированию с помощью специального набора инструментов. Комплект Мини-ассистент представлен кольцевидным ранорасширителем, набором крючков-зеркал с системой освещения.

Для удобства понимания предложенной методики представлено сравнение ее с холецистэктомией из минидоступа по М.И. Прудкову (табл. 4).
Недостатками прототипа являются:
- необходимость иметь в арсенале специальный комплект инструментов Мини-ассистент;
- длительность установки системы крючков-зеркал и освещения;
- не всегда удается установить зеркала правильно, достигая полной фиксации ранорасширителя, добиться адекватного освещения в подпеченочном пространстве;
- разрез на 3-4 см правее срединной линии не всегда позволяет выйти к месту хирургических манипуляций;
- неудобства при необходимости расширения операционного доступа.
Результаты
Все больные активизируются на 1-2-е сутки. Средняя длительность пребывания больных в стационаре: 1-я группа - 16-20 койко-дней, 2-я группа - 10-14 койко-дней, 3-я группа - 10-12 койко-дней.
Парез кишечника в 1-й группе проходил на 2-3-и сутки, во 2-3-й группах уже к вечеру дня операции появлялась вялая перистальтика, а к утру выслушивалась активная перистальтика кишечника.
Дренажные трубки, установленные в послеоперационную рану, в 1-й группе удаляли на 3-4-е сутки, во 2-й группе такие дренажи не устанавливали, в 3-й группе их удаляли на 2-е сутки, так как по причине малой операционной травмы отделяемого практически не было.
Страховочные дренажи из подпеченочного пространства в 1-й группе удаляли на 3-и сутки, во 2-й и 3-й группах - на 2-4-е сутки.
В 1-й группе у 5 больных в послеоперационной ране образовалась серома, которая была опорожнена на 5-7-е сутки, что увеличило срок пребывания больных в стационаре.
В период от 6 до 24 мес с послеоперационной вентральной грыжей повторно обратилось 8 больных, и это, возможно, не истинная цифра таких больных, так как сюда не включены пациенты, которые обращались в другие стационары или вовсе не обращались.
Во 2-й группе с троакарной грыжей обратилось 3 больных в период от 3 до 6 мес. Больные были повторно оперированы.
У всех больных 3-й группы был достигнут отличный косметический результат, повторных обращений за период наблюдения не было. П.С. Ветшев и соавт. [1, 2], А.С. Ермолов и соавт. [5] отмечают, что из осложнений после холецистэктомии из традиционного доступа следует отметить нагноение раны в 2,7-3,1%, послеоперационную грыжу в 1,3-1,7% наблюдений. Авторы подчеркивают, что оставляют желать лучшего и косметические свойства послеоперационного рубца.
А.А. Голубев и соавт. [4], сравнивая послеоперационное течение после лапароскопической холецистэктомии и холецистэктомии из трансректального минидоступа, отмечают, что при использовании минидоступа частота послеоперационных легочных осложнений составила 20%, после лапароскопической операции - 28,9%. Частота развития инфильтратов в области послеоперационных ран или их нагноения при холецистэктомии из минидоступа составила 7%, при лапароскопической - 8,3%.
Низкий процент осложнений, по мнению многих авторов, объясняется минимальной послеоперационной травмой, более быстрым выходом из наркоза, незначительной выраженностью болевого синдрома в раннем послеоперационном периоде, практически не изменяющейся функцией внешнего дыхания после операции, отсутствием пареза кишечника. Все перечисленное позволяет считать метод холецистэктомии из минидоступа достаточно эффективным и заслуживающим более активного внедрения в клиническую практику.
Больная Х., 42 лет, поступила в экстренном порядке с диагнозом: ЖКБ. Острый калькулезный холецистит, холедохолитиаз, механическая желтуха.
На момент поступления общее состояние больной средней тяжести, она в сознании, предъявляет жалобы на интенсивные, связанные с нарушениями в диете боли в правом подреберье, которые появились на фоне ноющих болей, беспокоящих больную последние 6 мес, однократную рвоту, горечь во рту, желтушность кожных покровов, общую слабость.
Дыхание над всеми отделами легких ослабленное, везикулярное, хрипов нет, частота дыханий 19 в 1 мин, тоны сердца приглушены, ритмичны, частота сердечных сокращений 96 в 1 мин, АД 100/70 мм рт.ст.
Язык сухой, обложен белесоватым налетом. Живот умеренно вздут, при пальпации болезненный в правом подреберье и эпигастральной области. Симптомы Кохера, Лепене, Ортнера положительные, симптомов раздражения брюшины нет, перистальтика вялая. Стул ахоличный.
При УЗИ гепатодуоденальной зоны выявлены конкременты желчного пузыря диаметром от 9 до 25 мм, конкременты в общем желчном протоке, признаки реактивного панкреатита.
Больная оперирована; произведена холецистэктомия из минидоступа, холедохолитотомия, дренирование общего желчного протока. Выписана на 12-е сутки после операции в удовлетворительном состоянии.
Таким образом, на наш взгляд, преимуществами холецистэктомии из минидоступа являются:
- минимальная операционная травма и отсутствие необходимости наложения пневмоперитонеума;
- снижение числа ранних и поздних раневых осложнений;
- отсутствие нарушений функции внешнего дыхания, пареза кишечника, снижение потребности в анальгетиках вследствие минимальной травматичности операции;
- раннее восстановление двигательной активности, быстрое восстановление трудоспособности;
- отсутствие необходимости специального инструментария, кроме крючка с осветителем.
В отличие от общепринятого минидоступа достигается более объемная визуализация и более полная ревизия органов брюшной полости, практически сопоставимые с таковыми при традиционной холецистэктомии, а по травматичности - с видеолапароскопической холецистэктомией.
При таком минидоступе возможно проведение манипуляций на внепеченочных желчных протоках, что расширяет показания к минилапаротомии в лечении ЖКБ.
Минимальная травматизация, как интраоперационно, так и в целом, позволяет снизить необходимость инфузионной терапии в раннем послеоперационном периоде, сократить продолжительность госпитализации. Имеется возможность быстрого при необходимости перехода на традиционный доступ.
Читайте также:
