Эффективность коррекции объема гемиторакса. Селективная торакопластика при резекции легкого
Добавил пользователь Евгений Кузнецов Обновлено: 28.01.2026
1 Саратовский городской центр торакальной хирургии, (ГУЗ «Саратовская городская клиническая больница №2 им. В.И. Разумовского»)
2 ГОУ ВПО «Саратовский государственный медицинский университет им. В.И. Разумовского Минздравсоцразвития России»
Проведен анализ особенностей клинического течения спонтанного пневмоторакса у больных, находившихся на лечении в Саратовском центре торакальной хирургии. Проведена оценка тактики и принципов хирургического лечения при спонтанном пневмотораксе. Применявшиеся виды торакоскопических вмешательств оценивались по эффективности достигнутого аэростаза во время самого вмешательства и в ближайшем послеоперационном периоде, по срокам и стойкости расправления легкого, по возникшим осложнениям и рецидивам спонтанного пневмоторакса. В дополнение к проведенным торакоскопическим вмешательствам всем больным проводился плевродез в целях профилактики рецидива спонтанного пневмоторакса. Анализ проведенных наблюдений позволил выработать рациональную тактику по оптимальному выбору вида торакоскопического вмешательства у каждого конкретного больного в зависимости от патологии, обнаруженной во время торакоскопии. Установлены преимущества торакоскопического метода лечения перед традиционными: торакотомным и операцией из мини- доступа.
3. Филатова А. С., Гринберг Л. М. Патоморфология легочно-плевральных поражений при спонтанном пневмотораксе (по данным резекций) // Уральский медицинский журнал. 2009. № 4. С. 14-25.
5. Викторова И. А., Нечаева Г. И., Конев В. П. и др. Клинико-прогностические критерии дисплазии соединительной ткани // Российские медицинские вести. 2009. T. XIV. № 1. С. 76-86.
6. Вершинина М. В., Говорова С. Е., Нечаева Г. И., Ратынская И. А. Лечение пациентов с буллезной эмфиземой на фоне дисплазии соединительной ткани в первичном звене здравоохранения // Лечащий Врач. 2011. № 9. С. 14-16.
7. Cardillo G., Facciolo F., Regal M. et al. Recurrences following videothoracoscopic treatment of primary spontaneous pneumothorax: the role of redo-videothoracoscopy // Eur. J. Cardiothorac. Surg. 2001. - Vol. 19. - P. 396 -399.
8. Leo F., Pastorino U., Goldstraw P. Pleurectomy in primary pneumothorax: is extensive pleurectomy necessary? // J. Cardiovasc. Surg. (Torino). 2000. - Vol. 41 (4). P. 633 - 636.
9. Loeys B. L. et al. The revised Ghent nosology for the Marfan syndrome // Am J Med Gen. 2010. V. 47. № 7. P. 476-485.
10. Massaro G. D., Radaeva S, Clerch L. B., Massaro D. Lung alveoli: endogenous programmed destruction and regeneration // Am J Physiol Lung Cell Mol Physiol. 2002. V. 283. P. 305-309.
По мнению некоторых авторов [1,2,4,9] при традиционных методах лечения спонтанного пневмоторакса в 25-35 % наблюдаются его рецидивы. Это вынуждает торакальных хирургов искать пути улучшения результатов, поэтому в настоящее время у таких пациентов все шире используются видеоторакоскопические вмешательства [3,6,7,]. Однако при выборе рационального вида торакоскопического вмешательства, показанного в каждом конкретном случае до сих пор встречаются затруднения [5,8,10].
Цель исследований: разработка эффективной тактики и выбор рационального вида торакоскопических вмешательств при спонтанном пневмотораксе.
1. Анализ особенностей клинического течения спонтанного пневмоторакса у больных, находившихся на лечении в Саратовском центре торакальной хирургии.
2. Оценка тактики и принципов хирургического лечения при спонтанном пневмотораксе.
Материал и методы
В Саратовском центре торакальной хирургии, расположенном на базе торакального отделения 2 городской клинической больницы г. Саратова за период с 2006 по 2015 гг. находилось на лечении 379 больных со спонтанным пневмотораксом. Из них традиционное хирургическое лечение, включающее торакотомию, проводилось у 243 (64,1 %) больных.
С 2003 года в центре лечение спонтанного пневмоторакса стало проводиться с применением видеоторакоскопии. Таким образом, пролечено 136 (35,9 %) таких больных (таблица 1).
Виды торакоскопических вмешательств и их исходы
Виды торакоскопических вмешательств
Перевязка и прошивание булл
Атипичная резекция легкого
Для осуществления плевродеза париетальную и висцеральную плевру обрабатывали 2-3% спиртовым раствором йода. Если во время торакоскопии установлено, что восстановился аэростаз легкого и в нем нет других буллезных изменений, то ограничивались проведением только мероприятий по обеспечению плевродеза. Таких наблюдений было 11 (8,1 %).
В дополнение к проведенным торакоскопическим вмешательствам всем больным проводился плевродез в целях профилактики рецидива спонтанного пневмоторакса.
При наличии в легком небольших булл с диаметром до 1 см удавалось достигнуть успешный аэростаз электрокоагуляцией булл. Такая операция выполнена у 6 (4,4 %) больных.
Буллы размером от 1 до 5 см приходилось перевязывать циркулярной лигатурой. Если основание буллы широкое и есть угроза соскальзывания обычной циркулярной лигатуры, то накладывают прошивную лигатуру. Перевязка булл выполнена у большинства - 77 (56,6 %) больных.
Если имелась большая более 5 см одиночная булла и участок легкого с выраженными изменениями в виде множественных мелких булл, то проводили перевязку большой буллы и атипичную резекцию участка легкого. Такое вмешательство выполнено у 5 (3,7 %) больных. Применение такой тактики позволяло ограничить объём резекции легкого.
При выявлении сливающихся в гроздь булл или буллезном перерождении сегмента легкого проводилось выполнение атипичной резекции с удалением пораженного участка легкого, но резекция выполнялась с наложением на легкое ручных П-образных швов [6 (4,4 %) больных] или с применением эндоскопических сшивающих аппаратов [11(8,1 %) больных].
При застарелом спонтанном пневмотораксе и с фиксированным спайками коллабированным легком в условиях стойкого аэростаза для расправления легкого было достаточно осуществить пневмолиз торакоскопическим пережиганием плевральных спаек. Такое вмешательство было выполнено 4 (2,9 %) больных. Выявление обширного буллезного участка легкого, пневмокист или при невозможности технического выполнения обычных эндоскопических вмешательств применялись радикальные видеоассистированные операции с использованием из миниторакотомического доступа длиной 6 см. Этот прием позволял осуществить более широкую атипичную резекцию легкого с применением традиционных сшивающих аппаратов типа УО, что и осуществлено у 18 (13,2 %) пациентов.
Возможности и последствия различных видов операций при спонтанном пневмотораксе
Эффективность коррекции объема гемиторакса. Селективная торакопластика при резекции легкого
Характерной особенностью последних десятилетий является увеличение частоты рецидивов туберкулеза как после терапевтического, так и после хирургического лечения [1, 2, 5, 8, 13]. Многие хирурги связывали это в первую очередь с увеличением частоты лекарственной устойчивости микобактерий туберкулеза [3, 6, 20, 21].
Несмотря на все возрастающую роль хирургии в лечении легочного туберкулеза и ее высокую непосредственную эффективность, проблема послеоперационных рецидивов туберкулеза остается серьезным сдерживающим фактором на пути ее широкого применения. Частота послеоперационных рецидивов, по данным изученной нами литературы, составляет в среднем 5,7% и имеет в последние годы тенденцию к увеличению.
Эффективность консервативного лечения послеоперационных реактиваций туберкулеза, по данным большинства авторов, невелика [6-8, 13-15, 18, 25, 26]. Согласно публикации В.Д. Ямпольской [26], интенсивным консервативным лечением удалось излечить только 7 из 23 послеоперационных реактиваций туберкулеза (30%). По данным В.А. Краснова [13], успешным консервативное лечение было лишь у 36% из 590 больных с послеоперационными рецидивами. Из опыта А.В. Елькина и соавт. [8] при лечении 241 пациента с послеоперационными реактивациями лишь в 78 (32%) случаях достигнут клинический эффект.
Закономерным следствием низкой эффективности химиотерапии послеоперационных рецидивов туберкулеза является высокая хирургическая активность (до 94,8%) у этой категории больных [16]. Проанализировав данные 9 публикаций [4-6, 8, 10, 16, 21, 26, 28] о частоте использования хирургических методов в лечении послеоперационных реактиваций туберкулеза (1684 случая), мы подсчитали, что повторное хирургическое лечение проведено 903 (53,6%) больным из их числа.
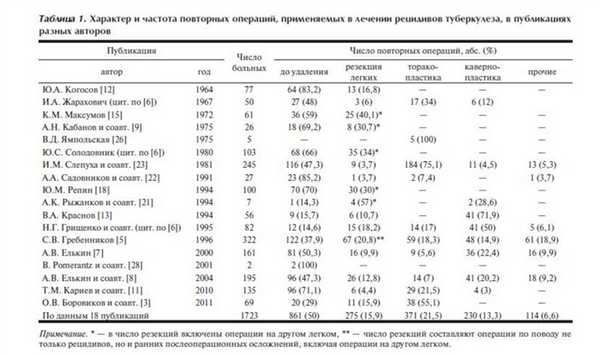
Чаще всего в лечении послеоперационных рецидивов туберкулеза используются такие оперативные вмешательства, как пневмонэктомия (удаление ранее резецированного легкого) и экстраплевральная торакопластика (табл. 1 ). Обобщив литературные публикации 18 авторов о хирургическом лечении 1723 пациентов с рецидивами туберкулеза, мы подсчитали, что до удаления легкого у половины оперированных (50%) были выполнены экстраплевральная торакопластика - у 371 (21,5%), резекции ранее оперированного или противоположного легкого - у 275 (15,9%) и кавернопластики - у 230 (13,3%) [3, 5-9, 11-13, 15, 18, 21-23, 26, 28], другие виды операций - лишь в 6,6% случаев.
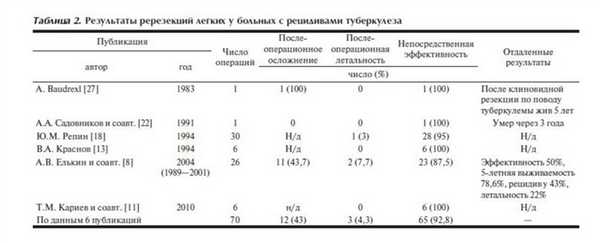
В целом ререзекции применяются по поводу рецидивов туберкулеза крайне редко. Нами найдено лишь 6 публикаций [8, 11, 13, 18, 22, 27] за последние три десятилетия, в которых приводились результаты этих операций раздельно от других повторных операций (табл. 2 ) и описывались в общей сложности последствия 70 ререзекций. Однако суммарное число этих вмешательств, скорее всего, еще меньше, поскольку при описании наибольших групп этих операций в разные годы сотрудниками Санкт-Петербургского НИИ фтизиопульмонологии (Ю.М. Репин - 30 случаев [18], А.В. Елькин и соавт. - 26 случаев [8]) в последней публикации, обобщающей материал с 1989 по 2001 г., по видимому, частично включены и больные, описанные в 1994 г. [18].
Частота послеоперационных осложнений повторных резекций легких у больных туберкулезом, по данным доступной литературы, составляет в среднем 43%, а послеоперационная летальность - 4,3%, что намного превышает уровень осложнений и летальности первичных резекций легких по поводу туберкулеза.
Непосредственная эффективность всех хирургических методов лечения послеоперационных рецидивов туберкулеза в большинстве статистик остается невысокой (от 60 до 88%, а в отдаленном периоде она снижается до 50-72%) [8, 11, 13, 17, 18] при большой послеоперационной летальности (в среднем 9%) и летальности в отдаленный период до 25% и более [5-8, 12].
В литературе подчеркивается высокий травматизм повторных радикальных операций (большая кровопотеря, длительность операции), высокий риск интраоперационных осложнений (до 58%) [14] и, в частности, ранений крупных сосудов (в среднем 13,7% случаев). Радикальные резекционные операции, в том числе и ререзекции, сопровождаются высоким риском смерти во время операции от кровотечения (до 16%) [14].
Материал исследования
Материалом для настоящего исследования послужили повторные резекции легких по поводу послеоперационного рецидива туберкулеза в оперированном легком у 50 больных, выполненные первым автором этой статьи c 2004 по 2011 г. в клинике фтизиопульмонологии ГБОУ ВПО "Первый МГМУ им. И.М. Сеченова" и ФГБУ ЦНИИТ РАН. Были прооперированы 28 мужчин и 22 женщины в возрасте от 15 до 67 лет: 10% из них в возрасте до 18 лет,
30% - от 19 до 29 лет, 32% - от 30 до 39 лет и
28% - старше 40 лет. У всех больных до операции был установлен рецидив туберкулеза легких.
Анализ распространенности основного процесса в легком по сегментам показал, что при деструктивных процессах чаще всего поражалось 5 и более сегментов. Размеры каверн в большинстве случаев составляли от 2 до 4 см. Лишь у 8% пациентов размеры деструкции в легком превышали 6 см. Двустороннее поражение легких было у 24 (48%) больных, в том числе деструктивные формы - у 6 (12%).
Бациллярным на момент операции был 41 (82%) пациент. Данные о лекарственной чувствительности микобактерий туберкулеза (МБТ) к антибактериальным препаратам были получены в 34 (68%) случаях, о множественной и экстремальной лекарственной устойчивости - в 21 (42%) и 8 (16%) случаях соответственно.
Легочный процесс осложнялся у 40 (80%) больных. Самым частым осложнением была дыхательная недостаточность (35 случаев), реже отмечались эмпиема плевры (9), легочное кровотечение (4), кахексия (7). У 39 (78%) пациентов имелись сопутствующие заболевания (101 случай различной патологии), наиболее частыми среди них были: сердечно-сосудистая патология (а именно легочное сердце), нарушения сердечного ритма и миокардиодистрофия, хронические обструктивные заболевания легких.
При фибробронхоскопии изменения выявлены в 11 (22%) случаях: дренажный гнойный эндобронхит и рубцовый стеноз главного бронха (по одному случаю), туберкулез бронхов (2), диффузный хронический эндобронхит (6), микрофистула культи бронха после первичной операции (1).
После резекций легкого в отдаленный период показания к повторной резекции на стороне предшествующей операции чаще всего возникают при послеоперационных рецидивах деструктивного туберкулеза легких ограниченной распространенности без очаговой диссеминации и вне основной зоны поражения, не имеющих тенденции к закрытию полостей распада и абациллированию на фоне достаточно длительной (4-6 мес) химиотерапии. Дополнительными доводами в пользу операции в подобной ситуации является наличие множественной или широкой лекарственной устойчивости МБТ, а также непереносимости химиотерапии.
Наиболее частым показанием к ререзекции у наших больных был фиброзно-кавернозный туберкулез оперированного легкого (48%), причем часто при наличии очагового обсеменения остающихся отделов легкого к ререзекции приходилось прибегать вынужденно из-за низких функциональных резервов организма и поражения контралатерального легкого. Объемом ререзекций у больных ФКТ являются комбинированные резекции, лоб- и билобэктомии, требующие в послеоперационном периоде применения методов коррекции гемиторакса из-за малого объема остающейся легочной ткани и наличия очаговых изменений.
Более редким показанием для ререзекции легкого у наших больных служил кавернозный туберкулез оперированного легкого (16% оперированных). Все пациенты с этой формой туберкулеза лечились по поводу послеоперационного рецидива в терапевтических отделениях от 5 мес до 8 лет, в том числе четверо (50%) - с применением пневмоперитонеума, в 7 из 8 случаев срок консервативного лечения превысил 8 мес. Наиболее часто при рецидиве кавернозного туберкулеза выполнялись анатомические резекции легких.
На нашем опыте туберкулемы с распадом послужили показанием к выполнению ререзекций легкого у 24% больных. При этой форме туберкулеза во многих случаях оказались возможны атипичные ререзекции легкого небольшого объема, однако при множественных туберкулемах объем операции мог доходить до обширных комбинированных ререзекций. Более редким показанием к ререзекции явился цирротический туберкулез (1 случай, 2%) и эмпиема плевры или ложная каверна (5 случаев, 10%). При наличии эмпиемы плевры этим больным чаще
выполняются комбинированные ререзекции легких с плеврэктомией, плевролоб- и плевробилобэктомия, реже плеврэктомия с частичной ререзекцией легкого.
Особо следует подчеркнуть, что подавляющее большинство наших больных (66%) получали консервативное лечение по поводу послеоперационного рецидива в течение 12 и более месяцев без положительной клинико-рентгенологической динамики, а большинство даже с отрицательной динамикой. Столь длительная химиотерапия при резектабельном процессе только ухудшает прогноз хирургического лечения за счет усиления лекарственной устойчивости.
Среди первичных операций, после которых были выполнены ререзекции, отмечены атипичные (29 случаев), сегментарные анатомические (4) и комбинированные (7) резекции легкого, а также лоб- и билобэктомия (9 и 1 случай соответственно).
Авторами статьи было выполнено 85 операций 50 пациентам, включая резекции противоположного легкого при двусторонних процессах (2 случая), отсроченные корригирующие торакопластики (29) и повторные операции по поводу послеоперационных осложнений ререзекций (4). У 13 больных повторная резекция легкого сочеталась с плеврэктомией и декортикацией легкого.
Объем повторной резекции легкого в большинстве случаев был значительным. У 24 больных
выполнены комбинированные резекции, в том числе объемом более доли у 11 оперированных. Лобэктомия произведена в 1 случае, анатомические полисегментарные ререзекции - в 8, а частичные атипичные ререзекции - только в 17 (34%) случаях.
У 47 (94%) пациентов, с учетом большого объема произведенных резекций и высокого риска повторного рецидива, применены различные способы коррекции объема гемиторакса, в том числе торакопластика отсроченная (у 29), предшествующая (у 4), на противоположной стороне (у 1), а также одномоментное перемещение диафрагмы с ререзекцией (у 1), одномоментный экстраплевральный пневмолиз с пломбировкой (у 1), френикотрипсия (у 3) и пневмоперитонеум у 39, причем последний часто сочетался с другими методами уменьшения объема плевральной полости.
Из 85 операций, выполненных 50 нашим пациентам, 61 произведена из минидоступа с применением видеоторакоскопии. При этом для прошивания легочной ткани использовался сшиватель органов для малоинвазивной хирургии, разработанный проф. Д.Б. Гиллером совместно с фирмой "Уникон" (Россия). Примером подобной операции может служить наблюдение повторной резекции после ранее произведенной нижней лобэктомии слева (рис. 1-4 ).
Результаты и обсуждение
При выполнении 50 повторных резекций легкого у 50 пациентов мы обнаружили плевральные сращения во всех случаях, при этом в 2 (4%) они были ограниченными, в 13 (26%) субтотальными (более 1 / 2 поверхности плевральной полости) и в 35 (70%) тотальными. Длительность операции составила в среднем 220,7 мин, средняя интраоперационная кровопотеря - 346,6 мл. Гемотрансфузий удалось избежать у всех больных.
Интраоперационные осложнения отмечены у
7 (14%) пациентов, в том числе вскрытие полости эмпиемы и скальпированные ранения легкого по
2 случая, вскрытие прикультевого абсцесса, ранение v. azygas и разрыв мембранозной части трахеи перераздутой манжеткой интубационной трубки - по
В послеоперационном периоде у 5 (10%) больных развились осложнения, в том числе (по одному случаю) раннее, позднее интраплевральные кровотечения, эмпиема с бронхиальным свищом, остаточная плевральная полость и раневое осложнение. Эти послеоперационные осложнения были ликвидированы и послеоперационной летальности не отмечено. Все пациенты на момент выписки не выделяли МБТ в мокроте. Полный клинический эффект был достигнут в 48 (96%) случаях, 2 пациента были выписаны с кавернами в противоположном легком, отказавшись от операции на второй стороне.
Отдаленные результаты удалось проследить у
36 пациентов. Полный клинический эффект сохранялся в 35 (97,3%) случаях, реактивация туберкулеза отмечена в 1 (2,8%). Работали или учились в вузах
29 (80,6%) оперированных.
В доступной литературе нами найдено лишь
одно исследование, приводящее подробный анализ отдаленных результатов ререзекций легких у больных с рецидивами туберкулеза, с данными которого мы могли бы сравнить полученные нами результаты.
Согласно публикации А.В. Елькина и соавт. [8], после 26 ререзекций послеоперационные осложнения возникли в 11 (43,7%) случаях, умерли в стационаре 2 (7,7%) пациента. Непосредственная эффективность (87,5%) в отдаленном периоде снизилась до 50%. Реактивация туберкулеза произошла после ререзекций в 43% случаев, 2% оперированных умерли от туберкулеза в отдаленном периоде, а всего в срок до 5 лет погибли более 20% оперированных. Пятилетняя выживаемость у всей группы больных, по данным А.В. Елькина и соавт.,
составила 78,6% [8]. Сравнительно высокую эффективность операций в нашей серии больных
мы связываем с более частым использованием
различных методов уменьшения объема плевральной полости после повторных резекций легкого.
Коррекция объема гемиторакса при такого рода вмешательствах, по нашему мнению, показана во всех случаях и не была нами применена только у 3 пациентов, отказавшихся от корригирующей операции и имевших противопоказания (спаечный процесс в брюшной полости после абдоминальных операций) к наложению пневмоперитонеума. При резекции верхних отделов легких мы отдавали предпочтение отсроченным экстраплевральным торакопластикам, при резекции нижних отделов - френикотрипсии, перемещению диафрагмы или пневмоперитонеуму.
Заключение
Таким образом, несмотря на большую тяжесть состояния пациентов, техническую сложность и более высокий хирургический риск повторных резекций, чем у коллапсохирургических и органоуносящих вмешательств, хорошие отдаленные результаты и высокая частота трудовой реабилитации оперированных убедительно доказывают преимущество выполнения повторных резекций легких при рецидивах туберкулеза в ранее резецированном легком.
Российская медицинская академия последипломного образования, Москва, Россия
Клиническая больница №1 «Медси», Москва, Россия
ФГБУ «Лечебно-реабилитационный центр» Минздрава России, Москва, Россия
Торакоскопические резекции легкого при метастатическом поражении без установки плеврального дренажа: начальный опыт
Журнал: Хирургия. Журнал им. Н.И. Пирогова. 2018;(4): 68‑70
Статья посвящена проспективному исследованию возможности бездренажного ведения пациентов после торакоскопической резекции легких при метастатическом поражении. Материал и методы. Группа пациентов состояла из 10 человек. Средний возраст больных 53,8 года. У большинства пациентов имелось солитарное поражение легкого, расположенное на расстоянии до 3 см от висцеральной плевры. Хирургическое лечение выполняли по стандартной методике — проводили аппаратную атипичную резекцию опухоли легкого в пределах здоровых тканей. Дренировали плевральную полость дренажем 24 Fr. Под контролем зрения расправляли легкое. После послойного ушивания троакарных вколов эвакуировали остаточный воздух с помощью активной аспирации и удаляли дренаж. Рентгенологический контроль органов грудной клетки выполняли через 2 ч и в 1-е сутки после операции. Результаты. Применение методики было успешным у всех 10 пациентов. Продолжительность операции составила в среднем 52 мин. Кровопотеря у всех пациентов отсутствовала. При рентгенологическом исследовании в первые часы и в 1-е сутки послеоперационного периода пневмо- и/или гидроторакса не было ни у одного пациента. Средний срок послеоперационного пребывания пациентов в стационаре составил 3 сут (медиана 2 сут). Случаев повторной госпитализации не было.
Торакоскопические резекционные операции при метастатическом поражении легких являются рутинными в торакальной онкохирургии. По данным некоторых авторов, подобные операции составляют 50—60% общего числа хирургических вмешательств в специализированных отделениях. До 70% из них — это органосохраняющие, экономные (атипичные) резекции легких [1, 2].
Многочисленные исследования, посвященные сравнению результатов открытых и эндоскопических операций, показали преимущества видеоассистированных торакоскопических (ВАТС) вмешательств: безопасность, небольшое число послеоперационных осложнений и хороший косметический эффект [4]. В то же время, несмотря на меньшую травматичность торакоскопических резекций легкого по сравнению со стандартными вмешательствами, необходимость дренирования плевральной полости как завершающего этапа операции редко оспаривается торакальными хирургами.
В последние годы многие аспекты периоперационного ведения пациентов подвергаются переосмыслению в рамках концепции ранней послеоперационной реабилитации, которая основана на внедрении так называемых стандартизированных протоколов ускоренного восстановления (ПУВ, «фаст-трэк») [3]. Одним из ключевых положений ПУВ является переход от рутинного к индивидуализированному применению катетеров, зондов, дренажей. После знакомства с результатами ретроспективного исследования, опубликованными коллективом авторов под руководством A. Watanabe в 2004 г. [8], мы решили иначе взглянуть на необходимость дренирования плевральной полости после небольших по объему резекционных операций на легких. Авторы исследования не обнаружили значимой разницы в частоте раннего и позднего пневмоторакса, в степени болевого синдрома и послеоперационном койко-дне при установке и без установки плеврального дренажа после ВАТС-клиновидной резекции легкого в двух клинически равнозначных группах, в которых было 34 и 42 пациента соответственно. Схожие результаты, но уже в проспективном рандомизированном контролируемом исследовании получили H. Luckraz и соавт. в 2007 г. [6]. По их данным, клинически значимых осложнений не было в группе из 30 пациентов, которым не устанавливали дренаж в плевральную полость после резекции легкого с целью биопсии, однако в этих наблюдениях достигли уменьшения длительности послеоперационного пребывания в клинике.
С учетом того, что объем резецируемой паренхимы легкого при клиновидной резекции или биопсии нередко сопоставим с объемом препарата при резекции по поводу метастатического поражения легкого, объектом нашего исследования явилась именно эта группа пациентов.
Материал и методы
В наше проспективное исследование были включены 10 пациентов (3 мужчин и 7 женщин) с солитарными или единичными метастазами в легкие. Возраст больных от 32 до 73 лет (в среднем 53,8 года).
У 2 пациентов было по 2 метастатических очага в оперируемом легком, у остальных отмечено солитарное метастатическое поражение легкого. У всех пациентов, по данным КТ, очаги располагались на периферии ткани легкого на расстоянии не более 3 см от висцеральной плевры. В качестве контрольной группы мы отобрали из нашей проспективно заполняемой базы данных 10 пациентов с метастатическим поражением легких, у которых послеоперационный период сопровождался дренированием и активной аспирацией плевральной полости.
Предоперационное обследование всех пациентов включало наряду с лабораторными и функциональными тестами МСКТ органов грудной клетки.
Методика проведения операций также была стандартизирована. Все операции проведены на фоне селективной (однолегочной) вентиляции легких. Положение пациента на здоровом боку с подложенным ретракционным валиком, рука со стороны операции отводится на подставке к голове. Используем два монитора, расположенных друг против друга по обеим сторонам от пациента. Перед разрезом кожи проводим инфильтрационную анестезию в местах установки торакопортов 0,5% раствором ропивакаина с целью снижения послеоперационной боли и более эффективной реабилитации пациентов.
Первый порт устанавливаем по передней подмышечной линии в пятом межреберье, еще два порта — под контролем зрения в седьмом межреберье по средней и в шестом межреберье по задней подмышечным линиям. После ревизии органов грудной клетки выполняем аппаратную резекцию легкого с патологическим образованием в пределах здоровых тканей и удаление препарата из плевральной полости в контейнере. Необходимым этапом для оценки герметичности механического шва мы считаем заполнение плевральной полости стерильным физиологическим раствором и проведение вентиляционной (воздушной) пробы. После санации в плевральную полость до ее купола через задний троакарный вкол устанавливаем дренажную трубку диаметром 24 Fr (8 мм). Под визуальным контролем проводим расправление легкого, после чего торакоскоп удаляем, а передний и средний троакарные вколы послойно ушиваем. Остаточный воздух из плевральной полости эвакуирует хирург с помощью активной аспирации. Анестезиолог продолжает вентиляцию до достижения нормативных показателей дыхательного объема и давления на вдохе, что предупреждает развитие ателектазов. После достижения герметичности и при полном отсутствии сброса воздуха удаляем ранее установленный дренаж с последующим ушиванием троакарного вкола и окончательным созданием герметичности плевральной полости. Пациента экстубируют на операционном столе и переводят в палату пробуждения.
Обзорную рентгенографию органов грудной клетки в вертикальном положении больного выполняем через 2 ч после операции и на следующие сутки.
Результаты
Применение методики послеоперационного ведения без дренажа было успешным у всех 10 пациентов. Интраоперационно дополнительного укрепления механического шва не потребовалось ни в одном наблюдении. Мы отметили незначительное увеличение длительности операции, обусловленное необходимостью эвакуации остаточного воздуха. В среднем продолжительность операции составила 52 мин. Кровопотеря у всех пациентов отсутствовала.
При рентгенологическом исследовании в первые часы и в 1-е сутки послеоперационного периода мы не отметили пневмо- и/или гидроторакса ни у одного пациента. Послеоперационных осложнений со стороны других органов и систем не было отмечено. Только у одного пациента боль в области операции потребовала введения трамадола. Средний срок послеоперационного пребывания пациентов в стационаре составил 3 сут (медиана 2 сут). Течение послеоперационного периода после выписки прослежено у всех пациентов, случаев повторной госпитализации не было.
Современный уровень развития хирургии и анестезиологии позволяет по-новому взглянуть на многие устоявшиеся догмы периоперационного ведения пациентов. Анализируя статьи отечественных и зарубежных авторов, посвященных применению ПУВ в различных областях хирургии, стоит отметить, что в торакальной хирургии широко обсуждается возможность проведения резекционных операций на легких без значимой подготовки в день госпитализации с ранним переводом пациентов на амбулаторное ведение [5]. По данным M. Gosh-Gastidar и соавт. [7], выполнение диагностической медиастиноскопии, ВАТС-биопсии легкого и ВАТС-плевродеза без установки дренажа оказалось успешным у 84 из 90 пациентов в рамках стационара одного дня. Шесть пациентов были позднее госпитализированы в разные сроки в связи с отклонениями от гладкого течения послеоперационного периода.
Полученный нами опыт позволяет задуматься о возможности контролируемых сравнительных исследований, посвященных оценке результатов бездренажного ведения пациентов после резекции легкого небольшого объема. Преимуществами этой методики мы считаем возможность проводить более раннюю активизацию и реабилитацию пациентов в связи с уменьшением выраженности послеоперационного болевого синдрома. Потенциально использование этой методики способно не только повысить удовлетворенность пациента проведенной операцией, но и сократить длительность пребывания в стационаре до 1 дня. Окончательный ответ на вопрос о показаниях к применению такого метода, его безопасности и эффективности могут дать лишь хорошо спланированные многоцентровые рандомизированные исследования.
Килевидная деформация грудной клетки (КДГК) - врожденный порок развития, который характеризуется выпячиванием вперед грудины и сочленяющихся с ней ребер. В отличие от воронкообразной деформации КДГК встречается значительно реже и составляет от 5 до 22% всех деформаций грудной клетки [1, 2, 5, 10].
Консервативные способы лечения КДГК подразумевают использование различных наружных компрессионных устройств. Однако применение таких устройств требует длительного их ношения (до 2 лет), а рецидив заболевания после лечения возникает более чем в 50% наблюдений. При использовании этой технологии также бывают осложнения в виде некроза кожи грудной стенки вследствие ее компрессии такими устройствами.
В настоящее время наибольшее распространение при лечении КДГК получили хирургические методы с использованием внутренних или наружных фиксаторов или без фиксирующих конструкций [1, 3, 4-10, 11-17, 19]. Если первые два способа подразумевают выполнение повторного вмешательства для удаления фиксатора, то третий способ позволяет получить хороший косметический результат после одномоментной операции.
В настоящее время среди хирургов нет единодушия в оценке эффективности той или иной техники оперативного лечения КДГК, поэтому сохраняется актуальность поиска новых методов торакопластики, позволяющих получить хорошие косметические и функциональные результаты.
Материал и методы

В ДГКБ №13 им. Н.Ф. Филатова с 1994 по 2009 г. оперирован 91 ребенок с КДГК. Мальчиков было 76 (83,5%), девочек - 15 (16,5%). Все дети оперированы в возрасте 9-15 лет, когда деформация грудной клетки имела выраженный характер (табл. 1).
У всех пациентов КДГК имелась с раннего возраста. Наибольший темп прогрессирования деформации приходился на пубертатный период. К этому времени имел место грубый косметический дефект, что служит основным показанием к оперативному лечению. Мы отмечали грудинохрящевой (корпорокостальный) тип деформации грудной клетки, который характеризовался выступанием нижних реберных хрящей и тела грудины, а также рукояточно-хрящевой (манубриокостальный) тип деформации, характеризовавшийся дислокацией вперед грудины и II-III реберных хрящей, нижние сегменты грудины были смещены кзади.
В каждой группе по форме деформации выделены симметричные и асимметричные варианты. В наших наблюдениях грудинохрящевой тип и симметричные формы КДГК встречались чаще других.
Наследственные заболевания отмечены у 15 (16,5%) детей: синдром Марфана - у 2 (2,2%), марфаноподобный синдром - у 5 (5,5%), синдром Элерса-Данло - у 8 (8,8%). Сопутствующие заболевания выявлены у 35 (40%) детей: бронхиальная астма - у 2 (2,2%), детский церебральный паралич - у 1 (1,1%), уретероцеле - у 1 (1,1%), полителия - у 1 (1,1%), шизофреноподобный синдром - у 1 (1,1%), сколиотическая осанка - у 29 (31,9%). У 33 (36,3%) детей обнаружены изменения со стороны сердечно-сосудистой системы: нарушение сердечного ритма и внутрижелудочковой проводимости (неполная блокада правой ножки пучка Гиса, синдром ранней реполяризации желудочков), пролапс митрального или трикуспидального клапана, ложная хорда желудочка. Нарушения гемодинамики при этом не было ни в одном наблюдении. При выявлении сопутствующих заболеваний дети были консультированы соответствующими специалистами.
Методы хирургического лечения. В нашей клинике при хирургическом лечении КДГК используется торакопластика, в основе которой лежит операция Равича. За указанный период (1994-2009 гг.) торакопластика претерпела существенные изменения. В зависимости от выполненных оперативных вмешательств больных разделили на 2 группы: в 1-ю включены 32 (35,2%) ребенка, оперированных в период 1994-2001 гг., во 2-ю - 59 (64,8%) детей, оперированных в период 2002-2009 гг.
Техника операции в 1-й группе. Для стабилизации грудинореберного комплекса (ГРК) использовали титановую пластину. Для этого на грудной стенке выполняли вертикальный разрез кожи (рис. 1, а) Рисунок 1. Варианты разреза кожи при торакопластике. а - вертикальный; б - субмаммарный; в - «Мерседес»; г - поперечный, длиной не более 8 см. от рукоятки грудины до мечевидного отростка, послойно мобилизовывали кожу с подкожной клетчаткой и грудные мышцы, с двух сторон субперихондриально резецировали реберные хрящи от II до VII, VIII, в месте наибольшей деформации выполняли клиновидную стернотомию с сохранением заднего листка и дополнительно ретростернально устанавливали титановую пластину (рис. 2). Рисунок 2. Рентгенограммы больного. а - до операции; б - после торакопластики с фиксацией ГРК пластиной (техника, использованная в 1994-2001 гг.). Таким способом оперированы 8 (8,8%) детей. Всем им через 6 мес потребовалось повторное оперативное вмешательство для удаления пластины.
С 1996 г. метод торакопластики был изменен, основными ее этапами послужили: использование волнообразного субмаммарного разреза кожи (рис. 1, б) длиной до 12 см или разреза типа «Мерседес» (рис. 1, в); послойное обнажение ГРК, билатеральная субперихондриальная резекция реберных хрящей со II по VIII. При этом не пересекали реберные дуги и не проводили клиновидную стернотомию грудины, как было предложено автором, а отсекали мечевидный отросток и подшивали его на 3-5 см выше, на переднюю поверхность грудины. На оставшуюся в местах удаления хрящей надхрящницу накладывали кетгутовые швы, сморщивая ее в «гармошку». Всего по такой технологии оперированы 24 (26,7%) ребенка.
Техника операции во 2-й группе. С 2002 г. по настоящее время разработан оптимальный метод торакопластики, основными этапами которой являются:
- выполнение на грудной стенке поперечного разреза кожи длиной не более 8 см (рис. 1, г);
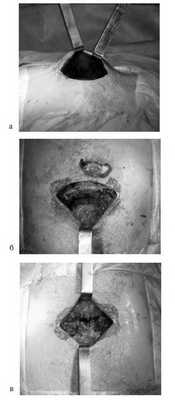
- мобилизация кожи, подкожной клетчатки и грудных мышц единым лоскутом (рис. 3, а); Рисунок 3. Интраоперационные фотографии при торакопластике. а - единый кожно-мышечный лоскут; б - резекция грудины; в - сшивание грудины конец в конец.
- поднахрящничная резекция деформированных реберных хрящей (II-VIII ребра) с двух сторон;
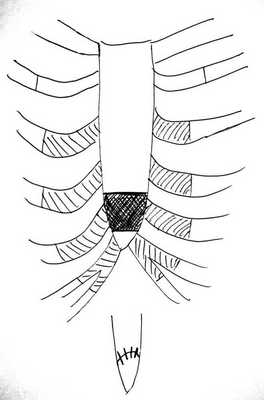
- резекция тела грудины до 2-2,5 см в месте наибольшей деформации и сшивание ее конец в конец отдельными узловыми швами (рис. 3, б, в и 4); Рисунок 4. Схема торакопластики при КДГК (2002-2009 гг.).
- послойное ушивание раны с наложением косметического кожного шва.
По данной технологии оперированы 59 (64,8%) детей. Операцию выполняли под комбинированной общей анестезией в сочетании с эпидуральной анестезией.
Сравнительная оценка методов хирургического лечения КДГК представлена в табл. 2. Отдаленные результаты хирургического лечения в сроки от 6 мес до 1 года оценивали у 11 (12%) детей, от 1,5 до 3 лет - у 30 (33%) детей, от 3 до 5 лет - у 50 (55%) детей. Для оценки полученного косметического результата торакопластики использовали метод анкетирования (табл. 3): отличный результат - полная коррекция деформации, отсутствие остаточных явлений деформации, отсутствие асимметрии грудной клетки (грудная клетка имеет форму, как у здорового ребенка), нормотрофический кожный рубец; хороший результат - полная коррекция килевидной деформации, отсутствие остаточных явлений деформации, отсутствие асимметрии грудной клетки, гипертрофический кожный рубец; удовлетворительный результат - умеренные явления остаточной деформации, умеренная асимметрия грудной клетки, умеренная девиация реберных дуг кпереди или келлоидный кожный рубец; неудовлетворительный результат - рецидив КДГК.
Результаты и обсуждение
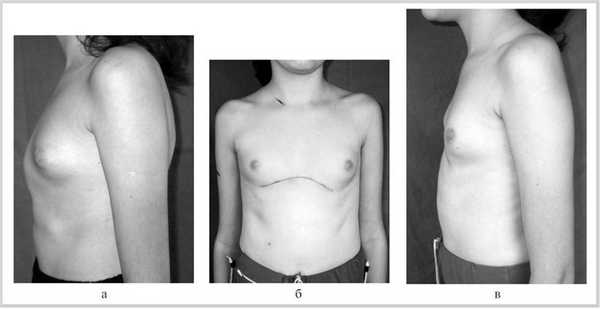
У всех 32 детей в 1-й группе (1994-2001 гг.) после торакопластики полностью ликвидирован косметический дефект. Однако протяженность кожного разреза в послеоперационном периоде не принесла эстетического удовлетворения больным (рис. 5). Рисунок 5. Внешний вид ребенка. а - КДГК до операции; б и в - после торакопластики (1994-2001 гг.).
У 24 (75%) детей этой группы в результате перемещения мечевидного отростка сохранялся выступ в послеоперационном периоде в течение от 6 до 9 мес, что вызывало негативную реакцию, в 8 (25%) наблюдениях потребовалось повторное оперативное вмешательство - удаление фиксирующей металлической пластины.
У 3 (2,2%) детей развились ранние послеоперационные осложнения. У 2 (2,2%) больных на 2-е сутки определялась подкожная гематома мягких тканей. С помощью пункции эвакуировано около 50 мл геморрагической жидкости. Наложена давящая повязка. Рана зажила первичным натяжением. Больные выписаны на 11-е и 14-е сутки. У 1 (1,1%) ребенка на 6-е сутки отмечено расхождение швов послеоперационной раны. Потребовалось наложение вторично-отсроченных швов. Больной выписан на 16-е сутки после операции.
Возникший у 1 /3 больных гемоторакс - довольно частое явление. В наших наблюдениях при контрольном УЗИ плевральных полостей выявлялось в среднем до 100 мл жидкости. Одному ребенку на 4-е сутки в связи с дыхательными расстройствами потребовались плевральная пункция и удаление гемолизированной крови.
Длительность операции составляла от 60 до 110 мин. Продолжительность обезболивания наркотическими анальгетиками в послеоперационном периоде составила в среднем 2-3 дня, ненаркотическими - 5-6 дней. Выписка осуществлялась после полной активизации детей на 13-15-е сутки.
Во 2-й группе (2002-2009 гг.) всего по предложенной методике оперированы 59 (65%) детей. У 98,3% из них полностью устранена деформация. Анкетирование пациентов указывает на отличные и хорошие результаты в 96,6% наблюдений. У подростков исчезло чувство стеснения перед сверстниками, стали преобладать положительные эмоции.
У 2 (3,4%) детей развились осложнения. Раннее осложнение встретилось в 1 (1,7%) наблюдении. На 2-е сутки после оперативного вмешательства возникло расхождение фиксирующих швов грудины. Потребовалась повторная операция - ревизия послеоперационной раны, наложение швов на грудину.
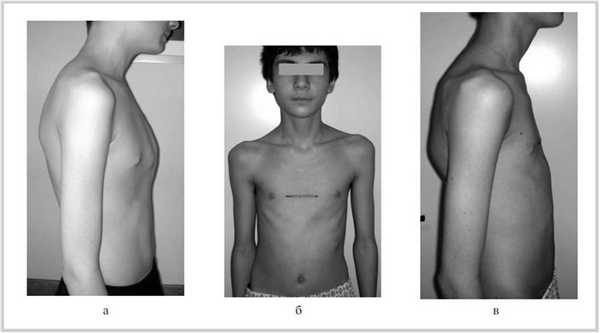
Одному ребенку, которому была выполнена двусторонняя поднадхрящничная резекция только IV, V, VI реберных хрящей, через 6 дней в связи с сохраняющейся деформацией на месте прикрепления третьих ребер потребовалась повторная операция - резекция хрящей третьих ребер, что позволило полностью устранить косметический дефект. Данное обстоятельство не относится к осложнениям, так как не связано с выбором метода оперативного лечения, а обусловлено погрешностью в технике операции. Пациенты осмотрены через 6, 9, 12, 24 мес, отмечен отличный косметический результат (рис. 6). Рисунок 6. Внешний вид ребенка. а - КДГК до операции; б и в - после торакопластики (2002-2009 гг.).
У 59% оперированных выявлен гемоторакс как довольно частое явление после торакопластики. Как правило, к 6-7-м суткам отмечается самостоятельная его регрессия, что подтверждается при проведении контрольного УЗИ или рентгенологического исследования. Лишь в одном наблюдении потребовалась плевральная пункция с эвакуацией около 250 мл геморрагической жидкости.
Позднее осложнение выявлено в 1 (1,7%) наблюдении. Через 8 мес после первой торакопластики была обнаружена локальная костная деформация за счет реберных хрящей, потребовавшая повторного оперативного вмешательства. Резекция хрящей VI-VII ребер справа и хряща VII ребра слева позволила полностью устранить деформацию. Пациент осмотрен через год, отмечен отличный косметический результат. Возникновение рецидива деформации, по-видимому, связано с неправильным, патологическим ростом реберных хрящей этой зоны.
Продолжительность оперативного вмешательства по предложенной методике составила 50-60 мин. Обезболивание наркотическими анальгетиками проводили в течение 2 дней, ненаркотическими - до 4 дней. На 3-4-е сутки больные начинали ходить. Швы снимали на 6-7-е сутки. Пациентов выписывали из стационара на 7-9-е сутки.
Основной принцип пластической хирургии состоит в минимальном хирургическом вмешательстве и получении максимального функционального результата. По данным литературы, вопрос о выборе кожного разреза для проведения торакопластики остается дискуссионным. В наших наблюдениях после использования волнообразных, вертикальных разрезов и разрезов кожи типа «Мерседес» основной жалобой больных был грубый и протяженный послеоперационный рубец. Нелогично устранять один косметический дефект - деформацию грудной клетки и формировать другой - грубые протяженные рубцы на коже. Используемый нами поперечный, протяженностью не более 8 см кожный разрез с отслойкой подкожной жировой клетчатки, фасции и мышц единым лоскутом позволил получить минимально инвазивный доступ для проведения торакопластики и тем самым улучшить эстетический вид больных. Это подтверждается в результате опроса оперированных детей.
Разработанный нами метод торакопластики снижает травматичность хирургического вмешательства, что способствует отказу от применения обезболивания и соответственно ранней активизации больных.
В настоящее время для удержания ГРК в правильном положении предложены методы с использованием и без использования дополнительных фиксаторов. Преимущество нашего метода заключается в одномоментной коррекции КДГК. Больным не требуется повторное оперативное вмешательство - удаление пластины и соответственно исключена вероятность такого осложнения, как смещение фиксатора.
Большинство авторов предложенных методов торакопластики вследствие большой кровопотери в ходе операции применяют различные дренирующие системы. Это приводит к более длительному заживлению послеоперационной раны. В нашем варианте - отслойка подкожной жировой клетчатки, фасции и мышц единым лоскутом, билатеральная резекция только патологически измененных реберных хрящей, резекция малого участка грудины значительно снижают кровопотерю во время оперативного вмешательства и вероятность образования гематом в послеоперационном периоде, мы отказались от использования дополнительных дренирующих систем.
Торакопластика, используемая в нашей клинике с 2002 г., позволила сократить продолжительность операции. В 1-й группе эти показатели хуже, чем во 2-й. Такие же результаты получены и при сравнении средних сроков пребывания в стационаре после операции (1-я группа - 14,0±1,6 сут, 2-я группа - 8,7±1,5 сут). Полученные данные подтверждают экономическую значимость метода торакопластики, примененного во 2-й группе.
Таким образом, поперечный разрез кожи длиной до 8 см и мобилизация кожи, подкожной клетчатки и грудных мышц единым лоскутом создают достаточный операционный доступ для выполнения торакопластики и косметически выгодна для пациента.
Фиксация грудинореберного каркаса после резекции грудины и ее сшивание конец в конец обеспечивают надежное ее удержание в анатомически правильной позиции без использования эндокорректоров и позволяют получить отличный результат.
Торакопластика, применяемая в нашей клинике, менее травматична, дает возможность сократить длительность послеоперационного пребывания больного в стационаре и может быть рекомендована для использования в практике детской хирургии.
1 ФГАОУ ВО «Дальневосточный федеральный университет» (ДВФУ), Медицинский центр, Министерства науки и высшего образования РФ
Ведение пациентов с недостаточной герметичностью после объемной резекции легкого - одна из наиболее распространенных проблем торакальной хирургии. Цель исследования - изучение эффективности корригирующей торакопластики для достижения аэростаза при длительном сбросе воздуха у пациентов с остаточной плевральной полостью после резекции легкого большого объема. Исследованы 22 случая длительного сброса воздуха после резекции легкого большого объема по поводу злокачественных новообразований, которые разделены на группы с активной хирургической тактикой и пролонгированным дренированием. Результаты оценивались по прекращению сброса воздуха, ликвидации остаточной плевральной полости, наличию осложнений и длительности нахождения в стационаре. Длительно сохраняющаяся остаточная плевральная полость, более 1/3 гемиторакса, при неэффективности проводимых мероприятий по достижению аэростаза (смены активной и пассивной аспирации, пневмоперитонеум, химический плевродез), корригировалась 4-реберной экстраплевральной верхнезадней торакопластикой. Проведенное исследование свидетельствует, что в группе с нехирургическими методами аэростаза достижение герметизма легочной ткани наступало спустя четыре недели после вмешательства (р
Читайте также:
- Сочетанные ранения груди и живота
- Антигенная структура дифтерийной палочки. Патогенез поражений дифтерии. Клинические проявления дифтерии. Клиника дифтерии. Признаки дифтерии.
- Пример интрамурального инфаркта миокарда. Пример инфаркта без зубца Q
- Глупо улыбаетесь, когда вас обвиняют? Улыбка
- Примеры профессиональных невритов и плекситов: течение, прогноз
