Эффективность применения лейкоцитарного концентрата. Прямое переливание крови
Добавил пользователь Владимир З. Обновлено: 22.01.2026
Посттрансфузионное увеличение, являющееся традиционным методом оценки эффективности переливания компонентов крови, для переливания лейкоцитов не является адекватным, т.к. перелитые лейкоциты быстро покидают сосудистое русло и мигрируют в очаг воспаления. Поэтому лучшим показателем терапевтической эффективности перелитых лейкоцитов является динамика клинической картины: снижение температуры тела, уменьшение интоксикации и физикальных проявлений воспаления, улучшение рентгенологической картины в легких при наличии пневмонии, стабилизация ранее нарушенных органных функций.
10.5. Профилактические трансфузии лейкоцитного концентрата
Переливание лейкоцитов с профилактической целью реципиентам, имеющим гранулоцитопению без признаков инфекции, не находит применения, т.к. побочные результаты превосходят ожидаемый положительный результат.
10.6. Побочные реакции при переливании лейкоцитного концентрата
Переливание лейкоцитов может сопровождаться развитием патологических явлений со стороны легких или выраженной фебрильной реакцией.
Температурная реакция, нередко с ознобом, как правило, средней тяжести, обусловлена связыванием лейкоцитов донора антителами реципиента с последующей дегрануляцией гранулоцитов и активацией комплемента. Предупреждать эти явления можно путем назначения кортикостероидов, замедления скорости инфузии, введения промедола для купирования озноба. Если эти лечебные мероприятия не достигают эффекта, в дальнейшем использование лейкоцитарного концентрата противопоказано. Иногда гипертермия сопровождается развитием одышки и гипотонии, что требует немедленного прекращения переливания, введения больших доз преднизолона, при его неэффективности вазопрессоров.
Симптомами побочных реакций со стороны легких при переливании лейкоцитов являются пароксизму кашля, инспираторная одышка, гипертермия. Чаще подобные реакции наблюдаются у больных с инфекционной патологией в легких. Причинами этих реакций могут быть:
1) волемическая перегрузка при выраженной сердечной недостаточности (в терапии эффективны диуретики);
2) уплотнение альвеолярной мембраны донорскими гранулоцитами, которые локализуются в пневмоническом очаге;
3) эндотоксинемия, наблюдаемая при септицемии, может вызвать дегрануляцию донорских лейкоцитов, активацию комплемента и легочные нарушения.
11. Посттрансфузионные осложнения
Переливание компонентов крови является потенциально опасным способом коррекции и замещения их дефицита у реципиента. Осложнения после трансфузии, ранее объединяемые термином "трансфузионные реакции", могут быть обусловлены самыми различными причинами и наблюдаться в разные сроки после переливания. Одни из них могут быть предупреждены, другие - нет, но в любом случае медицинский персонал, проводящий трансфузионную терапию компонентами крови, обязан знать возможные осложнения, уведомлять пациента о возможности их развития, уметь их предупреждать и лечить.
11.1. Непосредственные и отдаленные осложнения переливания компонентов крови
Осложнения от переливания компонентов крови могут развиваться как во время и в ближайшее время после трансфузии (непосредственные осложнения), так и спустя большой период времени - несколько месяцев, а при повторных трансфузиях и лет после трансфузии (отдаленные осложнения). Основные виды осложнений представлены в таблице 3.
Групповая несовместимость эритроцитов донора и реципиента
Гипертермическая негемолитическая реакция
Гранулоциты донора в переливаемой среде
Антитела класса IgA
Антитела к белкам плазмы
Некардиогенный отек легких
Антитела к лейкоцитам или активация комплемента
Разрушение эритроцитов донора вследствие нарушения температурного режима хранения или сроков хранения, подготовки к переливанию, смешивания с гипотоничным раствором
Бактериальное инфицирование переливаемой среды
Острая сердечно-сосудистая недостаточность, отек легких
Повторные трансфузии с образованием антител к антигенам эритроцитов
Реакция "трансплантат против хозяина"
Переливание стволовых клеток необлученных
Развитие антитромбоцитарных антител
Аллоиммунизация антигенами эритроцитов, лейкоцитов, тромбоцитов или плазменными белками
Действие антигенов донорского происхождения
Перегрузка железом - гемосидероз органов
Многочисленные переливания эритроцитов
Чаще вирус С, реже - В, очень редко А
Синдром приобретенного иммунодефицита
Вирус иммунодефицита человека
11.1.1. Острый гемолиз.Время между подозрением на гемолитическое посттрансфузионное осложнение, его диагностикой и началом терапевтических мероприятий должно быть, по возможности, коротким, ибо от этого зависит тяжесть последующих проявлений гемолиза. Острый иммунный гемолиз является одним из основных осложнений эритроцитсодержащих гемотрансфузионных сред, зачастую тяжелых.
В основе острого посттрансфузионного гемолиза лежит взаимодействие антител реципиента с антигенами донора, в результате которого происходит активация системы комплемента, системы свертывания и гуморального иммунитета. Клинические проявления гемолиза обусловлены развивающимся острым ДВС, циркуляторным шоком и острой почечной недостаточностью.
Наиболее тяжело острый гемолиз протекает при несовместимости по системе АВО и резус. Несовместимость по другим группам антигенов также может быть причиной гемолиза у реципиента, особенно если стимуляция аллоантител происходит вследствие повторных беременностей или предыдущих трансфузий. Поэтому важен подбор доноров по пробе Кумбса.
Начальные клинические признаки острого гемолиза могут появиться непосредственно во время переливания или вскоре после него. Ими являются боли в груди, животе или пояснице, чувство жара, кратковременное возбуждение. В дальнейшем появляются признаки циркуляторных нарушений (тахикардия, артериальная гипотония). В крови обнаруживаются разнонаправленные сдвиги в системе гемостаза (повышение уровня продуктов паракоагуляции, тромбоцитопения, снижение антикоагулянтного потенциала и фибринолиза), признаки внутрисосудистого гемолиза - гемоглобинемия, билирубинемия, в моче - гемоглобинурия, позже - признаки нарушения функции почек и печени - повышение уровня креатинина и мочевины в крови, гиперкалиемия, снижение почасового диуреза вплоть до анурии. Если острый гемолиз развивается во время операций, проводимой под общим обезболиванием, то клиническими признаками его могут быть немотивированная кровоточивость операционной раны, сопровождаемая стойкой гипотонией, а при наличии катетера в мочевом пузыре - появление мочи темно-вишневого или черного цвета.
Терапия острого гемолиза предусматривает немедленное прекращение переливания эритроцитсодержащей среды (с обязательным сохранением этой трансфузионной среды) и одновременное начало интенсивной инфузионной терапии (иногда в две вены) под контролем центрального венозного давления. Переливание солевых растворов и коллоидов (оптимально - альбумина) проводится с целью не допустить гиповолемии и гипоперфузии почек, плазмы свежезамороженной - для коррекции ДВС. При отсутствии анурии и восстановленном объеме циркулирующей крови для стимуляции диуреза и уменьшения осаждения продуктов гемолиза в дистальных канальцах нефронов назначают осмодиуретики (20% раствор маннитола из расчета 0,5 г/кг массы тела) или фуросемид в дозе 4-6 мг/кг массы тела. При положительном ответе на назначение диуретинов тактика форсированного диуреза продолжается. Одновременно показано проведение экстренного плазмафереза в объеме не менее 1,5 л с целью удаления из циркуляции свободного гемоглобина, продуктов деградации фибриногена с обязательным возмещением удаляемой плазмы переливанием плазмы свежезамороженной. Параллельно с этими терапевтическими мероприятиями необходимо назначение гепарина под контролем АЧТВ и показателей коагулограммы. Оптимальным является внутривенное введение гепарина по 1000 ЕД в час с помощью дозатора лекарственных веществ (инфузомата).
Иммунная природа острого гемолиза посттрансфузионного шока требует назначения в первые часы терапии этого состояния внутривенно преднизолона в дозе 3-5 мг/кг массы тела. Если возникает необходимость коррекции глубокой анемии (гемоглобин менее 60 г/л), осуществляют переливание индивидуально подобранной эритроцитной взвеси с физиологическим раствором. Назначение допамина в малых дозах (до 5 мкг/кг массы тела в мин) усиливает почечный кровоток и способствует более успешному лечению острого гемотрансфузионного гемолитического шока.
В тех случаях, когда комплексная консервативная терапия не предотвращает наступления острой почечной недостаточности и у больного анурия продолжается более суток, или выявляется уремия и гиперкалиемия, показано применение экстренного гемодиализа (гемодиафильтрации).
11.1.2. Отсроченные гемолитические реакции. Отсроченные гемолитические реакции могут возникнуть спустя несколько дней после переливания переносчиков газов крови в результате иммунизации реципиента предшествующими трансфузиями. Образующиеся de novo антитела появляются в русле крови реципиента через 10-14 дней после переливания. Если очередная трансфузия переносчиков газов крови совпала с началом антителообразования, то появляющиеся антитела могут вступать в реакцию с циркулирующими в русле крови реципиента эритроцитами донора. Гемолиз эритроцитов в этом случае выражен не резко, может быть заподозрен по снижению уровни гемоглобина и появлению антиэритроцитарных антител. В целом отсроченные гемолитические реакции наблюдаются редко и поэтому сравнительно мало изучены. Специфического лечения обычно не требуется, но необходим контроль за функцией почек.
11.1.3. Бактериальный шок. Основной причиной пирогенных реакций вплоть до развития бактериального шока является попадание эндотоксина бактерий в трансфузионную среду, что может произойти при пункции вены/подготовке крови к переливанию или в процессе хранения консервированной крови при несоблюдении правил консервации и температурного режима. Риск бактериальной контаминации возрастает по мере увеличения срока хранения компонентов крови.
Клиническая картина при переливании бактериально загрязненной трансфузионной среды напоминает таковую при септическом шоке. Наблюдается резкое повышение температуры тела, выраженная гиперемия верхней половины туловища, быстрое развитие гипотонии, появление озноба, тошноты, рвоты, диареи, болей в мышцах.
При выявлении подозрительных на бактериальную контаминацию клинических признаков необходимо немедленно прекратить переливание. Исследованию на наличие бактерий подлежат кровь реципиента, подозреваемая трансфузионная среда, а также все другие переливаемые внутривенно растворы. Исследование необходимо проводить как на аэробную инфекцию, так и на анаэробную, желательно с использованием аппаратуры, обеспечивающей экспресс-диагностику.
Терапия включает немедленное назначение антибиотиков широкого спектра действия, проведение противошоковых мероприятий с обязательным применением вазопрессоров и/или инотропных средств с целью быстрой нормализации артериального давления, коррекцию нарушений гемостаза (ДВС).
Предупреждение бактериальной контаминации при трансфузиях компонентов крови заключается в использовании аппаратуры одноразового применения, тщательном соблюдении правил асептики при пункции вены и пластикатного контейнера, постоянном контроле температурного режима и сроков хранения компонентов крови, визуальном контроле компонентов крови перед их переливанием.
11.1.4. Реакции, обусловленные антилейкоцитными антителами.Негемолитические фебрильные реакции, наблюдаемые во время переливания или непосредственно после его окончания, характеризуются повышением температуры тела реципиента на 1С или более. Подобные фебрильные реакции являются следствием наличия в плазме крови реципиента цитотоксических или агглютинирующих антител, вступающих в реакцию с антигенами, находящимися на мембране переливаемых лимфоцитов, гранулоцитов или тромбоцитов, Переливание эритроцитной массы, обедненной лейкоцитами и тромбоцитами, существенно снижает частоту развития фебрильных негемолитических реакций. Значительно повышает безопасность трансфузионной терапии использование лейкоцитарных фильтров.
Негемолитические фебрильные реакции чаще наблюдаются при повторных переливаниях или у женщин, имевших много беременностей. Назначение жаропонижающих средств обычно купирует фебрильную реакцию.
Однако следует отметить, что повышение температуры тела, связанное с переливанием, нередко может являться первым признаком таких более опасных осложнений, как острый гемолиз или бактериальная контаминация. Диагноз фебрильной негемолитической реакции следует ставить методом исключения, предварительно исключив другие возможные причины повышения температуры тела в ответ на трансфузию крови или ее компонентов.
11.1.5. Анафилактический шок. Характерными отличительными чертами анафилактического шока, обусловленного переливанием крови или ее компонентов, являются развитие его немедленно после введения нескольких миллилитров крови или ее компонентов и отсутствие повышения температуры тела. В дальнейшем могут наблюдаться такие симптомы, как непродуктивный кашель, бронхоспазм, одышка, тенденция к гипотонии, спазматические боли в животе, тошнота и рвота, расстройство стула, потеря сознания. Причиной анафилактического шока в данных обстоятельствах является дефицит IgA у реципиентов и образование у них анти-IgA антител после ранее проведенных переливаний или перенесенных беременностей, но нередко иммунизирующий агент не может быть четко верифицирован. Хотя дефицит IgA встречается с частотой 1 на 700 человек, частота анафилактического шока по этой причине существенно реже, что обусловлено наличием антител различной специфичности.
Терапия анафилактической трансфузионной реакции у взрослых реципиентов включает прекращение переливания, немедленное введение адреналина под кожу, внутривенную инфузию физиологического раствора, назначение 100 мг преднизолона или гидрокортизона внутривенно.
При наличии осложненного трансфузиологического анамнеза и подозрении на дефицит IgA возможно использование предоперационно заготовленных аутологичных компонентов крови. При отсутствии такой возможности используют только размороженные отмытые эритроциты.
11.1.6. Острая волемическая перегрузка. Быстрое повышение систолического артериального давления, одышка, сильная головная боль, кашель, цианоз, ортопноэ, появление затрудненного дыхания или отека легких, во время или сразу после переливания, могут свидетельствовать о гиперволемии, обусловленной резким повышением объема циркулирующей крови вследствие трансфузии компонентов крови или коллоидов типа альбумина. Быстрое повышение объема крови в циркуляции плохо переносится больными с заболеваниями сердца, легких и при наличии хронической анемии, когда отмечается увеличение объема циркулирующей плазмы. Трансфузии даже небольших объемов, но с большой скоростью, могут быть причиной сосудистой перегрузки у новорожденных.
Прекращение трансфузии, перевод больного в сидячее положение, дача кислорода и мочегонных быстро купируют эти явления. Если же признаки гиперволемии не проходят, возникают показания к экстренному плазмаферезу. При склонности больных к волемическим перегрузкам в трансфузионной практике необходимо использовать медленное введение: скорость переливания - 1 мл/кг массы тела в час. При необходимости переливания больших объемов плазмы показано назначение диуретиков перед переливанием.
11.1.7. Трансмиссивные инфекции, передающиеся при переливании компонентов крови. Наиболее частым инфекционным заболеванием, осложняющим переливание компонентов крови, является гепатит. Передача гепатита А наблюдается крайне редко, т.к. при этом заболевании период виремии очень, короток. Риск передачи гепатита В и С остается высоким, имеющим тенденцию к снижению благодаря тестированию доноров на носительство HbsAg, определению уровня ALT и анти-НВs антител. Самоанкетирование доноров также помогает повысить безопасность трансфузий.
Все компоненты крови, не подвергающиеся вирусной инактивации, несут в себе риск передачи гепатита. Отсутствие в настоящее время надежных гарантированных тестов на носительство антигенов гепатита В и С делает необходимым посеянный скрининг всех доноров компонентов крови по вышеназванным тестам, а также внедрение карантизации плазмы. Следует отметить, что безвозмездные доноры несут меньший риск трансфузионной передачи вирусных инфекций по сравнению с платными донорами.
Цитомегаловирусная инфекция, обусловленная трансфузией компонентов крови, наиболее часто наблюдается у пациентов, подвергшихся иммуносупрессии, прежде всего - у больных после пересадки костного мозга или у больных, получающих цитостатическую терапию. Известно, что цитомегаловирус передается с лейкоцитами периферической крови, поэтому и в этом случае использование лейкоцитарных фильтров при переливании эритроцитов и тромбоцитов будет способствовать существенному снижению риска развития цитомегаловирусной инфекции у реципиентов. В настоящее время нет достоверных тестов для определения носительства цитомегаловируса, но установлено, что в общей популяции его носительство составляет 6-12%.
Передача вируса иммунодефицита человека трансфузионным путем составляет около 2% всех случаев синдрома приобретенного иммунодефицита. Скрининг доноров на наличие антител к вирусу иммунодефицита человека существенно снижает риск передачи этой вирусной инфекции. Однако наличие длительного периода образования специфических антител после заражения (6-12 недель) делает практически невозможным полное исключение риска передачи ВИЧ. Поэтому для предупреждения вирусных инфекций, передающихся трансфузионным путем, необходимо соблюдение следующих правил:
переливания крови и ее компонентов должны производиться только по жизненным показаниям;
тотальный лабораторный скрининг доноров и их селекция, отвод доноров из групп риска, преимущественное использование безвозмездного донорства, самоанкетирование доноров снижают риск передачи вирусных инфекций;
более широкое использование аутодонорства, карантинизации плазмы, реинфузии крови также повышают вирусную безопасность трансфузионной терапии.
Переливание лейкоцитарной массы
Лейкоцитарная масса — препарат крови, который получают путем пропускания через особый фильтр в виде ионообменных сред, после чего примешивают специальный консервант. Таким образом добиваются отделения лейкоцитов от других форменных элементов.
Применение лейкоцитарной массы
Лейкоцитарная масса применяется в случаях, когда собственных лейкоцитов в крови очень мало и высок риск инфекционных осложнений.
Чаще всего такое лечение назначается крайне ослабленным пациентам, при тяжелом сепсисе, лучевой болезни, а также при состояниях, когда имеет место подавление функции костного мозга, в частности, при проведении химиотерапии у пациентов с онкологической патологией.
Лейкоцитарные концентраты
Сегодня в онкологии используются так называемые лейкоцитные концентраты, которые применяются в свежезаготовленном виде, со сроком хранения не более суток. В состав лейкоцитарной массы также могут входить эритроциты, тромбоциты.
Для инактивации лимфоцитов крови лейкоцитарную массу подвергают воздействию гамма-облучения.
Колониестимулирующие факторы
В настоящее время все чаще вместо классической лейкоцитарной массы используются так называемые колониестимулирующие факторы — Г-КСФ и ГМ-КСФ. Эти препараты основаны на особом белке, который стимулирует синтез белых клеток крови в костном мозге.
Назначение колониестимулирующих факторов
Колониестимулирующие факторы способствуют созреванию и выходу гранулоцитов (лейкоцитов) из костного мозга в кровоток. Эти препараты могут использоваться в сочетании с другими препаратами крови, а также со стволовыми клетками.
Показания к переливанию лейкоцитарной массы
Перед введением любых препаратов крови, в том числе лейкоцитного концентрата, пациенту проводится биологическая и индивидуальная проба на переносимость и совместимость данного препарата.
Преимущества Европейского онкологического госпиталя
В Европейской онкологической клинике сегодня используются современные методы лечения пациентов с выраженным подавлением функций костного мозга после химиотерапии, включая лейкоцитарную массу и препараты колониестимулирующих факторов.
Препараты крови
Физиологи неслучайно называют кровь внутренней средой организма. Она взаимодействует со всеми органами, выполняет многие жизненно важные функции. Иногда у онкологических больных эти функции нарушаются. Причины бывают разными: непосредственно злокачественная опухоль, побочные эффекты препаратов, серьезные хирургические вмешательства, кровотечения, тяжелые сопутствующие заболевания, поражения красного костного мозга. Если проблему не удается решить с помощью медикаментозных препаратов, пациенту показано переливание компонентов крови.
Кровь имеет сложный состав. Ее жидкая часть — плазма — представляет собой «коктейль» из электролитов, альбумина, глюкозы, ферментов, антител, факторов свертывания и других веществ. В этом растворе плавают клетки (форменные элементы) крови: эритроциты доставляют к тканям кислород и уносят углекислый газ, лейкоциты обеспечивают защиту организма, тромбоциты помогают останавливать кровотечения.
Чаще всего больному не нужны все эти компоненты сразу. Например, при иммунодефиците требуются только лейкоциты, при анемии — эритроциты. Поэтому цельную кровь в настоящее время переливают редко. Обычно ее использование — крайняя мера, когда у больного одновременно снижен объем крови и количество эритроцитов, и нет в наличии заменителей плазмы и компонентов крови.
Эритроциты (эритроцитарная масса)
1. Эритроцитарная масса
Что это такое? Эритроцитарную массу получают, удаляя из крови часть плазмы с помощью центрифуги. В препарате сохраняются практически все эритроциты, частично — лейкоциты и тромбоциты, их количество зависит от метода центрифугирования. Средний объем одной порции составляет 280 мл, гематокрит (соотношение объема форменных элементов и плазмы) — 0,65-0,75, содержание гемоглобина — 45 г на дозу и более.
В каких случаях применяют? При острой и хронической кровопотере, анемии, вызванных разными причинами:
- Острые и хронические кровотечения, в том числе большая кровопотеря во время операции.
- Нарушение кроветворения из-за злокачественной опухоли, поражения красного костного мозга (например, при лейкозах), побочных эффектов лучевой терапии, химиотерапии.
- Гемолиз — разрушение эритроцитов в кровеносном русле.
- Тяжелая железодефицитная анемия.
- Интоксикации, тяжелые инфекции.
- Тяжелые нарушения работы пищеварительной системы.
Переливание эритроцитарной массы при острых кровопотерях проводят, когда в крови пациента сильно падает уровень гемоглобина и возникают такие симптомы, как одышка, бледность кожи и слизистых оболочек, учащенное сердцебиение. При хронической кровопотере показаниями являются уровень гемоглобина ниже 80 г/л и гематокрит ниже 0,25.
2. Эритроциты с удаленным лейкотромбоцитарным слоем
Что это такое? Это та же эритроцитарная масса, только более «чистая», из нее удалено 20-60 мл лейкотромбоцитарного слоя. Средний размер порции — 250 мл. Содержание лейкоцитов в ней не превышает 1,2×109, тромбоцитов — 20×109. Гематокрит 0,65-0,75, содержание гемоглобина не менее 43 граммов на порцию.
В каких случаях применяют? Показания те же, что и для переливания обычной эритроцитарной массы, но есть некоторые особенности. Эритроциты с удаленным лейкотромбоцитарным слоем реже вызывают некоторые осложнения после трансфузии, поэтому они более предпочтительны для пациентов, у которых ранее такие осложнения возникали. При повторных переливаниях ниже риск сенсибилизации организма к лейкоцитарным антигенам, заражения цитомегаловирусной инфекцией.
3. Эритроцитарная взвесь
Что это такое? Эритроцитарная масса, из которой удалена плазма, вместо нее добавлен взвешивающий раствор. Чаще всего в его состав входят растворенные в воде хлорид натрия, маннитол, глюкоза и аденин. Гематокрит эритроцитарной взвеси 0,5-0,7. В одной порции должно содержаться не менее 45 г гемоглобина. Существует также эритроцитарная взвесь с удаленным лейкотромбоцитарным слоем.
В каких случаях применяют? Показания те же, что и для эритроцитарной массы. За счет разных сочетаний антикоагулянтов и взвешивающего раствора, срок хранения препарата может быть увеличен.
4. Отмытые эритроциты
Что это такое? Эритроциты, максимально очищенные от лейкоцитов, тромбоцитов и компонентов плазмы. Сначала готовят эритроцитарную массу и очищают ее от лейкоцитов, тромбоцитов, плазмы. Затем красные кровяные тельца обрабатывают изотоническим раствором при температуре +4 градуса. Гематокрит препарата может различаться, обычно составляет от 0,65 до 0,75. В порции должно содержаться не менее 40 граммов гемоглобина.
В каких случаях применяют? Переливание отмытых эритроцитов показано в тех же случаях, что и эритроцитарной массы, если у больного имеется одно из следующих состояний:
- Посттрансфузионные осложнения (кроме гемолиза — разрушения эритроцитов) после предыдущих переливаний компонентов крови.
- Сенсибилизация (повышенная чувствительность) к антигенам лейкоцитов и тромбоцитов, белков плазмы и тканевым антигенам.
- Синдром массивных трансфузий — осложнение, которое развивается в результате того, что в организм пациента вместе с кровекомпонентами попадает много цитрата (консервант крови) и токсичных веществ, накапливающихся в препарате за время хранения.
- Тяжелая анемия в сочетании с почечной и печеночной недостаточностью.
- Антитела к иммуноглобулину A в плазме.
- Пароксизмальная ночная гемоглобинурия — редкая патология, при которой разрушаются эритроциты, и в моче появляется гемоглобин.
5. Эритроциты, обедненные лейкоцитами
Что это такое? Эритроцитарная масса, из которой максимально удалены лейкоциты. В ней должно содержаться не более 1×106 лейкоцитов и не менее 40 граммов гемоглобина на одну порцию.
В каких случаях применяют? Эритроциты, обедненные лейкоцитами, переливают пациентам вместо обычной эритроцитарной массы, когда нужно:
- Избежать осложнений из-за присутствия антилейкоцитарных антител в организме реципиента.
- Предотвратить развитие иммунного ответа против антигенов лейкоцитов при многократных трансфузиях.
- Предотвратить заражение цитомегаловирусной инфекцией.
6. Криоконсервированные эритроциты
Что это такое? Эритроциты, которые были заморожены в течение недели после получения от донора и хранятся при температуре минус 60-80 градусов. Перед переливанием их размораживают, отмывают и разбавляют в изотоническом растворе или специальном взвешивающем растворе. Объем порции препарата должен составлять не менее 185 мл, в ней должно содержаться не менее 36 граммов гемоглобина, гематокрит — 0,65-0,75. Если поддерживать нужную температуру, криоконсервированные эритроциты можно хранить, по крайней мере, 10 лет.
В каких случаях применяют? Заморозка и хранение эритроцитов обходятся дорого, поэтому данный препарат крови применяют только в крайних случаях:
- Если у пациента редкая группа крови и много антител, из-за которых кровь большинства доноров не подходит.
- Если нужна эритроцитарная масса, не опасная в плане заражения цитомегаловирусами, и нет возможности получить ее другим способом.
- Иногда можно заготовить для переливания заранее собственную кровь пациента — то есть провести аутотрансфузию.
7. Эритроциты, полученные методом афереза
Что это такое? Эритроциты — отдельно или в сочетании с другими компонентами крови — выделяют из крови донора, которую пропускают через специальный аппарат для афереза. Всё, что осталось, возвращают в организм донора. К полученным эритроцитам добавляют специальный раствор. Объем порции и гематокрит могут различаться, содержание гемоглобина должно быть не менее 40 граммов на порцию.
В каких случаях применяют? Показания те же, что и для эритроцитарной массы.
Тромбоциты (тромбоцитарная масса, тромбоконцентрат)
1. Восстановленные тромбоциты
Что это такое? Препарат, который получают из цельной крови. Он содержит большую часть тромбоцитов: 45—85×109 на 50-60 мл ресуспендирующей среды, некоторое количество лейкоцитов (0,05—1×109) и эритроцитов (0,2 —1×109). «Стандартная» порция для взрослого человека включает количество тромбоцитов, полученных из 4-6 доз цельной крови.
В каких случаях применяют? Основные показания к переливанию восстановленных тромбоцитов:
- Для профилактики кровотечений, если уровень тромбоцитов в крови пациента снижен менее 10 000/мкл.
- Для профилактики кровотечений, если пациенту планируется установить центральный венозный катетер, при плазменном нарушении свертываемости крови и сепсисе — при уровне тромбоцитов ниже 20 000/мкл.
- Для профилактики кровотечений, если планируется диагностическая люмбальная пункция в плановом порядке, хирургическое вмешательство — при уровне тромбоцитов ниже 50 000/мкл.
- Для профилактики кровотечений, если необходимо установить или удалить эпидуральный катетер — при уровне тромбоцитов ниже 80 000/мкл.
- Для профилактики кровотечений, если планируется хирургическое вмешательство на центральной нервной системе — при уровне тромбоцитов ниже 100 000/мкл.
- При уровне тромбоцитов ниже 30 000/мкл и длительном носовом кровотечении, кровавой рвоте, черном дегтеобразном стуле из-за примесей крови (мелена).
- При уровне тромбоцитов ниже 50 000/мкл, если имеется сильное кровотечение, сопровождающееся нарушением циркуляции крови, сильное внутреннее кровотечение, нарушающее функции внутренних органов.
- При уровне тромбоцитов ниже 100 000/мкл и кровотечениях в центральной нервной системе, глазном яблоке.
- После массивных переливаний других кровекомпонентов, когда из-за сильного разбавления крови в ней снижается количество тромбоцитов.
2. Тромбоциты, полученные методом афереза
Что это такое? Тромбоконцентрат, полученный путем «очищения» крови донора с помощью аппарата для афереза (сепаратора клеток). За одну процедуру от одного донора получают 200—800×109 тромбоцитов. Препарат содержит также некоторое количество лейкоцитов и эритроцитов. Оставшиеся компоненты крови возвращают в организм донора.
В каких случаях применяют? Показания аналогичны таковым для переливания обычной тромбоцитарной массы. Тромбоциты, полученные методом афереза, предпочтительны для пациентов с антителами анти-HLA, анти-НРА.
3. Тромбоциты, обеднённые лейкоцитами
Что это такое? Это тромбоцитарная масса или тромбоциты, полученные методом афереза, максимально очищенные от лейкоцитов.
В каких случаях применяют? Данный препарат крови применяется по тем же показаниям, что и тромбомасса, в следующих случаях:
- При многократных переливаниях тромбоцитов.
- Если у пациента планируется трансплантация стволовых клеток красного костного мозга.
- Если нужно избежать заражения цитомегаловирусной инфекцией у пациентов с иммунодефицитом или после трансплантации органов.
4. Отмытые тромбоциты
Что это такое? Тромбоциты, которые максимально очищены от плазмы крови и находятся в физиологическом растворе.
- Если у пациента имеются антитела к белкам плазмы, особенно иммуноглобулину A.
- Если у пациента возникают тяжелые аллергические реакции после переливания препаратов крови.
5. Криоконсервированные тромбоциты
Что это такое? Тромбоциты, полученные методом афереза и замороженные с добавлением специальных веществ — криопротекторов. Заморозку нужно выполнить в течение 24 часов после того, как тромбоциты получены от донора. Их хранят при температуре минус 80-150 градусов.
В каких случаях применяют? Показания те же, что и для переливания тромбомассы. Тромбоциты замораживают главным образом для того, чтобы иметь при необходимости под рукой препарат, совместимый с реципиентом по HLA и/или HPA.
Лейкоциты (лейкоцитарная масса)
Гранулоциты, полученные методом афереза
Что это такое? Гранулоциты — разновидность лейкоцитов, которые получили свое название за то, что при изучении под микроскопом в них обнаруживают гранулы. Это все те клетки, которые защищают организм от инфекций и не относятся к лимфоцитам. Их основная функция — фагоцитоз, они «заглатывают» и уничтожают чужеродные агенты, попавшие в организм. Объем порции препарата составляет не более 500 мл, в ней должно содержаться не менее 10×109 гранулоцитов. Получают препарат методом афереза.
В каких случаях применяют? Переливания лейкоцитарной массы необходимы при инфекционных осложнениях, таких как сепсис, некротическая энтеропатия, пневмония, если лечение антибиотиками не приносит эффекта, и уровень гранулоцитов в крови пациента ниже 0,75×109/л.
Свежезамороженная плазма
Что это такое? Плазма — жидкая часть крови. Ее получают из цельной крови методом центрифугирования либо путем плазмафереза. В ней содержатся: альбумин, иммуноглобулины, факторы свертывания крови. Готовый препарат замораживают и хранят при температуре минус 18-25 градусов в течение 3 месяцев или ниже минус 25 градусов в течение 12 месяцев. Заморозка помогает сохранить в рабочем состоянии факторы свертывания крови.
В каких случаях применяют? Свежезамороженную плазму переливают, когда в крови пациента не хватает факторов свертывания крови. Основные показания:
- Заболевания печени.
- Дефицит витамина K.
- Передозировка некоторых антикоагулянтов — препаратов для снижения свертываемости крови.
- Синдром диссеминированного внутрисосудистого свертывания крови.
- Нарушение свертываемости в результате переливаний, сильного разбавления крови.
- Наследственная нехватка факторов свертывания крови.
- Тромботическая и тромбоцитопеническая пурпура.
- Гемолитико-уремический синдром.
Криопреципитат
Что это такое? Криопреципитатом называют белки-криоглобулины, которые выпадают в осадок и образуют гель, когда свежезамороженная донорская плазма оттаивает в определенном режиме. Криопреципитат бывает замороженным, в виде массы желтого цвета, и высушенным, в виде порошка для растворения в воде.
В каких случаях применяют? Препарат содержит факторы свертывания крови. Его применяют при гемофилии, диссеминированном внутрисосудистом свертывании и некоторых других патологиях.
«Евроонко» сотрудничает с одним из крупнейших банков донорской крови в России. Мы проводим переливания препаратов крови на основе лицензии на «трансфузиологию в амбулаторных и стационарных условиях», которую нашей клинике выдал Департамент здравоохранения Москвы. У нас есть всё необходимое, чтобы выполнить трансфузию максимально оперативно, с соблюдением современных стандартов и рекомендаций.
Как быстро поднять количество лейкоцитов после химиотерапии?
Снижение уровня лейкоцитов в крови, или лейкопения - один из наиболее серьезных побочных эффектов химиотерапии. Многие онкологические пациенты наслышаны о нем, и сильно его боятся. «Можно ли быстро, за 3 дня, поднять уровень лейкоцитов после лечения, и если можно - как это сделать?» - такой вопрос часто приходится слышать врачам-онкологам, и это довольно распространенный запрос в поисковых системах в интернете. Можно встретить немало рекомендаций о том, как повысить лейкоциты после курса лечения, в том числе из области народной, нетрадиционной медицины. Мы постараемся максимально подробно ответить на этот вопрос с профессиональной точки зрения.
Лейкопения - что это такое и чем опасна?
В организме человека есть несколько разных видов лейкоцитов: нейтрофилы, базофилы, эозинофилы, моноциты, T- и B-лимфоциты, натуральные киллеры. Все эти виды лейкоцитов объединены общей функцией: эти клетки защищают организм человека от возбудителей инфекций и других чужеродных агентов. Таким образом, закономерным следствием лейкопении является развитие иммунодефицита и риск опасных инфекций. Организм становится беззащитен перед бактериями и вирусами, которые окружают нас буквально повсюду.
В итоге даже банальная ОРВИ, которая протекает легко у большинства людей, у человека с ослабленной иммунной системой способна привести к тяжелым последствиям. Некоторые относительно безвредные микроорганизмы, которые находятся в составе естественной микрофлоры тела, при снижении иммунитета тоже могут активироваться и начать вести себя агрессивно.
Количество лейкоцитов оценивают с помощью общего анализа крови. Помимо их общего числа, можно подсчитать лейкоцитарную формулу - уровни и процентное соотношение разных типов, а также число зрелых и юных форм. Все эти показатели имеют клиническое значение и важны в определенных случаях.
Лейкопения - состояние, имеющее четкие лабораторные критерии. Ее диагностируют, когда уровень лейкоцитов в крови опускается ниже 4000 клеток в 1 мкл или ниже 4×109/л. Можно выделить четыре степени тяжести этого состояния, они представлены в таблице ниже.
| Степень лейкопении | Уровень лейкоцитов в крови, 10 9 /л |
| Легкая - 1 степень | 4 - 3 |
| Средней тяжести - 2 степень | 3 - 2 |
| Тяжелая - 3 степень | 2 - 1 |
| Агранулоцитоз (снижение происходит за счет гранулоцитов и моноцитов) - 4 степень |
Кроме того, выделяют разновидности лейкопении, в зависимости от того, количество каких именно лейкоцитов снизилось:
- Нейтропения - снижение уровня нейтрофилов менее 1200-1500/мкл. Этот вид лейкоцитов обеспечивает врожденный иммунитет, и именно они в первую очередь участвуют в развитии воспаления. Они «пожирают» патогенные микроорганизмы, а также фрагменты разрушенных клеток.
- Лимфопения - снижение уровня лимфоцитов менее 1000/мкл. Этот вид лейкоцитов обеспечивает адоптивный иммунитет. Это главные клетки иммунной системы: B-лимфоциты вырабатывают антитела, которые распознают возбудителей инфекции, а T-клетки разрушают патогены. Последствия лимфопении зависят от того, количество какой разновидности лимфоцитов снизилось.
- Моноцитопения - снижение уровня моноцитов менее 500/мкл. Этот тип лейкоцитов проникает из крови в ткани и обеспечивает там местную защиту.
Причин развития лейкопении существует масса. Эта проблема нередко возникает у онкологических больных, и поэтому вопрос о том, как поднять лейкоциты при раке, весьма актуален.
Почему во время противоопухолевой терапии может снижаться уровень лейкоцитов?
В организме человека постоянно образуются новые лейкоциты. Это происходит в красном костном мозге - главном кроветворном органе. Причины развития лейкопении во время курса противоопухолевой терапии кроются в принципе действия химиопрепаратов. Эти лекарственные средства по сути представляют собой клеточные яды. Они поражают быстро размножающиеся клетки - в первую очередь раковые. Но нормальные клетки костного мозга тоже активно размножаются, и поэтому они тоже попадают под удар. Таким образом, противоопухолевая терапия способна приводить к снижению уровней любых клеток крови:
- анемия - снижение уровня эритроцитов и гемоглобина;
- лейкопения - снижение уровня лейкоцитов;
- тромбоцитопения - снижение уровня тромбоцитов.
Это распространенные осложнения, и риск их развития во время лечения рака химиопрепаратами зависит от многих факторов: возраста пациента (вероятность лейкопении выше у людей старше 70 лет), исходного состояния иммунной системы, общего состояния здоровья, сопутствующих заболеваний, типов химиопрепаратов, их дозировок, типа и стадии рака. Риск лейкопении увеличивается, когда применяется комбинация нескольких химиопрепаратов, когда лечение химиопрепаратами сочетается с лучевой терапией и другими методами.
Чтобы предотвратить осложнения, связанные со снижением уровней клеток крови, и своевременно при необходимости принять меры, врачи-онкологи назначают пациентам во время лечения регулярные лабораторные анализы.
Обычно лейкопения развивается спустя несколько дней после начала противоопухолевой терапии - чаще всего через неделю. Сниженный уровень лейкоцитов сохраняется в течение 1-2 недель после завершения лечения, а затем начинает возвращаться к норме. Это самый простой ответ на вопрос о том, чем повысить лейкоциты в крови после химиотерапии - организму нужно просто дать время, чтобы он сам восстановился.
Насколько увеличивается риск инфекции при низком уровне лейкоцитов у онкобольного?
В первую очередь вопрос о том, как поднять лейкоциты при онкологии , актуален, потому что лейкопения повышает вероятность заражения инфекциями и их тяжелое течение. Риск развития инфекционных осложнений можно примерно оценить по абсолютному числу нейтрофилов (ANC):
- более 1500 клеток на мкл - риска заражения нет;
- 1000-1500 клеток на мкл - низкий риск заражения;
- 500-1000 клеток на мкл - умеренный риск заражения;
- 100-500 клеток на мкл - высокий риск заражения;
- менее 100 клеток на мкл - крайне высокий риск заражения.
Этот показатель тоже оценивается по общему анализу крови с лейкоцитарной формулой, и лечащий врач учитывает его, оценивая риски, принимая решение о том, какие меры нужны, чтобы обеспечить безопасность пациента.
Помогает ли диета увеличить уровень лейкоцитов после химиотерапии?
На данный момент нет доказательств того, что какие-либо продукты помогают быстро привести в норму уровень лейкоцитов в крови. На это никак нельзя повлиять, употребляя определенные виды пищи или, напротив, избегая каких-либо блюд. Однако, организму можно немного помочь правильным, полноценным питанием:
- В первую очередь необходимо достаточное количество белка. В рационе должны регулярно присутствовать такие продукты, как мясо, птица, рыбы и морепродукты, яйца, молоко, йогурт, творог, крупы, бобовые.
- Увеличить уровень белых кровяных клеток могут помочь продукты, богатые витамином B12 и фолиевой кислотой - эти соединения необходимы для нормального кроветворения. Витамином B12 богата печень, свинина, говядина, баранина, грудка индейки. Фолиевая кислота содержится в субпродуктах, печени, спарже, шпинате, льняном масле. Можно принимать витамины, купленные в аптеке.
Если хочется получить компетентные рекомендации по поводу питания, чтобы вернуть к норме количество лейкоцитов после лечения рака и в целом восстановить ресурсы организма - лучше обратиться к диетологу.
Биологически активные добавки
- В исследованиях на животных астрагал, действительно, помогает укрепить иммунную систему. Но на людях такие испытания не проводились, и неизвестно, увеличивается ли так же число лейкоцитов у человека. Зато риск побочных эффектов вполне реален. Биологически активные добавки с астрагалом могут приводить к диарее, низкому кровяному давлению и обезвоживанию.
- Исследования эхинацеи у людей с онкологическими заболеваниями не проводились, и неизвестно, может ли она влиять на число лейкоцитов и другие показатели крови. Однако, известно, что эхинацея не очень хорошо влияет на печень и способна усиливать токсичность некоторых химиопрепаратов.
Биологически активные добавки, витаминные комплексны, адаптогены, фитопрепараты, - все эти средства сильно разрекламированы и пользуются большой популярностью, в том числе среди онкологических больных. К сожалению, они далеко не всегда приносят пользу и далеко не всегда безопасны. Особенно нежелательно применять их параллельно с химиотерапией, потому что они могут влиять на эффекты противоопухолевых препаратов, повышать их токсичность. Поэтому, если онкологический больной всё же решил использовать подобные средства, чтобы поднять уровень лейкоцитов, предварительно нужно обязательно проконсультироваться с лечащим врачом.
Насколько эффективна народная и альтернативная медицина?
Еще более широкий арсенал способов увеличить уровень лейкоцитов после применения химиопрепаратов предлагает народная и альтернативная медицина. Число методик и рецептов измеряется десятками и сотнями, если не тысячами. Нет смысла подробно рассматривать отдельные из них. Альтернативные методы лечения потому так и называются, что они не прошли клинических испытаний, и их эффективность ничем не доказана. В противном случае их бы давно взяли на вооружение все врачи - представители «официальной медицины».
Конечно, никто не запрещает человеку самостоятельно воспользоваться этими способами. Но тут, как и в случае с биологически активными добавками работает принцип: главное не навредить. Поэтому предварительно обязательна консультация с лечащим врачом.
Лекарственные препараты для поднятия уровня лейкоцитов во время лечения
В первую очередь важно заранее принять меры, чтобы не допустить низкие лейкоциты после химиотерапии и во время нее. Для этого в клиниках «Евроонко» состояние всех пациентов перед началом курса лечения тщательно оценивают, проводят все необходимые исследования, лабораторные анализы. Если имеются хронические заболевания, которые могут повлиять на число лейкоцитов, их лечением также занимаются.
Для борьбы с раком чаще всего применяют комбинации химиопрепаратов с разными механизмами действия: это помогает сделать лечение более эффективным. Но ослабленному пациенту может быть назначен и всего один препарат (монотерапия), чтобы снизить риски. В процессе лечения состояние пациента постоянно контролируют, в том числе с помощью лабораторных анализов. Если уровень лейкоцитов значительно снижается, противоопухолевая терапия может быть на время отменена, пока этот показатель не вернется к норме.
Уровень лейкоцитов можно увеличить с помощью препаратов из группы колониестимулирующих факторов (КСФ):
- гранулоцитарные колониестимулирующие факторы (Г-КСФ) филграстим (нейпоген), ленограстим (граноцит);
- гранулоцитарно-макрофагальный колониестимулирующий фактор (ГМ-КСФ) - молграмостин (лейкомакс).
Эти лекарственные средства стимулируют образование новых лейкоцитов в красном костном мозге, и новые клетки поступают в кровь. Но они применяются только строго по показаниям и под контролем врача - их нельзя просто купить в аптеке и принимать самостоятельно. КСФ используют для профилактики тяжелого, угрожающего жизни состояния - фебрильной нейтропении. Это осложнение сопровождается повышением температуры тела более 38 градусов на фоне снижения уровня нейтрофилов менее 500 клеток на мкл (0,5х109/л). В таких случаях лечение необходимо начинать немедленно. Если в течение ближайших 48 часов ничего не предпринять, то больной погибнет с вероятностью 50%. И даже при своевременно начатой антибиотикотерапии смертность составляет 10%. Фебрильная нейтропения говорит о том, что у пациента развилась инфекция. И ее единственным проявлением зачастую становится именно высокая температура.
В частности, риск фебрильной нейтропении возникает при лечении лимфом комбинациями нескольких химиопрепаратов, при агрессивных схемах противоопухолевой терапии, особенно у пациентов старше 65 лет. При афебрильной (то есть без повышения температуры тела) нейтропении КСФ не используют. Опасность этих препаратов в том, что при частом применении можно сильно истощить ресурсы красного костного мозга, и это приведет к еще более тяжелым последствиям.
КСФ не применяют прямо во время курса противоопухолевой терапии: их назначают, выждав некоторое время после последнего введения химиопрепаратов.
Таким образом, доступных и безопасных препаратов, которые можно было бы применять всем пациентам после курса химиотерапии, чтобы быстро увеличить уровень лейкоцитов, не существует.
Так существует ли быстрый способ?
К сожалению, на вопрос о том, как поднять лейкоциты после химиотерапии за 3 дня, ответа нет. Иммунная система человека устроена очень сложно, в ней много звеньев. В норме количество лейкоцитов восстановится самостоятельно, помочь можно с помощью полноценного питания и в целом здорового образа жизни. Если же этому мешают какие-либо проблемы со здоровьем - нужно заниматься их лечением.
Куда важнее подумать о том, как защититься от инфекций, пока иммунитет ослаблен и не может обеспечить эффективную защиту. На этот счет существует ряд рекомендаций:
- Избегайте торговых центров, общественного транспорта и других мест скопления людей - там можно легко «поймать» инфекцию.
- Избегайте контактов с людьми, у которых есть симптомы ОРВИ.
- Если вам всё же нужно пойти туда, где находится много людей - надевайте маску, респиратор. Соблюдайте социальную дистанцию - 1,5-2 метра.
- Придерживайтесь правил «пищевой безопасности». Такие продукты, как мясо, яйца должны быть тщательно термически обработаны. Для контроля можно приобрести специальный пищевой термометр. Овощи и фрукты нужно тщательно мыть. Молоко разрешается пить только пастеризованное. И вообще, не стоит покупать продукты с рук, на рынках. Лучше в магазине. Внимательно смотрите на срок годности.
- Не пейте «сырую» воду - кипятите, используйте фильтры.
- Не ешьте продукты, которые долго хранились и могли испортиться.
- Чаще мойте руки с мылом.
- Избегайте повреждений кожи и слизистых оболочек. Когда работаете дома, во дворе, готовите пищу - надевайте перчатки. Не расчесывайте кожу. Используйте зубную щетку с мягкой щетиной.
- Тщательно соблюдайте личную гигиену.
- Если в доме есть домашние животные - не стоит с ними лишний раз контактировать, нельзя выносить за ними лотки, чистить клетки, кормушки.
При любом повышении температуры онкологическому пациенту нужно срочно сдать анализ крови. А если появились какие-либо признаки, которые могут свидетельствовать об инфекции - кашель, насморк, диарея, покраснение и припухлость на коже - о них нужно незамедлительно сообщить врачу.
Врачи в клиниках «Евроонко» принимают все меры для того, чтобы пациент перенес курс химиотерапии максимально комфортно, без выраженных побочных эффектов. Они тщательно оценивают состояние пациента и имеющиеся риски до начала лечения, регулярно проводят необходимые контрольные исследования, анализы крови, дают все необходимые рекомендации. Химиотерапия в наших клиниках при необходимости проводится под прикрытием поддерживающей терапии. Если у пациента имеются тяжелые сопутствующие заболевания и высокие риски - наши врачи назначат лечение, которое поможет нормализовать состояние и сделает возможным проведение активного противоопухолевого лечения.
Переливание крови
Иногда онкологическим больным требуется переливание крови. Если врач сказал, что планирует назначить гемотрансфузию, у пациента обычно возникает масса вопросов. Для чего нужна процедура? Случилось что-то страшное? Насколько безопасно переливание крови — можно ли заразиться от донора ВИЧ и другими опасными инфекциями? Как организм отреагирует на чужую кровь? Не возникнут ли осложнения? Можно ли отказаться от гемотрансфузии или заменить её на что-то другое? [1,2]
Ниже вы найдете ответы на многие вопросы.
Что нужно знать о крови?
Врачи и ученые часто называют кровь внутренней средой организма. Она омывает все органы. Кровь выполняет много важных функций: переносит кислород, питательные вещества и гормоны, удаляет отработанные продукты обмена веществ, обеспечивает иммунную защиту, помогает регулировать температуру тела.
Кровь состоит из двух основных частей:
- Жидкая часть — плазма. Представляет собой раствор солей, ионов, белков и других веществ.
- Клетки крови. Эритроциты (красные кровяные тельца) содержат гемоглобин и обеспечивают транспорт кислорода. Лейкоциты (белые кровяные тельца) обеспечивают неспецифическую и иммунную защиту. Тромбоциты (кровяные пластинки) образуют тромб, когда нужно остановить кровотечение. [1,3,4]
В каких случаях онкологические больные нуждаются в переливании крови?
Состояния, требующие гемотрансфузии, могут быть вызваны самой злокачественной опухолью или побочными эффектами противоопухолевого лечения.
Некоторые виды рака, особенно опухоли желудочно-кишечного тракта, опухоли женской половой сферы (влагалища, шейки матки, матки), способны вызывать внутренние кровотечения.
При длительном течении онкологического заболевания в организме возникают различные нарушения, которые вызывают так называемую анемию хронического заболевания.
Некоторые злокачественные опухоли поражают красный костный мозг (главный орган кроветворения), или органы, которые необходимы для поддержания нормального количества кровяных клеток (селезенка, почки). При таких формах рака также может потребоваться переливание крови.
Гемотрансфузия донорской крови нужна пациентам после сложных операций, которые сопровождаются большой кровопотерей.
Химиопрепараты и лучевая терапия действуют не только на опухолевые, но и на другие быстро делящиеся клетки в организме. Иногда они наносят достаточно большой урон красному костному мозгу. В нем нарушается выработка кровяных телец, это грозит анемией, кровотечениями, тяжелыми инфекциями на фоне снижения иммунитета. Переливание крови помогает нормализовать состояние пациента и предотвратить осложнения. 5
При необходимости переливания крови онкологическому пациенту в клинике «Евроонко» эта процедура организуется максимально оперативно. Мы сотрудничаем с крупнейшими банками крови. У клиники «Евроонко» имеется лицензия на «трансфузиологию в амбулаторных и стационарных условиях», у нас работают опытные врачи-специалисты.
Какие бывают виды гемотрансфузии?
У доноров кровь берут «целиком» (иногда только плазму), обычно в количестве 450 мл. Но онкологическому пациенту может быть не нужно всё сразу. В зависимости от ситуации, назначают переливание отдельных компонентов крови.
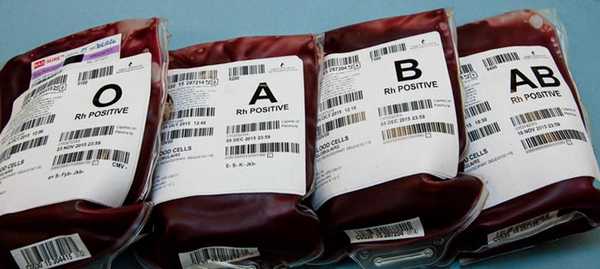
Переливание эритроцитарной массы
Главная функция эритроцитов (красных кровяных телец) — доставка кислорода к тканям и обратный транспорт углекислого газа в легкие. Состояние, при котором количество эритроцитов в крови уменьшается, называется анемией. Собственно, оно и является показанием к переливанию эритроцитарной массы. Врач принимает решение в зависимости от того, как быстро нарастает анемия:
- При хронической анемии, которая нарастает постепенно, спешка не нужна. Врач наблюдает за состоянием пациента, контролирует уровень эритроцитов и гемоглобина. Если эти показатели сильно снижаются, или ухудшается состояние больного, переливают эритроцитарную массу. При заболеваниях сердца и легких, из-за которых кислород хуже доставляется к тканям, переливание может потребоваться даже при относительно небольшом снижении уровня гемоглобина.
- Острая кровопотеря требует немедленных мер. Обычно это происходит во время хирургических вмешательств. Если врач планирует сложную операцию, во время которой пациент потеряет много крови, гемотрансфузия может быть проведена заранее. [8]
Переливание плазмы
Плазма — жидкая часть крови — выглядит как прозрачная жидкость желтоватого цвета. Она содержит факторы свертывания крови — вещества, которые необходимы для образования кровяного сгустка и остановки кровотечения. Также в плазме находятся вещества, защищающие организм от инфекции.
Плазму можно хранить в замороженном состоянии до 12 месяцев. Когда нужно, её размораживают и переливают полученную свежезамороженную плазму больному.
Основное показание к переливанию плазмы у онкологических больных — повышенная кровоточивость. Также процедура необходима при ДВС-синдроме (синдром диссеминированного внутрисосудистого свертывания) — тяжелом состоянии, при котором в мелких сосудах образуются тромбы, в итоге расходуется весь запас тромбоцитов и факторов свертывания крови, возникает риск тяжелых кровотечений. 9
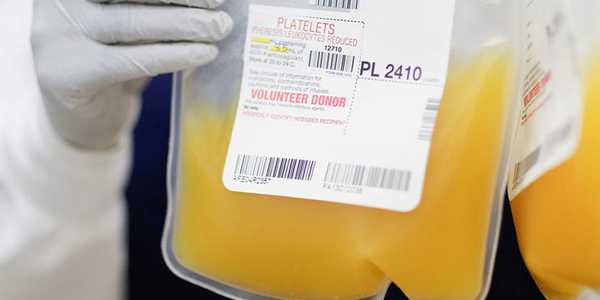
Переливание плазмы крови
Переливание тромбоцитарной массы
Тромбоциты, или кровяные пластинки, принимают участие в образовании тромба и остановке кровотечения. Их уровень может упасть из-за химиотерапии, лучевой терапии, или если опухоль вытеснила нормальную ткань красного костного мозга. Переливание тромбоцитарной массы обычно требуется онкологическим больным в одном из трех случаев:
- если уровень тромбоцитов в крови упал ниже критического значения;
- если имеется повышенная кровоточивость, риск кровотечения;
- если предстоит хирургическое вмешательство, во время которого предполагается большая кровопотеря. [11,12]
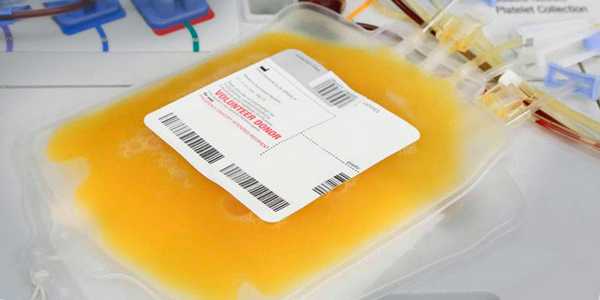
Переливание криопреципитата
Если плазму крови заморозить, а потом отстоять в холодильнике, можно получить концентрированный раствор факторов свертывания крови (фактор VIII, фактор Виллебранда, фибриноген). Иногда, при повышенной кровоточивости, онкологическим больным бывает необходимо переливание такого криопреципитата. [13]
Лейкоцитарная масса может помочь пациентам, у которых в крови сильно снижено содержание белых кровяных клеток и, как следствие, ослаблена иммунная защита. Современные врачи переливают лейкоцитарную массу очень редко. Вместо этого обычно применяют колониестимулирующие факторы (КСФ) — препараты, которые помогают организму производить лейкоциты самостоятельно. [14]
Как проходит процедура переливания крови?
Хотя переливание крови формально и приравнивают к хирургическим вмешательствам, процедура эта совсем не страшная и практически безболезненная. Гемотрансфузию проводят через иглу, которую вводят в вену. Это не больнее, чем обычная внутривенная инъекция. Если у пациента уже установлен центральный венозный катетер, донорскую кровь можно ввести через него.
Процедура гемотрансфузии может занимать разное время, в зависимости от того, какие компоненты крови переливают: от 30-60 минут (переливание тромбоцитарной массы) до 2-4 часов (переливание эритроцитарной массы).
От кого можно переливать кровь?
- Для вас могут сдать кровь родные или друзья. Главное условие — чтобы кровь данного человека подходила для вас. Такое донорство называют целевым.
- Возможно, врач разрешит вам сдать заранее собственную кровь для себя. Она будет сохранена в банке крови, затем её будут переливать вам по мере необходимости.
- Иногда врачи могут собрать кровь, которую пациент потерял во время операции, и перелить её обратно.
Как проверяют кровь доноров?
Человек, который сдает кровь впервые, должен заполнить анкету, пройти осмотр терапевта, дерматовенеролога, сдать анализы на группу крови, резус фактор, на инфекции: ВИЧ, вирусный гепатит B и C, сифилис, цитомегаловирус. Иногда программа обследования может быть расширена.
Если в крови донора будут обнаружены признаки той или иной инфекции, её отбраковывают и в дальнейшем не используют.
Совместимость крови донора и реципиента проверяют при помощи специального анализа — перекрестной пробы на совместимость крови.
Есть ли альтернативы?
Иногда нарушения со стороны крови можно скорректировать лекарственными препаратами без гемотрансфузии. Например, для увеличения количества лейкоцитов применяют колониестимулирующие факторы.
Однако, в случаях, когда необходимо переливание крови, альтернатив нет. Не существует кровезаменителей, которые могли бы обеспечить аналогичные эффекты. Именно поэтому во всех странах мира, включая Россию, постоянно проводится пропаганда донорства, периодически проходят дни донора. Это важно. Это помогает спасти жизни многих людей. [15]

Насколько это безопасно?
Можно ли заразиться инфекцией от донорской крови во время гемотрансфузии? Донорская кровь проходит тщательную проверку, и всё же риски существуют, хотя они и ничтожны. Так, вероятность заразиться ВИЧ через донорскую кровь ниже, чем вероятность того, что в течение жизни человека ударит молния. Риск заражения гепатитом C — 1 к 2 000 000. Врачи и ученые постоянно работают над тем, чтобы свести риски к нулю. [16]
Могут ли перелить несовместимую кровь? Перед гемотрансфузией у реципиента обязательно определяют группу крови и резус-фактор, врач должен убедиться, что кровь донора и реципиента совместимы.
Но кровь разных людей может различаться не только по группе AB0 и резус-фактору. Все нюансы учесть очень сложно. Поэтому во время гемотрансфузии есть незначительный риск аллергической реакции. Чаще всего она проявляется в виде повышения температуры тела, озноба, сыпи. Такие осложнения редко бывают опасны для жизни. Для того чтобы, в случае необходимости, оказать пациенту помощь, во время процедуры за его состоянием постоянно наблюдает медицинский работник.
Можно ли отказаться от переливания крови?
Пациент всегда имеет право отказаться от назначенного лечения, будь то химиотерапия, операция или переливание крови. Но нужно помнить о некоторых моментах:
- Врач не станет назначать процедуру, особенно такую серьезную, как переливание крови, просто так. Если доктор решил провести гемотрансфузию — значит, на то есть веские причины, и в первую очередь это в интересах пациента.
- Большая кровопотеря во время операции и значительные нарушения со стороны крови могут привести к смерти или серьезным осложнениям, ухудшить эффективность противоопухолевого лечения.
- Во время гемотрансфузии есть некоторые риски, но они ничтожны, при этом процедура зачастую помогает спасти жизнь пациента.
Клиники «Евроонко» официально сотрудничают с крупнейшими банками крови страны. Мы работаем на основании лицензии на «трансфузиологию в амбулаторных и стационарных условиях», выданные департаментами здравоохранения Москвы и Санкт-Петербурга.
Стоимость услуг в «Евроонко»
- Консультация врача-трансфузиолога — 5 100 р.
- Общий анализ крови (CITO) — 3 200 р.
- Проба на совместимость перед переливанием крови — 4 200р.
- Эритроцитная взвесь, обедненная лейкоцитами (фильтрованная) — 31 200 р.
- Переливание компонентов крови — 6 900р.
- Стоимость свежезамороженной плазмы (1 доза 250 мл) — 28 900р.
- Тромбоцитный концентрат (1 доза) — 104 000 р.
В соответствии с законодательством Российской Федерации (Закон РФ от 9 июня 1993 г. N 5142-I «О донорстве крови и ее компонентов»), заготовка крови, получение кровекомпонентов и их хранение осуществляется исключительно государственными бюджетными учреждениями. Переливание крови нашим пациентам осуществляется на основании лицензий на «трансфузиологию в амбулаторных и стационарных условиях».
Читайте также:
- Тест на нитратредуктазную активность бактерий. Хроматография при идентификации бактерий. Индикаторные бумажки для идентификации бактерий.
- Синдром гемолитический
- Прием солнечных ванн. Солнечные ванны для закаливания
- Скорость окисления алкоголя. Влияние алкоголя на желудочно-кишечный тракт
- Тепловой удар спортсменов. Возмещение потери хлорида натрия и калия у спортсменов
