Ганглионеврома и ганглионевробластома детей. Феохромоцитома и тератомы у детей
Добавил пользователь Евгений Кузнецов Обновлено: 02.02.2026
В обзорной статье проанализированы современные данные о этиологии, патогенезе, клинике, генетической диагностике феохромоцитом/параганглиом. Представлены методы инструментального обследования и современные рекомендации лечения.
Pheochromocytoma/paraganglioma in children and adolescents: causes, pathogenesis, clinics, diagnostics, treatment (part 2)
In the survey article, modern data on etiology, pathogenesis, clinics, genetics and diagnostics of pheochromocytomas/paragangliomas are analyzed. It also presents methods of instrumental examination and current recommendations for treatment.
Дифференциальный диагноз
У детей с артериальной гипертензией распространенность феохромоцитом/параганглиом составляет около 1,7% [15]. Гиперфункции симпатико-адреналовой системы при феохромоцитоме является составляющей частью многих заболеваний, протекающих c артериальной гипертензией.
АГ при гипоталамическом синдроме пубертатного периода связывают с гемодинамическими изменениями: увеличением объема циркулирующей крови, ударного и сердечного выброса при «неадекватно нормальном» периферическом сопротивлении. При вторичной форме она усугубляется гиперпродукцией АКТГ и кортизола. Клинически АГ может проявляться в виде умеренного повышения артериального давления; у некоторых больных могут развиваться гипертонические кризы.
Механизмы развития АГ при сахарном диабете (СД) 1 и 2 типов различаются. При СД 1 типа АГ в 90% случаев формируется вследствие диабетической нефропатии (ДН). Микроальбуминурия (ранняя стадия ДН) выявляется у больных СД 1 типа с длительностью болезни менее 5 лет, а повышение АД, как правило, развивается через 10-15 лет от дебюта СД 1 типа.
АГ при гиперпаратиреозе обусловлена действием избыточного количества ионизированного кальция на тонус сосудов. Для сокращения гладкомышечных клеток сосудов необходимы ионы кальция, которые поступают в цитоплазму клеток и взаимодействуют с белком кальмодулином. Образующийся комплекс (кальций + кальмодулин) активирует киназу легких цепей миозина, результатом чего является сокращение гладких мышечных волокон.
Абдоминальное ожирение, ассоциированное с метаболическим синдромом, является ключевым механизмом в формировании АГ. Жировая ткань занимает второе место после печени по образованию ангиотензиногена. При ожирении в адипоцитах повышено содержание ренина, активность ангиотензинпревращающего фактора, увеличено содержание ангиотензина II (АТ11), повышена экспрессия рецепторов АТ II типа 1 (АТ1-рецепторов). Активность тканевой РААС тесно связана с продукцией адипокинов жировой тканью.
Повышение АД и высокий тонус симпатической нервной системы характерны для тиреотоксикоза. Тиреоидные гормоны непосредственно связываются с кардиомиоцитами, оказывая положительный инотропный эффект. Они повышают чувствительность и экспрессию адренорецепторов и, как следствие, повышают чувствительность к катехоламинам. Происходит увеличение частоты сердечных сокращений, ускоряется кровоток. Систолическое АД нарастает.
АГ при тиреотоксикозе называют синдромом высокого выброса, при этом гипертрофия левого желудочка отсутствует. Последнее объясняют снижением диастолического АД. Повышение систолического АД и тенденция к снижению диастолического АД сопровождаются увеличением пульсового АД.
Для тиреотоксикоза не свойственны кризы с повышением АД, подобные феохромоцитоме. Выделение катехоламинов при тиреотоксикозе может быть повышено за счет экскреции норадреналина, но не достигает уровня, характерного для больных феохромоцитомой.
При дифференциальном диагнозе феохромоцитомы и другой причины артериальной гипертензии следует прежде всего обратить внимание на пароксизмальный характер гипертонии [16]. Опухоль мозгового слоя надпочечников особенно следует иметь в виду при обследовании детей, страдающих стойкой гипертонией. При ФХЦ больные, как правило, худеют, эффект от проводимой гипотензивной терапии отсутствует. При феохромоцитоме наряду с головной болью, болями за грудиной, которые могут наблюдаться и при гипертонической болезни, нередко отмечается боль и в области опухоли (в животе, поясничной области).
Феохромоцитомный криз может сопровождаться существенным повышением основного обмена и температуры (даже до 40 °C). Провоцировать криз может физическая нагрузка и травма.
Определенное дифференциально-диагностическое значение имеет ортостатическая проба: при феохромоцитоме может быть резкая гипотония, а у больных с гипертензий другой этиологии при переходе в положение стоя давление повышается.
Может помочь в дифференциальной диагностике феохромоцитомы и гипертонической болезни определение содержания хромогранина А в сыворотке крови. Уровень хромогранина А в сыворотке крови значительно повышен у больных феохромоцитомой, тогда как у больных с гипертонической болезнью он может незначительно превышать его содержание у практически здоровых лиц. Хромогранин А высвобождается из мозгового слоя надпочечников и симпатических нейрональных гранул вместе с катехоламинами.
Хромогранин А является также маркером пептидобразующих нейроэндокринных опухолей.
Диагностика
Для подтверждения диагноза феохромоцитомы измеряют уровень свободных метанефринов в плазме или фракционированных метанефринов в суточной моче. Они повышены у большинства больных. Наиболее достоверным для постановки диагноза является определение метанефрина, норметанефрина, метокситирамина методом электрохимического анализа или жидкостной хроматографии с масс-спектрометрией [15, 17].
Определение концентрации ванилилминдальной кислоты в суточной моче простой и доступный метод, но он наименее надежен, поскольку часто дает ложноотрицательные или ложноположительные результата [18, 19].
Всем больным с повышенными показателями метанефринов следует проводить исследование глазного дна, ЭКГ, ЭхоКГ, хромогранина А, кортизола, кальцитонина, паратиреоидного гормона, АКТГ, кальция, фосфора.
Для определения локализации опухоли применяются:
1) УЗИ надпочечников;
2) томография (КТ или МРТ) надпочечников;
3) экскреторная урография;
4) селективная артериография почечных и надпочечниковых артерий;
5) при атипичной локализации опухоли для ее верификации проводят сцинтиграфию с метайодбензилгуанидином (МЙБГ);
6) для исключения параганглиом рекомендуется МРТ головы, шеи.
В случаях выявления компонентов семейных синдромов проводят генетические исследования больных и ближайших родственников [9].
Лечение
Радикальным способом лечения феохромоцитомы является хирургическое удаление новообразования.
Важным условием удачной операции является назначение α- и β-адреноблокаторов до оперативного вмешательства.
Для стабилизации артериального давления используются α1- и β1-адреноблокаторы (тропафен, фентоламин, празозин, доксазозин и др.). Одним из наиболее распространенных препаратов является феноксибензамин* (Дибензилин). Схема его применения может быть различна. Начальная доза обычно не превышает 10 мг 2-3 раза в день. В дальнейшем эта доза может быть увеличена до 20-40 мг до достижения оптимального эффекта. Критерием эффективности лечения считается появление у больного ортостатической реакции в ответ на изменение положения тела. Некоторые клиницисты считают, что при этой пробе артериальное давление не должно быть ниже 80/45 мм рт. ст. и не превышать 160/90 мм рт. ст., на ЭКГ в течение 2 недель не должно быть отрицательной динамики сегмента ST6 и зубца Т, а экстрасистолы возникали бы не чаще одной в течение 5 мин наблюдения.
При назначении адреноблокаторов следует учитывать возможность коллапса у больных даже при выраженной гиперфункции хромаффинной ткани [15].
Избирательными α-адреноблокаторами являются празозин, теразозин, доксазозин. Они лишены некоторых недостатков феноксибензамина. Наибольшее применение нашел празозин. Этот препарат является блокатором постсинаптических α1-адренорецепторов, препятствует сосудосуживающему влиянию катехоламинов. Понижает АД за счет уменьшения ОПСС, уменьшает постнагрузку на сердце. Расширяет периферические вены, уменьшая также преднагрузку на сердце. Он назначается в дозе 2-5 мг 3-4 раза в день [9].
Избирательная блокада постсинаптических рецепторов не приводит к тахикардии и имеет короткий период действия. Поэтому ускоряется подбор оптимальной дозы препарата, уменьшается период послеоперационной гипотонии.
Принимая во внимание особенности клинических проявлений АГ при различных формах заболевания, лекарственная терапия должна подбираться индивидуально. В частности, при пароксизмальной форме с редкими кризами АГ следует отдавать предпочтение антагонистам кальция (нифедипин, дилтиазем, верапамил и др.). Эти препараты не приводят к резкой гипотонии и ортостатическому коллапсу. Они могут быть использованы у больных с нормальным артериальным давлением для предупреждения кризов при их провокации.
Многообещающими представляются результаты применения у больных феохромоцитомой α-метилпаратирозина (Метирозин*, Демсер*). Этот препарат блокирует гидроксилирование тирозина, соответственно, приводит к снижению синтеза катехоламинов. Лечение рекомендуется начинать с дозы 250 мг каждые 6 часов, затем доза увеличивается на 250-500 мг в день, иногда до 4 г в сутки. Введение его в дозе 500-2000 мг/сут ликвидирует гиперкатехоламинемию и дает возможность с меньшим риском для больного провести операцию.
При наличии тахикардии или нарушении ритма сердца применяют β-адреноблокаторы, при этом предпочтительно использовать селективные β1-адреноблокаторы. Назначение этих препаратов допустимо после осуществления α-блокирующего результата, т. к. в противном случае возможно парадоксальное повышение давления вследствие устранения дилатирующего эффекта адреналина, реализующегося через β2-адренорецепторы.
Действие этих препаратов избирательно и направлено на блокаду β1-адренорецепторов (не влияют на β2-рецепторы), при этом наблюдаются преимущественно кардиальные эффекты. Они снижают силу и уменьшают частоту сердечных сокращений, подавляя проводимость через атриовентрикулярный узел, снижают возбудимость сердца. К этой группе относятся препараты атенолол (Атенобене, Принорм и др.), бисопролол (Конкор, Бисомор и др.), бетаксолол (Глаокс, Керлон и др.). За день до плановой операции адреноблокаторы отменяют [20].
В процессе предоперационной подготовки весьма важен динамический контроль за состоянием больного. Недооценка активно секретирующей опухоли связана с высоким риском во время и после операции развития гипертензивных кризов, отека легких, синдрома «неуправляемой гемодинамики», острой сердечной недостаточности.
Настоятельное выполнение этого условия диктуется все той же особенностью опухоли, связанной с гиперпродукцией катехоламинов, не допускающей не только грубых манипуляций при ее удалении, но даже осторожного давления на нее.
Хирургическая тактика при множественной феохромоцитоме окончательно не отработана. При невозможности удаления злокачественной опухоли, рецидиве ее или мультицентричном росте феохромоцитомы, когда невозможна радикальная операция, имеются данные об успешном применении при лечении α-метилпаратирозина феохромоцитомы. Этот препарат в дозе 1-2 г в день приводил к уменьшению опухоли, снижению уровня катехоламинов в плазме и к нормализации артериального давления [9, 15].
После удаления феохромоцитомы артериальное давление быстро нормализуется. Сохранение АД после оперативного вмешательства требует исключения остатков опухоли или наличия эссенциальной гипертензии. Радикальное оперативное вмешательство приводит к практически полному выздоровлению большинства больных. У пациентов с доброкачественной опухолью прогноз наиболее благоприятный, если иметь в виду угрозу повторного развития опухоли. Вероятность появления ее в здоровом надпочечнике или в других тканях организма невелика. При этом наибольшая опасность наблюдается у детей с множественными и эктопическими опухолями.
Литература
В. В. Смирнов 1 , доктор медицинских наук, профессор
Н. С. Баронина
ФГБОУ ВО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
Феохромоцитома/параганглиома у детей и подростков:причины, патогенез, клиника, диагностика, лечение (часть 2)/ В. В. Смирнов, Н. С. Баронина
Ганглионейробластома
Ганглионейробластома — злокачественная неврогенная опухоль, содержащая нейробласты и находящиеся на различных стадиях дифференцировки ганглиозные клетки. Ганглионейробластома характеризуется анорексией, похуданием, лихорадкой, симптомами избытка катехоламинов (повышение АД, потливость, гиперемия лица, тахикардия). В зависимости от локализации опухоли могут наблюдаться симптомы сдавления органов брюшной полости или средостения, очаговая неврологическая симптоматика. Диагностика ганглионейробластомы основана на визуализации опухоли при помощи УЗИ, КТ, МРТ, МСКТ и ее морфологической верификации при изучении биопсийного материала. Наиболее эффективный способ лечения ганглионейробластомы — это радикальное или расширенное удаление опухоли.
МКБ-10
Общие сведения
Ганглионейробластома представляет собой лишенный капсулы серо-розовый или серый опухолевый узел, имеющий очаги кровоизлияний и некротические участки. Среди опухолей симпатической нервной системы ганглионейробластома занимает второе место по частоте возникновения. Она составляет около 40% опухолей этой группы. В половине случаев ганглионейробластома располагается в забрюшинном пространстве, 40% ее локализации приходится на заднее средостение. Ганглионейробластома ЦНС является редким видом опухоли и составляет всего 0,5% наблюдений.
Ганглионейробластома является результатом злокачественной трансформации ганглионевромы и занимает промежуточное положение между этой доброкачественной опухолью и крайне злокачественной нейробластомой. На сегодняшний день неврология и медицина в целом не имеют точных сведений о причинах, приводящих к развитию ганглионейробластомы. Наиболее часто ганглионейробластома встречается у детей, преимущественно в возрастном промежутке от 4 до 10 лет. Отдельно выделяют так называемую комбинированную ганглионейробластому, имеющую строение ганглионевромы с участками из нейробластов. Такая ганглионейробластома встречается в основном среди пациентов старше 10 лет, а средний возраст заболевших составляет 20 лет.
Симптомы ганглионейробластомы
Ганглионейробластома забрюшинного пространства проявляется общими симптомами: снижением массы тела, анорексией, анемией, лихорадкой. Может наблюдаться периорбитальный отек. Поскольку ганглионейробластома сопровождается повышением в крови котехоламинов (адреналина, дофамина, норадреналина), клинически зачастую наблюдаются обусловленные их избытком симптомы: повышенное потоотделение, артериальная гипертензия, тахикардия, покраснение лица, иногда — хронический понос.
Ганглионейробластома средостения характеризуется прежде всего нарушением дыхательной функции: одышкой, кашлем, стенотическим дыханием или стридором, приступами асфиксии. Указанные симптомы чаще бывают вызваны рефлекторными механизмами и нейропатическим парезом гортани, возникающими при сдавлении опухолью блуждающего нерва или его ветвей. Они отличаются внезапным появлением и быстрым развитием клиники в течение нескольких дней. При этом опухоль может иметь небольшой размер, не вызывать смещения структур средостения и не распространяться на легкие. Если ганглионейробластома оказывает давление на верхнегрудные симпатические узлы, то в клинической картине наблюдается нарушение потоотделения, анизокория (разный размер зрачков), синдром Горнера: опущение верхнего века (птоз), расширение зрачка (миоз), энофтальм.
Ганглионейробластома головного мозга имеет клиническую картину внутримозговой опухоли с очаговыми симптомами, соответствующими ее расположению. Как правило, она метастазирует в пределах центральной нервной системы. Ганглионейробластома внемозговой локализации дает метастазы в лимфатические узлы, кости, печень и другие внутренние органы.
Диагностика ганглионейробластомы
В лабораторной диагностике ганглионейробластомы имеет значение определение содержания катехоламинов в крови и их метаболитов (ванилилминдальной кислоты и гомованилиновой кислоты) в моче.
Рентгенологическое исследование позволяет получить лишь косвенные данные за опухоль. При ее локализации в забрюшинном пространстве на обзорной рентгенографии органов брюшной полости выявляется растяжение петель кишечника и паравертебральные кальцификаты, при расположении опухоли в средостении на рентгенографии органов грудной клетки можно выявить округлую плотную тень, локальное расширение межреберных промежутков, наличие «узур» на ребрах в местах их примыкания к опухоли.
С целью визуализации ганглионейробластомы применяется МСКТ или УЗИ органов брюшной полости, КТ органов грудной клетки, пневмомедиастинография, МРТ головного мозга. Для обнаружения метастазов опухоли применяется рентгенография и сцинтиграфия скелета, УЗИ печени, пункционная биопсия лимфатического узла и пр.
Окончательно ганглионейробластома может быть диагностирована лишь при микроскопическом исследовании образца опухоли, полученного интраоперационно или в ходе биопсии. В диагностике ганглионейробластомы головного мозга может применяться стереотаксическая биопсия. При гистологическом исследовании в случае ганглионейробластомы в препарате обнаруживаются мелкие незрелые нейроциты с разной степенью дифференцировки, крупные многоядерные нейроциты с вакуолями в цитоплазме, участки некроза и мелкие кисты. Комбинированная ганглионейробластома характеризуется сходным с ганглионевромой строением, отличительной особенностью является наличие очагов, состоящих из нейробластов, которые могут иметь или не иметь признаков дифференцировки.
Ганглионейробластома нуждается в дифференцировке от других злокачественных новообразований, имеющих мелкоклеточное строение, например, от лимфомы, глиобластомы и метастатических опухолей.
Лечение ганглионейробластомы
Удаление ганглионейробластомы головного мозга производится нейрохирургами в соответствии с принципами операций при опухолях головного мозга. Оперативное вмешательство при ганглионейробластоме средостения и забрюшинного пространства производят хирурги и торакальные хирурги. При этом, если ганглионейробластома не прорастает в окружающие ткани, то осуществляется ее радикальное удаление. Однако чаще приходится выполнять расширенное удаление опухоли, включающее резекцию жировой клетчатки и регионарных лимфатических узлов. В случаях, когда ганглионейробластома не может быть удалена полностью для декомпрессии окружающих ее анатомических структур производят паллиативное удаление опухоли, т. е. ее частичную резекцию.
Хирургическое лечение ганглионейробластомы сочетают с химиотерапией препаратами винкристин и циклофосфамид. У детей более старшего возраста возможно применение лучевой терапии. В тяжелых случаях может потребоваться пересадка костного мозга.
Прогноз ганглионейробластомы
Средняя 2-летняя выживаемость пациентов с ганглионейробластомой составляет 70%. Как показали клинические наблюдения, ганглионейробластома, локализующаяся в заднем средостении, имеет более благоприятный прогноз. При ней 2-летняя выживаемость приближается к 80%, в то время как при ганглионейробластоме забрюшинной локализации она находится на уровне 60%. Пациенты с нераспространенной ганглионейробластомой и после радикальной операции живут дольше 2-х лет более, чем в 95% случаев. При распространенном характере опухоли и наличии метастазов 2-летняя выживаемость составляет лишь 50%.
Ганглионеврома ( ганглиома , ганглионарная неврома , ганглиоцитома )
Ганглионеврома (ганглиома, ганглионарная неврома, ганглиоцитома) — доброкачественная опухоль, сформированная из элементов симпатических нервных узлов (ганглиев). Ганглионеврома может иметь самую разную локализацию. Наиболее часто она связана с различными отделами позвоночника, может располагаться в головном мозге, реже — в надпочечниках, желудочно-кишечном тракте, коже, стенке мочевого пузыря. Клинические симптомы, которыми проявляется ганглионеврома, не имеют специфики и зависят от расположения опухоли. Диагностика осуществляется в основном методами компьютерной и магнитно-резонансной томографии, а также путем гистологического исследования биопсийного образца тканей опухоли. Лечение ганглионевромы возможно только хирургическим путем.
Ганглионеврома представляет собой плотно-эластический узел, не имеющий отчетливо выраженной капсулы. Форма узла может быть неправильной или округлой. На разрезе ганглионеврома имеет дольчатое или волокнистое строение; характерна белесовато-серая окраска опухоли. Микроскопически ганглионеврома состоит из нервных волокон, ганглиозных клеток и волокон соединительной ткани. Соотношение структурных элементов ганглионевромы может быть весьма разным. Так, ганглиозные клетки могут быть единичными в препарате, а могут присутствовать в большом количестве; количество соединительнотканных волокон бывает и значительным, и минимальным; нервные волокна чаще безмякотного типа, но встречаются ганглионевромы, в состав которых входят миелиновые нервные волокна.
Причины возникновения ганглионевромы
В современной неврологии на первый план выходит мнение, что ганглионеврома возникает в результате нарушений, происходящих во внутриутробном периоде при закладке симпатической нервной системы. Это предположение подтверждается частым наличием у пациентов с ганглионевромой других врожденных пороков (аномалий развития позвоночника, волчьей пасти, заячьей губы, врожденной базилярной импрессии, ассимиляции атланта, аномалии Кимерли и др.).
Вероятно факторами, способствующими образованию ганглионевромы, являются неблагоприятные воздействия на организм матери и плода. Это не только радиоактивное облучение, но и различные инфекции (краснуха, цитомегаловирус, корь, сифилис, хламидиоз и пр.), интоксикации (алкоголем, наркотическими веществами, химикатами), хронические заболевания матери, приводящие к гипоксии плода.
Классификация ганглионевромы
В зависимости от локализации процесса выделяют следующие виды опухолей: ганглионевромы головного мозга, ганглионевромы симпатического нервного ствола, ганглионевромы надпочечников и ганглионевромы прочей локализации (кожа, мочевой пузырь, стенка желудка или кишечника). Существенное клиническое значение имеет деление ганглионевром на зрелые и созревающие, из которых первые имеют более благоприятный прогноз.
Симптомы ганглионевромы
Более, чем в 50% случаев ганглионеврома обнаруживается у лиц моложе 20 лет. По некоторым данным эта опухоль чаще поражает лиц женского пола. Клинические проявления ганглионевромы зависят от ее местонахождения, размеров и распространения в соседствующие с ней анатомические структуры.
Наиболее часто ганглионевромы берут свое начало из клеток симпатического ствола на уровне различных отделов позвоночника. При этом в зависимости от уровня расположения опухоль распространяется в позвоночный канал и кзади — в заднее средостение, забрюшинное пространство или клетчатку малого таза. Реже встречаются опухоли шейного отдела. Ганглионеврома, прорастающая в позвоночник, имеет вид песочных часов, поскольку она состоит из двух узлов, один из которых расположен паравертебрально, а второй — в позвоночном канале. Клинически такая опухоль проявляется симптомами сдавления спинного мозга, а при прорастании в него — неспецифической клиникой опухоли спинного мозга. Ганглионеврома отличается медленным ростом, что при локализации в забрюшинном пространстве позволяет ей достигать огромных размеров, не вызывая никаких клинических симптомов.
Ганглионеврома головного мозга чаще носит название ганглиоцитома. На ее долю приходится от 0,1 до 0,4 % всех опухолей внутричерепной локализации. Опухоль может локализоваться в любом отделе головного мозга, но наиболее часто встречаются ганглионевромы дна III желудочка, гипоталамуса, подкорковых структур, височной и лобной долей, а также диффузная ганглионеврома коры мозжечка. Как правило, ганглиоцитома имеет размер не более 3-4 см, характеризуется медленным ростом и полным отсутствием капсулы. Такая опухоль может в виде выростов распространяться в ткань мозга и прорастать мозговые оболочки. Ганглионеврома головного мозга не имеет специфических симптомов. Как и другие внутримозговые опухоли ганглионеврома проявляется общемозговыми и очаговыми симптомами, соответствующими ее расположению. Внутримозговая ганглионеврома может претерпевать бластоматозную трансформацию, перерождаясь в злокачественную нейробластому (ганглионейробластому).
В редких случаях ганглионеврома имеет органную локализацию. Она может поражать надпочечники, органы ЖКТ, мочевой пузырь. При этом отмечается клиническая картина, характерная соответственно для опухолей надпочечников, опухоли желудка, пищевода или тонкого кишечника, доброкачественной опухоли мочевого пузыря.
Диагностика ганглионевромы
Характерный медленный рост приводит к длительному бессимптомному развитию ганглионевромы и затрудняет ее своевременную диагностику. В некоторых случаях она является случайной находкой при обследовании пациента. Так, при рентгенографии позвоночника или органов грудной клетки ганглионеврома может визуализироваться как примыкающее к позвоночнику однородное затемнение округлой формы. В случае опухоли большого размера может наблюдаться симптом «раздвигания ребер» и появления на них «узур» (вдавлений), обусловленных постоянным давлением опухоли. При озлокачествлении ганглионевромы рентгенологически определяются деструктивные изменения расположенных рядом с ней позвонков и ребер.
Широкий диапазон локализации ганглионевромы способствует тому, что с ней в своей практике сталкиваются не только неврологи, но и вертебрологи, гастроэнтерологи, эндокринологи, урологи и др. специалисты. Клинически заподозрить опухоль невролог может по результатам неврологического обследования пациента. Для подтверждения диагноза в зависимости от расположения опухоли необходимо проведение МРТ или КТ позвоночника, КТ грудной клетки и средостения, МРТ головного мозга. Подтвердить диагноз опухолевого образования и верифицировать его как ганглионеврому возможно только при гистологическом исследовании образца ткани, который получают в ходе пункционной биопсии позвонка или стереотаксической биопсии головного мозга.
Лечение ганглионевромы
В отношении ганглионевромы возможно только хирургическое лечение. Оно проводится в соответствии с принципами операций на позвоночнике и оперативных вмешательств при опухолях головного мозга. Сложность радикального удаления опухоли заключается в том, что она зачастую имеет значительные размеры и располагается в жизненно важных структурах ЦНС, оперативное вмешательство на которых сопряжено с опасностью для жизни оперируемого. Возможность проведения операции и ее объем рассматривается нейрохирургом индивидуально в каждом конкретном случае.
Полное удаление опухоли типа «песочных часов» зачастую требует двух хирургических доступов: ламинэктомии и вскрытия грудной или брюшной полости. Подобная операция может потребовать участия не только нейрохирургов, но и торакальных хирургов. Радикальное удаление интрамедуллярной опухоли часто не представляется возможным. В таких случаях ганглионеврома удаляется частично, производится декомпрессия спинного мозга и восстановление ликвороциркуляции.
Удаление ганглионевромы головного мозга часто представляет собой паллиативное вмешательство с частичным удалением опухоли из-за ее больших размеров и значительного распространения в мозговой ткани. При невозможности полного удаления вентрикулярных опухолей хирургическое вмешательство дополняют шунтирующей операцией — вентрикулоперитонеальным шунтированием или наружным вентрикулярным дренированием. После удаления ганглионевромы проводится обязательное гистологическое исследование опухоли для исключения ее трансформации в ганглионейробластому.
Прогноз ганглионевромы
Зрелые ганглионевромы небольших размеров, успешно удаляемые хирургическим путем, имеют благоприятный прогноз, хотя в некоторых случаях наблюдается их рецидивирование. Опухоли больших размеров и созревающие ганглионевромы прогностически менее благоприятны. Худший прогноз как для выздоровления, так и для жизни, имеют опухоли с бластоматозным перерождением.
Феохромоцитома ( Хромаффинома )
Феохромоцитома - это опухоль с преимущественной локализацией в мозговом веществе надпочечников, состоящая из хромаффинных клеток и секретирующая большие количества катехоламинов. Феохромоцитома проявляется артериальной гипертензией и катехоламиновыми гипертоническими кризами. С целью диагностики феохромоцитомы проводят провокационные пробы, определение содержания катехоламинов и их метаболитов в крови и моче, УЗИ надпочечников, КТ и МРТ, сцинтиграфию, селективную артериографию. Лечение феохромоцитомы заключается в выполнении адреналэктомия после соответствующей медикаментозной подготовки.
Феохромоцитома (хромаффинома) - доброкачественная или злокачественная гормонально-активная опухоль хромаффинных клеток симпатико-адреналовой системы, способная продуцировать пептиды и биогенные амины, включая норадреналин, адреналин, дофамин. В 90% наблюдений феохромоцитома развивается в мозговом слое надпочечников; у 8% пациентов локализуется в области аортального поясничного параганглия; в 2% случаев - в грудной или брюшной полости, в малом тазу; крайне редко (менее 0,1%) - в области головы и шеи.
В клинической эндокринологии описаны феохромоцитомы с интраперикардиальной и миокардиальной локализацией, с преимущественным расположением в левых отделах сердца. Обычно феохромоцитома выявляется у лиц обоего пола в возрасте 20-40 лет; у детей чаще встречается среди мальчиков (60% наблюдений). Феохромоцитома является частой причиной артериальной гипертонии и выявляется примерно в 1% случаев у больных с устойчиво повышенным диастолическим артериальным давлением.
Злокачественные феохромоцитомы составляют менее 10% случаев, они, как правило, имеют вненадпочечниковую локализацию и продуцируют дофамин. Метастазирование злокачественных феохромоцитом происходит в регионарные лимфоузлы, мышцы, кости, печень и легкие.
Причины феохромоцитомы
Довольно часто феохромоцитома является компонентом синдрома множественных эндокринных неоплазий 2А и 2В типов, наряду с медуллярной карциномой щитовидной железы, гиперпаратиреозом и нейрофиброматозом. В 10% случаев наблюдается семейная форма заболевания с аутосомно-доминантным типом наследования и высокой степенью вариабельности в фенотипе. В большинстве случаев этиология хромаффинных опухолей остается не известной.
Патогенез
Клиническая симптоматика феохромоцитомы связана с действием на организм избыточно продуцируемых опухолью катехоламинов. Кроме катехоламинов (норадреналина, адреналина, дофамина) феохромоцитома может секретировать АКТГ, кальцитонин, серотонин, соматостатин, вазоактивный интестинальный полипептид, сильнейший вазоконстриктор - нейропептид Y и другие активные вещества, вызывающие многообразные эффекты.
Феохромоцитома представляет инкапсулированную опухоль с хорошей васкуляризацией, размером около 5 см и средней массой до 70 г. Встречаются феохромоцитомы как больших, так и меньших размеров; при этом степень гормональной активности не зависит от величины опухоли.
Симптомы феохромоцитомы
Наиболее постоянным симптомом феохромоцитомы служит артериальная гипертензия, протекающая в кризовой (пароксизмальной) или стабильной форме. Во время катехоламинового гипертонического криза АД резко повышается, в межкризовый период держится в пределах нормы или остается стабильно повышенным. В некоторых случаях феохромоцитома протекает без кризов с постоянно высоким АД.
Гипертонический криз при феохромоцитоме сопровождается сердечно-сосудистыми, желудочно-кишечными, нервно-психическими проявлениями, обменными нарушениями. Развитие криза характеризуется беспокойством, чувством страха, дрожью, ознобом, головной болью, бледностью кожных покровов, потливостью, судорогами. Отмечаются боли в сердце, тахикардия, нарушение ритма; возникают сухость во рту, тошнота и рвота. Характерными изменениями со стороны крови при феохромоцитоме служат лейкоцитоз, лимфоцитоз, эозинофилия, гипергликемия.
Криз может продолжаться от нескольких минут до 1 и более часов; типично его внезапное окончание с резким снижением АД вплоть до гипотензии. Завершение пароксизма сопровождается профузным потоотделением, полиурией с выделением до 5 л светлой мочи, общей слабостью и разбитостью. Кризы могут провоцироваться эмоциональными расстройствами, физической нагрузкой, перегреванием или переохлаждением, проведением глубокой пальпации живота, резкими движениями тела, приемом лекарственных препаратов или алкоголя и другими факторами.
Частота возникновения приступов различна: от одного в течение нескольких месяцев до 10 - 15 в день. Исходом тяжелого криза при феохромоцитоме может явиться кровоизлияние в сетчатку глаза, инсульт, отек легких, инфаркт миокарда, почечная недостаточность, расслаивающая аневризма аорты и др. Злокачественная феохромоцитома (феохромобластома) сопровождается болями в животе, значительным похуданием, метастазирование в отдаленные органы.
Осложнения
Наиболее тяжелым осложнением клинического течения феохромоцитомы служит катехоламиновый шок, проявляющийся неуправляемой гемодинамикой - беспорядочной сменой эпизодов гипер- и гипотензии, не поддающихся коррекции. У беременных феохромоцитома маскируется под токсикозы беременности, преэклампсию и эклампсию и часто приводит к неблагоприятному исходу родов.
Стабильная форма феохромоцитомы характеризуется стойко высоким АД с постепенным развитием изменений со стороны почек, миокарда и глазного дна, изменчивостью настроения, повышенной возбудимостью, утомляемостью, головными болями. Обменные нарушения (гипергликемия) у 10 % больных приводят к развитию сахарного диабета. Заболеваниями, часто сопутствующими феохромоцитоме, являются ЖКБ, болезнь Реклингхаузена (нейрофиброматоз), синдром Иценко-Кушинга, синдром Рейно и др.
Диагностика
При оценке физикальных данных пациентов с феохромоцитомой обращает внимание повышение АД, ортостатическая гипотония, тахикардия, бледность кожи лица и груди. Попытка пальпации объемного образования в брюшной полости или в области шеи может спровоцировать катехоламиновый криз. У 40% пациентов с артериальной гипертензией обнаруживается гипертоническая ретинопатия различной степени, поэтому больные с феохромоцитомой должны быть проконсультированы офтальмологом. Диагностический стандарт включает:
- Лабораторные исследования. Биохимическими критериями феохромоцитомы служат повышение содержания катехоламинов в моче, катехоламинов в крови, хромогранина А в сыворотке крови, глюкозы крови, в некоторых случаях - кортизола, кальцитонина, паратиреоидного гормона, АКТГ, кальция, фосфора и др.
- Фармакопробы. Важное дифференциально-диагностическое значение имеют провокационные и супрессивные фармакологические пробы. Тесты направлены либо на стимуляцию секреции катехоламинов феохромоцитомой, либо на блокирование периферического вазопрессорного действия катехоламинов, однако при проведении проб можно получить как ложноположительные, так и ложноотрицательные результаты.
- Методы инструментальной диагностики. С целью топической диагностики феохромоцитомы выполняются УЗИ надпочечников и томография (КТ или МРТ) надпочечников, экскреторная урография, селективная артериография почечных и надпочечниковых артерий, сцинтиграфия надпочечников, рентгеноскопия или рентгенография органов грудной клетки (для исключения внутригрудного расположения опухоли). Изменения на ЭКГ неспецифичны, разнообразны и обычно носят временный характер, обнаруживаясь во время приступов.
Дифференциальную диагностику феохромоцитомы проводят с гипертонической болезнью, неврозами, психозами, пароксизмальной тахикардией, тиреотоксикозом, заболеваниями ЦНС (инсультом, преходящей ишемией головного мозга, энцефалитом, ЧМТ), отравлениями.
Лечение феохромоцитомы
Консервативная терапия
Основной метод лечения феохромоцитомы - хирургический. Пред планированием операции проводится медикаментозное лечение, направленное на снятие симптомов криза, уменьшения тяжести проявлений заболевания. Для снятия пароксизмов, нормализации АД и купирования тахикардии назначают сочетание a-адреноблокаторов (феноксибензамин, тропафен, фентоламин) и b-адреноблокаторов (пропранолол, метопролол). При развитии гипертонического криза показано введение фентоламина, нитропруссида натрия и др. При злокачественной феохромоцитоме с распространенными метастазами назначается химиотерапия (циклофосфамид, винкристин, дакарбазин).
Хирургическое лечение
В ходе операции по поводу феохромоцитомы используется только лапаротомический доступ ввиду высокой вероятности множественных опухолей и вненадпочечниковой локализации. На протяжении всего вмешательства осуществляется контроль гемодинамики (ЦВД и АД). Обычно при феохромоцитоме выполняется тотальная адреналэктомия. Если феохромоцитома является частью множественной эндокринной неоплазии, прибегают к двусторонней адреналэктомии, что позволяет избежать рецидивов опухоли на противоположной стороне.
Обычно после удаления феохромоцитомы АД снижается; в случае отсутствия снижения артериального давления следует думать о наличии эктопированной опухолевой ткани. У беременных с феохромоцитомой после стабилизации АД выполняется прерывание беременности или кесарево сечение, а затем удаление опухоли.
Прогноз
Удаление доброкачественных феохромоцитом приводит к нормализации показателей АД, регрессу патологических проявлений. 5-летняя выживаемость после радикального лечения доброкачественных опухолей надпочечников составляет 95%; при феохромобластоме - 44%. Частота рецидивов феохромоцитомы составляет около 12,5%. С целью раннего обнаружения рецидивов пациентам показано наблюдение эндокринолога с ежегодным проведением необходимого обследования.
Феохромоцитома - симптомы и лечение
Что такое феохромоцитома? Причины возникновения, диагностику и методы лечения разберем в статье доктора Лукьянова Сергея Анатольевича, онколога со стажем в 18 лет.
Над статьей доктора Лукьянова Сергея Анатольевича работали литературный редактор Вера Васина , научный редактор Сергей Федосов и шеф-редактор Маргарита Тихонова
Определение болезни. Причины заболевания
Феохромоцитома — это злокачественная гормонально-активная опухоль, которая выделяет катехоламины: адреналин и в меньших количествах норадреналин. В 90 % случаев она образуется в мозговом веществе надпочечников. Основные симптомы заболевания: рост артериального давления, головная боль и повышенная потливость.
Ранее феохромоцитомы относили как к доброкачественным, так и к злокачественным опухолям, но по последней классификации (ВОЗ, 2017), они все считаются злокачественными [37] .
Что такое надпочечники
Надпочечники — это парные эндокринные железы, расположенные над верхней частью почек. Каждый из них состоит из двух слоёв: коркового и мозгового. В корковом слое образуются кортикостероиды, среди которых — эстрогены и андрогены. В мозговом слое вырабатываются катехоламины: норадреналин, адреналин и дофамин [33] .
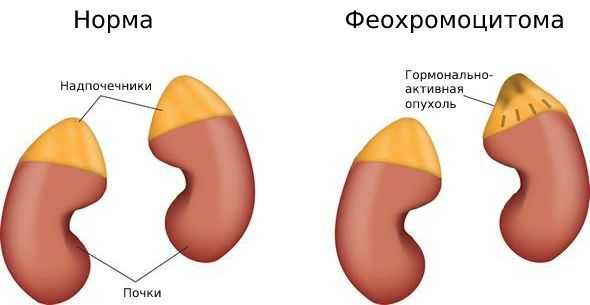
Распространённость
Ежегодная заболеваемость феохромоцитомами составляет 0,4-9,5 случаев на 1 миллион населения [29] . Они могут возникнуть в любом возрасте, но чаще всего выявляются в 20-50 лет. Среди мужчин и женщин феохромоцитомы встречаются примерно с одинаковой частотой.
До 60 % опухолей обнаруживаются случайно при ультразвуковом исследовании (УЗИ) и мультиспиральной компьютерной томографии (МСКТ) брюшной полости.
Причины феохромоцитомы
Единственная известная причина феохромоцитомы — наследственная предрасположенность [34] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Большинство симптомов вызвано избыточным производством катехоламинов с последующим их высвобождением в кровоток.
Клинические проявления
Основной симптом феохромоцитомы — артериальная гипертензия.
Другие признаки феохромоцитомы:
Катехоламиновые кризы
Катехоламиновый криз — это патологическое состояние, вызванное выбросом катехоламинов. При этом повышается артериальное давление, возникает головная боль и сердцебиения, усиливается потоотделение.
Катехоломиновый криз — наиболее опасное проявление феохромоцитомы, которое часто становится причиной тяжёлых осложнений: отёка лёгких, инфаркта миокарда, инсульта и смерти пациента. Чтобы предотвратить эти последствия требуется немедленное лечение [36] .
Спровоцировать криз могут различные факторы - физические нагрузки, психоэмоциональные переживания, переохлаждения и т. д.
Феохромоцитома у беременных
Феохромоцитома при беременности встречается крайне редко. У 87 % пациенток она сопровождается значительным повышением артериального давления. Однако оно может расти и при гестационной гипертонии, преэклампсии и эклампсии, поэтому отличить гормонально-активную опухоль от этих заболеваний по клиническим симптомам очень сложно [7] [8] [11] .
Феохромоцитому можно заподозрить при сочетании артериальной гипертензии с головной болью, сердцебиением, потливостью, повышенным уровнем глюкозы в крови и кардиомиопатией, а также при наличии следующих заболеваний и симптомов:
- медуллярный рак щитовидной железы;
- первичный гиперпаратиреоз (при деформации скелета);
- ганглионейроматоз;
- гемангиомы ЦНС и сетчатки;
- кисты и нейроэндокринные опухоли поджелудочной железы;
- опухоль эндолимфатического мешочка среднего уха;
- папиллярная цистаденома придатка яичка и широкой связки матки;
- гиперпигментация подмышечной и/или паховой области;
- пигментные пятна цвета "кофе с молоком";
- гамартомы радужной оболочки глаза (узелки Лиша) [8][9] .
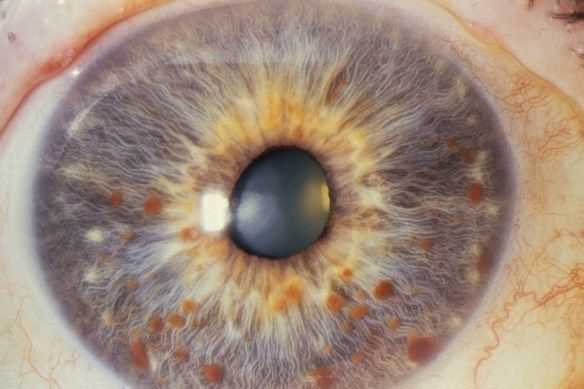
Патогенез феохромоцитомы
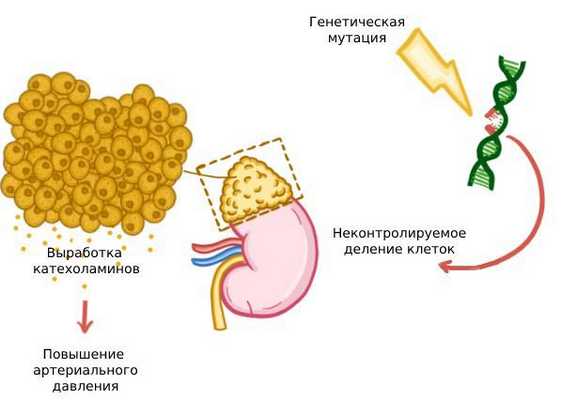
У пациентов с опухолями часто выявляется генетическая предрасположенность к их развитию. Появление феохромоцитом связано со следующими генам: протоонкогеном RET, генами супрессоров опухоли фон Гиппеля — Линдау (VHL), нейрофиброматоза типа 1 (NF1), TMEM127 и MAX, а также генами, кодирующими комплексные субъединицы сукцинатдегидрогеназы (SDHА, SDHB, SDHC и SDHD) и фактора её сборки (SDHAF1 и SDHAF2) [32] . Мутации в генах семейства SDH — наиболее распространённая причина наследственной формы заболевания.
Основные патофизиологические изменения в организме при феохромоцитоме связаны с высоким уровнем катехоломинов в крови. Они вырабатываются клетками опухоли, а некроз её ткани, изменение кровотока и другие причины приводят к их выбросу.
Взаимосвязь феохромоцитомы с другими опухолями
Обнаружена взаимосвязь феохромоцитомы с аденомой гипофиза, почечно-клеточным раком и опухолью желудочно-кишечного тракта. Эти открытия позволят с помощью молекулярно-генетического типирования выявить предрасположенность и предупредить развитие в будущем других опухолей. Такой подход называется персонализированной медициной.
Классификация и стадии развития феохромоцитомы
По локализации:
- Надпочечниковые (90 % случаев):
- двусторонние;
- односторонние.
- Вненадпочечниковые:
- в околопозвонковых симпатических ганглиях — скоплениях нервных клеток, которые проходят по обе стороны спинного мозга ;
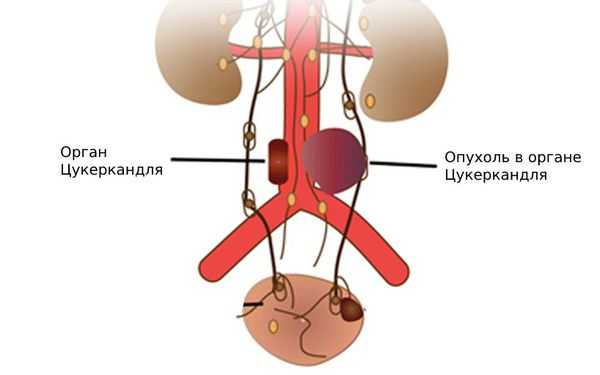
- в брюшной полости — 53 % вненадпочечниковых феохромоцитом выявляются в органе Цукеркандля, расположенном на брюшной аорте у начала нижней брыжеечной артерии [31] ;
- в области шеи .
По клиническому течению:
- Бессимптомная:
- "немая" форма — артериальное давление и уровень катехоламинов в норме;
- "скрытая" форма — повышенный уровень катехоламинов и нормальное артериальное давление.
- Клинически выраженная форма:
- пароксизмальная — артериальная гипертензия с кризами, возникает примерно у половины взрослых пациентов;
- персистирующая — постоянная артериальная гипертензия, встречается у 50 % взрослых и у 60 - 90 % детей [30] ;
- смешанная.
- Атипичная форма:
- с пониженным артериальным давлением;
- в сочетании с гиперкортицизмом — повышенным уровнем глюкокортикоидов.
По тяжести течения:
- лёгкое — бессимптомная форма или с редкими кризами;
- среднее — частые кризы, но без осложнений;
- тяжёлое — осложнения со стороны почек, сердечно-сосудистой и центральной нервной системы, развитие сахарного диабета.
Осложнения феохромоцитомы
- острое нарушение мозгового кровообращения; ;
- отёк лёгких;
- во время беременности: отслойка плаценты, гипоксия и задержка роста плода, его смерть и/или матери.
Помимо осложнений, причиной летального исхода при феохромоцитоме может стать распространение опухолевого процесса в другие органы. Чаще всего феохромоцитома метастазирует в кости и печень.
Диагностика феохромоцитомы
Лабораторные анализы
Самый надёжный лабораторный тест для выявления феохромоцитомы — определение уровня метанефринов мочи [11] . Для подтверждения диагноза феохромоцитомы значение метанефрина или норметанефрина должно минимум в два раза превышать верхнюю границу нормы. Однако его незначительное повышение может быть ложноположительным, особенно на фоне приёма метилдопы и лабеталола.
В большинстве случаев причиной ложноположительного результата является нарушение техники проведения исследования, что требует повторной сдачи анализов. При повторном незначительном повышении метанефринов возможно проведение подавляющего теста с клонидином [10] .
Инструментальные методы исследования
Для визуализации феохромоцитомы применяется компьютерная томография (КТ) и магнитно-резонансная томография (МРТ).
Также используется функциональная визуализация с помощью сцинтиграфии 123I-МИБГ (с метайодбензилгуанидином). При сцинтиграфии в организм вводят радиоактивные изотопы, испускаемое ими излучение позволяет получить двухмерное изображение.
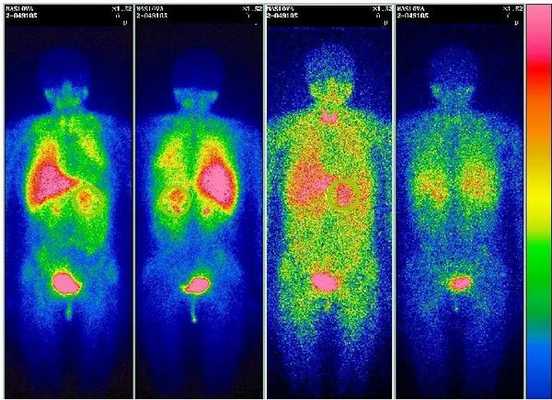
Метод обладает высокой чувствительностью и специфичностью и помогает подтвердить диагноз в спорных случаях. Он предпочтителен для выявления метастазов феохромоцитомы или дополнительных параганглиом — опухолей вненадпочечниковой ткани, выделяющих катехоламины.
Новое направление функциональной диагностики — позитронно-эмиссионная томография (ПЭТ/КТ) с препаратами 18F-FDOPA и 68Ga-DOTATATE. С их помощью можно обнаружить даже микроскопические опухоли, но эти методы ещё изучаются и широко не распространены.
Генетические тесты при феохромоцитоме
Наследственные мутации присутствуют у 30-100 % больных феохромоцитомой. По этой причине генетические исследования рекомендовано проводить всем пациентам с этой опухолью, и особенно беременным женщинам — это позволит информировать их о риске передачи ребёнку повреждённого гена [13] [14] .
Современные технологии позволяют выполнить экстракорпоральное оплодотворение (ЭКО) с генетической диагностикой до имплантации и исключить рождение ребёнка с мутантным геном [12] .
Дифференциальная диагностика
Проводится, прежде всего, с гипертонической болезнью , которая возникла по неизвестной причине. Чётких симптомов, позволяющих их различить, нет.
Медикаментозное лечение
Лечение феохромоцитомы только хирургическое. Медикаментозная терапия используется для подготовки к операции. Для этого минимум за 10 - 14 дней до неё назначают безопасные селективные α-адреноблокаторы. Цель лечения — постепенно снизить артериальное давление, при необходимости плавно увеличивая дозу препарата [7] [11] [18] . Если, несмотря на приём α-адреноблокаторов, тахикардия сохраняется, то назначают β-адреноблокаторы или блокаторы кальциевых каналов.
По возможности следует прекратить приём глюкокортикоидов, опиоидов, метоклопрамида, тиопентала, кетамина и эфедрина, так как они могут спровоцировать гипертонический криз [10] [21] .
Для лечения метастазов феохромоцитомы показана терапия радиоактивными изотопами, а именно 131I-МЙБГ (метайодбензилгуанидином, меченным йодом-131).
В большинстве случаев можно применять радиотаргетную терапию препаратами 177Lu-DOTA-octreotate и 90Y-DOTA-octreotate. В отличие от химиотерапии, которая воздействует на все клетки организма, таргетное лечение блокирует только определённые факторы роста опухоли.
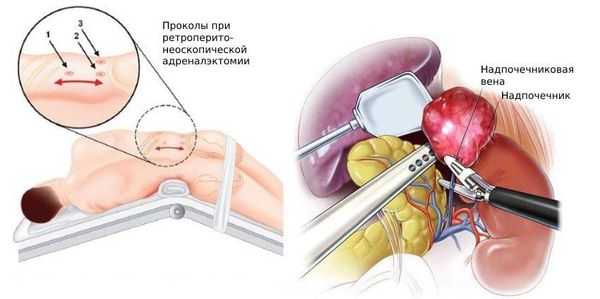
Для хирургического лечения используется адреналэктомия — удаление одного или обоих надпочечников. Операция может проводиться:
- ретроперитонеоскопическим доступом — хирургические инструменты вводятся через поясничную область без вскрытия брюшной полости;
- лапароскопическим — через небольшие разрезы.
При больших размерах опухоли, метастазах и опухолевых тромбах допустима открытая операция. При выявлении двухсторонних феохромоцитом для снижения риска осложнений адреналэктомию можно выполнять в два этапа с интервалом в 2 - 3 месяца [26] .
После двухсторонней адреналэктомии пациенты вынуждены пожизненно принимать заместительную терапию — глюкокортикоиды.
Противопоказания к операции
Удалить опухоль нельзя лишь в одном случае — когда она неоперабельная, то есть проросла в соседние органы, сосуды, имеется множество метастазов. В такой ситуации показана симптоматическая терапия, направленная на снижение артериального давления.
Прогноз. Профилактика
Прогноз зависит от возможности удалить феохромоцитому и её генетического профиля. Единственный надёжный метод лечения — полное удаление опухоли.
Наследственные мутации SDHB связаны с самым высоким риском метастазирования, имеют худший прогноз и более низкую продолжительность жизни, чем другие генетические нарушения.
Если феохромоцитома выявлена и удалена до того, как распространилась на другие органы, пятилетняя выживаемость составляет 95 %, при появлении метастазов — 34-60 % и, как правило, менее пяти лет, если они поражают печень или лёгкие [15] .
Местное распространение опухоли является плохим прогностическим фактором, её неполное удаление или разрушение капсулы при операции может привести к рецидиву.
Поэтому до операции запрещено проводить биопсию любых новообразований надпочечников, чтобы не повредить капсулу опухоли, если она окажется феохромоцитомой.
Раннее генетическое тестирование на наследственные мутации поможет подобрать подходящие таргетные методы лечения метастазов.
Профилактика заболевания не разработана. Генетические тесты могут выявить мутантные гены, повышающие вероятность развития феохромоцитомы, а технология ЭКО поможет не передать их потомству.
Читайте также:
