Гидропс лабиринта. Сосудистые поражения внутреннего уха
Добавил пользователь Евгений Кузнецов Обновлено: 22.01.2026
Представлены отдельные вопросы определения, классификации, клинической интерпретации и лечения 155 пациентов с гидропсом лабиринта различной этиологии, разделенных на четыре группы: 1 - болезнь Меньера, 2 -посттравматический гидропс, 3 - гидропс сосудистой этиологии и 4 - гидропс вирусной этиологии. Работа выполнена с использованием современных методов обследования в соответствии с особенностями диагностики каждой группы больных. Описаны основные заболевания, сопровождающиеся головокружением, выделены опорные информативные дифференциально-диагностические критерии. Установлены степени нарушения слуховой и вестибулярной функции при воздействии различных факторов, в четырех группах обследуемых больных. Оптимизированы комплексные дифференциальные диагностические и лечебные методы гидропса лабиринта, даны рекомендации по их практическому применению.
Ключевые слова: стабилография, вестибулярный анализатор, хлыстовая травма, синдром позвоночной артерии, болезнь Меньера, гидропс лабиринта.
Korkmazov M.Y. 1 , Nalimova Т.А. 2 , Sergeeva S.А. 3 , Korkmazov А.М. 4
1 MD, 2 MD, 3 PhD in Biology, 4 Resident Medical Practitioner, South-Ural State Medical University
ON THE ENDOLYMPHATIC HYDROP OF THE EAR LABYRINTH
Abstract
Single questions on definition, classification, clinical interpretation and treatment of 155 patients suffering from a hydrop of the ear labyrinth of various aetiology divided into four groups: 1 - Meniere's disease, 2 - post-traumatic hydrop, 3 - hydrop of vascular aetiology and 4 - hydrop of virus aetiology, are provided. The work is performed with use of modern methods of medical examination according to the diagnostic features of each group of patients. Basic diseases followed by vertigo are described, basic informative differential and diagnostic criteria are allocated. Extents of acoustical and vestibular function disturbance at influence of various factors, in four groups of the examined patients are established. Complex differential diagnostic and medical methods of ear labyrinth hydrop are optimized, recommendations on their practical use are provided.
Keywords: stabilography, the vestibular analyzer, traumatic injuries, vertebral artery syndrome, Meniere's disease, labyrinth hydrops.
По происхождению и клиническому течению гидропс лабиринта представляет собой не воспалительную реакцию эпителия внутреннего уха на раздражение, приводящее к эндолимфатическому отеку [1,3,7]. Проявляясь, как клинический симптом головокружение, является важной междисциплинарной медико-социальной проблемой, решение которой направлено на совершенствование существующих и разработку новых методов диагностики и лечения [5,8]. Выраженность клинической симптоматики, ургентность состояния пациента во время приступа головокружения требуют от врача хорошего знания алгоритма постановки диагноза и оказания лечебной помощи [8].
Патогенетически гидропс лабиринта, характеризуется скоплением эндолимфы в перепончатом лабиринте системы внутреннего уха, который проявляется симптомами перераздражения всей системы внутреннего уха: слуховой и вестибулярной. Заболевание сопровождается головокружением, требующим выделения опорных информативных дифференциально-диагностических критериев, обоснования целесообразности использования тех или иных лекарственных препаратов с учетом возрастных групп и коморбидных состояний.
Единая система сохранения гомеостаза жидких сред внутримозговых структур определяется взаимоотношением между ними, сохранением трех барьеров: а) барьера между жидкостями внутреннего уха и системой кровообращения, б) барьера между этими жидкостями и цереброспинальной ликворной циркуляцией[2,4,7,], с) барьера между полостями внутреннего и среднего уха[12].
Наиболее часто встречающаяся взаимосвязь повышения внутричерепного давления и дисфункции системы внутреннего уха вызвано нарушением защиты гематолабиринтного барьера[13], где система возникновения, функционирования, сорбции жидких сред лабиринта: эндолимфы и перилимфы являются основными причинами [2,6,10,12].
По данным ряда авторов [2,3,6,8,11] этиологическим фактором гидропса лабиринта являются: посттравматические, сосудистые и воспалительные процессы. Классическим примером данной патологии представляет собой болезнь Меньера.
В настоящее время воспалительный характер возникновения гидропса лабиринта под воздействием вирусной этиологии приобретает все более широкое распространение в связи с возрастанием вирусной агрессии во всем мире. Приведенные данные многочисленных клинических и некоторых экспериментальных исследований [1,7,10,12] убедительно указывают на высокую актуальность изучаемой проблемы. Тем не менее, вопросы определения, классификации, клинической интерпретации и лечения гидропса лабиринта до настоящего времени остаются дискуссионными.
Цель исследования - на основе установления степени нарушения слуховой и вестибулярной функции при воздействии различных факторов, представленных в четырех группах обследуемых, усовершенствовать отдельные диагностические методики и оптимизировать лечебную тактику гидропса лабиринта.
Материалы и методы исследования
Под наблюдением находились 155 пациентов с гидропсом лабиринта различной этиологии, на клинических базах медицинского университета г.Челябинска в течении шести лет с 2009 по 2015 гг. (таблица 1).
Таблица 1. Распределение больных по группам, по возрасту и по полу
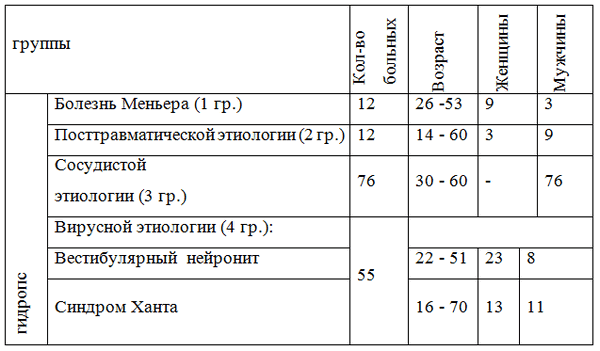
Критерием отбора больных служили либо субъективные жалобы больных на нарушение функции слухового и вестибулярного анализаторов, либо верифицированные инструментальные подтверждения нарушения функции вестибулярного анализатора без субъективных жалоб [4,7,9,10].
Для исследования состояния системы внутреннего уха проводился детализированный сбор жалоб и изучение анамнеза. При этом особое внимание уделялось состоянию сердечно - сосудистой системы, включая показатели вертебро-базилярной гемодинамики, артериального давления в динамике, перенесенным инфекционным и хирургическим заболеваниям (травматические повреждения головы и шеи) заболеваниям нервной и т.д.
По необходимости были выполнены следующие исследования (таблица 2).
Таблица 2. Методы обследования
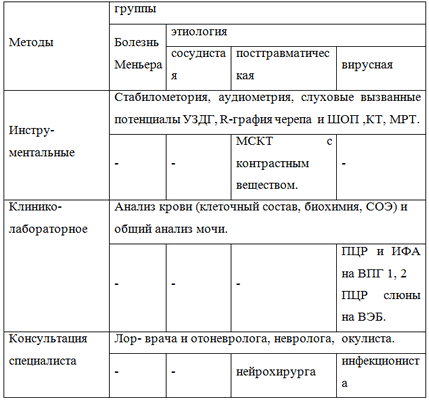
Результаты и обсуждения:
- Болезнь Меньера. Первые годы, как правило, носит односторонний характер и только через несколько лет, а иногда десятки лет возникает двустороннее поражение. Классическая триада симптомов по данным литературы [1,3,5,8,10] включает: приступы головокружения в разных временных интервалах, шум в ушах, флюктуирующее снижение слуха. Кроме этого, наблюдается спонтанный нистагм, тошнота, рвота, падение в сторону, противоположную направлению нистагма, гиперакузия.
Критерием отбора больных данной группы было: продолжительность заболевания не менее 3-х лет, инвалидность в соответствии с МКБ-10, частота приступов составила от 1-2 приступов в неделю до 1-2 приступов в месяц. Наблюдение за приступами выполнялось в условиях стационара при субъективной регистрации нистагма и клинических характеристик приступа. Аудиометрическое исследование проводилось в начале и в конце наблюдения. На протяжении одного года больным дважды были проведены регламентируемые курсы лечения. В течении этого периода все больные овладели навыками контроля и оказания самопомощи по уменьшению продолжительности или снятию приступа. Сорок семь пациентов сменили профессию в соответствии с адаптацией к новым условиям работы. Статистически значимого снижения остроты слуха по данным аудиометрических исследований не установлено.
- Посттравматический гидропс (травмы шеи и головы). Основным механизмом повреждения позвоночника является его резкое сгибание или разгибание (хлыстовая травма), особенно в сочетании с элементами ротации, а также придания чрезмерной нагрузки действующей перпендикулярно или по вертикали (сжатие или растяжение). Мышцы, связки, нервы, кости, межпозвоночные диски, кровеносные сосуды и глаза при этом испытывают аномальное напряжение, когда голова и шея совершают резкие движения за пределами физиологических возможностей [1,10]. К общей картине повреждений шейного отдела позвоночника следует добавить высокий процент диагностических ошибок (особенно верхнешейных позвонков, более 50%), клинические проявления которых (при хлыстовой травме) часто ошибочно трактуются как «обострение остеохондроза, спровоцированное травмой» [5,9,11].
Клинические проявления хлыстовой травмы 1-го периода определяются резким сдвигом всех жидких сред: спинно-мозговой жидкости, эндолимфы и перилимфы; что может привести к развитию гидропса лабиринта, возможному разрыву связочного аппарата подножной пластинки стремени, мембраны круглого окна, возможному разрыву цепи слуховых косточек, вероятному возникновению перилимфатической фистулы[6,9,10]. Симптомами могут быть: появление шума в ушах низкой тональности или звона, головокружения системного характера при наличии травматической гиперрефлексии полукружных каналов; чувства проваливания при нарушении функции отолитов; выраженная вегетативная дисфункция - постоянное чувство тошноты, отсутствие аппетита, возникновение рвоты. Нистагменная реакция направлена в сторону поврежденного уха (нистагм иритации), реакция отклонения рук, туловища, падение в позе Ромберга в здоровую сторону
Количество больных: 12 пострадавших в возрасте от 14 до 60 лет (женщин-3, мужчин-9). Хлыстовая травма 1 степени, сопряженная с травмой головы сотрясение головного мозга-4 мужчин.
Критерии отбора в данной группе были - жалобы на появление шума в ушах низкой тональности и звона в ушах высокой тональности (по данным аудиометрии снижение слуха 1 степени на 20-25%).
Головоружение системного характера на фоне гиперрефлексии полукружных каналов по данным калорических проб. У 4-х мужчин отмечено доброкачественное пароксизмальное головокружение при укладывании на бок. Нистагменная реакция (без графической регистрации) направлена в сторону поврежденного уха, реакция отклонения рук, туловища, падение в позе Ромберга в здоровую сторону. Исчезновение данных симптомов произошло к концу второго месяца. Полное выздоровление после проведенного однократно курса лечения отмечен у всех пациентов (таблица 3).
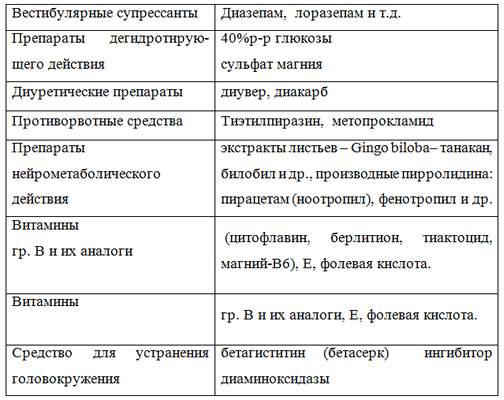
Клинические проявления хлыстовой травмы 2-го периода: таких больных было 8, из них 2 женщин и 6 мужчин. Критерием отбора было наличие жалоб больных через 6 месяцев после травмы, время наблюдения в течение года. Субъективное исследование при выполнении калорических проб (100мл, температурой 25гр) представлено полным выпадением вестибулярной функции на стороне поражения, что отмечено изменением направления спонтанного нистагма в здоровую сторону (нистагм выпадения), изменением направления отклонения рук и туловища, падение в позе Ромберга в больную сторону. Вовлечение стволовых и корковых структур вносит изменения в клинические проявления: возникают приступы с кратковременной потерей сознания, чувством проваливания, присоединяются вегетативные симптомы: чувство жжения, головные боли. Здесь хотелось бы отметить, при проведеннии стабилометрических исследований (в период 2009 по 2015 гг.) у одной больной 36 лет была выявлена отрицательная динамика, что проявилось, прежде всего, наиболее выраженным увеличением коэффициента Ромберга (9579,72 от 2014 г. по сравнению с 2010 г, где он составил 5525).
- Гидропс сосудистой этиологии. Всего обследовано 76 мужчин в возрасте от 30 до60 лет. Из них с диагнозом начальных проявлений недостаточности кровоснабжения мозга (НПНКМ) -21 пациент, дисциркуляторной энцефалопатией, чаще смешанного генеза (ДЭП) 1 стадии 41 пациент. Группу контроля составили 14 мужчин, не имеющих указанных жалоб. Наблюдение проводилось в начале и в конце года наблюдения с аудиометрическим контролем, объективной оценкой функции равновесия с использованием аппарата Стабило-МБН. В группе с диагнозом НПНКМ отмечено снижение слуха от30 до40%. В группе контроля снижение слуха до5 %. Наиболее выраженные изменения отмечены при выполнении пробы Ромберга. Во всех пробах увеличивается скорость общего центра давления, увеличивается длина статокинезиограммы.
В группе пациентов с НПНКМ наблюдались следующие нарушения: площадь статокинезиограммы увеличивается в основной стойке с закрытыми глазами и в пробе Ромберга с закрытыми глазами (21,9% и 19,9%.). Длина статокинезиограммы (ДСКГ) увеличивается в пробах Ромберга. (14,2% и 24,8%). Проведен курс лечения (таблица 4).
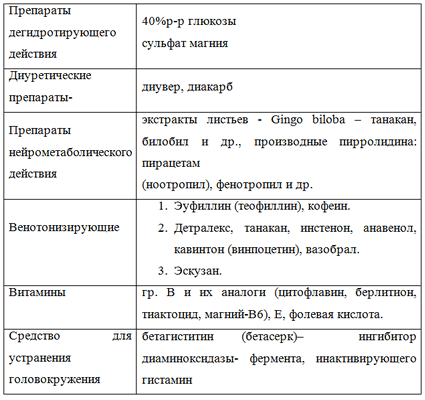
Результаты повторного обследования:
В группе больных с ДЭП-1и НПНКМ отмечено как субъективное, так и объективное улучшение вестибулярной функции, что выражалось в
статистически значимом возрастании устойчивости в позе Ромберга, укорочении длины статокинезиограммы. Значительное улучшение общего состояния всех больных. В группе больных с НПНКМ индекс устойчивости увеличился в основной стойке с закрытыми глазами до33,4%,- 11,6% -43%.
Все больные прошли 15-дневный курс лечения в условиях терапевтического стационара. 4. Гидропс вирусной этиологии. Всего обследовано 55 больных. Из них вестибулярный нейронит 31 больной (23 женщины и 8 мужчин), и с синдромом Ханта 24 больных (13женщин и 11мужчин) возраст составил 22 до 51.
Критерии отбора: указания в анамнезе на герпетические высыпания кожи, слизистых оболочках лица не менее одного-двух раз в течение года, анализы крови ПЦР и ИФА на ВПГ1,2, ПЦР слюны на ВЭБ. Результаты: ИФА на ВПГ 1,2 от 1:32,0 до1:54,0.
Критерии отбора по клиническим данным: вестибулярный нейронит в острой стадии 31больной. Отсутствие выраженных нарушений слуха 3 пациента. Различные формы незначительных нарушений слуха-28больных (двустороннее субъективное чувство заложенности ушей при отсутствии нарушений слухового паспорта 24 больных, положительный ФУНГ у 4х больных). Головокружение системного характера, продолжительностью до 7 дней 4 мужчин и 18 женщин. Головокружение до 30 дней 4мужчин и 15 женщин. Вестибулярная гиперрефлексия при субъективном исследовании спонтанного нистагма 19 больных. Положительная проба Де Клейна у 8 больных.
Критерии отбора пациентов с синдромом Ханта:
- Перенесенный в анамнезе herpes Zoster.
- Высыпания на коже и слизистых оболочках лица, в наружном слуховом проходе либо на барабанной перепонке.
- Шум в ухе односторонний.
Результаты наблюдений в течении одного года: по данным аудиометрии снижение слуха на высокие тоны до 50-70% 23 больных, полная потеря слуха у 1-го больного. Вестибулярная функция по данным калорической пробы с субьективной оценкой нистагма. При первичном обследовании гиперрефлексия у 24больных. При повторном обследовании вестибулярная гипорефлексия у 23х больных, арефлексия у 1го больного.
Функция лицевого нерва при первичном обследовании парез лицевого нерва у 22 больных, паралич лицевого нерва у 2х больных (1М,1Ж). При повторном обследовании парез лицевого нерва восстановился у всех больных, а паралич лицевого нерва не изменился (таблица 5).
Таблица 5. Сравнительная характеристика клинических проявлений
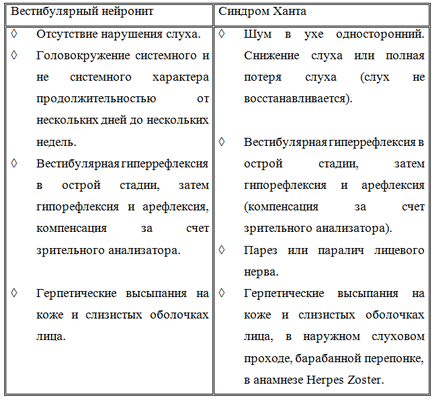
Проведено два курса этиопатогенетического лечения. Результаты лечения оценивались по отсутствию рецидивов в течение 2х месяцев как удовлетворительные. Таких было 3 пациента и отсутствие рецидивов в течение года как положительные у 21 больного.
Таким образом, гидропс лабиринта является единым симптомом, объединяющим различные заболевания, сопровождающиеся повышением количества жидкости внутримозговых структур.
Пример№1: Больная Е…на 58 лет. В течение 20 лет страдает невралгией тройничного нерва. Жалобы на приступы головокружения, которое впервые отмечено в 1997 году после перенесенного стресса. Частота 1-2 приступа в год, продолжительностью 1-2 часа, а последние 1,5 года приступы головокружения усилились, стали более частыми (2-3 в неделю) и более продолжительными (от нескольких часов до нескольких дней). Беспокоит шум в ушах низкочастотного характера, снижение слуха (справа - смешанная тугоухость 3 ст, слева - нейросенсорная тугоухость 4 ст.). Из анамнеза известно, что в студенческие годы перенесла опоясывающий лишай, при лабораторном обследовании в 2012 г ИФА крови на ВПГ1,2 превышало 50 ед. ПЦР слюны на вирусы ВЭБ-не установлены.
Данные отоневрологического осмотра: зев - мелкие герпетические высыпания в области мягкого неба, передних и задних дужек, незначительная гиперемия задней стенки глотки. В пробе Де Клейна нистагм- отсутствует. Чувствительность, обоняние, вкус -сохранены. Снижен правый корнеальный рефлекс. Функция правого лицевого нерва: недостаточность 1 ветви лицевого нерва. При выполнении координаторных проб мелкое интенционное дрожание пальцев. В позе Ромберга покачивание в обе стороны. В усложненной позе Ромберга - падение в обе стороны.
Заключительный диагноз: Гидропс лабиринта с вовлечением кохлеарной и вестибулярной порции восьмой пары черепных нервов, недостаточность по ходу 1-й ветви правого лицевого нерва - вирусной этиологии.
Выводы:
1.Обладая полиэтиологичностью возникновения, гидропс лабиринта в своих клинических проявлениях имеет много общего: больше выражена головная боль, снижена работоспособность, поражается центральное звено слухового и вестибулярного анализаторов, наблюдается прогредиентное ухудшение состояния здоровья больных.
2.Симптом гидропса лабиринта не должен рассматриваться изолированно. Его развитие может быть нарушением трех основных систем: эндокринной, иммунной при ведущей роли нервной системы.
3.При верифицированном диагнозе гидропса лабиринта вирусной этиологии, представленым вестибулярным нейронитом и синдромом Ханта требуется выполнение срочного и длительного курса противовирусной терапии.
4.Предполагается, что освещение и критический анализ затрагиваемых вопросов поможет клиницистам, с одной стороны, в диагностике некоторых отиатрических, неврологических и соматических расстройств, сопровождающихся гидропсом лабиринта внутреннего уха, а с другой - повысит эффективность терапии и профилактики этого страдания.
Синдром Лермуайе ( Лабиринтный ангиоспазм , Пароксизм Лермуайе )
Синдром Лермуайе - это редкая патология внутреннего уха, обусловленная спазмом артерий лабиринта, характеризующаяся слуховыми и вестибулярными нарушениями. Проявляется двухфазными пароксизмами. В первой фазе присутствует шум в ушах, значительное снижение слуха, во второй слух восстанавливается на фоне приступа головокружения. Диагностируется на основании клинической картины после исключения других заболеваний со сходной симптоматикой. Назначается симптоматическое лечение диуретиками, антигистаминными препаратами и бетагистином. При отсутствии эффекта выполняются хирургические операции.
МКБ-10
Общие сведения
Синдром (пароксизм) Лермуайе (лабиринтный ангиоспазм) является редким патологическим состоянием. Впервые был описан французским врачом-оториноларингологом Марселем Лермуайе в 1919 году. Большинство авторов представляют синдром Лермуайе как атипичную форму болезни Меньера, некоторые считают его отдельной нозологией. Дебют заболевания приходится на возраст 30-40 лет, в отличие от болезни Меньера, первые признаки которой выявляются у пожилых людей. У детей подобные состояния встречаются крайне редко. Чаще наблюдается односторонняя симптоматика. В медицинской литературе описаны случаи патологии с единственным, больше не повторявшимся пароксизмом. Иногда попеременно поражается то правое, то левое ухо.
Причины
Непосредственные причины, вызывающие синдром Лермуайе, не установлены. Существуют различные предположения относительно этиологии данного заболевания. Считается, что болезнь развивается из-за ангиоспазма, возникающего на фоне аллергической или аутоимунной реакции, приступа мигрени или выброса катехоламинов при психоэмоциональном стрессе. Пароксизмы Лермуайе также могут быть спровоцированы нейропатией VIII черепно-мозгового нерва, обусловленной патологией шейного отдела позвоночника, сосудистыми аномалиями.
Патогенез
Пусковым механизмом пароксизма Лермуайе служит спазм одной из ветвей внутренней слуховой артерии, ведущий к острой гипоксии лабиринта. Нарушается метаболизм. В тканях внутреннего уха накапливаются недоокисленные продукты обмена. Увеличивается сосудистая проницаемость, ткани набухают. Повышается давление жидкости в системе лабиринта - развивается эндолимфатический гидропс. Происходит раздражение рецепторов внутреннего уха. Появляются кохлеовестибулярные нарушения, которые купируются самостоятельно после восстановления кровотока.
Симптомы
Синдром Лермуайе имеет пароксизмальное течение. Сам пароксизм можно разбить на две фазы. В первом периоде наблюдаются кохлеарные симптомы, для второго характерны вестибулярные дисфункции с одновременным улучшением или полным восстановлением слуха. Болезнь манифестирует внезапно среди кажущегося полного здоровья. Некоторые пациенты связывают начало заболевания с недавно перенесённым психоэмоциональным стрессом.
Синдром Лермуайе дебютирует появлением высокотонального тиннитуса (шума в больном ухе). Пациенты описывают его как «писк» или «звон». Интенсивность шума колеблется от небольшой до мучительной, невыносимой. Тиннитус сопровождается ощущением заложенности уха. Больной перестаёт различать высокие звуки. Наблюдается значительное одностороннее снижение слуха вплоть до полной глухоты. Длительность первой фазы составляет от нескольких дней до 2-3 недель. Кохлеарные симптомы постепенно нарастают, достигая своего пика перед приступом головокружения.
Вторая фаза пароксизма короткая, продолжается от 20-30 минут до нескольких часов. На данном этапе синдром Лермуайе проявляется интенсивным системным головокружением. Присутствуют выраженные вестибуловегетативные симптомы - тошнота, рвота, обильное потоотделение. Иногда приступ заканчивается потерей сознания. Патогномоничным признаком лабиринтного ангиоспазма является существенное (вплоть до полного восстановления) улучшение слуха, наступающее на высоте головокружения.
Осложнения
Течение заболевания обычно благоприятное, симптомы обычно полностью купируются после эпизода головокружения. Иногда синдром Лермуайе сопровождается частыми эпизодами ангиоспазма с поражением одного или обоих ушей. Такое течение болезни существенно ухудшает качество жизни пациентов, нередко приводит к возникновению вторичной нейросенсорной тугоухости. Возможны травмы из-за падений в фазе вестибулярных расстройств.
Диагностика
Диагностический поиск при подозрении на синдром Лермуайе осуществляют специалисты в сфере оториноларингологии совместно с неврологами и отоневрологами. Основанием для подтверждения диагноза служат двухфазное течение пароксизма болезни, характерные клинические симптомы. Диагноз устанавливается только после исключения иной патологии, сопровождающейся кохлеарной и вестибулярной дисфункцией. Болезнь Меньера отличается от данного синдрома снижением слуха на низкие тона, головокружение предшествует кохлеарным расстройствам.
Синдром Лермуайе необходимо дифференцировать с невриномой VIII черепного нерва, очаговыми поражениями головного мозга, локализованными в задней черепной ямке и височной области. Шейный вестибулярный синдром, другие лабиринтопатии и лабиринтиты часто дают похожую клиническую картину. В целях дифференциальной диагностики выполняются следующие исследования:
- Визуализационные методики. Одним из визуализационных методов исследования является рентгенография. На рентгенограмме височных костей может обнаруживаться характерное для невриномы преддверно-улиткового нерва расширение внутреннего слухового прохода. Рентгенография позвоночника даёт возможность исключить деформацию шейного отдела. С помощью КТ и МРТ головного мозга, внутреннего уха выявляются заболевания ЦНС, патология ЛОР органов.
- Измерение остроты слуха. При аудиометрии, импедансометрии определяется тугоухость, устанавливается наличие флюктуации слуха (колебание его остроты). Электрокохлеография позволяет подтвердить наличие признаков эндолимфатического гидропса. Органическое поражение ЦНС, вертебробазилярная недостаточность обычно не приводят к нарушению слуха. При вестибулярном нейроните, лабиринтитах не наблюдается значительных колебаний его остроты.
- Эндоскопические методы.Отомикроскопия и эндоскопия уха используются для исключения наружных и средних отитов. С помощью данных исследований можно обнаружить признаки перилимфатической фистулы тимпаногенного происхождения. При синдроме Лермуайе патологические изменения уха отсутствуют.
- Исследование вестибулярных функций. Осмотр пациента выявляет признаки нарушения равновесия. Наблюдается шаткость походки, неустойчивость в позе Ромберга. При исследовании нистагма с помощью очков Френзеля, методом электронистагмографии и видеоокулографии определяется горизонтальный или горизонтально-ротаторный нистагм. Направление быстрого компонента нистагма зависит от фазы течения болезни.
Лечение синдрома Лермуайе
Этиотропные и патогенетические лечебные мероприятия не разработаны. Симптоматическая консервативная терапия направлена на устранение тяжело переносимых острых симптомов болезни - головокружения с тошнотой и рвотой, интенсивного тиннитуса. В большинстве случаев патология подлежит консервативному лечению, не является показанием для хирургического вмешательства. Операции осуществляются при неэффективности консервативной терапии.
Консервативная терапия
Для снижения давления эндолимфы в лабиринте пациенту рекомендуется ограничить употребление жидкости, поваренной соли. Следует полностью отказаться от алкоголя. В целях устранения дисфункции вестибулярного аппарата показана лечебная физкультура. При подборе фармакологического лечения к каждому больному требуется индивидуальный ступенчатый подход. У некоторых пациентов синдром Лермуайе поддаётся терапии антигистаминными препаратами, кортикостероидными гормонами. Широко используется бетагистин, седативные средства.
Для улучшения обменных процессов назначаются нейропротекторы, витамины А, Е, С, группы В. Острый пароксизм обычно купируется в амбулаторных условиях. Пациенту рекомендуется соблюдать постельный режим. При выраженной симптоматике - интенсивном головокружении, многократной рвоте - больной нуждается в стационарном лечении. Для устранения симптомов пароксизма применяются блокаторы м-холинорецепторов, диуретики и нейролептики.
Хирургическое лечение
Хирургические вмешательства осуществляются при неконтролируемых частых мучительных пароксизмах, возникающих на фоне консервативного лечения. Снизить эндолимфатическое давление помогает установка вентиляционной трубки в барабанную перепонку. Другой часто выполняемой операцией является декомпрессия эндолимфатического мешка. С целью уменьшения шума в ушах применяются деструктивные методы - разрушение лабиринта с помощью химического (абляция спиртом, гентамицином), физического (ультразвуковая, крио- или лазеродеструкция) или механического способов.
Прогноз и профилактика
Синдром Лермуайе отличается от других лабиринтопатий и классического варианта болезни Меньера благоприятным течением. Описаны случаи с единственным в жизни пациента эпизодом заболевания. Данная патология крайне редко осложняется нейросенсорной тугоухостью. Прогноз для восстановления вестибулярных функций хороший. Меры, предотвращающие возникновение вестибулокохлеарных нарушений, на сегодняшний день не разработаны.
1. Lermoyez Syndrome: further mystifying Meniere’s disease / B. Workman // Hearing health & technology matters - 2018.
2. Министерство здравоохранения Российской Федерации: Клинические рекомендации по головокружению (периферическому) пересмотр 2016 г.
3. Слуховые и вестибулярные расстройства на ранних стадиях болезни Меньера: диагностика и лечение / Лиленко С.В.// Лечение заболеваний нервной системы - 2009 г.
Гидропс лабиринта. Сосудистые поражения внутреннего уха
АФК — активные формы кислорода
БМ — болезнь Меньера
ВВМП — вызванные вестибулярные миогенные потенциалы
мРНК — матричная рибонуклеиновая кислота
МРТ — магнитно-резонансная томография
СП — суммационный потенциал улитки
ПД — потенциал действия слухового нерва
GLAST — glutathion aspartate transporter
HLA — human leukocyte antigens
КТ — компьютерная томография
Гидропс лабиринта — невоспалительная реакция эпителия внутреннего уха на раздражение, обусловливающая развитие эндолимфатического отека [1]. Фактически гидропс — патологически расширенное эндолимфатическое пространство, приводящее к увеличению эндолимфатического объема [2]. Заболевание характеризуется системным головокружением, нейросенсорной тугоухостью, низко- и высокочастотными шумами в ушах. Гидропс лабиринта — проблема отнюдь не только медицинского характера, она отражается на качестве жизни больного, затрагивает практически все сферы его жизнедеятельности. Следовательно, состояние требует особого избирательного подхода к диагностике, при этом сохраняя субъективные и объективные методы выявления гидропса лабиринта с учетом возраста и индивидуальных особенностей пациентов. Отметим также, что на сегодняшний день назрела острая необходимость совершенствования имеющихся методов диагностики патологии [3].
Гидропс лабиринта характеризуется избыточным накоплением эндолимфатической жидкости, вследствие чего повышается давление в перепончатом лабиринте системы внутреннего уха. Подавляющая часть экспертов уверены, что развитию гидропса способствуют два составляющих фактора: выработка большого количества эндолимфы сосудистой полоской спирального органа улитки и нарушение процесса ее удаления в эндолимфатическом мешке и эндолимфатической протоке, либо оба этих процесса, действующих совместно [4].
Причины нарушения резорбции лимфы могут быть врожденными и приобретенными. Врожденные причины встречаются крайне редко, например недоразвитие улитки. Приобретенный гидропс в основном может быть связан с аутоиммунными, травматическими, воспалительными, метаболическими заболеваниями [5].
На сегодняшний день все большее распространение получает теория вирусной этиологии гидропса лабиринта. Исследователи связывают это в целом с популяризацией изучения вирусной природы различных заболеваний [6]. Для понимания нарушений, которые приводят к гидропсу лабиринта, ученые обращаются к физиологии жидких сред мозга. Ключевыми в гомеостазе этих жидкостей являются несколько барьеров: 1 — барьер между жидкостями внутреннего уха и кровью, 2 — барьеры, связанные со спинномозговой жидкостью (ликвором), 3 —барьеры между отделами полостей среднего и внутреннего уха [1]. Чаще всего поражается гематолабиринтный барьер, причиной является нарушение тока эндолимфы, а также перелимфы [5].
Существуют две основные теории относительно тока эндолимфы. Первая, предложенная S. Guild еще в 1927 г., основана на механизме продольного тока, при котором эндолимфа продуцируется в улитке, протекает в переднюю часть перепончатого лабиринта, а именно в сферический мешочек, а затем абсорбируется в эндолимфатическом мешочке. Прерывание тока лимфы ведет к скоплению эндолимфы в верхних отделах и формированию гидропса [7]. Данная концепция противопоставляется концепции радиального тока, согласно которой лимфа секретируется и абсорбируется в улитковом канале. Исследование A. Salt и Y. Ma с использованием специальных ионных маркеров показало, что гомеостаз эндолимфы распределен по всему улитковому ходу [8].
Радиальный ток регулируется разными молекулами и ионными каналами, важную роль играют белки семейста аквапоринов. Во внутреннем ухе человека были обнаружены аквапорины 2, 3, 6 в эпителии эндолимфатического мешка. Аквапорины 1, 4, 5 экспрессируются в неэпителиальных клетках улитки, в частности в спиральной связке и фиброцитах [7]. T. Takeda и соавт. продемонстрировали, что введение вазопрессина, повышающего активность аквапорина 2, через 1 нед приводит к развитию гидропса у морских свинок [9]. Эти же исследователи показали, что введение антагониста вазопрессина — OPC 31260 может привести к коллапсу эндолимфатического протока, а также предотвратить развитие гидропса после хирургической облитерации протока. Эти исследования подтверждают роль аквапоринов в развитии гидропса лабиринта.
Недавнее исследование F. Di Berardino и A. Cesarini подтвердило возможную аллергическую природу гидропса. У 83% пациентов с гидропсом лабиринта, вошедших в исследование, были обнаружены положительные кожные пробы к одному или нескольким аллергенам, у 55% — чувствительность к глиадину, главному антигену при аллергии на пшеницу. К слову, данные тесты в контрольной группе, которую составляли здоровые пациенты, были отрицательными [10].
По данным исследований ряда ученых, спровоцировать гидропс лабиринта могут заболевания, связанные с расстройством кровообращения, например синдром позвоночной артерии — заболевание, которое напрямую никак не связано с проблемами внутреннего уха. В этой ситуации гидропс лабиринта проявляется как вторичное заболевание [11].
Важным возможным патогенетическим звеном в возникновении гидропса лабиринта является оксид азота (NO). Существует три основных типа NO-синтазы (NOS); ряд исследований показал, что экспрессия NOS II повышена у морских свинок в кортиевом органе, спиральных ганглиозных клетках, вестибулярных сенсорных и поддерживающих клетках после хирургической индукции гидропса [12]. Хроническая индукция NOS NMDA-рецепторами приводит к накоплению большого количества оксида азота и активных форм кислорода (АФК) [13]. Большое количество АФК в свою очередь способствует увеличению количества цитохрома С — важного элемента внутреннего пути апоптоза. Таким образом, возможно, гидропс лабиринта приводит к хронической активации NMDA-рецепторов и нейрональному повреждению [14].
Помимо оксида азота, серьезное действие на различные патологии внутреннего уха оказываает глутамат. Глутамат аспартатный транспортер GLAST важный фактор поддержания нетоксичного уровня глутамата в улитке [15]. Эксперименты показали, что при гидропсе лабиринта при определенных состояниях внутреннего уха повышаются мРНК GLAST и глутатион-синтаза, что позволяет предполагать новые пути для методов исследования природы гидропса [16].
Исторически диагноз гидропса устанавливался преимущественно на основании длительного анамнеза, так как большинство рутинных методов диагностики не является достаточно чувствительным и специфичным [17]. В современном мире существует несколько инструментальных методов диагностики данного патологического состояния.
Тональная пороговая аудиометрия — достаточно эффективный метод диагностики гидропса лабиринта. Большинство исследователей сходятся в одном: аудиологическое исследование — первый и необходимый этап инструментальной диагностики. При выявлении гидропса наблюдается повышение слуховых порогов с изменением восприятия низких тонов, аудиометрическая кривая носит преимущественно горизонтальный тип [4].
Использование надпороговой аудиометрии также считается важным методом для диагностики гидропса лабиринта. К таким исследованиям в первую очередь относят определение порога дискомфорта методом выравнивания громкости (проба Фаулера) и речевую аудиометрию. Проба Фаулера основана на психофизическом свойстве органа слуха, которое заключается в выравнивании громкости при повышении интенсивности звука на хуже слышащее ухо в том случае, если в нем присутствует ФУНГ. Выравнивание громкости в данном тесте можно объяснить следующим образом: наличие в хуже слышащем ухе ФУНГ обусловливает при каждом новом приращении интенсивности звука все меньшую ее прибавку, так как при этом феномене с увеличением интенсивности ощущение громкости возрастает в несколько раз больше, чем в норме или при кондуктивной тугоухости, при которой ФУНГ отсутствует. При проведении речевой аудиометрии в случае сенсоневральной тугоухости и значительном ФУНГ разборчивость речи при повышении интенсивности понижается, так как начинает влиять феномен слухового дискомфорта: звук кажется слишком громким и невнятным. Наличие ФУНГ обусловливает более крутое восхождение кривой разборчивости речи, а наличие слухового дискомфорта при высокой интенсивности звука — более ранний обрыв кривой [18].
Отечественными исследователями для диагностики гидропса лабиринта также предлагается определение чувствительности к ультразвуку и его латерализации по методу Б.М. Сагаловича. Было показано, что при гидропсе лабиринта слуховая чувствительность к ультразвуку составляет от 61 до 100 кГц. При наличии одностороннего гидропса он латерализуется в хуже слышащее ухо, при двустороннем — в лучше слышащее. В зарубежной литературе указанные методы не описываются [19].
G. Gates и соавт. отмечают, что дегидратационный тест, несмотря на его популярность среди клиницистов, представляет собой косвенный метод диагностики гидропса лабиринта [20]. После тональной пороговой аудиометрии пациенту вводят глицерол и повторяют аудиометрию через 1, 2, 3, 24, 48 ч. Если после введения препарата слух улучшается как минимум на 10 дБ или разборчивость речи повышается на 12% и более, то тест принято считать положительным [21].
Электрокохлеография (ЭКоГ) является еще одним стандартным методом, который используют для выявления гидропса лабиринта. Метод представляет электрофизиологический тест, который отражает повышение давления внутреннего уха через вздутие базилярной мембраны. При электрокохлеографии регистрируется электрическая активность улитки и слухового нерва, возникающая после предъявления звукового стимула. ЭКоГ измеряет отношение суммарного потенциала (СП) к потенциалу, который возникает в ответ на слуховое раздражение (ПД). Отношение менее чем 35% указывает на признаки гидропса лабиринта [17, 22]. Однако, по мнению некоторых авторов, подобная картина изменений ЭКоГ выявляется и при синдроме «третьего окна» (дигисценция полукружного канала, расширенный водопровод преддверия, улитки).
Решающее слово в этом случае принадлежит КТ височных костей, которая в настоящий момент является обязательным инструментальным исследованием для дифференциальной диагностики патологии внутреннего уха. Так, выполнение компьютерной реконструкции позволяет оценить объем лабиринта, эндолимфы и перилимфы, а также саккулюса и утрикулюса [23]. При этом нормальный объем эндолимфы составляет около 5 мкл, в мешочках преддверия и полукружных каналах — около 24 мкл. При наличии гидропса лабиринта объем эндолимфы увеличивается [24—27].
Метод регистрации вызванных вестибулярных миогенных потенциалов (ВВМП) является относительно новым в диагностике гидропса лабиринта [28, 29]. Это нейроэлектрофизиологический тест, который оценивает состояние отолитовых органов утрикулюса и саккулюса. Метод регистрации ВВМП применяют относительно мышц шеи через грудино-ключично-сосцевидную мышцу — цервикальные ВВМП или глазодвигательных мышц через нижние косые мышцы — окулярные ВВМП [30]. Отсутствие или снижение амплитуды ВВМП является признаком гидропса. Ряд экспертов считают, что метод ВВМП позволяет уточнить локализацию и распространенность гидропса [31]. Однако зачастую исследование проводят дополнительно к другим базовым методикам.
Сегодня для исследования микромеханики структур среднего и внутреннего уха применяют метод широкополосной импедансометрии [32]. Данный метод позволяет регистрировать акустический рефлекс стременной мышцы и определять резонансную частоту, что позволяет усовершенствовать метод низкочастотной тимпанометрии. Для исследования применяют зондирующие тоны на частотах от 200 до 8000 Гц, что обеспечивает более точную дифференциальную диагностику патологических изменений в структурах среднего и внутреннего уха, в частности при гидропсе лабиринта [33, 34].
К вестибулологическим методикам исследования гидропса лабиринта можно отнести статокоординаторные и статокинетические пробы, видеоимпульсный тест, битермальную калорическую пробу и метод регистрации вызванных вестибулярных миогенных потенциалов. Статокинетические и статокоординатные тесты хорошо переносятся пациентами и не требуют использования специального оборудования. Видеоимпульсный тест используют для изучения вестибулоокулярного рефлекса [35]. В основе метода лежит измерение скорости поворота головы и одновременного противовращения глазных яблок при зрительной фиксации. В качестве нормативных значений принимают диапазон коэффициента усиления рефлекса 0,76—1,18 и асимметрию между лабиринтами не более 8% [36—38].
Калорическая проба может проводиться как с использованием воды (водная), так и воздуха (воздушная), температуры выше и ниже на 7—12° температуры тела. Преимуществом воздушной методики является возможность ее применения у пациентов с хроническим гнойным процессом в среднем ухе, при котором проведение водной пробы противопоказано [39—41]. При наличии гидропса лабиринта отмечается асимметрия результатов калорической пробы. При этом у большинства (>82%) пациентов наблюдали снижение функции лабиринта с пораженной стороны [34].
Магнитно-резонансная томография (МРТ) является одним из современных методов обнаружения гидропса лабиринта различной локализации, в частности улитки, преддверия или системы полукружных каналов. При данном методе в качестве контрастного вещества используют гадолиний. Через 24 ч после интратимпанального введения данного вещества возможно оценить состояние эндо- и перилимфатического пространства внутреннего уха. Данный метод имеет большие перспективы в объективной верификации пери- и эндолимфатического гидропса лабиринта, так как описанные ранее методики исследования свидетельствуют о признаках общего гидропса лабиринта [42].
Однако, несмотря на достаточное количество применяемых методик выявления гидропса лабиринта, из изложенного в статье ясно, что однозначно информативного, высокочувствительного и специфичного метода на данный момент времени не существует, а известные способы часто имеют значительные ограничения. Все это обусловливает необходимость дальнейшей оптимизации диагностической стратегии описанного патологического состояния.
Читайте также:
- Дополнительные отведения ЭКГ. Двухполюсные грудные отведения по Небу
- Ганглионевромы детей. Опухоли надпочечников детей
- Особенности транслокации по флоэме растения. Строение ситовидных трубок растения.
- Хламидиоз: что такое хламидии, симптомы и лечение у мужчин и женщин
- Диагностика злокачественного плеврального выпота на рентгене, КТ
