Иммунотерапия при раке легких, иммунотерапия при мелкоклеточном раке легкого
Добавил пользователь Валентин П. Обновлено: 28.01.2026
Любая клетка организма способна дать начало злокачественной опухоли. Такое случается при поломке генетического аппарата (ДНК), в том числе, в клетках лёгкого. Всё, что не похоже на нормальные клетки собственного организма, уничтожается нашей иммунной системой. В том числе, клетки опухолей.
Некоторые опухолевые клетки скрывают свою атипичность (непохожесть на нормальные) с помощью молекул на поверхности, сообщающих иммунной системе ложный сигнал «свои». Существует несколько вариантов таких опознаваемых молекул, контрольных точек, способных останавливать лимфоциты и мешать иммунной системе ликвидировать опухоль.
В середине десятых годов XXI века международная группа ученых обнаружила молекулы для опознавания нормальных клеток. Это чек-поинты, контрольные точки иммунной системы. Их наличие сообщает иммунной системе: «клетка „своя“, хорошая». Когда такие молекулы есть у опухолевых клеток, лимфоциты не распознают их как чужеродные и не уничтожают.
Вслед за этим открытием были созданы антитела, блокирующие контрольные точки. В контексте рака легкого для выбора лечения имеют значение контрольные точки PD-L1 и PD-1, а также CTLA4. Именно на них нацелена иммунотерапия.
Если «выключить» контрольные точки антителами, ничто не мешает иммунной системе распознать опухолевую клетку как чужеродную и попытаться её уничтожить.
Рак легкого — область онкологии, где иммунотерапия ингибиторами («выключателями или блокаторами») иммунных контрольных точек — PD-1 и PD-L1 — прочно вошла в арсенал лекарственного противоопухолевого лечения.
Кому показана иммунотерапия?
В каких случаях пациенту с раком легкого могут предложить иммунотерапию ингибиторами контрольных точек:
1) Мелкоклеточный рак легкого с отдаленными метастазами, опухолевыми очагами за пределами пораженного лёгкого — иммунотерапия применяется вместе (в рамках одной схемы лечения) с платино-содержащей химиотерапией в объёме 4 циклов лекарственной терапии, раз в 3 недели.
2) Немелкоклеточный рак легкого с отдаленными метастазами — перед назначением иммунотерапии исследуют полученные при биопсии клетки опухоли для оценки:
Наличия и количества в опухоли иммунных контрольных точек (иммуногистохимия). Это позволяет прогнозировать эффективность иммунотерапии: ожидать хороших результатов лечения немелкоклеточного рака легкого ингибиторами контрольных точек можно, когда в опухоли есть мишени для них.
Наличия некоторых мутаций в клетках аденокарциномы — присутствие таких мутаций как EGFR, ALK, ROS-1, MET и некоторых других позволяет начать лечение с таргетной терапии. При отсутствии этих мутаций решается вопрос об иммунотерапии.
Назначение иммунотерапии в качестве единственного лечения при немелкоклеточном раке лёгкого возможно, если:
Нет признаков агрессивного течения рака легкого — нарушения функции внутренних органов при их метастатическом поражении/быстром росте опухолевых очагов.
Содержание в опухоли иммунной контрольной точки PD-L1 высокое, 50% и выше.
При сочетании этих условий иммунотерапия позволяет добиться большей выживаемости, чем платиносодержащая химиотерапия, и возможно назначение пембролизумаба или атезолизумаба в качестве единственного препарата.
При наличии признаков агрессивного течения рака лёгкого и/или умеренном содержании в опухоли PD-L1 (1-49%) лучше сочетать иммунотерапию с платино-содержащей химиотерапией. При уровне PD-L1 в опухоли ниже 50% сочетание химио- и иммунопрепаратов возможно в первой линии терапии как аденокарциномы, так и плоскоклеточного рака легкого.
3) немелкоклеточный рак легкого III стадии после химиолучевой терапии — иммунотерапия в поддерживающем режиме рекомендуется в связи с наличием данных о ее положительном влиянии на выживаемость пациентов в этой ситуации.
При III стадии немелкоклеточного рака легкого вариантов лечения несколько. Иммунотерапия может быть предложена, когда методом лечения выбрана не операция, а химиолучевая терапия.
4) немелкоклеточный рак легкого с отдаленными метастазами после прогрессирования на фоне применения химио- или таргетных препаратов — иммунотерапия может быть одним из вариантов второй или последующих линий терапии.
Как понять, какая терапия лучше?
Решение о выборе терапии основывается на результатах исследований эффективности и безопасности препаратов в конкретных клинических ситуациях — при разных вариантах рака легкого, стадий заболевания, предшествующего лечения.
Иммунотерапия при раке легкого
Рак легких — одна из самых распространенных злокачественных опухолей. Врачи ежегодно выявляют около 1,8 миллионов новых случаев. Заболевание встречается одинаково часто среди мужчин и женщин. Ежегодно 1,6 миллионов человек погибают от рака легких, и это ведущая причина смертности от онкологических заболеваний.
Каждый пятый онкологический больной погибает от рака легких
Чаще всего опухоль выявляют на поздних стадиях — IIIB и IV. Химиотерапия, лучевая терапия и хирургические вмешательства могут продлить жизнь таких пациентов, но вероятность полного излечения крайне низкая. Несмотря на появление новых, более эффективных, химиопрепаратов, прогноз для многих больных по-прежнему остается неблагоприятным — нередко после лечения происходят рецидивы. Поиск новых методов лечения, которые помогли бы более эффективно бороться с раком легких — очень актуальная задача, стоящая перед современной онкологией. Многие ученые видят большие перспективы в применении иммунотерапии.
Рак легких всегда относили к опухолям, имеющим низкую иммуногенность — в опухолевых клетках очень мало антигенов, которые могли бы стать мишенями для иммунопрепаратов. Тем не менее, исследования показали, что иммунотерапия при раке легких может быть эффективна.
Какие виды иммунотерапии применяются при раке легких?
Существует две основные разновидности рака легких: мелкоклеточный (МРЛ) и немелкоклеточный (НМРЛ). Также встречается мезотелиома — злокачественная опухоль плевры. На данный момент дальше всего удалось продвинуться в применении иммунопрепаратов для лечения немелкоклеточного рака, который встречается в 85% случаев. Но ученые также активно занимаются разработкой новых методов иммунотерапии, которые были бы эффективны против мелкоклеточного рака легких и мезотелиомы.
Существует 4 направления иммунотерапии в лечении рака легких:
- моноклональные антитела;
- ингибиторы «контрольных точек»;
- лечебные вакцины;
- адаптивный перенос Т-лимфоцитов.
Моноклональные антитела
Моноклональные антитела — это молекулы, которые прицельно связываются с определенными антигенами опухолевых клеток. Сегодня многие из них применяются для лечения онкологических заболеваний.
Например, Американским управлением по надзору за качеством пищевых продуктов и медикаментов (FDA) утвержден для лечения немелкоклеточного рака легких препарат Бевацизумаб (Авастин). Его мишенью является фактор роста эндотелия сосудов (ФРЭТ, VEGF).
Ингибиторы «контрольных точек»
Применение ингибиторов «контрольных точек» является одним из наиболее перспективных направлений иммунотерапии рака. Эти молекулы блокируют вещества, которые подавляют иммунные реакции. Таким образом, иммунные клетки избавляются от «наручников» и начинают атаковать раковые клетки.
Ипилимумаб (Ipilimumab, Ервой, Yervoy). В 2011 году этот препарат был одобрен для лечения пациентов с метастатической меланомой. В настоящее время Ипилимумаб проходит испытания при НМРЛ и МРЛ.
Ниволумаб (Nivolumab, Опдиво, Opdivo). В марте 2015 года одобрен для лечения пациентов с плоскоклеточным НМРЛ, устойчивым к химиотерапии.
Пемброзилумаб (Pembrolizumab, Кейтруда, Keytruda). Препарат был одобрен FDA для лечения меланомы в сентябре 2014 года, а для лечения немелкоклеточного рака легкого — в октябре 2014 года.
Лечебные вакцины
Задача лечебных вакцин — активировать B- и T-лимфоциты, чтобы они могли атаковать определенные типы раковых клеток. Для этого в организм пациента вводят соответствующий антиген. Мишенью для лечебных вакцин являются общие или опухоль-специфические антигены, такие как:
- MAGE-3 — экспрессируется в 42% случаев рака легких;
- NY-ESO-1 — экспрессируется в 30% случаев рака легких;
- р53 — мутирует в 50% случаев рака легких.

Адаптивный перенос Т-лимфоцитов
Четвертым направлением иммунотерапии рака легкого является адаптивный перенос T-лимфоцитов. Иммунные клетки, полученные от пациента, подвергают генетической модификации или обработке специальными веществами — таким образом их «обучают» атаковать раковые клетки. Затем Т-лимфоциты вводят обратно в организм. Это повышает иммунный ответ, направленный против опухолевой ткани, и помогает бороться с раком.
Лечение рака легких в «Евроонко»
Ученые, которые занимаются исследованиями в области иммунотерапии рака легкого и других злокачественных опухолей, сталкиваются с рядом сложностей. Далеко не все попытки увенчиваются успехом, не все предположения оказываются верны при проверке на практике. Исследования занимают много времени, требуют больших затрат и задействования многих ресурсов. Самые мощные препараты зачастую имеют серьезные побочные эффекты и могут применяться не у всех пациентов.
Несмотря на это, наука постоянно движется вперед. Иммунотерапия имеет большие перспективы. Многие препараты уже одобрены и успешно применяются в онкологических клиниках — они помогают улучшить прогнозы, продлить жизнь пациентов.
«Зепзелка»: новое лекарство против мелкоклеточного рака легкого
…должно стать новым стандартом терапии второй линии вместо топотекана.
Главное
- «Зепзелка» (Zepzelca, лурбинектедин) — новый лекарственный препарат, предназначенный для терапии взрослых пациентов с метастатическим мелкоклеточным раком легкого, который прогрессировал во время или после платиносодержащей химиотерапии. Новинка, разработанная испанской «ФармаМар» (PharmaMar) и продвигаемая «Джаз фармасьютикалс» (Jazz Pharmaceuticals), одобрена Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA). Регулятор вынес положительный вердикт в ускоренном порядке, то есть «Зепзелка» предстоит окончательно подтвердить собственную эффективность.
- «Зепзелка» стал альтернативной терапией второй линии мелкоклеточного рака легкого, новых способов лечения которого не предлагалось вот уже как два десятка лет. До появления лурбинектедина второлинейное ведение этого онкологического заболевания, чувствительного к платиносодержащей химиотерапии, осуществлялось топотеканом. Для резистентной к химиопрепаратам на основе препаратов платины патологии вариантов лечения предложено не было.
- Мелкоклеточный рак легкого (МРЛ) — высокозлокачественная эпителиальная опухоль, состоящая из мелких клеток со скудной цитоплазмой, неясными клеточными границами, мелкозернистым ядерным хроматином и отсутствующими или незаметными ядрышками. МРЛ, на долю которого приходится 13-15% всех случаев рака легкого, характеризуется стремительным удвоением опухолевых клеток, высокой ростовой фракцией (пролиферативным пулом), распространенными метастазами уже на ранних стадиях заболевания. В более чем 90% случаев мелкоклеточного рака легкого он встречается у курильщиков, включая бывших. Медиана выживаемости при МРЛ, оставляемом без лечения после постановки диагноза, ограничена двумя-четырьмя месяцами. Пятилетняя общая выживаемость при МРЛ в целом составляет 6,3%: при локализованном заболевании — 27,3%, с отдаленным метастазированием — 2,8%.
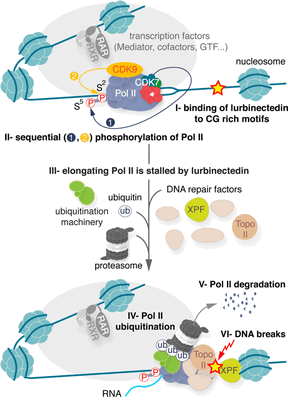
Лурбинектедин: механизм действия
Мелкоклеточный рак легкого почти неизлечим ввиду отсутствия подходящих молекулярных мишеней, на которые могли бы таргетироваться лекарственные препараты. Но поскольку это заболевание является зависимым от регуляторов онкогенной транскрипции, имеет смысл их блокировать.
Лурбинектедин (lurbinectedin, PM1183), ранее проходивший под брендовым названием «Зепсир» (Zepsyre), представляет собой селективный ингибитор онкогенных транскрипционных программ, от работы которых зависит выживаемость многих солидных опухолей. Лурбинектедин относится к классу алкилирующих антинеопластических препаратов.
Лурбинектедин подавляет активную транскрипцию в опухолевых клетках путем избирательного ковалентного связывания с CG-насыщенными ДНК-последовательностями, необратимого торможения и деградации элонгирующей РНК-полимеразы II на матрице ДНК, генерации XPF-зависимых одно- и двухцепочечных разрывов ДНК. Итогом становится апоптоз раковых клеток. Молекула не затрагивает РНК-полимеразу I или митохондриальную РНК-полимеразу и не влияет на базальную транскрипцию. Лурбинектедин оказывает селективный апоптоз-индуцирующий эффект на мононуклеарные фагоциты и ингибирует выработку воспалительных цитокинов.
Путем сдерживания активной транскрипции в опухолеассоциированных макрофагах (TAM) лурбинектедин оказывает влияние на опухолевое микроокружение, сдерживая экспрессию:
- интерлейкина 6 (IL-6) и интерлейкина 8 (IL-8), индуцирующих пролиферацию опухолевых клеток;
- хемокина ССL2 и IL-6, ингибирующих иммунный ответ и активирующих иммунные контрольные точки;
- фактора роста эндотелия сосудов (VEGF) и IL-8, способствующих ангиогенезу.
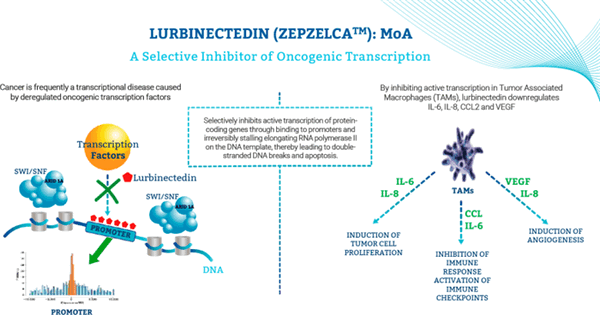
Лурбинектедин является синтетическим аналогом трабектедина (trabectedin) — природного тристетрагидроизохинолинового алкалоида, выделенного из морского беспозвоночного обитателя Карибского бассейна Ecteinascidia turbinata. Трабектедин одобрен в октябре 2015 года под названием «Йонделис» (Yondelis) и продвигается совместно с «Янссен» (Janssen) в составе «Джонсон энд Джонсон» (Johnson & Johnson) для лечения неоперабельной или метастатической липосаркомы или лейомиосаркомы после курса антрациклинов. Структурное различие между молекулами очень незначительно, однако их фармакологические характеристики разнятся существенно, обеспечивая лурбинектедину усиленную противоопухолевую активность на фоне сниженной токсичности и повышенной максимально переносимой дозы.
Мелкоклеточный рак легкого
Среди всех злокачественных новообразований легкого на долю мелкоклеточного рака приходится около 15%. Тем не менее, эта форма отличается высокой агрессивностью, быстрым течением и далеко не всегда поддается лечению. Поэтому врачи и ученые активно изучают данное заболевание, разрабатывают новые методы диагностики и создают современные препараты, которые помогли бы улучшить показатели выживаемости.
Морфологически этот вид рака характеризуется образованием опухолевых клеток небольшого размера, большую часть которых занимает ядро. По одной теории, их предшественниками являются клетки эпителия бронхов, которые имеют схожее строение. Другая теория рассматривает в качестве предшественников APUD-клетки, которые являются составной частью диффузной эндокринной системы легкого.
Причины возникновения мелкоклеточного рака легкого
Чаще всего заболевание выявляется у курящих мужчин, возраст которых составляет от 40 до 60 лет. Именно этим двум факторам (связь с курением и возраст) отводится главная роль в структуре причин возникновения мелкоклеточного рака легкого. В последние десятилетия отмечается увеличение числа курящих женщин, поэтому их доля в структуре заболеваемости постепенно увеличивается. Среди других факторов, которые могут способствовать развитию мелкоклеточного рака отмечаются:
- Неблагоприятная экологическая обстановка.
- Работа во вредных условиях труда.
- Отягощенный наследственный анамнез (выявление у близких родственников рака легкого или других онкологических заболеваний).
- Влияние на организм ионизирующего излучения.
- Сопутствующие заболевания легких (туберкулез, ХОБЛ).
Чем больше на человека воздействует неблагоприятных факторов, тем выше риск развития рака легкого.
Симптомы заболевания
У большинства пациентов на начальных стадиях рака какие-либо клинические проявления отсутствуют. У курильщиков может отмечаться продолжительный кашель, который они связывают с бронхитом и другими последствиями этой пагубной привычки. Другим характерным симптомом является появление крови в мокроте. Именно в этот момент пациент должен насторожиться и как можно скорее обратиться к врачу. Дополнительно могут отмечаться боли в области грудной клетки, одышка, слабость, быстрая утомляемость и др.
Симптомы рака легких на более поздних стадиях обусловлены распространением процесса на соседние органы и ткани. В таких случаях могут отмечаться следующие проявления:
- Осиплость голоса.
- Дисфагия (нарушение глотания).
- Сдавление верхней полой вены.
- Синдром Кушинга и др.
При распространении (метастазировании) мелкоклеточного рака в другие органы, развиваются специфические симптомы, например, желтуха. Могут возникать неврологические нарушения, боль в позвоночнике и т. д.
Стадии и виды мелкоклеточного рака легкого
Классификация болезни проводится по нескольким параметрам. Как и для других видов рака, актуальной является TNM-классификация, которая учитывает особенности роста опухоли и ее распространение по организму. Буква Т описывает первичный опухолевый очаг в следующих вариантах:
- Х — раковые клетки не обнаружены или недостаточно данных для оценки мелкоклеточного рака.
- 0 — первичный очаг не выявлен.
- Is (рак in situ) — рак легкого не распространяется на соседние ткани и ограничен небольшой группой клеток.
- 1 — размер опухоли легкого не превышает 3 см, и она не переходит на главный бронх.
- 2 — размер опухоли более 3 см, она не распространяется на все легкое.
- 3 — опухоль может иметь любой размер и распространяться на диафрагму, плевру, перикард и др.
- 4 — В этом случае первичный очаг мелкоклеточного рака легкого поражает средостение, сердце, пищевод и другие жизненно важные органы.
N описывает состояние регионарных лимфоузлов. Если недостаточно объективных данных для изучения их состояния, то присваивается индекс «Х», если признаков распространения рака легкого не обнаружено, то присваивается индекс «0». В остальных случаях, в зависимости от объема поражения и распространения процесса, присваивается индекс от 1 до 3.
М описывает процесс метастазирования рака легкого. Как и в предыдущих случаях, индекс «Х» и «0» ставятся тогда, когда недостаточно данных для выявления метастазов или они не обнаружены. При наличии метастазов рака в отдаленных органах и тканях, ставится индекс «1». Если они не выходят за пределы грудной клетки, то индекс меняется на «1а», а если выходят за пределы грудной клетки, то он изменяется на «1b». Таким образом, диагноз Т2N1M0 можно интерпретировать следующим образом: мелкоклеточный рак легкого, размер первичного очага более 3 см, который прорастает плевру, но не поражает все легкое, с поражением регионарных лимфоузлов, без признаков отдаленных метастазов.
По совокупности показателей T, N, и M, мелкоклеточный рак легкого делится на 4 стадии. На первой — размер опухоли не превышает 3 см, она локализована в пределах одного сегмента, метастазы (регионарные и отдаленные) не выявляются. Для второй стадии рака характерны размеры до 6 см и могут быть единичные метастазы в близлежащих лимфоузлах (N0-1). На третьей стадии опухоль превышает 6 см и характеризуется инвазивным ростом — переходит на соседние доли, поражает главный бронх и может давать метастазы в отдаленные лимфоузлы. Четвертая стадия заболевания характеризуется распространением за границы грудной клетки с множественными отдаленными метастазами и тяжелыми осложнениями.
Гистологическая классификация мелкоклеточного рака подразумевает его деление на овсяноклеточный, веретеноклеточный и плеоморфный, в зависимости от клеточного строения опухоли.
Методы диагностики
Для того, чтобы установить точный диагноз, определить стадию мелкоклеточного рака и подобрать лечение, назначается комплексная диагностика. На первом этапе необходимо выявить опухоль, установить ее точную локализацию, размеры, особенности роста. С этой целью назначают лучевую диагностику (рентген и КТ грудной клетки), МРТ легких, ПЭТ-КТ и т. д.

Далее врач должен подтвердить диагноз мелкоклеточного рака морфологически. Для этого необходимо взять образец ткани и исследовать его под микроскопом. Получить материал позволяют следующие методы:
- Биопсия легкого при диагностической торакоскопии.
- Бронхоскопия с биопсией.
- Биопсия лимфоузла.
- Плевральная пункция с забором экссудата.
После выполнения данных исследований можно подтвердить или опровергнуть диагноз мелкоклеточного рака. Однако для того, чтобы узнать, насколько распространен опухолевый процесс, может потребоваться пройти дополнительную диагностику. В частности, выявить наличие метастазов могут помочь такие методы, как сцинтиграфия костей, МРТ головного мозга, МСКТ брюшной полости и др.
В комплексный план диагностики мелкоклеточного рака обязательно включаются лабораторные методы — общий и биохимический анализ крови, анализ мочи, определение уровня онкомаркеров и т. д. Эти исследования помогут получить дополнительную информацию о состоянии здоровья пациента, отследить динамику изменений после лечения, а также своевременно выявлять осложнения рака. Точный план обследования всегда составляется индивидуально для каждого пациента.
Как лечат мелкоклеточный рак легкого
Тактика лечения во многом зависит от установленного диагноза. Хирургическому лечению поддаются лишь ранние стадии мелкоклеточного рака. При этом оперативное вмешательство обязательно дополняется послеоперационной полихимиотерапией или лучевой терапией. В таком случае можно добиться увеличения показателей выживаемости.
Отличительной особенностью мелкоклеточного рака легкого является высокая вероятность метастазирования, поэтому достаточно эффективным вариантом лечения оказывается химиотерапия. При этом, редко назначается одно лекарственное средство. Наиболее распространены схемы лечения рака, в которых применяют препараты на основе платины в сочетании с ингибиторами топоизомеразы II. Такой вид лечения позволяет подавить деление клеток мелкоклеточного рака и остановить прогрессирование заболевания. Химиотерапия назначается курсами (до 6-7) с интервалом между ними около месяца.
Одним из активно развивающихся направлений является таргетная терапия. Она подразумевает применение моноклональных антител, которые «заставляют» иммунную систему атаковать клетки рака легкого. Среди других методик могут применяться фотодинамическая терапия, лучевая терапия и др. Лечение мелкоклеточного рака легкого может выполняться и с паллиативной целью. В этом случае речь идет об улучшении качества жизни пациента.
Прогноз и продолжительность жизни
Как и при других видах рака, у пациентов со злокачественными новообразованиями легкого оценивают пятилетнюю выживаемость. Этот показатель зависит от многих факторов — особенностей опухоли, вида лечения, возраста пациента и др. Например, при удалении опухоли на ранней стадии с последующим применением полихимиотерапии, показатель пятилетней выживаемости составляет около 40%.
Если мелкоклеточный рак легкого был диагностирован на более поздних стадиях, то комбинированное лечение позволяет продлить жизнь пациенту на 1.5-2 года. В самых сложных и запущенных случаях, когда рак легкого быстро метастазирует и не поддается лечению, выживаемость не превышает нескольких месяцев.
Лечение рака легкого
Рак легких — одно из самых распространенных онкозаболеваний во всем мире. Ежегодно он уносит больше жизней, чем в совокупности рак кишечника, предстательной железы, молочных желез и яичников. Основной фактор риска — курение. Чем дольше человек курит и чем больше сигарет выкуривает ежедневно, тем выше у него риск возникновения злокачественной опухоли в легких. Расставаться с вредной привычкой не поздно ни в каком возрасте: в любом случае риски постепенно снизятся.
Причины рака легкого
В случае с большинством онкологических заболеваний корректнее говорить не о причинах, а о факторах риска. Они не приводят к раку со стопроцентной вероятностью, но повышают риск заболеть:
- Как мы уже упомянули, основной фактор риска рака легких — курение. Причем, не только активное, но и пассивное. Если рядом с вами постоянно кто-то курит, ваше здоровье в опасности.
- Некоторые люди на рабочем месте контактируют с такими веществами, как асбест, никель, хром, мышьяк. Эти канцерогены повышают риск рака легких.
У некоторых людей отягощенная наследственность. Риски повышены, если злокачественная опухоль в легких диагностирована у одного из родителей, родного брата или сестры. - В почве, скальных породах и воде содержится небольшое количество урана. Он распадается с образованием газа радона, который затем попадает в воздух. Иногда он скапливается в помещениях в опасных концентрациях.
Прогноз при раке легкого
Серьезность прогноза предстоящей жизни при диагностированном раке легкого для жизни очевидна. Обычно для оценки прогноза опухоли используется показатель пятилетней выживаемости, он зависит от вида опухоли, стадии заболевания и наличия (распространенности) метастазов.
На ранних стадиях заболевания (немелкоклеточный рак легкого в первой стадии) 5-летняя выживаемость при раке легких отмечается примерно у 60% пациентов; во II стадии — примерно у 40% пациентов, в IIIa стадии — около 15%. На поздних стадиях заболевания шансы достигнуть 5-летней выживаемости стремятся к нулю.
Мелкоклеточный рак легкого наиболее «злой» из известных видов опухолей легких, в зависимости от распространенности дающий от 1 до 5% 5-летней выживаемости. При этом наиболее чувствителен и к химио- и к лучевой терапии, поэтому рано начатое лечение существенно улучшает прогноз при мелкоклеточном раке легкого 1-3 стадии..
Успешное лечение немелкоклеточного рака легкого зависит от возможности проведения адекватного хирургического пособия. Своевременное применение современных схем полихимиотерапии в совокупности с таргетными препаратами увеличивает продолжительность жизни до 6-8 месяцев, а у 20-25% пациентов — свыше года.
Виды злокачественных опухолей легких
Выбор тех или иных методов лечения сильно зависит от того, какой тип рака легких обнаружен у пациента. Выделяют два основных типа, в зависимости от того, как раковые клетки выглядят под микроскопом:
- Чаще всего встречается немелкоклеточный рак легкого, который включает разные подтипы опухолей:плоскоклеточный рак, аденокарциному, крупноклеточный рак.
- Менее распространен мелкоклеточный рак легкого. Он встречается практически только у курильщиков.
Методы лечения рака легких
К сожалению, психологический шок, вызываемый диагнозом онкологического заболевания вообще и рака легких в частности, лишает многих людей способности трезво оценивать ситуацию и доверять мало-, а то и совсем непроверенным методам народной медицины.
Вокруг лечения онкологии легких существует множество не имеющих под собой никакого основания мифов об эффективности лечения березовым грибом, настойками лопуха, календулы с ромашкой, мухоморов, водки с прополисом, вплоть до самых анекдотичных методов.
Современная доказательная медицина в обосновании лечения онкологии легких исходит из строго научного обоснования применения тех или иных протоколов. Основой выбора, осуществляемого лечащим врачом, служит морфологическая характеристика опухоли, ее распространенность, наличие или отсутствие метастазов, общее состояние больного.
Хорошо известно, что мелкоклеточный вариант заболевания лучше поддается лечением химиотерапии, а немелкоклеточные варианты предполагают оперативное лечение или комбинированные схемы, в зависимости от стадии и распространенности.
Помимо хирургического лечения при раке легкого могут использоваться различные программы лучевой терапии в сочетании с химиотерапией. Психологические сложности и душевные переживания, возникающие у пациента и родственников, помогут решить специалисты-психоонкологи.

Химиотерапия при раке легкого
В последнее время наиболее перспективными для лечения немелкоклеточного рака считаются таргетные препараты (небольшие молекулы и моноклональные антитела, целенаправленно действующие на определенные тканевые мишени — фактор роста эпителия и образования новых сосудов в злокачественной опухоли. Препараты этого ряда гефитиниб (Иресса) и эрлотиниб (Тарцева) используют в качестве терапии второй или третьей линии при некоторых видах рака легких, экспрессирующих определенный вид рецепторов - EGFR. В значительном количестве случаев химиотерапия позволяет не только добиться уменьшения размеров опухоли, предупреждения ее метастазирования и восстановления качества жизни, но и добиться стойкой долгосрочной ремиссии или выздоровления пациента.
- Условия клиники позволяют проводить как неоадъювантную, так и адъювантную химиотерапию любого уровня сложности и комплексности, как в условиях стационара, так и в амбулаторно в условиях дневного стационара.
- Выбор оптимального курса химиотерапии (в соответствии с точным диагнозом, гистологией опухоли, конкретной стадией болезни у конкретного пациента) проводится строго по международным протоколам, которые показали свою эффективность в рандомизированных двойных слепых контролируемых клинических исследованиях.
- Применяются препараты последнего поколения, обладающие наибольшей эффективностью и наименьшим токсическим эффектом, «под прикрытием» поддерживающей терапии, минимизирующей побочные действия химиопрепаратов на клетки крови и внутренние органы.
- По показаниям устанавливаются индивидуальные одноразовые помпы, позволяющие обеспечить равномерное введение препаратов в течение длительного периода времени, либо автоматические дозаторы. В ряде случаев устанавливается специальная инфузионная порт-система для химиотерапии.
- При развитии и рецидивировании опухолевого плеврита (канцероматозе плевры) в клинике возможно проведение паллиативных хирургических вмешательств (торакоцентез, облитерация грудной полости).
В сложных, сомнительных и противоречивых случаях возможно привлечение внешних консультантов — ведущих химиотерапевтов России, а также клиник Швейцарии и США. При необходимости мы проводим консилиумы с зарубежными коллегами, с целью получить «второе мнение» докторов из США и Европы.
Хирургическое лечение рака легкого
Немелкоклеточный рак легкого поддается хирургическому лечению, как правило, лучше, чем мелкоклеточный. В зависимости от размеров и расположения опухоли, врач может удалить ее, захватив некоторое количество здоровой ткани вокруг, или полностью удалить легкое. Обычно хирургическое вмешательство дополняют курсом адъювантной химиотерапии или лучевой терапии. Это помогает уничтожить оставшиеся раковые клетки и снизить вероятность рецидива.
В настоящее время хирурги все чаще применяют миниинвазивные вмешательства, когда на стенке грудной клетки делают прокол, и внутрь вводят гибкий тонкий торакоскоп, оборудованный источником света и видеокамерой.
Иногда при немелкоклеточном раке легкого прибегают к лечению радиочастотной аблацией. В опухоль вводят тонкую иглу и подают на нее электрический ток, который сжигает раковые клетки.
Мелкоклеточный рак значительно чаще по сравнению с немелкоклеточным является неоперабельным. Приходится прибегать к другим методам лечения.
Лучевая терапия при раке легкого
Лучевая терапия эффективна как при немелкоклеточном, так и при лечении мелкоклеточного рака легкого. Врач может назначить этот метод лечения с разными целями:
- Перед хирургическим лечением (неоадъювантная лучевая терапия). Это помогает сократить опухоль в размерах, хирургу становится проще ее удалить, а пациент лучше переносит вмешательство.
- После хирургического лечения (адъювантная лучевая терапия). Нужна для того, чтобы уничтожить опухолевые клетки, которые остались в организме после операции, и предотвратить рецидив.
- В качестве самостоятельного метода лечения для борьбы с симптомами запущенного рака легкого: болью, кровотечением и др.
Иногда курс лучевой терапии сочетают с химиотерапией. Такое лечение называется химиолучевой терапией.
Таргетная терапия при раке легкого
Чтобы бесконтрольно размножаться, выживать и защищаться от иммунной системы, раковые клетки используют некоторые молекулярно-генетические механизмы. Знания о них помогают создавать особые таргетные препараты. По сравнению с химиопрепаратами, они действуют более прицельно, блокируют лишь определенные вещества, которые находятся в раковых клетках.

При раке легкого применяют следующие таргетные препараты:
- Блокаторы ангиогенеза (роста новых сосудов в злокачественной опухоли): бевацизумаб (Авастин), рамуцирумаб (Цирамза).
- Блокаторы EGFR (белка-рецептора, который в норме активирует деление клеток, а в раковых клетках становится слишком активным и способствует их бесконтрольному размножению): эрлотиниб (Тарцева), афатиниб (Гилотриф), гефитиниб (Иресса).
- Блокаторы ALK (мутантного белка, который обычно возникает у некурящих людей и тех, которые курят понемногу): кризотиниб (КСАЛКОРИ), церитиниб (Зыкадия), алектиниб (Алеценса), бригатиниб (Алунбриг).
- Блокаторы BRAF (мутантный белок, который заставляет клетки бесконтрольно размножаться): дабрафениб (Тафинлар), траметиниб (Мекинист).

Раковое поражение плевры
Лечение пациентов с опухолевым плевритом начинается с плевроцентеза — эвакуации жидкости из плевральной полости, что сразу приводит к улучшению самочувствия, уменьшению одышки, болей и улучшению качества жизни больного. Исследование удаленной жидкости, проводимые непосредственно после плевроцентеза позволяет более точно установить причину опухолевого плеврита. Уточнить степень распространенности не только плеврита, но и специфических изменений, которые вызвали это состояние помогает целый арсенал современных методов исследования, доступный пациентам клиники (рентгенологическое исследование, компьютерная томография органов грудной полости, ультразвуковое исследование и пр.).
Через некоторое время после пункции в плевральной полости может снова скапливаться выпот. Если жидкость нужно повторно вывести менее чем через месяц после плевроцентеза, врач может установить внутриплевральную порт-систему - небольшую титановую емкость с силиконовой мембраной, которую помещают под кожу и соединяют катетером с плевральной полостью. В дальнейшем, для того чтобы вывести плевральный выпот, нужно всего лишь нащупать под кожей мембрану порт-системы и ввести в нее специальную иглу.
Также через внутриплевральную порт-систему можно вводить химиопрепараты. Внутриплевральная химиотерапия помогает уменьшить образование выпота. Она особенно эффективна у больных с мезотелиомой, раком легкого и молочной железы.
При необходимости возможно проведение видеоторакоскопии, которая позволяет исследовать плевральную полость через прокол в грудной стенке с помощью специального инструмента - торакоскопа произвести прицельную биопсию подозрительного участка ткани с последующим морфологическим исследованием, что в большинстве случаев позволяет установить точный диагноз.
Системная химиотерапия не только воздействует на саму раковую опухоль, но и при хорошей чувствительности к химиопрепаратам может привести к ликвидации плеврита у большинства пациентов.
Плевродез
При невозможности химиотерапии возможно проведение плевродеза в результате которого листки плевры спаиваются между собой за счет введения различных химических веществ с местным противоопухолевым действием.
Внутриплевральная терапия при раке может быть дополнена иммунотерапией LAK-клетками, рекомбинантным интерлейкином - 2 или их сочетанием.
Выбор в пользу того или иного варианта иммунотерапии или последовательности иммунотерапевтического воздействия проводится онкологом на основании результатов обследования пациента с учетом скорости накопления жидкости, общего состояния, чувствительности к химиопрепаратам, ранее проводимого лечения и т.д.). Плевроцентез проводится опытными специалистами при помощи специального устройства Pleurocan (США) и только под ультразвуковой навигацией, что обеспечивает безопасность, быстроту и точность вмешательства.
Лечение рака легких 4 стадии с метастазами
На 4 стадии рака легкого (распространенной по организму опухоли), возможно паллиативное или симптоматическое лечение в Москве. Паллиативное лечение — это вынужденный подход, при невозможности имеющимися на сегодняшний день средствами победить онкологию, оно направлено на уменьшение страданий, продление и улучшение качества жизни больных. Наши пациенты получают адекватное обезболивание, кислородотерапию, детоксикацию, при необходимости проводятся паллиативные операции (наложение трахеостомы, торакоцентез, плевродез и т.д.). При раковых пневмониях осуществляется все необходимое противовоспалительное лечение, при легочных кровотечениях — гемостатическая терапия.
Паллиативное лечение рака легкого
Отделение симптоматической и паллиативной терапии клиники располагает всеми необходимыми возможностями ухода за тяжелобольными пациентами, не способными себя обслужить, включая дополнительное наблюдение за пациентом силами патронажной сестры, медицинской сестры или врача-реаниматолога.
Используются современные европейские протоколы интенсифицированного лечения больных злокачественными заболеваниями легкого для уменьшения массы опухоли и торможения темпов ее роста. При необходимости производится эвакуация полостных выпотов, различные виды обезболивания, дезинтоксикационная, противорвотная терапия, общеукрепляющее лечение, многокомпонентная терапия, направленная на поддержку функционирования жизненно важных органов (сердца, печени, почек, легких), предпринимаются все меры, направленные на улучшение самочувствия и качества жизни больного.
Правильное лечение рака легких 4 степени с метастазами помогает продлить жизнь пациента, повысить её качество. В современной онкологии изменилось само понимание неизлечимых злокачественных опухолей. Такой диагноз воспринимается не как приговор, а как хроническое заболевание, при котором пациенту все еще можно помочь. В «Евроонко» для этого есть всё необходимое.
Этапы лечения на разных стадиях
Если подводить итог всему вышесказанному, то лечение злокачественных опухолей легких в зависимости от стадии будет выглядеть следующим образом:
- При раке стадии 0, когда опухоль не прорастает за пределы слизистой оболочки, обычно ограничиваются хирургическим вмешательством. Лучевая терапия и химиотерапия не требуется.
- На стадии 1 также зачастую ограничиваются хирургическим лечением. При высоком риске рецидива проводят адъювантную химиотерапию или лучевую терапию. Во время операции может быть удалена доля или меньшая часть легкого, а также некоторые лимфоузлы, которые находятся в средостении.
- На 2 стадии перед хирургическим вмешательством врач может назначить курс неоадъювантной химиотерапии или лучевой терапии. Объем операции может быть разным, вплоть до удаления всего легкого. После удаления опухоли всегда проводят курс химиотерапии, иногда — лучевой терапии.
- Лечение рака легкого 3 стадии начинают с химиотерапии и лучевой терапии. Затем, если опухоль может быть удалена, и состояние пациента позволяет, проводят операцию. В противном случае лучевая терапия и химиотерапия становятся основными методами лечения рака легких 3 степени..
- При немелкоклеточном раке легкого 4 стадии проводится паллиативная и симптоматическая терапия.
Врачи «Евроонко» знают, как помочь
Мы уверены, что помочь можно всегда, поэтому беремся за лечение пациентов с раком легкого на любой стадии:
Где лучше лечить рак легкого: в России или за границей?

Среди российских онкобольных, решивших лечиться за границей, наибольшей популярностью пользуются израильские, европейские, в меньшей степени (из-за высокой стоимости услуг) — американские клиники. Несомненно, за рубежом зачастую можно получить более качественную медицинскую помощь.
Но и в России есть клиники, где доступны практически те же процедуры, препараты, врачи работают по международным протоколам, у нас есть все необходимое. Здесь лечат не хуже, чем в известных европейских или израильских клиниках. Причем, для пациента это обходится дешевле.
Больных регулярно консультируют наши коллеги из-за рубежа. А в случаях, когда это действительно необходимо, мы помогаем нашим пациентам получить медицинские услуги за границей у ведущих специалистов.
Читайте также:
- Анатомия: Развитие вилочковой железы (тимуса). Функция, сосуды (кровоснабжение), нервы (иннервация) вилочковой железы (тимуса)
- Техника тимпанопластики без разреза кожи наружного слухового прохода
- Хиломикроны. ЛПОНП. ЛПНП. ЛПВП.
- Варианты сочетания лучевой и химиотерапии опухоли головы и шеи
- Преждевременное половое созревание: причины, симптомы и лечение
