Клиника ( проявления ) синдрома длительного сдавления ( СДС ). Диагностика краш-синдрома ( сдс )..
Добавил пользователь Евгений Кузнецов Обновлено: 28.01.2026
Массовые аварии и катастрофы, стихийные бедствия и землетрясения, завалы в шахтах и карьерах, военные действия являются главными причинами развития синдрома длительного сдавления тканей (СДС) у пострадавших. При землетрясении в Армении почти у четверти пострадавших отмечалось длительное сдавление тканей обломками зданий, которое в дальнейшем привело к развитию СДС. Нижние конечности повреждаются в 5—6 раз чаще, чем верхние.
Что такое СДС
СДС имеет и другие названия: синдром длительного раздавливания, синдром освобождения, краш-синдром. Разновидностью СДС является синдром позиционного сдавления. Он развивается при длительном сдавлении руки или ноги массой тела пострадавшего. Чаще эго происходит при алкогольном опьянении, меди каментозном отравлении или потере сознания.
СДС (синдром длительного сдавления тканей) — это своеобразный вариант травматической болезни, который развивается в результате длительной ишемия и сдавления мягких тканей и перелома костей конечностей, травматизации нервных стволов, интоксикации метаболитами разрушенных тканей.
Патогенез
Патогенез СДС определяют два основных момента: сильное сдавление и длительная ишемия тканей. Ведущими звеньями патогенеза СДС являются:
- гиповолемический шок,
- эндогенная интоксикация метаболитами и гуморальными агентами,
- метаболический дисбалансный каскад, (ПОН),
- и прежде всего острая почечная недостаточность (ОПН),
- ДВС-синдром,
- болевой фактор.
Длительное сдавление конечности вызывает грубые нарушения циркуляции крови в сосудах, в дальнейшем нарушается и микроциркуляция. Резкое замедление кровотока способствует образованию микротромбов в просвете сосудов, которые при освобождении конечности и восстановлении перфузии с током крови распространяются в различные органы, что приводит к нарушению их функций и способствуют развитию полиорганной недостаточности. Грубые нарушения микроциркуляции сопровождаются повышением проницаемости сосудистой стенки, что проявляется бурным нарастанием отека освобожденной конечности.
При этом плазмопотеря может достигать 25—35 % ОЦК. Кроме того, в просвете микрососудов при сдавлении образуется избыточное количество глобулдезэмульгированного жира, которые при восстановлении кровотока попадают в легкие, почки, мозг, печень и нарушают их функциональную активность. Последствия ишемического повреждения мышц проявляются не сразу, а спустя несколько часов после сдавления.
При преимущественно травматическом разрушении мышечной ткани, костей и нервов к ишемическому фактору присоединяются неспецифические реакции организма на травму, которые могут носить характер шоковых и развиваться довольно быстро. В этом случае может быстро наступить смерть, даже при непродолжительном сдавлении.
Ишемическое и травматическое повреждение мышечной ткани приводит к грубым нарушениям метаболизма в ней, образованию и выбросу в общий кровоток таких «тканевых ядов», как гистамин, серотонин, брадикинин и т. д. Установлено, что все названные вещества проявляют высокую специфическую активность по отношению к гладкомышечной ткани сосудов. Так, брадикинин вызывает длительный паралич сфинктеров микрососудов, в результате чего значительная часть ОЦК депонируется и выключается из кровотока, что поддерживает состояние гиповолемии. Одновременно брадикинин повышает порозность сосудистой стенки, что способствует выходу жидкой части крови в интерстиций. Кроме того, брадикинин является чрезвычайно сильным специфическим раздражителем нервных окончаний, что в сочетании с прямым травмирующим моментом вызывает сильную болевую реакцию. Но по мере гибели нервных окончаний в условиях ишемии уровень болевой реакции снижается вплоть до полной анестезии.
В результате потери плазмы нарастает гемоконцентрация, снижается резистентность эритроцитов и они разрушаются, что способствует развитию гемолиза и анемии. Высвобождение гемоглобина является одним из факторов, способствующих нарушению выделительной функции почек. Оно развивается в результате закупорки почечных канальцев. Анемия становится неотъемлемым спутником СДС. Однако в первые сутки лабораторными методами ее обнаружить не удается (вследствие гемоконцентрации).
Из зоны поврежденных тканей в кровоток поступает большое количество тромбопластических веществ, активирующих гемокоагуляцию и развитие ДВС-синдрома. Повышение вязкости и свертываемости крови существенно ухудшает ее реологические свойства, что также играет важную роль в развитии шока.
В плазме крови повышается уровень креатина, что свидетельствует о глубоком повреждении тканей. Нарушение углеводного и жирового обмена в ишемизированных тканях сопровождается избыточным образованием лактата, пирувата и других составляющих метаболического ацидоза, выходок из клеток многих ферментов, калия, фосфора. Особое значение имеет высвобождение и поступление в ток крови мышечного пигмента миоглобина.
Миоглобин также обтурирует сосуды почек, легких, печени и других внутренних органов, способствуя развитию ПОН. Молекулы миоглобина вследствие малой величины могут фильтроваться через почечные клубочки и частично реабсорбироваться канальцевой системой. Но в кислой среде при метаболическом ацидозе миоглобин превращается в солянокислый гематин, который непосредственно обтурирует восходящее колено петли Генле и вызывает воспалительно-дегенеративные изменения в почечном эпителии вплоть до некроза. Попадание миоглобина в просвет канальцев, гипоперфузия почек и высвобождение эндогенных медиаторов являются патогенетическими факторами острой почечной недостаточности.
В ишемизированной конечности многократно увеличивается содержание гуморальных агентов (эндотоксина, фактора некроза опухолей — TNF, интерлейкинов, фрагментов комплемента и др.). Уже через 2 ч при ишемии отмечается 15-кратное повышение уровня TNF в оттекающей венозной крови. При этом в 3 раза увеличивается проницаемость сосудистой стенки и на 70 % снижается региональный кровоток в ишемизированной конечности. Предполагается, что TNF и другие гуморальные агенты, высвобождающиеся из поврежденных конечностей при реперфузии, способствуют системному повреждению тканей, развитию ПОН, феномена невосстановления кровотока, гиповолемического шока, сердечно-легочной недостаточности. Возможна даже внезапная смерть.
Важными факторами, способствующими развитию сердечной недостаточности, являются резкое повышение содержания калия в сыворотке крови, нарушение соотношения калия и натрия, кальция и других электролитов в условиях метаболического ацидоза при реперфузии сдавленных тканей.

Симптомы
В клинике СДС тканей выделяют три довольно типичных периода.
Ранний период (до 3 сут после травмы). Преобладают явления шока на фоне психоэмоциональных и нервно-болевых реакций. В первые часы после освобождения из-под завалов пострадавшие возбуждены или заторможены, жалуются на боль и нарушение движений в травмированной конечности.
Общее состояние некоторое время может оставаться стабильным. Местно отмечаются прогрессирующий отек конечности, гипо- или анестезия, ослабление или отсутствие сухожильных рефлексов, частичный или полный паралич. Однако в дальнейшем появляются слабость, холодный пот, нарастают заторможенность, бледность кожных покровов, последствия крово- и плазмопотери, нарушения внешнего дыхания, гемоконцентрация, гиперкалиемия, анемия, миоглобинемия, гемолиз. Моча темно-коричневого цвета из-за высокого содержания миоглобина, в ней много белка, эритроцитов и цилиндров. Возникают олигурия и анурия. Шок развивается лишь при тяжелых формах СДС.
Промежуточный период (3-и—14-е сутки). Наблюдаются такие проявления:
- острая недостаточность почек,
- ПОН,
- вялость, апатия, ,
- тошнота, рвота,
- анемия,
- ацидоз,
- гиперкалиемия,
- анурия, возможна уремическая кома.
Отек конечности нарастает вплоть до появления субэпидермальных пузырей и экстравазатов. Гемоконцентрация сменяется гемодилюцией, нарастают признаки печеночной недостаточности, нарушения гемостаза. ОПН может развиваться и при легких формах СДС, без клиники шока.
Восстановительный период (со 2-й недели до 2 мес) характеризуется нормализацией гемодинамических показателей, внешнего дыхания, функции почек и печени. Отмечаются осложнения в виде инфицированных ран, некроза тканей, гангрены, остеомиелита и т. п.
Помощь
Оказание медицинской помощи пострадавшим с СДС начинают с освобождения конечности. Однако это является пусковым механизмом развития заболевания. Поэтому до освобождения конечности выше сдавленной области необходимо наложить жгут, так как характер повреждений и степень сохранности конечности можно будет определить только после тщательного ее осмотра.
В идеальном варианте интенсивная терапия СДС должна начинаться до извлечения пострадавшего из-под завала (внутривенные инфузии, обезболивание и др.). После извлечения пострадавшего производят осмотр конечностей и решают вопрос о целесообразности использования жгута. Для этого необходимо определить степень сохранности конечности. Возможны следующие варианты:
1. Конечность сохранена, жизнеспособна, ишемия обратимая, компенсированная. Несмотря на длительное сдавление и ишемию необратимых изменений кровотока, метаболизма и структуры тканей не произошло, о чем свидетельствует наличие болевой и тактильной чувствительности, а также активных движений. Жгут необходимо срочно снять, иначе будет поддерживаться ишемия.
2. Конечность относительно сохранена, ишемия некомпенсированная. Тактильная и болевая чувствительность отсутствует, активных движений нет, но пассивные движения свободны, следовательно, трупного окоченения еще нет. Поэтому жгут также следует снять, чтобы не наступила гибель конечности.
3. Конечность омертвела, отмечается необратимая ишемия. Отсутствуют все виды чувствительности, а также активные и пассивные движения.
Развилось трупное окоченение мышц. Жгут остается на конечности вплоть до ее ампутации.
Разногласия по поводу наложения жгута на жизнеспособную конечность связаны с устаревшими представлениями о том, что жгут якобы предупреждает развитие токсемии. Упускается из виду то обстоятельство, что эндотоксины из ишемизированных тканей попадают в системный кровоток не только но кровеносным, но и по лимфатическим сосудам. Подтверждением этому положению служит высокая эффективность раннего применения лимфосорбции при лечении эндотоксикозов.
Жгут целесообразно оставлять на кровоточащих, размозженных или омертвевших конечностях.
Интенсивная терапия СДС
Интенсивная терапия СДС на догоспитальном этапе должна быть направлена на компенсацию основных патогенетических сдвигов.
Она включает следующее:
1. Уменьшение плазмопотери и восполнение ОПК.
С этой целью конечность необходимо плотно забинтовать, предварительно обработав раневые участки, произвести иммобилизацию и начать охлаждение. Адекватная скорость внутривенной инфузии для коррекции гиповолемии — 300—400 мл/ч. Из состава инфузионных сред полностью исключают растворы, содержащие калий. При переохлаждении пострадавшего инфузионные растворы подогревают до 36—38 °С.
2. Раннее ощелачивание организма. В целях коррекции метаболического ацидоза и предупреждения почечной недостаточности внутривенно вводят 200—300 мл 4 % раствора натрия гидрокарбоната, затем — по 100 мл на каждые 2 л вводимой жидкости. Если пострадавшие способны глотать, то натрия гидрокарбонат назначают внутрь по 2—4 г через каждые 3-4 часа. Однократно вводят 2 мл фуросемида (лазикса).
Использование наркотических анальгетиков нежелательно при видимых нарушениях внешнего дыхания и при необходимости последующей диагностики возможных сопутствующих повреждений головы и внутренних органов. Нейролептаналгезия опасна из-за наличия гиповолемии и вероятности развития гиповолемического шока. Препаратом выбора считается кетамина гидрохлорид (кеталар) в дозе 0,5—1 мг на 1 кг массы тела в сочетании с седуксеном. Возможен наркоз закисью азота в сочетании с кислородом. Эффективна футлярная блокада конечности 0,25 % раствором новокаина в дозе 200—400 мл. При открытых переломах костей проводят местную анестезию, вводят антибиотик широкого спектра действия.
4. Для снижения опасности гиперкалиемии внутривенно вводят 40— 60 мл 40 % раствора глюкозы с инсулином (1 ЕД на 5 г глюкозы), 20—40 мл 10 % раствора кальция хлорида или кальция глюконата.
5. Поддержание адекватной вентиляции легких.
6. Снижение проницаемости сосудистой стенки.
Назначают гормональные препараты, рутин и аскорбиновую кислоту. Показаны димедрол (1—2 мл 1 % раствора) или супрастин (1—2 мл 2 % раствора), которые вводят внутривенно или внутримышечно.
Пострадавших с СДС обязательно госпитализируют в отделение интенсивной терапии (реанимации).
Классификация СДС (формы)
При сортировке пострадавших и решении вопроса об очередности оказания медицинской помощи используют следующую классификацию СДС:
Синдром длительного раздавливания
Синдром длительного раздавливания - это шокоподобное состояние, наступающее после длительного сдавления туловища, конечностей или их сегментов тяжелыми предметами. Проявляется болью, ухудшением состояния, отеком пораженных отделов тела, острой почечной недостаточностью. Без медицинской помощи пациенты погибают от ОПН, нарастающей интоксикации, легочной или сердечно-сосудистой недостаточности. Лечение включает дезинтоксикационную и плазмозаменяющую инфузионную терапию, экстракорпоральную гемокоррекцию, антибиотикотерапию, иссечение участков некроза или ампутацию раздавленной конечности.
МКБ-10

Общие сведения
Синдром длительного раздавливания (СДР), другие названия - травматический токсикоз, краш-синдром, синдром Байуотерса, миоренальный синдром - патологическое шокоподобное состояние, наступающее после длительного сдавления туловища, конечностей или их сегментов тяжелыми предметами. Краш-синдром развивается сразу после освобождения больного и восстановления крово- и лимфотока в пораженных частях тела. Сопровождается ухудшением общего состояния, развитием токсемии и острой почечной недостаточности, при большой площади поражения нередко заканчивается смертью пациента. В травматологии и ортопедии выделяют бытовую разновидность краш-синдрома - так называемый синдром позиционного сдавления (СПС), который развивается в результате длительного (более 8 часов) сдавливания частей тела во время неподвижного положения человека на твердой поверхности.
Причины СДР
Обычно синдром длительного раздавливания возникает у пострадавших во время оползней, землетрясений, обвалов в шахтах, строительных работ, дорожных аварий, заготовки леса, взрывах и разрушениях зданий в результате бомбардировки.
Синдром позиционного сдавления обычно выявляется у пациентов, которые на момент травмы находились в состоянии отравления снотворными препаратами, наркотического или алкогольного опьянения. Чаще страдают подвернутые под туловище верхние конечности. По причинам развития, симптомам и методам лечения синдром позиционного сдавления практически не отличается от синдрома длительного раздавливания, однако, обычно протекает более благоприятно вследствие меньшей площади поражения.
Возникновение синдрома длительного раздавливания обусловлено сочетанием трех факторов:
- болевого синдрома;
- массивной потери плазмы, обусловленной выходом жидкой части крови через стенки сосудов в поврежденные ткани;
- травматической токсемии (интоксикации организма продуктами тканевого распада).
Продолжительное болевое раздражение при краш-синдроме приводит к развитию травматического шока. Потеря плазмы становится причиной сгущения крови и вызывает тромбоз мелких сосудов. Травматическая токсемия при краш-синдроме развивается вследствие всасывания в кровь продуктов тканевого распада травмированных мышц. Сразу после освобождения конечности из поврежденных тканей в сосудистое русло поступает значительное количество ионов калия, которые могут вызвать аритмию, а в тяжелых случаях - прекращение работы легких и сердца.
В дальнейшем раздавленные мышечные ткани пациента с краш-синдромом теряют до 66% калия, 75% миоглобина, 75% фосфора и 70% креатинина. Продукты распада поступают в кровь, вызывая ацидоз и нарушения гемодинамики (в том числе - резкое сужение сосудов почечных клубочков). Миоглобин повреждает и закупоривает почечные канальцы. Все это приводит к развитию острой почечной недостаточности, угрожающей жизни больного краш-синдромом.
Классификация
По степени тяжести:
- Легкая форма краш-синдрома. Возникает при раздавливании сегментов конечности в течение 4 и менее часов.
- Среднетяжелая форма краш-синдрома. Развивается в результате раздавливания одной конечности в течение 4-6 часов. При своевременном начале лечения прогноз благоприятный.
- Тяжелая форма краш-синдрома. Возникает при раздавливании одной конечности в течение 6-8 часов. Сопровождается расстройствами гемодинамики и острой почечной недостаточностью. При своевременном начале лечения прогноз относительно благоприятный.
- Крайне тяжелая форма краш-синдрома. Развивается в результате раздавливания двух и более конечностей в течение 6 и более часов. Сопровождается тяжелым шоком. Прогноз неблагоприятный.
По клинической симптоматике:
- ранний период (с момента освобождения до 3 суток);
- токсический период (начинается на 4-5 сутки);
- период поздних осложнений (развивается, спустя 20-30 суток с момента травмы).
Симптомы СДР
Сразу после устранения сдавления общее состояние пострадавшего улучшается. Пациента с синдромом длительного раздавливания беспокоит боль и ограничение движений в раздавленной конечности. В течение первых часов после освобождения постепенно нарастает отек пострадавшего участка, который становится плотным, деревянистым. На коже конечности образуются пузыри с серозно-геморрагическим содержимым. При осмотре поврежденной части тела выявляется ослабление пульсации артерий, снижение чувствительности и местной температуры.
Нарастает общая симптоматика. Состояние пострадавшего с краш-синдромом ухудшается. После короткого периода возбуждения пациент становится вялым, заторможенным. Отмечается снижение артериального давления и температуры тела, аритмия, тахикардия, выраженная бледность кожных покровов. Кожа больного краш-синдромом покрыта липким холодным потом. Возможна потеря сознания, непроизвольная дефекация и мочеиспускание. Иногда развивается отек легких. Уменьшается количество выделяемой мочи. Без адекватной врачебной помощи есть вероятность смертельного исхода в течение 1 или 2 суток.
На раздавленной конечности формируются очаги некроза. При отторжении мертвых тканей обнажаются мышцы, имеющие характерный вид вареного мяса. Развивается нагноение ран и эрозированных поверхностей. Появляется и постепенно нарастает острая почечная недостаточность. На 5-6 сутки у больных с синдромом длительного раздавливания развивается уремический синдром. Повышение уровня калия в крови вызывает аритмию и брадикардию.
На 5-7 сутки выявляются признаки легочной недостаточности. Нарастающая интоксикация, обусловленная поступлением в кровоток продуктов тканевого распада и бактериальных токсинов из раздавленной конечности, вызывает токсический гепатит. Возможен эндотоксический шок. Явления полиорганной недостаточности у пациентов с краш-синдромом постепенно уменьшаются в течение 2-3 недель.
Острая почечная недостаточность при краш-синдроме купируется примерно через месяц после травмы. Состояние пациента улучшается, температура его тела нормализуется. Уменьшаются боли и отек конечности. Некротизированные мышцы замещаются соединительной тканью, что приводит к атрофии мышц и развитию контрактур. При неблагоприятном развитии событий возможны местные (нагноение) и общие (сепсис) осложнения.
Диагностика
Патология диагностируется врачом-травматологом на основании характерного анамнеза (продолжительного сдавливания части тела), жалоб и данных внешнего осмотра. Для оценки общего состояния назначают комплекс лабораторных анализов. Для своевременного выявления и лечения ОПН осуществляют лабораторный мониторинг функции почек.
Лечение СДР
Перед освобождением конечности на нее необходимо наложить жгут выше места повреждения. После устранения сдавления конечность туго бинтуют и фиксируют на шине. Раны и поверхностные повреждения кожи обрабатывают по общим правилам. Пациенту с синдромом длительного раздавливания вводят наркотические анальгетики. Конечность обкладывают грелками со льдом. Если это возможно, выполняют футлярную новокаиновую блокаду раздавленной конечности или паранефральную блокаду по Вишневскому. Пострадавшего срочно доставляют в стационар.
Для улучшения микроциркуляции, борьбы с шоком и острой почечной недостаточностью в стационаре проводится инфузионная терапия (под контролем диуреза и центрального венозного давления). Для детоксикации и возмещения плазмопотери пациенту с краш-синдромом вводят 5% раствор глюкозы, солевые растворы, замороженную плазму, физ. раствор и раствор альбумина. Для улучшения микроциркуляции назначают гепарин (5000 ЕД) и реополиглюкин.
В целях компенсации метаболического ацидоза больному краш-синдромом капельно вводят 4% раствора гидрокарбоната натрия. Назначают антибиотики широкого спектра действия внутримышечно. Проводят симптоматическую терапию (диуретики, анальгетики, антигистаминные и противоаритмические препараты). При синдроме длительного раздавливания экстракорпоральную гемокоррекцию (гемодиализ, плазмаферез, плазмо- и гемосорбцию) проводят в как можно более ранние сроки.
При сохранении жизнеспособности мышечных тканей и выраженном субфасциальном отеке с нарушением местного кровообращения травматолог выполняет фасциотомию с ревизией и иссечением некротизированных мышечных пучков. Если нет нагноения, рану ушивают на 3-4 день, после уменьшения отека и улучшения общего состояния больного краш-синдромом.
В случаях необратимой ишемии проводят ампутацию конечности выше места наложения жгута. В других случаях показано иссечение некротизированных участков с сохранением жизнеспособных мышечных пучков. Жизнеспособность мышц определяют в ходе хирургического вмешательства. Критериями жизнеспособности является сохранение нормальной окраски, способность к кровоточивости и сокращению. После иссечения тканей рану обильно промывают антисептиками. Швы не накладывают. Рана заживает вторичным натяжением.
В отдаленном периоде больным с синдромом длительного раздавливания показаны курсы реабилитационного лечения (массаж, ЛФК), направленные на восстановление мышечной силы и устранение контрактур.
1. Диагностика и патогенетическое лечение синдрома длительного сдавления / Нечаев Э.А., Савицкий Г.Г. - 1992
3. Рекомендации ERBP по оказанию помощи пострадавшим с синдромом длительного сдавления при массовых катастрофах / перевод Камышовой Е.С. под ред.Захаровой Е.В. // Нефрология и диализ - 2015 - Т.17, №3
Диабетическая стопа - симптомы и лечение
Что такое диабетическая стопа? Причины возникновения, диагностику и методы лечения разберем в статье доктора Есипенко И. А., сосудистого хирурга со стажем в 37 лет.
Над статьей доктора Есипенко И. А. работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
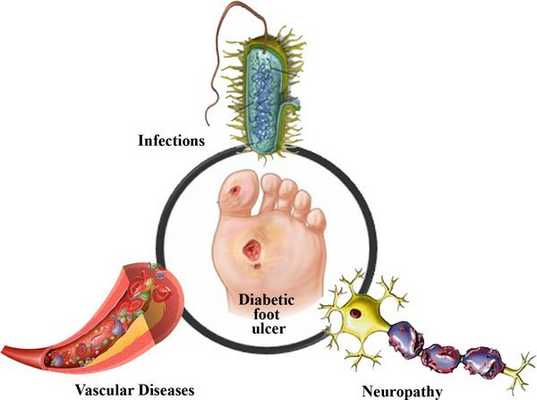
Диабетическая стопа (синдром диабетической стопы, СДС) — это тяжёлое осложнение сахарного диабета в виде инфекции, язв или разрушения глубоких тканей, которое возникает в связи с нарушением макроструктуры стопы и микроциркуляции крови, по причине разрушения нервных окончаний и нервных волокон. [10]
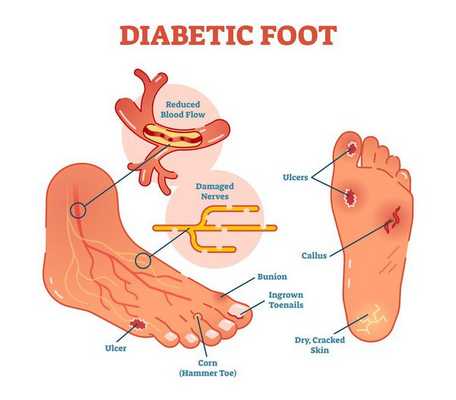
Главная причина ДС — это сахарный диабет (СД). И хотя синдром диабетической стопы не развивается с первого дня увеличения уровня глюкозы в крови более 7,0-8,0 ммоль/л, каждый пациент с диагнозом «сахарный диабет» должен помнить о таком грозном возможном осложнении.
Хронические раны на ногах у людей с сахарным диабетом встречаются в 4-15 % случаев. В некоторых случаях они становятся первым признаком развившегося диабета [10] .
Основные «пусковые механизмы» развития язв при СДС:
1. Ношение неудобной обуви. К изменению нагрузки на суставы стопы, сдавливанию или потёртости кожи, локальной микроишемии, инфильтрату, или некрозу могу привести любые дефекты обуви:
- несоответствующий размер обуви (меньше или больше, чем нужно);
- стоптанные и/или высокие каблуки;
- рубец на стельке;
- дефект подошвы;
- мокрая обувь;
- несоответствие обуви времени года.
2. Увеличенный вес тела. Учитывая площадь стоп, при увеличении веса тела (даже на 1 кг) увеличивается и нагрузка на каждый сустав стопы. Самая уязвимая область — подошвенная поверхность.
3. Разрастание эпидермиса (поверхности) кожи. Этот процесс происходит из-за нарушенных обменных процессов в коже на фоне СД (под утолщённым эпидермисом-"мозолью" в слоях кожи нарушается микроциркуляция, что приводит к микроишемии и некрозу).
4. Микротравмы:
- укусы животных;
- уколы шипами растений;
- порезы при педикюре и т. п.
5. Стенозы (сужение) и окклюзии (закупорка) магистральных артерий. В результате отсутствия кровоснабжения в стопах и голенях к микроишемии присоединяется макроишемия и развитие гангрены конечности.
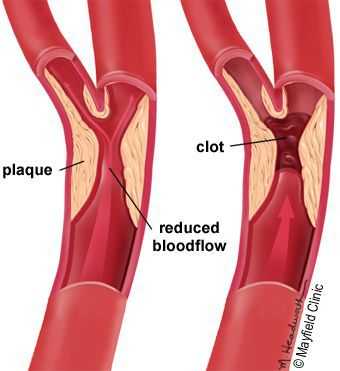
6. Условно патогенная или патогенная микрофлора. Активизация флоры (микробов и других микроорганизмов) на поверхности кожи в условиях СД приводит к воспалению кожного покрова, а в условия ишемии или микротравмы значительно ускоряется развитие гангрены.
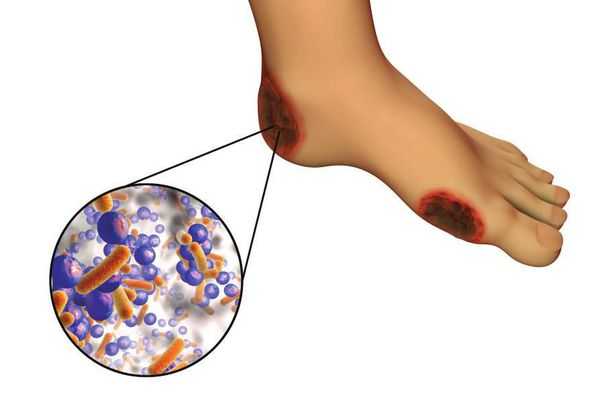
Часто наблюдается сочетание нескольких причин возникновения язв при СДС.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы диабетической стопы
Отправной точкой развития СДС считается не дата установления диагноза «Сахарный диабет», а время, когда были выявлены первые симптомы СД (однократные подъёмы глюкозы крови, сухость во рту и другие).
Симптомы СДС:
- онемение, зябкость, жжение, отёки в стопах и другие неприятные ощущения;
- выпадение волос на на стопах и голенях, потливость стоп;
- изменение окраски кожи (гиперемия, гиперпигментация, цианоз);
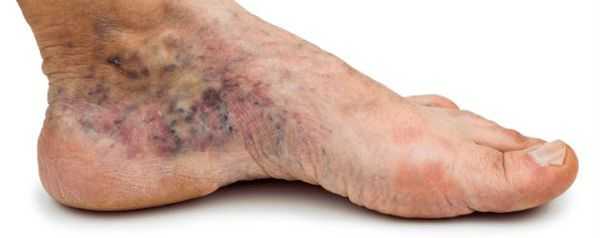
- утолщение, расслаивание, изменение формы и цвета ногтевых пластинок;
- кровоизлияния под ногтевой пластинкой в виде «синяков» под ногтями;
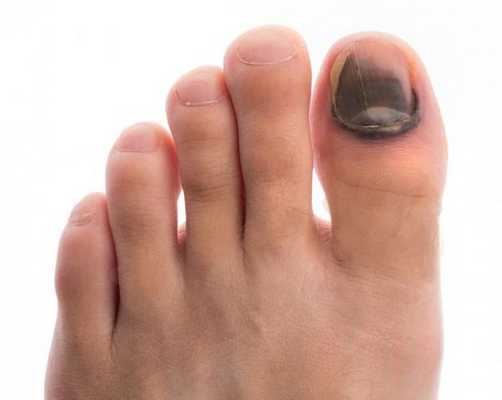
- деформация стоп;
- снижение чувствительности стоп — вибрационного, температурного, болевого и тактильного восприятия;
- боль в области стопы и язвы, возникающая как в покое или ночью, так и при ходьбе на определённые расстояния;
- истончение кожи, шелушение;
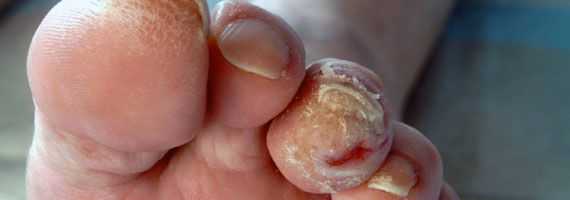
- понижение или увеличение температуры стоп и голеней;
- длительная эпителизация (заживление) микротравм — до двух месяцев, при этом остаются коричневые рубцы;
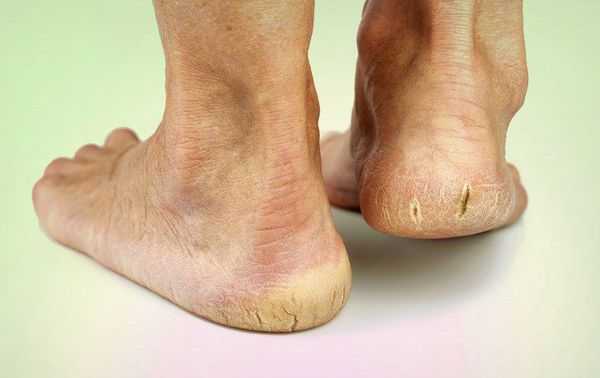
- трофические язвы, длительно не заживающие на стопах.
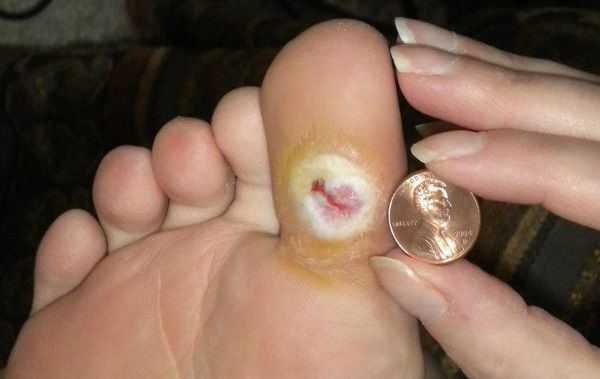
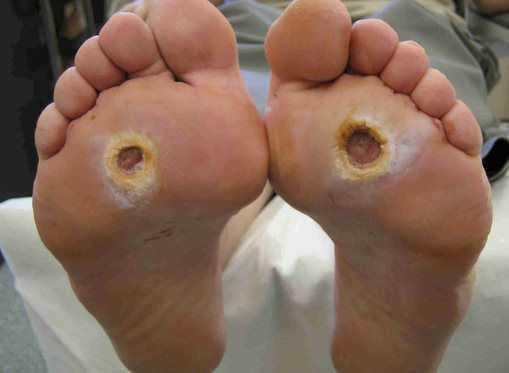
Чаще всего трофическим изменениям подвержены дистальные отделы конечности: пальцы и подошвенная поверхность стопы в проекции головок плюсневых костей. Зона образования трофической язвы зависит от причины её возникновения.
Патогенез диабетической стопы
Механизм развития СДС представляет собой следующую последовательность нарушений:
- Снижается выработка гормона инсулина.
- Увеличивается уровеь глюкозы в крови — развивается гипергликемия.
- Блокируется кровоток в мелких сосудах, через сосудистую стенку перестаёт поступать кислород и другие микроэлементы.
- Разрушаются нервные волокна и рецепторы.
- Наступает микро- и макроишемия тканей стопы.
- Образуются трофические язвы.
Таким образом, при СДС происходит повреждение всех тканей ноги.
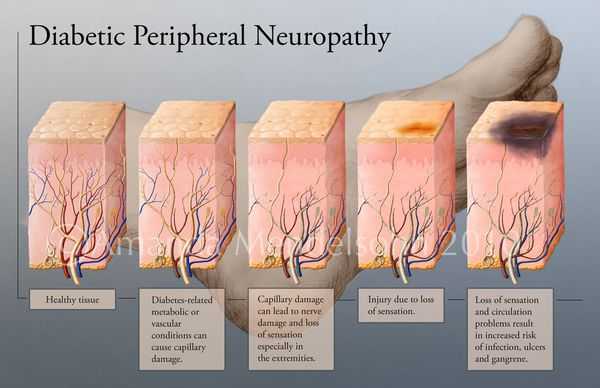
В результате дефицита инсулина в организме диабетика количество глюкозы в крови увеличивается. Это в свою очередь негативно сказывается на состоянии как мелких, так и крупных сосудов:
- на стенках сосудов скапливаются иммунологические вещества;
- мембраны становятся отёчными;
- просвет сосудов сужается.
В результате этих изменений кровообращение нарушается и образуются небольшие тромбы. Эти изменения в организме препятствуют поступлению достаточного количества микроэлементов и кислорода в клетки и тем самым приводят к нарушениям обменного процесса. Кислородное голодание тканей замедляет процесс деления клеток и провоцирует их распад.
Увеличение уровня глюкозы в крови также становятся причиной поражения нервных волокон — снижается чувствительность.
Все деструктивные процессы, происходящие в тканях стопы приводят к тому, что любое повреждение кожи становится лёгким процессом, а заживление — длительным. Усугубить состояние стопы могут присоединившиеся инфекции, которые способны привести к образованию гангрены — некрозу тканей. [9]
Классификация и стадии развития диабетической стопы
Классификация I Международного симпозиума по диабетической стопе
В 1991 году в Нидерландах на I Международном симпозиуме была принята классификация СДС, которая является наиболее распространённой. [1] Она предполагает разделение заболевания на три типа в зависимости от преобладающего патологического процесса:
- нейропатическая инфицированная стопа:
- длительное течение сахарного диабета;
- позднее возникновение осложнений;
- отсутствие болевого синдрома;
- цвет и температура кожи не изменены;
- уменьшение всех видов периферической чувствительности;
- наличие периферического пульса.
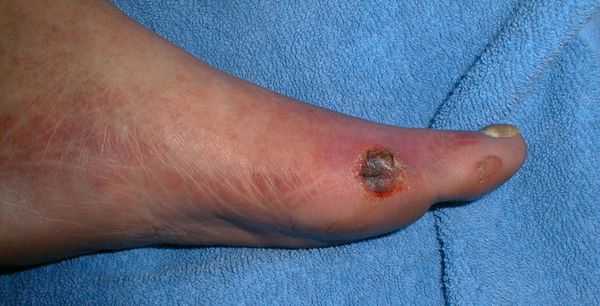
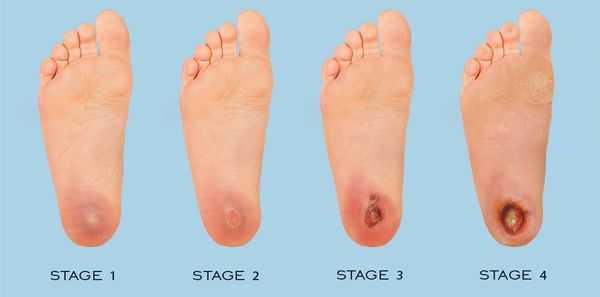
Классификация Вагнера
По степени выраженности поражений тканей стопы выделяют следующие стадии СДС: [6] [7]
- Стадия 0 — изменение костной структуры стопы — артропатия;
- Стадия 1 — изъязвление (язвы) кожи;
- Стадия 2 — изъязвление всех мягких тканей, дном язвы являются кости и сухожилия;
- Стадия 3 — абсцедирование и остеомиелит (воспаление костной ткани);
- Стадия 4 — образование гангрены дистальных отделов стопы (пальцев);
- Стадия 5 — образование гангрены стопы и отделов голени.
Классификация Техасского университета
Данная классификация была разработана в 1996-1998 годах. [8] В её основе лежит оценка язвы по глубине, наличию инфицирования и ишемии — риска ампутации конечности.
Синдром позиционного сдавления
Синдром позиционного сдавления - это комплекс симптомов, которые возникают при травме мягких тканей, вызванной длительным сдавлением собственной массой тела. Он развивается при отсутствии первичного повреждения и чаще всего связан с бессознательным состоянием пациента. Для синдрома характерны багровые пятна, ссадины и поверхностный некроз пораженного участка тела, признаки дисфункции почек. Диагностика включает тщательный сбор анамнеза и осмотр пациента, анализы крови и мочи, УЗИ и рентгенографию пораженной зоны. Лечение предполагает экстракорпоральные методы детоксикации, инфузионную терапию, симптоматические препараты.



Впервые заболевание было описано в 1754 году в Вене при вскрытии тел погибших во время пожара. Истинная частота синдрома позиционного сдавления (СПС) не установлена. Это связано со сложностями его диагностики при первичном обследовании и замалчиванием пострадавшими условий получения травмы, если она появилась в результате тяжелого алкогольного или наркотического опьянения. Тяжесть ближайших и отдаленных последствий СПС требуют от практикующих врачей усовершенствования протоколов оказания помощи, разработки более эффективных методов лечения.
Причины
Синдром позиционного сдавления многими авторами определяется как компрессионная травма. Большинство случаев СПС связано с бессознательным состоянием пострадавшего, из-за которого человек не способен контролировать положение своего тела и может часами находиться в неудобной позе. Причинами такого состояния выступают:
- Употребление ПАВ. Наиболее частой причиной патологии считается чрезмерный прием алкоголя или его суррогатов, которые вызывают глубокое опьянение и потерю сознания. СПС также развивается при наркотическом опьянении, особенно при введении опиатов, приеме транквилизаторов и других веществ с сильным седативным эффектом.
- Интоксикации. Отравление с потерей сознания характерно для вдыхания угарного и выхлопных газов. Такая ситуация бывает при пожаре, длительном нахождении в непроветриваемом гараже. Намного реже причиной позиционного сдавления выступает интоксикация нитрокрасителями, другими ядовитыми веществами.
- Черепно-мозговые травмы. Тяжелые повреждения головного мозга сопровождаются длительной потерей сознания. Если человеку вовремя не оказана помощь, он падает в неудобной позе и находится в ней продолжительное время.
В механизме развития СПС выделяют общие и местные изменения. Общие нарушения обусловлены действием этиологического фактора заболевания, который приводит к кислотно-основному дисбалансу, ухудшению микроциркуляции, переохлаждению организма. Эти причины накладываются на бессознательное или коматозное состояние, вызывая тяжелые местные изменения в пораженных тканях.
Ключевым моментом патогенеза считается ухудшение кровоснабжения тканей, которое вызывает образование миоглобина. В норме он находится только внутриклеточно, наибольшие количества пигмента найдены в скелетной и сердечной мускулатуре. При синдроме позиционного сдавления возникает миоглобинемия и миоглобинурия. Избыток пигмента накапливается в почечных канальцах и закупоривает их, становясь причиной острой почечной недостаточности.

В практической травматологии и реаниматологии выделяют 5 периодов болезни: острый, ранний, промежуточный, поздний и этап отдаленных результатов. Они важны для прогнозирования возможных симптомов и их своевременного лечения, чтобы предупредить развитие осложнений СПС. Большую значимость для практикующих врачей имеет классификация по тяжести, согласно которой синдром подразделяют на 3 степени:
- Легкая. Возникает при поражении небольших по площади участков тела: предплечий, голени, головы. При легкой степени тяжести время позиционного сдавления не превышает 6 часов.
- Средняя. Развивается при поражении обширных зон тела: бедра, верхняя или нижняя конечность полностью. Длительность компрессии увеличивается до 6-10 часов.
- Тяжелая. Проявляется при массивных сдавлениях одного или нескольких участков тела. Время компрессии составляет 10-24 часа: чем дольше длится компрессионный синдром, тем хуже прогноз для пациента.
В клиническом течении синдрома позиционного сдавления выделяют 5 периодов, которые последовательно сменяют друг друга. В первой (острой) фазе наблюдается интоксикация, потеря сознания и другие признаки, зависящие от конкретного этиологического фактора. У большинства пациентов развивается коматозное состояние, которое продолжается от нескольких часов до нескольких суток. Этот период характеризуется разнообразными изменениями в сдавленных тканях и во всем организме.
На втором (раннем) этапе проявляются симптомы повреждения тканей. Чаще всего сдавлению подлежат верхние и нижние конечности. При осмотре наблюдаются красно-синюшные пятна на коже, изредка они покрыты ссадинами, небольшими гематомами и участками мацерации. При длительном сдавлении определяют отслойку эпидермиса с образованием пузырьков, которые заполнены мутной или кровянистой жидкостью. Пациенты жалуются на боли, чувство распирания, онемение конечности.
После ликвидации сдавления к конечности начинает активно притекать кровь, что внешне проявляется отеками. Ткани резко напряжены, кожа становится бледной и холодной. Отечность сопровождается сдавлением артерий, поэтому на дистальных отделах конечностей сосудистая пульсация резко ослаблена или вовсе не определяется. Такие симптомы дополняются резким ограничением подвижности, которое связано с сильными болями и отечностью.
Ранний этап позиционного сдавления сопровождается эндогенной интоксикацией. Сразу после выхода из коматозного состояния появляется общее недомогание, заторможенность, тошнота и рвота. Характерно повышение температуры до субфебрильных значений. У пациентов наблюдается одышка, глухость сердечных тонов, сухость во рту. Поражение почек и других органов с развитием полиорганной недостаточности знаменует переход к третьему (промежуточному) периоду болезни.
Четвертый (поздний) этап синдрома сдавления характеризуется постепенным восстановлением работы всех органов и систем. Он начинается в сроки 10-25 суток после травматизации мягких тканей. При успешном лечении СПС переходит в пятую фазу - период отдаленных результатов. Она продолжается от 3 месяцев до 2 лет, характеризуется поздними последствиями со стороны пораженной конечности, почек и других органов.
Осложнения
Основной проблемой синдрома позиционного сдавления является острая недостаточность функции почек, которая связана с массивной миоглобинемией. Развитие ОПН в 3 раза повышает вероятность летального исхода у пострадавшего и коррелирует с неблагоприятным отдаленным прогнозом. Большое значение имеют осложнения основного заболевания либо интоксикации, которые стали причиной сдавления мягких тканей тела.
Обследование пациента проводится врачом отделения интенсивной терапии либо травматологом, что зависит от преобладающей симптоматики. На первый план выходит подробный сбор анамнеза: необходимо уточнить обстоятельства, предшествовавшие травме, выяснить точное положение пострадавшего, исключить химические аддикции и другие факторы риска. Для диагностики синдрома позиционного сдавления применяются следующие методы:
- УЗИ мягких тканей. При ультразвуковой диагностике отмечаются признаки повреждения компрессированных мышц: стертость мышечного рисунка, отсутствие поперечной исчерченности, мозаичные гипоэхогенные зоны (очаги миолиза). Для исключения венозных причин СПС назначают допплерографию сосудов пораженного участка.
- Рентгенография. Рентгенологическая визуализация информативна для исключения вывихов и переломов, которые в сочетании с внешними повреждениями кожи дают сходную клиническую картину. При синдроме позиционного сдавления рентгенографические изменения отсутствуют.
- ЭКГ. На электрокардиограмме определяются признаки гиперкалиемии: изменение интервала QT, возрастание зубцов T в грудных отведениях, единичные бигеминии и желудочковые экстрасистолы. Исследование дополняют УЗИ сердца, при котором патологические изменения не обнаруживаются.
- Биохимический анализ крови. Основным диагностическим признаком является повышение миоглобина крови свыше 1000 нг/мл, что коррелирует с высоким риском поражения почек. Возрастание уровня креатинина крови свидетельствует о развитии почечной дисфункции, в сочетании со сниженной клубочковой фильтрацией диагноз подтверждается.
- Анализ мочи. При СПС удельный вес мочи превышает 1015, в ней содержится большое количество миоглобина. Осмолярность составляет свыше 500 мосм/л, уровень натрия не превышает 20 ммоль/л. Характерно соотношение осмолярности мочи и плазмы свыше 1,1.
Дифференциальная диагностика
При поступлении пациента с синдромом сдавления проводится сложная дифференциальная диагностика межу позиционной компрессией тканей и классическим краш-синдромом. Отличительными признаками СПС выступают отсутствие болевого и травматического шока, отсутствие информации о попадании пациента под завалы. Обязательно исключают венозный тромбоз и тромбофлебит, вывих и перелом конечности.
Что надо знать о синдроме длительного давления

Синдром длительного сдавления (краш-синдром, СДС) - жизнеугрожающее состояние, которое возникает в связи с длительным сдавлением любой части тела и последующим её высвобождением, вызывающее травматический шок и часто приводящее к смерти.
Проявляется болью, ухудшением состояния, отеком пораженных отделов тела, острой почечной недостаточностью. Без медицинской помощи пострадавшие погибают от острой почечной недостаточности, нарастающей интоксикации, легочной или сердечно-сосудистой недостаточности.
Возникновению данного синдрома способствуют два условия:
1) массивный объём сдавленных тканей;
2) длительный период сдавления (от 40 минут и более).
В зоне сдавления образуются токсические продукты (свободный миоглобин, креатинин, калий, фосфор), которые не «размываются» жидкостью, скопившейся из-за механического препятствия циркуляции её тока. В связи с этим после устранения причины сдавления возникает системная реакция организма - продукты разрушенных тканей попадают в кровоток. Так
происходит отравление организма - токсемия.
Обычно синдром длительного сдавления (СДС) возникает у пострадавших во время оползней, землетрясений, обвалов в шахтах, строительных работ, дорожных аварий, заготовки леса, при взрывах и разрушениях зданий и сооружений.
ПРИЧИНЫ ВОЗНИКНОВЕНИЯ СИНДРОМА ДЛИТЕЛЬНОГО СДАВЛЕНИЯ
Синдром длительного сдавления мягких, преимущественно мышечных тканей, развивается в результате сочетания трех обязательных элементов:
1) потеря жидкой части крови по причине травматизации сосудов и иных тканей;
2) развитие болевого синдрома, возможно, шоковых состояний;
3) отравление организма некротическими тканями и другими токсичными продуктами, образованными при тканевом распаде.
ПРИЗНАКИ СИНДРОМА ДЛИТЕЛЬНОГО СДАВЛЕНИЯ
Состояние человека на момент обнаружения может быть вполне удовлетворительным, а может быть крайне тяжелым:
1) Если с момента начала компрессии прошло немного времени, то конечность будет отечной, кожа бледной и холодной на ощупь, периферическая пульсация будет снижена или полностью отсутствовать.
2) Если пострадавший находился под завалом длительное время (4-6 часов и более), то пораженные участки тела могут быть красно-синюшного цвета, сильно отечными, пульсация сосудов отсутствует, движение конечностями невозможно, попытки пошевелить ими вызывают сильнейшую боль.
ПЕРВАЯ ПОМОЩЬ ПРИ СИНДРОМЕ ДЛИТЕЛЬНОГО СДАВЛЕНИЯ
При обнаружении пострадавших, находившихся под какими-либо сдавливающими предметами, категорически нельзя освобождать передавленные конечности сразу. Принцип оказания помощи - не допустить залпового выброса токсинов, то есть «запереть» их в освобождённой от груза конечности, чередуя наложение жгута, снятие груза и тугое бинтование одновременно с оказанием помощи при сопутствующих повреждениях и общими противошоковыми мероприятиями.
В первую очередь, необходимо наложить жгут выше места повреждения, и только после этого осторожно убрать предметы, под которыми оказался человек. Если убрать их сразу, не накладывая жгут, токсичные продукты, образовавшиеся при массивном разрушении мышечной
ткани, попадут в общий кровоток. Это вызовет повреждение почек, развитие острой почечной недостаточности, что может привести к гибели пострадавшего до того, как удастся доставить его в медицинское учреждение.
Первая помощь до оказания медицинской помощи
Пострадавшую конечность необходимо туго забинтовать, максимально охладить и иммобилизировать, предварительно сняв с нее одежду и обувь, если речь идет о нижних конечностях.
Открытые раны (ссадины, порезы) при возможности следует обработать.
Если есть возможность, дать пострадавшему обезболивающие препараты, учитывая при этом возможную аллергическую реакцию организма пострадавшего.
Если пострадавший находится в сознании и нет подозрения на травму живота, то ему можно давать питье.
Пострадавшего нужно в кратчайшие сроки доставить в медицинское учреждение для оказания квалифицированной помощи. Следует отметить, что к жгуту обязательно прикрепляется записка, в которой будет указано время наложения.
Если время трагедии неизвестно, оказывают стандартную первую помощь, особенностью которой является отказ от быстрого освобождения от давящего груза.
Читайте также:
- Открытый пневмоторакс. Физиология открытого пневмоторакса
- Дарвин и Пуркинье в эмбриологии. История становления экспериментальной эмбриологии
- Сексуальные расстройства, связанные с беременностью
- УЗИ при синдроме черносливого живота у плода
- Состав панкреатического сока. Свойства панкреатического сока. Ферменты поджелудочной железы.
