Лечение диффузного токсического зоба. Лекарства для терапии болезни Грейвса
Добавил пользователь Skiper Обновлено: 22.01.2026
Среди пациентов, обращающихся к эндокринологу, все более многочисленна группа пациентов с патологией щитовидной железы. С одной стороны, это результат большей социальной осведомленности, более эффективных и доступных методов диагностики, а с другой стороны, это связано с реальным ростом заболеваемости различными заболеваниями щитовидной железы.
Цель этой статьи — кратко описать заболевания щитовидной железы, приводящие к гипертиреозу, представить диагностические и терапевтические возможности, с особым акцентом на гиперактивный узловой зоб и болезнь Грейвса.
Основные концепции по гипертиреозу
- Гипертиреоз — это увеличение выработки и высвобождения гормонов щитовидной железы и набор клинических симптомов в результате этого избытка.
- Тиреотоксикоз — совокупность клинических симптомов, связанных с избытком гормонов щитовидной железы в крови вне зависимости от причины (это может быть как заболевание щитовидной железы, так и передозировка гормональными препаратами).
Мы можем разделить гипертиреоз на комбинированный с гипертиреозом или нет.
В первой группе обнаруживается:
- Ненормальная стимуляция щитовидной железы, включая болезнь Грейвса -Базедова, при которой стимулирующим фактором являются антитела против рецептора ТТГ;
- Гиперактивность, вызванная наличием ткани в щитовидной железе (и, следовательно, работающей независимо от ТТГ) в виде одиночной аденомы, многоузлового зоба или диффузной автономии;
- Чрезмерная продукция ТТГ опухолью гипофиза;
- Гиперактивность, связанная с избытком ТТГ в случае устойчивости гипофиза к гормонам щитовидной железы.
Конечно, наиболее частыми причинами гипертиреоза являются вегетативная ткань щитовидной железы и болезнь Грейвса. Другие редки, а некоторые, например, резистентность гипофиза, спорадически.
Вторая группа гипертиреоза — это клинические ситуации, не связанные с гипертиреозом, такие как:
- Избыток экзогенных гормонов, так называемые фактиция тиреотоксикоза;
- Повреждение клеток щитовидной железы и «перетекание» гормонов в кровь, например, после лечения 131 I или в результате воспаления;
- Спорадическая выработка эктопических гормонов.
Тест, который позволяет нам различать эти два типа гиперфункции, — это тест на поглощение йода. При гипертиреозе потребление йода увеличивается, при других заболеваниях — снижено.
Причины гипертиреоза
Несмотря на множество заболеваний, ведущих к гипертиреозу, эндокринологи чаще всего имеют дело с пациентом с гиперактивным зобом или болезнью Грейвса. Во многих европейских странах до 60% гипертиреоза возникает именно из-за узлового зоба.
Это типично для районов с дефицитом йода. Дефицит йода вызывает локальную активацию факторов роста, что приводит к гиперплазии клеток щитовидной железы (т.е. увеличению их количества). Кроме того, он вызывает повышенный выброс ТТГ из гипофиза. ТТГ, воздействуя на тироциты, вызывает их гипертрофию (то есть увеличение клеток). Эти два процесса вместе, гиперплазия и гипертрофия, ответственны за формирование зоба.
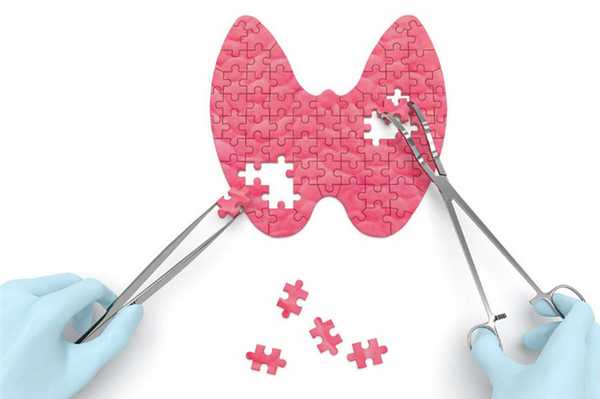
Дефицит йода
Выделяют три формы заболевания:
- Единичная вегетативная опухоль (болезнь Гетча) — около 30% случаев;
- Множественные вегетативные опухоли (болезнь Пламмера) — около 60%;
- Диффузная — около 10%.
Заболевание вызвано гиперплазией фолликулярного эпителия щитовидной железы, автономно выделяющего гормоны.
Узловой зоб характеризуется периодом эутиреоза, субклинической гиперактивностью и, наконец, явной гиперактивностью. Возникновению явного гипертиреоза способствует повышенное поступление йода, поскольку вегетативные опухоли не имеют правильного механизма адаптации к его избытку.
Второе заболевание, приводящее к гипертиреозу, — болезнь Грейвса. Это иммуноопосредованное заболевание, при котором щитовидная железа стимулируется антителами к рецепторам ТТГ, а не ТТГ, как обычно.
Для возникновения болезни Грейвса должны сосуществовать три фактора:
- генетический (дефект Т-супрессорных лимфоцитов);
- окружающая среда (стресс, инфекция, курение, повышенное потребление йода, гормонов, например, андрогенов или экзогенного тироксина);
- интратироидный фактор (способность железы вырабатывать слишком много гормонов).
Симптомы гипертиреоза
Клинические симптомы гипертиреоза хорошо известны. К ним относятся:
- ощущение учащенного сердцебиения;
- ощущение постоянного тепла;
- повышенная жажда;
- нарушение сна;
- повышенная нервная возбудимость;
- потеря веса;
- диарея;
- повышение температуры тела;
- повышенная влажность кожи
- тахикардия;
- высокая амплитуда давления;
- тр емор рук ;
- миастения.
Особенно распространены сердечно-сосудистые симптомы — увеличиваются сердечный выброс и скорость кровообращения. В результате тахикардии над сердцем иногда появляется систолический шум. В тяжелых случаях тиреотоксикоза могут возникнуть сердечные аритмии (часто в виде фибрилляции предсердий), сопровождающиеся недостаточностью кровообращения.
Развивающиеся нарушения в системе кровообращения, особенно чувствительной к избытку гормонов щитовидной железы, могут привести к образованию так называемого тирео-кардиальный синдром (тиреокардиальный).
Поскольку симптомы гипертиреоза при узловом зобе и болезни Грейвса схожи, иногда бывает трудно дифференцировать эти единицы. Следующие критерии дифференциации (таблица 1) могут оказаться полезными.
Тиреотоксикоз (гипертиреоз) - симптомы и лечение
Что такое тиреотоксикоз (гипертиреоз)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Курашова О. Н., эндокринолога со стажем в 28 лет.
Над статьей доктора Курашова О. Н. работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов
Определение болезни. Причины заболевания
Тиреотоксикоз (гипертиреоз) — гиперметаболический процесс, вызванный избытком тиреоидных гормонов в организме и их токсическим воздействием на различные органы и ткани. Клинически характеризуется увеличением щитовидной железы и поражением других систем и органов. [3] [5] [11]
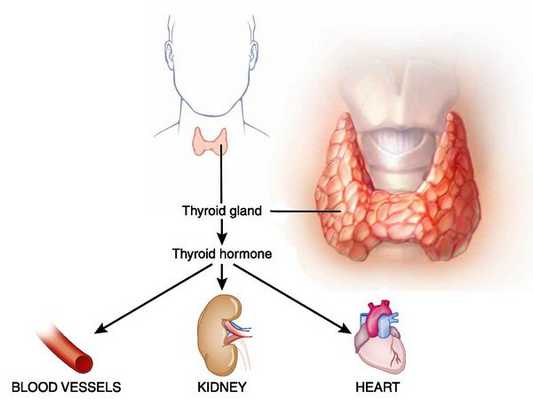
Первые описания этой патологии были найдены в работах персидского врача Джурджани, созданных в 1100 году. [5] [11]
Данный синдром встречается как у женщин (до 2%), так и у мужчин (до 0,2%). Чаще он возникает у людей в возрасте 20-45 лет.
Причины тиреотоксикоза
Причин возникновения тиреотоксикоза множество. К основным относятся:
- повышение продукции гормонов щитовидной железой вследствие различных заболеваний (диффузно-токсический, узловой зоб и другие);
- избыточный приём препаратов, содержащих гормоны щитовидной железы (нарушение назначенной схемы лечения гипертиреоза).
Факторы риска
Провоцирующим фактором синдрома является дополнительное количество йода, поступающее в организм при самостоятельном использовании йодных добавок.
Состояние тиреотоксикоза при диффузно-токсическом зобе является аутоиммунным заболеванием. Обычно оно развивается в результате избыточной выработки антител к рецептору тиреотропного гормона (ТТГ), производимого гипофизом.
Возникновение тиреотоксического состояния возможно при возникновении функциональной автономии уже существующего узла щитовидной железы — одно- и многоузлового зоба. Это заболевание развивается достаточно долго, в основном у людей, старше 45 лет. Так, в отсутствие воздействия ТТГ — основного физиологического стимулятора [7] [8] — узлы синтезируют количество тиреогормонов, превышающее потребность организма. [5] [6] [11]
Тиреотоксикоз при беременности
Во время беременности потребность организма женщины в тиреоидных гормонах возрастает на 30-50 %, поэтому изменение работы щитовидной железы происходит уже с первых недель беременности. Вследствие этого у 2 % беременных развивается гестационный гипертиреоз. Беременным рекомендуется вовремя обратиться к лечащему врачу, провести диагностику и подобрать необходимое индивидуальное лечение.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы тиреотоксикоза (гипертиреоза)
При опросе пациентов с подозрением на повышенную функцию щитовидной железы выявляются:
- непредсказуемая возбудимость, эмоциональная неустойчивость, беспричинная плаксивость;
- беспокойство и нарушение концентрации внимания, возникающее при нахождении в обществе;
- ежедневное нарушение сна;
- суетливость при выполнении любой работы;
- слабость во время ходьбы;
- повышенная потливость диффузного характера, не зависящая от физического или эмоционального напряжения, ощущение «жара»;
- периодические сердцебиения;
- дрожь в теле и нарастающая потеря веса (наблюдаются редко).
Эмоциональные расстройства сочетаются с двигательно-волевыми: появляется необходимость в постоянном движении и хореоподобные подёргивания. Причём тремор конечностей и тела - типичный симптом тиреотоксикоза. [2] [3] [5] [11]
Диффузный токсический зоб (Базедова болезнь, или болезнь Грейвса) - симптомы и лечение
Что такое диффузный токсический зоб (Базедова болезнь, или болезнь Грейвса)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Родионова Е. А., терапевта со стажем в 14 лет.
Над статьей доктора Родионова Е. А. работали литературный редактор Елена Бережная , научный редактор Сергей Федосов
Диффузный токсический зоб — это аутоиммунное поражение щитовидной железы.
Диффузный токсический зоб впервые был описан в трудах Роберта Джеймса Грейвса и Карла Адольфа фон Базедова в середине ХIХ века. Кроме данного заболевания, тиреотоксикоз может встречаться и при других заболеваниях щитовидной железы (тиреоидит, токсическая аденома и др.), что требует дифференциальной диагностики, так как лечение этих состояний не является однотипным, а осложнения из-за отсутствия или неправильного лечения могут привести к необратимым патологическим изменениям. [1] , [2]
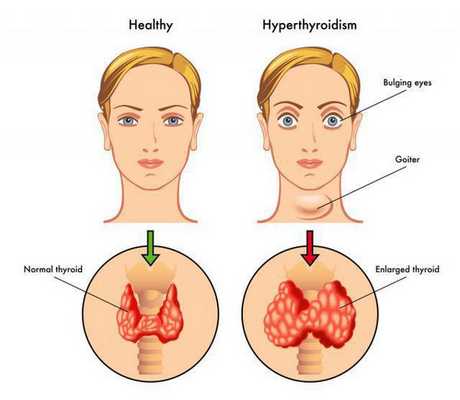
В англоязычных странах это заболевание называют болезнью Грейвса, а немецкоязычных — Базедовой болезнью. Диффузный токсический зоб развивается из-за нарушенной функции СД8+-лимфоцитов и выработки антитиреоидных антител, среди которых особое значение придаётся тем, которые имеют сродство к рецепторам тиреотропного гормона в щитовидной железе. Эти антитела выявляются в среднем у 50% пациентов с диффузным токсическим зобом. С этими рецепторами в норме связывается тиреотропный гормон (ТТГ), что стимулирует выработку и выделение тиреоидных гормонов (ТГ). Антитела при связывании с рецепторами ТТГ увеличивают секрецию тироксина (Т4) и трийодтиронина (Т3) «в обход» регуляции ТТГ. Повышенный уровень тиреотропного гормона обуславливает развитие тиреотоксикоза. До конца не ясна причина такого дефекта иммунной системы. Имеются данные, позволяющие говорить о роли генетической предрасположенности, в частности, более широкой распространённости аллелей HLA-B8 и BW-35 у пациентов с этой болезнью. [4] Однако не выявлено какой-то одной аллели, ответственной за болезнь Грейвса. Вероятно, здесь имеет место взаимодействие нескольких аллелей.
Симптомы диффузного токсического зоба
Диффузный токсический зоб чаще развивается у женщин моложе тридцати лет. [1] Синдром тиреотоксикоза связан с более интенсивным метаболизмом. Увеличивается частота сердечных сокращений, поднимается артериальное давление. Характерен подъём систолического («верхнего») давления и снижение диастолического, то есть поднимается пульсовое давление, проявляющееся выраженной пульсацией крупных и мелких артерий. [4] Характерно повышенное потоотделение, так как организм старается отдать избыточно вырабатываемое тепло (из-за нарушенной регуляции окислительного фосфорилирования). Стимуляция нервной системы проявляется раздражительностью, тремором рук. Аппетит повышается, однако масса тела снижается из-за ускоренного распада белков в организме. Редко встречается так называемый fat-Базедов-вариант, при котором масса тела увеличивается. [4] Пациенты с ДТЗ часто жалуются на слабость мышц, утомляемость, одышку. Щитовидная железа может быть увеличенной, однако нет зависимости между степенью ее увеличения и тяжестью состояния. В норме объём щитовидной железы у мужчин не превышает 25 см 3 , а у женщин — 18 см 3 . Симптомы, как правило, развиваются относительно быстро — за 6-12 мес. В 80% случаев пальпаторно определяется увеличенная, безболезненная щитовидная железа. На раннем этапе болезни пациенты могут обратиться с какой-либо одной из перечисленных жалоб, поэтому врач должен быть хорошо осведомлён о признаках тиреотоксикоза и необходимых диагностических мероприятиях. У бессимптомных пациентов с субклиническим тиреотоксикозом болезнь выявляется случайно, если по каким-либо показаниям сдаётся анализ крови на ТТГ.
При Базедовой болезни могут появляться признаки эндокринной офтальмопатии, возникающей из-за поражения периорбитальной клетчатки: выраженный экзофтальм (не всегда симметричный), диплопия, отечность век, ощущение «инородного тела в глазах». Это сильно облегчает работу врача в плане диагностики, так как среди всех состояний с тиреотоксикозом эндокринная офтальмопатия характерна именно для диффузного токсического зоба. Не следует путать эндокринную офтальмопатию с глазными симптомами тиреотоксикоза, среди которых можно выделить синдром Грефе и синдром Кохера (верхнее веко отстаёт при взгляде вверх и вниз соответственно), синдром Мебиуса (взгляд не фиксируется вблизи), синдром Штельвага (уменьшение частоты морганий). Стоит отметить, что выраженность глазных симптомов не зависит от тяжести дисфункции щитовидной железы. [4]
Некоторые авторы в развитии диффузного токсического зоба выделяют четыре стадии:
- Невротическая (вегетативный невроз и незначительное увеличение или нормальные размеры щитовидной железы);
- Нейрогормональная (увеличенные размеры щитовидной железы и клиническая картина тиреотоксикоза);
- Висцеропатическая (нарушение функции органов);
- Кахектическая (тиреотоксические кризы и общая дистрофия). [4]
Патогенез диффузного токсического зоба
Кроме генетических факторов, есть предположения о роли стресса и инфекции в развитии болезни Грейвса, а также действия токсических веществ. [4] Из-за иммунологических нарушений, происходит инфильтрация щитовидной железы лимфоцитами, выработка антител к различным её компонентам, главным образом — к рецепторам ТТГ, что приводит к стимуляции выработки ТГ и пролиферации тироцитов. Эти антитела также называют тиреостимулирующими иммуноглобулинами. Избыточное действие ТГ в организме приводит к развитию тиреотоксикоза, с признаками которого больные диффузным токсическим зобом обычно обращаются к врачу. [1] , [2]
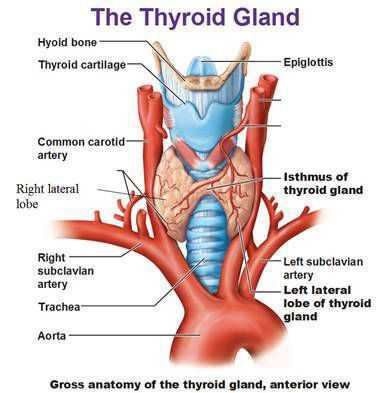
Классификация и стадии развития диффузного токсического зоба
Согласно классификации тиреотоксикоза по Фадееву В.В. и Мельниченко Г.А., выделяется:
- субклинический;
- манифестный;
- осложнённый.
Также существует классификация зоба (патологического увеличения щитовидной железы), в которой выделяется три степени зоба, в зависимости от данных осмотра и пальпации щитовидной железы.
Классификация зоба, рекомендованная ВОЗ (2001)
- 0 cтепень: зоба нет (объём каждой доли не превышает объёма дистальной фаланги большого пальца руки обследуемого);
- I степень: зоб пальпируется, но не виден при нормальном положении шеи, или же имеются узловые образования, не приводящие к увеличению щитовидной железы;
- II степень: зоб чётко виден при нормальном положении шеи. [4] , [5]
Патоморфологическая классификация диффузного токсического зоба (три варианта заболевания) опирается на данные гистологического исследования биоптата или удалённой щитовидной железы. [4] , [5]
Осложнения диффузного токсического зоба
Развившийся при диффузном токсическом зобе тиреотоксикоз поражает все системы организма. Если надлежащим образом не лечить это заболевание, то оно грозит тяжёлой инвалидизацией, а аритмии и сердечная недостаточность даже могут привести к летальному исходу.
Наиболее опасным осложнением болезни Грейвса является тиреотоксический криз, развитие которого связывают с неблагоприятными факторами (стресс, различные заболевания, выраженная физическая нагрузка, операция и др.). Появляется резкое возбуждение, температура повышается до 40 о С, частота сердечных сокращений достигает 200 ударов в минуту, может развиться фибрилляция предсердий, усиливаются явления диспепсии (тошнота, рвот, понос, жажда), повышается пульсовое артериальное давление. Затем могут появиться признаки недостаточности надпочечников (гиперпигментация, нитевидный пульс, нарушение микроциркуляции). Состояние ухудшается за несколько часов. Это ургентная ситуация, требующая неотложных мер, направленных на снижение концентрации ТГ, борьбу с надпочечниковой недостаточностью, дегидратацией, гипертермией, метаболическими нарушениями и недостаточностью кровообращения. В/в вводится гидрокортизон, проводится дезинтоксикационная и тиреостатическая терапия. К осложнениям диффузного токсического зоба также можно отнести осложнения хирургического его лечения: гипопаратиреоз, повреждение n. laryngeus recurrens (при повреждении одного нерва появляется осиплость голоса, при повреждении двух может возникнуть асфиксия), кровотечения, аллергические реакции на препараты. Об осложнениях тиреостатической терапии будет сказано ниже. [5]
Диагностика диффузного токсического зоба
При наличии у пациента признаков тиреотоксикоза ему определяют уровень тиреотропного гормона (ТТГ) высокочувствительным методом (чувс. 0,01 мЕд/л). Если уровень ТТГ меньше нормы, то исследуют концентрацию св. Т4 (тетрайодтиронин, тироксин) и Т3 (трийодтиронин). Существует понятие о так называемом субклиническом тиреотоксикозе, когда уровни Т4 и Т3 оказываются в норме. Среди антител наибольшее клиническое значение имеет уровень антител к рецепторам ТТГ (АТ-рТТГ). Высокие их титры с большой долей вероятности указывают на то, что мы имеем дело именно с болезнью Грейвса. Другие антитела, такие, как антитела к тиреоидной пероксидазе и тиреоглобулину (АТ-ТПО и АТ-ТГ), выявляются и при других состояниях, поэтому имеют значение только в комплексной оценке, и их определение может помочь в некоторых ситуациях.
На УЗИ при болезни Грейвса характерными признаками являются сниженная эхогенность и увеличение объёма (около 80% случаев). При обнаружении очаговых образований, при подозрении на опухолевые, проводится биопсия с цитологическим исследованием. В некоторых ситуациях (дифференциальная диагностика с функциональной автономией, загрудинный зоб) проводится сцинтиграфия щитовидной железы. Дифференциальная диагностика проводится с функциональной автономией щитовидной железы (характерно наличие узлов на УЗИ, «горячих» при сцинтиграфии, отсутствие антител, нет эндокринной офтальмопатии), подострым тиреоидитом (острое начало, боли в щитовидной железе, повышение температуры, связь с перенесённым инфекционным заболеванием), безболевым («молчащим») тиреоидитом (чаще бывает субклинический тиреотоксикоз), послеродовым тиреоидитом (возникает в течение 6 месяцев после родов). [3] , [5]
Лечение диффузного токсического зоба
Лечение болезни Грейвса может проводиться эндокринологом или терапевтом. К сожалению, в настоящее время лечение диффузного токсического зоба направлено только на орган-мишень, то есть щитовидную железу, а не на выработку антител, являющуюся непосредственной причиной развития болезни. Даже после удаления щитовидной железы продолжают синтезироваться антитела к рецепторам тиреотропного гормона, хотя тиреотоксикоза уже не возникает (при адекватной заместительной терапии). [9]
Итак, существует три способа лечения диффузного токсического зоба:
- консервативное лечение;
- радиойодтерапия;
- оперативное лечение.
Выбор метода зависит от возраста, сопутствующих заболеваний, степени увеличения щитовидной железы, желания пациента и возможностей лечебного учреждения. Консервативный метод лечения диффузного токсического зоба заключается в назначении тиреостатиков. В некоторых случаях (до 30%) курс такого лечения способен привести к стойкой ремиссии, в некоторых — является подготовкой к использованию другого, более радикального метода (хирургическое лечение или терапия йодом-131). Считается, что консервативная терапия неэффективна при выраженном увеличении щитовидной железы (более 40 см 3 ) и с признаками сдавления окружающих тканей, при наличии крупных узлов в ней, а также при наличии осложнений (фибрилляция предсердий, остеопороз и др.). При рецидиве после курса терапии тиреостатиком, повторный длительный курс не назначается. [5] В подобных случаях проводится курс медикаментозной подготовки к радиойодтерапии или операции.
Важным условием адекватного проведения консервативного лечения является приверженность пациента к лечению и доступность лабораторного контроля. Тиреостатики блокируют синтез тиреоидных гормонов и купируют тиреотоксикоз. По прошествии 4-6 недель тиреостатической терапии, при наступлении эутиреоидного состояния, обычно к лечению добавляют левотироксин. [4] В период тиреотоксикоза (до нормализации Т4) также целесообразно назначение препаратов из группы β-адреноблокаторов: они подавляют тканевое превращение Т4 в Т3, снижают частоту сердечных сокращений. Критерием адекватности лечения является нормальный уровень Т4 и ТТГ. Курс лечения продолжается 12-18 месяцев. Во время лечения необходимо контролировать показатели общего анализа крови. Это необходимо для контроля грозных осложнений тиреостатической терапии — агранулоцитоза и тромбоцитопении, требующих немедленной отмены препаратов. Симптомы агранулоцитоза: лихорадка, боль в горле, жидкий стул. [4] При их появлении пациенту необходимо экстренно сдать кровь на общий анализ и прекратить приём тиреостатиков до получения результатов анализа. Рецидив чаще всего наступает в первые 12 месяцев после завершения курса.
Под хирургическим лечением подразумевается удаление всей или большей части щитовидной железы. [8] Операция проводится только в состоянии эутиреоза. В настоящее время удаление этого органа не является фатальным для человека, так как имеются все возможности адекватной и недорогой заместительной терапии левотироксином. С другой стороны, при оставлении даже небольшого фрагмента железы, сохраняется вероятность рецидива заболевания, это орган-мишень для антитиреоидных антител, выделяемых иммунной системой. Таким образом, послеоперационный гипотиреоз теперь не рассматривается в качестве осложнения операции, а является её целью. Доза левотироксина после операции подбирается индивидуально и обычно составляет 1,7 мкг/кг в сутки.
В России радиойодтерапия мало распространена, что связано с дефицитом йода-131. Противопоказанием к радиойодтерапии является только беременность и период кормления грудью. Даже детский возраст не является помехой к её проведению. [6] Данный метод заключается в приёме внутрь предварительно рассчитанной дозы йода-131, который накапливается в щитовидной железе, распадается в выделением β-частиц, что приводит к лучевой деструкции тироцитов. Радиойодтерапия по сути является нехирургическим методом удаления ткани щитовидной железы. [1] , [5] , [7]
Прогноз. Профилактика
Прогноз при своевременной диагностике и надлежащем лечении благоприятный. Не рекомендуется приём лекарств, побочным эффектом которых является влияние на выработку тиреоидных гормонов, например амиодарона. Диффузный токсический зоб в большинстве случаев успешно лечится и не является приговором. Благодаря общедоступной и относительно недорогой заместительной терапии, удаётся добиться нормализации метаболических процессов и исчезновения клинических проявлений. Однако осложнения болезни Грейвса способны привести к необратимым патологическим изменениям в организме. Профилактика диффузного токсического зоба у прямых родственников больных чётко не разработана, однако можно рекомендовать отказ от курения, йод-содержащих лекарств, соблюдение оптимального режима дня для минимизации стрессовых ситуаций и регулярный контроль ТТГ. Чёткой связи между поступлением йода с пищей и болезнью Грейвса не выявлено, в регионах с недостаточным содержанием йода диффузный токсический зоб встречается не чаще; в отличие от функциональной автономии, которая в этих областях становится основной причиной тиреотоксикоза. [3] , [7]
Консервативное лечение диффузного токсического зоба: возможности, проблемы, пути решения
Известно, что лечение аутоиммунных заболеваний до сегодняшнего дня является нерешенной проблемой. Это в полной мере относится к группе эндокринных заболеваний, имеющих аутоиммунную природу. В их число входит сахарный диабет типа 1, Аддисонова болезнь, аутоиммунный тиреоидит, диффузный токсический зоб.
ак известно, в настоящее время существует три основных метода лечения диффузного токсического зоба. Это консервативная терапия, хирургическое лечение и лечение радиоактивным йодом (2, 4). Так как ни один из перечисленных методов не является патогенетическим, отношение к ним эндокринологов в разных странах мира не одинаково (26, 48). Этому во многом способствует тот факт, что ни один из методов лечения не гарантирует потенциально идеального исхода - сохранения эутиреоидного статуса.
Основной проблемой консервативного лечения диффузного токсического зоба является высокая частота рецидивов после прекращения лечения и объективные трудности их прогнозирования (45). Частота ремиссий после 1-2 лет тио-намидной терапии колеблется от 13 до 80%, а по данным США составляет 20-30%. Meng W. et al. (36) сообщают о возникновении рецидивов после лечения тиреостатиками у 53-54% больных (срок наблюдения после окончания лечения - 1 год), Lucas et al. при пятилетнем наблюдении сообщают о 60-67% случаев реци-дивирования тиреотоксикоза (34). Наиболее низкие цифры рецидиви-рования при длительном наблюдении приводят Volpe et al. - 35% (51), самые пессимистичные результаты получены Chiovato L., Pinchera A. -70-80% рецидивирования (21). Достаточно оптимистический прогноз дан в одном из обзоров Weetman A.P. (12). Он указывает, что спустя год после достижения эутиреоза тиреостатиками, у 40-50% больных развивается длительная ремиссия заболевания, которая у 30-40% больных сохраняется на протяжении 10 и более лет.
В московской популяции, по данным ретроспективного анализа кафедры эндокринологии ММА им. И.М. Сеченова (заведующий кафедрой - И.И. Дедов), рецидивы тиреотоксикоза составляют 63%, стойкий эутиреоз достигнут у 35% больных и спонтанный гипотиреоз - у 2% больных (8). При этом было показано, что при повторных попытках назначения тиреостатических препаратов, показатель сохранения ремиссии прогрессивно снижается. Так, 78% больных имели стойкую ремиссию после первой попытки консервативного лечения, 14% -после второй, 5,5% - после третьей и только 2,5% - после четвертой попытки (9, 11). На основании полученных результатов авторы работы делают вывод об очевидной нецелесообразности повторного назначения тиреостатиков: шанс таким образом добиться стойкой ремиссии очень небольшой.
Предполагается, что частота ремиссий зависит от исходного уровня потребления йода, но этот вопрос остается дискутабельным (54). Неясно также, связана ли ремиссия с приемом тионамидов, или она просто отражает естественное течение заболевания со спонтанными иммунологическими ремиссиями. Так, при лечении гиперти-реоза одним только пропраноло-лом частота ремиссий составляла 31%, то есть почти не отличалась от таковой при использовании тиона-мидов в США. Авторы делают вывод о том, что это может свидетельствовать в пользу развития спонтанных иммунологических ремиссий и при лечении тионамидами.
Интересны результаты проведенного в 1993 году Европейского многоцентрового исследования эффективности различных доз ме-тимазола, в котором приняли участие 509 больных диффузным токсическим зобом. Сравнивалась эффективность малых доз метимазола (10-20 мг) и относительно более высоких (40 мг/сутки). Частота рецидивов диффузного токсического зоба в этих двух группах, которую регистрировали в течение 12 месяцев после окончания терапии, была одинаковой. Reinwein D. et al высказано мнение, что полученные результаты не согласуются с гипотезой об иммунодепрессивном действии тиреостатических препаратов (40). В тоже время исследователи сообщили о том, что от используемой дозы тиреостатика зависит в последующем шанс сохранения ремиссии. Так, в тех случаях, когда была использована доза тиамазола 60 мг, в последующем длительную ремиссию сохраняли 75% пациентов, при дозе 15 мг - только 42%.
Говоря о вероятности сохранения ремиссии после консервативной терапии, большинство авторов (5, 39) указывают на значимость таких аспектов, как величина суточной дозы, длительность приема тирео-статиков и сочетание их с левоти-роксином. Как уже было отмечено выше, в отношении влияния суточной дозы на сохранение ремиссии тиреотоксикоза, мнения различных специалистов противоречивы. Многие исследователи указывают на отсутствие достоверных различий в эффективности высоких и низких доз (6, 35, 40), хотя Bromberg N., Romaldini J.H. et al. считают, что применение более высоких поддерживающих доз тионамидов более эффективно (42).
В отношении же длительности приема тиреостатиков мнение большинства ученых совпадает - медикаментозная терапия на протяжении 12-18 месяцев имеет преимущество в том смысле, что после ее отмены частота рецидивов тиреотоксикоза меньше, чем при лечении в течение менее 12 месяцев. При изучении литературы по поводу влияния длительности приема тиреостатиков на исход консервативного лечения наблюдается следующий подход к исследованию данного вопроса: обычно у двух групп пациентов, получавших фиксированную дозу метимазола, одна из них - длительное время, другая - короткое. Через определенный период времени проводят количественное сравнение рецидивов - ремиссий. Так Allanic H. Et al. (18) проведя подобное рандомизированное исследование, сообщили о 78% случаев рецидивирования тиреотоксикоза среди пациентов, принимавших тионамиды в течение 6 месяцев, и 38% - получавших лечение в течение 18 месяцев. Эффективность более длительного приема тиреостатиков подтверждается и работами других авторов (23, 37, 44) Известно, что с учетом этого факта, в детской практике используют более длительные курсы тионамидной терапии - до 3-4 лет, а при отсутствии иммунологической ремиссии и дольше (13). Lippe B.M. (33) сообщает, что через 2 года после начала тионамидной терапии ремиссия наблюдается в 25% случаев, а через 11 лет - уже в 75%. Douglas S. с соавторами (26) считают, что если у больных на фоне длительной тионамидной терапии имеется подавленный уровень ТТГ и они отказываются от радикальных методов лечения, прерывать консервативную терапию не следует, не смотря на длительность предыдущего лечения. Сходной точки зрения придерживается Volpe R. (50). В случаях предполагаемого тяжелого дефекта нельзя рассчитывать на иммунологическую ремиссию, независимо от длительности применения антити-реоидной лекарственной терапии. У этих больных низкие шансы спонтанной ремиссии и они нуждаются в ятрогенной деструкции щитовидной железы.
Исследование, проведенное в Бразилии, посвящено оценке сохранения ремиссии в зависимости от комбинации тиреостатика с ле-вотироксином. (41). Частота ремиссии у больных, получавших большие дозы тионамидов (для предотвращения симптомов гипотиреоза осуществлялась комбинация с левотироксином), составляла 75%, а у тех, кто получал монотерапию тионамидами в малых дозах - 42%. Авторы этой работы сделали вывод о большей эффективности высоких доз. Однако результаты европейского исследования ставят под сомнение этот вывод. В отличие от бразильского исследования, лево-тироксин одновременно с тиона-мидами получали все больные (40). Частота ремиссий среди больных, получавших метимазол в суточной дозе как 10, так и 40 мг, оказалась совершенно одинаковой. Таким образом, не исключается, что причиной более частых ремиссий, наблюдавшихся бразильскими авторами, среди больных, получавших высокие дозы тионамидов, является одновременное применение левотироксина.
Исследования Hashizume K. et al (30), проведенные в Японии в начале 90 годов прошлого века, привлекли внимание тиреоидологов. В одном из них больные диффузным токсическим зобом получали первые 6 месяцев метимазол в суточной дозе 30 мг. После этого их разделили на две группы: больные первой группы получали ежедневно 10 мг метимазола и 100 мкг ле-вотироксина, а пациенты второй группы - метимазол и плацебо. Лечение продолжалось в течение года. Затем метимазол был отменен, а прием левотироксина или плацебо продолжали еще 3 года. В течение этого периода в группе больных, получавших тироксин, рецидив диффузного токсического зоба наблюдался лишь у одного пациента (1,7%), тогда как в группе больных, получавших плацебо, рецидив диффузного токсического зоба отмечен у 34,7% (17 человек) больных. В другом исследовании лечение левотироксином после ме-тимазола во время беременности заметно снизило частоту рецидивов тиреотоксикоза в послеродовом периоде (4). До конца механизм, посредством которого реализуется помощь левотироксина в поддержании ремиссии диффузного токсического зоба, неизвестен. В первом исследовании эффект связывали с более низким уровнем ТТГ, но во втором - разницы в уровнях ТТГ в исследуемой и контрольной группах не наблюдалось. Еще в 1970 году W.Alexander с соавторами (17) назначали больным тиреотоксикозом после окончания приема тиреостатиков трийодтиро-нин и не обнаруживали различий в частоте рецидивов. В нескольких опубликованных исследованиях последних лет также не удалось подтвердить данных бразильских и японских авторов о большей частоте ремиссий при комбинированной терапии тиреотоксикоза (26, 47). Согласно данным греческих авторов дополнительное применение левотироксина не только не снижало, но напротив, увеличивало частоту рецидивов, даже на фоне низких цифр антител к рецептору ТТГ (48). В исследованиях, проведенных на московской популяции Г.А. Мельниченко с соавт. (9, 10), не было выявлено достоверного влияния левотироксина на иммуносу-прессивное действие тионамидов. Процент рецидивов в группе, получавшей и не получавшей левоти-роксин, составил 67,92 и 78,56% соответственно. Возможные причины противоречивости данных о влиянии левотироксина усматривались в высоком потреблении йода в Японии, других этнических различиях, неодинаковых схемах лечения и разном построении самих исследований.
Возможным маркерам постоянной ремиссии при тиреостатиче-ской терапии посвящена довольно обширная литература. Существует мнение, что наличие большого зоба и развитие преимущественной секреции Т3 обусловливает плохой прогноз заболевания. Winsa B. Dahlberg P.A. (58) Headly FJ (31) и другими авторами приводятся данные о том, что риск рецидива при консервативной терапии выше у лиц молодого возраста с большими размерами зоба, исходно высоким уровнем тиреоидных гормонов, при ассоциации с HLA-DR3 и DRW3, высоким уровнем тиреостимули-рующих антител на фоне лечения. На возможную роль генетических факторов в течении ДТЗ, в том числе и не ассоциированных с HLA, указывает Weetman A.P. (12, 54). Несколько иные прогностические факторы называют авторы, мнение которых заключается в том, что прогноз заболевания благоприятен у пациентов с неосложненным тиреотоксикозом, исходно высоким уровнем антител к тиреоперокси-дазе и у пациентов, щитовидная железа которых уменьшилась на фоне консервативной терапии (25, 27). Ряд исследователей не находит прогностической значимости уровня антител к тиреоглобулину и тиреопероксидазе (14, 16, 19, 20, 22, 28). Высокое соотношение Т3 к Т4 (более чем 20) некоторые авторы отмечают в качестве неблагоприятного прогностического признака (26, 48), в то же время подобную зависимость нашли не все.
Большинство исследователей с целью контроля эффективности лечения предлагают использовать определение тиреоидстиму-лирующих антител (20, 30, 32, 57) и результаты пробы с угнетением секреции Т3 (31). Было показано, что у лиц с положительными результатами пробы с Т3 риск рецидивов ниже на 50%, чем у лиц с отрицательными результатами этой пробы. Hedley A.J. et al. в 1989 году показали, что при отрицательной пробе с трийодтиронином 79% больных дали рецидивы тиреотоксикоза, причем 72% - в первый год наблюдения. При положительной пробе с Т3 рецидив отмечался только у 26-44% больных и в первый год наблюдения процент рецидивов был значительно ниже - 30%. Оценивать иммунологическую ремиссию предложено также с помощью пробы с тиреолиберином, отсутствие должного повышенияТТГ и Т 3 после лечения тионамида-ми - плохой прогностический признак (156). Помимо перечисленных выше, многие авторы (15, 18, 43, 46) к предикторам рецидива относят: субнормальный уровень ТТГ в сыворотке крови, «плоскую» кривую реакции ТТГ на введение ТРГ, высокий уровень тиреоглобулина при одновременном применении L-T4, высокое поглощение радиоактивного йода при одновременном применении с L-T4, гипоэхоген-ность тиреоидной ткани при УЗИ, HLA-D3 аллель DQA24. Однако в вопросе о том, что ни один из перечисленных маркеров сам по себе не является настолько точным, чтобы его можно было рекомендовать в практику, мнение большинства авторов совпадает (12). На наш взгляд, только группа факторов, имеющих единую направленность - риск развития тиреотоксикоза - может быть использована у конкретного пациента в выборе тактики его ведения.
Возможные механизмы наступления ремиссии у больных диффузным токсическим зобом можно разделить на три варианта:
1.Вследствие уменьшения продукции тиреоидстимулирующих антител;
2. Аутоиммунная деструкция тире-оидной ткани вследствие повышения уровня антител к тиреоидной пероксидазе и выраженной лимфо-идной инфильтрации;
3. Появления антител, блокирующих рецепторы ТТГ.
Volpe R. (52) считает, что первый вариант ремиссии может наблюдаться только у больных с относительно легкими нарушениями им-мунорегуляции. В последних двух случаях, речь, по-видимому, идет о сочетании ДТЗ с аутоиммунным ти-реоидитом, и вероятным исходом этих механизмов является развитие спонтанного гипотиреоза. По данным литературы (4, 12, 26, 49) количество таких больных составляет 3-5%. При развитии третьего варианта, в зависимости от преобладания титров стимулирующих или блокирующих иммуноглобулинов наблюдаются колебания от гипер- к гипотиреозу.
Одним из вариантов достижения иммунологической ремиссии, по мнению Volpe R. (50), является разрушение достаточного для предотвращения рецидива количества ти-реоидной паренхимы при лечении I 131 или тиреоидэктомии.
Терапия радиоактивным йодом широко используется в США и странах Западной Европы, является достаточно простым, эффективным и наиболее экономичным методом лечения диффузного токсического зоба (8, 29). С пониманием безопасности радиойодтерапии и растущим ее признанием больными, как считает Wartofsky L. (53), операция в качестве метода радикального лечения диффузного токсического зоба теряет популярность. Особенно это касается США, где операцию рекомендуют не более 1% американских тиреоидологов. Однако в настоящих условиях, на наш взгляд, говорить об отказе от хирургического метода лечения, как минимум, преждевременно, а возможно и вообще нереально. Это обусловлено целым рядом причин. Во-первых, число пациентов, получающих лечение радиоактивным йодом, у нас в стране крайне незначительно (8). Это связано как с объективными (нехватка медицинских учреждений проводящих лечение I 131 ), так и субъективными (настороженное отношение, как пациентов, так и врачей, большое количество противопоказаний) факторами. Во-вторых, ни у кого не вызывает сомнений, что большой зоб (поскольку радиойодтерапия в таких случаях может потребовать многократного введения изотопа в течение нескольких месяцев или лет, а также риск развития радиационного тиреоидита с дальнейшим увеличением объема ЩЖ), нефункциони-рующий «холодный» узел являются показанием к хирургическому лечению (7). Учитывая, что по данным различных авторов при гистологическом исследовании карцинома щитовидной железы сопутствовала диффузному токсическому зобу в 4,3-5,8% случаев, при использовании радиоактивного йода как метода лечения такие случаи могут быть пропущены. В-третьих, единственно возможной альтернативой у беременных женщин с неэффективностью тиреостатической терапии также является операция. И, наконец, в-четвертых, в настоящее время мнение о гипотиреозе, как безобидном и легко устранимом последствии радикальных методов лечения, подвергается критической переоценке. Проведенное недавно катамнестическое исследование показало, что среди больных, подвергнутых радиойодтерапии в связи с тиреотоксикозом, смертность от сердечно-сосудистых заболеваний и остеопороза возросла на 13%, что возможно, связано с неадекватной заместительной терапией гипотиреоза. Незначительная, но хроническая передозировка препаратов тиреоидных гормонов, не сопровождаясь классическими клиническими симптомами, вызывает гипертрофию миокарда, предсердную фибрилляцию и тромбоэмболию. С другой стороны, недостаточная доза тиреоидных гормонов и субклинический гипотиреоз, проявляющийся лишь слегка повышенным уровнем ТТГ, также достоверно увеличивает риск кар-диоваскулярной смерти.
В нашей стране преимущество традиционно отдается медикаментозной терапии. В идеале терапия тиреотоксикоза должна устранять его первопричину, однако при ДТЗ это невозможно, поскольку до сих пор не разработаны методы коррекции иммунных нарушений, в частности гиперпродукции антител к рецептору ТТГ.
В настоящее время основной группой препаратов, использующихся в лечении гипертиреоза при ДТЗ, являются тионамиды: метима-зол, карбимазол, пропилтиоурацил. Их механизм действия заключается в том, что, попадая в ЩЖ, они подавляют действие тиреоидной пе-роксидазы, ингибируют окисление йода, йодирование тиреоглобули-на и конденсацию йодтирозинов. В результате прекращается синтез тиреоидных гормонов и купируется тиреотоксикоз.
Как было указано выше, имеется гипотеза о том, что тионамиды влияют на иммунологические изменения, развивающиеся при ДТЗ. В частности, предполагается, что они влияют на активность и количество некоторых субпопуляций лимфоцитов, снижают иммуногенность ти-реоглобулина за счет уменьшения его йодирования, снижают продукцию простагландинов Е2, IL-1, IL-6 и продукцию белков теплового шока тироцитами.
Поскольку в организме карбима-зол почти полностью превращается в метимазол, то их эффекты совпадают. Пропилтиоурацил обладает дополнительным эффектом, тормозя конверсию Т4 в Т3 в периферических тканях. Однако, несмотря на это преимущество, метимазол быстрее нормализует уровень Т4 и Т3 в сыворотке крови. Это может быть связано с более выраженной активностью метимазола и с большей продолжительностью его действия. ПТУ отличается более коротким периодом действия, что требует соответственно более частого приема препарата. Поскольку тионамиды не блокируют транспорт йодида и не тормозят освобождение гормонов из их депо в щитовидной железе, компенсация тиреотоксикоза требует времени и в большинстве случаев на это уходит от 2 до 6 недель.
токсического зоба. Тирозол обладает менее выраженным риском возникновения побочных эффектов, разрешен к применению во время беременности, выпускается в дозах 5 и 10 мг. Применение дозировки Тирозола 10 мг позволяет снизить в два раза количество таблеток, принимаемых пациентом. Всю суточную дозировку Тирозола можно принимать 1 раз, т.к. препарат кумулирует в тиреоцитах, продолжительность действия однократно принятой дозировки - около 24 часов.
Лечение начинают с дозы 20-40 мг/сут. После достижения эутирео-идного состояния дозу препарата уменьшают до 5-10 мг/сут. Необходимо отметить, что для успешного лечения, длительность консервативной терапии должна быть не менее 12-18 месяцев.
Литература
Гипертиреоз

Наиболее опасен гипотиреоз для младенцев. Если не провести своевременное лечение гипертиреоза, то малыши получат многочисленные и необратимые осложнения, особенно при врождённом гипертиреозе щитовидки. Если до двух лет не вылечить у ребёнка гипертиреоз щитовидной железы, даже при последующем хорошем лечении невозможно предотвратить его умственную отсталость. Статистика гласит, что врождённым гипотиреозом страдает 1-2 из 5000 новорождённых, причем девочки в два раза чаще мальчиков.
Гипертиреоз щитовидной железы — это не самостоятельное заболевание, а комплекс симптомов, возникающий при ряде аутоиммунных заболеваний и состояний щитовидной железы:
- (болезнь Грейвса, Базедова болезнь, болезнь Перри, болезнь Флаяни);
- узловой токсический зоб (болезнь Пламмера);
- токсическая аденома щитовидной железы;
- начальная стадия подострого тиреоидита;
- бессимптомный (безболевой) тиреоидит;
- некоторые формы аутоиммунного тиреоидита;
- искусственный тиреотоксикоз (передозировка тиреоидных гормонов);
- опухоли других органов (весьма редко).
При гипертиреозе все процессы в организме человека происходят с повышенной интенсивностью, организм работает «на износ», в отличие от гипотиреоза, при котором все процессы замедляются.
Дисфункциями щитовидной железы страдает сегодня более трети землян. Данная железа в форме бабочки расположена в средней трети шеи между кадыком и началом грудины. Щитовидка — «королева» всех эндокринных желез, главный поставщик гормонов, влияющих на абсолютно все процессы в организме человека: на вес, настроение, работоспособность, физическое и психическое самочувствие и прочие. К примеру, никому ещё не удавалось снизить или увеличить свой вес по желанию при нездоровой щитовидке. Несмотря на главенствующую роль этой железы, люди весьма безответственно забывают о ней, а симптомы, указывающие на проблемы именно в щитовидной железе, списывают на переутомление, наследственность — на что угодно, теряя при этом драгоценное время и усложняя исход заболевания.
Классификация гипертиреоза
Многообразие причин гипертиреоза щитовидной железы создало, соответственно, большее количество этиологических вариаций болезни. Классификация позволила более чётко разделять особенности болезни, что важно при диагностировании для оценки индивидуального характера проблемы.
Объективно, по серьёзности нарушений гипертиреоз разделяют на:
- первичный, возникший в результате повреждений щитовидной железы лучевыми воздействиями, травмами, инфекциями, нападками собственной иммунной системы и другими патологиями;
- вторичный, возникший по причине патологических изменений в гипофизе или гипоталамусе.
Вспомним, что гипофиз — это железа, расположенная в основании головного мозга, вырабатывающая тиреотропный гормон (ТТГ) для регуляции работы щитовидной железы, а гипоталамус — это отдел промежуточного мозга, контролирующий работу гипофиза и щитовидной железы.
Первичный гипертиреоз, в свою очередь, подразделяется на несколько функциональных форм:
- субклиническую: уровень Т4 в норме, ТТГ понижен, отсутствие симптоматики;
- манифестную (проявленную) уровень Т4 повышен, ТТГ существенно снижен, присутствуют характерные признаки;
- осложнённую: наличие мерцательной аритмии, сердечной или надпочечниковой недостаточности, дистрофии паренхиматозных органов, психозов, существенной потери веса тела и прочее.
Морфологические формы гипертиреоза:
- Диффузный тиреотоксический (гипертиреоидный) гипертиреоз, как вариант общей активности ткани железы без её разрастания.
- Диффузный токсический зоб — интенсивная и распространённая деятельность железистой ткани практически во всей железе.
- Гипертиреоидный узел (одноузловой, автономный) — источник избытка тиреоидных гормонов щитовидки.
- Узловой гипертиреоз (многоузловой, автономный) — переизбыток тиреоидных гормонов двух и более узлов железы.
Этиологические формы гипертиреоза:
- острый и подострый тиреоидит (в период тиреотоксической фазы);
- послеродовой или гипертиреоз беременных;
- тиреотоксикоз новорожденных;
- наследственный (семейный);
- радиационно-индуцированный;
- йод-индуцированный;
- гиперпродукция ТТГ;
- гипертиреоз нетиреоидной гиперпродукции гормонов;
- ятрогенный (медикаментозный);
- травматический.
Осложнения гипертиреоза
При неудачном течении гипертиреоза может возникнуть тиреотоксический криз, спровоцированный большим физическим напряжением, стрессом или инфекционными заболеваниями, тогда вся симптоматика гипертиреоза усиливается до:
- сильной тахикардии с признаками сердечной недостаточности;
- отёчности и сильной истощённости;
- лихорадки, бреда и прочим.
Дальнейшее прогрессирование тиреотоксического криза может закончиться коматозным состоянием пациента и летальным исходом. Другой вариант криза — апатический — протекает с развитием равнодушия, апатии, кахексии. Примечательно, что тиреотоксический криз случается только у женщин.
В связи с этим обстоятельством специалисты различают от трёх до пяти стадий гипертиреоза, которые правильнее называть степенями.
Прогноз и профилактика гипертиреоза
Больные гипертиреозом, как правило, находятся на диспансерном учёте у эндокринолога. Грамотно избранная и вовремя проведенная терапия помогут в краткие сроки восстановить здоровье, хорошее самочувствие, а также избежать развития нежелательных осложнений. После достоверной диагностики следует срочно начать правильное лечение и помнить, что самолечение категорически противопоказано и чревато.
Профилактические подходы во избежание развития гипертиреоза заключаются в постоянном наблюдении и лечении патологий щитовидной железы, в рациональном питании (не злоупотреблять продуктами, содержащими йод) и соблюдении осторожности с солнечным излучением во время летнего отпуска — в общем, выполнении несложных правил.
Причины гипертиреоза
Признаки гипертиреоза возникают чаще всего как итог иных патологических процессов в щитовидной железе в возрасте от 20 до 50 лет и в большей степени у женщин (в 10 раз чаще, чем у мужчин). Гипертиреоз у женщин развивается вследствие гормональных колебаний в их организме во время критических дней, беременности, климаксе.
Самыми значимыми причинами возникновения гипертиреоза считаются:
- диффузно-токсический зоб (Базедова болезнь) — основная причина более чем в 80% случаев;
- болезнь (синдром) Пламмера — узловой токсический зоб, доброкачественная опухоль, клетки которой независимо (бесконтрольно) продуцируют тиреоидные гормоны;
- генетическая предрасположенность;
- аутоиммунные патологии;
- воспаление щитовидной железы (аутоиммунный/лимфоматозный/хронический тиреоидит);
- токсическая аденома щитовидной железы;
- аденома струмы яичника;
- цитокин-индуцируемый тиреоидит в начале заболевания;
- избыток потребляемого йода;
- передозировка тиреоидных гормонов при терапии от гипотериоза;
- продолжительные солнечные облучения;
- длительное пребывание в состоянии стресса;
- инфекционное заражение;
- заболевания гипофиза.
Симптомы гипертиреоза
У такого заболевания, как гипертиреоз, симптомы зависят от генетического преимущества симпатической или парасимпатической активности у человека, могут быть характерными или обратно противоположными, а потому не все симптомы должны быть обязательными, специфическими.
К наиболее типовым симптомам, зависящим от коэффициента пораженности органа, ткани, системы, относят:
- чётко выраженные нервно-психические нарушения — гипервозбуждённость, нервозность, раздражительность, плаксивость, появление скороговорения с повышением умственной деятельности, лёгкий тремор рук, чувство страха, беспокойства и бессонница;
- ощущение постоянного внутреннего жара, чрезмерная потливость;
- стремительная потеря веса (до анорексии у пожилых пациентов);
- постоянная слабость и усталость;
- сердечно-сосудистые нарушения — тахикардия, мерцание и трепетание предсердий, снижение диастолического и повышение систолического артериального давления, аритмия, сердечная недостаточность;
- нарушения со стороны органов зрения (около 45% случаев) — увеличение разреза глаз, выпячивание глазного яблока вперед (экзофтальм), двоением объектов, сокращение миганий, снижение подвижности глазного яблока, отечность и гиперпигментация век, также появляется эрозия и сухость роговицы, слезотечение и резь в глазах, при сдавливании и дистрофии зрительного нерва — слепота;
- ускорение и изменение обмена веществ (при повышенном аппетите — снижение массы тела);
- развитие тиреогенного диабета;
- почечная недостаточность как итог быстрого распада кортизола под воздействием гормонов щитовидной железы;
- изменения состояния кожных покровов — истончение, влажность, повышение температуры, изменения ногтей;
- ранняя седина, истончение и выпадение волос;
- развитие отёков мягких тканей голени;
- выпячивание щитовидной железы при диффузном токсическом зобе;
- одышка и снижение жизненной ёмкости лёгких в результате застоя и отёка лёгких;
- нарушение пищеварения и желчеобразования, повышенный аппетит (сниженный у пожилых), неустойчивый стул (диарея), увеличение печени (проявления желтухи в тяжелых случаях), приступообразные боли в животе;
- нарушения водного обмена (частое, обильное мочеиспускание и сильная жажда);
- признаки тиреотоксической миопатии — мышечная утомляемость, гипотрофия мышц, развитие остеопороза, дрожь во всем теле и постоянная слабость, нарушение двигательной активности (трудно выполнять обычные действия) вплоть до обратимого тиреотоксического мышечного паралича;
- нарушения секреции женских и мужских гонадотропинов, расстройство функций половой сферы (у мужчин — снижение потенции и гинекомастия, у женщин — нарушение менструального цикла, обмороки и общая слабость).
В зависимости от индивидуальных и других обстоятельств, все изменения могут иметь обратимое или мало обратимое действие. У такого недуга, как гипертиреоз, симптомы и лечение напрямую зависят от человеческого фактора.
Диагностика гипертиреоза
В силу своеобразной симптоматики гипертиреоза и сложности в её дифференцировки основными методами диагностики определены:
- опрос, осмотр, составление анамнеза пациента; на определение соотношения гормонов тироксина (Т3), трийодтиронина (Т4) и тиреотропного гормона (ТТГ); для определения её размеров, её структуры и наличия узлов, а также для оценки кровотока в железе (цветное доплеровское картирование) с помощью специального датчика;
- компьютерная томография (КТ) для определения места нахождения узлов;
- КТ, а лучше МРТ головного мозга для оценки состояния гипофиза при аденоме; для фиксации отклонений в работе сердечно-сосудистой системы;
- сцинтиграфия щитовидной железы с радиоизотопами для определения активности функций железы и узлов;
- пункционная тонкоигольная биопсия щитовидной железы, узла с целью исследования их тканей на злокачественность.
Лечение гипертиреоза
Тактика лечения выбирается, опираясь на понимание специалистами механизма развития заболевания, индивидуально для каждого человека, заболевшего гипертиреозом, с учетом анамнеза пациента, его возраста, наличия сопутствующих заболеваний, аллергии на лекарства, патологии, вызвавшей гипертиреоз и степень её тяжести.
При постановке диагноза «гипертиреоз» лечение происходит несколькими способами:
Консервативное лечение гипертиреоза
Медикаментозная терапия с назначением тиреостатических препаратов для блокировки активного продуцирования гормонов щитовидной железой и затрудняющие накопление йода —Тирозола, Пропицила, Мерказолила и прочих, требующая соблюдения системы в приеме и осуществления контроля за уровнем гормонов железы.
Следует знать, что лечение подобными препаратами противопоказано беременным и кормящим женщинам, и после лечения в течение года необходимо предохраняться от беременности.
Метод, издавна применявшийся ведущими российскими клиницистами и основанный на седатации сегментарной вегетативной нервной системы, позволяет успешно восстанавливаться больным гипертиреозом, особенно эффективен при диффузном токсическом зобе (клиника д-ра А.В. Ушакова).При отсутствии улучшений через 1,5-2 года рекомендуется удаление железы хирургическим путём или разрушение её клеток с помощью лучевой терапии.
Обязательным к консервативному лечению дополнением должно быть рациональное и полноценное питание, обогащенное всеми полезными для здоровья компонентами: зелень, овощи, ягоды, фрукты, мясо, рыба, молочные продукты. Очень важны для больного гипертиреозом человека — спокойная обстановка окружения, полноценный и регулярный отдых и сон.
Хирургическое лечение гипертиреоза
Хирургический метод лечения показан:
- в случае неудачной консервативной терапии;
- при сдавлении органов средостения;
- при развитии тяжелых побочных эффектов от тиреостатиков;
- при подозрении на злокачественное новообразование в щитовидной железе.
После обсуждения и выбора метода лечения с пациентом обсуждается объём оперативного вмешательства — резекция или полное удаление щитовидной железы.
Наличие одиночного узла или множественного разрастания определённого участка щитовидной железы с повышенным выделением гормонов также требует хирургического вмешательства, а послеоперационный остаток железы будет нормально функционировать. Послесубтотальной резекции, когда удаляется большая часть щитовидной железы, может развиться гипотиреоз, а пациент всю свою жизнь будет принимать искусственные гормоны, но риск рецидива тиреотоксикоза намного снижается.
Лечение гипертиреоза радиоактивным йодом
Употребление пациентом капсулы или водного раствора (без вкуса и запаха) препарата радиоактивного йода (радиойодотерапия) происходит единственный раз. Из кровяного русла радиойод попадает в клетки щитовидной железы, страдающей гиперфункцией, скапливается там и разрушает их за несколько недель. В итоге размеры щитовидной железы уменьшаются, продуцирование гормонов и их уровень в крови снижаются. Радиойодотерапия обычно совмещается с медикаментозным лечением и снижает степень гипертиреоза, однако полное выздоровление не наступает. Возможно проведение повторного курса плюс пожизненный приём тиреоидных гормонов.
Другие методы лечения гипотиреоза
В терапии гипертиреоза возможно применение ß-адреноблокаторов, парализующих действие тиреоидных гормонов на организм, и больной может почувствовать улучшение на несколько часов, хотя избыток тиреоидных гормонов в крови останется. К ß-адреноблокаторампринадлежат препараты: атенолол, метопролол, надолол, индерал-ла, имеющие пролонгированное действие. Как исключительный метод лечения эти медикаменты могут использоваться при гипертиреозе, возникшем из-за тиреоидита. Данные блокаторы могут сочетаться с другими видами терапии.
Данная статья размещена исключительно с целью ознакомления в познавательных целях и не является научным материалом или профессиональным медицинским советом. За диагностикой и лечением обратитесь к врачу.
Введите ваши данные, и наши специалисты свяжутся с Вами, и бесплатно проконсультируют по волнующим вас вопросам.
Читайте также:
