Лучевая диагностика травмы тонкой кишки и ее брыжейки
Добавил пользователь Дмитрий К. Обновлено: 28.01.2026
Научно-исследовательский институт скорой помощи им. Н.В. Склифосовского, Москва
Хирургические доступы к забрюшинным органам и структурам при травме живота
Журнал: Хирургия. Журнал им. Н.И. Пирогова. 2015;(7): 75‑77
Представлено подробное описание с иллюстрациями трех хирургических доступов, которые авторы используют для ревизии забрюшинных органов и структур у пострадавших с закрытой травмой и ранением живота. Приведены клинические наблюдения успешного использования разработанных доступов.
По данным Федеральной службы государственной статистики травмы, отравления и другие последствия воздействия внешних причин устойчиво занимают второе место в структуре заболеваемости населения Российской Федерации (86,2—91,7 на 1000 человек), уступая только болезням органов дыхания. Травма живота имеет место примерно у 8% пострадавших и у 20—40% из них приводит к образованию забрюшинного кровоизлияния. Таким образом, актуальность проблемы диагностики и лечения травматических забрюшинных кровоизлияний не вызывает сомнений.
Причиной образования забрюшинного кровоизлияния может быть повреждение крупных кровеносных сосудов и жизненно важных органов: абдоминального отдела пищевода, двенадцатиперстной кишки (ДПК) и толстой кишки, поджелудочной железы, почек, надпочечников, мочеточников, мочевого пузыря, абдоминального отдела аорты и ее ветвей, нижней полой вены и ее притоков. Почти все исследователи [1, 2, 5, 6, 8, 10, 11, 13, 16, 17, 20] считают ревизию раневого канала в забрюшинном пространстве абсолютно необходимой. Ревизия забрюшинного кровоизлияния при закрытой травме имеет и сторонников [3, 7], и противников [18]. Большинство авторов [9, 12, 14, 15, 19, 21] пропагандируют дифференцированный подход к ревизии.
Методы ревизии органов и структур забрюшинного пространства (за исключением приема Кохера) малоизвестны практическим хирургам. Выполнить ревизию органов и структур, расположенных выше или на уровне корня брыжейки поперечной ободочной кишки, т. е. тела и хвоста поджелудочной железы (особенно по задней поверхности), аорты и ее ветвей, нижней полой вены и ее притоков не просто. Особенно важен адекватный оперативный доступ при ранении, когда ревизию раневого канала необходимо выполнить по всей его длине. Как правило, его рассечение производят в условиях ограниченного пространства, сложных топографоанатомических взаимоотношений и плохой визуализации структур на фоне забрюшинного кровоизлияния.
Мы используем три принципиально разных доступа в зависимости от локализации забрюшинного кровоизлияния.
1. Левосторонний доступ (прием Mattox [4]) применяем при локализации забрюшинного кровоизлияния слева от диафрагмы до корня брыжейки поперечной ободочной кишки. Этот доступ дает возможность выделить и осмотреть аорту от диафрагмы до инфраренального отдела, чревный ствол, верхнюю брыжеечную и левую почечную артерии, селезенку, хвост и тело поджелудочной железы, нисходящую ободочную кишку, селезеночную артерию, левую почку и левый мочеточник. Схема левостороннего доступа представлена на рис. 1 (см. и далее).
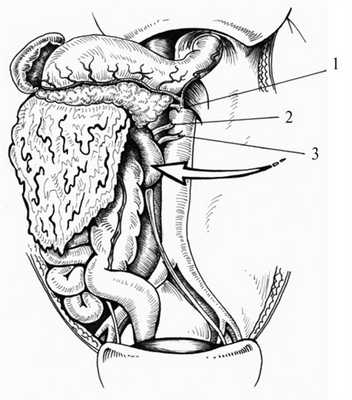
Рис. 1. Схема левостороннего доступа. 1 — чревный ствол, 2 — верхняя брыжеечная артерия, 3 — левая почечная артерия. Стрелка — направление смещения органов.
Производим тотальную срединную лапаротомию. Рассекаем париетальную брюшину на 1—2 см латеральнее и вдоль нисходящей ободочной кишки и пересекаем диафрагмально-ободочную связку (линия рассечения брюшины на рис. 2, а маркирована бриллиантовым зеленым). Тупым путем отделяем нисходящую ободочную кишку с питающими сосудами вместе с левой почкой, селезенкой, хвостом и частично телом поджелудочной железы в медиальном направлении (см. рис. 2, б). Мобилизацию названных выше органов продолжаем таким образом, чтобы вся забрюшинная клетчатка была отсепарована от мышц задней поверхности живота (см. рис. 2, в). После этого постепенным разделением забрюшинной клетчатки в нижней части разреза в медиальном направлении выделяем аорту в инфраренальном отделе. Затем, продолжая диссекцию краниально вдоль левой и передней стенок аорты, выделяем левую почечную и верхнюю брыжеечную артерии, чревный ствол (см. рис. 2, г). После разделения позадипочечной клетчатки полностью доступной осмотру становится левая почка и проксимальная часть левого мочеточника (см. рис. 2, д). Разделение парапанкреатической клетчатки позволяет осмотреть хвост и, частично, тело поджелудочной железы, а также дистальную часть селезеночной артерии (см. рис. 2, е). Осторожная мобилизация заднелевой стенки брюшного отдела аорты позволяет выделить поясничные артерии. При таком доступе также доступны осмотру поясничная часть диафрагмы и мышцы задней брюшной стенки.
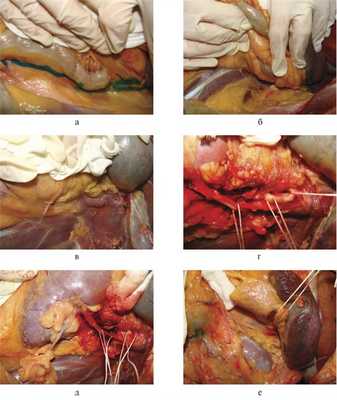
Рис. 2. Аутопсийные фотографии. Этапы выполнения левостороннего доступа (объяснение в тексте).
2. Правосторонний доступ (рис. 3) сочетает одновременное выполнение приема Кохера и мобилизации правой половины ободочной кишки. Применяем его при локализации забрюшинного кровоизлияния справа от диафрагмы до корня брыжейки тонкой кишки. Этот прием делает доступным осмотру нижнюю полую вену от инфрагепатического отдела до подвздошных вен, правую почку и мочеточник, восходящую ободочную кишку, верхнегоризонтальную, нисходящую и частично нижнегоризонтальную часть ДПК, правую почечную и подвздошную артерию.
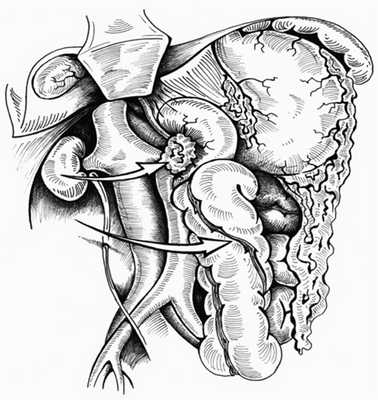
Рис. 3. Схема правостороннего доступа. Стрелки — направление смещения органов.
Производим верхнесредне-срединную лапаротомию. Рассекаем париетальную брюшину на 1—2 см латеральнее и вдоль восходящей ободочной кишки до уровня ее правого изгиба, затем разрез продлеваем краниально вдоль нисходящей части ДПК (прием Кохера). Восходящую ободочную кишку и ДПК с головкой поджелудочной железы в едином блоке отводим медиально так, чтобы диссекция тканей проходила во фронтальной плоскости кпереди от правой почки и почечных сосудов. Таким образом, верхнегоризонтальную, нисходящую и частично нижнегоризонтальную части ДПК, головку поджелудочной железы, восходящую ободочную кишку с питающими сосудами отводим медиально и кпереди. При этом становятся доступными осмотру не только перечисленные выше органы, но и нижняя полая вена от инфрагепатического отдела до подвздошных вен, обе почечные вены, правая почка и мочеточник, правая общая подвздошная артерия (рис. 4).
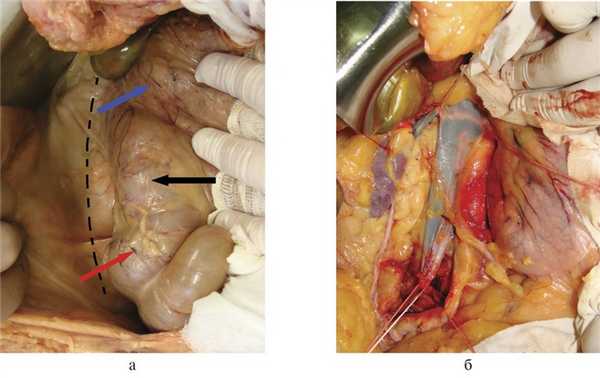
Рис. 4. Аутопсийные фотографии. а — правосторонний доступ. Пунктиром обозначена линия разреза брюшины вдоль восходящей ободочной кишки, красная стрелка — слепая кишка, черная стрелка — восходящая ободочная кишка, синяя стрелка — двенадцатиперстная кишка; б — вид операционного поля после выполнения доступа.
3. Нижний доступ (рис. 5) применяем при локализации забрюшинного кровоизлияния в области тела поджелудочной железы, корня брыжейки поперечной ободочной и тонкой кишки. Этот доступ позволяет визуализировать нисходящую, нижнегоризонтальную, восходящую части ДПК. Также оказываются доступными осмотру и оперативному приему передняя и задняя поверхности головки и тела поджелудочной железы, аорта от устьев почечных артерий и нижняя полая вена.
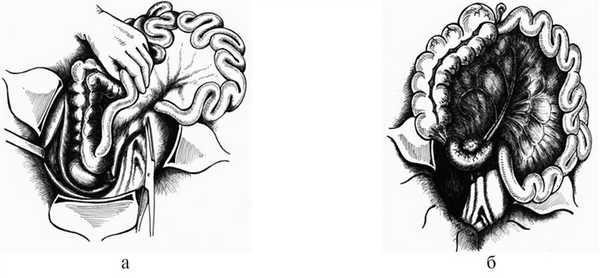
Рис. 5. Схема нижнего доступа. а — начало, б — окончание.
После верхнесредне-срединной лапаротомии рассекаем париетальную брюшину на 1—2 см латеральнее слепой и восходящей ободочной кишок и параллельно им (рис. 6, а). Затем разрезом париетальной брюшины огибаем снизу слепую кишку и продолжаем его краниально и влево вдоль корня брыжейки тонкой кишки (см. рис. 6, б). Начиная со слепой кишки, отслаиваем ее и восходящую ободочную кишку с питающими их сосудами в медиальном и краниальном направлениях, а также брыжейку тонкой кишки (краниально). Последовательно отделяем всю нижнегоризонтальную и восходящую части ДПК, головку и тело поджелудочной железы, нисходящую и верхнегоризонтальную части ДПК от задней стенки живота (см. рис. 6, в). Перечисленные выше органы отводим также краниально. Затем отделяем переднюю стенку нисходящей части ДПК от корня брыжейки поперечной ободочной кишки (см. рис. 6, г).
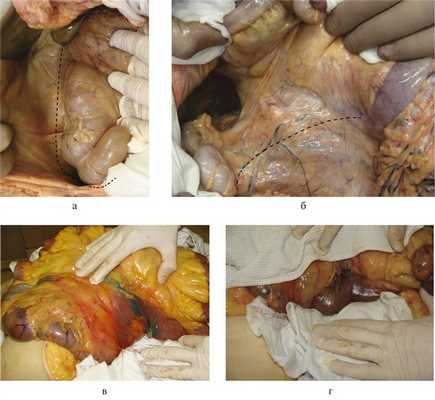
Рис. 6. Аутопсийные фотографии. Этапы выполнения нижнего доступа (объяснение в тексте).
Среди 166 пострадавших с проникающими колото-резаными ранениями живота, поступивших в Институт скорой помощи им. Н.В. Склифосовского, технические трудности отмечены у 3 (5,9%) из 51 пострадавшего с левосторонним латеральным забрюшинным кровоизлиянием, у 3 (7,7%) из 39 с нижнемедиальным, у 1 (8,3%) из 12 с верхнемедиальным, у 4 (10,8%) из 37 с правосторонним латеральным, у 1 (14,3%) из 7 с тазовым, у 4 (23,5%) из 17 с распространенным кровоизлиянием. Применение представленных доступов позволило выполнить полноценную ревизию, обнаружив все повреждения.
Приводим клинические наблюдения.
Больной Т., 28 лет, доставлен через 2 ч после травмы. При поступлении состояние средней тяжести. Вентиляционных и гемодинамических расстройств нет. Живот болезненный в левой половине, перитонеальные симптомы не определяются. Колото-резаная рана размером 30×8 мм в левой боковой области живота. При УЗИ обнаружены признаки большого левостороннего забрюшинного кровоизлияния.
Под эндотрахеальным наркозом выполнена верхнесредне-срединная лапаротомия. В брюшной полости крови нет. Через брюшину в области левого брыжеечного синуса просвечивает кровоизлияние с пропитыванием (рис. 7, а).
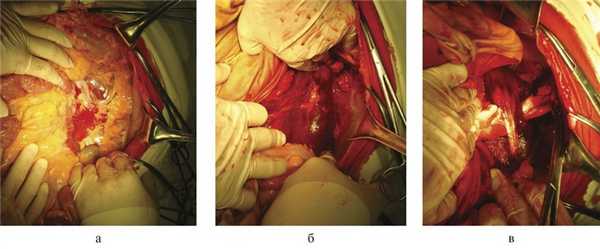
Рис. 7. Операционные фотографии. а — левостороннее латеральное забрюшинное кровоизлияние; б — вид после левостороннего доступа, гематома левой большой поясничной мышцы; в — рана большой поясничной мышцы.
Больная С., 30 лет, доставлена через 1,5 ч после травмы с клинико-инструментальной картиной наружного и внутрибрюшного кровотечения, причиной которого были множественные колото-резаные раны груди, правой поясничной области и конечностей. При катетеризации мочевого пузыря отмечена макрогематурия.
Под эндотрахеальным наркозом выполнена верхнесрединная лапаротомия. В брюшной полости 100 мл крови. Обнаружена рана бокового ската правой половины диафрагмы и рана сегмента VII печени, рана бокового ската левой половины диафрагмы и рана желудочно-ободочной связки, размер всех ран 10×2 мм. Визуализировано правостороннее забрюшинное паранефральное кровоизлияние с образованием свертков и переходом на парадуоденальную, параколическую и парапанкреатическую (кпереди от головки и перешейка поджелудочной железы) клетчатку. Раны печени и обеих половин диафрагмы ушиты. Выполнен правосторонний доступ, обнаружена сквозная рана нижнего полюса правой почки размером 10×3 мм, проходящая через нижнюю чашечку, и рана наружной стенки нисходящей части ДПК размером 3×1 мм с подтеканием желчи. При ревизии парапанкреатического кровоизлияния повреждения органов и сосудов не обнаружено. Выполнена правосторонняя нефрэктомия. Рана ДПК ушита двухрядными отдельными швами нитью PGA 4/0 и лаваном 2/0 на атравматической игле. Операция закончена дренированиием брюшной полости и ушиванием лапаротомной раны.
Несмотря на проведение антиферментной терапии (октреотид 900 мг/сут), течение послеоперационного периода осложнилось развитием травматического панкреатита, парапанкреатического инфильтрата. Больная выписана после проведения курса консервативной терапии, которая привела к резорбции инфильтрата.
Больной К., 18 лет, доставлен через 1 ч после травмы с признаками внутрибрюшного кровотечения. Колото-резаная рана размером 15×5 мм находилась справа в мезогастральной области.
Под эндотрахеальным наркозом выполнена верхнесрединная лапаротомия. В брюшной полости 900 мл крови и сгустков. При ревизии выявлена сквозная рана поперечной ободочной кишки размером 3×2 мм, рана брыжейки поперечной ободочной кишки, две сквозные раны тонкой кишки размером 2×2 мм на расстоянии 2 м от связки Трейтца, дистальнее на 10 см две сквозные раны брыжейки тонкой кишки размером 2×2 мм. При дальнейшей ревизии обнаружено массивное забрюшинное кровоизлияние с образованием свертков, распространяющееся от нижнегоризонтальной ветви ДПК до малого таза. Произведена ревизия структур забрюшинного пространства с использованием нижнего доступа. Выявлены рана передней стенки нижней полой вены размером 2×1 мм, отсечение правой яичковой вены в месте ее впадения в нижнюю полую вену, а также сквозная рана нижнегоризонтальной части ДПК размером 2×2 мм. Раны нижней полой вены ушиты нитью Prolene 4/0. Достигнут гемостаз. Выполнено поэтапное ушивание ран ДПК, тонкой и ободочной кишки, ушивание ран брыжейки ободочной и тонкой кишки. Операция закончена назоинтестинальной интубацией и дренированием брюшной полости. Течение послеоперационного периода без осложнений.
Таким образом, использование разработанных универсальных доступов позволяет выполнить полноценную ревизию забрюшинных органов и структур в сложных топографоанатомических условиях и при наличии забрюшинного кровоизлияния различной локализации и распространения.
Заворот кишок (K56.2)
Примечание
В данную подрубрику включены:
- странгуляция ободочной или тонкой кишки;
Из данной подрубрики исключены:
- "Непроходимость двенадцатиперстной кишки" - K31.5
- "Врожденные аномалии фиксации кишечника" - Q43.3
- "Другая уточненная непроходимость кишечника у новорожденного" - P76.8
- "Непроходимость кишечника у новорожденного неуточненная" - P76.9

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 800 RUB / 4500 KZT / 27 BYN - 1 рабочее место в месяц

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место - 800 RUB / 4500 KZT / 27 BYN в месяц
Мне интересно! Свяжитесь со мной
Классификация
Этиология и патогенез
Возникновение заворота в значительной степени связано со следующими факторами:
- состояние брыжейки и особенности ее прикрепления;
- наличие рубцовых изменений, которые обуславливают сближение между собой кишечных петель и удлинение участка кишки и брыжейки вследствие застоя и растяжения;
- фиксация петель кишечника и брыжейки спайками.
Поворот петли происходит вокруг оси брыжейки и при ее достаточной длине. Степень перекрута различна - от 90° до одного-двух полных оборотов. Чем сильнее перекручивание, тем больше нарушаются проходимость петли и ее питание.
Способствующие завороту кишок факторы:
- повышение внутрибрюшного давления при физическом напряжении (поднятие тяжестей);
- усиление перистальтики при переполнении кишечника неудобоваримой пищей в больших объемах, особенно после длительного голодания;
- запоры.
Наиболее часто встречаются завороты тонкой, сигмовидной и слепой кишок.
Тонкий кишечник
Практически все завороты тонкой кишки связаны с врожденными аномалиями. Основная из не связанных с врожденными аномалиями причин - приобретенные спайки брюшной полости.
Заворот тонкой кишки чаще происходит по ходу часовой стрелки. Длина вовлеченных в процесс кишечных петель различна. Возможен и тотальный заворот тонкой кишки.
- спайки;
- беременность;
- объемные образования в малом тазу;
- состояния после оперативного вмешательства на кишечнике;
- применение препаратов, влияющих на моторику кишечника.
Заворот кишок может развиваться в любой части толстой кишки. Наиболее часто развивается в сигмовидной кишке из-за особенностей анатомии брыжейки. Реже заворот кишок встречается в правом отделе толстой кишки и терминальном отделе подвздошной кишки или только в слепой кишке. В редких случаях может развиться заворот поперечно-ободочной кишки или толстой кишки в области селезеночного изгиба.
Полный заворот приводит к развитию замкнутой обструкции пострадавших сегментов кишечника. Увеличение дилатации петли кишечника вызывает нарушения кровоснабжения кишечника. В конечном итоге все это приводит к ишемии, гангрене и перфорации кишечной стенки.
Эпидемиология
Возраст: преимущественно зрелый и пожилой
Признак распространенности: Распространено
Соотношение полов(м/ж): 2
Локализация. Наиболее распространены завороты толстого кишечника:
- сигмовидной кишки - 80%;
- слепой кишки - 15%;
- поперечно-ободочной кишки - 3%;
- заворот в области селезеночного изгиба - 2%.
Возраст
Заворот сигмовидной кишки характерен для людей зрелого и пожилого возраста (средний возраст - 60 лет). Заболеваемость увеличивается с возрастом.
Заворот слепой кишки развивается в более молодом возрасте. Средний возраст возникновения - 50 лет. В отдельных регионах средний возраст возникновения заболевания значительно моложе (например, в Индии - 33 года).
В детском возрасте заворот толстого кишечника и слепой кишки является редкостью. Преобладающими в детском возрасте являются завороты тонкого кишечника, связанные с врожденной патологией и рассматривающиеся в отдельной подрубрике. Приобретенные завороты кишечника у детей считаются редкостью.
Пол. В разных возрастных группах и разных регионах соотношение полов различно. По усредненным оценкам преобладают мужчины, однако заворот слепой кишки встречается немного чаще у женщин.
Раса. Данные противоречивы. По общему мнению, лица африканской расы болеют в 2 раза чаще.
Другие условия
После спаек, заворот сигмовидной кишки является второй наиболее распространенной причиной непроходимости кишечника во время беременности (25-44% всех случаев). Предполагается, что во время беременности увеличенная матка может смещать сигмовидную кишку, что иногда приводит к скручиванию толстой кишки. В результате большинство (75%) случаев заворота у беременных происходит в течение третьего триместра.
Пациенты домов престарелых и психоневрологических клиник составляют значительную долю пациентов с заворотом толстого кишечника.
Факторы и группы риска
Заворот тонкой кишки (как правило, ассоциирован с врожденной патологией):
- врожденные аномалии развития;
- спаечные процессы в брюшной полости;
- внутренние грыжи брюшной полости
Заворот слепой кишки (преимущественно ассоциирован с врожденными аномалиями):
- аномально удлиненная брыжейка;
- хирургические операции на слепой кишке с ее мобилизацией;
- аппендицит с образованием спаек;
- колоноскопия Колоноскопия - метод исследования внутренней поверхности толстой кишки, основанный на ее осмотре с помощью колоноскопа.
;
- объемные образования органов малого таза и брюшной полости.
Клиническая картина
Клинические критерии диагностики
рвота; вздутие живота; запор; ассиметрия живота; каловая рвота; отсутствие симптомов раздражения брюшины; пальпируемое образование в проекции кишечника; шум плеска; тимпанит при перкуссии живота; дегидратация; тахикардия; боль в животе; усиление перистальтики
Cимптомы, течение
Типично острое начало. Появляется интенсивная боль в брюшной полости. Боль может иметь различную локализацию: эпигастральная или пупочная область, правая половина, нижние отделы живота.
Вслед за болью возникает рефлекторная рвота съеденной накануне пищей. Затем рвота становится частой и обильной, рвотные массы представлены застойным кишечным содержимым. На поздних стадиях заворота рвота приобретает каловый характер.
При тонкокишечном завороте всегда присутствует задержка стула и газов. В некоторых случаях в первые часы заболевания может наблюдаться акт дефекации за счет содержимого дистального отдела кишечника.
Больные находятся в тяжелом состоянии, которое прогрессивно ухудшается. Язык сухой и обложеный налетом грязного цвета.
При пальпации в начале заворота живот безболезнен и не вздут. У худощавых больных иногда удается прощупать узловатый конгломерат петель кишечника.
Заворот сигмовидной кишки
1. Остро протекающая форма:
- внезапная интенсивная схваткообразная боль с локализацией в левой половине живота;
- рвота;
- нередко - коллапс;
- быстрое развитие некроза кишечных петель с нарастанием перитонита.
2. Подостро прогрессирующая форма. Имеет постепенное начало и более легкое течение. Больные с данной формой поступают в больницу спустя 3-4 дня после появления симптомов. Как правило, в анамнезе у 50% пациентов уже наблюдались подобные приступы боли. Рвота возникает поздно. Живот вздут. При перкусии выявляется тимпанит Тимпанит (перкуторный звук тимпанический) - громкий, средней высоты или высокий перкуторный звук, возникающий при перкуссии над полым органом или полостью, содержащей воздух
. Ампула прямой кишки пуста и расширена.
Наряду с общими симптомами кишечной непроходимости, при завороте сигмовидной кишки присутствуют следующие типичные признаки:
При завороте слепой кишки длительность периода от возникновения симптомов до поступления в больницу может колебаться от 2 часов до 10 дней, (в среднем 2 дня).
Примечание. При любом виде заворота симптоматология, особенно в начале заболевания, зависит от быстроты наступления заворота.
Диагностика
Визуализация играет решающую роль в диагностике и дифференциальной диагностике заворота кишок.
1. Обзорная рентгенография.
1.1 Заворот сигмовидной кишки. На обзорной рентгенограмме брюшной полости выявляют резко увеличенную в объеме сигмовидную кишку, доходящую до диафрагмы, с двумя уровнями жидкости: одним в проксимальном конце непроходимой кишки, другим - в дистальном.
2.1 Заворот сигмовидной кишки. Место заворота имеет вид "клюва" ("пикового туза"), над которым определяется значительно расширенная петля сигмы. При ориентации “клюва” в правую сторону присутствует заворот по ходу часовой стрелки, влево - в обратном направлении.
2.2 Заворот слепой кишки. Во время ирригографии барий проходит только до середины восходящей ободочной кишки.
3. Оральное контрастирование (применяется только при подозрении на непроходимость тонкого кишечника):
- препятствие прохождению контраста;
- раздувшиеся петли тонкого кишечника;
- понижение наполнения толстого кишечника.
4. Компьютерная томография - "золотой стандарт" диагностики. Исследование особенно полезно при завороте слепой и тонкой кишок. При завороте возможно выявление специфического признака "знак бури" (спираль), расширение кишки, отек брыжейки, утолщение стенки кишки.
Диагностика заворота у беременных
При появлении болей в верхней части живота у беременных (вне зависимости от срока беременности) рекомендуется начинать обследование с УЗИ. При завороте, несмотря на затрудненное исследование газосодержащих органов, УЗИ может выявить раздутые петли кишечника, выпот в брюшной полости и др. признаки заболевания.
Диагностическая лапароскопия - высокоинформативный метод диагностики при кишечной непроходимости в I триместре беременности и в послеродовом периоде. Начиная со II триместра, использование метода затруднено вследствие увеличенных размеров матки и негативного влияния наркотических средств на плод.
Проведение колоноскопии нежелательно из-за возможного развития угрозы прерывания беременности.
Рентгенологические методы исследования противопоказаны при беременности и могут проводиться только в случае крайней необходимости, при подозрении на острую кишечную непроходимость и сроке беременности больше 13 недель (обзорная рентгенография брюшной полости).
Лабораторная диагностика
Не существует специфических лабораторных тестов, подтверждающих диагноз заворота кишок. Тем не менее надлежащие анализы должны быть выполнены для диагностики осложнений (некроз кишечника) и дифференциальной диагностики.
1. Общий анализ крови:
- умеренный лейкоцитоз;
- повышение СОЭ.
Значительное повышение этих показателей указывает на некроз кишечника. Повышение гематокрита может быть связано с рвотой.
3. Печеночные пробы: амилаза и липаза, как правило, в норме.
4. Анализ кала: иногда выявляется примесь крови в стуле (признак некроза слизистой).
Дифференциальный диагноз
Заворот тонкой кишки, если он не связан со спайками брюшной полости и опухолями, почти всегда связан с аномалиями развития. Дополнительно тонкокишечную непроходимость могут вызвать дивертикулы , опухоль, камни тонкого кишечника, спайки.
Заворот сигмовидной кишки. Дифференциальный диагноз включает рак толстой кишки, дивертикулит, брыжеечную ишемию и другие виды непроходимости кишечника.
Заворот слепой кишки обычно встречается в молодом возрасте и поэтому наиболее часто его приходится отличать от аппендицита, разрыва кисты яичника, инфекции мочевыводящих путей, дивертикулита, воспалительных заболеваний кишечника и непроходимости кишечника другой этиологии.
Решающую роль в дифференциальной диагностике, как и в установке диагноза, играют методы визуализации.
Осложнения
Прочие осложнения при хронической, неполной непроходимости:
- кисты брыжейки и хилезный асцит;
- спайки и стенозы кишечника.
Лечение
4. Контроль сопутствующей патологии.
5. Поскольку давление на нижнюю полую вену может привести к нарушению венозного возврата, пациент должен находиться в положении на левом боку (для улучшения венозного возврата).
6. Катетер Фолея для контроля диуреза .
При завороте тонкой кишки показано только хирургическое вмешательство - расправление заворота.
Если перитонит отсутствует, нежизнеспособные кишечные петли резецируются и формируется межкишечный анастомоз .
При наличии перитонита накладывается двуствольная илеостома с восстановлением целостности кишечника через 2-3 месяца.
Показания к хирургическому вмешательству:
- острая форма заворота сигмовидной кишки;
- неэффективность консервативных мероприятий при подостро прогрессирующей форме заворота.
При жизнеспособности сигмы применяются паллиативные и радикальные операции.
Паллиативные вмешательства: расправление заворота, реторсия в сочетании с мезосигмопликацией или сигмопексией.
Сигмопексии:
- подшивание кишки к париетальной брюшине;
- фиксация брыжейки кишки к париетальной брюшине;
- помещение сигмовидной кишки под выкроенный лоскут париетальной брюшины или в карман в предбрюшинном пространстве.
Данные операции характеризуются высоким процентом рецидивов.
Радикальные операции предполагают выполнение резекции сигмовидной кишки с первичным анастомозом "конец в конец", "конец в бок".
Резекция сигмы с первичным анастомозом редко применяется в случае заворота сигмы, осложненного гангреной. Это связано с высокой опасностью несостоятельности швов вследствие имеющегося нарушения микроциркуляции в стенке кишки.
Наиболее часто применяется операция Гартмана: резекция нежизнеспособного участка сигмы с ушиванием ее дистального конца и выведением проксимального противоестественного заднепроходного отверстия. После улучшения состояния больного (в среднем через 3 месяца) на втором этапе операции кишечный свищ закрывается.
Послеоперационное лечение:
- инфузионная терапия;
- антибактериальная терапия.
Возможные послеоперационные осложнения:
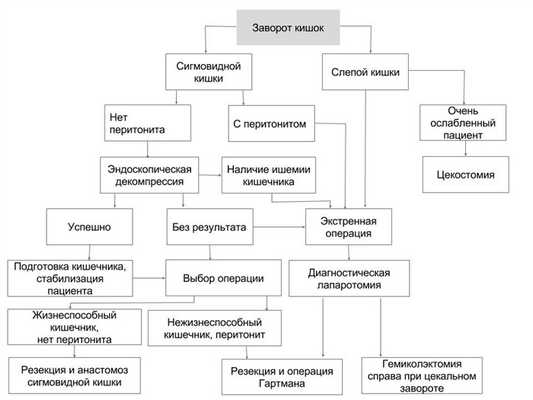
Схема выбора метода лечения при завороте кишки
Прогноз
Рецидивы. Частота рецидивов после эндоскопической декомпресии составляет до 50%.
Госпитализация
Профилактика
1. Профилактика запоров:
- контроль применения психотропных, слабительных и иных фармакологических препаратов, влияющих на моторику желудочно-кишечного тракта;
- ограничение в питании чрезмерного количества грубой клетчатки.
Лучевая диагностика травмы тонкой кишки и ее брыжейки
ГБУЗ «Научно-исследовательский институт скорой помощи им. Н.В. Склифосовского» Департамента здравоохранения Москвы, Москва, Россия
ГБУЗ «Научно-исследовательский институт скорой помощи им. Н.В. Склифосовского» Департамента здравоохранения Москвы, Москва, Россия;
ФГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования», Москва, Россия
- SPIN РИНЦ: 4044-9661
- Scopus AuthorID: 55970485700
- ResearcherID: P-9151-2017
- ORCID: 0000-0003-1270-5414
ГБУЗ Научно-исследовательский институт скорой помощи им. Н.В. Склифосовского, Москва, Россия
НИИ скорой помощи им. Н.В. Склифосовского, Москва
ГБУЗ Москвы «Научно-исследовательский институт скорой помощи им. Н.В. Склифосовского» Департамента здравоохранения Москвы, Москва, Россия
Закрытая травма живота с повреждением кишечника, изолированная и сочетанная
Журнал: Хирургия. Журнал им. Н.И. Пирогова. 2019;(5): 82‑87
Приведены 3 клинических наблюдения закрытой травмы живота с повреждением кишечных петель и развитием перитонита. Авторы подчеркивают значение лучевых методов диагностики, прежде всего УЗИ, и диагностической видеолапароскопии в ранней диагностике особенностей травматического повреждения.
Количество пострадавших с травмой органов брюшной полости, по данным [1, 2], составляет 21—25% и не имеет тенденции к снижению. По оценке разных авторов [3—5], повреждение кишечника при закрытой травме живота составляет от 6,3 до 38,5%, летальность достигает 12—15%, а при разрывах брыжейки кишки, стенки кишки и массивных гематомах ее брыжейки с перитонитом летальность составляет 19—24%.
Материал и методы
Представляем 3 клинических наблюдения изолированной и сочетанной травмы живота с повреждением кишечника за период с августа 2017 г. по февраль 2018 г.
Больная М., 48 лет, поступила в приемное отделение НИИ СП им. Н.В. Склифосовского с жалобами на боль в левой половине живота, общую слабость, на 2-е сутки с момента получения травмы (удар копытом лошади в живот). При осмотре отмечены болезненность при пальпации грудной клетки слева, в левых отделах живота, развитие подкожной эмфиземы грудной клетки.
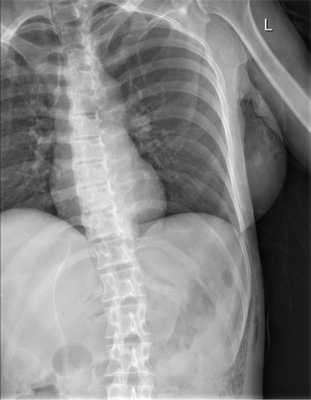
При рентгенологическом исследовании органов грудной клетки и брюшной полости (рис. 1) Рис. 1. Рентгенограмма органов грудной клетки и брюшной полости больной М. при поступлении. выявлена подкожная эмфизема слева от переднего отрезка VI ребра с переходом на брюшную полость. При УЗИ в 5 областях брюшной полости определяется свободная жидкость.
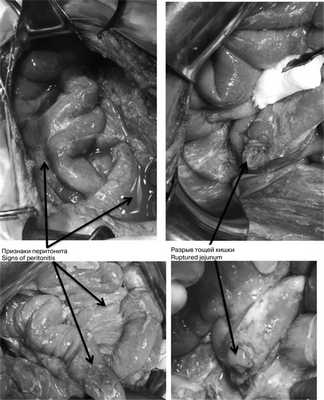
В экстренном порядке выполнена диагностическая видеолапароскопия. При ревизии в брюшной полости около 1000 мл мутного содержимого во всех отделах. Париетальная и висцеральная брюшина тусклая, с наложением фибрина, гиперемирована. При ревизии париетальной брюшины передней брюшной стенки в левом подреберье визуализирован дефект париетальной брюшины и разрыв внутренней косой, поперечной мышц без активного кровотечения размером 4×3 см. Принято решение о конверсии — выполнена широкая срединная лапаротомия. При ревизии тонкой кишки непосредственно за связкой Трейца обнаружен разрыв тощей кишки на 1/3 по противобрыжеечному краю (рис. 2), Рис. 2. Признаки перитонита и разрыва тонкой кишки (интраоперационные фотографии). при осмотре сальниковой сумки выявлено геморрагическое пропитывание парапанкреатической клетчатки. Выполнена назоинтестинальная интубация. Произведена мобилизация участка тощей кишки из-под связки Трейца с иссечением краев разрыва стенки тощей кишки, ушиванием разрыва тощей кишки в поперечном направлении двухрядным швом. Прядь большого сальника фиксирована к линии швов на тощей кишке. Выполнена санация брюшной полости 4 л 0,9% раствора NaCl. Ушит травматический разрыв мышц передней брюшной стенки, двухпросветный дренаж оставлен в ране, выведен через контрапертуру на переднюю брюшную стенку. Двухпросветные дренажи также установлены в подпеченочное пространство справа, в полость малого таза, в левый латеральный канал. С целью дренирования полости сальниковой сумки установлен однопросветный дренаж.
После операции больная переведена в отделение реанимации и интенсивной терапии для хирургических больных, где проводили инфузионную, антибактериальную, антисекреторную терапию, лабораторный и лучевой контроль, делали перевязки, осуществляли динамическое наблюдение.
При УЗИ брюшной полости на 3-и сутки после операции выявлено разобщение листков брюшины поддиафрагмально слева до 0,3 см, у нижнего полюса селезенки до 0,6 см, по ходу правого латерального канала до 0,7 см, в полости малого таза до 0,8 см и межпетельно слева до 0,9 см за счет анэхогенных зон с фибрином. Петли тонкой кишки не расширены, стенка до 0,8—1 см, содержимое гетерогенное и с газом, перистальтика прослеживается. Заключение: эхопризнаки свободной жидкости в брюшной полости, отек стенок тонкой кишки.
При УЗИ брюшной полости на 5-е сутки после операции: неоднородность структуры поджелудочной железы за счет участков пониженной эхогенности в головке и теле, минимальный подкапсульный отек в виде анэхогенной зоны шириной 0,2 см, парапанкреатическая клетчатка несколько пониженной эхогенности.
Послеоперационный период осложнился развитием реактивного панкреатита. На фоне проведенного комплексного лечения состояние больной улучшилось, на 12-е сутки после операции пациентка выписана под наблюдение хирургом по месту жительства.
Больной Л., 24 лет, поступил в 1-е сутки после производственной травмы (падение с 6-го этажа во время строительных работ) в отделение реанимации и интенсивной терапии для экстренных больных. При поступлении состояние тяжелое, на передней поверхности груди и брюшной стенки обширная ссадина; в левой мезогастральной области рана размером 6×0,5 см; поверхностные раны и множественные ссадины на верхних и нижних конечностях. Живот вздут, асимметричен из-за кровоизлияния в брюшную стенку слева, там же определяется пропитывание гематомы брюшной стенки с переходом на поясничную область; при пальпации живот мягкий, болезненный преимущественно в левых отделах.
При УЗИ органов брюшной полости определяется свободная жидкость: в правом подпеченочном пространстве 2 см, в правом латеральном канале 2,8 см, поддиафрагмально справа 0,8—1 см, поддиафрагмально слева 2 см, у нижнего полюса селезенки 2,5 см, в нижней трети левого латерального канала до 1,8 см, в полости малого таза 4,3 см; «шоковые» диффузные изменения почек и селезенки; травма селезенки; эхопризнаки гастростаза, пареза кишечника, посттравматических изменений стенок тонкой кишки в мезогастрии слева, жидкостного пропитывания тканей брыжейки тонкой кишки.
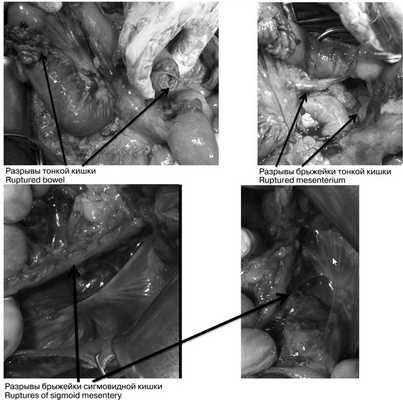
При динамическом наблюдении отмечено нарастание явлений геморрагического шока. С учетом клинико-инструментальной картины заболевания закрытой травмы живота с повреждением внутренних органов и продолжающимся внутрибрюшным кровотечением в экстренном порядке выполнена лапаротомия. Во время доступа в брюшную полость выявлено, что кожа и подкожная клетчатка полностью отсепарированы от подлежащего слоя прямых и косых мышц, имбибированных кровью из-за размозжения (межмышечная гематома) на всем протяжении доступа. Множественные более мелкие гематомы в подкожной клетчатке. В брюшной полости во всех отделах большое количество крови и сгустков (1800 мл), кровь аспирирована с помощью аппарата CellSaver. Продолжающегося активного кровотечения не выявлено. При ревизии органов брюшной полости: в проекции V—VI сегментов правой доли печени по краю выявлена подкапсульная гематома размером около 6×2 см, не пульсирующая, в объеме за время операции не увеличилась. Других повреждений печени по диафрагмальной и висцеральной поверхностям не установлено; на расстоянии 30, 40 и 45 см от связки Трейца 3 разрыва стенки тощей кишки с вскрытием просвета и 1 десерозированный участок. В области разрывов кишки также отмечены участки повреждения брыжейки тонкой кишки (рис. 3), Рис. 3. Разрывы петель тонкой и толстой кишки (интраоперационные фотографии). откуда продолжалось кровотечение. На расстоянии 60 см от связки Трейца выявлен полный поперечный разрыв тощей кишки с разрывом брыжейки кишки до уровня ее корня и активно продолжающимся кровотечением из сосудов брыжейки. Гематома в области брыжейки поперечной ободочной кишки, просвет кишки не вскрыт, гематома в размерах не увеличивается. Помимо этого гематома околокишечной клетчатки вдоль нисходящей ободочной кишки и сигмовидной кишки, брыжейка которой на уровне дистальной трети разорвана; сама сигмовидная кишка в области разрыва брыжейки не изменена, спастически сокращена, просвет не вскрыт, серозная оболочка обычной окраски с небольшими петехиальными кровоизлияниями из-за травмы. Обширная забрюшинная гематома по левому латеральному каналу с распространением на парааортальное клетчаточное пространство и корень брыжейки тонкой кишки. Париетальная брюшина в области левого латерального канала также разорвана, визуализирован левый мочеточник, без повреждений (моча концентрированная, макрогематурии нет). В области боковой стенки живота со стороны париетальной брюшины разрыв стенки размером около 10×5 см с повреждением прямых и косых мышц живота и продолжающимся низкоинтенсивным кровотечением из мышечных сосудов.
Выполнена резекция 30 см тощей кишки, начиная с первого разрыва на 30 см от связки Трейца до полного поперечного разрыва на 60 см с формированием энтероэнтероанастомоза конец в конец. Произведена назоинтестинальная интубация. Далее ушиты поврежденные мышцы передней брюшной стенки и восстановлена непрерывность париетальной брюшины. Брюшная полость промыта 3000 мл 0,9% раствора NaCl, установлены двухпросветные дренажи в полость малого таза, в правое подпеченочное пространство и в левый латеральный канал. Выполнена петлевая трансверзостомия.
После операции пациент переведен в отделение реанимации, где проводили антибактериальную, инфузионно-трансфузионную, антисекреторную, анальгетическую терапию, лабораторный и лучевой контроль, выполняли перевязки, динамическое наблюдение.
При УЗИ органов брюшной полости на 4-е сутки после операции отмечены признаки послеоперационного пареза кишечника, отек стенок тонкой кишки, диффузные изменения поджелудочной железы, гематомы правой доли печени, жидкостное пропитывание тканей брыжейки тонкой кишки, забрюшинная гематома слева.
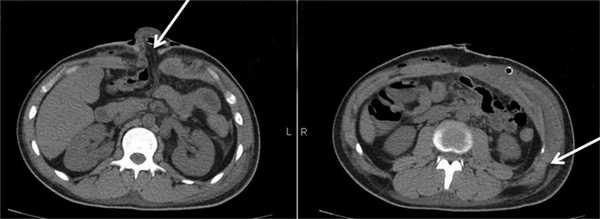
На 6-е сутки после операции выполнена КТ брюшной полости с контрастным усилением (рис. 4): Рис. 4. Компьютерные томограммы органов брюшной полости больного Б. на 6-е сутки после операции. признаки межмышечных и подкожных гематом брюшной стенки с включениями газа, небольшое количество жидкости межпетельно в полости таза, отек подкожной клетчатки поясничной области, контузионные изменения в задних сегментах нижних долей обоих легких (преимущественно правого), перелом крыла левой подвздошной кости.
Пациенту ежедневно выполняли перевязки послеоперационных ран, промывание дренажей из брюшной полости и межмышечного пространства брюшной стенки. Назоэнтеральный и назогастральный зонды установлены на активную аспирацию с введением капельно физиологического раствора в малый канал назоэнтерального зонда. Ежедневно в зонды вводили по 100 мл вазелинового масла. С 3-х суток после операции у пациента начали отходить газы, с 5-х суток появился стул по колостоме. Дренажи из брюшной полости удалены на 4-е и 6-е сутки после операции, назоэнтеральный зонд — на 6-е сутки. По данным УЗИ, КТ и биохимического анализа крови выявлены признаки травматического панкреатита, в связи с этим с 6-х послеоперационных суток пациент получал октреотид по 300 мкг 3 раза в сутки в течение 5 сут.
При УЗИ на 12-е сутки после операции в брюшной полости определяются свободная жидкость неоднородного характера (до 4 см в полости малого таза), отек стенок тонкой кишки, диффузные изменения поджелудочной железы, гематома правой доли печени по типу пропитывания, эхопризнаки спленомегалии.
При УЗИ мягких тканей передней брюшной стенки в области послеоперационной раны слева в гипогастрии на глубине 1 см жидкостное скопление с взвесью и инфильтрацией тканей до 1 см вокруг.
На фоне комплексного лечения состояние пациента стабилизировалось. На фоне антибактериальной терапии у пациента развились явления антибиотикоассоциированного колита (многократный неоформленный стул до 6 раз в сутки), которые регрессировали после отмены антибиотиков. В удовлетворительном состоянии пациент выписан под наблюдение хирургом по месту жительства.
Больной К., 46 лет, поступил с жалобами на боль в левой половине грудной клетки, во всех отделах живота в 1-е сутки после травмы (со слов, был избит неизвестным, тошноты, рвоты не было, сознание не терял). При поступлении состояние больного средней степени тяжести; дыхание при аускультации в легких с жестким оттенком, ослаблено в нижних отделах слева, хрипов нет. Живот не вздут, при пальпации напряжен, болезненный во всех отделах; перитонеальные симптомы положительные.
Status localis: разлитая боль при пальпации грудной клетки слева по задней подмышечной и лопаточной линии с VI по IX ребро. Подкожной эмфиземы грудной клетки нет.
При УЗИ брюшной полости при поступлении выявлено разобщение листков брюшины под печенью до 0,9 см, в полости малого таза — до 0,9 см. Заключение: эхопризнаки свободной жидкости в брюшной полости.
При рентгенографии органов брюшной полости при поступлении: газ и плотное содержимое по ходу толстой кишки на всем протяжении; в мезогастрии единичные пневматизированные петли тонкой кишки, диаметром 3,3 см с нечеткими уровнями жидкости. Заключение: функциональный фон.
В экстренном порядке выполнена диагностическая лапароскопия: в брюшной полости мутный геморрагический выпот до 300 мл во всех отделах живота, на висцеральной брюшине мезогастральной области налет фибрина. На расстоянии 80 см от илеоцекального угла сквозной дефект тонкой кишки с вывернутыми краями размером 3×2 см. Принято решение о конверсии — выполнена широкая срединная лапаротомия. В брюшной полости 450 мл геморрагического содержимого с примесью кишечного отделяемого. В 80 см от илеоцекального угла определяются 3 линейных разрыва подвздошной кишки диаметром до 1,5 см (рис. 5). Рис. 5. Множественные разрывы стенки тонкой кишки (интраоперационные фотографии). Брыжейка тонкой кишки с множественными поверхностными разрывами, кровоподтеками, гематомой (рис. 6). Рис. 6. Разрыв брыжейки тонкой кишки (интраоперационная фотография). В верхней трети сигмовидной кишки дефект серозно-мышечного слоя размером 2×1 см. При дальнейшей ревизии повреждений желчного пузыря, желудка, начального отдела двенадцатиперстной кишки не выявлено. Выполнена резекция около 15 см участка подвздошной кишки с тремя разрывами. Сформирован энтероэнтероанастомоз конец в конец. Произведена назоинтестинальная интубация. Выполнено ушивание дефекта стенки сигмовидной кишки. Произведено дренирование брюшной полости в полость малого таза, правое подпеченочное пространство и в левый латеральный канал.
После операции пациенту проводили антибактериальную, инфузионно-спазмолитическую, антисекреторную терапию, лабораторный контроль, динамическое наблюдение.
На 3—4-е сутки после операции удалены дренажи из брюшной полости.
На 4-е сутки после операции выполнено радиоизотопное исследование всасывающей способности кишки — нарушений не выявлено.
Для оценки состоятельности энтероэнтероанастомоза и пассажа по тонкой кишке на 6-е сутки после операции дано 100 мл водорастворимого контрастного вещества через назоинтестинальный зонд: петли тонкой кишки диаметром до 3 см; энтероэнтероанастомоз диаметром до 0,6 см. Затекания контрастного вещества за его контуры не выявлено. Через 2 ч контраст распределился по толстой кишке на всем протяжении.
Послеоперационный период гладкий. Швы с послеоперационной раны сняты на 12-е сутки. В удовлетворительном состоянии пациент выписан под наблюдение хирургом по месту жительства.
Таким образом, у 1 (37,9%) больной с закрытой травмой живота имеются повреждения кишечника, что является причиной развития перитонита. Основной задачей диагностического поиска является установка объема и тяжести повреждений, требующих неотложного хирургического вмешательства. Прогностически важно динамическое наблюдение за пациентом в 1-е сутки после получения травмы. В настоящее время приоритет в диагностике закрытой травмы живота мы отдаем динамическому ультразвуковому исследованию и диагностической видеолапароскопии.
Компьютерная томография в диагностике заболеваний тонкой кишки

Введение. Актуальность работы обусловлена трудностями диагностики заболеваний тонкой кишки. Ввиду распространенности и широкого внедрения в клиническую практику рентгеновской компьютерной томографии ее возможности в диагностике заболеваний тонкой кишки представляют большой интерес и потенциал.
Цель — раскрытие возможностей компьютерной томографии с применением внутривенного болюсного контрастного усиления в выявлении симптома «утолщения стенки» тонкой кишки и ее прогностической значимости при различных нозологиях.
Методы. Анализ данных исследований мультиспиральной компьютерной томографии, выполненных по протоколу исследования органов брюшной полости с применением внутривенного болюсного контрастного усиления и перорального приема воды взрослым пациентам от 18 до 87 лет с заболеваниями тонкой кишки.
Результаты. В работе показаны возможности мультиспиральной компьютерной томографии, выполняемой по стандартному протоколу, в выявлении утолщения стенки тонкой кишки. Определен круг заболеваний, для которых утолщение стенки тонкой кишки являлось одним из основных рентгенологических симптомов поражения. Представлена прогностическая значимость этого рентгенологического симптома. Описаны особенности утолщения стенки кишки при различных заболеваниях и другие отличительные признаки, которые можно использовать в дифференциальной диагностике.
Заключение. Утолщение стенки — распространенный признак поражения тонкой кишки, который убедительно обнаруживается при КТ-исследовании с болюсным контрастным усилением. В нашей выборке частыми причинами утолщения стенки тонкой кишки при первичном заболевании являлись болезнь Крона (37%), лимфома (20%), анастомозит (13%). Однако утолщение стенки тонкой кишки в 7% определено нами как следствие первичных опухолей (аденокарцинома, саркома) и в 18,6% — как следствие вторичного опухолевого поражения. Рассмотренные заболевания были различны по степени утолщения стенки кишки (от 6 до 70 мм), ее протяженности (фокальное утолщение 48%; сегментарное 52%), количеству пораженных участков (от 1 до 3), их локализации (проксимальный — средний или дистальный участок), форме перехода пораженной части кишки в неизмененную (резко очерченный или плавный), наличию или отсутствию симптомов кишечной непроходимости и особенностям контрастного усиления (степень выраженности и тип).
Ключевые слова
Полный текст
АКТУАЛЬНОСТЬ
На протяжении многих десятилетий в диагностике патологии тонкого кишечника (ТК) использовался рентгенологический метод, который включал заполнение кишечника per os, зондовую энтерографию со взвесью бария или двойным контрастированием. Заполнение кишечника per os легко переносится больными, но получаемая при этом информация — минимальна. Зондовая энтерография (энтероклизис), предложенная в 1986 г. как альтернатива оперативной энтероскопии, используемой с 50-х годов, позволяет провести более детальную оценку ТК, но вызывает дискомфорт для пациента, поэтому требует использования обезболивания [1, 2]. С появлением энтероскопов стала возможной эндоскопическая диагностика: метод активной энтероскопии (push-энтероскопия) позволяет осмотреть проксимальные отделы тощей кишки, но не более чем 100 см за связкой Трейтца. Обследование являлось технически сложным по исполнению, длительным и дискомфортным для пациента, предполагающим седацию и внутривенную анестезию [3, 4].
Внедрение в клиническую практику в 2001 г. видеокапсульной энтероскопии открыло новый этап в диагностике заболеваний ТК. Этот неинвазивный метод позволяет оценивать внутренний просвет ТК на всем протяжении, выявлять внутрипросветные образования, стриктуры. С внедрением видеокапсульной энтероскопии появилась возможность визуализации дистального отдела ТК, что привело к увеличению выявленных случаев ее патологии [5, 6]. Диагностическая ценность видеокапсульной энтероскопии варьирует от 63 до 90%. Однако метод также имеет свои ограничения: невозможность взятия биоптата, ошибки в определении локализации патологического процесса ввиду анатомической вариабельности протяженности ТК, задержка видекапсулы в области стриктуры с необходимостью неотложного оперативного вмешательства.
Безусловным прорывом в диагностике патологии ТК стали разработка и внедрение в практику инструментально-ассоциированных видов видеоэнтероскопии — двух- и однобаллонной энтероскопии. Двухбаллонная энтероскопия разработана доктором H. Yamamoto в 2001 г. и соавт. [7]. Дальнейшее усовершенствование и упрощение техники исполнения привело к внедрению в 2007 г. однобаллонной энтероскопии, не уступающей по диагностической эффективности двухбаллонной [8, 9]. Фиксация кишки повышает маневренность эндоскопа с возможностью неоднократного визуального прохождения по одному и тому же участку, с выполнением биопсии, постановки локализационной «метки» и даже резекции небольших внутрипросветных образований. Диагностическая точность метода двухбаллонной энтероскопии достигает 80-96%, а осложнения, по данным литературы, — весьма редки и ограничиваются в основном болью в брюшной полости [10].
Как более простой и относительно быстрый альтернативный метод сравнительно недавно была разработана спиральная энтероскопия, чаще применяемая специалистами Европы и США, с использованием спиральной шинирующей трубки [11]. Концепция «вращение для продвижения» в спиральной энтероскопии, реализованная в устройстве, облегчающем продвижение энтероскопа, предложена в 2006 г. Полем Акерманом [12]. Спиральная энтероскопия использует превращение ротационной силы в линейную, «присобирая» тонкую кишку на энтероскопе. Однако для выполнения процедуры обязательно нужен ассистент, вращающий тубус. Метод, как и двух-/однобаллонная энтероскопия, требует глубокой седации или наркоза. Осложнения в виде перфорации стенки ТК при данном виде исследования составляют 0,3%.
С развитием компьютерных томографов (КТ) и появления мультисрезовых/мультидетекторных аппаратов с получением субмиллиметровых срезов в практическую работу внедрены специализированные методики исследования, такие как КТ-энтероклизис и КТ-энтерография. При КТ-энтероклизисе рентгенонегативное или рентгенопозитивное контрастное вещество вводится, как правило, через назоинтестинальный зонд в двенадцатиперстную кишку или проксимальные отделы тощей кишки, примерно на 30 см дистальнее связки Трейтца, с балонной фиксацией наконечника. КТ-энтерография не требует дополнительных устройств. Рентгенонегативный или рентгенопозитивный контрастный препарат принимается перорально. Чувствительность метода КТ-энтерографии достигает 90%, специфичность при болезни Крона и опухолевых поражениях — до 95-98% [13, 14]. В сравнении с капсульной эндоскопией и инструментально-ассоциированными видеоэнтероскопиями методика КТ-энтерографии немногим уступает в оценке слизистой оболочки ТК, существенно превосходя их при оценке трансмуральных поражений стенки, при патологических изменениях, выходящих за ее пределы, а также в диагностике кровотечений и опухолей [15]. Методика не является инвазивной, не требует седации или наркоза пациента. Затрудняющими моментами являются зависимость от подготовки пациента к исследованию, спазм кишки и возможное наличие аллергии на йодсодержащий контрастный препарат. Тем не менее КТ-методики исследования ТК дают великолепный результат, поскольку обеспечивают визуализацию толщины стенки кишки, позволяют обнаружить внутри-/внепросветные и интамуральные образования, оценить состояние прилежащей жировой клетчатки и брыжейки, сосудов и лимфатических узлов [16].
Публикации по магнитно-резонансной (МР) энтерографии и МР-энтероклизисе не так многочисленны. Для контрастирования кишечника применяют жидкости. МРТ ТК предусматривает заполнение кишки водой через введенный за связку Трейтца интестинальный зонд или per os. Используются методики «светлого просвета» (bright lumen), основанной на получении Т2-ВИ в быстрой импульсной последовательности, и «темного просвета» (dark lumen), основанной на получении Т1-ВИ с одновременным внутривенным введением контрастного вещества и динамическим контрастированием 18. Ограничения МРТ в изучении ТК, помимо противопоказаний данного метода, опосредованы долгой «экспозицией» при получении среза и зависимости от перистальтики. Применяемый для подавления перистальтики препарат Глюкагон противопоказан при сахарном диабете, гипергликемии, образованиях поджелудочной железы и надпочечников.
Таким образом, диагностика и лечение заболеваний ТК были и остаются актуальными проблемами. Благодаря внедрению новых методов и методик в практику врача диагностика патологии ТК подверглась эволюционному развитию. Старые методы, такие как оперативная энтероскопия, зондовая энтерография, остались в прошлом. На смену им пришли новые виды инструментально-ассоциированной энтероскопии: двух-/однобаллонная энтероскопия, которые обладают рядом существенных недостатков, к которым следует отнести длительность процедуры в первом случае и ограничение осмотра проксимальными отделами тощей кишки — во втором. Недостатками большинства перечисленных методов также являются трудоемкость, нередко необходимость привлечения к исследованию врачей других специальностей (эндоскописта, ассистента эндоскописта, анестезиолога), необходимость седации или наркоза. Вероятно, по этим причинам перечисленные методики не получили широкого применения в диагностике патологии ТК и ограниченно используются только для решения конкретных диагностических и клинических задач. Активно изучаются и освещаются возможности узкоспециализированных МР- и КТ-энтерографии/энтероклизиса. Новая техника и специализированные методики открывают еще бóльшие диагностические и терапевтические возможности в данной области.
Несмотря на широкое внедрение в России МРТ и КТ-исследований, по нашему мнению, недостаточно освещены роль и возможности в диагностике патологии тонкого кишечника КТ брюшной полости и забрюшинного пространства, выполняемой с болюсным контрастным усилением по стандартному протоколу.
Цель настоящего исследования — раскрытие возможностей мультидетекторной или мультисрезовой компьютерной томографии (МСКТ), выполняемой по стандартному протоколу с применением внутривенного болюсного контрастного усиления, в выявлении одного из ведущих и распространенных, по нашему мнению, симптомов — утолщения стенки ТК. Выполнена оценка прогностического значения этого рентгенологического симптома при различных нозологиях.
МЕТОДЫ
КТ исследования проводились на мультисрезовых компьютерных томографах по стандартным программам исследования брюшной полости и забрюшинного пространства.
В группу исследования вошли взрослые пациенты с известной патологией тонкой кишки и утолщением ее стенки более 4 мм, выявленным при МСКТ брюшной полости и забрюшинного пространства с болюсным контрастным усилением. Пациенты с отсутствием утолщения стенки ТК по данным МСКТ брюшной полости и забрюшинного пространства с болюсным контрастным усилением в исследовательскую группу не включались.
Условия проведения
Для реализации поставленной цели проведен анализ результатов МСКТ брюшной полости и забрюшинного пространства с болюсным контрастным усилением больных, поступивших в хирургические и гастроэнтерологические отделения ФГБУ «НМХЦ им. Н.И. Пирогова» МЗРФ и ГКБ № 1 им. Н.И. Пирогова ДЗ г. Москвы. Возраст больных составлял от 18 до 87 лет, в среднем 55 лет.
Описание медицинского вмешательства
МСКТ выполнялось по протоколу исследования органов брюшной полости с применением внутривенного болюсного контрастного усиления и перорального приема воды в объеме 500 мл непосредственно перед исследованием. Томография проводилась субмиллиметровой толщиной среза, питчем 1, с внутривенным болюсным контрастным усилением неионным рентгеноконтрастным препаратом. Объем контрастного препарата зависел от веса пациента — 1,5 мл/кг. Скорость введения контрастного препарата — 4 мл/сек.
Измерение толщины стенки ТК проводили в плоскости, перпендикулярной оси просвета. Стенку ТК считали утолщенной при толщине >4 мм. Из всего количества исследований было отобрано 86 случаев с утолщением стенки ТК.
Дизайн исследования
Из просмотренных нами историй болезни и снимков КТ были включены 86 наблюдений пациентов с заболеваниями тонкой кишки. Предварительно наблюдения были разделены на изменения, связанные с ограниченным по протяженности утолщением стенки ТК и с сегментарным утолщением. Оценивалась степень контрастного усиления утолщенной стенки ТК, и его тип, просвет ТК, изменения примыкающих тканей и структур. КТ-картину и заключения по наблюдениям сопоставляли с окончательными верифицированными диагнозами (клинико-инструментального; морфологического или интраоперационного).
РЕЗУЛЬТАТЫ
Характеристика пациентов
Все больные были разделены нами на 2 группы: в первой группе стенка ТК у пациентов имела фокальное утолщение протяженностью
Дополнительно определяли солитарность или множественность утолщения, степень, характер контрастного усиления, изменения примыкающих органов и структур. Случаи множественных локализаций фокальных утолщений относили в группу сегментарных изменений ТК (2-я группа).
Основные результаты исследования
Проанализировано 86 случаев утолщения стенки ТК. Распределение по типу утолщения, частоте и прогностическому показателю симптома «утолщение стенки кишки» по нозологиям представлено в табл. 1.
Сравнительная характеристика пациентов групп исследования
Читайте также:
