Лучевые признаки поражения легких при дерматомиозите (полимиозите)
Добавил пользователь Владимир З. Обновлено: 28.01.2026
Клинические варианты поражения легких при поли- и дерматомиозите
Аннотация
Идиопатические воспалительные миопатии представляют собой группу редких гетерогенных заболеваний соединительной ткани, характеризующихся воспалением скелетных мышц. Четыре основные формы идиопатических воспалительных миопатий - это дерматомиозит, полимиозит, миозит с включенными тельцами и некротизирующая иммуноопосредованная миопатия. Каждая форма миозита, кроме миозита с включенными тельцами, может быть связана с поражением многих органов, включая легкие, сердце, суставы и кожу. Наиболее часто наблюдается поражение легочной ткани с развитием интерстициальной болезни легких, возникающей на фоне миозита или без него. Тяжесть течения варьирует от легкой до тяжелой, с быстрым развитием дыхательной недостаточности. Интерстициальные болезни легких могут стать причиной смерти у пациентов с миозитом, поэтому необходимо проводить оценку поражения легочной ткани на ранних стадиях развития заболевания.
Ключевые слова: полимиозит, дерматомиозит, интерстициальные болезни легких.
Для цитирования: Бондаренко И.В., Пономарева Л.А., Попова Е.Н. Клинические варианты поражения легких при поли- и дерматомиозите. Клинический разбор в общей медицине. 2021; 4: 34-39. DOI: 10.47407/kr2021.2.4.00058
Clinical types of lung disease in polymyositis and dermatomyositis
Abstract
The idiopathic inflammatory myopathies are a group of rare, heterogeneous connective tissue disorders characterized by skeletal muscle inflammation. The four main forms of idiopathic inflammatory myopathies are dermatomyositis, polymyositis, inclusion body myositis, and necrotizing immune-mediated myopathy. Each form of myositis, other than inclusion body myositis, can be associated with damage to many organs, including the lungs, heart, joints, and skin. The most often observed damage to the lung tissue with the development of interstitial lung disease, which occurs with or without myositis. The severity of the course varies from mild to severe, with rapid development of respiratory failure. Interstitial lung disease can be fatal in patients with myositis, therefore, it is necessary to assess the damage to the lung tissue in the early stages of the disease.
Key words: dermatomyositis, polymyositis, interstitial lung disease.
For citation: Bondarenko I.B., Ponomareva L.A., Popova E.N. Clinical types of lung disease in polymyositis and dermatomyositis. Clinical review for general practice. 2021; 4: 34-39. DOI: 10.47407/kr2021.2.4.00058
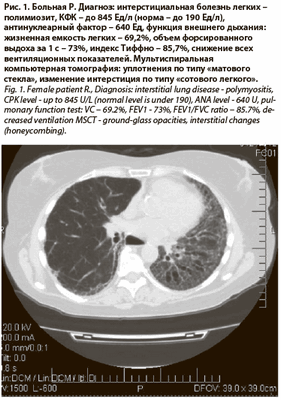
Полимиозит (ПМ) и дерматомиозит (ДМ) относятся к системным заболеваниям, связанным с поражением кожи и скелетных мышц в виде воспалительной, преимущественно лимфоцитарной, инфильтрации [1]. Повреждение мышц приводит к потере нормальной структурно-функциональной организации мышечных волокон, при присоединении к миопатии кожных поражений заболевание приобретает признаки ДМ.
Заболевание нередко не диагностируется вследствие многообразия клинических проявлений и частоты субклинических вариантов течения [2]. Чаще заболевают женщины в среднем и пожилом возрасте. Известны семейные случаи болезни [1].
Патогенез ПМ/ДМ связывают с появлением антисинтетазных антител. Антисинтетазный синдром - это аутоиммунное заболевание, характеризующееся аутоантителами против одной из многих синтетаз РНК-трансмиссии аминоацила (тРНК) с клиническими признаками, которые могут включать интерстициальное заболевание легких (ИБЛ), неэрозивный артрит, миозит, феномен Рейно, необъяснимую лихорадку и/или «руки механика». У пациентов с ПМ/ДМ были описаны различные миозит-специфические и ассоциированные аутоантитела, которые часто тестируются при оценке идиопатических ИБЛ [3]. Отличительной чертой антисинтетазного синдрома является наличие антисинтетазных антител, специфичных для миозита. Из антител против синтетазы чаще всего идентифицируют анти-Jo-1, анти-гистидил-тРНК-синтетазу. Менее распространенные антисинтетазные антитела включают анти-треонил (анти-PL7), анти-аланил (анти-PL12), анти-изолейцил (анти-OJ) и анти-гилцил (анти-EJ), а также другие, которые нечасто тестируют в клинических условиях, но о них сообщается в литературе [4].
Поражение легких при антисинтетазном синдроме представлено прежде всего интерстициальным воспалением в виде МСКТ-паттерна «матового стекла» и тракционных бронхоэктазов (рис. 1) [5].
В типичных случаях болезни появляется слабость в мышцах тазового и плечевого пояса. Жалобы, возникающие у больных, прежде всего обусловлены трудностями при подъеме по лестнице, причесывании, одевании, больным трудно выбраться из ванны, присесть и встать с согнутых колен, подняться со стула. У части пациентов возникает слабость передних мышц шеи, дисфункция орофарингеальных мышц, что приводит к аспирации, дисфагии и дистонии [6], возможно нарушение моторики пищевода. Кроме того, иногда наблюдаются нарушения ритма сердца, свидетельствующие о поражении миокарда [7].
При тяжелой форме болезни быстро развивается массивная деструкция мышц, миоглобинопатия, миоглобинурия, тяжелые нарушения функции почек. Гибель возможна в течение нескольких недель [8].
При легких вариантах заболевания клинические проявления выражены настолько слабо, что не воспринимаются как болезнь и расцениваются как последствия недостаточной физической активности. С другой стороны, при амиопатической форме ПМ/ДМ может быть и тяжелое течение за счет висцеральных поражений.
Из лабораторных проявлений следует отметить повышение СОЭ, достигающее у 1/2 больных значений более 60-70 мм/ч. Повышение сывороточной креатининфосфокиназы (КФК) относится к ключевым признакам заболевания и вместе с увеличением СОЭ коррелирует с активностью болезни. Определение других ферментов - альдолазы, лактатдегидрогеназы, трансаминазы - используется для динамического наблюдения за больными. Уровень КФК порою превышает нормальные показатели в 80-100 раз. Низкие показатели КФК встречаются при вялотекущих вариантах болезни, но существует мнение, что отсутствие энзимопатии при выраженных клинических проявлениях сопряжено с неблагоприятным прогнозом [9]. Электромиография позволяет дифференцировать ПМ от слабости, обусловленной поражением периферических мотонейронов, или мышечной дистрофии. Важную информацию позволяет получить биопсия мышц.
Поражения легких при ПМ/ДМ
Одними из первых тяжелую мышечную слабость у больного с небактериальной пневмонией описали E.S. Mills и W.H. Mathews в 1956 г. В клинических исследованиях, проведенных в конце прошлого века с привлечением больших групп больных ПМ/ДМ и использованием рутинных рентгенологических методов, изменения в легких обнаруживались у 10-15% больных [10]. По более поздним данным, функциональные нарушения и КТВР-признаки воспаления и фиброза в интерстиции легких выявлялись более чем у половины больных ПМ/ДМ [11].
Пусковой этиологический фактор ПМ/ДМ остается неизвестным. Определенным аргументом в пользу инфекции служит частое обнаружение антител к токсоплазме при ПМ [12]. ПМ/ДМ-подобные реакции встречаются у больных с вирусным гепатитом. При вирусном гепатите С внепеченочные проявления с миопатией, кожными поражениями, фиброзирующим альвеолитом (ФА) развиваются на почве васкулита, обусловленного криоглобулинами [13].
Вирус гепатита С стимулирует моно- или олигоклональную пролиферацию В-лимфоцитов и различные лимфопролиферативные состояния, обозначаемые как «монотипические лимфопролиферативные нарушения неуточненного значения» (lymphoproliferative disorders of undetermined significance - MLDUS), в рамках которых происходит образование иммунных комплексов, содержащих криоглобулины, ревматоидный фактор и органоспецифические и неспецифические антитела. Проявления, укладывающиеся в картину ПМ/ДМ, диагностируются у больных, инфицированных вирусами группы герпеса, аденовирусами, вирусом иммунодефицита человека [14]. Замечено, что миопатический синдром и легочный фиброз могут наблюдаться после операций трансплантации органов [15]. Иммунокомплексное поражение при ПМ/ДМ нередко затрагивает сосудистое русло [16]. Особенно часто признаки ассоциированного с ПМ/ДМ васкулита обнаруживаются у детей [17].
Появление мышечной слабости в сочетании с системными проявлениями может быть и осложнением лекарственной терапии иммуносупрессивными препаратами. Эти расстройства, приводящие к тяжелым нарушениям легочных функций с трудно купируемой дыхательной недостаточностью, порою и определяют прогноз болезни [18].
Клиническая картина
Подтверждение диагноза становится возможным только в результате сопоставления клинических и инструментальных данных, цитоморфологические изменения в легких при ИБЛ-ПМ/ДМ во многом неспецифичны. Морфологические признаки организующейся интерстициальной пневмонии (ОрИП) выявляются достаточно часто, идиопатическая, или криптогенная, форма острой интерстициальной пневмонии относится к редким состояниям. С другой стороны, ОрИП может развиваться при вирусных и бактериальных инфекциях. S. Prahalad в 2005 г. описал ребенка с ювенильной формой ДМ с длительно неразрешавшейся пневмонической инфильтрацией в легких. При морфологическом исследовании изменения в легких имели признаки ОрИП с элементами фибринозного воспаления.
ОрИП встречается как внепеченочное проявление хронических заболеваний печени [21], обнаруживается также при хронических воспалительных заболеваниях кишечника (язвенном колите, болезни Крона), миелопролиферативных заболеваниях, опухолях, болезни Шегрена, системных гранулематозах [22]. Много диагностических затруднений возникает при лекарственно-обусловленной ОрИП (вызванной приемом блеомицина, противовирусных препаратов, антибиотиков и т.д.), поскольку в этих случаях заболевание может имитировать опухолевое поражение легких, среднедолевой синдром [23]. Вместе с тем при ПМ/ДМ рентгенологические изменения в легких часто ошибочно трактуются как банальная пневмония, что влечет за собой избыточное назначение антибиотиков. Повышенный риск бактериальных осложнений вследствие аспирации при ПМ/ДМ как аргумент в пользу длительной терапии антибиотиками представляется несомненным, но показания для антибактериальной терапии, в особенности ex juvantbus, должны быть тщательно продуманы.
При ПМ/ДМ морфологические изменения типа ОрИП обнаруживаются у 30% больных и сочетаются с васкулитами и признаками выраженного ангиогенеза, склеротическими изменениями в стенках сосудов. Ремоделирование сосудистого русла легких во многом идентично наблюдаемому при других системных заболеваниях соединительной ткани, сопровождающихся легочной гипертензией, структурно-функциональные признаки которой представлены повреждением эндотелия легочных сосудов, усилением экспрессии адгезивных молекул, в культуре легочных фибробластов, полученных от таких больных, отмечается повышенная продукция факторов роста [24].
В жидкости бронхоальвеолярного лаважа (БАЛ) у больных ПМ/ДМ даже в отсутствие рентгенологических изменений в легких наблюдается некоторое увеличение уровня лимфоцитов. Для морфологически активного ИБЛ-ПМ/ДМ типичен нейтрофильно-лимфоцитарный состав БАЛ [25]. При типировании лимфоцитов выявляется гетерогенность лимфоцитарной популяции с преобладанием СД8+-фенотипов (I. Yamadori и соавт., 2001).
Прогноз больных ИБЛ-ПМ/ДМ
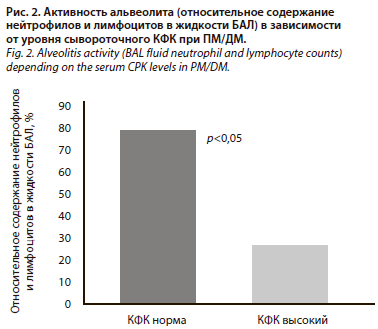
Присоединение ИБЛ, несомненно, усугубляет прогноз больных с ПМ/ДМ. Продолжительность заболевания составляет в среднем 6 лет [21]. По данным госпиталя Mayo, 5-летняя выживаемость достигает 60% [26]. У больных с высокой активностью иммуновоспалительных реакций в легких, лабораторными признаками миопатии (повышение активности КФК, миоглобинурия) ответ на терапию и прогноз более благоприятные. Показано, что в наибольшей степени признаки морфологической активности воспаления в интерстиции легких (альвеолита) представлены у больных с низкой активностью КФК; рис. 2 (И.Б. Бондаренко, 2007).
Среди новых прогностически значимых факторов следует отметить и сывороточный уровень цитокератинов 19, отражающий степень деструктивных изменений в эпителии бронхов.
По прогностической значимости при ИБЛ-ПМ/ДМ с интерстициальными поражениями легких конкурируют инфекционные осложнения [21]. Уточнить риск аспирации можно при помощи эндоскопических методов исследования или путем рентгеноконтрастных исследований пищевода. Следует отметить, что при ПМ/ДМ так же, как и при CREST-синдроме, наблюдаются рентгенологические признаки ахалазии пищевода и регургитация бариевой взвеси.
К терапии ИБЛ-ПМ/ДМ необходим комплексный подход с назначением препаратов, восстанавливающих дренажную функцию бронхов, разжижающих мокроту, а также физиотерапевтических процедур, направленных на восстановление подвижности грудной клетки [27].
Наибольший опыт в лечении ПМ/ДМ касается кортикостероидов. Убедительного подтверждения эффективности цитостатиков нет. Показанием к их назначению является тяжелое прогрессирующее течение болезни. Появление признаков пневмопатии при ПМ/ДМ также служит показанием к назначению цитостатиков. Развернутая картина легочного фиброза с формированием «сотового легкого» при ПМ/ДМ наблюдается редко.
В последние годы убедительный эффект получен от ингибиторов T-лимфоцитов [28]. Недавно небольшое рандомизированное открытое исследование показало возможное влияние внутривенных инфузий ингибиторов T-лимфоцитов на мышечную слабость у резистентных к лечению пациентов с ПМ или ДМ [29].
Хотя фактор некроза опухоли (ФНО) α может играть роль в патогенезе ПМ/ДМ, лечение пациентов анти-ФНО-α дало противоречивые результаты. Даже если некоторые авторы сообщили о возможной роли данных препаратов при ДМ [30], то другие исследования не подтвердили это наблюдение, и у некоторых пациентов состояние ухудшилось. Более того, некоторые авторы сообщили, что терапия анти-ФНО-α может вызывать миозит у пациентов с ревматоидным артритом, псориатическим артритом и псориазом. Таким образом, блокаторы ФНО-α обычно не рекомендуются взрослым пациентам с ПM, и их следует использовать только тогда, когда другие методы лечения неэффективны [31].
Отдельную проблему составляют формы ПМ/ДМ, развивающиеся при злокачественных опухолях. Как ДМ, так и ПМ связаны с повышенным риском злокачественных новообразований, но ДМ больше связан с любым типом рака, чем полимиозит. Несмотря на противоопухолевую терапию, выживаемость пациентов с онкоассоциированными злокачественными образованиями была очень низкой. Выживаемость в группе первичных ПМ и ДМ через 5 лет была значительно выше (100% и 100%) по сравнению с группой пациентов с онкоассоциированным миозитом, где выживаемость составила 15,4% для ПМ и 27,5% для ДМ. Хотя риск рака у пациентов с ПМ ниже, вероятность длительного выживания меньше. Что касается противомиозитной терапии, иммунодепрессанты у пациентов с онкоассоциированным миозитом применялись реже, чем у пациентов с простым миозитом. Несмотря на широко изученную связь между миозитом и раком, лучшая стратегия диагностики и лечения рака у пациентов с ПM отсутствует [32]
Тяжесть паранеопластического ПМ/ДМ не всегда определяется активностью опухолевого процесса. Опухоли, даже небольшие, могут становиться причиной яркой картины миопатии и кожных изменений. Высокая частота паранеопластических реакций с вовлечением легких и ПМ/ДМ наблюдается при опухолях
молочной железы, желудочно-кишечного тракта (B.B. Forster, 1990; H. Kondo, 2005). K.M. Kee и соавт. (2004 г.) наблюдали HCV-инфицированного больного с поражением кожи, миопатическим синдромом и изменениями в легких, очаговыми образованиями в печени. При обследовании выявлен высокий уровень альфа-фетопротеина, циркулирующих иммунных комплексов. Частота поражения легких ПМ/ДМ при опухолях молочной железы достигает 30% и во многих случаях предшествует развернутой стадии опухолевого процесса. Паранеопластический вариант поражения легких и ПМ/ДМ устойчиво сочетаются друг с другом, так что у больных в первую очередь следует предпринимать диагностические мероприятия, имеющие целью выявление наиболее часто встречающихся опухолей.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Информация об авторах / Information about the authors
Бондаренко Инна Борисовна - канд. мед. наук, ассистент каф. внутренних, профессиональных болезней и ревматологии, ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» (Сеченовский Университет)
Inna B. Bondarenko - Cand. Sci. (Med.), Sechenov First Moscow State Medical University (Sechenov University)
Статья поступила в редакцию / The article received: 24.05.2021
Статья принята к печати / The article approved for publication: 27.05.2021
Лучевые признаки поражения легких при дерматомиозите (полимиозите)
Для цитирования: Особенности дебюта и течения антисинтетазного синдрома как наиболее тяжелого подтипа полимиозита/дерматомиозита. РМЖ. 2009;21:1443.
Идиопатические воспалительные миопатии (ИВМ) - группа аутоиммунных ревматических заболеваний, которые могут встречаться в виде как самостоятельных нозологических форм, так и синдромов при различных аутоиммунных заболеваниях, в первую очередь ревматических. Наиболее частыми формами ИВМ являются полимиозит (ПМ) и дерматомиозит (ДМ) [1,2].
Литература
1. Dalakas, MC, Hohlfeld, R. Polymyositis and dermatomyositis. Lancet 2003, 362, 971.
2. Plotz, PH, Dalakas, M, Leff, RL, et al. Current concepts in the idiopathic inflammatory myopathies: Polymyositis, dermatomyositis and related disorders. Ann Intern Med, 1989; 111-143.
3. Идиопатические воспалительные миопатии. Клинические рекомендации. Ревматология. Гл.ред. чл.-корр. РАМН Е.Л.Насонов. Москва 2005, 192-201.
4. Насонов Е.Л., Штутман В.З., Саложин К.В, Гусева Н.Г., Насонова В.А, Плотц П. Клинико - иммунологическая гетерогенность идиопатических воспалительных миопатий. Клиническая Медицина 1995, 2, 3-8.
5. Антелава О.А., Бондаренко И.Б., Хитров А.Н., Насонов Е.Л. Поражение дыхательной системы при полимиозите/дерматомиозите. Русский медицинский журнал, 2008,16,24,334, 1633-1637.
6. Бондаренко И.Б., Мухин Н.А., Насонов Е.Л. Поражение легких при полимиозите и дерматомиозите. Интерстициальные заболевания легких. Руководство для врачей. Под редакцией Ильковича М.М. Кокосова А.Н., Санкт-Петерург. Нордмедиздат 2005, 274-287.
7. Hashish L, Trieu EP, Sadanandan P, Targoff IN. Identification of autoantibodies to tyrosyl-tRNA synthetase in dermatomyositis with features consistent with antisynthetase syndrome (absract). Arthritis Rheum. 2005, 52, Suppl.9, 312.
8. Santy A., Rochat Th., Schoch 0.D., Hamacher J. Pulmonary fibrosis with predominant CDg lymphocytic alveolitis and anti-Jo-1 antibodies. Eur Respir J - 1997 ; 10 : 2907-12.
9. Targoff J.N., Amett F.С. Clinical manifestation in patients with antibody to PL-12 antigen. Am J Med 1990; 88: 241-51
10. Bohan A., Peter JB. Polymyositis and dermatomyositis (first of two parts). N. EngI. J. Med., 1975, 292, 344-347.
11. Bohan, A, Peter, JB. Polymyositis and dermatomyositis (second of two parts). N Engl J Med 1975, 292, 403.
12. Антелава О.А., Насонов Е.Л. Современные методы оценки активности и повреждения при идиопатических воспалительных миопатиях. Научно-практическая ревматология 2007,1, 59-62.
13. Yoshifuji H, Fujii T, Kobayashi S et al. Anti-aminoacyl-tRNA synthetase antibodies in clinical course prediction of interstitial lung disease complicated with idiopathic inflammatory myopathies. Autoimmunity 2006, 39, 233-41.
14. Fathi М, Vikgren J, Boijsen M, Tylen U, Jorfeldt L. et al Interstitial lung disease in Polymyositis and Dermatomyositis: longitudinal evaluation by pulmonary function and radiology. Arthritis and Rheumatusm (Arthritis Care and Research) 2008, 59, 5, 15, 677-685.
15. Yang CJ, Sheu CC, Ou TT, Hwang JJ, Huang MS. Combined lung fibrosis and ‘mechanic’s hand’: a clinical diagnostic clue to amyopathic antisynthetase syndrome. Respirology. 2008?13,4,611-614.
16. Chen IJ, Jan Wu YJ, et all. Interstitial lung disease in polymyositis and dermatomyositis. Clin Rheumatol. 2009, 27.
17. Fujisawa T., I SUDA Т, NAKAMURA Y., ENOMOTO N, IDE K., TOYOSHIMA M., UCHIYAMA H., et al. Differences in Clinical Features and Prognosis of Interstitial Lung Diseases Between Polymyositis and Dermatomyositis. The Journal of Rheumatology 2005,32,1, 58-64.12
18. Betteridge Z., Gunawardena H., North J., Slinn J., McHugh N. Anti-synthetase syndrome: a new autoantibody to phenylalanyl transfer RNA synthetase (anti-Zo) assotiated with polymyositis and interstitial pneumonia. Rheumatol. 2007, 46, 1005-1008.
19. Targoff IN. Autoantibodies and their significance in myositis. Curr.Rheumatol.Rep. 2008, 10, 4, 333-340.
20. Kalluri M, Sahn SA, Oddis CV, еt all. Clinical Profile of Anti-PL-12 Autoantibody: Cohort Study and Review of the Literature. Chest., 2009, 18.
Полимиозит - симптомы и лечение
Что такое полимиозит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Лазаревой Оксаны Юрьевны, ревматолога со стажем в 19 лет.
Над статьей доктора Лазаревой Оксаны Юрьевны работали литературный редактор Елизавета Цыганок , научный редактор Ирина Семизарова и шеф-редактор Маргарита Тихонова

Определение болезни. Причины заболевания
Полимиозит (Polymyositis) — это аутоиммунная болезнь, при которой воспаляется поперечно-полосатая мускулатура. Причиной обращения к врачу обычно становится нарастающая слабость в мышцах рук, ног, шеи и спины [1] [2] [3] .

Симптомы полимиозита похожи на проявления дерматомиозита, однако дерматомиозит помимо мышц поражает кожу, причём кожные симптомы обычно появляются раньше мышечной слабости [7] .
Распространённость полимиозита
По данным разных авторов, в год выявляют от 2 до 10 новых случаев полимиозита на 1 млн населения. Женщины болеют чаще мужчин примерно в 3 раза. Болезнь может начаться в любом возрасте, но отмечают два возрастных пика заболеваемости: в 5-15 лет и в 45-55 лет [1] [2] .
Причины развития полимиозита
Причины развития болезни до конца не ясны, однако существует две теории: генетическая и инфекционная. Теорию о генетической предрасположенности подтверждают случаи болезни среди кровных родственников, в том числе у близнецов. На влияние инфекций косвенно указывает рост заболеваемости зимой и ранней весной во время сезонных эпидемий.
Полимиозиту также могут предшествовать солнечное облучение и работа с химикатами [1] [2] [3] .
В 3,8 % случаев болезнь связана со злокачественным новообразованием. Для дерматомиозита эта цифра больше - 23,5 % случаев [6] [7] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы полимиозита
Как правило, первые симптомы полимиозита неспецифичны и часто встречаются при других болезнях: повышенная утомляемость, слабость, недомогание, потеря веса, попеременные боли в разных мышцах, повышение температуры. Иногда появляется боль и отёк в суставах, после чего становится тяжелее их сгибать и разгибать [11] .
В течение нескольких недель или месяцев постепенно нарастает слабость в мышцах рук и ног. Пациенту тяжело заходить в транспорт, подниматься по лестнице, вставать со стула, отрывать голову от подушки (человек помогает себе руками). Некоторые больные используют специальные «вожжи», которые они прикрепляют к опоре (например, к батарее) и подтягиваются за них руками, чтобы встать с постели. В некоторых случаях пациент может упасть из-за резкой слабости в ногах, которые будто подкосились.
Когда у пациентов зудит и краснеет кожа (чаще всего в зоне декольте и верхней части спины по типу «шали»), речь идёт о дерматомиозите.
При поражении мышц глотки, гортани и пищевода голос становится гнусавым, пациенту тяжело глотать, при этом человек может поперхнуться едой, а жидкая пища вылиться через нос [3] .
В редких случаях у человека с полиомиозитом меняется цвет пальцев рук (синдром Рейно). Обычно наблюдают три последовательные фазы: побеление — посинение — покраснение. Это связано с резким сужением (спазмом) мелких сосудов на кончиках пальцев, когда пациент замёрз или нервничает [1] [2] .

Редким, но опасным симптомом является поражение лёгких с развитием альвеолита. При этом появляется кашель без мокроты, одышка и чувство нехватки воздуха [9] .
Патогенез полимиозита
Поперечно-полосатая мышечная ткань у животных и человека формирует скелетную (туловищную) и мимическую мускулатуру, язык и стенку пищевода. Она состоит из множества мышечных волокон, способных сокращаться. Скелетная мускулатура помогает нам двигаться, прыгать и бегать. Она участвует в дыхании, жевании, глотании и звукообразовании. Но при поражении мышц привычные для нас действия становятся затруднительными.
Полимиозит — это аутоиммунное заболевание, связанное с нарушением работы иммунной системы. В этом случае иммунная система воспринимает свои собственные ткани как чужеродные и повреждает их с помощью клеточных и гормональных гуморальных (внеклеточных) иммунных реакций. В мышцах скапливается воспалительная жидкость, наполненная макрофагами, Т- и В-лимфоцитами. Образовавшиеся иммунные комплексы с антителами повреждают мелкие сосуды и мышцы, т. е. иммунная система работает сильно, но неправильно, разрушая собственные ткани. Постепенно мышечные волокна истончаются, что приводит к атрофии мышц [1] [2] .

Классификация и стадии развития полимиозита
Воспалительные миопатии — это целая группа болезней, объединённых общим признаком — поражением скелетной мускулатуры. Помимо полимиозита в эту группу входят дерматомиозит, паранеопластический миозит (т. е. миозит на фоне злокачественного новообразования), миозит с включениями и миозит при системных заболеваниях соединительной ткани. Их симптомы похожи, но механизмам развития отличается.
Встречаются также редкие формы воспалительных миопатий: эозинофильный, гранулематозный, узелковый и оссифицирующий миозит, а также миозит глазных мышц и миозит при васкулитах [1] [2] .
![Оссифицирующий миозит [12]](https://probolezny.ru/media/bolezny/polimiozit/ossificiruyushiy-miozit-12_s.jpg)
Особая форма полимиозита — антисинтетазный синдром. Это наиболее тяжёлый вариант миопатии. Антисинтетазный синдром начинается остро и сопровождается:
- лихорадкой;
- припухлостью суставов кистей;
- болью в мышцах;
- синдромом Рейно.
Тяжесть состояния связана с поражением лёгких по типу альвеолита. Пациенты жалуются на одышку, чувство нехватки воздуха и кашель без мокроты [4] [7] . Усугубляет ситуацию нарушение глотания, попёрхивание и невозможность проглотить твёрдую пищу [9] .
Осложнения полимиозита
Нарушение глотания может привести к аспирации пищи, когда еда попадает в дыхательные пути вместо пищевода, и развитию аспирационной пневмонии. Такие больные мало двигаются, у них снижен кашлевой рефлекс, слабо работают межрёберные мышцы и диафрагма. Аспирационный синдром встречается часто — в 30 % случаев. У таких пациентов нарушена нормальная вентиляция лёгких и отмечается склонность к инфекционным осложнениям. Всё это создаёт благоприятные условия для развития пневмонии [1] [2] .

Поражение лёгких может сопровождаться развитием дыхательной недостаточности. Со стороны сердечно-сосудистой системы могут быть нарушения ритма сердца и сердцебиения, а также сердечная недостаточность. Со стороны желудочно-кишечного тракта могут быть запоры или диарея [3] .
Внезапные падения могут закончиться переломами костей, что усугубляет болезнь. Особенно высок риск падений и переломов у пожилых пациентов.
Диагностика полимиозита
Диагностика полимиозита базируется на данных анамнеза, результатах осмотра, лабораторного и инструментального обследования, в том числе исследования биоматериала из скелетной мышцы.
Сбор анамнеза и физикальный осмотр
При беседе врач уточняет у пациента, есть ли боль или слабость в мышцах плечевого и тазового пояса, при каких обстоятельствах слабость усиливается, а что приносит облегчение, какие события предшествовали болезни и как быстро она развивалась, принимает ли пациент лекарства, как долго и в каких дозах. Например, при использовании гормональных препаратов и лекарств, снижающих уровень холестерина, а также Пеницилламина, Хлорохина, Гидроксихлорохина, Колхицина, Гемфиброзила, Эритромицина, Эметина и Зидовудина могут развиться лекарственные миопатии [1] .
Так как щитовидная железа влияет на работу скелетно-мышечной мускулатуры, врачу важно знать, наблюдается ли пациент у эндокринолога, принимает ли препараты заместительной терапии и сдавал ли анализ крови на гормоны щитовидной железы [1] [2] .
При осмотре врач оценивает кожные симптомы, возможные при дерматомиозите, определяет мышечную силу и болезненность при прощупывании мышц. Ранним признаком болезни могут быть покраснение околоногтевых валиков и разрастание кожи вокруг ногтевого ложа [11] .
Чтобы исключить артрит, поражения лёгких, сердца и желудочно-кишечного тракта, врач проверяет суставы и органы.
Важным диагностическим симптомом является нарушение глотания. Если он присутствует, пациенту проводят уточняющие обследования [3] .
Лабораторные обследования
При подозрении на полимиозит назначают:
- Общий анализ крови — проводят, чтобы исключить заболевания крови [8] . Может быть повышенный уровень СОЭ (скорости оседания эритроцитов).
- Общий анализ мочи — обычно остаётся в норме, изредка в моче находят белок (протеинурия). У некоторых пациентов моча становится красной или бурой, после того как в неё попадает миоглобин при массивном распаде мышечной ткани.
- Биохимический анализ крови - обязательное обследование при подозрении на полимиозит. Наиболее важный и чувствительные маркер повреждения скелетной мускулатуры — креатинфосфокиназа (КФК). В разные периоды болезни она повышается у 95 % больных. Нормальный уровень КФК при полимиозите сохраняется в начале болезни и на поздних стадиях, когда уже развилась тяжёлая мышечная атрофия, а также у пациентов, которые прошли курс лечения и находятся в стадии ремиссии [1][2][3] .
- Исследование функции щитовидной железы — чтобы исключить эндокринную миопатию, определяют уровень тиреотропного гормона (ТТГ), трийодтиронина (Т3) и тироксина (Т4) в сыворотке крови.
- Иммунологические исследования — так как полимиозит — это аутоиммунное заболевание, при котором организм выделяет аутоантитела, направленные против собственных клеток организма (антинуклеарные антитела). Повышенный уровень антинуклеарного фактора (АНФ) присутствует у 50-90 % больных [1][2] . Выделяют миозитспецифические и миозитассоциированные антитела. Наибольшее диагностическое значение имеют миозитспецифические антитела: анти-Jo-1, анти-Mi-2, частицы сигнального распознавания SRP. Среди миозитассоциированных антител выявляют анти-RNP, анти-Scl-70, анти-Ku, анти-Ro/SS-A, анти-La/SS-B [4] . При этом активность миозитспецифических ферментов определяют до проведения игольчатой электромиографии, так как иЭМГ травмирует мышцу, что повышает активность ферментов в крови.
Оценку лабораторных показателей проводит только доктор с учётом клинической картины болезни и всего перечня обследований. Например, уровень КФК может быть повышен и у здорового человека после интенсивной физической нагрузки, операции, внутримышечных инъекций или употребления алкоголя. КФК также может повышаться при травмах, ожогах, гипотиреозе, опухолях, инфаркте миокарда, миокардите, судорогах, приёме некоторых лекарств (например, снижающих уровень холестерина, а также Дексаметазона или Амфотерицина В) [1] [2] .
Часто повышение уровня КФК сопровождается повышением активности разных ферментов, например альдолазы, лактатдегидрогеназы (ЛДГ), аспартатаминотрансферазы (АСТ), аланинаминотрансферазы (АЛТ), а также миоглобина [8] .
Инструментальные исследования
- Игольчатую электромиографию (иЭМГ) — помогает уточнить диагноз в сомнительных случаях и полезна для контроля эффективности лечения. Игольчатые электроды возбуждают мышечные волокна, после чего электромиограф регистрирует электрическую активность мышц.

- Капилляроскопию — позволяет оценить микроциркуляцию крови. Под специальным микроскопом врач исследует капилляры ногтевого ложа. При полимиозите число капилляров уменьшается, при этом их размер увеличивается, а форма меняется на «кустовидную» [1][2] .
- Рентгеновскую компьютерную томографию (РКТ) лёгких высокого разрешения — назначают всем больным, чтобы оценить состояние лёгких. С помощью рентгена можно увидеть линейные тени, кистозные просветления, очаги снижения прозрачности лёгочных полей по типу «матового стекла» и утолщение бронхиальных стенок. Наибольшие изменения находят в нижних и субплевральных отделах лёгких [9] .
- Спирометрию — исследование функции внешнего дыхания. При поражении лёгких снижается объём воздуха, который человек может вдохнуть или выдохнуть (в том числе за секунду) [9] .
- МРТ мышц — полезна для ранней диагностики полимиозита. Позволяет увидеть отёк мышечной ткани (признак воспаления мышц) даже у пациентов с нормальной активностью миозитспецифических ферментов. Этот метод более чувствителен, чем УЗИ или КТ. МРТ мышц используют при выборе зоны для диагностической биопсии, с её помощью также контролируют эффективность терапии [10] .
- Ультрасонографию — вспомогательная методика. Это ультразвуковая визуализация мышц, которую используют для дифференциальной диагностики с другими нервно-мышечными заболеваниями, например поражением мышц при токсоплазмозе, трихинеллёзе, цистицеркозе, эхинококкозе и миозите с включениями. УЗИ — довольно доступный, недорогой и безвредный метод, но чувствительность у него намного ниже, чем у МРТ, поэтому ставить диагноз только про результатам УЗИ нельзя.
- Мышечную биопсию — обязательный метод диагностики, так как для полимиозита характерна особенная морфологическая картина: скопление в мышцах мононуклеарных клеток (в основном лимфоцитов), некроз и регенерация мышечных волокон. Мононуклеарные клетки чаще всего находятся в кровеносных сосудах, рыхлой соединительной ткани (эндомизии) и вокруг оболочек (фасций), покрывающих органы и мышцы. Определяются признаки васкулопатии: утолщение эндотелия, скопление тромбоцитов в капиллярах, отёк, разрастание и изменение клеток эндотелия, а также образованием в цитоплазме клетки вакуолей, содержащих воду, гликоген или липиды . На поздних стадиях болезни у пациента обнаруживают атрофию мышечных волокон, разрастание соединительной ткани (фиброз) и замещение миофибрилл на жировую ткань [1][2] . Предпочтительно проводить открытую биопсию, т. е. через разрез кожи. Это позволяет получить большой мышечный образец.
При подозрении на опухоль пациенту назначают анализ на онкомаркеры: СА-125, СА-15.3 для исключения рака яичников и груди, а также на простатспецифический антиген (ПСА) для диагностики рака предстательной железы [6] .
Лечение полимиозита
Для лечения полимиозита применяют высокие дозы стероидных гормонов. Важно начать лечение как можно раньше, желательно в течение первых трёх месяцев от появления симптомов. Пациентам назначают трёхмесячный курс Преднизолона или Метилпреднизолона. Дозу рассчитывают в соответствии с массой тела (1 мг/кг в сутки внутрь). При положительной динамике симптомов через три месяца дозу постепенно снижают до поддерживающей (примерно 5 - 10 мг в сутки).
Если болезнь протекает тяжело и гормональные средства малоэффективны или часто случаются рецидивы, назначают противоопухолевые препараты.
В качестве базисной противовоспалительной терапии применяют:
- — внутрь или подкожно; — внутрь; — внутривенная капельница раз в месяц; — внутрь; — внутрь.
Эти препараты позволяют контролировать симптомы и снизить дозу стероидных гормонов, что очень важно для профилактики глюкокортикоидного остеопороза и стероидной миопатии [1] [2] .
При нарушении глотания и тяжёлом течении болезни врач может назначить иммуноглобулин внутривенно в течение 4-6 месяцев. В комплексном лечении иногда дополнительно используют плазмаферез (фильтрацию плазмы).

Есть единичные случаи успешного применения Ритуксимаба при дерматомиозите, который блокирует распространение (пролиферацию) В-лимфоцитов. При серьёзном поражении лёгких Ритуксимаб вводят внутривенно с помощью капельницы [5] .
Прогноз. Профилактика
Эффективность терапии и прогноз при полимиозите зависят от ряда условий. К факторам неблагоприятного прогноза относятся пожилой возраст, поражение лёгких, позднее начало лечения, недостаточная стартовая доза гормонов и слишком быстрое снижение дозы.
При полимиозите на фоне злокачественного новообразования прогноз зависит от того, когда найдут и начнут лечить опухоль. При раннем выявлении новообразования и полном его удалении прогноз благоприятный.
Чем раньше начинается лечение полимиозита, тем эффективнее результаты.
Профилактика полимиозита
Специфической профилактики полимиозита не существует, однако непосредственно во время лечения пациентам назначают бисфосфонаты, препараты кальция и витамина D, чтобы предотвратить развитие глюкокортикоидного остеопороза, и гастропротекторы для профилактики язвенных осложнений желудочно-кишечного тракта. При лечении также проводят профилактику стероидного диабета.
Помимо этого, пациентам рекомендуют избегать переохлаждения, контакта с инфекционными больными и физические перегрузки [1] [2] .
Важно каждый год проходить профилактические осмотры кожи, слизистых губ и рта, щитовидной железы и лимфатических узлов, чтобы снизить риск развития онкологических заболеваний, а также другие скрининги по назначению врача:
Полимиозит
Полимиозит — системное воспалительное поражение мышечной ткани преимущественно поперечно-полосатой мускулатуры конечностей с развитием болевого синдрома, прогрессирующей слабости и атрофии пораженных мышц. Возможно появление патологических изменений в легких и сердце. Диагностика полимиозита включает консультации ревматолога и смежных специалистов, лабораторные исследования, электромиографию, биопсию мышечной ткани, обследование соматических органов (ЭКГ, УЗИ, рентгенографию). Лечение полимиозита проводят стероидными гормонами и иммунодепрессантами.
МКБ-10
Общие сведения
Полимиозит относится к системным аутоиммунным заболеваниям и входит в группу идеопатических воспалительных миопатий. Случаи возникновения полимиозита наблюдаются у людей любого возраста, однако пик заболеваемости отмечается среди детей от 5 до 15 лет и среди взрослых в возрасте от 40 до 60 лет. Примерно 70% случаев полимиозита приходится на лиц женского пола. Довольно часто возникновение полимиозита наблюдается на фоне другой аутоиммунной патологии и у пациентов со злокачественными новообразованиями.
Причины возникновения полимиозита
На сегодняшний день этиологические факторы полимиозита находятся в стадии изучения. Предполагается провоцирующая роль некоторых вирусов (например, цитомегаловируса, вирусов Коксаки) в запуске аутоиммунного механизма заболевания. Немаловажная роль в этом отводится антигенному сходству отдельных видов вирусов и мышечной ткани. Проведенные в последние годы генетические исследования обнаружили у некоторых пациентов маркеры наследственной предрасположенности к возникновению полимиозита.
Среди триггерных факторов, возможно запускающих развитие полимиозита, выделяют переохлаждение, повышенную инсоляцию, хроническую инфекцию, травмы, лекарственную аллергию (крапивница, медикаментозный дерматит, токсикодермия, синдром Стивенса-Джонсона).
Классификация полимиозита
Согласно одной из классификаций, которыми пользуется клиническая ревматология, выделяют 6 форм полимиозита. Первичный полимиозит — проявляется поражением мышц проксимальных отделов конечностей и шеи, а также глотки, гортани и пищевода. В некоторых случаях сопровождается артралгией. Первичный дерматомиозит — полимиозит, сопровождающийся кожными проявлениями в виде эритематозных пятен на лице и в области суставов. Возможны поражения слизистой глаз (конъюнктивит), ротовой полости (стоматит), и глотки (фарингит).
Полимиозит при злокачественных процессах — чаще всего наблюдается у лиц старше 40 лет. Наиболее часто он развивается на фоне рака легкого, молочной железы, желудка, толстого кишечника, предстательной железы, яичников. Возможно его появление при лимфоме. Детский полимиозит — в большинстве случаев сопровождается кожными проявлениями, появлением внутрикожных и подкожных кальцификатов. Характеризуется прогрессирующим течением с образованием мышечных атрофий и контрактур; поражением сосудов ЖКТ с развитием васкулита и тромбоза, приводящих к появлению острых болей в животе, желудочно-кишечных кровотечений, иногда — изъязвлений и перфораций стенки кишечника.
Полимиозит при других аутоиммунных болезнях — может возникать при системной красной волчанке, болезни Шегрена, ревматоидном артрите, склеродермии. Миозит с включениями — является редко встречающейся формой полимиозита и отличается поражением мышц дистальных отделов конечностей. Свое название эта форма полимиозита получила благодаря тому, что при исследовании биоптата пораженных мышц в мышечных волокнах наблюдаются включения.
Для полимиозита наиболее типично подострое начало с постепенно развивающимся поражением мышц тазового и плечевого пояса. Зачастую к мышечному синдрому присоединяются различного рода поражения соматических органов: ЖКТ, сердца, легких. У 15% больных полимиозитом наблюдается суставной синдром.
Мышечный синдром проявляется в первую очередь болями в мышцах при движении, прощупывании и даже в покое. Боли сопровождаются прогрессирующей мышечной слабостью, из-за которой пациент не может полноценно осуществлять активные движения: поднять и удержать конечность, держать предметы в руках, поднять голову с подушки, встать, сесть и т. п. Наблюдается уплотнение и отечность пораженных мышц. Со временем при полимиозите в пораженных мышцах развиваются атрофии, миофиброз и контрактуры, в некоторых случаях - кальциноз. Выраженное и распространенное поражение мышц может приводить к полной обездвиженности пациента.
Возможно течение полимиозита с поражением гладкой мускулатуры глотки, гортани и пищевода. В таких случаях развивается дисфагия (трудности при проглатывании пищи, поперхивания во время еды) и дизартрия (нарушение речи). При распространении процесса на глазодвигательные мышцы может отмечаться опущение верхнего века (птоз), двоение предметов (диплопия), косоглазие. При вовлечении в процесс мимической мускулатуры лицо пациента с полимиозитом принимает обездвиженный маскообразный вид.
Суставной синдром характеризуется поражением лучезапястных суставов и мелких суставов кисти. Реже при полимиозите наблюдается поражение плечевых, локтевых, голеностопных и коленных суставов. В области пораженного сустава отмечаются типичные признаки его воспаления: отечность, болезненность, покраснение, ограничение движений в суставе. В коже над суставами возможно отложение кальцификатов. Артрит у больных полимиозитом, как правило, протекает без деформации сустава.
Поражения внутренних органов у половины пациентов с полимиозитом проявляются различными желудочно-кишечными симптомами: боли в животе, анорексия, запор или понос, симптомы кишечной непроходимости. Возможно эрозивное поражение слизистой ЖКТ с развитием кровотечения, прободной язвы желудка или перфорации кишечника. Возникновение пневмонии при полимиозите обусловлено гиповентиляцией легких из-за слабости дыхательной мускулатуры и попаданием пищи в дыхательные пути при поперхиваниях. Со стороны сердечно-сосудистой системы у пациентов с полимиозитом может наблюдаться синдром Рейно, аритмии, миокардит, гипотония, развитие сердечной недостаточности.
Течение полимиозита
Острое течение полимиозита развивается на фоне лихорадки и интоксикации. Характеризуется быстро прогрессирующим поражением мышц, сопровождающимся дисфагией и дизартрией. Очень скоро наступает обездвиженность больного, развиваются сердечно-легочные поражения. При отсутствии лечения высока вероятность смертельного исхода заболевания.
Подострое течение полимиозита отличается более плавным течением с периодами улучшения. Однако оно сопровождается неуклонным прогрессированием мышечной слабости от обострения к обострению, присоединением поражений соматических органов. Хроническое течение полимиозита является наиболее благоприятным и отличается поражением отдельных мышечных групп, что позволяет пациентам длительное время сохранять трудоспособность.
При подозрении на полимиозит пациенты направляются на консультацию ревматолога. Для дифференциации мышечного синдрома от миастении может потребоваться консультация невролога. Наличие симптомов со стороны сердечно-сосудистой системы, легких, органов ЖКТ являются показанием для консультации соответственно кардиолога, пульмонолога, гастроэнтеролога.
В клиническом анализе крови у пациентов с полимиозитом выявляются признаки воспалительного процесса: ускорение СОЭ и лейкоцитоз. Данные биохимического анализа крови свидетельствуют о повышении уровня «мышечных ферментов» (АЛТ, АСТ, КФК, альдолазы). При полимиозите их используют для оценки степени активности происходящего в мышцах воспалительного процесса. В 20% случаев полимиозита наблюдается наличие антинуклеарных антител, у небольшой части пациентов выявляется ревматоидный фактор.
Электромиография при полимиозите проводится для исключения других нервно-мышечных заболеваний. Она определяет повышенную возбудимость и спонтанные фибрилляции, низкую амплитуду потенциалов действия. Оценку состояния внутренних органов проводят по данным копрограммы, УЗИ органов брюшной полости, гастроскопии, ЭКГ, УЗИ сердца, рентгенографии легких.
Большую диагностическую ценность при полимиозите представляет собой гистологическое исследование мышечных волокон, для получения которого проводится биопсия мышц. Забор материала чаще производят из участка двуглавой мышцы плеча, бицепса или квадрицепса. Гистологическое исследование выявляет характерное для полимиозита наличие в мышечной ткани полостей (вакуолей), дегенерацию и некроз мышечных волокон, лимфоцитарную инфильтрацию мышечной ткани и стенок проходящих в ней сосудов.
Базовая терапия пациентов с полимиозитом заключается в назначении глюкокортикостероидов (преднизолон) с постепенным снижением дозы до поддерживающего уровня. Однако такое лечение не всегда эффективно. Терапия глюкокортикостероидами дает результат лишь у 25-50% пациентов и оказывается вовсе неэффективной при миозите с включениями.
Отсутствие улучшения в состоянии пациента спустя 20 дней от начала лечения является показанием к назначению иммунодепрессантов. В первую очередь это парентеральное введение метотрексата. Препаратом запаса является азатиоприн. Лечение этими препаратами требует ежемесячного проведения биохимических проб печени. В терапии полимиозита также возможно применение хлорамбуцила, циклоспорина, циклофосфамида или их комбинаций.
Прогноз полимиозита
Наиболее неблагоприятный прогноз имеет острая форма полимиозита, особенно в случаях, когда пациент не получает адекватного лечения. Летальный исход может быть обусловлен развитием легочно-сердечной недостаточности или аспирационной пневмонии. Развитие полимиозита в детском возрасте является ухудшающим прогноз признаком, так как в этих случаях заболевание, как правило, неуклонно прогрессирует и приводит к обездвиженности больного. Пациенты с хронической формой полимиозита в большинстве случаев имеют благоприятный прогноз как для жизни, так и для трудовой деятельности.
Миозит
Миозит - это воспалительный процесс в скелетных мышцах. Может поражать любые мышцы. Наиболее характерным общим симптомом является локальная боль в мышце (или мышцах), усиливающаяся при движениях и пальпации. Со временем вследствие защитного напряжения мышц может возникать ограничение объема движений в суставах. При длительном течении некоторых миозитов отмечается нарастание мышечной слабости, а иногда - даже атрофия пораженной мышцы. Диагноз устанавливается на основании жалоб и результатов осмотра. По показаниям назначаются дополнительные исследования. Схема лечения подбирается индивидуально и зависит от формы заболевания и вызвавшей его причины.

Миозит - воспалительный процесс в одной или нескольких скелетных мышцах. Этиология заболевания отличается редким многообразием. Чаще всего причиной развития миозита становятся различные инфекции (ОРВИ, грипп, хронический тонзиллит). Кроме того, миозит может возникать при аутоиммунных заболеваниях, вследствие паразитарных инфекций, воздействия токсических веществ и т. д. Болезнь может протекать как остро, так и хронически. В некоторых случаях в процесс вовлекается кожа. При определенных условиях (местном инфицировании) возможно развитие гнойного процесса в мышце.
Тяжесть миозита может сильно варьироваться. Самые распространенные миозиты - шейный и поясничный - хотя бы раз в жизни развиваются почти у всех людей. Часто они остаются недиагностированными, поскольку пациенты принимают проявления миозита за обострение шейного или поясничного остеохондроза. Но встречаются и тяжелые формы миозита, требующие госпитализации и длительного лечения.

Причины миозита
Первое место по частоте заболеваемости занимают поражения мышц, вызванные наиболее распространенными вирусными инфекционными заболеваниями (ОРВИ, грипп). Реже миозит возникает при бактериальных и грибковых инфекциях. Возможно как непосредственное воздействие микроорганизмов на мышцы, так развитие миозита вследствие действия токсинов.
Системные аутоиммунные заболевания являются не самой частой причиной миозитов, но именно они вызывают развитие самых тяжелых форм болезни. Как правило, наиболее тяжелое поражение мышц возникает при полимиозите, дерматомиозите и болезни Мюнхеймера (оссифицирующем миозите). Для других системных заболеваний (ревматоидного артрита, склеродермии, системной красной волчанки) характерны умеренно выраженные миозиты. В числе паразитарных инфекций, наиболее часто вызывающих миозит - токсоплазмоз, эхинококкоз, цистицеркоз и трихинеллез.
Причиной развития миозита может становиться действие различных токсических веществ, как постоянное, так и относительно кратковременное. Так, токсический миозит нередко развивается при алкоголизме или кокаиновой зависимости. Нестойкие поражения мышц могут возникать и при приеме некоторых медикаментов (альфа-интерферона, гидроксихлорохина, колхицина, статинов и т. д.). Такие поражения не всегда носят воспалительный характер, поэтому, в зависимости от симптомов, их могут относить как к миозитам, так и к миопатиям.
Благоприятно протекающие миозиты легкой, реже - средней степени тяжести могут возникать после переохлаждения, травм, мышечных судорог или интенсивных физических нагрузок (особенно - у пациентов с нетренированными мышцами). Боль, отек и слабость в течение нескольких часов или нескольких дней в последнем случае обусловлена мелкими надрывами мышечной ткани. В крайне редких случаях, обычно при экстремальных физических нагрузках возможно развитие рабдомиоза - некроза мышечной ткани. Рабдомиоз также может возникать при полимиозитах и дерматомиозитах.
У людей определенных профессий (скрипачей, пианистов, операторов ПК, водителей и т.д.) миозит может развиваться вследствие неудобного положения тела и продолжительной нагрузки определенных групп мышц. Причиной возникновения гнойного миозита может стать открытая травма с заносом инфекции, очаг хронической инфекции в организме либо местное инфицирование вследствие нарушения правил гигиены при проведении внутримышечных инъекций.
Классификация
С учетом характера процесса в хирургии, неврологии, травматологи и ортопедии выделяют острые, подострые и хронические миозиты, с учетом распространенности - локальные (ограниченные) и диффузные (генерализованные). Кроме того, различают несколько особых форм миозита:
- Инфекционный негнойный миозит. Возникает при вирусных инфекциях (энтеровирусных заболеваниях, гриппе), сифилисе, бруццелезе и туберкулезе. Сопровождается сильной болью в мышцах и заметной общей слабостью.
- Острый гнойный миозит. Обычно является проявлением септикопиемии или осложнением хронического гнойного процесса (например, остеомиелита), характеризуется наличием гнойных и некротических процессов в мышцах. Сопровождается местным отеком и выраженной локальной болью. Возможно повышение температуры тела, озноб и лейкоцитоз.
- Миозит при паразитарных инфекциях. Возникает вследствие токсико-аллергической реакции. Сопровождается болью, отеком и напряжением мышц. Возможно недомогание, небольшое повышение температуры, лейкоцитоз. Нередко имеет волнообразное течение, обусловленное циклом жизнедеятельности паразитов.
- Оссфицирующий миозит. Как правило, возникает после травм, но может быть и врожденным. Отличительной чертой является отложение солей кальция в соединительной ткани. Чаще всего поражаются плечи, бедра и ягодицы. Сопровождается слабостью мышц, прогрессирующей мышечной атрофией, уплотнением мышц и образованием кальцинатов. Боли обычно нерезкие.
- Полимиозит. Множественное поражение мышц. Полимиозит обычно развивается при системных аутоиммунных заболеваниях, является одной из наиболее тяжелых форм миозита. Сопровождается болью и нарастающей мышечной слабостью. В отдельных случаях при таких миозитах возможна атрофия мышц и исчезновение сухожильных рефлексов. У детей может сочетаться с поражением легких, сердца, сосудов и кожи. У мужчин в возрасте старше 40 лет в половине случаев отмечается одновременное образование опухолей внутренних органов.
- Дерматомиозит (болезнь Вагнера-Унферрихта-Хеппа, болезнь Вагнера). Дерматомиозит является системным заболеванием, сопровождается поражением кожи, скелетных и гладких мышц, а также внутренних органов.
Симптомы миозита
Чаще всего локальный процесс (поражение одной или нескольких, но не множества мышц) развивается в мышцах шеи, поясницы, грудной клетки и голеней. Характерным симптомом миозита является ноющая боль, усиливающаяся при движении и пальпации мышц и сопровождающаяся мышечной слабостью. В отдельных случаях при миозите наблюдается незначительное покраснение (гиперемия) кожи и небольшая отечность в области поражения. Иногда миозиты сопровождаются общими проявлениями: субфебрильной температурой или лихорадкой, головной болью и увеличением количества лейкоцитов в крови. При пальпации пораженной мышцы могут определяться болезненные уплотнения.
Миозит может развиваться остро или иметь первично хроническое течение. Острая форма также может переходить в хроническую. Обычно это происходит в отсутствие лечения или при неадекватном лечении. Острые миозиты возникают после мышечного перенапряжения, травмы или переохлаждения. Для инфекционных и токсических миозитов характерно постепенное начало с менее ярко выраженными клиническими симптомами и первично хроническим течением.
Хронический миозит протекает волнообразно. Боли появляются или усиливаются при продолжительных статических нагрузках, изменении погоды, переохлаждении или перенапряжении. Отмечается слабость мышц. Возможно ограничение движений (обычно незначительное) в расположенных рядом суставах.
Виды миозита
Шейный и поясничный миозиты
Шейный миозит - самый распространенный из всех миозитов. Обычно развивается в результате простуды, после перенапряжения мышц или длительного пребывания в неудобной позе. Сопровождается тупой болью, которая чаще локализуется только с одной стороны шеи. Иногда боль отдает в затылок, в висок, ухо, плечо или межлопаточную область. При движениях больной миозитом щадит шею, движения в шейном отделе позвоночника могут быть несколько ограничены из-за боли.
Поясничный миозит также достаточно широко распространен. Из-за одинаковой локализации боли пациенты иногда путают его с любмаго, однако, боль в этом случае не такая острая, преимущественно ноющего характера, не уменьшается в покое, усиливается при движениях и надавливании на мышцы пораженной области.
Шейный миозит и миозит поясничных мышц обычно приходится дифференцировать с обострением остеохондроза, а поясничный миозит - еще и с грыжей соответствующего отдела позвоночника. При постановке диагноза обращают внимание на характер боли (ноющая), усиление болезненности при пальпации мышц и наличие или отсутствие неврологической симптоматики. Для уточнения диагноза может быть выполнена рентгенография позвоночника, МРТ шеи, магнитно-резонансная томография позвоночника или компьютерная томография.
Следует учитывать, что иногда постоянная, не слишком интенсивная ноющая боль в поясничной области свидетельствует о заболевании почек. Поэтому при возникновении таких болей следует обязательно обратиться к врачу, чтобы он оценил клиническую симптоматику, подтвердил или исключил диагноз миозит и при необходимости направил пациента на дополнительные исследования (анализ крови и мочи, УЗИ почек и т.д.).
Дерматомиозиты и полимиозиты
Дерматомиозит относится к группе системных заболеваний соединительной ткани. Встречается достаточно редко - по данным зарубежных исследователей болеет пять человек на 1 миллион населения. Обычно поражает детей в возрасте до 15 лет или людей зрелого возраста (50 лет и старше). У женщин наблюдается вдвое чаще, чем у мужчин.
Классическими проявлениями таких миозитов считаются типичные симптомы со стороны кожи и мышц. Наблюдается слабость мышц тазового и плечевого пояса, мышц брюшного пресса и сгибателей шеи. Пациенты испытывают затруднения при вставании с низкого стула, подъема по лестнице и т.д. При прогрессировании дерматомиозита больному становится трудно удерживать голову. В тяжелых случаях возможно поражение глотательных и дыхательных мышц с развитием дыхательной недостаточности, затруднением глотания и изменением тембра голоса. Болевой синдром при дерматомиозите выражен не всегда. Отмечается уменьшение мышечной массы. Со временем участки мышц заменяются соединительной тканью, развиваются сухожильно-мышечные контрактуры.
Со стороны кожи наблюдаются гелиотропная сыпь (красные или лиловые высыпания на веках, иногда - на лице, шее и туловище) и симптом Готтрона (розовые или красные шелушащиеся бляшки и узелки по разгибательной поверхности мелких и средних суставов конечностей). Возможно также поражение легких, сердца, суставов, желудочно-кишечного тракта и нарушения со стороны эндокринной системы. Примерно у четверти пациентов возникают проявления только со стороны мышц. В этом случае болезнь носит название полимиозит.
Диагноз выставляется на основании клинической картины и данных биохимических и иммунологических исследований крови. Для подтверждения диагноза может выполняться биопсия мышц. Основу терапии составляют глюкокортикоиды. По показаниям применяются цитостатические препараты (азатиоприн, циклофосфамид, метотрексат), а также лекарственные средства, направленные на поддержание функций внутренних органов, устранение нарушений обмена веществ, улучшение микроциркуляции и предотвращение развития осложнений.
Оссифицирующий миозит
Является не одним заболеванием, а группой болезней соединительной ткани. Характеризуется образованием участков окостенения в мышцах. Может возникать вследствие травмы или быть врожденным, генетически обусловленным. Травматический оссифицирующий миозит отличается относительно благоприятным течением. Поражаются только мышцы и суставные связки в области травмы. Лечится хирургически. Конечный результат операции зависит от локализации и распространенности повреждения.
Прогрессирующий оссифицирующий миозит является наследственным заболеванием. Начинается спонтанно, постепенно охватывает все группы мышц. Течение миозита отличается непредсказуемостью. Специфической профилактики и лечения пока не существует. Смерть при прогрессирующем миозите наступает вследствие окостенения глотательных и грудных мышц. Встречается крайне редко - 1 заболевший на 2 миллиона человек.
Лечение миозита
Лечением занимаются врачи различного профиля, выбор специалиста определяется причиной заболевания. Так, миозиты паразитарной этиологии обычно лечат паразитологи, инфекционные миозиты - терапевты или инфекционисты, травматические миозиты и миозиты, развившиеся после значительной физической нагрузки - травматологи-ортопеды и т. д. Терапия миозитов включает в себя патогенетические и симптоматические мероприятия. При бактериальном поражении назначаются антибиотики, при паразитарном - антигельминтные средства. При миозитах, являющихся следствием аутоиммунного заболевания, показаны длительные курсы иммуносупрессоров и глюкокортикоидов.
При острых миозитах и обострении хронических миозитов пациенту рекомендуют постельный режим и ограничение физической активности. При повышении температуры назначают жаропонижающие средства. Для борьбы с болевым синдромом применяют анальгетики, для устранения воспаления - противовоспалительные препараты, обычно из группы НПВС ( кетопрофен, ибупрофен, диклофенак и т. д.). При локальных миозитах эффективны согревающие мази. Местное раздражающее действие этих препаратов способствует расслаблению мышц и позволяет уменьшить интенсивность болевого синдрома. Применяется также массаж (противопоказан при гнойном миозите), физиотерапевтические процедуры и лечебная физкультура. При гнойных миозитах выполняется вскрытие и дренирование гнойного очага, назначаются антибиотики.
Читайте также:
- Техника заднелатерального доступа к коленному суставу по Henderson
- Onс минус вирусы. Вирусы не содержащие онкоген. Свойства вирусов без онкогенов.
- Гипнотерапия при шуме в ухе. Лечебный эффект гипноза
- Приобретенная эпителиома беспигментного эпителия цилиарного тела: признаки, гистология, лечение, прогноз
- Возможности абдоминопластики. Показания к пластике живота
