Общая онкология - эпидемиология, общие методы лечения онкологических заболеваний
Добавил пользователь Владимир З. Обновлено: 22.01.2026
Онкология - наука об опухолях, изучающая механизмы их развития, диагностику, лечение и профилактику.
Опухоль - патологическое разрастание тканей, состоящее из клеток с особыми свойствами размножения и дифференцировки. Опухоль - это новообразование = неоплазма (доброкачественное или злокачественное)
Рак - злокачественное новообразование из эпителия, саркома - злокачественное новообразование из неэпителиальных тканей.
Классификация опухолей.
2. Местно деструирующие
- системные (лейкемия, лимфома)
- солидные (рак органа)
1.2. Основные свойства опухолей (беспредельность роста, относительная автономность, клеточная структурная и функциональная атипия, метастазирование, увеличение потенциала злокачественности со временем).
1. Беспредельность роста (иммортальность):
- опухоль растет и развивается беспредельно
- деление опухолевых клеток происходит в геометрической прогрессии
- опухолевые клетки становятся иммортальными (обязательный этап злокачественного перерождения)
2. Относительная автономность:
- снижение вплоть до полной утраты зависимости размножения раковых клеток от эндогенных и экзогенных факторов
- проявляется в повышенном метаболизме аминокислот, глюкозы, низкомолекулярных компонентов сыворотки
- опухоль способна к синтезу собственных факторов роста, обеспечивающих независимость деления
- изменения в регуляции роста наследуются на клеточном уровне, что связано с активацией протоонкогенов .
- отличие от интактных клеток, из которых возникла опухоль
а) структурная - полиморфизм, необычные размеры и форма клеток, изменение ядер, ядрышек, отсутствие секреторных гранул и т.д.
б) функциональная - утрата специализированных функций в результате дедифференцировки
4. Метастазирование:
- процесс возникновения дочерних очагов опухолевого роста на каком-то удалении от первичного очага.
а) лимфогенный б) гематогенный в) имплантационный г) периневральный
1) появление группы опухолевых клеток, опухолевый ангиогенез (происходит из-за синтеза опухолевыми клетками ангиогенных факторов)
2) отделение клетки от очага (с помощью протеаз)
3) инвазия окружающей опухолью стромы и интравазация (проникновение опухоли в сосудистое русло); в сосудистом русле выживает только 0,1% проникших в него клеток
4) циркуляция опухолевых клеток с током крови и лимфы
5) экстравазация опухолевых клеток
6) иплантация опухолевых клеток
Нарастание злокачественности: 1) чем больше исходный объем опухоли, тем короче сроки удвоения ее объема 2) чем больше объем опухоли, тем больше в ней низкодифференцированных элементов.
1.3. Метастазирование, основные этапы лимфогенного и гематогенного метастазирования.
1.4. Этиология опухолей. Определяющие факторы и внешние этиологические факторы. Канцерогенез.
1) определяющие - оказывают постоянное влияние на организм (пол, возраст, этническая принадлежность, наследственность):
- рак молочной железы встречается у женщин в 100 раз чаще, чем у мужчин, а рак щитовидной железы - в 5 раз чаще.
- рак легкого в 10 раз чаще возникает у мужчин и т.д.
- мутации генов BRCA-1 и BRCA-2 (2-3% рака молочной железы). Наличие мутаций приводит к риску РМЖ 50-80%.
- семейные опухолевые синдромы (Li-Fraumeni - множественные семейные опухоли различных локализаций; Gorlin - базалиома, медуллобластома; MEN-IIA, MEN-IIB - рак щитовидной железы, феохромоцитома, опухоль паращитовидных желез)
- в процессе деления в каждой клетке человека возникает 5000 спонтанных повреждений ядерной и митохондриальной ДНК; спонтанная нестабильность генома в 1 млн раз превышает индуцированную
2) модифицирующие (внешние) - не влияют на организм постоянно (место жительства, условия труда и быта, вредные привычки и т.д.):
- неправильное питание - 35%
- репродуктивный статус - 7%
- профессиональные вредности - 5%
- генетические дефекты - 4%
- геофизические факторы - 3%
Канцерогенез (основные этапы воздействия канцерогена на организм):
1. Воздействие канцерогенного вещества на человека, которое характеризуется:
а) наружной дозой - конценрацией канцерогена в окружающей среде
б) внутренней дозой - концентрацией канцерогена во внутренней среде организма (кровь, моча, ткани и т.д.)
в) биологически эффективной дозой - количеством экзогенного канцерогена или его метаболита, которое связывается с ДНК или белками.
2. Ранний биологический эффект: повреждение генетического аппарата клетки, активация онкогенов и инактивация генов-супрессоров с появлением хромосомных аберраций, микроядер и др.
3. Клиническое проявление злокачественной опухоли.
В реализации всех этих этапов важное значение имеют особенности генетической / метаболической репарации ДНК, иммунный статус, питание и ряд других факторов.
Общая онкология - эпидемиология, общие методы лечения онкологических заболеваний
1. World Health Organization. Global Health Observatory. Geneva: World Health Organization, 2018. Р.45-48.
2. Gersten O., Wilmoth J.R. The cancer transition in Japan since 1951. Demogr Res. 2002. V. 7. P. 271-306.
3. Bray F. Transitions in human development and the global cancer burden. In: BW Stewart, CP Wild, eds. World Cancer Report 2014. Lyon: IARC Press, 2014. P.42‐ 55.
4. Ferlay J., Colombet M., Soerjomataram I., Mathers C., Parkin D.M., Piñeros M., Znaor A., Bray F. Global and Regional Estimates of the Incidence and Mortality for 38 Cancers: GLOBOCAN 2018. Lyon: International Agency for Research on Cancer/World Health Organization, 2018. Р.33-39.
5. Hankey B.F., Feuer E.J., Clegg L.X., Hayes R.B., Legler J.M., Prorok P.C., Ries L.A., Merrill R.M., Kaplan R.S. Cancer surveillance series: interpreting trends in prostate cancer - Part I: evidence of the effects of screening in recent prostate cancer incidence, mortality, and survival rates. J. Natl. Cancer Inst. 1999. vol.91. P. 1017‐ 1024.
6. Bray F., Colombet M., Mery L. Cancer Incidence in Five Continents, Vol. XI (electronic version). Lyon: International Agency for Research on Cancer, 2018. Р. 67-72.
7. Doll R., Payne P., Waterhouse J. Cancer Incidence in Five Continents: A Technical Report. New York: Springer, 1966. Р.23-25.
9. Alonso R., Pineros M., Laversanne M., Musetti C., Garau M., Barrios E., Bray F. Lung cancer incidence trends in Uruguay 1990-2014: an age‐period‐cohort analysis. Cancer Epidemiol. 2018. V. 55. P. 17‐ 22.
10. Lortet‐Tieulent J., Renteria E., Sharp L., Weiderpass E., Comber H., Baas P., Bray F., Coebergh J.W., Soerjomataram I. Convergence of decreasing male and increasing female incidence rates in major tobacco‐related cancers in Europe in 1988-2010. Eur. J. Cancer. 2015. V. 51. P. 1144‐1163.
11. Jha P. Avoidable global cancer deaths and total deaths from smoking. Nat. Rev. Cancer. 2009. V. 9. P. 655‐ 664.
12. Ziegler R.G., Hoover R.N., Pike M.C., Hildesheim A., Nomura A.M., West D.W., Wu-Williams A.H., Kolonel L.N., Horn-Ross P.L., Rosenthal J.F., Hyer M.B. Migration patterns and breast cancer risk in Asian‐American women. J. Natl. Cancer Inst. 1993. V. 85. P. 1819‐ 1827.
13. Brinton L.A., Gaudet M.M., Gierach G.L. Breast cancer. In: M.J. Thun, M.S. Linet, J.R. Cerhan, C.A. Haiman, D. Schottenfeld eds. Cancer Epidemiology and Prevention. 4th ed. New York: Oxford University Press. 2018. P. 861‐888.
14. Arnold M., Sierra M.S., Laversanne M., Soerjomataram I., Jemal A., Bray F. Global patterns and trends in colorectal cancer incidence and mortality. Gut. 2017. V. 66. P. 683‐ 691.
15. Schreuders E.H., Ruco A., Rabeneck L., Schoen R.E., Sung J.J., Young G.P., Kuipers E.J. Colorectal cancer screening: a global overview of existing programmes. Gut. 2015. V. 64. P. 1637‐1649.
16. Wu K., Keum N., Nishihara R., Giovannucci E.L. Cancers of the colon and rectum. In: M.J. Thun, M.S. Linet, J.R. Cerhan, C.A. Haiman, D. Schottenfeld eds. Cancer Epidemiology and Prevention. 4th ed. New York, NY: Oxford University Press, 2018. P. 681‐706.
17. Magalhaes B., Peleteiro B., Lunet N. Dietary patterns and colorectal cancer: systematic review and meta‐analysis. Eur J Cancer Prev. 2012. V. 21. P. 15‐ 23.
18. Rebbeck T.R., Devesa S.S., Chang B.L., Bunker C.H., Cheng I., Cooney K., Eeles R. Global patterns of prostate cancer incidence, aggressiveness, and mortality in men of African descent [serial online]. Prostate Cancer. 2013. V. 2013. P. 560-567.
19. IARC Working Group on the Evaluation of Carcinogenic Risks to Humans. Infection with Helicobacter pylori. IARC Monogr Eval Carcinog Risks Hum. 1994. V. 61. P.177‐ 240.
20. deMartel C., Parsonnet J.. Stomach cancer. In: M.J. Thun, M.S. Linet, J.R. Cerhan, C.A. Haiman, D. Schottenfeld eds. Cancer Epidemiology and Prevention. 4th ed. New York: Oxford University Press, 2018. P. 593‐610.
По определению Всемирной организации здравоохранения, рак - это группа заболеваний, характеризующихся тем, что происходят неконтролируемый рост и распространение аномальных клеток. В настоящее время существует понятие эпидемиологии неинфекционных заболеваний, к которым относятся и злокачественные опухоли. На первом месте по смертности находятся сердечно-сосудистые заболевания, которые являются причиной смерти в 31% случаев, а злокачественные опухоли находятся на втором месте с показателем 16% [1].
Общие уровни смертности от рака в развитых странах постепенно снижаются. Например, в Японии смертность уменьшается с 1960-х гг. (стандартизированные по возрасту показатели смертности в возрасте 30-69 лет). В снижении смертности от некоторых форм злокачественных опухолей (рака желудка, рака шейки матки) в Японии сыграли роль рост экономики страны и улучшение оказания онкологической помощи населению. Однако внедрение западного образа жизни (курение, употребление алкоголя и др.) привело к росту других форм рака (рака толстой кишки, рака эндометрия, рака простаты и др.). Таким образом, инфекционные причины развития рака, такие как Helicobacter pylori (H. pylori) и вирус папилломы человека, не стали основными этиологическими факторами, и на первый план стали выходить неинфекционные факторы риска (ожирение, курение, гормональные сдвиги, промышленные профессиональные вредности) [2]. Об этом также упоминает Bray F., который отмечает, что те виды рака, которые чаще встречаются в экономически развитых странах мира, такие как рак легких, рак молочной железы, стали все чаще выявляться в неразвитых государствах [3]. Обзор литературы проведен на основе данных по опухолям основных локализаций, представленных GLOBOCAN 2018 и Международным агентством по исследованию рака (МАИР) [4].
Цель исследования - изучить основные показатели заболеваемости и смертности при злокачественных новообразованиях в мире.
Количество новых случаев рака было взято из базы данных GLOBOCAN 2018 для некоторых видов рака. Эпидемиологи отмечают, что сейчас наблюдается увеличение показателей заболеваемости раком во всем мире. Некоторые исследователи (Hankey B.F. и др.) связывают это с улучшением диагностики, регистрации и частично с гипердиагностикой, как это произошло в США в 1990-х гг. в случае с внедрением теста на простат-специфический антиген (ПСА) при раке предстательной железы [5]. Bray F. и иные отмечают, что не все страны охвачены высококачественными раковыми регистрами, их только около 15%. В большинстве неразвитых стран, к сожалению, только 1-7% населения охвачены адекватными регистрами. В последнее время наблюдаются положительные сдвиги в африканских странах - охват раковыми больными достиг 13% [6]. Показатели заболеваемости раком в обзоре отражены в виде стандартизованных величин [7].
Распределение случаев заболевания и смертности по регионам мира и видам рака
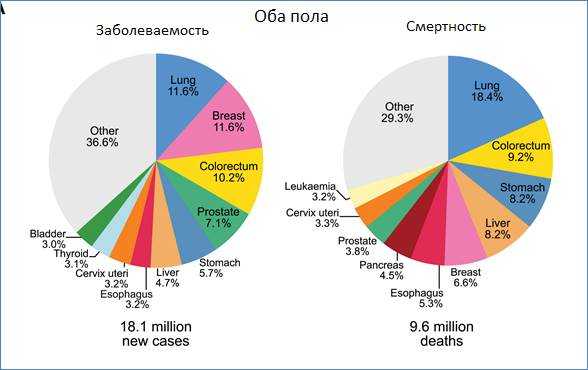
Рис. 1. Заболеваемость и смертность при злокачественных новообразованиях в мире
Глобальные модели рака
В мире наблюдается значительная глобальная вариабельность ведущих локализаций рака. Например, рак простаты - это наиболее частая опухоль в 105 странах, за ним следует рак легких в 37 странах и рак печени в 13 странах. При некоторых опухолях отмечается повышенная сосредоточенность в определенных регионах. Так, рак печени чаще встречается в странах Африки, а рак губы и полости рта - в Южной Азии, особенно в Индии. Также наблюдается повышенная заболеваемость саркомой Капоши в Восточной Африке или неходжкинской лимфомой в субэкваториальной Африке.
Рак легких является основной причиной смертности в большинстве стран ввиду высокой доли распространенных и запущенных стадий, а также отсутствия адекватного специального и радикального лечения.
Среди женской популяции мира в большинстве стран, особенно в развитых и развивающихся, наиболее часто встречается рак молочной железы: из 180 стран мира в 154. В остальных 36 государствах самой частой онкологической патологией является цервикальный рак. Как причина смертности у женщин на первом месте в большинстве стран также находятся рак молочной железы и рак шейки матки. Такая ситуация прослеживается в 105 странах из 180, а в остальных - это рак легких.
Региональная вариабельность заболеваемости и смертности при раке
Показатели смертности также были различными в странах. Самые высокие показатели смертности у мужчин наблюдались в Восточной Европе - 171,0 на 100 тыс., а самые низкие - в Центральной Америке - 67,4 на 100 тыс. У женщин ситуация со смертностью была следующей - самая высокая смертность отмечена в Меланезии - 120,7 на 100 тыс., а самая низкая - также в Центральной Америке - 64,2 на 100 тыс.
Уругвай - страна с одним из самых высоких показателей заболеваемости РЛ в мире - инициировал в 2005 г. серию всеобъемлющих антитабачных мер. С использование данных Национального регистра рака Уругвая Alonso R. и другими был проведен возрастно-когортный анализ тенденций РЛ за 1990-2014 гг. У мужчин стандартизированные по возрасту (мировые) показатели снизились с пика 165,6 в 1995 г. до 103,1 к 2014 г., что привело к снижению риска развития РЛ у мужчин, родившихся в 1970 г., на 70% по сравнению с родившимися в начале 1940-х гг. У женщин этот показатель неуклонно повышался - с 18,3 в 1991 г. до 30,0 к 2014 г., причем последовательное увеличение риска происходило среди поколений женщин, родившихся в 1940-1960 г. Однако имеются данные о снижении наблюдаемых показателей у женщин, родившихся в последнее время. Экстраполяция этих тенденций показывает, что к 2035 г. среднее число новых случаев РЛ у мужчин сократится на 8%, а у женщин - на 69%. [9]. Lortet-Tieulent J. и иные показали, что по-прежнему существуют значительные, но изменяющиеся различия в показателях заболеваемости раком, связанным с употреблением табака, в разных европейских регионах. Как правило, высокие показатели среди мужчин снижаются, в то время как более низкие показатели среди женщин увеличиваются, что приводит к их сближению. В Дании, Исландии и Швеции показатели заболеваемости РЛ у женщин были выше, чем у мужчин (35-64 года). При раке легких и гортани, где курение является основным фактором риска, показатели заболеваемости были самыми высокими в Центральной и Восточной Европе, Южной Европе и странах Балтии. Несмотря на снижение распространенности курения среди женщин, показатели заболеваемости раком легких, гортани и полости рта среди женщин увеличились в большинстве стран Европы, но в странах Балтии они были стабильными [10]. Однако в Китае у женщин тоже имеются высокие показатели заболеваемости РЛ. По мнению Jha P., это вызвано повышенным воздействием дыма от сжигания древесного угля в бытовых целях [11].
Рак молочной железы у женщин (РМЖ)
Уровень заболеваемости РМЖ исторически был в 4-7 раз выше в США, чем в Китае или Японии. Когда китайские, японские или филиппинские женщины мигрируют в США, риск развития у них РМЖ возрастает в течение нескольких поколений и приближается к тому значению, которое отмечается у белых американок. Ziegler R.G. и иные показали, что наблюдался шестикратный градиент риска развития РМЖ по характеру миграции. У женщин азиатского происхождения, родившихся на Западе, риск развития РМЖ был на 60% выше, чем у женщин азиатского происхождения, родившихся на Востоке. Среди тех, кто родился на Западе, риск определялся тем, родились ли их бабушки и дедушки, особенно бабушки, на Востоке или на Западе. Этнически специфичные показатели заболеваемости РМЖ в мигрирующем поколении были явно выше, чем в странах происхождения, в то время как показатели среди американцев азиатского происхождения, родившихся на Западе, приближались к уровню показателей заболеваемости РМЖ белых в США. Следовательно, воздействие западного образа жизни оказало существенное влияние на риск развития РМЖ у азиатских мигрантов, прибывших в США [12]. Brinton L.A. и иные продемонстрировали, что повышенные показатели заболеваемости в странах с более высоким уровнем дохода объясняются влиянием репродуктивных факторов риска [13].
Колоректальный рак (КРР)
Также существуют широко распространенные различия в статусе и стратегии осуществления скрининга КРР. Они могут быть объяснены географическими несходствами в распространенности КРР, экономическими ресурсами, структурой здравоохранения и инфраструктурой для поддержки скрининга, такими как способность идентифицировать целевую популяцию в группе риска и доступность регистра рака [15]. Это заболевание можно рассматривать как маркер социально-экономического развития, и в странах, переживающих значительный переходный период развития, показатели заболеваемости имеют тенденцию к равномерному росту [16]. Magalhaes B. и иные провели обзор 8 когортных и 8 контрольных исследований, определяющих закономерности влияния диеты и развития КРР. Метаанализы были проведены для трех паттернов: высокое потребление алкоголя, фруктов/овощей и красного/обработанного мяса («западный стиль»). Риск развития рака толстой кишки был повышен при использовании паттернов, характеризующихся высоким потреблением красного и обработанного мяса, и снижен при использовании паттернов, связанных с фруктами и овощами («здоровый стиль»). Никаких значимых ассоциаций для рака прямой кишки не наблюдалось [17].
Рак предстательной железы (РПЖ)
В последние годы во многих странах мира РПЖ занимает ведущие позиции и входит в тройку наиболее распространенных опухолей у человека. Об этом говорят следующие факты - 1,3 млн мужчин заболели РПЖ в 2018 г. и примерно 400 тыс. умерли. Четко показано, что уровни заболеваемости РПЖ очень высоки у афроамериканцев в США. По данным Rebbeck T.R. и иных, в 2008 г. среди этих мужчин было диагностировано более 30 000 случаев РПЖ. Также высокие уровни заболеваемости были отмечены на островах Карибского бассейна и в районах ниже Сахары. При этом стандартизированные по возрасту показатели заболеваемости РПЖ варьировались от 159,6 на 100 тыс. среди афроамериканцев до 71,1 на 100 тыс. в Карибском бассейне и 17,5 на 100 тыс. в Африке. Однако число смертельных случаев от РПЖ в Африке было более чем в 5 раз больше, чем среди афроамериканцев, или в 4 раза больше, чем среди мужчин, проживающих на Карибских островах. Существуют различия в показателях заболеваемости и смертности между мужчинами африканского, азиатского, латиноамериканского и европейского происхождения, что подтверждает генетическую предрасположенность. Тем не менее изучено и доказано влияние и экологических факторов, так как между мужчинами одной и той же расы могут быть неодинаковые уровни заболеваемости РПЖ [18].
Хроническое инфицирование бактерией Helicobacter pylori (H. pylori) вызывает некардиальную карциному желудка и низкодифференцированную мантийно-клеточную лимфому из В-клеток. Было показано, что 660 000 случаев рака в мире в 2008 г. были связаны с H. pylori, что соответствует 32,4% из 2 млн случаев рака, связанных с инфекционными агентами, и 5,2% из 12,7 млн общих случаев рака, имевших место во всем мире. Подавляющее большинство раковых заболеваний, связанных с H. pylori (650 000), были опухолями некардиального отдела желудка [19]. Helicobacter pylori является основным фактором риска развития РЖ, причем почти 90% новых случаев некардиального РЖ вызвано этой бактерией [20].
Таким образом, обзор литературы подтвердил, что рак является актуальной проблемой в медицине. Это обусловлено высокими показателями заболеваемости, увеличением смертности, недостаточной регистрацией первичных случаев рака, неудовлетворительными результатами лечения, продолжающимися воздействиями неблагоприятных факторов внешней среды.
В мире наблюдается выраженная неравномерность распространения рака по регионам и по основным формам рака. Наиболее частыми опухолями являются рак легких, рак молочной железы, рак простаты, рак желудка, рак шейки матки и рак печени.
Знание основных закономерностей распространения злокачественных опухолей в определенных регионах способствует своевременному проведению профилактических мероприятий, направленных на снижение уровней заболеваемости и выяснение этиологических причин и возможных патогенетических аспектов развития рака.
Что такое рак: онкология
Многие пациенты совершенно однозначно интерпретируют термины «рак», «онкология», «злокачественное новообразование». Однако нужно понимать, что это не одна болезнь, а скорее целый класс заболеваний, имеющих между собой как сходства, так и значительные отличия.
Рак — это злокачественная опухоль, при которой происходит бесконтрольное размножение клеток, сопровождающееся инвазией в подлежащие ткани и метастазированием в отдаленные органы с током лимфы и/или крови. В народе раком называют любую злокачественную опухоль, но ученые сюда относят только карциномы — опухоли, произрастающие из эпителиальных тканей. Злокачественные новообразования из других тканей называют саркомами, злокачественные новообразования лимфатической системы называют лимфомами, а кроветворной — лейкозами.
Зачастую онкология воспринимается пациентами, как смертный приговор. Однако в реальности далеко не все злокачественные опухоли приводят к гибели человека. Более половины всех пациентов благополучно излечиваются и люди забывают о перенесенном заболевании навсегда.
Несмотря на значительные успехи в лечении онкологии, все же данная патология характеризуется достаточно высоким уровнем летальности и, безусловно, для успешного лечения требует к себе самого пристального внимания со стороны высококвалифицированных докторов.
Механизм возникновения рака
В основе онкологического заболевания лежит нарушение процессов регуляции тканевого роста.
Клетки нашего организма постоянно обновляются. В процессе их деления всегда существует вероятность возникновения ошибок в генах (мутации). Это происходит и в норме, но их частота значительно возрастает при воздействии на организм таких неблагоприятных факторов, как канцерогенные вещества, ионизирующее излучение и др.
Для предупреждения и исправления мутаций существуют различные механизмы. Если они не срабатывают, клетка с поврежденной ДНК развивается и многократно делится, не подчиняясь контролирующим системам организма. В итоге формируется образование, которое принято называть термином «злокачественная опухоль».

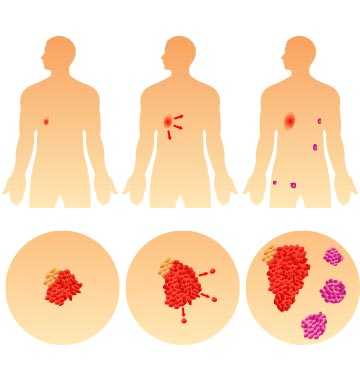
Злокачественные опухоли характеризуются тремя ключевыми отличиями от доброкачественных:
- Неконтролируемый бесконечный рост.
- Прорастание (инвазия) в соседние ткани и органы с нарушением их функционирования.
- Способность к метастазированию — процессу миграции раковых клеток с током крови или лимфы в другие части тела
Именно данные характеристики определяют агрессивность процесса и его злокачественность.
Опухоль может состоять из плотной ткани и тогда говорят о солидном образовании. Однако она может иметь и жидкую консистенцию, как при лейкозах и лимфомах.
Трудности в лечении рака
Онкологическое заболевание может возникнуть у любого живого организма в любом возрасте. Однако данный риск увеличивается с возрастом. Считается, что более 64% случаев заболевания выявляются у людей старше 65 лет. Тем не менее, в настоящее время онкологи говорят об омоложении таких пациентов. Все чаще болезнь диагностируется в возрасте до 40 лет.
Существуют две основные проблемы в лечении данной патологии:
- Распространенность опухолевого процесса, что ограничивает возможности радикального хирургического лечения.
- Гетерогенность клеточного состава опухоли. Можно подобрать препараты, которые убьют 99% опухолевых клеток, но если хотя бы несколько из них уцелеют, то они снова будут делиться, и разовьется рецидив
заболевания.

Причины появления рака
Причины онкологических заболеваний очень разнообразны, но все они приводят
к тому, что в клетках организма возникает мутация, которая приводит к их
бесконтрольному размножению. Спровоцировать образование и размножение
таких клеток могут следующие факторы:
Неправильное питание
Оно является одной из главных причин возникновения рака. И здесь есть несколько аспектов. Во-первых, во многих продуктах, которые люди употребляют ежедневно, содержится определенное количество пищевых канцерогенов. К таким продуктам относят копчености, маринады и другие консервированные и жареные блюда, овощи и фрукты, выращенные с применением химических удобрений и пестицидов и др. Во-вторых, имеет значение сбалансированность питания. Например, есть данные, что избыток мяса в рационе приводит к увеличению риска развития колоректального рака, в то же время большое количество растительных волокон и клетчатки снижает эти риски. Несбалансированное питание может привести к развитию ожирения, которое является фактором риска таких злокачественных новообразований как рак поджелудочной железы.
Старение
В подавляющем большинстве случаев злокачественные опухоли возникают у людей старше 50 лет. Это связывают с накоплением действия факторов риска и ослаблением механизмов защиты и уничтожения мутировавших клеток.
Наследственность
Когда говорят о наследственных причинах онкологии, имеют ввиду два аспекта — генетическую предрасположенность и наследственные формы злокачественных новообразований. В целом вероятность заболеть той или иной формой рака в течение жизни составляет 5-10%. Однако при наличии в семье случаев злокачественных новообразований, эта вероятность увеличивается более, чем в два раза. Это называется генетической предрасположенностью. Помимо этого, есть наследственные формы рака, при которых имеются мутации в определенных генах. В качестве примера можно привести мутации в генах BRCA, при наличии которых вероятность развития рака молочной железы или яичников составляет около 80%.
Вирусы
Вирус папилломы человека высокого онкогенного риска вызывает рак шейки матки. Вирусы гепатитов В и С увеличивают вероятность возникновения рака печени. Инфицирование вирусом Эпштейна-Барр может привести к развитию лимфомы, а Т-лимфотропный вирус может вызвать развитие лейкоза.
Вредные привычки и химическая зависимость
Курение, злоупотребление алкоголем и наркомания также являются серьезными причинами развития рака. Например, каждый пятый случай развития злокачественного новообразования связывают именно с курением. Причем речь идет не только о раке легких. Табачный дым увеличивает риск развития рака ЛОР-органов и органов пищеварительной системы, то же касается и алкоголя. Наркомания приводит к серьезным нарушениям обмена веществ и работы всех систем организма, в том числе и иммунной. На этом фоне развиваются неоплазии, характерные для иммунодефицитов — лимфомы, лейкозы, саркомы.
Ионизирующее излучение
Когда говорят об ионизирующем излучении как о причине развития онкологии на постсоветском пространстве, большинство людей имеет ввиду катастрофу на ЧАЭС. И с этим сложно спорить, поскольку после взрыва отмечалось увеличение случаев развития злокачественных неоплазий, в том числе лейкозов, лимфом и рака щитовидной железы. Однако, помимо этого, нельзя забывать об опасности воздействия солнечного излучения, которое может неблагоприятно воздействовать на кожу и органы зрения. Также увеличивает риск развития вторичных раковых опухолей прохождение лучевой терапии.
Предраковые заболевания
Некоторые виды рака развиваются на фоне имеющейся патологии. Например, колоректальный рак в большинстве случае происходит из аденоматозных кишечных полипов, рак эндометрия может происходить на фоне миом или эндометриоза, раку кожи могут предшествовать пигментный кератоз, лейкоплакия или кожный рог, раку легкого — некоторые профессиональные заболевания легких, раку шейки матки — воспалительные и диспластические процессы. Поэтому важно регулярно проходить скрининговое обследование для своевременного выявления предраковых заболеваний и их лечения.
Неблагоприятная экологическая обстановка и воздействие промышленных и химических канцерогенов
Наиболее агрессивные канцерогены — это асбест, сажа, выхлопные газы автомобилей, некоторые виды продуктов переработки нефти.
Методы лечения рака
Еще несколько лет назад диагноз «рак» зачастую звучал как приговор. Но онкология, как и любая сфера медицины, не стоит на месте. Классическая триада лечения онкологических заболеваний — хирургия, химиотерапия и лучевая терапия — сегодня дополнилась новыми методиками. Современные онкологи имеют в своем распоряжении широкий арсенал, который помогает спасать многие жизни, а в случаях, когда это невозможно — существенно продлевать жизнь пациента и избавлять от мучительных симптомов.
Врач-онколог разрабатывает программу лечения, исходя из типа, локализации, стадии опухоли, состояния здоровья больного. С пациентом работает команда специалистов, которая может включать онкологов, терапевтов, химиотерапевтов, радиологов, анестезиологов, психоонкологов, реабилитологов, хирургов-онкологов.
В данной статье будут рассмотрены основные методы лечения онкологических заболеваний, мы коротко остановимся на каждом из них и расскажем о важных моментах.
Хирургическое лечение
Во время операции хирург удаляет опухолевую ткань, пораженные близлежащие лимфатические узлы. Цели хирургического лечения могут быть разными:
- Удаление опухоли целиком.
- Удаление части опухоли (циторедуктивные операции). От рака это не излечит, но поможет повысить эффективность химиотерапии и других методов лечения.
Паллиативные операции обычно выполняют на поздних стадиях рака. Они помогают уменьшить боли, частично восстановить функции пораженного органа.
Иногда можно прибегнуть к миниинвазивному лапароскопическому вмешательству, в других случаях приходится делать большой разрез. Это зависит от размеров и локализации опухоли. При больших новообразованиях приходится удалять много тканей или даже целые части тела, например, молочную железу. В дальнейшем восстановить внешность помогают реконструктивно-пластические операции, протезы.
В случаях, когда это возможно, современные хирурги обходятся без скальпеля и прибегают к криохирургии (разрушение новообразования при помощи низкой температуры), лазерной хирургии, фотодинамической терапии (введение в опухоль специального препарата, который делает её чувствительной к свету, с последующим облучением).
Химиотерапия
Химиопрепараты уничтожают быстро делящиеся клетки. Химиотерапия может применяться как самостоятельно, так и в сочетании с другими методами, например, хирургическими вмешательствами, лучевой терапией. Химиотерапия может преследовать разные цели:
- Уменьшить опухоль перед хирургическим вмешательством или курсом лучевой терапии. В данном случае химиотерапия будет называться неоадъювантной.
- Уничтожить раковые клетки, которые остались в организме пациента после операции. Такую химиотерапию называют адъювантной.
- Повысить эффективность других методов лечения рака.
- Предотвратить рецидив после операции, лучевой терапии.
- Облегчить боль и другие симптомы, вызванные опухолью.
Химиопрепараты применяют в виде таблеток и капсул, внутривенных инъекций, также их могут вводить в организм другими способами.

Лучевая терапия
Лучевая терапия применяет ионизирующее излучение, которое, как и химиопрепараты, уничтожает быстро делящиеся клетки. Её можно использовать как для уничтожения опухоли, так и для облегчения боли и других симптомов.
Существуют две разновидности лучевой терапии:
- При внешнем облучении аппарат находится на расстоянии от пациента и посылает пучок лучей в область тела, где находится опухоль.
- При внутреннем облучении источник излучения вводят в тело пациента. Если источник излучения представляет собой твердый предмет (капсулу или ленту), такой вид лечения называется брахитерапией. В качестве источника излучения может выступать и жидкость, которую вводят внутривенно. Она распространяется по всему организму и уничтожает раковые клетки в разных органах. Такую методику используют, в частности, при раке щитовидной железы.
Лучевую терапию нередко сочетают с хирургическим лечением:
- Перед операцией она помогает уменьшить размеры опухоли.
- Во время операции хирург имеет возможность облучать опухоль непосредственно, так, чтобы лучи не проходили через кожу.
- После операции лучевая терапия помогает уничтожить оставшиеся раковые клетки.

Гормональная терапия
Рост злокачественных опухолей простаты и молочной железы сильно зависит от гормональных эффектов. Если раковые клетки имеют рецепторы к мужским или женским половым гормонам, врач назначит гормональную терапию. Препараты, которые при этом применяются, могут бороться с опухолью двумя путями:
Подавлять выработку «виновного» гормона.
«Мешать» гормонам оказывать свои эффекты, связываясь с рецепторами на поверхности раковых клеток.
Гормональную терапию очень редко назначают отдельно, чаще всего она дополняет другие виды лечения. Иногда прибегают к хирургическим вмешательствам, во время которых удаляют яичники или яички, чтобы половые гормоны в организме больше не вырабатывались.
Иммунотерапия
Современные ученые научились редактировать гены в иммунных клетках. У пациента берут Т-лимфоциты, изменяют их гены таким образом, чтобы они могли атаковать опухоль, искусственно размножают новые клетки в пробирке и возвращают в организм.
Таргетная терапия
В последние годы ученые многое узнали о молекулярных механизмах, которые помогают раковым клеткам расти, размножаться, выживать. Новые знания помогли создать новое направление в лечении рака — таргетную терапию. У таргетного препарата всегда есть конкретная цель — специфическая молекула, которая образуется в раковых клетках и нужна для роста, выживания опухоли.
Разные таргетные препараты действуют по-разному:
- работают как препараты для иммунотерапии;
- блокируют молекулярные сигналы, которые заставляют раковые клетки бесконтрольно делиться;
- блокируют молекулярные сигналы, которые нужны для роста новых сосудов и питания опухоли;
- делают клетки опухоли чувствительными к химиопрепаратам, излучению;
- вызывают естественную гибель раковых клеток — апоптоз;
- работают как препараты для гормональной терапии.
Таргетную терапию можно применять как отдельно, так и в сочетании с другими методами лечения.
Генная инженерия в лечении онкологических заболеваний
Несмотря на то, что за последние годы онкология шагнула далеко вперед, перед ней стоит еще много проблем. Даже современные методы лечения не всегда оказываются эффективными. Ученые постоянно ищут новые пути.
Например, в октябре 2016 года китайские ученые сообщили о том, что впервые применили новую технологию редактирования генома у пациента, страдающего раком легкого с метастазами. Исследователи взяли у мужчины лейкоциты и при помощи системы CRISPR-cas9 отредактировали в них гены, которые мешают иммунной системе атаковать опухоль. «Исправленные» клетки размножили в лаборатории и вернули обратно в организм больного. Если испытание увенчается успехом, аналогичный метод применят для лечения рака мочевого пузыря, почек, предстательной железы.
Много лет назад ученые обнаружили, что в геноме бактерий есть странные повторяющиеся последовательности. Долгое время считалось, что они «лишние» и не выполняют никаких функций. Но потом обнаружилось, что эти последовательности — копии генов фагов, которые поражают бактериальные клетки, и они работают как аналог иммунитета у человека. Когда соответствующий фаг инфицирует бактерию, она распознает его с помощью системы CRISPR-Cas и активирует фермент, который «разрезает» ДНК фага, тем самым инактивируя его.
Ученые обнаружили, что в лаборатории с помощью CRISPR-Cas можно разрезать любые гены в нужном месте. Был открыт относительно простой, быстрый и недорогой метод редактирования генов. Он нашел применение во многих сферах, в том числе в онкологии. С помощью CRISPR-Cas изучают гены, ответственные за развитие злокачественных опухолей, создают новые лекарственные препараты, модифицируют иммунные клетки таким образом, чтобы они могли распознавать и атаковать раковые клетки. Несколько клинических исследований проводится прямо сейчас.
В 2016 году онкологам из США впервые удалось вылечить женщину от рака молочной железы IV стадии с помощью адаптивной T-клеточной иммунотерапии. 46-летняя Джуди Перкинс перенесла несколько курсов химиотерапии, но лечение оказалось безуспешным, опухоль продолжала прогрессировать, появились метастазы в печени.
Специалисты из Национального института рака (NCI) в Мэриленде решили применить у пациентки инновационный метод лечения, который ранее хорошо зарекомендовал себя в борьбе с меланомой. Из ее крови извлекли T-лимфоциты, «обучили» их атаковать раковые клетки и ввели обратно в организм. Предварительно было проведено секвенирование генома опухолевых клеток, чтобы выявить произошедшие в них мутации. На основе этой информации были отобраны подходящие T-клетки.
В результате у женщины наступила ремиссия. В 2018 году ученые сообщили, что в ее организме вот уже два года не обнаруживаются признаки присутствия злокачественной опухоли. До этого врачи говорили, что Джуди осталось жить не более трех лет.
Такое лечение все еще носит характер экспериментального. Оно не до конца изучено, есть много сложностей с его внедрением. Например, при использовании T-клеточной терапии невозможно создать «универсальные» T-клетки, которые помогали бы всем больным, для каждого пациента их нужно «обучать» персонально, с учетом мутаций, обнаруженных в конкретной злокачественной опухоли. Это стоит очень дорого. Но прогресс не стоит на месте. Кто знает, как изменится ситуация в будущем. Ведь уже сегодня стало реальностью то, что десятилетия назад считалось чем-то из разряда научной фантастики.
Разработка и испытания новых методик — не быстрый процесс, он может продолжаться многие годы. Но со временем это даст шанс многим онкологическим больным.
Современная диагностика и лечение рака в «Евроонко»
Лечение онкологических заболеваний в клиниках федеральной сети «Евроонко» проводится в соответствии с высочайшими международными стандартами:
- Для борьбы с раком применяются все новейшие оригинальные препараты последних поколений с проверенной эффективностью. В онкологических центрах сети всегда в наличии инновационные противоопухолевые средства, и врачи готовы немедленно приступить к проведению терапии.
- Лечение в соответствии с актуальными редакциями международных онкологических протоколов.
- В клиниках «Евроонко» работают ведущие врачи-онкологи, каждый из которых обладает обширным опытом и является экспертом в своей сфере.
- Проводится широкий спектр хирургических вмешательств в операционной, оснащенной новейшим оборудованием. Применяются все возможности современной эндоскопической, интервенционной хирургии.
- При необходимости есть возможность собрать врачебный консилиум с участием ведущих экспертов, организовать онлайн-консультацию с зарубежными коллегами.
- Для нас не существует безнадежных пациентов, и мы беремся за лечение рака на любых стадиях. Даже в случаях, когда добиться ремиссии невозможно, правильно подобранная терапия помогает затормозить прогрессирование заболевания, нормализовать состояние и продлить жизнь пациента.
3. Эпидемиология рака. Виды эпидемиологических исследований в онкологии.
В настоящее время под эпидемиологией рака понимают раздел онкологии,который изучает частоту, причины возникновения закономерности распространения злокачественных новообразований на определенной территории среди всего населения или отдельных его групп. В онкологической эпидемиологии применяется комплексный метод, включающий статистические исследования, эпидемиологическое обследование, сравнительно-исторический анализ, элементы медицинской географии, экспериментальное моделирование.
1.2. ОПИСАТЕЛЬНАЯ (ДЕСКРИПТИВНАЯ) ЭПИДЕМИОЛОГИЯ РАКА.
Описательная эпидемиология изучает особенности распространения отдельных форм злокачественных опухолей в конкретных группах населения. Предмет изучения описательной эпидемиологии - заболеваемость и смертность вразных географических регионах, населенных пунктах. Основными задачами онкологической статистики являются:
определение современного состояния и основных тенденций заболеваемости, болезненности и смертностей населения от злокачественных опухолей;
оценка эффективности мероприятий в области, профилактики и раннего выявления злокачественных новообразований, лечения и реабилитации онкологических больных;
обеспечение органов здравоохранения постоянной информацией для оперативного руководства системой противораковой борьбы
Объектами изучения онкологической статистики являются:
распространение опухолей среди всего населения и отдельных его групп;
1.3. АНАЛИТИЧЕСКАЯ ЭПИДЕМИОЛОГИЯ РАКА
Этиологические гипотезы, возникающие из таких наблюдений, подкрепляются углубленным изучением населения, причинно-следственных связей между заболеванием и его возможным фактором риска и особенностей распространения рака по времени, месту возникновения, а также по индивидуальным характеристикам заболевших, что и составляет основу аналитической эпидемиологии.
Основными задачами аналитической эпидемиологии рака являются:
ответственных за возникновение зпокачественных новообразовании у человека;
определение опасности канцерогенного воздействия различных факторов окружающей среды на человека, в том числе изучение проблем профессионального рака;
анализ причин неэффективности( эффективности) тех или иных мероприятий по профилактике и лечению злокачественных опухолей.
Связь между злокачественными новообразованиями и социальными, географическими и природно-этническими факторами. 1.4. ЭКСПЕРИМЕНТАЛЬНАЯ ЭПИДЕМИОЛОГИЯ РАКА
Экспериментальные эпидемиологические исследования или так называемые интервенционные контролируемые исследования предполагают проведение в какой-то степени эксперимента на человеке. Таких исследованиях обычно изучается аффект удаления или снижения воздействия предполагаемого канцерогена
на заболеваемость и смертность от рака, этиологически возможно связанного с ним. Включенные в них лица подвергаются влиянию факторов с предположительно ингибирующим канцерогенез.
Понятие о рандомизации. Процесс случайного распределения вариантов лечения (другого воздействия) между пациентами называется рандомизацией. Метод конвертов: 1. Слепой (исследователь знает, а пациент нет). 2 . Двойной слепой( никто не знает).
Кагортный метод 1. Ретроспективный
Случай -контроль 2. Проспективный
Деонтология в онкологии.
Медицинская деонтология - наука о врачебном долге; совокупность этических норм при выполнении медиком своих профессиональных обязанностей, основанная на гуманизме.
Особенности медицинской деонтологии в онкологии:
а) самоизлечения практически не бывает, выздоровления больного всецело зависит от компетенции врача
б) страх населения перед злокачественными опухолями особенно велик
в) распространено мнение о бесперспективности лечения
Учитывая вышеперечисленное, при общении с пациентов врач должен:
1. Успокоить пациента и психологически подготовить его к предстоящему лечению, внушив веру в излечимость заболевания. Информировать пациента о методах лечения, их эффективности, исходя из данных научных исследований или основываясь на благоприятных исходах заболевания у конкретных, известных больному, людей.
2. Уметь оказать психологическую коррекцию состояния пациента согласно его стадии адаптации (шок - отрицание - агрессия - депрессия - попытки сговора с судьбой - принятие болезни).
3. Индивидуально подходить к вопросу информирования больного о его заболевании
4. Уметь убедить больного в необходимости того или иного метода диагностики или вида операции и др.
Эпидемиология рака. Понятие о демографическом и эпидемиологическом переходах.
Эпидемиологический переход. Этот термин используется для динамической характеристики структуры заболеваемости и смертности населения Земли. Сдвиг структуры заболеваемости населения в сторону увеличения и устойчивого преобладания хронических неинфекционных болезней над инфекционными получил название «эпидемиологического перехода». Доля хронических неинфекционных заболеваний, и в том числе рака, в структуре заболеваемости и смертности населения в большинстве стран мира на протяжении последнего столетия неуклонно возрастает и постепенно начинает занимать доминирующее положение, принадлежавшее ранее инфекционным болезням.
Понимание природы изменений в структуре заболеваемости населения возможно только при учете наблюдающихся особенностей его демографического состояния. Теория демографического перехода, разработанная F. Notestein и К. Davis (1944-45), предполагала, что все общества проходят три стадии развития:
от доиндустриальной через индустриальную к постиндустриальной, при которой достигается демографическое равновесие в мире вследствие демографического перехода. Дословно термин «демографический переход» означает переход от роста к стабилизации численности населения Земли.
В концептуальном плане явление демографического перехода заключается в первоначально резком увеличении скорости роста популяции, которое сменяется затем стремительным ее уменьшением, после чего население стабилизируется в своей численности. На завершающих этапах демографического перехода происходит резкое увеличение продолжительности жизни и изменение возрастной структуры населения (соотношение между молодым и старшими поколениями) . Одновременно, в процессе перехода происходит рост производительных сил общества и урбанизация населения. Таким образом, составляющими демографического перехода являются такие понятия, как численность населения планеты, продолжительность его жизни и возрастно-половая структура.
Понятие о противораковой борьбе, ее основные направления.
Понятие «противораковая борьба» подразумевает комплекс мероприятий, направленных на защиту человека от воздействия известных канцерогенных агентов, активное.выявление заболевших на доступных для обнаружения начальных этапах опухолевого роста, своевременную диагностику и лечение больных с применением современных методов, их медицинскую и социальную реабилитацию" и при необходимости - оказание паллиативной помощи.
Лечение. Главная цепь в печении онкологических больных состоит в том, чтобы добиться полноговыздоровления или максимально возможно длительной ремиссии при высоком качестве жизни пациентов. Решение ее непосредственно связано с последовательным расширением и укреплением и развитием соответствующих специализированных лечебных учреждений, оснащенных современной аппаратурой и оборудованием, обеспечением их необходимыми лекарствами и высококвалифицированным персоналом.
Первичная профилактика - комплекс санитарно-гигиенических мероприятий, устраняющих влияние факторов риска и повышающих противоопухолевую резистентность организма.
Примеры: санпросвет работа, борьба с вредными привычками, пропаганда рационального питания, охрана окружающей среды, защита рабочих мест
Рациональное питание и режим:
- ежедневно фрукты до 5 раз в день (минимум 400 г.)
- уменьшение потребления говядины, баранины, жирного мяса
- увеличение потребления рыбы и растительного масла
- сохранение стабильного правильного веса
- ограниченное употребление алкоголя, отказ от курения
- избегать прямого солнечного воздействия
- подвижный и активный образ жизни
Медицинская (вторичная) профилактика - выявление лиц с высокой степенью риска, их диспансеризация, систематический контроль и лечение хронических заболеваний.
При выявлении злокачественной опухоли на ранней стадии многократно повышается вероятность ее успешного лечения. Своевременное обнаружение предопухолевых заболеваний и злокачественных опухолей на доклинической стадии возможно только в результате скрининга онкологических заболеваний.
Третичная профилактика - снижение и предотвращение смертности от рака путем лечения уже существующего заболевания, предупреждения его рецидивов, а также развития другой формы рака.
Реабилитация. Реабилитация предполагает использование государственных, медицинских, социально-экономических, профессиональных, педагогических и других мероприятий, направленных на эффективное и раннее возвращение больных и инвалидов в общество и к общественно полезному труду. Реабилитация онкологического больного должна начинаться до применения того или иного лечения и продолжаться всю оставшуюся жизнь.
Паллиативная терапия. Разработка и широкое внедрение новых и эффективных методов паллиативного
лечения, облегчающих страдания заболевших раком, и предоставление этим людям возможностей для медицинской и социальной реабилитации позволили бы в значительной степени облегчить тягостные последствия этого заболевания на заключительных этапах жизни.
Диспансеризация онкологических больных. Учетная онкологическая документация.
Общий принцип проведения онкологического компонента диспансеризации состоит в формировании групп повышенного риска включающих лиц, имеющих ту или иную патологию и/или имеющие те или иные факторы риска, которые могут привести (или привели) к развитию опухолевого или предопухолевого заболевания.
Фактором, побудившим возложить на амбулаторно-поликлиническую сеть эту работу, является наличие постоянной и прочной связи между населением и общей лечебной сетью, построенной по участковому принципу и осуществляющей наблюдение и лечение одних и тех же контингентов населения .в пределах одной территории (участка).
Диспансерное наблюдение за онкологическими больными осуществляется в основном онкологической службой. Диспансеризация больных с онкологическими заболеваниями предполагает заполнение учетной документации,
Основные принципы диспансерной работы в онкологии:
Повсеместный и строгий учет больных раком и предопухолевыми заболеваниями.
Динамическое наблюдение и печение больных раком и предраковыми заболеваниями.
Изучение и своевременная коррекция условий труда и быта больных.
Оперативная связь онкологической службы с учреждениями общей лечебной сети.
Диспансеризация больных злокачественными новообразованиями осуществляется пожизненно.
Группы диспансерного учета:
К группе 1а, относят больных с неясной клинической картиной, подозрительной на злокачественное новообразование. Их обследование и уточнение диагноза должно быть организовано не позднее, чем через 10 дней с момента взятия на учет. Больных группы la при подтверждении диагноза рака переводят во II или IV группы или снимают с учета при исключении опухоли. На больных la группы учетная документация не заполняется.
Больные группы 16 - с предопухолевыми заболеваниями - наблюдаются у специалистов по профилю в зависимости от пораженного органа, больных облигатным предраком и наблюдоют врачи онкологи. После радикального лечения. Предопухолевых заболеваний больные подлежат диспансерному наблюдению в течение 2 лет (осматриваются 1 раз в 3 месяца). При полном выздоровлении и отсутствии рецидива больные снимаются с учета. Учетная документация - контрольная карта диспансерного наблюдения (ф. № 030/у-03-онко).
Больные II группу злокачественными новообразованиями подлежат специальному лечению. Учетная документация: извещение (ф. № 090(у-03) и контрольная карта диспансерного наблюдения (ф. № 030/у-03-онко). Кроме того, выделяют группу II а - больных, подлежащих радикальному печению. Под радикальным лечением понимают применение методов, направленных на полное излечение больного. После проведенного специального (радикального) лечения больные переводятся в III клиническую группу, а при обнаружении отдаленных метастазов - в IV.
К группе III относят больных после радикального печения, при отсутствии рецидивов и метастазов, т.е. это практически здоровые люди, излеченные от злокачественных новообразований. При возникновении рецидивов больные из этой группы могут переводиться в группу II для проведения специального лечения (хирургического, лучевого и др.) или в группу IV, если специальное лечение не показано или не может быть проведено.
К IV клинической группе относят больных с распространенной формой злокачественного новообразования, специальное лечение которых даже с паллиативной (симптоматической) целью невозможно. Если у больного впервые выявлена злокачественная опухоль в IV стадии, то заполняется извещение, контрольная карта и «Протокол на случай выявления у больного запущенной формы злокачественного новообразования».
Тактика врача общей лечебной сети зависит от клинической группы больного.


Учетные документы на онкологических больных:
1. форма 090/у - “Извещение о впервые в жизни установленным диагнозом рака или другого злокачественного новообразования” - заполняется на каждого вновь выявленного больного злокачественной опухолью; служит для анализа данных по системе «канцеррегистр». Отправляется в онкодиспансер в течение 3-х дней.
2. форма 027/у - “Выписка из медицинской карты стационарного больного злокачественным новообразованием” - заполняется лечащим врачом после лечения больных злокачественными опухолями в стационаре, отправляется в онкодиспансер.
3. форма 027-2/у - “Протокол на случай выявления у больного запущенной формы злокачественного новообразования” - заполняется на первичных больных любыми злокачественными опухолями в IV стадии и на больных с III стадией рака наружных форм злокачественных новообразований
4. форма 25/у - «Медицинская карта амбулаторного больного» - учетная форма, заполняемая на амбулаторного больного. Срок хранения - 5 лет.
5. форма 030-6/у - «Контрольная карта диспансерного наблюдения (онко)» - заполняется на больных злокачественными новообразованиями; ведется всю жизнь.
Читайте также:
- Синдром Уотерхауса-Фридериксена (Waterhouse-Friderichsen)
- Синдром Одри (Audry)
- Субдолевая резекция легкого на рентгенограмме, КТ
- Доброкачественное пароксизмальное позиционное головокружение (ДППГ) горизонтального полукружного канала, связанное с каналолитиазом
- Эритропоэтическая протопорфирия и протопорфирия, связанная с Х-хромосомой
