Отравление L-триптофаном - синдром эозинофильной миалгии
Добавил пользователь Morpheus Обновлено: 01.02.2026
Синдром эозинофилии-миалгии - редкое состояние, обусловленное приемом некоторых препаратов с содержанием аминокислоты триптофана и характеризующееся выраженными системными поражениями (легких, мышечной системы, суставов и фасций). Симптомами являются кашель, затрудненное дыхание, повышенная утомляемость, боли в мышцах, неврологические нарушения и воспаления суставов. Диагностика проводится посредством лабораторных анализов (общий анализ крови), рентгенологических методик и изучения анамнеза больного. Лечение заключается в отмене приема провоцирующего лекарства и проведении симптоматической терапии.
Дополнительные факты
Синдром эозинофилии-миалгии был впервые диагностирован и выделен как отдельная нозологическая единица в середине 80-х годов XX века. В те годы возникла вспышка данной патологии, обусловленная широким распространением препарата на основе триптофана, выпускаемого одним из японских фармацевтических предприятий. В настоящее время средства с содержанием такой аминокислоты в мире практически не выпускаются, однако случаи заболевания все равно встречаются. Обычно его причиной становится использование фальсификатов некоторых продуктов (рапсового масла) и лекарственных средств, содержащих в своем составе вредные примеси. Синдром с равной долей вероятности поражает как мужчин, так и женщин, представляет потенциальную опасность для жизни.
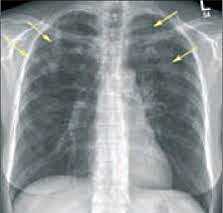
Синдром эозинофилии-миалгии
Причины
Расследование, проведенное вскоре после обнаружения патологии, показало, что ее причиной является не сам триптофан (жизненно важная аминокислота), а некоторые примеси в лекарственном средстве. Они попадали в препарат в процессе химического синтеза основных компонентов и считались условно безопасными по причине ничтожной концентрации. Предположительно эти примеси запускали необычные аллергические процессы, приводящие к поражению легких, резкому увеличению количества эозинофилов в крови, болезненности мышц и другим нарушениям. Развитие синдрома послужило основным поводом для запрета таких лекарственных препаратов.
Существует также предположение, что основной причиной развития патологии являлись метаболиты триптофана - соединения под условными названиями ЕВТ и МТСА. Еще несколько веществ подозреваются в участии в патогенезе синдрома. Однако исследования, проведенные с чистыми вариантами данных соединений, имели неоднозначные результаты, поэтому их роль в этиологии заболевания оспаривается некоторыми учеными. Помимо них в тех партиях лекарственных средств, использование которых связывают с патологическим состоянием, было найдено еще более 60 примесей. Ряд исследователей считают, что возникновение нарушений обусловлено сочетанным действием сразу множества веществ.
Существует мнение, что и сам L-триптофан при попадании в организм в повышенных дозах мог спровоцировать развитие эозинофилии, миалгии и иных нарушений. Установлено, что это аминокислота в чистом виде способна замедлять деградацию гистаминоподобных соединений, участвующих во многих воспалительных и аллергических реакциях. Лишь у некоторых больных, принимающих триптофан, развитие синдрома объясняется наличием особенностей реактивности или других механизмов предрасположенности. В тоже время, такая точка зрения не объясняет, из-за чего возникает патология при употреблении иных продуктов или лекарств (например, схожую симптоматику имеет синдром токсического масла).
Патогенез
Патогенетические процессы при синдроме эозинофилии-миалгии изучены еще хуже, чем его этиология, поскольку достоверно не определено соединение, провоцирующее заболевание. На основании клинических данных можно предположить, что определенный фактор провоцирует увеличение образования или замедление распада стимуляторов воспаления - гистамина, некоторых интерлейкинов и простагландинов. Это вызывает иммунную воспалительную реакцию в легких, фасциях мышц, суставах и нервах. Пораженные ткани инфильтрируются макрофагами и лимфоцитами, что еще больше усугубляет патологический процесс. Развитие эозинофилии, согласно данной гипотезе, связано с увеличением концентрации гистамина - эозинофилы играют центральную роль в процессах его распада.
Согласно другой теории патогенеза болезни, первопричиной, напротив, является именно активация эозинофилов, которые начинают проникать в ткани и способствовать накоплению в них токсических продуктов. Это, в свою очередь, провоцирует возникновение воспаления с вовлечением иных иммунокомпетентных клеток и развитием лимфоцитарной инфильтрации. Но, как и в предыдущей гипотезе, пусковой фактор заболевания остается неизвестным. Данные гистохимических исследований могут интерпретироваться в качестве доказательств как первого, так и второго предположения, поэтому изучение синдрома продолжается.
Клиническая картина
Проявления синдрома возникают после употребления лекарственных средств или других продуктов, содержащих триптофан и его метаболиты. Сроки развития заболевания могут сильно различаться - от нескольких дней до 3-5 месяцев после начала приема. Первоначально отмечается повышенная утомляемость и разбитость, которая сменяется выраженными болями в мышцах, усиливающимися при движениях. Одновременно появляются жалобы на слабость мышечной системы - пациент становится неспособен выдерживать привычные для него нагрузки. Миалгия может сочетаться с неприятными ощущениями в области сердца, что свидетельствует о вовлечении в патологический процесс миокарда.
Более чем у половины больных наблюдаются поражения дыхательной системы, проявляющиеся кашлем, хрипами при дыхании, одышкой. Течение патологии иногда осложняется симптомами плеврита - болями в груди при дыхании, усилением сухого кашля. Респираторные нарушения могут сохраняться в течение нескольких недель или даже месяцев. Зачастую определяются отеки подкожной жировой клетчатки на кистях или стопах. В особенно тяжелых случаях возникает накопление жидкости в полостях тела - брюшной, плевральной, перикардиальной. У ряда больных эозинофилией-миалгией отмечаются неврологические симптомы в виде нарушений чувствительности пальцев, кистей, стоп.
Ассоциированные симптомы: Кашель. Лейкоцитоз. Одышка. Разбитость. Рвота. Увеличение СОЭ. Эозинофилия.
Возможные осложнения
Эозинофилия-миалгия, по данным медицинской статистики, примерно в 4-5% случаев приводит к летальному исходу. Причиной смерти становится тяжелая дыхательная недостаточность или нарушения работы сердца, обусловленные миокардитом и накоплением жидкости в перикардиальной полости (гидроперикард). При длительном течении заболевания происходит уменьшение дыхательного объема легких за счет фиброза, что снижает качество жизни и трудоспособность пациента. Описаны случаи, когда после развития синдрома возникал ревматоидный полиартрит. Это свидетельствует о возможности иммунологических нарушений вследствие заболевания, но достоверной взаимосвязи между этими двумя патологиями пока не обнаружено.
Диагностика
Для определения синдрома эозинофилии-миалгии используют множество диагностических методик - опрос больного, рентгенографические исследования, общие лабораторные анализы. При возникновении затруднений могут дополнительно производить микроскопическое исследование мокроты, гистологические исследования пораженных тканей. Однозначным признаком патологии является использование пациентом лекарств либо продуктов, содержащих синтезированный свободный триптофан. Поэтапно диагностика состояния производится следующим образом:
• Опрос и сбор анамнеза. При общении с пациентом аллергологу-иммунологу важно выяснить, употреблял ли он в последние дни и недели какие-либо лекарственные средства, масляные продукты, некоторые виды спортивного питания. С учетом этого можно определить, контактировал ли больной с триптофаном и его токсичными метаболитами. Среди жалоб наиболее часто отмечаются одышка, боли в разных группах мышц, слабость.
• Рентгенологические исследования. На рентгенографии органов грудной клетки можно выявить признаки уплотнения легочной ткани в виде сетчато-узелкового или сетчатого поражения. Там же обнаруживаются признаки плеврита и изменения контуров сердца при гидроперикарде. Рентгенография не является основным методом диагностики, поскольку патологические изменения выявляются лишь в 20% случаев синдрома.
• Лабораторные анализы. В общем анализе крови определяется выраженная эозинофилия - до 1 000 клеток в одном микролитре. Нередко регистрируются признаки воспалительной реакции - увеличение СОЭ, лейкоцитоз.
• Гистологическое изучение. Для диагностики патологии могут производить биопсию легких (при респираторных нарушениях), мышц и фасций (при миалгии) и других тканей в зависимости от клинической картины. Гистологическое исследование тканей пораженных органов выявляет инфильтрацию кровеносных сосудов мелкого калибра моноцитами, эозинофилами, лимфоцитами.
Дифференциальная диагностика
Дифференциальную диагностику проводят с инфекционно-воспалительными поражениями легких (бронхит, пневмония), заболеваниями сердца и системными аутоиммунными состояниями - некоторыми формами ревматизма и полиартритов. Главными признаками синдрома являются наличие в анамнезе приема лекарств или продуктов с триптофаном, отсутствие признаков инфекции по анализам крови.
Лечение
Основным условием успешного лечения заболевания является исключение триптофан-содержащего препарата или продукта, вызвавшего патологический процесс. Поэтому в ходе диагностики важно определить, откуда больной получает провоцирующие вещества. Для уменьшения симптомов назначаются кортикостероидные средства, обладающие выраженным противовоспалительным действием. Схема и длительность их использования зависит от конкретной клинической ситуации. Примерно у половины пациентов симптомы патологии исчезают через несколько дней после начала лечения, тогда как у других сохраняются на протяжении 2-3 недель.
Симптоматические мероприятия требуются редко, при сильном кашле могут применяться лекарства, уменьшающие активность кашлевого центра. Отеки устраняют посредством использования диуретических препаратов. Антигистаминные средства не используют по причине их неоднозначного и слабого эффекта при данной патологии. Иногда назначают поддерживающее лечение с использованием поливитаминных препаратов.
Прогноз
Прогноз синдрома эозинофилии-миалгии условно благоприятный при раннем обнаружении и своевременном обращении к специалисту. После исключения провоцирующего вещества и проведения кортикостероидной терапии симптомы исчезают без последствий. В случае длительного течения в легких могут развиваться склеротические процессы, снижающие жизненную емкость и поверхность газообмена. Это приводит к одышке при умеренной физической нагрузке, цианотичности кожи и прочим нарушениям.
Профилактика
Профилактика синдрома заключается в отказе от использования препаратов, содержащих триптофан, особенно сомнительного происхождения. Следует как можно быстрее отменить прием таких средств, если на фоне их применения возникает болезненность мышц, кашель, одышка.
Эозинофильный эзофагит
Эозинофильный эзофагит — это хронический иммуноопосредованный воспалительный процесс, который характеризуется резко выраженной эозинофильной инфильтрацией слизистой оболочки пищевода. Патология проявляется затруднениями проглатывания твердой пищи, загрудинными болями, периодически возникающей рвотой. Для диагностики эзофагита используется эндоскопическое обследование с биопсией, гистологический анализ биоптатов. Для уточнения диагноза проводится исследование крови и мочи, иммунограмма. Лечение предполагает комбинацию индивидуально подобранной диеты с назначением топических стероидов и ингибиторов протонной помпы.
МКБ-10
Общие сведения
Заболевание относится к иммунным антигенопосредованным поражениям слизистого слоя ЖКТ, но его этиологические факторы до конца не определены. Существует мнение, что патология выступает как проявление общей атопической реакции организма. В современной гастроэнтерологии принята концепция, согласно которой выделяют 3 группы причин эозинофильного эзофагита:
- Генетические особенности. Доказана ассоциация болезни с генами, которые кодируют синтез стромального лимфопоэтина и эотаксина-3. У больных эозинофильным эзофагитом количество эотаксина-3 в эзофагеальной слизистой в 50 раз превышает норму, что способствует повышенной миграции эозинофилов к пищеводу. Семейный характер патологии наблюдается у 14,5% пациентов.
- Поражение эзофагеальной слизистой. Началу аутоиммунного эзофагита способствуют длительно протекающие воспалительные процессы в пищеводе или аномалии строения эпителиальной оболочки. Эти причины обуславливают быстрое и глубокое проникновение чужеродных антигенов в толщу стенки пищевода.
- Сенсибилизация к аллергенам. Попадание специфических для конкретного индивидуума пищевых или пылевых антигенов — пусковой фактор эозинофильного воспаления. Аллергены запускают каскад биохимических реакций и активируют иммунное воспаление в эзофагеальной стенке.
Факторы риска
Вероятность развития эозинофильного эзофагита возрастает при наличии у человека других аллергических заболеваний:
Установлена повышенная заболеваемость среди пациентов с наследственными поражениями соединительной ткани (синдромы Элерса-Данлоса, Марфана). К независимым факторам риска относят потребление ГМО-продуктов, повсеместное и неоправданное использование антибиотиков. Вероятность появления эзофагита увеличивается при проживании в регионах с неблагоприятной экологической ситуацией.
Патофизиологической основой эозинофильного эзофагита является миграция вглубь пищеводной слизистой эозинофилов — клеток лейкоцитарного ряда, которые в норме там отсутствуют. Под действием аллергенов происходит активация Т-лимфоцитов, индукция синтеза специфических провоспалительных интерлейкинов 4, 5 и 13. Эти вещества влияют на эпителий и усиливают выработку эотаксина-3.
Как следствие усиливается хемотаксис эозинофилов из периферической крови в эзофагеальную слизистую, повышается их пролиферация в костном мозге. Эозинофилы выделяют биологически активные вещества — МВР, катионные белки, пероксидазу и нейротоксин. Следующим этапом эозинофильного воспалительного процесса становится выброс гистамина и цитокинов, которые оказывают прямое повреждающее действие на пищевод.
Симптомы эозинофильного эзофагита
У детей дошкольного возраста заболевание проявляется трудностями с кормлением. Периодически по окончании приема пищи появляются срыгивание или рвота. Дети отказываются от еды, становятся нервными и беспокойными. Из-за сложностей с проглатыванием ребенок предпочитает жидкую или полужидкую пищу, длительно пережевывает каждый кусочек. Наблюдается медленный набор веса, отставание в росте и физическом развитии.
Школьники и подростки, страдающие эозинофильным эзофагитом, жалуются на изжогу, умеренные боли за грудиной. Возникает необходимость запивать водой любую твердую пищу, что облегчает глотание. Ребенок ест очень медленно, обычно оставляет половину порции на тарелке. Некоторые подростки сообщают о чувстве «застревания» еды в пищеводе, дискомфорте в верхних отделах живота. При попытке быстрого поглощения пищи начинается рвота.
У взрослых людей клиническая картина схожа, но в связи с длительным течением эозинофильного эзофагита симптомы выражены сильнее. Больные предъявляют жалобы на мучительные давящие или распирающие боли по ходу пищевода, которые беспокоят после еды. Дисфагия наблюдается постоянно, возникают сложности с употреблением даже полужидкой пищи. Неприятные симптомы провоцируют повышенную нервозность и раздражительность.
Осложнения
Опасное последствие эозинофильного эзофагита — острый разрыв пищевода (синдром Бурхаве), обусловленный обтурацией органа большим пищевым комком. Это состояние сопровождается подкожной эмфиземой, болевым шоком. На фоне разрыва иногда начинаются профузные кровотечения в виде кровавой рвоты, которые опасны геморрагическим шоком и без оказания медицинской помощи имеют неблагоприятный исход.
При длительном существовании эозинофильного воспаления в стенке органа образуется соединительная ткань. Фиброз проявляется стриктурами и стенозом пищевода, что усугубляет клиническую картину заболевания. Персистирующие воспалительные процессы являются предпосылкой для метаплазии эпителиальных клеток, поэтому наличие эозинофильного эзофагита сопряжено с риском появления злокачественных опухолей.
При первичной консультации врач-гастроэнтеролог использует несколько опросников для оценки частоты и тяжести симптомов. При физикальном обследовании эозинофильный эзофагит ничем не отличается от ГЭРБ. В пользу первого заболевания говорит отягощенный аллергологический анамнез. Для верификации диагноза обязательно проводится комплекс лабораторно-инструментальных методов, включающий:
- Эзофагоскопия. При эндоскопическом осмотре органа обнаруживают отек и контактную кровоточивость слизистой, продольные линейные борозды. Зачастую видны эозинофильные микроабсцессы, имеющие вид островков беловатого экссудата. У взрослых также визуализируются фиброзные изменения — концентрические кольца, стриктуры.
- Гистологическое исследование. Микроскопия более 6 биоптатов из разных участков эзофагеальной слизистой — золотой стандарт диагностики. В эпителии и подслизистом слое наблюдаются скопления эозинофилов и микроабсцессы. Для эозинофильного эзофагита характерно расширение межклеточных промежутков и фиброз наружного слоя оболочки.
- Лабораторные анализы. В общем анализе крови наблюдается эозинофилия, степень которой соотносится с тяжестью клинических проявлений болезни. В иммунограмме характерно повышение уровня IgE, эотаксина-3 и отдельных фракций интерлейкинов. В анализе мочи выявляют биомаркер 3-бромтирозин, который отражает активность эозинофилов.
- Малоинвазивные методы. В некоторых клиниках проводится String Test, который предполагает заглатывание специальной капсулы с последующим ее извлечением и анализом адсорбированных эозинофильных ферментов. Для малотравматичного забора образцов слизистого слоя используется цитогубка.
Лечение эозинофильного эзофагита
Консервативная терапия
Первый этап лечения — подбор рациона питания. Элементная диета с приемом аминокислотных смесей назначается редко, поскольку зачастую плохо переносится больными. Чаще прибегают к таргетной диете, которая предполагает исключение из рациона индивидуальных пищевых аллергенов. До проведения специфических тестов показана эмпирическая элиминационная диета, предусматривающая ограничение наиболее распространенных аллергизирующих веществ.
Эффективность диетотерапии составляет около 53% у детей и около 40% у взрослых. Если клинические проявления не удается купировать немедикаментозными способами, используют лекарственные препараты. Для лечения эозинофильного эзофагита рекомендована длительная поддерживающая терапия, которая в несколько раз снижает вероятность обострения. Схема включает:
- Топические кортикостероиды. Гормоны в форме аэрозоля относятся к первой линии терапии. Они уменьшают выраженность симптоматики, продлевают гистологическую ремиссию при эзофагите.
- Ингибиторы протонной помпы. Эффективность ИПП обусловлена повышением барьерной функции слизистой оболочки, что затрудняет проникновение аллергенов. Клиническое улучшение после добавления препаратов в схему лечения испытывают 80% больных.
Хирургическое лечение
К эндоскопическим методам прибегают при сужении пищеводного просвета до 13 мм и менее. Хирургические вмешательства в основном рекомендуются взрослым. Для снижения явлений дисфагии показана эндоскопическая баллонная дилатация или бужирование пищевода. Вмешательство выполняется в плановом порядке после стихания активности процесса в результате проведения медикаментозной терапии.
Экспериментальное лечение
На сегодняшний день существует успешный опыт применения моноклональных антител к интерлейкинам для редукции симптоматики и уменьшения эозинофильной инфильтрации. В клинических испытаниях установлена высокая эффективность препаратов для купирования дисфагии. Хорошие результаты наблюдаются при назначении селективных антител к ИЛ-13, эффект которых продолжается дольше 6 месяцев.
Прогноз и профилактика
Благодаря разработке новых методов терапии эозинофильного эзофагита стойкой ремиссии удается добиться у 80-90% больных. Прогноз благоприятный: большинство пациентов, которым правильно подобрано лечение, отмечают улучшение качества жизни и возвращение к привычному ритму активности. Профилактика включает раннее выявление и лечение атопических патологий, устранение пищевых и экологических факторов риска.
1. Эозинофильный эзофагит: современный взгляд на проблему и собственные клинические наблюдения/ В.О. Кайбышева, С.В. Кашин, Л.М. Михалева, Н.С. Сидяева и др.// Доказательная гастроэнтерология. — 2019.
2. Эозинофильный эзофагит у детей/ Т.Н. Будкина, И.С. Садиков, С.Г. Макарова, М.М. Лохматов и др.// Вопросы современной педиатрии. — 2016.
3. Эозинофильный эзофагит: учебное пособие для врачей / В.Т. Ивашкин, Е.К. Баранская, А.С. Трухманов, В.О. Кайбышева. — 2013.
4. ACG Clinical Guideline: Evidenced Based Approach to the Diagnosis and Management of Esophageal Eosinophilia and Eosinophilic Esophagitis (EoE). — 2013.
Синдром эозинофилии-миалгии
Расследование, проведенное вскоре после обнаружения патологии, показало, что ее причиной является не сам триптофан (жизненно важная аминокислота), а некоторые примеси в лекарственном средстве. Они попадали в препарат в процессе химического синтеза основных компонентов и считались условно безопасными по причине ничтожной концентрации. Предположительно эти примеси запускали необычные аллергические процессы, приводящие к поражению легких, резкому увеличению количества эозинофилов в крови, болезненности мышц и другим нарушениям. Развитие синдрома послужило основным поводом для запрета таких лекарственных препаратов.
Существует также предположение, что основной причиной развития патологии являлись метаболиты триптофана - соединения под условными названиями ЕВТ и МТСА. Еще несколько веществ подозреваются в участии в патогенезе синдрома. Однако исследования, проведенные с чистыми вариантами данных соединений, имели неоднозначные результаты, поэтому их роль в этиологии заболевания оспаривается некоторыми учеными. Помимо них в тех партиях лекарственных средств, использование которых связывают с патологическим состоянием, было найдено еще более 60 примесей. Ряд исследователей считают, что возникновение нарушений обусловлено сочетанным действием сразу множества веществ.
Существует мнение, что и сам L-триптофан при попадании в организм в повышенных дозах мог спровоцировать развитие эозинофилии, миалгии и иных нарушений. Установлено, что это аминокислота в чистом виде способна замедлять деградацию гистаминоподобных соединений, участвующих во многих воспалительных и аллергических реакциях. Лишь у некоторых больных, принимающих триптофан, развитие синдрома объясняется наличием особенностей реактивности или других механизмов предрасположенности. В тоже время, такая точка зрения не объясняет, из-за чего возникает патология при употреблении иных продуктов или лекарств (например, схожую симптоматику имеет синдром токсического масла).
Патогенетические процессы при синдроме эозинофилии-миалгии изучены еще хуже, чем его этиология, поскольку достоверно не определено соединение, провоцирующее заболевание. На основании клинических данных можно предположить, что определенный фактор провоцирует увеличение образования или замедление распада стимуляторов воспаления - гистамина, некоторых интерлейкинов и простагландинов. Это вызывает иммунную воспалительную реакцию в легких, фасциях мышц, суставах и нервах. Пораженные ткани инфильтрируются макрофагами и лимфоцитами, что еще больше усугубляет патологический процесс. Развитие эозинофилии, согласно данной гипотезе, связано с увеличением концентрации гистамина - эозинофилы играют центральную роль в процессах его распада.
Согласно другой теории патогенеза болезни, первопричиной, напротив, является именно активация эозинофилов, которые начинают проникать в ткани и способствовать накоплению в них токсических продуктов. Это, в свою очередь, провоцирует возникновение воспаления с вовлечением иных иммунокомпетентных клеток и развитием лимфоцитарной инфильтрации. Но, как и в предыдущей гипотезе, пусковой фактор заболевания остается неизвестным. Данные гистохимических исследований могут интерпретироваться в качестве доказательств как первого, так и второго предположения, поэтому изучение синдрома продолжается.
Симптомы
Проявления синдрома возникают после употребления лекарственных средств или других продуктов, содержащих триптофан и его метаболиты. Сроки развития заболевания могут сильно различаться - от нескольких дней до 3-5 месяцев после начала приема. Первоначально отмечается повышенная утомляемость и разбитость, которая сменяется выраженными болями в мышцах, усиливающимися при движениях. Одновременно появляются жалобы на слабость мышечной системы - пациент становится неспособен выдерживать привычные для него нагрузки. Миалгия может сочетаться с неприятными ощущениями в области сердца, что свидетельствует о вовлечении в патологический процесс миокарда.
Более чем у половины больных наблюдаются поражения дыхательной системы, проявляющиеся кашлем, хрипами при дыхании, одышкой. Течение патологии иногда осложняется симптомами плеврита - болями в груди при дыхании, усилением сухого кашля. Респираторные нарушения могут сохраняться в течение нескольких недель или даже месяцев. Зачастую определяются отеки подкожной жировой клетчатки на кистях или стопах. В особенно тяжелых случаях возникает накопление жидкости в полостях тела - брюшной, плевральной, перикардиальной. У ряда больных эозинофилией-миалгией отмечаются неврологические симптомы в виде нарушений чувствительности пальцев, кистей, стоп.
Кожные покровы пациента обычно бледные или цианотичные, что говорит о недостаточной оксигенации крови и нарушенной легочной функции. Иногда выявляется поражение суставов, сопровождающееся болями при движениях, отеками, покраснением области сочленения. Но чаще единственным признаком вовлечения суставов в процесс заболевания становится артралгия. Системные нарушения (повышение температуры, лихорадка, головные боли, рвота) возникают только у части больных с данным синдромом.
Для определения синдрома эозинофилии-миалгии используют множество диагностических методик - опрос больного, рентгенографические исследования, общие лабораторные анализы. При возникновении затруднений могут дополнительно производить микроскопическое исследование мокроты, гистологические исследования пораженных тканей. Однозначным признаком патологии является использование пациентом лекарств либо продуктов, содержащих синтезированный свободный триптофан. Поэтапно диагностика состояния производится следующим образом:
- Опрос и сбор анамнеза. При общении с пациентом аллергологу-иммунологу важно выяснить, употреблял ли он в последние дни и недели какие-либо лекарственные средства, масляные продукты, некоторые виды спортивного питания. С учетом этого можно определить, контактировал ли больной с триптофаном и его токсичными метаболитами. Среди жалоб наиболее часто отмечаются одышка, боли в разных группах мышц, слабость.
- Рентгенологические исследования. На рентгенографии органов грудной клетки можно выявить признаки уплотнения легочной ткани в виде сетчато-узелкового или сетчатого поражения. Там же обнаруживаются признаки плеврита и изменения контуров сердца при гидроперикарде. Рентгенография не является основным методом диагностики, поскольку патологические изменения выявляются лишь в 20% случаев синдрома.
- Лабораторные анализы. В общем анализе крови определяется выраженная эозинофилия - до 1000/мкл. Нередко регистрируются признаки воспалительной реакции - увеличение СОЭ, лейкоцитоз.
- Гистологическое изучение. Для диагностики патологии могут производить биопсию легких (при респираторных нарушениях), мышц и фасций (при миалгии) и других тканей в зависимости от клинической картины. Гистологическое исследование тканей пораженных органов выявляет инфильтрацию кровеносных сосудов мелкого калибра моноцитами, эозинофилами, лимфоцитами.
Лечение синдрома эозинофилии-миалгии
Основным условием успешного лечения заболевания является исключение триптофан-содержащего препарата или продукта, вызвавшего патологический процесс. Поэтому в ходе диагностики важно определить, откуда больной получает провоцирующие вещества. Для уменьшения симптомов назначаются кортикостероидные средства, обладающие выраженным противовоспалительным действием. Схема и длительность их использования зависит от конкретной клинической ситуации. Примерно у половины пациентов симптомы патологии исчезают через несколько дней после начала лечения, тогда как у других сохраняются на протяжении 2-3 недель.
Симптоматические мероприятия требуются редко, при сильном кашле могут применяться лекарства, уменьшающие активность кашлевого центра. Отеки устраняют посредством использования диуретических препаратов. Антигистаминные средства не используют по причине их неоднозначного и слабого эффекта при данной патологии. Иногда назначают поддерживающее лечение с использованием поливитаминных препаратов.
Прогноз синдрома эозинофилии-миалгии условно благоприятный при раннем обнаружении и своевременном обращении к специалисту. После исключения провоцирующего вещества и проведения кортикостероидной терапии симптомы исчезают без последствий. В случае длительного течения в легких могут развиваться склеротические процессы, снижающие жизненную емкость и поверхность газообмена. Это приводит к одышке при умеренной физической нагрузке, цианотичности кожи и прочим нарушениям. Профилактика синдрома заключается в отказе от использования препаратов, содержащих триптофан, особенно сомнительного происхождения. Следует как можно быстрее отменить прием таких средств, если на фоне их применения возникает болезненность мышц, кашель, одышка.
Эозинофильная пневмония ( Легочная эозинофилия , Пневмония Лёффлера , Синдром Лера-Киндберга , Эозинофильный летучий инфильтрат легкого )
Эозинофильная пневмония - это аллерго-воспалительное поражение легочной ткани, сопровождающееся образованием неустойчивых мигрирующих инфильтратов эозинофильной природы и развитием гиперэозинофилии. Заболевание обычно протекает с недомоганием, субфебрилитетом, небольшим сухим кашлем, иногда со скудной мокротой; при острой форме - с болью в груди, миалгией, развитием острой дыхательной недостаточности. Установить эозинофильную пневмонию позволяют данные рентгенографии и КТ легких, общего анализа крови, бронхоальвеолярного лаважа, аллергопроб, серодиагностики. Основу лечения составляют специфическая гипосенсибилизация и гормональная терапия.
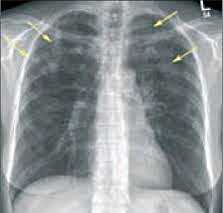
Эозинофильная пневмония (эозинофильный «летучий» инфильтрат легкого) - респираторное заболевание, связанное с патологическим накоплением эозинофилов в альвеолах и повышением их уровня в крови и мокроте. Эозинофильная пневмония чаще диагностируется у населения и туристов в странах с тропическим климатом (Индонезии, Индии, Малайзии, тропической Африке, Ю. Америке).
Эозинофильная пневмония протекает по типу долевой пневмонии или бронхопневмонии, затрагивает обычно верхние отделы легких. Отмечается очаговое или диффузное воспаление альвеол, интерстициальной ткани, сосудов, бронхиол с их обильной инфильтрацией эозинофилами. Типичен преходящий характер инфильтратов с полным регрессом без вторичных рубцовых и склеротических изменений тканей.
Выделяют 3 формы легочной эозинофилии - простую (пневмония Лёффлера), острую и хроническую (синдром Лера-Киндберга). На хронизацию процесса указывают длительное (>4 недель) сохранение и рецидивирование эозинофильных инфильтратов. Эозинофильной пневмонией одинаково часто болеют лица обоего пола, преимущественно в 16-40-летнем возрасте; хроническая форма чаще развивается у женщин, страдающих бронхиальной астмой.
Эозинофильное поражение легочной ткани инициируют патогены инфекционно-аллергической и аллергической природы, вызывающие сенсибилизацию организма пациента. В качестве них могут выступать:
- Паразитарная (глистная) инвазия. В 1932 г Лёффлер впервые определил роль гельминтов в этиологии эозинофильной пневмонии, возникающей при транзиторном повреждении легочной ткани в процессе миграции личинок паразитов через легкие. К появлению пневмонии Лёффлера может привести практически любой гельминтоз - аскаридоз, стронгилоидоз, шистосомоз, анкилостоматоз, парагонимоз, токсокароз, трихинеллез и др. Довольно часто при легочной эозинофилии выявляются нематоды Toxocara cati и T. canis, аскариды собак и кошек. Личинки и яйца глистов могут попадать в ткань легких с током крови, взрослые паразиты (Paragonimus westermani) - через кишечную стенку, диафрагму и плевру, вызывая эозинофильное воспаление с образованием инфильтратов.
- Ингаляционные и лекарственные аллергены. Эозинофильная пневмония может быть результатом аллергической реакции на прием медикаментов (пенициллина, ацетилсалициловой кислоты, сульфаниламидов, нитрофуранов, изониазида, гормональных и рентгенконтрастных препаратов, соединений золота), на контакт с химическими агентами на производстве (солями никеля), цветочной пыльцой (ландыша, лилии, липы). Пневмония Леффлера может быть проявлением сывороточной болезни, иметь связь с аллергией на туберкулин.
- Грибковая инфекция. Атопическая сенсибилизация дыхательного тракта к спорам грибов (особенно, рода Aspergillus) также способствует развитию эозинофильных легочных инфильтратов.
Развитие эозинофильной пневмонии опосредовано реакциями гиперчувствительности немедленного типа. Помимо гиперэозинофилии в крови пациентов часто выявляется повышенный уровень IgE (гипериммуноглобулинемия). За образование аллерго-воспалительных очагов в легочной ткани ответственны тучные клетки, активированные иммунными (IgE) и неиммунными (гистамином, системой комплемента) механизмами и продуцирующие медиаторы аллергии (главным образом, эозинофильный хемотаксический фактор анафилаксии). В ряде случаев эозинофильная пневмония развивается за счет выработки преципитирующих антител к антигенам (реакции по типу феномена Артюса).
Симптомы эозинофильной пневмонии
Клиническая картина бывает весьма вариабельной. Аллергическое воспаление легких может иметь бессимптомное течение с отсутствием или очень скудной выраженностью жалоб и определяться только рентгенологическим и клинико-лабораторным методом. Часто пневмония Лёффлера протекает с минимальными проявлениями, манифестируя симптомами катарального ринофарингита. Больные ощущают легкое недомогание, слабость, повышение температуры до субфебрильной, небольшой кашель, чаще сухой, иногда с незначительной вязкой или кровянистой мокротой, болезненность в области трахеи.
При массивном гематогенном распространении яиц и личинок глистов в организме присоединяется сыпь на коже, зуд, одышка с астматическим компонентом. Эозинофильная инфильтрация других органов сопровождается легкими, быстро исчезающими признаками их поражения - гепатомегалией, симптомами гастрита, панкреатита, энцефалита, моно- и полиневропатией.
Острая эозинофильная пневмония протекает тяжело, с интоксикацией, фебрилитетом, болью в груди, миалгией, быстрым (в течение 1-5 суток) развитием острой дыхательной недостаточности, респираторного дистресc-синдрома. Для хронической формы типично подострое течение с потливостью, потерей массы тела, нарастанием одышки, развитием плеврального выпота.
Эозинофильная пневмония обычно длится от нескольких дней до 2-4 недель. Выздоровление может наступать спонтанно. При хронической форме продолжительное существование инфильтратов и рецидивы способствуют постепенному прогрессированию заболевания, развитию легочного фиброза и дыхательной недостаточности.
Диагностика эозинофильной пневмонии включает проведение рентгенографии и КТ легких, общего анализа крови, анализа кала на яйца глист, бронхоальвеолярного лаважа, аллергопроб, серологических (РП, РСК, ИФА) и клеточных тестов (реакции дегрануляции базофилов и тучных клеток). Пациенты с эозинофильной пневмонией, как правило, имеют предшествующий аллергологический анамнез. Аускультация определяет небольшое количество влажных мелкопузырчатых хрипов или крепитацию. При обширных инфильтратах заметно укорочение легочного звука при перкуссии. Инструментально-лабораторный комплекс:
- Рентгенография легких. На снимках видны субплеврально расположенные одиночные (реже множественные, двусторонние) нечеткие затемнения средней интенсивности неправильной формы размером до 3-4 см. В окружении инфильтрата легочный рисунок усилен, тень корня легкого слегка расширена. Характерна быстрая динамика инфильтратов с миграцией по легочным полям и исчезновением не позднее 1-2 недель после обнаружения (чаще через 1-3 дня) без остаточной рубцовой деформации. При длительно поддерживающемся инфильтративном воспалении в ткани легких могут образоваться фиброзные очаги и кистозные полости.
- Лабораторные данные. В периферической крови на начальной стадии заболевания регистрируется лейкоцитоз, гиперэозинофилия (10-25%), при хронизации процесса уровень эозинофилов близок к норме. Часто выявляется высокое содержание в крови IgE (до 1000 МЕ/мл). В анализе лаважной жидкости также появляются эозинофилы (при острой форме - до 40% и более) и кристаллы Шарко-Лейдена. Анализ кала, проводимый с учетом цикла развития паразитов, при некоторых гельминтозах позволяет обнаружить яйца глист. По данным биопсии в альвеолах и интерстиции определяются эозинофилы, лимфоциты и макрофаги, гранулемы, поражение мелких сосудов.
- Аллергопробы. Этиологическая диагностика эозинофильной пневмонии включает провокационные назальные и ингаляционные тесты, кожные пробы с аллергенами пыльцы, гельминтов, спор грибов, серологические анализы. «Никелевая» эозинофильная пневмония обычно сочетается с аллергическим контактным дерматитом и подтверждается положительным компрессным (аппликационным) тестом с никелем.
- ФВД. Бронхиальную проходимость оценивают при проведении спирометрии, бронхомоторных тестов.
Дифференцировать эозинофильную пневмонию необходимо с пневмониями бактериального и вирусного генеза, туберкулезом, синдромом Вайнгартена, альвеолитом, десквамативным интерстициальным фиброзом. При атопической отягощенности показана консультация аллерголога, при респираторном рините - отоларинголога.
Лечение эозинофильной пневмонии
Основным в лечении является устранение действия этиологически значимого фактора: контакта с аллергенами (аэроаллергенами, лекарствами), проведение дегельминтизации. Назначаются антигистаминные препараты, противопаразитарные средства. Имеются случаи спонтанного выздоровления без фармакотерапии. В случае тяжелой глистной инвазии с обезвоживанием организма или невозможности полного изъятия аллергена из окружающей среды лечение проводится стационарно, в отделении пульмонологии.
При острой форме эозинофильной пневмонии применяются глюкокортикоиды, на фоне которых происходит быстрая (в течение 48 часов) регрессия воспаления. Дозу ГК подбирают индивидуально и снижают постепенно во избежание обострения. В тяжелых случаях требуются ИВЛ, длительная гормональная терапия. При бронхообструкции показаны ингаляционные ГК, бета-адреномиметики. Для лучшего отхождения мокроты используются отхаркивающие средства, дыхательная гимнастика. Проводится лечение сопутствующей бронхиальной астмы.
Прогноз эозинофильной пневмонии в целом благоприятный, возможно самопроизвольное разрешение инфильтратов. Правильное лечение и наблюдение пульмонолога позволяет избежать хронизации процесса и рецидивов. Профилактика эозинофильной пневмонии сводится к мерам гигиены, предотвращающим заражение организма гельминтами, контролю за приемом медикаментов, ограничению контакта с аэроаллергенами, проведению специфической гипосенсибилизации. При необходимости рекомендуется смена места работы.
2. Легочные эозинофилии: диагностика, подходы к терапии/ Э.Х.Анаев, А.Г.Чучалин// Пульмонология. - 2012 -№ 4.
3. Эозинофильная пневмония в практике врача-терапевта: трудности диагностики/ Болдырева Л.Н., Пантелеева Е.Н.//Справочник поликлинического врача. - 2011 - №9.
4. Трудности этиологической диагностики легочной эозинофилии/ Николаева С.С., Растомпахова Т.А.// Сибирский медицинский журнал. - 2011.
Эозинофилия ( по материалам статьи Anna Kovalszki and Peter F. Weller. Prim Care. 2016 Dec; 43 (4): 607-617. ) 2016)
Эозинофилия представляет собой повышенное количество эозинофилов в тканях и / или крови. Подсчет количества эозинофилов в тканях требует биопсии, однако, количество эозинофилов в крови измеряется более легко и регулярно. Абсолютное количество эозинофилов, превышающее от 450 до 550 клеток / мкл, в зависимости от лабораторных стандартов, считается повышенным. Процент, как правило, превышающий 5% от нормы, считается повышенным в большинстве учреждений, хотя абсолютное значение следует рассчитывать до определения эозинофилии. Это делается путем умножения общего количества белых клеток на процент эозинофилов.
Эозинофилы - это клетки, продуцируемые из костного мозга линии гранулоцитов. Они имеют приблизительный период полураспада от 8 до 18 часов в кровотоке и в основном находятся в тканях, где они могут сохраняться в течение по крайней мере нескольких недель. Функциональные роли эозинофилов многогранны и включают представление антигена; высвобождение липидных, пептидных и цитокиновых медиаторов при остром и хроническом воспалении; реакцию на очищение от гельминтов и паразитов путем дегрануляции; и продолжительные гомеостатические иммунные ответы. Они могут быть частью общей клеточной среды при злокачественных новообразованиях и аутоиммунных заболеваниях, а также при заболеваниях соединительной ткани.
Легкая эозинофилия часто встречается у пациентов с аллергическим заболеванием ( 1500 клеток / мкл ). Аллергический ринит и астма часто вызывают легкую эозинофилию. Атопический дерматит может вызывать более значительную эозинофилию, если он поражает большую часть тела и связан со значительной атопией. Эозинофильный эзофагит, а также другие эозинофильные желудочно-кишечные заболевания могут вызывать легкую периферическую эозинофилию. Хронический синусит, особенно полиповидной разновидности, наблюдаемой при респираторном заболевании, обостренном аспирином, вызывает более выраженный эозинофильный ответ, который может быть в диапазоне от легкой до умеренной. Часто эти пациенты начинают с аллергии на нос и астмы, но затем развивают аномальные каскады, метаболизирующие арахидоновую кислоту, и, следовательно, имеют более драматическое течение заболевания, так и большую выраженность эозинофилии.
Аллергический бронхолегочный аспергиллез, связанный как с грибком (Aspergillus), так и с сенсибилизацией у аллергического / астматического хозяина, может также вызывать различные и иногда значительные степени эозинофилии, а также повышенный общий иммуноглобулин (Ig) E. Хроническая эозинофильная пневмония часто начинается у сенсибилизированного, астматического организма человека. Хотя эти пациенты могут иметь более легкую периферическую эозинофилию в начале заболевания, они часто демонстрируют более умеренную эозинофилию в дальнейшем. У них также есть жидкость бронхоальвеолярного лаважа, которая содержит по крайней мере 40% эозинофилов в до 80% случаев. Эта форма эозинофильной пневмонии может быть предвестником более позднего развития эозинофильного васкулита, эозинофильного гранулематоза с полиангиитом (EGPA), ранее известного как васкулит Churg-Strauss.
Аллергия на лекарства может вызывать эозинофилию от легкой до тяжелой степени, часто быстро нарастает и остепенно замедляется; эозинофилия от аллергии на лекарства может пройти за несколько месяцев. Обычно есть, хотя и не всегда, связанная лекарственная сыпь диффузного / макулопапулезного характера. Пациенты могут также иметь бессимптомную эозинофилию из-за лекарств, особенно пенициллинов, цефалоспоринов или хинолонов. Легочные инфильтраты и периферическая эозинофилия связаны с различными препаратами, включая нестероидные противовоспалительные препараты, сульфаниламидные препараты и нитрофурантоин. Лекарственные заболевания других органов также могут вызывать эозинофилию тканей и крови (например, интерстициальный нефрит, вызванный лекарственными препаратами).
Лекарственная сыпь с синдромом эозинофилии и системных симптомов (DRESS) часто вызывает значительное повышение эозинофилов в дополнение к нарушениям функции печени, нарушению регуляции температуры и лимфаденопатии. В обзорах стационарных больных в Бразилии и Малайзии синдром DRESS был вызван главным образом антибиотиками, противоэпилептическими препаратами (карбамазепин, фенитоин, ламотриджин, вальпроевая кислот) , лекарствами против подагры (аллопуринол) , антиретровирусными препаратами (невирапин, эфавиренц) и нестероидными противовоспалительными препаратами (ибупрофен) . Синдром Стивенса-Джонсона и токсический эпидермальный некролиз, тяжелые и опасные для жизни формы лекарственной аллергии, обычно не вызывают эозинофилию, а скорее нейтрофилию и лимфоцитопению.
Гельминты, обитающие в тканях (глисты), - это паразитарные инфекции, которые часто вызывают эозинофилию легкой или средней степени тяжести. Инфекция Strongyloides является распространенной причиной, в то время как Giardia, паразит просвета, не вызывает эозинофилию.
Выделяют глистные инфекции , вызывающие эозинофилию:
Нематоды
Висцеральная личинка мигранта
филариоз
Тропическая легочная эозинофилия
плавники
Протозойные инфекции
В России паразиты, которых можно заразить без каких-либо поездок в зарубежные страны, включают стронгилоиды, трихинеллы, аскариды, анкилостомы и мигрирующих личинок внутренних органов (Toxocara от собак / кошек). При оценке состояния пациента на предмет возможной глистной этиологии эозинофилии необходимо проводить тестирование на стронгилоиды, поскольку, уникальное среди гельминтов, оно может сохраняться даже спустя десятилетия после первоначальной инфекции. Стронгилоиды могут быть бессимптомными или вызывать мимолетные расстройства, дерматографию, ангионевротический отек и / или боль в животе. Если пациент с недиагностированной стронгилоидной инфекцией получает высокие дозы системных кортикостероидов, может развиться диссеминированный стронгилоидоз. Это иногда связано с кишечным бактериальным сепсисом и может быть смертельным. Анализ иммуноферментного антитела на ферментативную связь является чувствительным тестом на стронгилоиды. Исследования кала на личинки нечувствительны. Серологические или другие доказательства продолжающегося стронгилоидоза заслуживают лечения ивермектином, особенно у пациентов с эозинофилией, которых в конечном итоге можно лечить кортикостероидами.
Некоторые грибы, такие как кокцидиоидомикоз (как острый, так и хронический), диссеминированный гистоплазмоз (реже эозинофильный) и криптококкоз (особенно при инфекциях центральной нервной системы) также связаны с эозинофилией. Coccidioides встречается на юго-западе США, а также в Мексике, Центральной и Южной Америке. Гистоплазма загрязняет птичий и летучий помет, поэтому исследование пещер и проживание в районах с большой популяцией голубей может привести к значительному поражению. Криптококк встречается в почве по всему миру. Эти инфекции часто более значительны и распространяются у людей с ослабленным иммунитетом.
Ретровирус, человеческий Т-клеточный лимфоцитарный вирус-1, является одним из немногих вирусов, связанных с эозинофилией. Он распространен в Японии, Африке, на Карибских островах и в Южной Америке, а также недавно обнаружен в Восточной Европе и на Ближнем Востоке. У пациентов, инфицированных вирусом иммунодефицита человека-1, может быть эозинофилия, не связанная напрямую с инфекцией, но вызванная вторичными явлениями (лекарственная аллергия, эозинофильный фолликулит).
В отличие от «правила», согласно которому только глистные паразиты могут вызывать эозинофилию, существуют 3 простейших, которые могут вызывать периферическую эозинофилию. Isospora belli и Dientamoeba fragilis , как кишечные простейшие, так и саркоцистит, редкие обитающие в тканях простейшие, обнаруживаются только у тех, кто подвергается воздействию в районах Юго-Восточной Азии.
EGPA, ранее известный как синдром Churg-Strauss, возникает, как правило, у атопического индивидуума и вызывает различные заболевания пазух, заболеваний легких и почек, а также может вызывать множественный мононеврит и сосудистые заболевания. EGPA ассоциируется со значительной эозинофилией, повышенными маркерами воспаления и тканевой эозинофилией в пораженных областях. Он имеет общее в дифференциальном диагнозе и разделяет многие аспекты с гиперэозинофильными синдромами. Васкулит часто выявляется на поздних стадиях заболевания, особенно если почка не поражена. EGPA с эозинофилией и преимущественно негеморрагическими проявлениями в легких имеет значительно более низкую распространенность позитивности антинейтрофильных цитоплазматических антител (перинуклеарных антинейтрофильных цитоплазматических антител), чем EGPA с вовлечением почек. EGPA вызывает эозинофилию и симптомы, несопоставимые с обычными аллергическими осложнениями, с поражением пазух, легких и других органов. В первоначальной оценке пациентов с возможным EGPA в последних согласованных рекомендациях от 2015 года предлагается серологическое тестирование на токсокароз и вирус иммунодефицита человека, специфические IgE и IgG для Aspergillus spp., Поиск Aspergillus spp. в мокроте и / или жидкости бронхоальвеолярного лаважа (для оценки аллергического бронхолегочного аспергиллеза), триптазы и витамина B12 уровни (для оценки миелопролиферативного гиперэозинофильного синдрома), мазок периферической крови (для выявления диспластических эозинофилов или бластов, наводящих на мысль о первичном эозинофильном процессе костного мозга) и компьютерная томография грудной клетки (для оценки поражения легких). Дополнительная проработка должна руководствоваться презентацией. Рекомендуется направление для более конкретной оценки квалифицированным ревматологом или иммунологом в центр, который лечит пациентов с васкулитом, учитывая стертый характер EGPA, а также клинические последствия, если он недостаточно пролечен.
Соединительная ткань / аутоиммунные заболевания в различной степени могут быть связаны с периферической эозинофилией. Эозинофилы присутствуют как часть общей воспалительной среды, даже если они не являются типами клеток, вовлеченных в патогенез заболевания. Степень эозинофилии в этих случаях не установлена. Например, в ретроспективном анализе было выявлено, что легкие степени эозинофилии связаны с определенными ревматическими расстройствами, но авторы считают, что лечение нестероидными противовоспалительными препаратами и кортикостероидами нарушает частоту обнаруженной эозинофилии. В одном случае тяжелого ревматоидного артрита было отмечено до 24 000 эозинофилов / мм. 3
При воспалительных заболеваниях кишечника уровень эозинофилов в крови может быть повышен, однако роль эозинофилов в желудочно-кишечных заболеваниях все еще выясняется. Например, уровни эозинофил-рекрутирующего хемокина, эотаксина-1, в тканях коррелировали с тканевой эозинофилией пациентов с язвенным колитом в активном состоянии заболевания. При саркоидозе легкая периферическая эозинофилия была обычным явлением, даже без других атопических заболеваний, присутствующих в ретроспективной когорте пациентов с саркоидозом. При заболевании, связанном с IgG4, относительно недавно признанном, о котором известно, что он вызывает инфильтрацию тканей и опухолевидное разрушение определенных желез, органов и лимфатических узлов, эозинофилия в крови может присутствовать примерно в 25%, и повышение уровня IgE и эозинофилия в крови от легкой до умеренной степени встречаются также. Несмотря на то, что эти расстройства в некоторой степени могут быть связаны с эозинофилией, часто пациенты принимают много лекарств, и необходимо исключить более распространенные причины эозинофилии, такие как лекарственная аллергия.
Эозинофилия, связанная с соединительной тканью, ревматологические и аутоиммунные заболевания
Читайте также:
