Папиллит - причины, симптомы, диагностика и лечение
Добавил пользователь Дмитрий К. Обновлено: 01.02.2026
Почечный папиллярный некроз — это разрушение сосочков почек, обусловленное ишемией мальпигиевых пирамид. Проявляется эпизодами почечных колик, тянущими болями в пояснице, гематурией, отхождением некротизированных сосочков. Диагностируется с помощью общего и бактериологического анализа мочи, экскреторной урографии, уретеропиелоскопии. Для лечения назначают антибактериальную терапию, периферические вазодилататоры, антикоагулянты, антиагреганты, мембраностабилизаторы, антиоксиданты, гемостатики, венотоники. При необходимости выполняют катетеризацию и стентирование мочеточника, лоханок, декапсуляцию почки, нефростомию, частичную и тотальную нефрэктомию.
МКБ-10
Общие сведения
Заболевание впервые было описано в 1877 году немецким терапевтом и патологом Николаусом Фридрейхом. Папиллярный почечный некроз (некротический папиллит, некроз почечных сосочков), по разным данным, диагностируется у 0,3-1% пациентов урологических и нефрологических стационаров. У страдающих пиелонефритом распространенность патологии достигает 3%.
Женщины заболевают вдвое чаще мужчин. В половине случаев папиллярный некроз возникает в 30-40-летнем возрасте. У 75% пациентов некротический папиллит развивается хронически с постепенным прогредиентным нарастанием почечной дисфункции. В 58% случаев воспалительно-деструктивный процесс является двухсторонним. По результатам наблюдений, ишемическая деструкция верхней части мальпигиевых пирамид ассоциирована с сахарным диабетом и серповидно-клеточной анемией, однако в последние годы все чаще возникает при других патологических состояниях.
Причины
Некротический папиллит является полиэтиологическим заболеванием, развивающимся на фоне других патологических состояний или приема нефротоксичных веществ. Предпосылкой к возникновению некроза считаются особенности анатомического строения медуллярного вещества - гипоксии почечных сосочков способствует сочетание относительно бедной васкуляризации анатомической структуры и высокого осмотического давления в данной зоне. Специалистами в сфере современной урологии и нефрологии установлено несколько групп причин, вызывающих папиллярную деструкцию:
- Нарушение кровоснабжения мозгового вещества. Недостаточное поступление крови к сосочковому аппарату наблюдается при изменениях сосудистой стенки у пациентов с атеросклерозом, сахарным диабетом, васкулитами. Ишемию папиллярных структур провоцируют заболевания, при которых возможен тромбоз почечных микрососудов, чаще всего некротическим папиллитом осложняется серповидно-клеточная анемия, реже — коагулопатии, ДВС-синдром и другие гиперкоагуляционные состояния.
- Повышение внутрилоханочного давления. При обструкции мочевыводящих путей нарушается отток мочи с ее накоплением в лоханочной системе. Возникающий пиелоренальный рефлюкс способствует обсеменению почечных сосочков бактериями, которые содержатся в урине, и началу воспалительной реакции. В большинстве случаев лоханочная гипертензия формируется при обтурации мочеточника камнем, новообразованием, случайной перевязке во время операции, наличии уретеровагинального свища.
- Гнойные заболевания почек. Вторичное воспаление верхушек почечных пирамид осложняет течение тяжелых гнойно-деструктивных процессов. Массивное размножение инфекционных патогенов, выделяющих протеолитические экзотоксины, способствует образованию гнойных инфильтратов и расплавлению паренхимы почек, вовлечению в процесс деструкции сосочков. Папиллярный некроз может развиться на фоне пиелонефрита, апостематозного нефрита, пионефроза, почечного карбункула, абсцесса.
- Лекарственная нефропатия. Длительный неконтролируемый прием некоторых безрецептурных анальгетиков и антипиретиков приводит к нарушению медуллярного кровотока, ухудшению перфузии коркового и мозгового слоя и развитию анальгетической нефропатии. В наиболее тяжелых случаях на фоне выраженных изменений прямых сосудов, питающих почечные сосочки, возникает их грубая ишемическая деструкция. НПВС также оказывают прямой токсический эффект на мозговое вещество почек, что усугубляет папиллярные некротические процессы.
Патогенез
Существует три основных патогенетических механизма развития почечного папиллярного некроза — ангиопатический, вазокомпрессионный, инфекционный, которые зачастую сочетаются между собой, приводя к ишемическому инфаркту мозгового слоя с его последующим гнойным расплавлением и отторжением некротизированных масс. Уменьшение просвета сосочковых артериол вследствие утолщения интимы, уплотнения стенки, сдавления гнойными очагами или инфильтрированным мочой интерстицием, полная обтурация их просвета тромбами способствуют возникновению ишемии и деструкции тканей.
Ситуация усугубляется сужением диаметра сосудов, кровоснабжающих сосочки, по направлению к вершине, что повышает вязкость поступающей крови. Дополнительным фактором, усиливающим ишемические процессы при обструкции мочевыделительных органов, становятся воспаление и венозная гиперемия жировой клетчатки, в которую проникает моча. Ишемизированный сосочек может подвергаться полной или частичной деструкции с повреждением отдельных участков по центру или периферии. В тяжелых случаях некротизируется вся мальпигиева пирамида, при множественной локализации — медуллярный слой пораженной почки на всем протяжении. При присоединении инфекции некротический процесс осложняется воспалительной реакцией.
Классификация
Систематизация форм папиллярного некроза учитывает механизм и динамику развития заболевания, выраженность клинической симптоматики. Специалисты-нефрологи различают первичный некротический папиллит, возникающий в результате нарушения кровоснабжения без предшествующей инфекционно-воспалительной патологии, и вторичный, обусловленный ишемией мозгового вещества на фоне воспалительно-склеротических изменения паренхимы и почечного синуса.
При изначальном поражении сосочка говорят о папиллярной форме деструкции, при первичном формировании очаговых инфарктов во внутренней мозговой зоне с последующим вовлечением верхушек мальпигиевых пирамид — о медуллярной. С учетом особенностей течения выделяют:
- Острый папиллярный некроз. Заболевание отличается бурной клинической картиной, выраженной интоксикацией, неоднозначным прогнозом. Острое течение более характерно для папиллитов, осложнивших пиелонефрит, другие гнойные нефрологические заболевания, нефролитиаз.
- Хронический папиллярный некроз. Обычно симптомы выражены слабо, неспецифичны. Возможно рецидивирующее течение. Зачастую хронический папиллит выявляется при ангиопатиях, серповидно-клеточной анемии и диагностируется только после тщательного обследования пациента.
Симптомы почечного папиллярного некроза
Клиническая картина заболевания характеризуется разнообразием признаков, большинство из которых являются неспецифичными. Часто при папиллярном некрозе встречается почечная колика вследствие отделения некротизированного сосочка, которая может сопровождаться тошнотой, рвотой, задержкой стула. Типичны постоянные тянущие боли в поясничной области, выделение крови с мочой.
У пациентов наблюдается интоксикационный синдром различной степени выраженности: субфебрильная или фебрильная лихорадка, ознобы, головная боль, повышенная потливость, слабость. Патогномоничный признак некротического папиллита, обнаруживающийся только на поздней стадии болезни, — выделение с мочой омертвевших участков почечной паренхимы в виде сероватых масс с включениями солей извести. При хроническом течении могут преобладать лабораторные симптомы при маловыраженной или отсутствующей клинической симптоматике.
Осложнения
В случае присоединения бактериальной инфекции возникает апостематозный пиелонефрит, проявляющийся образованием небольших гнойников в корковом слое почки. При обширном поражении выявляется клиническая картина острой почечной недостаточности - олигурия или анурия, повышение уровня мочевины и креатинина плазмы, нарушение сознания вследствие азотемии.
Хроническое течение некротического папиллита зачастую приводит к ХПН, которая осложняется развитием декомпенсированного метаболического ацидоза и полиорганной недостаточности. В 40% случаев у пациентов диагностируется почечнокаменная болезнь с высоким риском образования коралловидных камней. Массивный папиллярный некроз часто сопровождается профузными кровотечениями, которые представляют опасность для жизни больного и требуют неотложной помощи.
Диагностика
Из-за полиморфности клинической картины и отсутствия патогномоничных признаков на ранних стадиях заболевания постановка диагноза зачастую затруднена. Сложности в диагностике также обусловлены скрытым развитием почечного папиллярного некроза на фоне другой патологии мочевыделительной системы (пиелонефрита, нефролитиаза). План обследования пациента с подозрением на некротический папиллит включает следующие лабораторные и инструментальные методы:
- Клинический анализ мочи. Для папиллярного некроза характерны микро- и макрогематурия, лейкоцитурия, бактериурия, появление клеток Штернгеймера-Мальбина. На поздних стадиях обнаруживаются некротические массы в виде кусочков ткани серого цвета продолговатой или треугольной формы. Метод дополняют бактериологическим исследованием мочи с определением чувствительности флоры.
- Внутривенная урография. На снимках полученных при экскреторной урографии, просматриваются смазанные очертания зоны форникса, мелкие тени кальцификатов, кольцевидная тень в просвете почечной лоханки, форникально-медуллярные свищи. При полном отторжении сосочка на рентгенограмме выявляется дефект наполнения. Характерный признак тотального некроза - затекание контраста в паренхиму почек (симптом «пламени костра»).
- Уретеропиелоскопия. Для проведения нефроскопии используют гибкий эндоскоп, который вводят ретроградно (через уретру) или антеградно (через брюшную стенку), что позволяет оценить состояние мочеточников и чашечно-лоханочной системы почек. При папиллите наблюдаются множественные деструкции почечных сосочков, что нередко сопровождается кровотечением из форникальной зоны.
В клиническом анализе крови при папиллярном почечном некрозе определяются признаки бактериального воспаления: нейтрофильный лейкоцитоз с повышением числа палочкоядерных клеток, увеличение СОЭ. Для комплексной оценки состояния мочевыделительной системы выполняют УЗИ и КТ почек и других органов забрюшинного пространства. Эти методы менее информативны в диагностике некроза почечных сосочков, но позволяют выявить сопутствующие патологические состояния — мочекаменную болезнь, пиелонефрит.
Дифференциальная диагностика некротического папиллита проводится с острым и хроническим пиелонефритом, туберкулезом почек, нефролитиазом, аномалиями развития (медуллярной гипоплазией, почечной дисплазией, тубуломедуллярной дилатацией), гидронефрозом, лоханочно-почечным рефлюксом, злокачественными новообразованиями. Кроме наблюдения уролога или нефролога пациенту может потребоваться консультация онколога, инфекциониста, эндокринолога, гематолога.
Лечение почечного папиллярного некроза
Выбор врачебной тактики определяется причинами возникновения и особенностями течения некротического папиллита. По возможности лечение должно быть этиопатогенетическим, направленным на коррекцию первичного расстройства, которое осложнилось папиллярным некрозом, восстановление нормальной гемоперфузии почечной паренхимы, борьбу с уроинфекцией. При остром течении важную роль играет купирование возникших симптомов — почечной колики, окклюзии лоханок и мочеточника некротическими массами, кровотечения из поврежденных сосочков.
Комбинированная терапия острого папиллярного почечного некроза предусматривает стандартную схему лечения основного заболевания, на фоне которого развился папиллит, в сочетании с такими медикаментозными средствами и инвазивными методами, как:
- Антибактериальные препараты. Антибиотикотерапия по возможности назначается с учетом чувствительности возбудителя, вызвавшего воспалительный процесс. Наиболее эффективным является применение уроантисептиков без нефротоксического действия — фторхинолонов, нитрофуранов, цефалоспоринов, фосфомицинов, макролидов, производных налидиксовой и пипемидиновой кислот.
- Средства для улучшения почечной гемодинамики. При выборе медикамента учитывают причины ишемии. В качестве базовых рекомендованы периферические вазодилататоры, которые при необходимости дополняют прямыми антикоагулянтами, антиагрегантами. Вспомогательными препаратами являются антиоксиданты и мембраностабилизаторы, повышающие ишемическую стойкость папиллярных структур.
- Гемостатическая терапия. Средства для остановки кровотечения показаны при преобладании в клинической картине признаков выраженной и массивной гематурии. Обычно применяются свежезамороженная или антигемофильная плазма, препараты аминокапроновой кислоты, ингибиторы фибринолиза, аналоги этамзилата. Использование гемостатиков ограничено при папиллярных некрозах, вызванных тромбозами.
- Удаление некротических масс. Если отторгающаяся ткань сосочков вызывает окклюзию почечных лоханок и мочеточников, производится их катетеризация. Последующее стентирование мочеточника позволяет уменьшить лоханочную гипертензию и обеспечить нормальный пассаж мочи. Некротические массы также могут удаляться ходе уретероскопии, ретроградной или чрескожной нефроскопии (пиелоскопии).
При нарастании симптоматики на фоне проводимой консервативной терапии, возникновении терапевтически резистентного острого пиелонефрита, длящегося более 2-3 дней, некупируемой профузной гематурии рекомендовано оперативное лечение. При двухстороннем некротическом процессе предпочтительны органосохраняющие вмешательства — нефростомия, декапсуляция почки, резекция (частичная нефрэктомия) для удаления участка с кровоточащими папиллярными структурами. Радикальная нефрэктомия выполняется только при одностороннем папиллите с тотальным необратимым некрозом медуллярного слоя и достаточной функциональностью контрлатеральной почки.
Прогноз и профилактика
При ранней диагностике и проведении патогенетической терапии возможна регенерация эпителия с восстановлением всех функций почек. Прогноз при некрозе почечных сосочков относительно благоприятный. Благодаря использованию современных антибактериальных препаратов летальность при остром некротическом папиллите удалось сократить с 50% до 10%.
Профилактика папиллярного некроза заключается в своевременном лечении инфекционных процессов мочевыделительной системы, нефролитиаза, системных васкулитов, токсических поражений почек, обоснованном назначении НПВС. Важное звено в предупреждении заболевания — диспансерное наблюдение за пациентами из группы риска с тщательным медикаментозным контролем сахарного диабета, серповидно-клеточной формы анемии.
1. Инфекции мочевыводящих путей у больных сахарным диабетом/ Е.В. Хайкина, Г.К. Решедько, М.В. Морозов// Клиническая микробиология антимикробная химиотерапия. - 2008 - Т.10, №3.
2. Острый папиллярный некроз почек у девочки 5 лет/Т.А. Романова, И.Г. Винжего, А.П. Ничипоренко и др.// Научные ведомости БелГУ. Сер. Медицина. - 2004.
3. Лекарственные поражения почек/ С.С. Постников, А.Н. Грацианская, М.Н. Костылева// Детская нефроурология. - 2016.
Туберкулез почек ( Нефротуберкулез )
Туберкулез почек - это внелегочная инфекция, вызываемая микобактериями туберкулеза и поражающая почечную паренхиму. Клиника неспецифична, может включать недомогание, субфебрилитет, боли в пояснице, макрогемматурию, дизурию. Туберкулез почек диагностируется с помощью лабораторных анализов мочи, туберкулинодиагностики, УЗИ почек, урографии, ретроградной уретеропиелографии, нефросцинтиграфии, морфологического исследования. Лечение предусматривает назначение специфической противотуберкулезной терапии; при деструктивном процессе в почках может потребоваться выполнение кавернэктомии или нефрэктомии.
Среди органных внелегочных поражений туберкулез почек (нефротуберкулез) является наиболее распространенной формой заболевания и встречается в урологии в 30-40% наблюдений. Первоначально происходит поражение коркового слоя органа. Дальнейшее прогрессирование инфекции сопровождается распадом тканей, образованием полостей и каверн в почечной паренхиме, нарушением функционирования почек. В тяжелых случаях наблюдается развитие туберкулезного пионефроза (гнойного расплавления почечной ткани), вовлечение в инфекционный процесс лоханки, мочеточника, мочевого пузыря, половых органов.
При туберкулезе почек достаточно часто развивается генитальный туберкулез, поражающий у мужчин простату, яички, придатки яичек (туберкулезный простатит, орхит, эпидидимит); у женщин - придатки, фаллопиевы трубы, матку (туберкулезный сальпингоофорит, сальпингит, эндометрит).
Возбудителями туберкулеза почек являются микобактерии туберкулеза (М. tuberculosis). Как правило, патология возникает у пациентов с запущенным легочным или костным туберкулезом после 3-10 лет течения первичного туберкулезного процесса. Развитие заболевания, как правило, происходит на фоне имеющихся местных инфекционных или уродинамических процессов - хронического пиелонефрита, камней почек и др.
Проникновение инфекции в почку происходит преимущественно гематогенным путем. Попадая с током крови в клубочковый аппарат, микобактерии формируют множественные мельчайшие туберкулезные очаги. При хорошей местной и общей устойчивости к инфекции и малых размерах первичных очагов, последние могут подвергаться полному обратному развитию. При расстройствах уродинамики и гемодинамики, а также сниженных защитных силах из коркового слоя инфекция распространяется в мозговое вещество, вызывая специфическое воспаление почечных сосочков - туберкулезный папиллит.
По мере дальнейшего развития туберкулеза в процесс вовлекается вся толща почечных пирамид, происходит казеозный распад последних, что сопровождается образованием изолированных или сообщающихся с чашечно-лоханочными комплексами каверн. Прогрессирование туберкулеза почек может привести к формированию в почечной паренхиме множественных полостей (поликавернозная форма) и развитию пионефроза. Последующее заживление каверн протекает с обызвествлением казеозных очагов, в которых, однако, могут сохраняться жизнеспособные микобактерии туберкулеза.
Вторичное вовлечение мочевого пузыря, мочеточников и чашечно-лоханочных комплексов связано с лифогенным или уриногенным механизмом распространения туберкулезной инфекции.
В клинической урологии принята классификация, учитывающая клинико-рентгенологические особенности туберкулеза почек. Согласно данной классификации выделяют:
- Туберкулез почечной паренхимы, сопровождающийся образованием множественных очагов в корковом и медуллярном слое почки.
- Туберкулезный папиллит, протекающий с поражением почечных сосочков.
- Кавернозный туберкулез почек, характеризующийся слиянием деструктивных очагов с инкапсуляцией (полостная форма).
- Фиброзно-кавернозный туберкулез почек, сопровождающийся облитерацией чашечек с формированием в них замкнутых деструктивно-гнойных полостей.
- Омелотворение (обызвествление) почки, выражающееся в формировании ограниченных патологических очагов с большим количеством солей кальция (казеом, туберкулем).
Симптомы туберкулеза почек
Патогномоничная симптоматика отсутствует. На ранних стадиях патология может иметь латентное течение или характеризоваться нарушениями общего самочувствия: легким недомоганием, быстрой утомляемостью, субфебрильной температурой, прогрессирующим похуданием. Деструктивные изменения в почках сопровождаются появлением безболевой тотальной гематурии, вызванной эрозией сосудов при изъязвлении почечных сосочков. Кровотечение нередко сменяется пиурией, свидетельствующей о развитии пиелита или пиелонефрита.
При кавернозном туберкулезе почек отмечаются признаки инфекционной интоксикации, боли в пояснице. Болевые ощущения, как правило, выражены умеренно, носят ноющий тупой характер, однако при нарушениях оттока мочи могут прогрессировать до почечной колики. Двустороннее нарушение уродинамики сопровождается признаками хронической почечной недостаточности. При туберкулезном цистите присоединяются дизурические явления - императивные позывы к мочеиспусканию, поллакиурия, странгурия, постоянная боль над лоном, периодическая макрогематурия. В запущенных стадиях болезни нередко развивается артериальная гипертензия.
Учитывая, что туберкулез почек может протекать бессимптомно или в виде различных клинических вариантов, в диагностике первостепенное значение приобретает проведение лабораторных и аппаратно-инструментальных исследований. При подозрении на туберкулез почек показано проведение туберкулиновой пробы и консультация фтизиатра. При сборе анамнеза выясняют факт наличия легочного туберкулеза у самого пациента и его родственников, контакты с туберкулезными больными. У худых больных в ряде случаев удается пропальпировать плотную, бугристую почку. Определяется ярко выраженный симптом Пастернацкого.
Характерными изменениями общего анализа мочи служат стойкая резко кислая реакция, лейкоцитурия, протеинурия, эритроцитурия, пиурия. Достоверно судить о наличии туберкулеза почек позволяет выявление микобактериурии, которая обнаруживается при помощи бактериологического посева мочи или ПЦР-исследования. Проведение ИФА позволяет обнаружить антитела к туберкулезу, гамма-интерферон (квантифероновый тест) или сенсибилизированные Т-клетки (Т-спот.ТБ). В определенных случаях требуется выполнение провокационных тестов с туберкулином. После подкожного введения туберкулезного антигена происходит обострение процесса, что сопровождается выраженной протеинурией, пиурией и микобактериурией.
УЗИ почек при их туберкулезном поражении позволяет выявлять каверны, обызвествленные очаги, оценить степень вовлечения почечной паренхимы и динамику регресса заболевания под действием проводимой терапии. Рентгеновское исследование почек (обзорная урография, экскреторная урография, ретроградная уретеропиелография и антеградная пиелография) помогают комплексно оценить состояние паренхимы и чашечно-лоханочного аппарата почек, мочеточников, мочевого пузыря. Выполнение почечной ангиографии позволяет определить внутриорганную ангиоархитектонику в случае необходимости резекции почки.
Широкими диагностическими возможностями обладают КТ почек и МРТ. Данные о функциональном состоянии почек при туберкулезе получают с помощью радиоизотопной нефросцинтиграфии. Биопсия почки опасна диссеминацией инфекционного процесса, однако по показаниям может выполняться цистоскопия с биопсией слизистой мочевого пузыря. Морфологическое исследование биопатата мочевого пузыря в ряде случаев позволяет обнаружить гигантские клетки Пирогова-Лангганса даже при отсутствии визуальных изменений слизистой. Дифференциальная диагностика необходима с гидронефрозом, неспецифическим пиелонефритом, губчатой почкой, мегакаликозом, поликистозом почки.
Лечение туберкулеза почек
Лечение при туберкулезе почек может быть медикаментозным и комбинированным (хирургическим и медикаментозным). Медикаментозное лечение нефротуберкулеза включает назначение специфических противотуберкулезных препаратов разных групп на срок от 6 до 12 месяцев (рифампицин, изониазид, этамбутол, пиразинамид, протионамид, стрептомицин и др.).
Перспективно сочетание препаратов первого ряда с фторхинолонами (офлоксацином, ципрофлоксацином, ломефлоксацином). Специфическая химиотерапия при туберкулезе почек дополняется назначением ангиопротекторов, НПВС, предотвращающих рубцовое сморщивание почечной ткани. Следует учитывать, что длительное лечение антитуберкулезными препаратами может приводить к тяжелому дисбактериозу кишечника, аллергическим реакциям.
При нарушении оттока мочи из почки требуется установка мочеточникового стента или проведение нефростомии. В случае развития локального деструктивного процесса в почке консервативную терапию дополняют санацией пораженного сегмента (кавернотомией) или частичной резекцией почки (кавернэктомией). При тотальной деструкции органа показана нефрэктомия.
Основным прогностическим критерием является стадия заболевания. Раннее выявление нефротуберкулеза, отсутствие деструктивных процессов в чашечно-лоханочной системе, мочеточниках и мочевом пузыре на фоне адекватной специфической химиотерапии может сопровождаться полным излечением. Неблагоприятным в плане прогноза является двусторонний туберкулез почек с выраженным разрушением почечной паренхимы.
Все пациенты, перенесшие данное заболевание, находятся на диспансерном учете у фтизиатра и врача-нефролога с периодическим обследованием. Критериями излеченности служит нормализация показателей мочи, отсутствие рецидива нефротуберкулеза по рентгенологическим данным в течение 3-х лет. Предупреждение туберкулеза почек заключается в соблюдении мер специфической (вакцинация против туберкулеза) и неспецифической профилактики легочного туберкулезе.
Папиллит
Папиллит — это острое или хроническое воспаление гипертрофированных анальных сосочков. Проявляется периодической или постоянной болью в области прямой кишки, ощущением инородного тела, спазмом заднепроходного сфинктера, затруднениями при дефекации. Патология диагностируется с помощью проктологического осмотра, пальцевого ректального исследования, аноскопии и гистологического анализа биоптата. Для лечения используют антибиотики, антисептические и противовоспалительные препараты. В упорных случаях воспаленные анальные сосочки иссекают или подвергают криодеструкции.
Морфологической основой возникновения папиллита служит гипертрофия анальных сосочков (папилл) — естественных конических или шаровидных образований, являющихся остатками клоакальной мембраны, которая перфорируется на 7-9 неделях внутриутробного периода. Сосочки состоят из соединительнотканного основания, покрытого плоским многослойным эпителием, и располагаются на свободной части полулунных клапанов, окаймляющих естественные возвышения (столбики) и углубления (крипты) заднего прохода. В норме размеры папилл составляют от 0,2 до 1,0 см, однако под действием травмирующих факторов они могут увеличиваться до 2,5-3,0 см и воспаляться.
Папиллит возникает на фоне предшествующей гипертрофии папилл. Специалисты в сфере проктологии различают предпосылки к воспалительному процессу и факторы, которые непосредственно провоцируют начало заболевания. Вероятность папиллита существенно возрастает при наличии следующих патологических состояний или внешних вмешательств:
- Заболевания аноректальной зоны. Воспаление анальных сосочков часто развивается на фоне геморроя. Воспалительный процесс может контактно распространяться при влагалищно-ректальных свищах, инфекционных поражениях ануса и прямой кишки (проктитах, криптитах, парапроктитах). Возможно формирование папиллита при наличии трещин заднего прохода.
- Травматизация ректальной слизистой. Эпителий папилл может механически повреждаться непереваренной твердой пищей (осколками косточек, шелухой семечек), наконечником клизмы или плотным калом у пациентов, страдающих запорами. Химическое раздражение наблюдается при хронической диарее, длительном пользовании лекарственных препаратов в свечах.
Важным предрасполагающим фактором являются застойные явления в области малого таза, которые отмечаются при ожирении, гиподинамии и беременности. Непосредственной причиной папиллита обычно становится массивное бактериальное обсеменение, значительное механическое или химическое повреждение слизистого слоя прямой кишки в сочетании с локальным или общим снижением защитных сил организма.
Очагом инфекции при папиллите являются воспаленные морганиевы крипты или оболочка прямой кишки. При бактериальной инвазии, химическом или механическом повреждении многослойного эпителия, покрывающего анальные сосочки, возникает местная воспалительная реакция. В зоне поражения происходит выброс медиаторов воспаления, под действием которых расширяются кровеносные сосуды, нарушается микроциркуляция в тканях. Для папиллита характерен отек воспаленного сосочка, гиперемия слизистой и возникновение болевых ощущений.
Симптомы папиллита
На ранних стадиях заболевание протекает малосимптомно или бессимптомно. Пациентов может беспокоить дискомфорт в области заднего прохода, чувство инородного тела в прямой кишке. Для начального этапа папиллита болевой синдром нетипичен, боли появляются лишь иногда во время акта дефекации. При прогрессировании патологии и увеличении анальных сосочков в размерах нарастают болевые ощущения, которые могут иррадиировать в промежность, половые органы, область крестца и копчика.
При длительном течении заболевания возникает постоянный спазм сфинктера заднего прохода, пациенты жалуются на затруднения при дефекации, частые запоры. Признаком осложненного варианта папиллита может быть наличие слизисто-гнойных или кровянистых выделений. Иногда наблюдается мацерация кожи вокруг анального отверстия, сопровождающаяся интенсивным зудом и болезненностью. При неосложненных формах болезни общее состояние больных остается удовлетворительным.
В случае разрастания анальных сосочков до 3-4 см они могут выпадать и ущемляться анальным сфинктером. Такое состояние характеризуется резкой болью с иррадиацией в копчик. При присоединении вторичной инфекции папиллит осложняется гнойным воспалением, для которого характерно усиление болевого синдрома. Инфекционный процесс может распространяться по всей поверхности слизистой, вызывая проктит. При снижении общей реактивности воспаление переходит на смежные ткани с развитием парапроктита.
Из-за постоянной травматизации каловыми массами на поверхности папилл появляются поверхностные эрозии или язвы. При этом у пациентов с папиллитом периодически отмечаются кровотечения из заднего прохода различной интенсивности вплоть до профузных, возникает анемия. Хроническое течение болезни характеризуется грануляцией анальных сосочков. Наиболее опасное осложнение заболевания — злокачественное перерождение эпителия с формированием рака прямой кишки.
Постановка диагноза в большинстве случаев осуществляется клинически во время стандартного проктологического осмотра. Дополнительные методы исследования применяют для выявления проктологических заболеваний, которые могут приводить к воспалению анальных сосочков. Для обследования пациента с подозрением на папиллит наиболее информативными являются:
- Пальцевое исследование. Метод используется для оценки тонуса анального сфинктера, изучения стенок прямой кишки и выявления патологических образований. В случае папиллита прощупываются увеличенные и отечные сосочки, резко болезненные при пальпации. После извлечения пальца на перчатке могут оставаться следы гноя или крови.
- Инструментальное обследование. Проводится аноскопия - обследование нижней части прямой кишки с помощью специального оптического прибора (аноскопа) позволяет визуализировать состояние слизистой оболочки, обнаружить воспаленные участки. При необходимости проктолог проводит биопсию подозрительного образования для последующего цитоморфологического исследования.
- Ми кроморфологический анализ.Гистологическое изучение фрагмента ткани под микроскопом требуется в случае подозрения на аноректальные неоплазии. При папиллите клетки имеют нормальное строение, все слои слизистой оболочки сохранены. Наблюдается массивная лейкоцитарная и макрофагальная инфильтрация биоптатов, могут определяться участки некроза.
В стандартных лабораторных анализах при неосложненном папиллите все показатели находятся в пределах нормы. При кровотечениях из изъязвленных папилл может выявляться снижение концентрации гемоглобина и числа эритроцитов в общем анализе крови. При гнойном воспалении выполняется бактериологический посев кала для определения вида возбудителя.
В первую очередь папиллит дифференцируют с полипами — доброкачественными новообразованиями слизистой прямой кишки. Основной диагностический критерий — результаты гистологического исследования биоптатов образований. Также обращают внимание на анамнез болезни, связь гипертрофии сосочков с другими проктологическими заболеваниями. Обследованием пациента с папиллитом занимается проктолог, для консультации может привлекаться онколог.
Лечение папиллита
Схема ведения больных включает назначение противовоспалительного лечения для купирования симптомов папиллита и этиопатогенетическую терапию основного заболевания, осложнившегося воспалением гипертрофированных папилл. На начальном этапе из рациона пациента исключаются продукты, раздражающие слизистую оболочку кишечника, рекомендуется тщательное соблюдение правил личной гигиены, обеспечение регулярной незатрудненной дефекации, ЛФК для улучшения кровообращения в тазовых органах. Местно назначаются:
- Антибактериальные препараты. Для подавления патологической активности микрофлоры обычно используют хлорамфениколы и другие антибиотики местного действия. Лекарственные средства вводят в прямую кишку в виде свечей.
- Растворы антисептиков. Применяются в виде теплых сидячих ванн, микроклизм и свечей. Оказывают вяжущее, противогнилостное, бактериостатическое или бактерицидное действие, уменьшая выраженность воспаления.
- Противовоспалительные суппозитории. Показаны при наличии выраженного болевого синдрома. Наиболее часто назначают препараты месалазина, которые ингибируют синтез простагландинов и связывают свободные радикалы.
Хирургическое лечение папиллита требуется при неэффективности медикаментозной терапии, хроническом, часто рецидивирующем или осложненном течении заболевания со значительным увеличением размеров воспаленного анального сосочка, его регулярным вывихиванием из ануса, изъязвлением. В ходе классической операции Габриэля иссекается пораженный сосочек и подлежащая крипта. В некоторых случаях возможно проведение малоинвазивного вмешательства (криодеструкции).
Исход заболевания благоприятный, у большинства пациентов после комплексного медикаментозного лечения наблюдается полный регресс симптоматики. При развитии осложнений и проведении хирургических вмешательств прогноз ухудшается. Профилактика папиллита предусматривает раннюю диагностику и адекватную терапию проктологических заболеваний, нормализацию работы кишечника с недопущением хронических запоров. Рекомендуется исключить провоцирующие факторы — ограничить употребление спиртного, острых и пряных блюд, повысить двигательную активность.
2. Колопроктология. Учебное пособие для студентов медицинских вузов, ординаторов, хирургов/ сост. Ботезату А.А., Маракуца Е.В. - 2016.
Воспаление анальных сосочков или папиллит - симптомы диагностика, лечение
Разработчик сайтов, журналист, редактор, дизайнер, программист, копирайтер. Стаж работы — 25 лет. Область интересов: новейшие технологии в медицине, медицинский web-контент, профессиональное фото, видео, web-дизайн. Цели: максимально амбициозные.
- Запись опубликована: 17.11.2021
- Reading time: 2 минут чтения
В некоторых случаях естественные выросты прямой кишки - сосочки - повреждаются, воспаляются и причиняют дискомфорт. Больных беспокоят неприятные симптомы в виде ноющей боли.
Папиллит не опасен, успешно лечится консервативными методами, но при своевременном обращении. В запущенных стадиях при перерождении в фиброзный полип, значительном увеличении потребуется удаление хирургическим путем.
Сосочки - это очень маленькие конусообразные или похожие на соски выступы, находящиеся на зубчатой линии у столбиков Морганьи. Зубчатая линия - это переход анального канала в прямую кишку. Обычно сосочки размером примерно с половину спичечной головки, и их присутствие неизвестно человеку и не ощущается.
Папиллит - это воспалительный процесс нормальных (или увеличенных, гипертрофированных) в данном случае анальных сосочков. Папиллы находятся и в других органах, диагноз папиллит бывает в отношении зрительного нерва, желудка.
Причины и развитие
Эти структуры часто ушибаются, разрезаются, разрываются или иным образом травмируются в результате:
- прохождения твердого стула;
- присутствия в стуле каких-либо твердых частиц (например, фрагмента скорлупы ореха);
- введения ректальной трубки или контейнера с лекарством.
К другим причинам относят:
- плохое кровообращение в тазу, а именно - плохой кровоток, возникающий при геморрое;
- воспалительные заболевания анального канала (проктит и парапроктит, криптит, присоединение воспаления к анальной трещине).
Затем они резко воспаляются, опухают, увеличиваются в размерах и становятся очень болезненными. Набухшие образования распространяются в канал прямой кишки, имея вид “воспаленных пальцев”. Последующие прохождения стула усугубляют раздражение за счет трения и надавливания на них. По мере продолжения болезни сосочки увеличиваются в размерах. После стихания острого воспаления опухоль часто остается, а сосочки становятся жесткими и фиброзными.
- беременность;
- лишний вес;
- нарушение рациона питания;
- снижение иммунитета;
- малоподвижный образ жизни.
Симптомы
Наиболее частые признаки наличия одного или нескольких увеличенных и раздраженных сосочков заднего прохода:
- неясное стойкое чувство дискомфорта в прямой кишке;
- дискомфорт при сидении;
- тупая боль.
При длительном течении возможно вовлечение сфинктера с развитием нарушения опорожнения кишечника, запоров.
- Присоединение вторичной инфекции приводит к воспалению уже самой прямой кишки (проктиту) и/или окружающих тканей (парапроктиту).
- Постоянное повреждение совместно с уже имеющимся воспалением приводит к эрозии. Вначале самих сосочков, затем слизистой анального канала или верхних участков прямой кишки. Напомним, анальные сосочки находятся в месте перехода этих отделов. Эрозии могут превратиться в кровоточащие язвы.
- Хронический воспалительный процесс увеличенных сосочков сопровождается изменением, уплотнением их тканей. Гипертрофированные сосочки склонны к фиброзу и развитию из них полипов.
Диагностика папиллита
Проктолог опрашивает пациента и собирает его жалобы, выясняет анамнез. Затем осматривают задний проход в покое и при напряжении, натуживании. Кроме того, проводится пальцевое ректальное обследование, аноскопия, реже ректороманоскопия, чтобы осмотреть состояние анального канала и прямой кишки, выявить наличие анальных сосочков и других связанных заболеваний.
Чаще всего назначается аноскопия, поскольку структуры расположены в анальном канале и на зубчатой линии. Процедура безболезненна, проста в проведении, практически без подготовки (в отличие от других эндоскопических методов изучения прямой кишки). Ректоскопия или колоноскопия нужна при подозрении на другие более серьезные патологии, в первую очередь опухоли.
С проведением аноскопии совмещается биопсия. При рассмотрении тканей под микроскопом обнаруживается скопление лейкоцитов, макрофагов, иногда очаги некроза (параметры воспаления). Признаков атипии, патологического митоза не обнаруживается.
При осложненных формах и выраженном выделении гноя, назначают культуральное исследование (посев) для установления возбудителя.
Лечение папиллита консервативное, преследует следующие задачи:
- снятие воспаления;
- стимуляция восстановления тканей;
- устранение симптомов;
- терапия основного или присоединившегося заболевания.
Если обнаружен сфинктерит, проктит, осложненный папиллитом, всегда проводят комбинированное лечение с упором на основное заболевание.
При неосложненном папиллите лечение в основном местное.
Теплые сидячие ванны:
Для антисептического эффекта используют раствор фурацилина, успокаивающего и противомикробного отвары ромашки, шалфея, календулы.
- При болевых ощущениях назначают обезболивающие свечи или мазь (Релиф).
- При повреждении тканей, эрозивном процессе - суппозитории Облепиховое масло. Безвредный растительный препарат, стимулирующий регенерацию. Достаточно однократного применения на ночь в течение 14 дней. Метилурацил способствует заживлению и питанию, восстановлению поврежденных клеток. Применяют 1-2 раза в день (на ночь обязательно), курс длительный.
- Комбинированный препарат Постеризан форте (гидрокортизон+инактивированные клетки кишечной палочки) часто назначается при папиллите. Снимает воспаление, зуд, отек тканей. Стимулирует регенерацию, местную защиту к патогенной флоре. Применяют на ночь после дефекации и утром. Курс от 14-21 день.
Рекомендации по питанию:
- категорически исключить продукты, раздражающие слизистую ЖКТ (специи, пряности, маринады);
- обязательно исключить алкоголь;
- ограничить курение;
- преимущественно готовить на пару, отварные блюда;
- ограничить любые жареные блюда (фритюр, на мангале, обычные на сковороде/духовке).
- ежедневно соблюдать гигиену аноректальной области;
- предупреждать развитие запоров.
Нормализовать стул лучше с помощью мягких натуральных препаратов. Например, Мукофальк, Фитомуцил Норм. Препараты сенны не рекомендуются, поскольку они раздражают кишечник и вызывают привыкание.
Хирургическое лечение
Применяется редко, в отдельных случаях. Например, при изъязвлении сосочка достаточно большого размера. Вмешательство проводится после снятия активной фазы воспаления. Традиционную хирургию не используют, предпочтение отдается лазерному удалению и радиочастотной электрохирургии.
Это наименее травматичные методы без развития кровотечения и практически без осложнений с коротким восстановительным периодом. Выбор метода определяет проктолог индивидуально.
Гипертрофия анальных сосочков

- Запись опубликована: 15.11.2021
- Reading time: 2 минут чтения
Анальные сосочки обнаруживаются почти у 50-60% пациентов, обследованных по поводу проктологических заболеваний. Обычно образования небольшого размера, не вызывают никаких симптомов и могут рассматриваться в качестве нормальных структур. Однако, если развивается их гипертрофия и сосочки начинают выступать в анальном канале, это требует не только внимания, но и соответствующего лечения.
Что такое анальные сосочки
Анальные сосочки - полиповидные выросты телесного цвета на слизисто-кожном соединении верхнего анального канала, придающие ему зубчатый вид. Обычно небольшие по размеру (2-5 мм), но иногда становятся увеличенными, т.е. гипертрофированными.
Определение и особенности
Гипертрофированные анальные сосочки - это доброкачественные приобретенные полиповидные выросты плоского эпителия заднего прохода и субэпителиальной соединительной ткани в основании анальных столбов. Выступают вверх от зубчатой линии или соединения между кожей и эпителиальной выстилкой заднего прохода.
- Отдельно. Т.е. обнаруживаются изолированно, могут быть твердыми и пальпируемыми при пальцевом исследовании заднего прохода. В этой ситуации их необходимо дифференцировать от полипов, геморроя или других новообразований.
- Совместно с другими заболеваниями. Такая структура часто находится в верхней части хронической анальной трещины. Расширенные вены, белые участки и большой гипертрофированный анальный сосочек во многих случаях встречаются при выпадающем типе геморроя. Часто развиваются как часть классической триады хронической трещины, а именно самой трещины, гипертрофированного сосочка вверху и кожного пятна внизу.
Раньше этим структурам не уделялось никакого внимания и их не лечили. Если пациентам, провели курс терапии трещины заднего прохода, но при этом сопутствующие сосочки или полипы остались нетронутыми, они продолжали жаловаться на зуд, влажность или периодическое покалывание в анусе.
Даже при отсутствии в анамнезе проктологических болезней, но при наличии гипертрофированных анальных сосочков, многие чувствуют себя не полностью здоровыми из-за ощущения, что что-то выступает из ануса. Поэтому при их обнаружении, рекомендуется провести соответствующее лечение.
Кодирование МКБ
МКБ-10: K62.0 - полип анального канала.
Эпидемиология
Патология наиболее часто встречается пациентов, подвергающихся проктоскопии (~ 45%). Беспокоит больше мужчин, соотношение М:Ж равно 2: 1
Обычно возникает в среднем и позднем взрослом возрасте, но сообщалось о редких случаях у пациентов подросткового возраста.
Новообразования локализуются в анальном канале, у основания анальных столбиков (столбики Морганьи) по зубчатой линии.
Механизм развития
Патология - результат увеличения нормальных анальных сосочков. Основную роль в развитии играет реактивная гиперпластическая природа субэпителиальной соединительной ткани слизистой оболочки заднего прохода. Процесс запускается вследствие раздражения, инфекции или травмы нормального анального сосочка.
Процесс может быть: а) изолированный; б) вторичный по отношению к ближайшему воспалительному процессу или массовому поражению тканей анальной области.
Важную роль в патогенезе играют тучные клетки благодаря своей фиброгенной, фибролитической и ангиогенной активности.
В дальнейшем эти сосочки продолжают увеличиваться в размерах. Со временем сосочек склонен к значительному фиброзному утолщению, когда он приобретает округлый расширенный кончик (известен как фиброзный полип). Это происходит из-за скопления и уплотнения хронически воспаленных тканей.
Доказывает процесс тот факт, что у 16% пациентов с хронической трещиной заднего прохода регистрировали наличие сосочков, превратившихся в фиброзные полипы.
Иногда они становятся очень большими. Есть данные о случае гигантского гипертрофированного анального сосочка, осложненного массивным анальным кровотечением и пролапсом.
Пациенты сообщают о следующих симптомах:
- зуд;
- ощущение инородного тела;
- покалывание;
- тянущее ощущение неполного опорожнения;
- тяжесть в анальной области.
Во время консультации у проктолога после выяснения жалоб и сбора анамнеза, проктолог назначает ряд исследований. Их количество зависит от симптомов, состояния и подозрения на определенные патологии. При подозрении на наличие гипертрофированных анальных сосочков обязательно назначается эндоскопическое исследование (ректороманоскопия). Да, их можно ощутить при пальцевом обследовании, но для подтверждения нужны специальные методы.
Ректоскопия позволяет изучить состояние слизистой, установить наличие опухолей и полипов, провести дифференциальную диагностику. Отличить увеличенные сосочки от аденоматозного полипа можно по их белому внешнему виду и происхождению из нижней (чешуйчатой) части зубчатой линии анального канала. Кроме того, ректоскопия сочетается с биопсией - забором тканей для исследования в лаборатории.
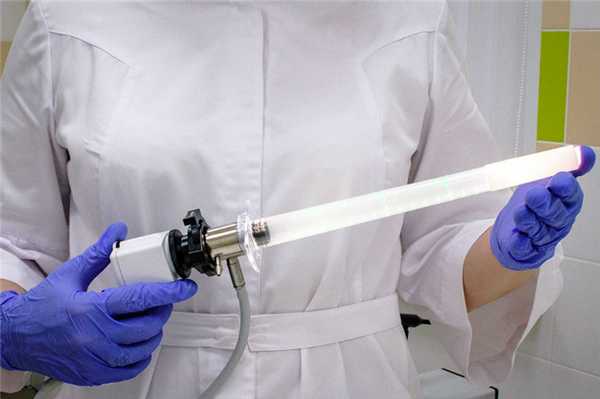
Ректоскопия
Гистопатологическая оценка полученных образцов необходима для установления диагноза и исключения сопутствующих поражений. К ним относятся плоскоклеточные интраэпителиальные поражения низкой или высокой степени.
Микроскопическое (гистологическое) описание гипертрофированных анальных сосочков:
- Миксоидная или коллагеновая строма, покрытая зрелым плоским эпителием.
- Плоский эпителий может быть слегка гиперпластическим и показывать очаговый гиперкератоз и паракератоз.
- Рыхлая сердцевина из фиброваскулярной соединительной ткани, морфологически похожая на нормальную слизистую оболочку заднего прохода.
- Часто наблюдаются большие многоядерные реактивные стромальные клетки (80% гипертрофированных сосочков), обычно разбросаны по отдельности в строме, но иногда демонстрируют небольшие участки агрегации.
- Атипичные, причудливые стромальные клетки могут встречаться в полипе большого размера.
- Фигуры митоза отсутствуют.
- Рассеянные гладкие мышечные волокна видны примерно в половине полипов.
- Часто присутствуют тучные клетки.
- Отсутствие толстостенных тромбированных сосудов (признаки геморроя).
- Хроническое воспаление, в основном в субэпителиальной области.
- Субэпителиальная зона кажется более клеточной и менее коллагеновой, чем центр.
Эндоваскулярное смещение эпителия (псевдоинвазия сосудов) наблюдается редко, что связано с морфологическими признаками травматизма.
Дифференциальная диагностика
- Видны расширенные толстостенные подслизистые сосуды и синусоидальные пространства.
- Часто протекает с тромбозом и кровоизлиянием в окружающие соединительные ткани.
Кондилома Accuminatum. Отличия:
- Акантоз соседствует с папилломатозом.
- Имеются различные диспластические изменения, в том числе койлоцитарная атипия (ядерная морщинка с околоядерным просветом), увеличение ядерной атипии/размера ядер, усиленный или атипичный митоз.
- Невооруженным взглядом и во время эндоскопии заметно неспецифическое острое и хроническое воспаление и грануляция ткани.
- Аноректальные опухоли (карцинома или анальная меланома, нейроэндокринная опухоль, лимфома). Отличить можно по гистологическим особенностям, характерным для каждого конкретного типа опухоли.
Лечение
Почему рекомендуется лечить гипертрофированные анальные сосочки:
- могут травмироваться и воспаляться во время и после дефекации (при их воспалении возникает папиллит);
- велика вероятность увеличения выработки слизи, что приведет к увеличению влажности анальной области;
- превращаясь в фиброзный полип, склонны выступать в анальном отверстии, выходить наружу во время дефекации, что часто требует вправления их обратно вручную. Эти полипы считаются одним из дифференциальных диагнозов выпадения прямой кишки;
- сопровождаются неприятными проявлениями.
Если такие структуры не причиняют неудобств, пациента оставляют под наблюдением. Лечение с помощью хирургического вмешательства применяют только при симптоматической форме заболевания. Его виды:
- эндоскопическое;
- хирургическая резекция;
- удаление путем дробления оснований;
- иссечение после перевязки; .
При сопутствующем хроническом процессе обязательно проводится коррекция первичной этиологии. Например, при наличии трещины или геморроидальных узлов - их лечение.
В последнее время все большее внимание уделяется современным наименее травматичным методам хирургической помощи. Обнаружено, что использование радиочастотных устройств для лечения этой патологии - процедура быстрая, простая и без значительных осложнений. Устройство удаляет сосочки мгновенно.
Радиочастотная хирургия направлена на рассечение или коагуляцию тканей с использованием высокочастотного переменного тока. Радиочастотный аппарат выполняет одновременную функцию разрезания и коагуляции тканей. Эффект разреза (высокочастотный разрез) выполняется без давления или раздавливания клеток ткани. Это происходит из-за тепла, создаваемого сопротивлением тканей прохождению высокочастотной волны, приводимой в движение оборудованием. Тепло заставляет внутриклеточную воду закипать, тем самым увеличивая внутреннее давление клетки до точки разрыва изнутри наружу (взрыв). Это явление называется клеточным улетучиванием.
Радиочастотный прибор производит электромагнитную волну очень высокой частоты. Устройство поставляется с ручкой, к ней можно прикрепить различные сменные электроды в соответствии с конкретными требованиями.
Сосочки удаляют с помощью шарикового электрода с радиочастотным блоком, работающим в режиме коагуляции. Они исчезают в кратчайшие сроки и без кровотечения. Если он уже приобрел вид фиброзного полипа заднего прохода, сначала коагулируют его основание по окружности с помощью шарикового электрода, а затем снимают массу, используя электрод с круглой петлей. Вся процедура занимает около 7-10 минут.
Прогноз излечения
Пациентам назначают анальгетики на 1 неделю и размягчители стула на срок до 1 месяца. Первое наблюдение проводится через 30 дней. Выполняется аноскопия, при правильно выполненном удалении, наблюдается полное отсутствие сосочков.
При наличии диагноза “гипертрофированные анальные сосочки” вне зависимости от того, было проведено лечение или нет, рекомендуются консультации проктолога один раз в год.
Читайте также:
- Лечение болезни Лайма. Тактика врача при болезни Лайма.
- Синдром Меньера (Meniere)
- Эффекты оральных контрацептивов не связанные с контрацепцией. Положительные моменты
- Эффективность дефибрилляции сердца. Как увеличить эффективность дефибрилляции?
- Аномальное предсердное возбуждение и проведение. Отклонения от нормы левого предсердия
