Послеоперационное течение пломбировки. Пациент после пломбировки плевральной полости парафином
Добавил пользователь Валентин П. Обновлено: 28.01.2026
1. После операции по экстрасклеральному пломбированию глаз заклеивают повязкой, защищающей его от случайных загрязнений. Утром следующего дня повязку следует снять и обработать веки (не глаз!) стерильной ватой с водным раствором 0,02% фурацилина либо водным раствором 0,25% левомицетина (продаются в аптечной сети). Начиная с первого послеоперационного дня, заклеивать глаз повязкой, которая не дает ему свободно двигаться и моргать, следует только на время.
2. В день операции, как и в реабилитационный период, в глазу и окологлазничной области (висок, надбровье) возможно возникновение болей. Болевой синдром целесообразно снимать приемом таблеток «Кетанов», «Кеторол» или «Анальгин» (согласно приложенным к препарату инструкциям), а также обратиться к лечащему врачу.
3. В послеоперационный период глаз нередко раздражен, наблюдается отек век с обильным отделяемым. Выраженность данных проявлений зависит от специфических особенностей выполненной операции и индивидуальной чувствительности организма к полученной операционной травме.
Период восстановления
Предлагаемые ниже рекомендации являются общепринятыми, т.е. разработанными для большинства пациентов. При индивидуальном течении послеоперационного периода может быть предложена персональная схема лечения с графиком осмотров пациента. Пожалуйста, при посещении врача каждый раз уточняйте рекомендации!
1. Режим. После перенесенной операции экстрасклерального пломбирования, определенное лечебное значение может иметь соблюдение некоторых правил (положение головы, специфика постельного режима). В этом случае, хирург или лечащий даст рекомендации о модели поведения в первые послеоперационные сутки. В дальнейшем следует самому уточнить особенности режима у лечащего врача. Первые несколько недель нельзя поднимать тяжести свыше 5 кг.
2. Гигиена. В процессе умывания необходимо избегать попадания воды и мыла в прооперированный глаз. Мытье головы осуществляется в положении наклона головы назад. При попадании воды в оперированный глаз нужно промыть его водным 0,02% раствором фурацилина либо водным 0,25% раствором левомицетина (приобретите в аптеке).
3. Не пропускайте назначенный врачом день приема!
4. Повязка. Несколько первых послеоперационных дней рекомендуется носить на оперированном глазу повязку для защиты его от воздействия яркого света и присутствующих в воздухе частиц пыли. Повязка должна представлять собой «занавеску», сделанную из двух слоев марли, которую крепят перед глазом на лбу с помощью лейкопластыря. При обильном отделяемом, повязку необходимо менять по возможности часто (1 раз в сутки или чаще).
5. Глазные капли. Для профилактики инфекционных осложнений и более быстрого заживления, необходимы определенные лекарственные средства. Как правило, в послеоперационный период хирург рекомендует закапывание нескольких препаратов, включая дезинфицирующие капли (к примеру, «Ципрофлоксацин», «Тобрекс», «Флоксал», и пр.), противовоспалительные капли («Индоколлир», «Наклоф» и пр.) либо комбинированные средства («Макситрол», «Тобрадекс»). Обычно внесение их назначают по убыванию: 1 неделя - четырежды в день, 2 неделя - трижды в день, 3 неделя - дважды в день, 4 неделя - раз в день однократно, затем следует отмена препаратов. Пожалуйста, все рекомендации уточняйте у лечащего врача при каждом посещении!
Острота зрения, подбор очков
После операции, выполненной по поводу отслойки сетчатой оболочки, улучшение зрения происходит постепенно и длится 2 - 3 месяца. В некоторых случаях, данный процесс может занять до полугода. Как правило, процесс может несколько замедляться у пациентов с миопией и пожилых людей.
Максимально возможная острота зрения будет зависеть от срока, который прошел со времени возникновения отслойки до момента проведения операции, а также от степени вовлеченности в процесс отслоения центральных отделов сетчатки, которые ответственны за остроту зрения.
В реабилитационный период глаза могут стать «разными». При этом, для исправления подобной ситуации может потребоваться временное ношение очков или контактных линз. Окончательную очковую коррекцию стоит проводить только спустя 2-3 мес. после операции, хотя определение срока подбора очков решаются строго индивидуально, если, к примеру, оперирован единственный глаз.
В процессе восстановления зрения, некоторые пациенты могут отмечать искажения предметов и линий, двоение в глазах. Как правило, данные симптомы постепенно ослабевают в течение недель или месяцев.
Рекомендации по дальнейшему уходу
Ограничения, необходимые в послеоперационном периоде, постепенно будут сняты. Ниже приведены некоторые полезные рекомендации, способствующие сохранению зрения в будущем:
- Не садитесь за руль, пока не заживет глаз.
- Не трите и не давите глаз.
- При просмотре телевизора либо чтении, делайте обязательные перерывы.
- Носите солнцезащитные очки, защищающие глаз от вредного ультрафиолета.
- Соблюдайте установленное расписание посещений врача.
Дополнительная информация
Завершающим этапом операции пломбирования склеры, является накладывание нескольких швов на конъюнктиву. Они могут создавать ощущение в глазу инородного тела или чувство дискомфорта при моргании. Обычно, такие швы снимают спустя 2 недели после оперативного вмешательства.
Послеоперационное течение пломбировки. Пациент после пломбировки плевральной полости парафином
Клиническая больница №1 «Медси», Москва, Россия
Российская медицинская академия последипломного образования, Москва, Россия
ФГБУ «Лечебно-реабилитационный центр» Минздрава России, Москва, Россия
Результаты применения стандартизованного протокола ускоренного выздоровления после онкологических операций на легком
Журнал: Хирургия. Журнал им. Н.И. Пирогова. 2019;(7): 58‑62
Рак легкого стойко лидирует среди злокачественных опухолей по заболеваемости и смертности. Согласно национальным рекомендациям [1], всем функционально операбельным больным с немелкоклеточным раком легкого 0—IIB (N0) стадии показано хирургическое лечение.
Операции на легких относятся к высокотравматичным вмешательствам [2]. Доля пациентов, у которых возникают послеоперационные осложнения при выполнении стандартной лобэктомии, может превышать 32% [3], а летальность достигает 2,6% [4].
Ряд авторов [5—8] считают, что применение стандартизованного протокола ускоренного выздоровления (ПУВ) по сравнению с традиционным периоперационным ведением пациентов позволяет снизить количество осложнений после операций на легких и сократить срок госпитализации. В то же время единое мнение в отношении отдельных компонентов ПУВ при операциях на легких отсутствует. Основная цель исследования — разработка и оценка результатов применения ПУВ пациентов после резекционных операций на легких.
Материал и методы
На основании данных литературы и собственного опыта мы разработали ПУВ пациентов после операций на легких. Периоперационное ведение пациента для удобства разделено на три периода: предоперационный, интраоперационный и послеоперационный.
Предоперационный период включает следующие составляющие:
1. Информирование пациента — предоставление исчерпывающей информации пациенту и его доверенным лицам о всех аспектах предстоящего лечения.
2. Оценка нутритивного статуса — выполняется с помощью шкалы NRS 2002 [9]. При выявлении дефицита питания назначают нутритивную поддержку.
3. Отказ от курения — мотивирование пациентов отказаться от курения.
4. Коррекция сопутствующих заболеваний — профильные специалисты назначают рекомендации по коррекции сопутствующих заболеваний.
5. Амбулаторный осмотр анестезиологом — уменьшает количество отмен операций после госпитализации пациента в стационар.
6. Госпитализация пациентов накануне вмешательства — достаточное количество времени перед операцией позволяет детально изучить результаты всех обследований, спланировать этапы предстоящей операции, оценить возможные трудности и предпринять меры для предотвращения осложнений.
7. Подготовка к операции — утренний душ, за 12 ч до операции введение низкомолекулярного гепарина. Нет ограничения в питании накануне операции, отказ от приема твердой пищи осуществляется за 6 ч, прием жидкости в объеме 400 мл обязателен за 2—3 ч до операции. Механическую подготовку кишечника не выполняют. Седативные препараты рутинно не назначают. В отделении устанавливают периферический венозный катетер, проводят антибиотикопрофилактику (обычно цефалоспорин II поколения). Эластическая компрессия нижних конечностей. В операционный блок пациент идет самостоятельно в сопровождении медицинского персонала.
Интраоперационный период
Анестезиологические аспекты ПУВ
1. Инвазивные манипуляции. Постановка центрального венозного катетера, перидурального катетера и прямой мониторинг артериального давления только при выполнении операции через торакотомный доступ или при высоком риске конверсии торакоскопической операции открытым доступом.
2. Перидуральный катетер. Устанавливается на уровне ThV—ThVI.
3. Мочевой катетер. При времени операции более 2 ч.
4. Интубация трахеи. Выполняется двухпросветной трубкой для однолегочной вентиляции.
5. Режим вентиляции. Малые объемы дыхательной смеси при однолегочной вентиляции — 3—4 мл на 1 кг массы тела.
6. Поддержание нормотермии. Используют системы обогрева конвекционного типа и надувные одеяла, подогрев растворов для внутривенного введения и обработки плевральной полости.
7. Инфузионная терапия. Объем инфузии направлен на поддержание нормоволемии и определяется индивидуально.
8. Ранняя экстубация. При неосложненной операции пациента экстубируют в операционной.
Хирургические аспекты ПУВ
1. Доступ. Предпочтительны торакоскопические операции с извлечением препарата через субксифоидальный доступ. Дренирование одним силиконовым дренажем, заведенным субксифодально.
2. Лигирование и разделение сосудов и бронхов. Предпочтительно с использованием автоматических электромеханических сшивающих аппаратов. На сосуды накладывают пластиковые клипсы с защелкой — по 2 на проксимальной части.
3. Разделение междолевых борозд. Предпочтительно использование сшивающих аппаратов.
4. Ведение без дренажа. При торакоскопических атипичных резекциях легкого без дополнительных факторов риска при надежном аэро- и гемостазе либо при операциях малого объема на средостении плевральный дренаж не устанавливают.
Послеоперационные аспекты ПУВ
1. Обезболивание. После видеоассистированных операций обезболивание осуществляем сочетанием нестероидных противовоспалительных препаратов, по потребности используем трамадол. После торакотомии применяем мультимодальную аналгезию: уровень аналгезии должен обеспечивать беспрепятственную мобилизацию пациента и свободный кашель.
2. Двигательный режим. Вертикализация в течение первых 3 ч после окончания операции. Активность пациента не ограничивают.
3. Дыхательная гимнастика. Выдаются побудительные спирометры и инструкция с упражнениями.
4. Питание. Спустя 2—3 ч после операции разрешают питье без ограничений и легкий ужин. С 1-го дня после операции ограничений по диете нет.
5. Удаление плеврального дренажа. Критериями являются менее 500 мл серозного экссудата за сутки, отсутствие сброса воздуха в течение суток при расправленном легком на обзорной рентгенографии органов грудной клетки.
6. Тактика при продленном сбросе воздуха. При продолжающемся (5—7 дней) сбросе воздуха активное дренирование прекращают и устанавливают пакет для амбулаторного дренирования плевральной полости, оснащенный клапаном типа Heimlich. В течение 1 сут пациент находится в стационаре для исключения возникновения подкожной эмфиземы и дыхательной недостаточности. Выполняют обзорную рентгенографию органов грудной клетки для измерения остаточной плевральной полости. Пациента выписывают с обязательным условием еженедельного контроля в отделении лечащим врачом, выполнения ежедневных перевязок и общих гигиенических рекомендаций.
7. Выписка. При температуре тела в течение суток ниже 37 °C, оценке боли по визуально-аналоговой шкале менее 3 баллов, мобильности пациента, возможности самообслуживания, завершенности этапа лечения.
Результаты
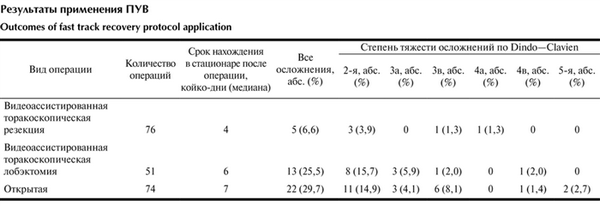
Описанный ПУВ применяли после операций на легком, которые произведены на базе отделения хирургической онкологии Лечебно-реабилитационного центра Минздрава России с декабря 2014 г. по январь 2017 г. Два хирурга выполнили более 200 резекционных операций на легком с использованием вышеописанного протокола. Результаты представлены в таблице. Результаты применения ПУВ
Анализируя специальную литературу, мы изучили различные рекомендации в отношении каждого из этапов периоперационного ведения пациентов, некоторые из которых требуют обсуждения.
На предоперационном этапе пациентам рекомендовано выполнение амбулаторных физических тренировок и физиотерапии. Многие исследователи [10—17] полагают, что это уменьшает количество осложнений и сокращает послеоперационный период. Внедрение в практику данных рекомендаций может быть сопряжено с трудностями из-за низкой приверженности пациента к выполнению рекомендаций в амбулаторных условиях. Не всегда может быть реализована и задача отказа от курения, несмотря на снижение общего количества осложнений и риска неблагоприятного исхода у бросивших курить пациентов [18—21].
Госпитализация в день операции [7, 22], с нашей точки зрения, не всегда безопасна для пациента. При этом количество времени до подачи пациента в операционную ограничено, что не способствует внимательной оценке данных обследований и спокойной разработке плана операции хирургом.
На интраоперационном этапе интерес вызывают публикации о безынтубационном анестезиологическом пособии [23—25]. Эта методика представляется перспективной у пациентов с тяжелыми сопутствующими заболеваниями и способна ускорить восстановление после операции.
Большое значение имеет минимизация травматичности доступа. Преимущества видеоассистированной торакоскопической хирургии продемонстрированы во многих исследованиях [4, 26—28]. Сейчас развиваются полностью внутрипросветные варианты эндоскопических операций и резекции легких из единого доступа.
Проблема отказа от дренирования при операциях на легких освещена H. Luckraz и соавт. [29, 30], которые показали, что установка плеврального дренажа после видеоассистированной торакоскопической биопсии легкого не влияет на частоту развития пневмоторакса, однако повышает длительность пребывания пациентов в стационаре. Согласно нашему опыту, методика бездренажного ведения безопасна и может применяться при торакоскопических операциях небольшого объема.
На послеоперационном этапе неоднозначным вопросом остаются аспекты дренирования плевральной полости. Многие исследователи [31] рекомендуют удалять дренаж при отсутствии сброса воздуха и объеме экссудата менее 250 мл/сут. В то же время L. Bjerregaard и соавт. [32], проанализировав результаты ВАТС лобэктомий, показали, что при удалении дренажа на фоне выделения менее 500 мл серозного экссудата в сутки и сброса воздуха менее 20 мл/ч частота повторных дренирований плевральной полости и госпитализаций не превышает этих показателей у остальных пациентов. Необходимость активной аспирации и степень разрежения системы также обсуждаются в литературе. Так, С. Prokakis и соавт. [30] указывают на отсутствие преимуществ активной аспирации после лобэктомий по сравнению с пассивным дренированием по Бюлау [33]. Ряд авторов [31] считают, что активная аспирация ускоряет заживление паренхимы легкого за счет сопоставления париетальной и висцеральной плевры, другие — что продленное разрежение в плевральной полости поддерживает дефекты паренхимы и замедляет выздоровление. Показано, что при продленном сбросе воздуха и формировании альвеоло-плевральных фистул безопасна выписка пациента из стационара с пакетом для амбулаторного дренирования, оснащенного клапаном типа Heimlich или другими переносными системами дренирования плевральной полости.
Таким образом, разработка и внедрение ПУВ после операций по поводу рака легкого возможны только при административной поддержке и согласованной работе мультидисциплинарного коллектива специалистов клинических и диагностических подразделений учреждения. По нашему мнению, применение стандартизованного ПУВ позволяет улучшить результаты операций на легких, уменьшить число послеоперационных осложнений и сократить среднюю длительность стационарного лечения пациентов.
Авторы заявляют об отсутствии конфликта интересов.
The authors declare no conflicts of interest.
Сведения об авторах
Кафедра и клиника хирургии Института последипломного образования Самарского государственного медицинского университета и Самарской областной клинической больницы им. М.И. Калинина
Повторные операции при длительном просачивании воздуха после видеоторакоскопических резекций легких
Журнал: Эндоскопическая хирургия. 2011;17(4): 10‑13
Корымасов Е.А., Бенян А.С. Повторные операции при длительном просачивании воздуха после видеоторакоскопических резекций легких. Эндоскопическая хирургия. 2011;17(4):10‑13.
Korymasov EA, Benian AS. Reoperations for continuous air leak after videothoracoscopic lung resections. Endoscopic Surgery. 2011;17(4):10‑13. (In Russ.).
Одно из наиболее частых осложнений после видеоторакоскопических резекций легких - длительное просачивание воздуха. Особенно очевидной представляется актуальность данной проблемы при диагностических резекциях с целью биопсии у пациентов с диффузными поражениями легких, когда резекция на уровне заведомо пораженных тканей сопряжена с высоким риском персистенции бронхопульмональных свищей. В послеоперационном периоде у этих пациентов применяются различные методы лечения: от консервативных и вспомогательных методов до повторных операций. Представленный опыт является попыткой иллюстрации общей характеристики видеоторакоскопических резекций легких, наиболее часто наблюдающихся осложнений, анализа их причин и введения лечебно-диагностического алгоритма при этих осложнениях.
В настоящее время в легочной хирургии отмечается тенденция к выбору вида операционного доступа в зависимости от объема резецируемой легочной ткани [1]. Видеоторакоскопические технологии прочно заняли свое место в хирургии буллезной эмфиземы и спонтанного пневмоторакса, округлых образований легких, патологических процессов в интерстициальной ткани легких [2]. Определяющими факторами выполнения эндоскопической операции при этом служат небольшой объем удаляемой легочной ткани и преимущественно краевой характер резекции [3]. Несмотря на то что параметры объема резецируемой ткани при открытых и видеоторакоскопических операциях существенно различаются, общей проблемой остается длительное просачивание воздуха, наблюдающееся у 3—25% пациентов [4]. Особую значимость данное осложнение приобретает при диагностических вмешательствах с целью биопсии у пациентов с диффузным поражением легких неясной этиологии, когда резекция на уровне заведомо пораженных тканей сопряжена с высоким риском персистенции бронхопульмональных свищей и развития послеоперационной эмпиемы плевры [5].
В данной работе представлена попытка определить роль и место повторных операций в тактике ведения пациентов после видеоторакоскопической резекции легкого при осложненном течении послеоперационного периода.
Материал и методы

В отделении торакальной хирургии кафедры и клиники хирургии ИПО Самарского государственного медицинского университета и Самарской областной клинической больницы им. М.И. Калинина видеоторакоскопические операции выполняются с 1999 г. За этот период выполнены 267 видеоторакоскопических и 116 видеоассистированных резекций легких. Диагностические резекции легочной ткани с целью биопсии выполнялись при диффузных процессах в легких (248 пациентов). Целью таких операций была морфологическая верификация заболевания легких. В результате хирургической диагностики выявлены злокачественные процессы легких у 33 (13,3%) пациентов, туберкулез — у 12 (4,8%), хроническая обструктивная болезнь легких — у 28 (11,3%), различные виды диссеминированных и интерстициальных заболеваний легких — у 175 (70,6%). Распределение оперированных пациентов в зависимости от установленного диагноза представлено в табл. 1.

В качестве основного лечебного вмешательства видеоторакоскопические и видеоассистированные резекции легких были применены у 135 пациентов: у 98 — при буллезной эмфиземе легких, у 9 — при туберкуломах, у 18 — при доброкачественных новообразованиях и кистах легких, у 3 — при метастатическом поражении легких, у 2 — при паразитарном поражении легких. Распределение оперированных пациентов в зависимости от характера патологии представлено в табл. 2.
При выборе доступа между видеоторакоскопией и видеоассистированной операцией с миниторакотомией ориентировались на объем предполагаемой резекции и возможность использования эндоскопических режущих и сшивающих инструментов, а также на навыки и предпочтения оперирующего хирурга. Учитывали также, что по травматичности оба вида доступа почти не различаются. В любом случае видеоторакоскопия была первым этапом вмешательства с целью ревизии органов плевральной полости, оценки объема предполагаемой резекции и степени спаечного процесса. Затем в зависимости от размеров патологических объектов, их распространенности, локализации, объемов и способов резекции определяли необходимость выполнения вспомогательной миниторакотомии.
Для выполнения видеоторакоскопических резекций были применены линейные и артикуляционные сшиватели. Всего выполнено 38 стейплерных резекций легкого. Эндоскопические аппаратные резекции выполняли при буллезной эмфиземе и доброкачественных образованиях легких. При выполнении диагностических резекций с целью биопсии отдавали предпочтение бесшовной технологии резекции легкого, которую осуществляли с помощью гармонического ультразвукового скальпеля. Применение этой технологии также обосновано при удалении глубоко расположенных образований. Ультразвуковая резекция легкого была выполнена у 251 пациента преимущественно с интерстициальными заболеваниями. В большинстве случаев при резекции легкого, осуществляемой по краю долей, дополнительное прошивание легочной ткани не требовалось. Однако при локализации патологических очагов на поверхностях долей и при большой поверхности поражения резекцию дополняли эндоскопическими швами на легочную ткань. Видеоассистированные резекции легких через мини-доступ с применением ранорасширителя и сшивающих аппаратов УО-40, УДО-38 выполняли при значительном объеме поражения, обусловливающем необходимость удаления большой части легкого, а также при необходимости осуществления механического шва легочной ткани и в отсутствие эндоскопических сшивателей (у 94 пациентов).
По окончании этапа резекции принимали решение о необходимости укрепления линии легочной резекции с целью достижения аэростаза. Для этого выполняли аппликацию коллагеновых пластин ТахоКомб, которые накладывали на линию легочного шва и зону резекции в сухом виде, желтой маркированной стороной к ране и прижимали в течение 4—5 мин. Описанный способ герметизации был применен у 82 (21,4%) пациентов.
Результаты и обсуждение
Общая тактика ведения пациентов после видеоторакоскопической резекции легкого, а также такие частные ее вопросы, как применение вспомогательных методов или определение показаний к реторакоскопии, базируются на оценке расправления легкого в послеоперационном периоде. Основными объективными критериями расправления легкого являются степень просачивания воздуха по подводному дренажу, рентгенологические признаки выполнения легким всей плевральной полости, отсутствие или наличие подкожной эмфиземы. В качестве дополнительных критериев учитывали характер фоновой патологии легких, объем и уровень выполненной резекции при первой операции, методику резекции, степень дыхательной недостаточности, возраст пациента. Оценка всех критериев, проведенная с учетом фактора времени (число дней, прошедших после операции), направлена на оптимизацию тактики ведения пациентов с длительным просачиванием воздуха.
Среди 383 пациентов, оперированных в нашей клинике, длительное просачивание воздуха было отмечено у 90 (23,5%). При этом нами были выделены следующие понятия: «затянувшееся», «продленное» и «патологическое» просачивание воздуха. Затянувшимся считали просачивание воздуха более 3 сут (58 пациентов/15,1%), продленным — более 7 сут (21 пациент/5,5%), патологическим — более 10 сут (11 пациентов/2,9%).
У пациентов с затянувшимся и продленным просачиванием применяли вспомогательные методы купирования бронхопульмонального свища и послеоперационного пневмоторакса. Повторное дренирование плевральной полости при неадекватном функционировании существующих дренажей применено у 7 (1,8%) больных. С целью уменьшения объема плевральной полости 11 (2,9%) пациентам был наложен пневмоперитонеум. Плевроаспирация была использована у 24 (6,3%). Длительное дренирование у пациентов с малой остаточной полостью было предпринято в 3 наблюдениях (0,8%). Пломбировка остаточной полости аутологичной кровью позволила обтурировать послеоперационный бронхопульмональный свищ у 2 (0,5%) больных.
При сохранении патологического просачивания воздуха в сроки более 10 сут после операции и, как правило, неэффективности вспомогательных методов лечения течение послеоперационного периода считали осложненным. В подобной ситуации считали дальнейшее консервативное ведение неоправданным ввиду высокого риска развития перманентного бронхоплеврального свища и эмпиемы плевры. У 11 (2,9%) пациентов были выставлены показания к повторной операции с целью выявления и устранения причины послеоперационного пневмоторакса. Из них у 9 пациентов первой операцией была диагностическая видеоторакоскопия по поводу диффузных легочных диссеминаций неясной этиологии. Два пациента оперированы повторно после предшествующей видеоторакоскопической резекции по поводу буллезной эмфиземы. Патологическое просачивание воздуха после диагностических видеоторакоскопических резекций именно у данных пациентов, на наш взгляд, связано с основным заболеванием, по поводу которого выполнялась биопсия легкого. Краевая резекция при этом производилась на уровне заведомо пораженных тканей.
Характер исходной патологии у пациентов, которым были проведены повторные вмешательства, представлен в табл. 3.
При выборе доступа для повторного вмешательства ориентировались на выполнение реторакоскопии (у 9 пациентов) или видеоассистированной операции (у 2). Доступ в плевральную полость осуществляли через места ранее стоявших торакопортов. Выполнения дополнительных разрезов не потребовалось. Конверсия в торакотомию после предшествующей реторакоскопии была предпринята у одного больного вследствие неэффективности эндоскопических приемов устранения бронхопульмонального свища.
Наиболее частой находкой во время повторных операций были бронхопульмональные свищи в зоне резекции; они были обнаружены у 7 (1,8%) пациентов. У 5 из них во время первой операции была выполнена резекция с помощью ультразвукового скальпеля, у 2 — аппаратная резекция легкого (УО-40). Свищи располагались преимущественно на поверхностях долей, где силы растяжения легочной ткани выше. Происхождение бронхопульмональных свищей наиболее вероятно было связано с исходным состоянием легочной ткани на уровне резекции или техническими погрешностями при выполнении резекции. Визуализация зоны бронхопульмональных свищей во время повторной операции была возможна после выполнения полноценного пневмолиза в зоне резекции легкого. Как правило, наличие остаточной полости облегчает выполнение манипуляций. В наших наблюдениях все выявленные бронхопульмональные свищи имели паренхиматозное происхождение, т.е. являлись следствием несостоятельности на уровне кортикального слоя паренхимы легкого. У 4 больных свищи располагались поверхностно на уровне резекции, у 3 других — в глубине воронкообразной раны легкого.
У одного (0,3%) пациента после диагностической краевой резекции легкого также сформировался персистирующий бронхопульмональный свищ. Плановое гистологическое исследование позволило выявить неясной этиологии организующую пневмонию, что было неблагоприятным прогностическим фактором в плане возможности спонтанного закрытия свища. При повторной видеоторакоскопии причиной персистенции свища оказались плевролегочная спайка в непосредственной близи от патологической зоны и постоянная тракция легочной ткани при дыхании.
В одном (0,3%) наблюдении при реторакоскопии были выявлены буллы, не замеченные во время первой операции.
Неадекватное функционирование дренажей вследствие их миграции обнаружено при повторной операции у одного (0,3%) пациента, обтурация дренажа — также у одного (0,3%).
Окончательное распределение пациентов в зависимости от причины патологического просачивания воздуха было следующим:
Бронхопульмональный свищ в зоне резекции — 7, незамеченная неликвидированная во время первой операции причина пневмоторакса — 1; надрыв легкого из-за наличия спайки с грудной стенкой — 1; миграция дренажа — 1; обтурация дренажа — 1.
С целью устранения причины послеоперационного пневмоторакса у 7 пациентов выполнено прошивание зоны свища П-образными атравматичными швами. Несмотря на воспаление, отек и рыхлость легочной ткани, подобное прошивание достаточно эффективно и технически просто выполнимо.
У 2 больных выполнена аппаратная резекция края легкого, несущего свищ или буллу. На линию шва с целью ее укрепления во всех наблюдениях проводилась аппликация пластин ТахоКомб соответствующего размера.
У 2 пациентов с неадекватным функционированием дренажной системы соответствующее редренирование позволило ликвидировать послеоперационный пневмоторакс. Во всех случаях интраоперационно легкое расправлено с помощью гипервентиляции. Осложнений после повторных операций не отмечено. Средние сроки просачивания воздуха составили 1,5 сут, окончательного расправления легкого и удаления дренажей — 2,6 сут.
Заключение
Хирургическая тактика при длительном просачивании воздуха базируется на оценке расправления легкого в послеоперационном периоде. Объективными критериями расправления легкого являются: степень просачивания воздуха по подводному дренажу, рентгенологическая картина выполнения легким плевральной полости, отсутствие или наличие подкожной эмфиземы. Показания к реторакоскопии возникают в тех случаях, когда примененный лечебно-диагностический алгоритм оказывается неэффективен и имеются веские основания для хирургического устранения причины пневмоторакса, поскольку дальнейшее выжидание сопряжено с высоким риском развития послеоперационной эмпиемы плевры с бронхоплевральным свищем. Во время повторного видеоторакоскопического вмешательства можно визуализировать область бронхопульмонального свища, выполнить прошивание этой зоны, провести дополнительные мероприятия по обеспечению аэростаза, выполнить прицельное адекватное дренирование плевральной полости.
ПРОСАЧИВАНИЕ ВОЗДУХА ПОСЛЕ РЕЗЕКЦИИ ЛЕГКИХ
Цель - провести анализ причин послеоперационного просачивания воздуха и предложить лечебно-диагностический алгоритм при этом осложнении. Материал и методы. В исследовании проведены анализ причин длительного просачивания воздуха после различных резекций легких, группировка причин по их принадлежности, предложены определения основных понятий. Результаты. Наиболее частыми причинами длительного просачивания воздуха являются несостоятельность линии резекции легкого, невыявленная (неустраненная) причина пневмоторакса, неадекватное функционирование дренажной системы. Описаны различные тактические подходы при данной проблеме. В зависимости от эффективности вспомогательных методик определены показания к повторным операциям. Выводы. Знание причин послеоперационного продленного и патологического просачивания воздуха является основой для оптимизации тактики ведения пациентов после резекции легких.
Ключевые слова
Полный текст
Причины боли после установки пломбы
Лечение зубов — медицинская процедура, корректирующая улыбку, исправляющая недостатки и избавляющая пациента от боли. Однако неприятные ощущения после стоматологического вмешательства, в частности — после установки пломбы, проходят не сразу.
В 90% случаев легкая болезненность закономерна, поскольку пломбирование затрагивает нервы, каналы, ткани. На то, чтобы пломба “прижилась”, требуется время. В этот период боль может быть постоянной затухающей либо переменной, спровоцированной раздражителями: горячим чаем, сильным нажатием на десну и пр.
Но есть и другие боли — патологические. Они требуют нового медицинского вмешательства и тщательного лечения. Рассмотрим каждый вариант подробнее.
Неопасная боль
Естественной постпломбировочной болью считается та, что возникла после лечения и прошла самостоятельно через относительно небольшой промежуток времени. По характеру такая боль ноющая и легкая, способная иногда усиливаться при:
- нажатии (сильной чистке зубов, кусании);
- чередовании горячих и холодных блюд;
- сильном стрессе;
- переохлаждении.
Период восстановления разный и зависит от типа лечения:
- если врач удалял кариозные образования, болезненность может сохраняться, в среднем, от 3 до 5 дней;
- после пломбировки каналов боль исчезает, как правило, через пару недель, иногда — через месяц;
- после депульпирования (удаления сосудисто-нервного пучка внутри канала) нормой становится период от одного до двух месяцев.
Правило общее: чем серьезнее и глубже было стоматологическое вмешательство, тем длительнее период реабилитации.
Боль под временной пломбой не считается опасной, если возникает при надавливании на зуб. Если же ощущения очень болезненные, необходимо повторно обратиться к врачу для дополнительного обследования.
Уточненная диагностика позволит избавиться от недостатков при замене временной пломбы на постоянную.
При лечении зуба важно подобрать размер пломбы правильно
Опасные постпломбировочные боли
Нередки случаи, когда боль после установки пломбы служит сигналом о серьезной проблеме, способной подорвать здоровье пациента. Такая боль не проходит сама, независимо от того, лечили вы кариес или пульпит.
Опасная боль связана с инфекцией в тканях и характеризуется:
- повышенной болезненностью в области лечения;
- болями во время еды и питья, даже если блюда комнатной температуры;
- повышением температуры тела, в некоторых случаях — лихорадкой и ознобом;
- припухлостью десны;
- сильным отеком и покраснением щеки;
- появлением ощущения, что зуб мешает: выпирает, готов выпасть;
- некрозом тканей, из-за чего во рту появляется гнилостный запах.
При появлении хотя бы одного из вышеперечисленных признаков следует обратиться за помощью к врачу, чтобы избежать осложнений.
Причины опасных болей
Установить причину, спровоцировавшую развитие инфекции, поможет диагностика. В этом случае важно выбрать грамотного стоматолога, поскольку в большинстве случаев именно неточность осмотра приводит к неправильному диагнозу и появлению зубных болей.
- Врачебная ошибка (спешка, халатность) включает в себя несколько подпричин, подтолкнувших пациента к повторному посещению зубного кабинета (как правило, в другой клинике и у другого специалиста), лечению и перепломбировке.
Итак, к таким причинам относят:
Чреват тем, что врач не заметит серьезных проблем: например, воспаления, начавшегося в каналах еще до лечения. В результате лечение будет неполноценным: кариес пролечен, а пульпит с инфицированными каналами остались.
- установку пломбы без соблюдения требований безопасности.
Такая процедура приведет резким болям как только пройдет действие анестезии.
- слишком большую или маленькую пломбу, нарушающую прикус.
При этом надо понимать, что на усадку любой пломбы, даже подобранной со всей точностью, требуется время.
Если через день-два после пломбирования ощущение дискомфорта (пломба выпирает, давит на зуб или, напротив, оседает; зуб мешает; неудобно/больно есть) не исчезло, необходим повторный осмотр и корректировка пломбы/установка новой.
Отлом инструмента при чистке каналов — одна из причин болей
Спешка при подготовке зуба к лечению чревата дальнейшем развитием инфекции. Профессионал всегда тщательно обрабатывает полость зуба, даже с учетом сложного строения каналов. Педантичность позволяет предотвратить возникновение и дальнейшее развитие инфекции.
Важно правильно высушить полость зуба, ведь если недосушить стенки, пломба не зафиксируется, если пересушить — появится повышенная чувствительность зуба.
Бормашина работает на больших оборотах, неизбежно нагревая обрабатываемый участок. Если врач не проводит охлаждение (воздушное и водное), ткани перегреваются, возникает ожог нерва.
В такой ситуации боль после пломбирования не исчезнет, а будет развиваться, приведя через некоторое время к пульпиту.
Спешка и невнимательность при работе с медицинскими инструментами недопустимы. В противном случае при пломбировании в полости может остаться осколок. Неудаленный вовремя, он провоцирует сильные боли, гнойное воспаление, приводит к отекам.
- Вторая причина связана уже не с врачом, а с пациентом и заключается в нарушении рекомендаций.
Главное требование к пациенту — не перегружать зуб и не забывать о регулярной гигиене.
После пломбирования врач объясняет, как правильно ухаживать вылеченным зубом и всей полостью рта. В первые два-три дня важно поберечь зуб, избегая сильного механического воздействия. От твердой пищи (орехов, сухарей) и вязких блюд (молочные каши, супы-пюре) стоит отказаться.
После анестезии стоит воздержаться от еды, поскольку из-за временной потери чувствительности можно повредить мягкие ткани: порезать твердой пищей, обжечь горячим напитком.
Зуд и покраснение - одни из признаков аллергии на композит
Индивидуальная непереносимость компонентов препарата способна спровоцировать постпломировочные боли. Аллергическая реакция проявляется обычно на красители и консерванты, входящие в состав пломбировочного материала. Если проблема именно в этом, в следующий визит врач подберет другой состав пломбы.
Признаки аллергии на пломбу:
- болезненность;
- опухшая десна;
- сыпь на коже, зуд;
- приступ астмы.
Лечение постпломбировочных болей
Домашнее лечение боли, возникшей после пломбирования, чревато серьезными осложнениями. Если оперативный поход к врачу приходится отложить на несколько дней (когда боль застает вас в отпуске или в командировке), можно временно ее заглушить при помощи:
- полоскания травами (успокаивающим действием обладают отвары из ромашки, календулы, шалфея);
- обеззараживания антисептиками (полоскание, использование спрея).
Болеутоляющие таблетки и противовоспалительные средства стоит принимать с осторожностью, обязательно в соответствии с инструкцией.
Поход к врачу не стоит откладывать никогда. Но в некоторых случаях это нужно делать незамедлительно. Промедление опасно, когда:
- боль стала непереносимой;
- поднялась температура;
- начались воспаления (десны, щеки);
- увеличились лимфоузлы;
- образовались гнойники.
Незавершенное лечение грозит серьезными осложнениями: развитием пульпита, некрозом тканей, разрушением и выпадением зуба. Потому постарайтесь не терять контакта с лечащим врачом, пока не пройдет период постпломбировочного восстановления.
Читайте также:
