Примеры метастаза рака легкого в хориоидею
Добавил пользователь Валентин П. Обновлено: 28.01.2026
Метастатическим или вторичным раком легких называются опухоли, которым дают начало раковые клетки, попавшие в легочную ткань из других органов.
Лёгкие - излюбленная мишень для метастазирования опухолей
Статистика говорит о том, что у 30-55% онкологических больных обнаруживаются метастазы в легких. Злокачественные опухоли дают отсевы в лёгочную ткань: рак любого органа, саркомы, меланомы, заболевания кроветворной и лимфатической системы. Через лёгкие проходит вся кровь, и условия благоприятны для выживания бактерий, вирусов, грибов и опухолевых клеток.
Собирающий лимфу общий лимфатический проток несёт её в крупные вены, которые впадают в верхнюю полую вену. При посредстве правых отделов сердца венозная кровь, смешанная с лимфой, тоже проходит через лёгкие. Площадь структурных единиц, составляющих то, что мы называем лёгкими - лёгочных альвеол - более 150 квадратных метров. Достаточно места, изумительное полнокровие, прекрасные условия для размножения злокачественных клеток.
Иными словами, присутствуют благоприятные условия для распространения раковых клеток в легкие гематогенным (через кровь) и лимфогенным (через лимфатическую систему) путем.

Классификация метастаз в лёгких
Метастатические узлы бывают очень разными, считают, что по плотности они полное отражение первичной опухоли. Если определять плотность на ощупь, то все опухоли тяготеют к каменистости или, по крайней мере, к костной плотности. Но плотность для очагов в лёгких понятие относительное, прощупать их можно только во время операции, которую в метастатической стадии делают чрезвычайно редко. Плотность определяют при рентгенологическом исследовании преимущественно для дифференциальной диагностики, то есть поиска признаков характерных отличий одного заболевания от другого.
Формально метастазы делят на лимфогенные и гематогенные, то есть занесенные в лёгочную ткань с лимфой или кровью, но в каждом конкретном случае разобрать, что принесло раковую клетку в альвеолу вряд ли можно, и практикующему онкологу совсем ненужно, ведь это уже ничего не изменит. Какие бы ни были метастазы по пути распространения, их надо лечить.
Метастазы в лёгких бывают разными по форме, ее определяют по рентгеновским снимкам:
- Очаговые метастазы, которые на рентгеновском снимке видны образования разного диаметра. Традиционно этот вариант метастазирования считается проявлением менее агрессивной злокачественной опухоли. При небольшом распространении более благоприятно протекают именно очаговые образования. Они как раз считаются преимущественно гематогенными, то есть занесёнными кровью.
- Инфильтративные метастазы, когда опухолевые клетки расползаются по эпителиальной выстилке альвеол, что на рентгенограмме проявляется в виде сетки или разной формы затемнений. Такой вариант традиционно считают вариантом более агрессивной опухоли - агрессивные по течению меланомы и саркомы дают преимущественно очаговые, а не инфильтративные метастазы в лёгких. Эти вторичные проявления относят к лимфогенным.
- Смешанные метастазы - сочетание очаговых и инфильтративных «теней» в лёгких - частое явление в клинической практике.
По числу метастазы могут быть:
- солитарными - один очаг;
- единичными - не более десяти;
- множественными.
Метастатические узлы бывают мелкими и крупными, а ещё сливающимися друг с другом, односторонними, когда поражено одно лёгкое и двухсторонними.
Вокруг метастазов тоже могут жить бактерии, всё-таки по бронхиальному дереву проходит нестерильный воздух, а опухоль меняет местный иммунитет, и возникает воспаление. Когда внутренняя часть опухоли не получает достаточного питания - она отмирает, и в центре образуется полость распада. Если такая полость соединится с бронхом, то в неё могут попасть бактерии, и полость заполнится гноем.
В чем разница между метастазами в легких и метастазами в плевре?
Плевра - пленка из соединительной ткани. Она состоит из двух листков: один покрывает снаружи легкие, а другой выстилает изнутри стенки грудной полости. Плевра интимно спаяна с лёгким. В ней тоже могут возникнуть метастазы, но намного реже. Опухоли из легких могут прорастать в плевру и наоборот. Зачастую в легких обнаруживаются метастазы, а плевра не поражена.
Диагностика
При подозрении на метастазы в легких прибегают к следующим методам диагностики:
- Рентгенография. Простой и быстрый, но не самый информативный метод диагностики. Обычно на снимках можно увидеть только опухоли размером более 1 см;
- Компьютерная томография. Позволяет обнаружить очаги менее 5 мм. Это недоступно для рентгенографии и МРТ;
- Биопсия легкого. Обычно проводится при помощи иглы. Получают небольшой фрагмент ткани опухоли для исследования;
- Бронхоскопия. Эндоскопическое исследование, во время которого специальный инструмент с источником света и видеокамерой - бронхоскоп - вводят в бронхиальное дерево. Во время процедуры можно провести биопсию.
Как правило, динамическое наблюдение за онкологическим пациентом после лечения первичной опухоли предполагает регулярную рентгенографию органов грудной клетки. При выявлении теней в лёгких, правильно будет сделать компьютерную томографию с введением контрастного вещества. КТ способна выявить очаги меньше 5 мм, что недоступно магнитно-резонансной томографии. В дальнейшем для контроля динамики процесса после лечения также необходимо будет делать КТ.
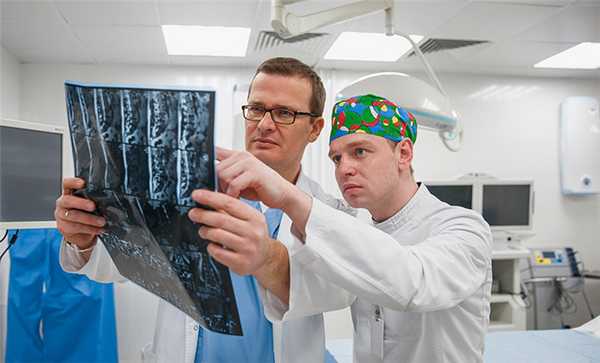
Бессмысленно перед лечением делать КТ, а после перейти на обычную рентгенографию лёгких, пытаясь сравнивать снимки, чтобы выявить отличие прошлого состояния лёгких с настоящим. КТ обнаружит более мелкие образования, рентген способен в лучшем варианте выявить очаги более 1 см, то есть опухоли меньше сантиметра «выпадают» из-под контроля, когда нет возможности сделать контрольное КТ-обследование. Нельзя оценивать эффект лечения по паре видимых крупных очагов. Некоторые опухоли от химиотерапии уменьшаются, какие-то увеличиваются, а другие месяцами стабильны.
Клиническая симптоматика
Клинические признаки метастазов в лёгких зависят от обширности поражения и присоединения воспалительных изменений.
- боль в груди;
- упорный кашель;
- примесь крови в мокроте;
- ослабленное дыхание;
- хрипы;
- слабость;
- снижение веса.
При одиночных очагах округлой формы, небольшого размера никаких признаков поражения может и не быть, их часто случайно обнаруживают при контрольном обследовании. Площадь лёгких огромна, и несколько квадратных сантиметров опухолевого поражения альвеол не отразятся на газообмене и состоянии пациента. Множество теней, когда их уже не пересчитать, ухудшат самочувствие, провоцируя сухой кашель, плохо откликающийся на средства от кашля.
Инфильтративные метастазы раньше меняют самочувствие, поскольку к ним часто присоединяется воспаление окружающей опухоль ткани - пневмонит. Появляется кашель, может быть температура, слабость, почти как пневмония, но чуть-чуть полегче. Закупорка бронха опухолью приведёт к ателектазу - полной безвоздушности части лёгкого, присоединение инфекции существенно ухудшит состояние, повысится температура, появится одышка. Приём антибиотиков помогает снять воспаление и самочувствие улучшается, но ненадолго, потому что опухоль растёт, и безвоздушная часть лёгкого тоже увеличивается. И опять воспаляется, так и идёт по замкнутому кругу.
Лечение метастазов в лёгкие
Сегодня оперировать метастазы в лёгких стали чаще, чем раньше, но всё-таки операции делают довольно редко. Радикальное лечение метастазов в лёгкие - оперативное в принципе возможно при определённых условиях:
- не должно быть первичной опухоли или рецидива;
- не должно быть метастазов в других органах;
- метастаз в лёгком очаговый и единственный или не более 3 очагов;
- скорость прогрессирования опухолевого процесса должна быть невысокой, как правило, после радикального лечения первичной опухоли до появления метастаза должно пройти более года;
- со времени появления метастаза в лёгком в течение полугода не должно появиться других метастазов;
- состояние пациента должно позволять довольно сложное оперативное вмешательство, потому что во время операции реальная ситуация может оказаться значительно хуже, чем описывалась при компьютерной томографии, и придётся удалять больше запланированного.
Основное лечение метастазов в лёгких - химиотерапия, схема которой определяется первичной опухолью, при раке молочной железы ещё и гормональная терапия, естественно, при наличии чувствительности к ней.
Лучевая терапия множественных метастазов в лёгких проводилась в экспериментальных группах, результаты неудовлетворительные. При единственном довольно крупном очаге облучение возможно, но эффективность много хуже, чем при раке лёгкого. Наличие метастаза, где бы то ни было, показатель диссеминации - разброса злокачественных клеток, что не предполагает хорошего прогноза в отношении возможности полного излечения.
Каковы прогнозы выживаемости?
Метастазы в любом органе говорят о том, что защитные силы организма исчерпаны, опухолевые клетки успели распространиться по разным органам. Ремиссия в большинстве случаев невозможна. Но это не означает, что врач совсем ничего не может сделать. Паллиативное лечение поможет продлить жизнь, избавит от мучительных симптомов.
Паллиативная помощь при метастазах рака в легкие
Часть легкого, занятая опухолью, выключается из процесса дыхания. Поначалу оставшаяся здоровая ткань успешно справляется и работает за целое легкое. Но постепенно опухоль растет, перестает реагировать на химиотерапию и занимает все больше места.Наступает момент, когда оставшаяся здоровая ткань перестает справляться. Легкие больше не могут обеспечить организм нужным количеством кислорода, развивается дыхательная недостаточность. Кислородное голодание затрагивает все органы, в первую очередь — сердечно-сосудистую систему.

Симптомы дыхательной недостаточности нарастают постепенно:
- Поначалу возникает лишь одышка после ходьбы и физических нагрузок;
- Затем одышка начинает беспокоить при минимальных нагрузках, при любой движении;
- В тяжелых случаях человек задыхается постоянно, даже когда лежит в постели. Больного мучит постоянный кашель, слабость, на ногах появляются отеки, сердцебиение учащается. Стоит совершить небольшое движение, и все симптомы усиливаются на порядок.
Страдания больного может облегчить кислородотерапия. Но проводить ее нужно по 15 часов в день. Существуют специальные дыхательные маски, их можно приобрести, и все же проводить такое лечение в домашних условиях очень сложно.
Государственные онкологические клиники не госпитализируют таких пациентов в экстренном порядке. Помощь можно получить в отделении паллиативной медицины, но таких в России пока еще очень мало. В обычном стационаре практически ничем не помогут. Кислородотерапию можно получить в хосписе, но там практически нет симптоматической терапии. При тяжелой дыхательной недостаточности одной кислородотерапии недостаточно. Нужна дыхательная поддержка — искусственная вентиляция легких. В данном случае ИВЛ проводят через маску, интубацию трахеи не проводят.
Такое лечение не избавит от рака и не уничтожит метастазы, но оно способно сильно облегчить состояние больного:
- уменьшится одышка;
- отдохнуть дыхательные мышцы, которым в последнее время пришлось интенсивно работать;
- нормализуется состав крови, уменьшится кислородное голодание;
- уменьшатся даже воспалительные изменения в легких;
- в конце концов, человек перестанет задыхаться, улучшится качество жизни.
Помочь человеку с тяжелым нарушением дыхания в домашних условиях невозможно. Родные постоянно слышат, как он тяжело дышит, хрипит, кашляет, но помочь ничем не могут. Страдают все.
Врачи онкологи и реаниматологи клиник «Евроонко» знают, как помочь пациенту с метастатическим раком легких в рамках паллиативной помощи. Грамотное лечение избавит от тяжелых симптомов, подарит драгоценное время.
Примеры метастаза рака легкого в хориоидею
Московский радиологический научный центр им. А.Ф. Цыба — филиал ФБГУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, Обнинск, Россия
Медицинский радиологический научный центр Минздравсоцразвития России, Обнинск
ФГБУ "МНИОИ им. П.А. Герцена" Минздрава России
Легочные метастазы: классификация и необходимость стадирования?
Журнал: Хирургия. Журнал им. Н.И. Пирогова. 2018;(3): 22‑26
В последние годы увеличивается интерес к хирургическому лечению метастазов в легких, на сегодняшний день одной из значимых проблем является отсутствие их единой классификации. Чаще всего литературные данные демонстрируют увеличение показателей выживаемости у пациентов, перенесших радикальное хирургическое лечение по поводу метастатического поражения легких. Но уровень доказательности остается слабым и базируется, в основном, на ретроспективных исследованиях. Дополнительную сложность создает использование различных классификаций метастазов, не всегда учитывающих не только их количественное, но и регионарное распространение. В настоящей статье представлен анализ классификаций легочных метастазов, используемых в отечественной и зарубежной литературе в настоящее время, предложен вариант стадирования метастатического поражения в легких в зависимости от количественного и локорегионарного процесса. Разработка классификации легочных метастазов поможет разделить пациентов с метастатическим поражением на однородные подгруппы и позволит провести проспективные и рандомизированные исследования для получения объективных результатов об итогах применения хирургического или иных методов локального лечения пациентов с внутрилегочными метастазами.
Примерно у 30% больных со злокачественными солидными опухолями в анамнезе при контрольных обследованиях выявляются легочные метастазы [1]. В настоящее время считается, что пациенты с легочными олигометастазами, контролируемой первичной опухолью и удовлетворительными функциональными запасами дыхательной системы потенциально излечимы. До 1985 г. в реферативных журналах было представлено около 300 работ, посвященных этой теме, к 2015 г. число публикаций увеличилось в 10 раз и достигло 3000. Наиболее крупное проспективное исследование (PulMiCC) было начато в Великобритании в 2010 г. и направлено на изучение метастазэктомий при колоректальном раке [2]. Спустя несколько лет исследования с похожим дизайном были открыты в Сербии, Италии и Китае [3, 4]. Пока полноценные результаты данных исследований в литературе не представлены.
Хотя на сегодняшний день нет результатов рандомизированных исследований, сравнивающих хирургическое лечение с другими методами, показатели 5-летней выживаемости после проведенной метастазэктомии легких для опухолей различного гистогенеза варьируют в пределах от 20 до 80% [5]. Одним из главных условий увеличения показателя общей выживаемости данных пациентов является выполнение радикальной операции (возможность резецировать все пораженные участки легочной ткани) [1]. Современные руководства рекомендуют торакотомию в качестве доступа при единичных и множественных очагах для адекватной интраоперационной пальпации легкого с целью выявления возможных дополнительных очагов, не визуализированных при дооперационных исследованиях [6]. Тем не менее, несмотря на эту агрессивную тактику, снижение респираторной функции и хронические боли, у 50% пациентов развиваются локальные рецидивы [7, 8].
Несмотря на повышение интереса к хирургическому методу, активные разработки новых способов воздействия на легочную паренхиму и внедрение новейших методов лечения, остается множество нерешенных вопросов в тактике лечения, особенно у пациентов с множественным поражением и рецидивными очагами в легких. Одной из причин является то, что на данный момент не существует общепринятой классификации метастазов, уточняющих их количество и учитывающих лимфогенное поражение.
Классификация легочных метастазов
При отборе пациентов на хирургическое лечение большинство исследователей пользуются критериями, разработанными N. Thomford и соавт. в 1965 г. [9], включающими в себя: возможность радикального выполнения операции, удовлетворительное состояние пациента (по шкале ECOG 0−1, либо по шкале Карновского >80%), наличие контроля над первичным очагом и отсутствие других отдаленных очагов. В последнее время критерии расширяются, например, наличие метастазов в печени не является абсолютным противопоказанием к операции на легком при колоректальном раке [10, 11].
На сегодняшний день в отечественной литературе общепринятым является деление очагов в легких на:
— солитарный (1 очаг);
— единичные (2—3 очага);
— множественные (4 и более очагов).
Также выделяют одно- и билатеральное поражение.
В середине 1990-х годов S. Hellman и R. Weichselbaum [12] предложили альтернативный термин «олигометастаз», означающий наличие изолированных метастазов (до 5), которые могут находиться в пределах нескольких органов. В зарубежной литературе под термином «oligometastases» подразумевается, что пациент потенциально излечим.
При использовании вышеприведенных классификаций в проведении исследований получаются подгруппы, которые могут различаться по распространенности процесса, но при этом они будут объединены в одну группу.
Например: у больных с идентичным гистогенезом первичной опухоли, по результатам спиральной компьютерной томографии органов грудной клетки, у одного пациента выявлено 25 очагов в обоих легких и увеличенные медиастинальные лимфатические узлы, у второго по результатам СКТ визуализируется лишь 4 очага без поражения лимфатических коллекторов. Таким образом, по данной классификации оба пациента попадают в группу с множественным поражением легких, несмотря на различную распространенность по легочной паренхиме и лимфатическим узлам.

По нашему мнению, стоит разработать и использовать классификацию легочных метастазов, в которой будет учитываться не только количество очагов в легких, но и поражение лимфатических узлов (табл. 1). Таблица 1. Стадирование метастатического поражения легких с учетом количественного и локорегионарного распространения Примечание. * — в категории М можно использовать префикс 1 или 2 для уточнения одностороннего или билатерального поражения.
В вышеприведенной классификации отображается метастатическое распространение не только гематогенным, но и лимфогенным путем. В данной классификации можно использовать префикс «ус» или «ур» после проведенного неоадъювантного лечения для оценки эффективности проведенной терапии [13].
Это позволит разграничить группы пациентов и поможет в проведении проспективных рандомизированных исследований.
В настоящее время ведущей теорией лимфогенного и гематогенного метастазирования онкологического процесса является «каскадная теория». Согласно ей метастазирование является многоступенчатым процессом. В 2011 г. Л. Нортон [14] предложил гипотезу «self-seeding» (теория самозасева), в которой процесс метастазирования является двунаправленным, распространение злокачественных клеток включает в себя рециркуляцию, реинфильтрацию и колонизацию первичного очага (преметастатическая ниша). Таким образом, после формирования отдаленного метастаза опухолевые клетки могут возвращаться в системный кровоток и колонизировать первичную опухоль. Это характеризует метастазирование не только как формирование отдаленных очагов, но и как продолженный рост первичного очага. Таким образом, эта гипотеза позволяет разделять метастатическое поражение на активность первичного очага, поражение лимфатических коллекторов и количество отдаленных внутрилегочных очагов.
Согласно критериям Thomford, которые незначительно поменялись за десятилетия, для выполнения хирургического лечения на легком одним из важных показаний является отсутствие внелегочных метастазов [9]. Мы выделили подгруппы по распространенности процесса первичного очага:
— T0 — нет рецидива первичной опухоли и внелегочных отдаленных метастазов;
— T1 — есть рецидив первичной опухоли и/или внелегочные отдаленные метастазы.
Отдельной когортой пациентов являются больные с первично-установленным диагнозом злокачественного новообразования и наличием очагов поражения в легочной паренхиме. Обнаружение солитарного узла в легочной ткани синхронно с первичной опухолью вызывает диагностические сложности в его трактовке. По данным литературы, в 37,5% случаев [15] выявленные очаги не окажутся метастатическими, что позволяет рестадировать пациента и поменять тактику лечения. Мы решили вынести эту подгруппу в отдельную.
— T1s — синхронное выявление первичного очага и отдаленных метастазов в легкие.
По данным литературы, распространение метастатического поражения на лимфатическую систему имеет неблагоприятный прогноз показателя общей выживаемости [16—18], а частота поражения лимфатических узлов составляет до 25% при различных видах опухолей. Поэтому более активно ставится вопрос о необходимости выделения подрупп с учетом поражения лимфатических узлов. Система стадирования, которая принимает во внимание метастазы как в легких, так и в лимфатических коллекторах, необходима с целью классифицировать эту когорту пациентов для прогнозирования результатов лечения.
Для увеличения показателя общей и безрецидивной выживаемости необходимо радикальное удаление легочных метастазов и пораженных лимфоколлекторов. Таким образом, желательно дооперационное морфологическое подтверждение поражения лимфатических узлов с помощью эндобронхиальной ультразвуковой трансбронхиальной аспирационной биопсии лимфатических узлов, медиастиноскопии, эндоскопических вмешательств, чтобы избежать ненужного хирургического вмешательства.
В данной классификации распространение процесса на лимфатические узлы ранжируется отдельно. Мы считаем, что лимфогенное метастазирование (категория N) должно определяться исходя не из размеров метастаза в лимфатическом узле, а от «региона» поражения.
— N0 — данных за увеличенные лимфатические узлы нет;
— N1 — поражение медиастинальных и/или корневых лимфатических узлов с одной стороны;
— N2 — билатеральное поражение медиастинальных и/или корневых лимфатических узлов;
— N3 — поражение внелегочных лимфатических узлов.
Стоит отметить, что увеличение лимфатических узлов по данным КТ не является абсолютным противопоказанием к хирургическому лечению метастазов в легких. Лимфодиссекция является важным прогностическим инструментом, который может влиять на дальнейшие терапевтические решения [19, 20].
В категории М показана распространенность метастатического поражения только легочной паренхимы. У пациентов с солитарным очагом прогноз общей выживаемости выше, чем при наличии большего количества метастазов, но в литературе мы не встретили верхнюю границу, после которой операция будет нецелесообразна.
При солитарном поражении хирургическое лечение является лечебно-диагностическим методом. Это позволяет нам присвоить категорию M1s.
При таком распространении целесообразно применение видеоторакоскопических операций. Это миниинвазивный доступ, при котором имеются преимущества для пациента, такие как менее выраженный послеоперационный болевой синдром, более короткий восстановительный период и соответственно меньший срок нахождения в стационаре по сравнению с традиционным хирургическим доступом торакотомией. По результатам исследований, при солитарном поражении [21] и единичных метастазах в легких показатель общей выживаемости не отличается от выбора эндоскопического доступа или торакотомного [22, 23].
Как уже упоминалось, в англоязычной литературе [24] встречается термин «олигометастазы», подразумевающий под собой наличие до 5 метастатических очагов — это соответствует M1о в нашей классификации. Под термином «oligometastases» понимают, что пациент потенциально излечим, и применение агрессивного хирургического подхода не вызывает сомнения. Также, наряду с традиционным хирургическим доступом (торакотомией) и операциями с малоинвазивными доступами (эндоскопические операции), могут быть использованы и операции с удалением опухоли in situ, такие как радиочастотная термоабляция. Четких критериев количества очагов в легких и их минимальных размеров на основе которых будет выбран определенный метод лечения, нет.
В представленных работах встречаются данные об удалении свыше 100 метастатических очагов [25, 26], но, основываясь на опыте нашей клиники, удаление свыше 25 очагов позволяет увеличить показатели выживаемости пациента (категория Mm) в крайне редких случаях у тщательно отобранных пациентов, учитывая и другие прогностические факторы (гистогенез первичной опухоли, время безрецидивной выживаемости). Количество очагов свыше 6, но менее 24, обозначается как ML.
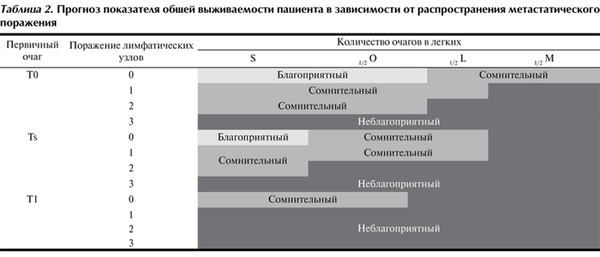
Можно использовать префикс 1 или 2 перед обозначением количественного распространения очагов для оценки одно- или билатерального поражения. Использование данной классификации может стать основой прогноза хирургического вмешательства (табл. 2). Таблица 2. Прогноз показателя общей выживаемости пациента в зависимости от распространения метастатического поражения
Стоит отметить, что в вышеприведенной классификации не учитываются прогностические факторы, такие как гистогенез первичного очага, показатель времени безрецидивной выживаемости, размер очагов. Поэтому до получения результатов проспективных исследований должен сохраняться индивидуальный подход к тактике лечения пациентов с метастатическим поражением легких.
Заключение
Данная классификация поможет онкологам и торакальным хирургам для стадирования легочных метастазов и в выборе адекватной тактики, в том числе и хирургии, как одного из этапов лечения. Первоочередной задачей классификации легочных метастазов является тщательное разграничение распространенности процесса для оценки возможности полного удаления метастазов в легких. Больных с синхронным поражением и ограниченным метастатическим поражением легких необходимо рассматривать в качестве кандидатов для симультанных операций по удалению первичного очага и метастазов. На основании данной классификации может быть разработана прогностическая шкала с сочетанием неблагоприятных факторов.
В последние годы наблюдается рост метастатических опухолей органа зрения, что, по всей вероятности, связано с увеличением продолжительности жизни онкологических больных [3]. Есть мнение, что процент прижизненной диагностики внутриглазных метастазов в несколько раз ниже, чем при аутопсийных исследованиях. Так, Eliasi-Rad В. с соавторами (1996 г.) при вскрытии 741 больных, умерших от рака, у 93 (12,6%) обнаружили внутриглазные метастазы [1]. Возможно, и эти данные не отражают частоту метастатического поражения органа зрения, так как далеко не каждый больной, умерший от злокачественной опухоли, подвергается вскрытию, а если вскрытие и производится, то глазное яблоко часто исключается из гистологического исследования, то есть истинная частота метастазов в глаз и орбиту может быть значительно выше. Существует даже точка зрения, что в наши дни метастатический рак хориоидеи является одной из наиболее часто встречающихся внутриглазных опухолей [2]. Последнее утверждение сомнительно, но очевидно, что офтальмологи выявляют далеко не все случаи метастатического поражения органа зрения, и значительная часть бессимптомно протекающих метастазов так и остается не выявленной.
Наиболее частыми первичными опухолями, при которых возникают метастазы в орган зрения, являются рак молочной железы, рак легкого и кожная меланома. С меньшей частотой, но практически все виды опухолей могут метастазировать в глаз и орбиту. По нашим данным, больные с метастазами рака молочной железы составляют 67,5% среди всех пациентов с метастатическим поражением органа зрения. Второе место по частоте метастазирования в глаз и орбиту занимает рак легкого - 14,4%. Совокупность всех остальных первичных опухолей (кожная меланома, рак кишечника, желудка, щитовидной и предстательной желез, матки, яичников и т.д.) составляет 18,1% (табл.).
Следует особо подчеркнуть, что метастатическое поражение органа зрения может быть первым проявлением скрыто протекающей первичной опухоли, что по нашим данным составляет около 11%. это особенно характерно для рака легкого.
Возможность выявления метастаза в орган зрения раньше первичной опухоли обязывает офтальмологов изучать особенности клинического проявления метастатических опухолей. Клиническая картина метастатической опухоли зависит от поражения определенного отдела органа зрения и гистогенеза первичной опухоли.
Метастатические опухоли глаза и орбиты при раке молочной железы, как правило, возникают через 2-4 года с момента диагностики первичной опухоли. Возможно развитие внутриглазного метастаза даже через 10-11 лет с момента диагностики рака молочной железы. При раке легкого и других злокачественных опухолях метастатическое поражение органа зрения развивается значительно раньше: в 77% случаев в течение первого года с момента диагностики первичной опухоли.
Среди метастазов в орган зрения солидных опухолей преобладают внутриглазные опухоли (рис. 1). В основном наблюдается поражение задних отделов сосудистой оболочки - хориоидеи. По нашим данным, метастазы в радужку и цилиарное тело возникают приблизительно в 10 раз реже, чем метастазы в хориоидею.
Метастатические опухоли радужки при раке молочной железы выглядят, как рыхлые белые или желтоватые образования с нечеткими границами, вызывающие в той или иной степени деформацию зрачка (рис. 2). Внешне они напоминают воспалительную гранулему или беспигментную лейомиому, но, в отличие от последних, характеризуются локальным расширением эпибульбарных сосудов на стороне поражения радужки, быстрыми темпами роста опухоли и отсутствием клеточного выпота в стекловидное тело. Метастаз рака легкого выглядит в виде слабо васкуляризированной опухоли с бугристой поверхностью и напоминает беспигментную меланому. Необходимо обратить внимание на то, что на поверхности метастатической опухоли, в отличие от первичных опухолей радужки, как правило, не видно сосудов. Нередко наблюдается многофокусное поражение радужки. Мы наблюдали у одной больной метастаз рака молочной железы в виде узкой полоски желтоватой ткани вдоль всего угла передней камеры, что привело к развитию вторичной некомпенсированной глаукомы. У другой больной метастаз кожной меланомы выглядел в виде диффузной инфильтрации радужки пигментированной тканью с формированием задних синехий. Метастатическое поражение радужки и цилиарного тела в 80% случаев сопровождается развитием вторичной глаукомы или иридоциклитом с “сальными” преципитатами на эндотелии.
Метастатическая опухоль хориоидеи, как правило, характеризуется быстрыми темпами роста и нарастанием симптоматики. Основным симптомом хориоидальных метастазов является снижение остроты зрения. Это обусловлено преимущественной локализацией метастатической опухоли в центральных отделах глазного дна. При отсутствии лечения в случае отказа больных или несвоевременной диагностики хориоидального метастаза у 13 больных мы наблюдали быстрое (в течение 1 месяца) значительное увеличение размеров опухоли и выраженное снижение остроты зрения от 0,8-1,0 до светоощущения.
Следует отметить, что приблизительно у 10% больных метастазы в хориоидею не сопровождаются какими-либо субъективными жалобами и выявляются случайно при осмотре.
На ранних стадиях метастаз в хориоидею выглядит как желтовато-беловатый рыхлый очаг с нечеткими границами. Для хориоидальных метастазов рака молочной железы характерно увеличение опухоли по площади, при незначительном росте в высоту - “стелющаяся опухоль” (рис. 3). При юкстапапиллярной локализации метастатической опухоли ее нередко принимают за переднюю ишемическую нейропатию. По мере роста опухоли появляется вторичная отслойка сетчатки, как правило, с выраженным транссудатом (рис. 4). Отслойка сетчатки возникает не только над опухолью, но и в отдалении от нее. В этих случаях внимательный осмотр всех отделов глазного дна помогает избежать ошибочного диагноза первичной отслойки сетчатки. Метастатическая опухоль бывает похожей на гемангиому хориоидеи, но, в отличие от нее, характеризуется быстрыми темпами роста. При раке легкого, щитовидной железы, кишечника, как правило, формируется умеренно проминирующий узел неправильной формы, нередко “двугорбый” или “трехгорбый”. Узловую форму роста метастатической опухоли при раке легкого или щитовидной железы приходится дифференцировать с беспигментной меланомой хориоидеи. Кровоизлияния на поверхности опухоли, гемофтальм встречаются редко. Кровоизлияние в стекловидное тело затрудняет диагностику, и диагноз метастатического рака хориоидеи устанавливается только при морфологическом исследовании удаленного глаза.
Нередко наблюдается многофокусное поражение хориоидеи. У каждого пятого больного с хориоидальными метастазами выявляется поражение обоих глаз. Учитывая это, необходимо проводить тщательный осмотр обоих глаз с широким зрачком.
При ультразвуковом исследовании метастазов отмечается небольшая плотность опухоли, малая ее проминенция (до 3 мм) при относительно большом диаметре. Мы ни разу не встретили грибовидную форму опухоли и не отметили экскавацию склеры, столь характерную для первичной меланомы хориоидеи.
Для метастазов в орбиту рака молочной железы характерно, как правило, медленное течение. Пристеночное расположение опухоли приводит к смещению глаза в контрлатеральную сторону. Постепенно развивается экзофтальм. Субъективно больных беспокоит диплопия из-за ограничения подвижности глаза. Нередко появляется образование, которое больные сами прощупывают под одной из стенок орбиты. Опухоль, доступная пальпации, имеет, как правило, плотную консистенцию, бугристую поверхность, спаяна с подлежащими тканями. Описанная выше клиническая картина характерна для аденокарциномы или инфильтративного протокового рака молочной железы. Метастаз скиррозной формы рака молочной железы имеет иную клиническую картину. Опухоль - более плотная, быстро прорастает в прилежащие ткани. Очень рано развивается офтальмоплегия в сочетании с энофтальмом. Метастатические опухоли рака желудка, легкого, щитовидной железы характеризуются, как правило, быстрым (в течение 1-2 мес) развитием симптомов, присущих злокачественной опухоли орбиты: появлением экзофтальма, чаще осевого, невоспалительного отека век, хемоза. Нередко развивается застойный диск зрительного нерва с последующим снижением остроты зрения.
Метастатические опухоли придаточного аппарата глаза встречаются крайне редко, и их клинические проявления плохо изучены. На ранних этапах заболевания метастатическое поражение век выглядит, как обычный халязион. У онкологических больных халязионы следует подвергать хирургическому лечению с обязательным направлением удаленного материала на гистологическое исследование. Определяющая роль в диагностике метастаза принадлежит морфологическому исследованию биоптата.
Таким образом, для метастатических опухолей радужки характерны следующие клинические признаки: слабая васкуляризация, возможность многофокусного поражения, быстрые темпы роста и раннее развитие вторичной глаукомы и иридоциклита.
Для хориоидального метастаза типичны небольшая плотность опухолевого узла, относительно маленькая проминенция опухоли при значительном ее диаметре, преимущественная локализация в парамакулярных и парапапиллярных отделах, возможность развития на глазном дне нескольких опухолевых узлов, вовлечение в опухолевый процесс обоих глаз.
При метастатическом поражении тканей орбиты преимущественно развивается безболезненный экзофтальм со смещением глаза. Рано появляются офтальмоплегия и диплопия. Для скирра молочной железы характерно развитие энофтальма в сочетании с офтальмоплегией и затруднением репозиции - “вколоченный глаз”.
Метастатическая опухоль должна быть включена в дифференциально-диагностический ряд заболеваний при обследовании больных с внутриглазной гипертензией, иридоциклитом, при подозрении на вторичную отслойку сетчатки, при синдроме одностороннего экзофтальма.
Знание клинических особенностей метастатических опухолей и тщательно собранный анамнез помогают своевременной диагностике метастатического поражения органа зрения. Ранняя диагностика и своевременное лечение метастатических опухолей позволяют предупредить слепоту и развитие болевого синдрома, обусловленного вторичной глаукомой, и улучшить качество жизни наиболее тяжелой категории онкологических больных с метастатическим поражением органа зрения.
Литература
1. Eliassi-Rad B., Albert D.M., Green W.R. Frequency of ocular metastases in patients dying of cancer in eye bank populations. // Br.J. of Ophthalmol. - 1996. - vol. 80 (2). - р. 125-128.
2. Maran R., Grinbaum A., Ashkenazi I. [Ocular metastatic carcinoma- rare or common?]. // Harefuah. - 1994. - vol. 129 (9). - p. 510-513, 563.
3. McCartney A. Intraocular metastasis. // Br. J. of Ophthalmol. - 1993. - vol. 77. - p.133.
4. Nelson C., Hertzberg B., Klintworth G. A historic study of 716 unselected eyes in patients with cancer of the time of death. // Ann J. Ophthalmol.- 1983. -vol.- 95. - p. 788-793.
Меланома хориоидеи
Меланома хориоидеи — это пигментная опухоль злокачественного характера собственной сосудистой оболочки глаза (хориоидеи). Данная опухоль является одной из самых частых внутриглазных новообразований. Меланома хориоидеи является основной причиной смертности и инвалидизации онкобольных с поражением органа зрения. Заболевание может протекать практически бессимптомно, но при этом имеет высокую склонность к метастазированию, поэтому проблема ее выявления на начальных стадиях является крайне актуальной.
Этиологические факторы
Большинство случаев меланомы хориоидеи являются спорадическими, то есть обусловлены теми или иными мутациями клетки-предшественницы меланоцитарного звена, которая может дать начало патологическому опухолевому клону. Кроме того, есть предположение о наследственной причине данного заболевания. Воздействие такого типичного провоцирующего фактора для меланомы кожи, как повышенная инсоляция, для этой опухоли также не исключается.
В группе риска находятся пожилые люди (средний возраст манифестации опухоли — 60 лет). Немного чаще болеют мужчины. Склонны к появлению меланомы хориоидеи обладатели светлой кожи и волос, невусов и веснушек.
Клиническая картина
Жалобы пациентов зависят от размера и локализации меланомы хориоидеи, а также от наличия сопутствующих осложнений, к которым относятся: отслойка сетчатки вторичного характера, появление дегенеративных процессов в сетчатке, помутнение хрусталика.
На первичном приеме у офтальмолога обычно определяется снижение остроты зрения, появление перед глазом слепых участков (скотом), гемианопсий (выпадения половин поля зрения). В случае позднего обращения, больные жалуются на боль в глазу (вторичная глаукома), расширение сети сосудов. Также на склере может определяться пигментное пятно (экстраокулярный рост новообразования).
Стадии развития меланомы хориоидеи
Согласно международной классификации различают 4 стадии развития данной опухоли. Критерии распространенности опухолевого процесса:
- Т1 — размер меланомы 10 мм и менее, толщина — 2,5 мм и менее.
- Т2 — размер новообразования 10-16 мм, наибольшая толщина составляет 2,5-10 мм.
- Т3 — размером 16 мм и/или толщина более 10 мм без распространения за пределы глазного яблока.
- Т4 — наибольший размер опухоли 16 мм и/или толщина более 10 мм с распространением за пределы глазного яблока.
Также выделены 4 клинические стадии меланомы хориоидеи. Для каждой из них характерны определенные симптомы заболевания:
- Для первой, так называемой стадии «спокойного глаза», свойственно отсутствие ярких клинических проявлений и жалоб. Возможно наличие помутнения сетчатки, также могут определяться дефекты поля зрения.
- Вторая стадия характеризуется появлением боли в глазах, воспаления, покраснения глазного яблока, отека век.
- На третьей стадии меланома хориоидеи выходит за границы глазного яблока, формируется экзофтальм, склера теряет целостность.
- Четвертая стадия сопровождается генерализацией процесса. Общее состояние пациента ухудшается. Больные жалуются на сильную боль, снижается масса тела, нарастает интоксикация. Появляются метастазы меланомы внутренних органов: печени, легких, костей. Поражение того или иного органа провоцирует появление соответствующих симптомов. Может выявляться дальнейшее снижение остроты зрения, чувство пелены или тумана перед глазами. Данные проявления вызываются кровотечениями в стекловидное тело, помутнением хрусталика.
Симптомы второй и третьей стадии меланомы хориоидеи ярко выражены при расположении опухоли в центральной или парацентральной части глазного дна. Для периферической локализации новообразования характерно длительное отсутствие субъективных ощущений. В этом случае меланома выявляется либо случайно, либо на стадии распада опухоли и ее вторичных проявлений.
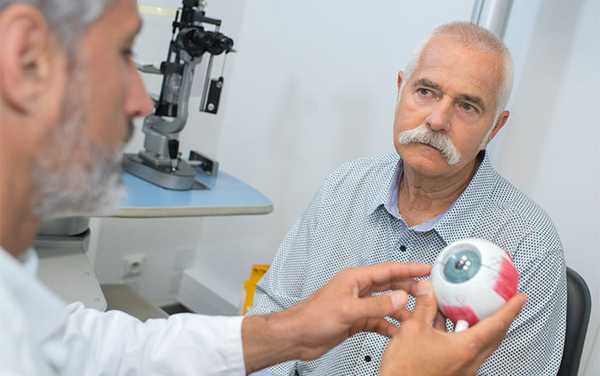
Виды меланомы глаза
Разработана классификация меланомы хориоидеи по морфологическому признаку. В зависимости от клеточной структуры, выделяют следующие типы данной опухоли:
- Веретеноклеточный.
- Эпителиоидный.
- Смешанный (микстмеланома).
- Фасцикулярный.
- Некротический.
Данная классификация имеет определенные недостатки, так как некротическая меланома хориоидеи определяется клинически, а вот определить ее клеточную принадлежность из-за обширного некроза невозможно. Веретенообразный и фасцикулярный тип имеют сходный прогноз. В связи с этим, в настоящее время морфологически принято выделять только 2 типа: веретеноклеточный и эпителиоидный. Смешанная форма занимает промежуточное положение. Ее прогноз зависит от преобладания тех или иных клеток. Наименее благоприятной прогностически считается эпителиоидноклеточная меланома хориоидеи.
Учитывая клинические особенности меланомы хориоидеи, ее диагностика, особенно на начальных этапах, представляет определенные трудности. Помимо анализа жалоб больного и клинико-анамнестических данных, учитываются результаты следующих инструментальных исследований:
- Биомикроскопии.
- Офтальмоскопии.
- Ультразвукового исследования глаза.
- Диафаноскопии и др.
Меланома хориоидеи является новообразованием с высоким риском появления метастазов. Поэтому при обследовании пациента необходимо использовать также методы диагностики метастатических очагов: УЗИ органов брюшной полости и лимфатических узлов, рентгенографию легких, КТ, МРТ.

Способы лечения меланомы хориоидеи
Выделяют органосохраняющие методы лечения данной опухоли и хирургический метод без сохранения глаза. В случаях, когда не удается сохранить глаз, производят энуклеацию — изолированное удаление глазного яблока или экзентерацию — иссечение вместе с глазным яблоком всего содержимого орбитальной полости.
Показания к энуклеации:
- Опухоль значительного размера.
- Распространение меланомы на диск зрительного нерва.
- Полное отсутствие зрительной функции.
- Экстрабульбарный рост опухоли.
- Вторичная глаукома.
После удаления глазного яблока, проводится имплантация внутреннего протеза и последующее наружное протезирование. Эти меры позволяют не только достичь хорошего косметического результата, но и препятствуют деформации лица.
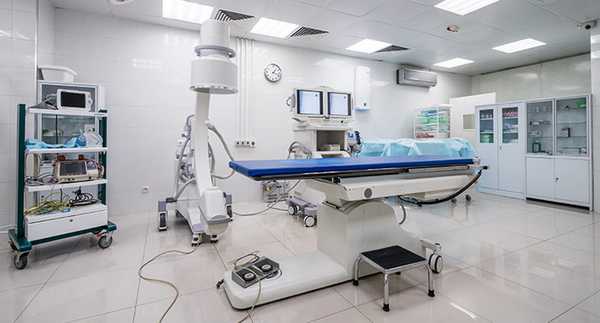
К органосохраняющим методам лечения меланомы хориоидеи относятся:
Лучевая терапия. В зависимости от способа подведения излучения, лучевую терапию при данном заболевании проводят контактным или дистанционным способом. Контактное облучение, или брахитерапия, представляет собой имплантацию радиоактивных элементов вблизи очага меланомы.
Показания к проведению брахитерапии:
- Отсутствие признаков распада.
- Диаметр новообразования до 15 мм.
- Отстояние от диска зрительного нерва не менее 2 диаметров самого диска.
Брахитерапия является самым эффективным методом органосохраняющего лечения при меланоме хориоидеи. Его применение способно снизить вероятность образования метастазов опухоли.

В составе системного лечения, актуально проведение иммунной терапии. Также при оказании помощи больным с меланомой хориоидеи в поздних стадиях учитываются особенности ее метастазирования. Для данной опухоли характерно изолированное поражение печени метастазами. В таких случаях с успехом применяется химиоэмболизация данного органа.
Такой распространенный метод лечения меланомы кожи, как таргетная терапия, при меланоме хориоидеи не применяется, так как при данном виде опухоли отсутствуют специфичные BRAF-мутации.
Профилактика и диспансерное наблюдение
Рекомендовано пожизненное наблюдение за больными, которые получали лечение меланомы хориоидеи. После проведения лучевой терапии и удаления новообразования, офтальмолог должен осматривать пациентов каждые полгода в течение 2 лет, а далее — 1 раз в год. С целью раннего выявления метастазов назначают УЗИ органов брюшной полости и рентгенографию легких 1-2 раза в год.
Прогноз для жизни при меланоме хориоидеи
Продолжительность жизни при данном виде рака зависит от локализации и размера опухоли, возраста пациента, морфологии новообразования, проведенного лечения и других особенностей. Пятилетняя выживаемость на начальных стадиях меланомы хориодиеи после применения органосохраняющих радикальных методов составляет 93%, десятилетняя — 89%. На поздних стадиях, при выявлении метастазов печени медиана выживаемости составляет лишь 4-6 месяцев. Для пациентов с метастатическим поражением других органов годичная выживаемость составляет 76%.
Рак легких с метастазами
Рак легких является достаточно опасным онкологическим заболеванием. Около половины всех пациентов умирают в течение года после постановки диагноза. Наиболее грозным является рак легких с метастазами, так как в этом случае опухолевый процесс распространяется на другие органы. Эта особенность затрудняет лечение и неблагоприятно сказывается на прогнозе.
Метастазы образуются в результате переноса раковых клеток из первичного очага. Наиболее значимым является гематогенное метастазирование ввиду активного кровоснабжения легких. Кроме того, метастазы могут развиваться и при переносе раковых клеток лимфатической жидкостью. Независимо от пути распространения, метастазы являются очень опасными, особенно если они поражают жизненно важные органы. В этом случае развиваются дополнительные симптомы, которые не характерны для локального рака легких.
Клинические проявления рака легких с метастазами
На начальных стадиях рак легкого, как правило, себя не проявляет. Первые симптомы затрагивают только дыхательную систему. Среди них отмечаются:
- Кашель с кровью.
- Затрудненное дыхание.
- Боль в проекции легких.
- Одышка.
- Изменение голоса.
- Развитие пневмонии.
Рак легких с метастазами в печени и почках
Почки и печень играют важную роль в процессе обезвреживания и выведения токсических веществ, поэтому эти органы хорошо кровоснабжаются и чаще всего поражаются метастазами. В частности, при раке легких метастазы данной локализации выявляются достаточно часто. В результате функция данных органов нарушается, что в конечном итоге сказывается на состоянии пациента.
Симптомы распространения метастазов на почки и печень при раке легких:
- Пожелтение кожных покровов и склер глаз из-за замедленного вывода билирубина.
- Потемнение мочи и осветление кала.
- Асцит (скопление жидкости в брюшной полости).
- Проблемы с перевариванием пищи из-за недостаточного продуцирования желчи.
- Постоянное ощущение тошноты, независимо от приема пищи.
- Появление крови в моче.
- Изменение показателей биохимического анализа крови.
Кроме того, пациенты могут предъявлять жалобы на боль в области поясницы (при появлении метастазов в почках) и в области правого подреберья (при метастазировании рака легких в печень).
Рак легких с метастазами в костях и позвоночнике
Поражение костных структур и позвоночника происходит на 3- 4 стадии рака легких. Наиболее часто метастазами повреждается тазобедренный сустав, позвоночник, ребра, плечевая кость и др. Помимо основных симптомов, характерных для рака легких, в этом случае могут развиваться следующие клинические проявления:
- Патологические переломы.
- Острые боли при ходьбе и выполнении различных движений.
- Нарушение подвижности рук и ног.
- Развитие межреберной невралгии.
Также при разрушении костей повышается уровень кальция в крови, что приводит к появлению таких симптомов, как усталость, плохой аппетит, сухость во рту, постоянная жажда.
Метастазы рака легких в головном мозге

При раке легких мозг реже повреждается вторичным опухолевым процессом, чем печень. Однако такие нарушения являются одними из самых тяжелых и существенно ухудшают прогноз. При распространении метастазов из первичного очага рака легких в различные отделы головного мозга, развиваются следующие симптомы:
- Нарушение зрения, слуха, речи, глотания.
- Сильные головные боли, которые сложно устранить обычными средствами.
- Нарушение чувствительности и двигательной активности различных участков тела.
- Нарушение процессов мочеиспускания и дефекации.
- Снижение интеллектуальных способностей.
Очень часто при метастазировании рака легких в головной мозг, пациент утрачивает способность к самообслуживанию и не может выполнять простейшие действия, поэтому он нуждается в регулярном наблюдении и уходе.
Метастазы рака легких в лимфатических узлах
При раке легких поражению подвергаются, в первую очередь, регионарные лимфатические узлы, расположенные рядом с опухолью. По мере прогрессирования основного заболевания, метастазы выявляются и в более отдаленных лимфоузлах. При этом развиваются симптомы, которые не характерны для рака легких на начальных стадиях. Среди них можно выделить:
- Выраженное снижение иммунитета.
- Увеличение и болезненность лимфоузлов при пальпации.
- Изменение в показателях крови.
- Значительное снижение массы тела.
В некоторых случаях симптомы поражения лимфатических узлов проявляются раньше, чем симптомы первичного очага в легких. Однако не все люди догадываются, что проблема связана со злокачественной опухолью и поэтому не придают значения данным проявлениям.
Лечение рака легких с метастазами
Эффективное лечение пациентов с раком легких при осложнениях в виде метастазов в других органах практически невозможно. Исключение составляют те случаи, когда первичную опухоль можно удалить хирургическим путем, и при этом у пациента обнаруживаются единичные метастазы, которые также поддаются удалению. В остальных случаях основной целью лечения является замедление развития рака легких, снижение выраженности симптомов, улучшение качества жизни пациента и увеличение ее продолжительности. Такое лечение рака легких подразумевает применение консервативных методов.
Таргетная терапия
Таргетная терапия воздействует непосредственно на клетки рака легких. Подходящие препараты назначают в зависимости от того, какой ген в организме подвергся мутации:
- Если изменения произошли в гене ALK или ROS1, то больным назначают Кризотиниб.
- При мутациях в гене EGFR назначают Афатиниб.
- При изменениях в гене BRAF применяют Траметиниб.
Препараты, которые применяются при таргетной терапии рака легких, действуют разными способами. Одни нарушают кровоснабжение опухоли, другие блокируют ферменты, которые необходимы для размножения раковых клеток. Независимо от механизма действия, отмечается один и тот же эффект — замедление роста, а в некоторых случаях и уменьшение первичного очага, снижение скорости распространения метастазов, улучшение общего состояния пациента.
Химиотерапия при раке легких
В большинстве случаев применяется полихимиотерапия, которая подразумевает назначение двух или более препаратов. Точные схемы, количество курсов и общая продолжительность лечения подбираются индивидуально для каждого пациента. В отличие от таргетной терапии, химиотерапия влияет и на здоровые клетки, которые активно делятся. Поэтому при лечении рака легкого таким способом отмечается высокая вероятность развития побочных эффектов.
Симптоматическое лечение рака легких с метастазами
В эту группу входят методы, направленные на устранение симптомов, которые связаны с поражением легких и других органов, пораженных метастазами. Наиболее часто пациенты нуждаются в снятии болезненных ощущений, которые невозможно устранить обычными препаратами, которые продаются в аптеке. В этих случаях при раке легких назначают наркотические анальгетики, которые вводятся при помощи капельниц в стационаре под контролем медицинского персонала. Дополнительно назначаются препараты других групп (антибиотики, противовоспалительные средства), которые призваны устранить симптомы у конкретного пациента.
Сколько живут при раке легких с метастазами
Вопрос продолжительности жизни всегда волнует пациентов, которые столкнулись со злокачественным поражением легких. При распространении процесса на другие органы, прогноз будет самым неблагоприятным. Точная продолжительность жизни при раке легких зависит от многих факторов. Наибольшее значение имеет точная локализация метастазов, их количество, размер и локализация первичного очага, общее состояние пациента. Например, при метастазировании рака легких в печень, средняя продолжительность жизни составляет около 6 месяцев. Если метастазы выявляются в головном мозге, то этот показатель увеличивается до года. При распространении рака легких на лимфатические узлы и костную систему, средняя продолжительности жизни может составить 2-3 года.
Читайте также:
