Пролапс жировой клетчатки глазницы: признаки, гистология, лечение, прогноз
Добавил пользователь Валентин П. Обновлено: 28.01.2026
Список сокращений:
ВЧП — верхнечелюстная пазуха
ВСТ — волокнистая соединительная ткань
РФКТ — ретикулофиброзная костная ткань
ПКТ — пластинчатая костная ткань
МСКТ — мультиспиральная компьютерная томография
Перелом стенки глазницы — распространенная патология, частота которой составляет от 18 до 80% среди всех черепно-мозговых травм [1, 2]. Перелом нижней стенки глазницы (типа blow-out) встречается в 15—20% всех орбитальных переломов [3, 4]. Восстановление нижней стенки глазницы является сложной и актуальной клинической проблемой, находящейся на стыке нескольких специальностей: оториноларингологии, офтальмохирургии и челюстно-лицевой хирургии. Выбор тактики ведения больных с указанной патологией определяется многими факторами: размерами дефекта, наличием пролапса содержимого орбиты в верхнечелюстную пазуху (ВЧП) или защемления глазодвигательных мышц (нарушения со стороны органа зрения, длительность периода, прошедшего с момента травмы), наличием энофтальма (нарушения подвижности глазного яблока) и др. [5, 6]. Повреждение нижней стенки глазницы обычно подтверждается компьютерной томографией, которая дает возможность оценить состояние костных структур орбиты, размер и местоположение дефекта, а также позволяет измерить любое смещение костных стенок и мягких тканей глазницы для выбора оптимального способа хирургического лечения [3, 7—9].
Известно, что раннее выполнение оперативного вмешательства улучшает прогноз для больного. Несмотря на то, что хирургическую реконструкцию дефекта нижней стенки орбиты можно отложить, при повреждении типа blow-out существует риск защемления мышц, при котором необходимо выполнить экстренное оперативное вмешательство [5, 6]. Для восстановления нижней стенки глазницы применяются различные материалы, в том числе титановые конструкции и разные варианты костных трансплантатов, однако экспериментальное обоснование по их применению отсутствует [2, 10—13].
Цель исследования — представить экспериментальное и клиническое обоснование применения нетканной титановой конструкции и аллогенного деминерализованного костного трансплантата для восполнения дефекта нижней стенки глазницы.
Материал и методы
На базе отдела морфологии ФГБУ «Всероссийский центр глазной и пластической хирургии» Минздрава России (Уфа) были выполнены экспериментальные исследования на 24 полуторагодовалых кроликах породы шиншилла обоего пола. У лабораторных животных стоматологическим бором моделировали дефект стенки ВЧП диаметром 4 мм. Ранее экспериментальным путем было установлено, что данный размер дефекта не замещается костной тканью самопроизвольно. Затем производили закрытие костного дефекта с помощью конструкции на основе пористого титана (n=12), аллогенного деминерализованного костного трансплантата (n=12) по технике press-fit («заглушка»), после чего выполняли послойное ушивание мягких тканей над областью пластики.
Разработанные технологии закрытия дефектов нижней стенки глазницы применяли в соответствии с регистрационным удостоверением №ФСР 2011/12012 от 30.09.11. С использованием данных технологий нами были прооперированы 15 пациентов с дефектами нижней стенки глазницы.
В тканевом банке ФГБУ «Всероссийский центр глазной и пластической хирургии» Минздрава России (Уфа) производятся аллогенные трансплантаты костного происхождения «Аллоплант» (ТУ 9398−001−04537642−2011), адаптируемые под размер дефекта нижней стенки глазницы. При обширных (более 3 см) дефектах верхней стенки ВЧП (n=7, или 47%) использовали нетканую титановую конструкцию производства ООО «Прототип» (Самара; ТУ 9437−002−01963143−2010).
Результаты
Применение нетканной титановой конструкции. Через 2 мес после имплантации титановой конструкции на гистологических препаратах выявлялся регенерат, представленный комплексом костных тканей, замещающих дефект.
Перифокальная зона, непосредственно прилежащая к титановой конструкции, была образована из незрелой грубоволокнистой костной ткани, состоящей из крупнопетлистых тонких трабекул. В межтрабекулярных пространствах выявлялась рыхлая волокнистая соединительная ткань (ВСТ), инфильтрированная фибробластами. В ней были обнаружены развитая сеть кровеносных сосудов, жировая ткань и клетки костного мозга. В полостях центральной зоны регенерата наблюдались мелкоячеистые (наноструктурированные) полые структуры, которые состояли из множества округлых ячеек, сгруппированных между собой в кластеры. Гематоксилином и эозином прокрашивались в розовый цвет только стенки ячеек, просветы были свободные. Данные образования не вызывали выраженной воспалительной реакции, однако в костных полостях они покрывались тонкой соединительнотканной капсулой.
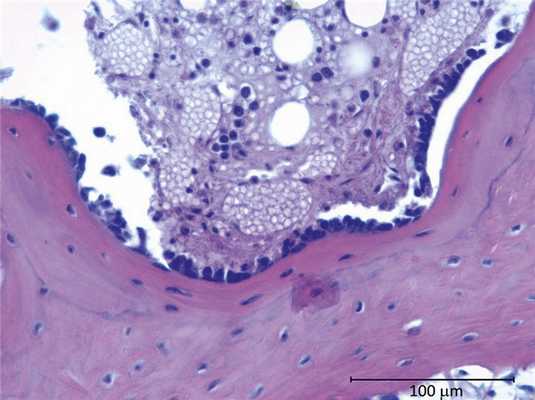
В дальнейшем объем коллагеновых волокон увеличивался, петли титана обрастали рыхлой соединительной тканью с небольшим количеством фибробластов, макрофагов и полностью погружались в волокнистый матрикс. Рыхлая ВСТ постепенно трансформировалась в плотную неоформленную соединительную ткань с толстыми пучками коллагеновых волокон, редуцированными кровеносными сосудами. Происходила остеоинтеграция: миграция остеогенных клеток со стороны материнской кости и минерализация коллагеновых волокон, образовавшихся вокруг петель титана (рис. 1). Рис. 1. Развившийся фиброз вокруг петель титана (контроль). Окраска гематоксилином и эозином. Staining with hematoxylin and eosin.
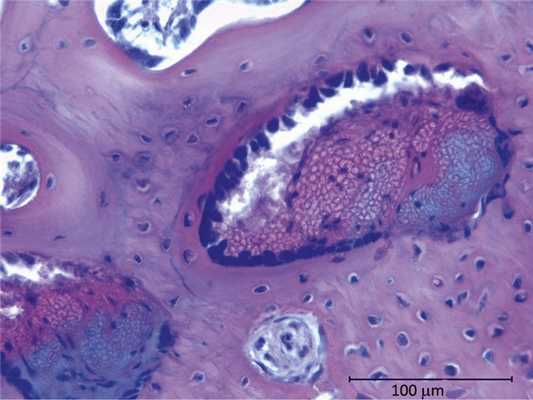
При этом петли титана оказывались в толще костного матрикса. Вокруг кластеров титана в кости определялись зоны активного аппозиционного костеобразования. Каналы выстилали активные остеобласты II типа, расположенные плотно друг к другу в один ряд и синтезирующие остеоид и костный матрикс. Сами ячейки титана приобретали более плотную структуру, между ними определялась ВСТ с утолщенными коллагеновыми пучками. При окраске гематоксилином и эозином просветы ячеек окрашивались ацидофильно в розовый цвет и базофильно — в голубой. Некоторые ячейки теряли свою первоначальную структуру и были деформированы. Их стенки лизировались, гомогенизировались и представляли собой плотную бесформенную массу (рис. 2). Рис. 2. Деструкция титана в костных полостях (контроль). Окраска гематоксилином и эозином. Staining with hematoxylin and eosin. Таким образом, титан подвергался деструкции. Причем скорость биодеградации имплантата была ниже скорости образования костной ткани.
В глубокой зоне костного регенерата, непосредственно прилегающей к материнской кости, выявлялись признаки последовательной трансформации грубоволокнистой незрелой кости в зрелую пластинчатую кость. По всей окружности дефекта определялась тонкая неравномерная полоса зрелой губчатой костной ткани с многочисленными костными лакунами, заполненными остеоцитами. Утолщенные костные трабекулы постепенно созревали в пластинчатую кость с характерной структурой. В костном матриксе пластинчатой кости обнаруживалась развитая сеть гаверсовых каналов, заполненных рыхлой соединительной тканью с кровеносными сосудами.
Таким образом, репаративное костеобразоование происходило центростремительно — от периферии к центру (аппозиционный остеопоэз). Причем скорость процессов остеогенеза и биодеградации титана была различной — темп деструкции имплантата оказался ниже. Механизм остеогенеза представлен интрамембранозным окостенением, т. е. костеобразование происходило через стадию формирования ВСТ с постепенной трансформацией в грубоволокнистую костную ткань и дальнейшим преобразованием в пластинчатую кость. Титановая конструкция не вызывает бурной воспалительной реакции и не обладает иммуногенной активностью, но окружающие ткани реагируют на имплантат как на инородное тело — происходит его инкапсулирование и развитие фиброза.
Применение деминерализованного костного трансплантата. Несколько иные механизмы заместительной регенерации были обнаружены в области имплантации деминерализованного костного трансплантата в трепанационный дефект переднелатеральной стенки ВЧП. В ранние сроки (на 14-е сутки) в области трансплантации определяется полиморфноклеточная инфильтрация. При этом в инфильтрате верифицируются клетки фибробластического, остеобластического и макрофагального дифферонов. Важно подчеркнуть отсутствие в составе клеточного инфильтрата представителей лимфоцитарного дифферона и сегментоядерных лейкоцитов, что свидетельствует об отсутствии гнойной инфекции в зоне подсадки аллогенного трансплантата.
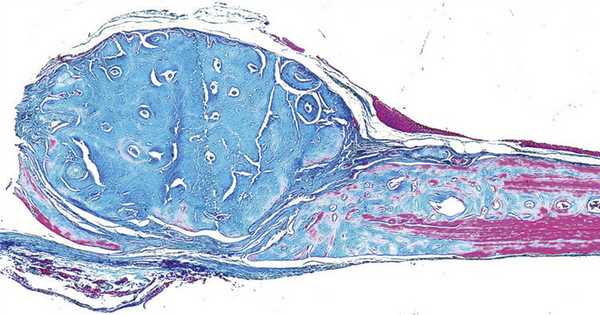
На 45-е сутки деминерализованный костный трансплантат подвергается интенсивной деградации и лизису, о чем свидетельствует изменение его тинкториальных свойств. Однако на данном сроке деминерализованный костный трансплантат все же сохраняет значительную часть объема (рис. 3). Рис. 3. Экспериментальная модель дефекта переднелатеральной стенки ВЧП с его последующим закрытием аллогенным костным трансплантатом. Первая опытная серия; 45-е сутки. Окраска по Маллори. Реконструкция. ×100. Mallory staining. Reconstruction. ×100. В периферической зоне наблюдалась активная сосудистая реакция со стороны костного ложа. Область подсадки аллогенного костного трансплантата обильно васкуляризировалась. Сосуды из периферической зоны прорастали в область трансплантации, что объясняется не только наличием каналов в костном трансплантате, но и стимулирующим влиянием продуктов его резорбции на процессы пролиферации сосудов. Следует отметить отсутствие выраженных сосудистой и клеточной реакций со стороны слизистой оболочки ВЧП. Наблюдались некоторое утолщение и клеточная инфильтрация собственной пластинки в краевой зоне трансплантации.
Процессы резорбции превалировали над синтетической активностью фибробластов и остеобластов, поэтому на 45-е сутки формирующийся регенерат имел незначительные включения костной ткани и на 36,48±4,81% был представлен рыхлой ВСТ.
Далее (90-е сутки) происходит дальнейшая деградация аллогенного костного трансплантата. Большая часть костного биоматериала замещена новообразованной ретикулофиброзной костной тканью (РФКТ). Выраженной инфильтрации макрофагами в области подсадки трансплантата не наблюдается. Скорость резорбции костного трансплантата преобладала над скоростью заместительного остеогенеза. Сам трансплантат частично сохранил структурную организацию пластинчатой костной ткани (ПКТ). Формирующийся регенерат представляет собой плотную оформленную ВСТ с относительно бόльшим, чем в окружающих тканях, количеством клеточных элементов и сосудов. При этом в регенерате менее выражены извилистость коллагеновых волокон и плотность их упаковки. В составе регенерата определялись включения РФКТ. Как показывает морфометрический анализ, костная ткань при этом составляет значительный объем от общей площади исследуемой области.
В результате слияния двух встречных фронтов замещения аллогенного биоматериала на 180-е сутки формируется непрерывный массив РФКТ с включениями ПКТ (см. таблицу). Относительная плотность тканей (в кг/м 3 ) в регенерате на 180-е сутки после трепанационного дефекта переднелатеральной стенки ВЧП с последующим закрытием аллогенным деминерализованным костным трансплантатом
Приводим описание клинических наблюдений пластики нижней стенки глазницы деминерализованным костным трансплантатом и нетканной титановой конструкцией.
Клинический пример 1
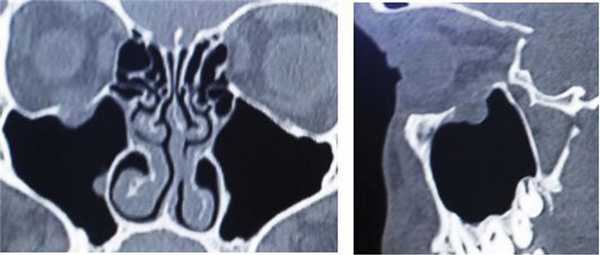
Пациент С., 17 лет, обратился в нейрохирургическое отделение стационара медико-санитарной части «Нефтяник» с жалобами на диплопию, сохраняющуюся в течение 1 мес после тупой травмы глазницы справа. На мультиспиральной компьютерной томографии (МСКТ) околоносовых пазух и орбиты определяется дефект верхней стенки правой ВЧП с пролабированием параорбитальной жировой клетчатки в пазуху (рис. 4). Рис. 4. МСКТ околоносовых пазух и глазницы справа: коронарная и сагиттальная проекции. Дефект нижней стенки правой глазницы (верхней стенки ВЧП) с пролабированием параорбитальной клетчатки. Defect of the lower wall of the right orbit (the upper wall of the maxillary sinus) with the prolapse of the paraorbital adipose tissue into the sinus.
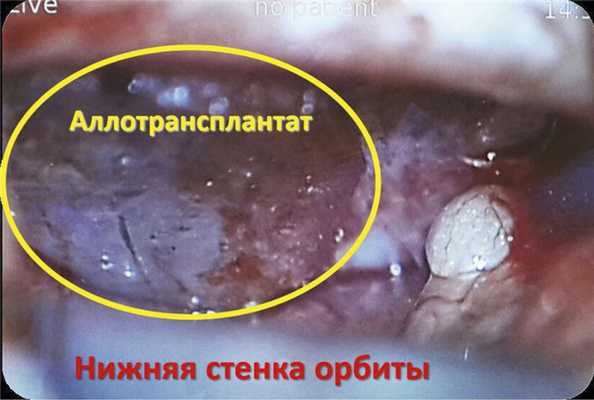
Под общим обезболиванием совместно с нейрохирургом выполнена нижняя орбитотомия. Область дефекта верхней стенки ВЧП освобождена от рубцов, параорбитальная клетчатка смещена кверху. Проведена ревизия ВЧП через верхнюю стенку с использованием эндоскопа «Элмед» 70° диаметром 4 мм. В область дефекта установлен предварительно смоделированный фрагмент деминерализованного костного аллогенного трансплантата (рис. 5). Рис. 5. Интраоперационное микрофото. Аллогенный транплантат фиксирован в дефекте нижней стенки глазницы по технике press fit. Мягкие ткани ушиты послойно, на кожу нижнего века наложен косметический шов. В полость носа на 10 мин были введены марлевые турунды, пропитанные 0,1% раствором оксиметазолина. Затем в целях профилактики кровотечения и дополнительной анестезии оперируемой области инфильтрировали слизистую оболочку полости носа (перед крючковидным отростком, у основания и передний конец средней носовой раковины) 1% раствором лидокаина с адреналином 1:100 000. Процедуру инфильтрации контролировали торцевым жестким эндоскопом Элмед диаметром 4 мм. Распатором провели щадящую медиализацию средней носовой раковины, в средний носовой ход ввели предложенный инструмент для мобилизации крючковидного отростка и выполнили расширение полулунной щели за счет медиального смещения крючковидного отростка.
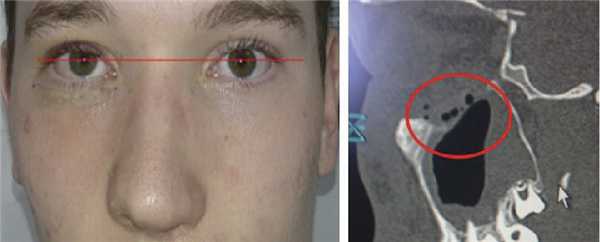
На 7-е сутки была выполнена контрольная МСКТ, которая подтвердила стабильное положение аллогенного трансплантата, при этом наблюдался незначительный реактивный отек слизистой оболочки ВЧП со стороны вмешательства (рис. 6). Рис. 6. Пациент С., 17 лет. Седьмые сутки после нижней орбитотомии справа с реконструкцией нижней стенки глазницы. Слева — зрачки на одном уровне. Справа — МСКТ околоносовых пазух и глазницы справа, сагиттальная проекция. Явления реактивного отека слизистой оболочки ВЧП. The identically leveled pupils (left). MSCT of the right-hand paranasal sinuses and the orbit in the sagittal projection (right). The signs of reactive oedema of the mucous membrane of the maxillary sinus. Произведено снятие косметического шва на нижнем веке, зрачки на одном уровне. Пациент отмечает отсутствие диплопии.
Клинический пример 2
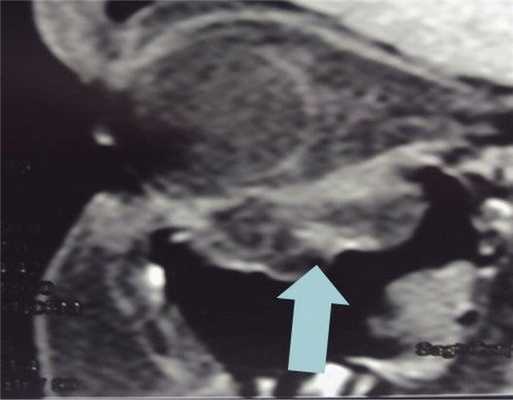
Пациент Ш., 18 лет, обратился в нейрохирургическое отделение стационара медико-санитарной части «Нефтяник» с жалобами на диплопию, сохраняющуюся в течение 2 нед после тупой травмы глазницы справа. На МСКТ околоносовых пазух и орбиты справа определяется дефект верхней стенки ВЧП с пролабированием параорбитальной жировой клетчатки в пазуху (рис. 7). Рис. 7. Пациент Ш., 18 лет. МСКТ. Посттравматический дефект нижней стенки глазницы. Пролабирование параорбитальной клетчатки в просвет ВЧП (указано стрелкой). Prolapse of the paraorbital adipose tissue into the maxillary sinus lumen (indicated by he arrow).
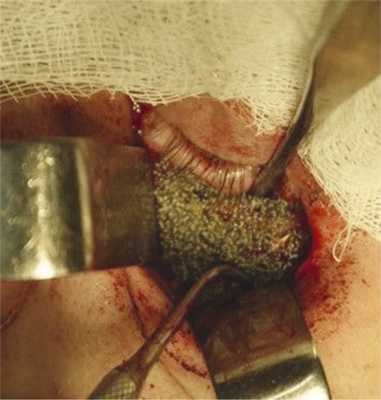
Под общим обезболиванием совместно с нейрохирургом выполнена нижняя орбитотомия. Область дефекта верхней стенки ВЧП освобождена от рубцов, параорбитальная клетчатка смещена кверху. Проведена ревизия ВЧП через верхнюю стенку с использованием эндоскопа Элмед 70° диаметром 4 мм. В область дефекта установлена предварительно смоделированная нетканная титановая конструкция (рис. 8). Рис. 8. Пациент Ш., 18 лет. Интраоперационное фото. Нетканная титановая конструкция установлена в область дефекта верхней стенки ВЧП. The non-woven titanium structure placed in the defective region in the upper wall of the maxillary sinus.
Мягкие ткани ушиты послойно, на кожу нижнего века наложен косметический шов. В полость носа на 10 мин были введены марлевые турунды, пропитанные 0,1% раствором оксиметазолина. Затем под контролем торцевого жесткого эндоскопа Элмед диаметром 4 мм инфильтрировали слизистую оболочку полости носа (перед крючковидным отростком, у основания и передний конец средней носовой раковины) 1% раствором лидокаина с адреналином 1:100 000. Распатором провели щадящую медиализацию средней носовой раковины, с помощью разработанного инструмента для мобилизации крючковидного отростка выполнили расширение полулунной щели за счет медиального смещения крючковидного отростка.
На 2-е сутки была выполнена контрольная МСКТ, которая подтвердила стабильное положение нетканной титановой конструкции и отсутствие реактивных изменений слизистой оболочки ВЧП. Произведено снятие косметического шва на нижнем веке, зрачки на одном уровне. Пациент отмечает отсутствие диплопии.
Заключение
Целью лечения орбитального перелома помимо освобождения заключенных мягких тканей является восстановление анатомии глазницы и предотвращение серьезных риногенных внутриглазничных осложнений. Клиническая оценка в сочетании с соответствующим рентгенологическим исследованием прооперированных пациентов подтверждает эффективность и безопасность использования нетканной титановой конструкции и аллогенного деминерализованного костного трансплантата при реконструкции нижней стенки орбиты. На основании экспериментального исследования сделан вывод о том, что использование пористого титана предпочтительнее при больших дефектах нижней стенки орбиты. Это связано с более низким темпом деструкции имплантата по сравнению с костным трансплантатом. В целом же выбор способа реконструкции дефекта нижней стенки орбиты типа blow-out должен осуществляться с учетом опыта хирурга и наличия соответствующего материала.
Липосаркома
Липоскаркома - злокачественная опухоль жировой ткани. Может поражать любые участки тела, но чаще локализуется в проксимальных отделах нижних конечностей, в забрюшинной клетчатке или в области плеча. Представляет собой одиночный узел неправильной формы с неравномерной плотностью. При прорастании костей и сдавливании нервов вызывает резкие боли. Может провоцировать тромбозы, парезы, параличи, отек и ишемию конечности. В запущенных случаях возникают лихорадка, истощение, анемия и симптомы общей интоксикации. Диагноз выставляется на основании осмотра, МРТ, биопсии и других исследований. Лечение - операция, радиотерапия, химиотерапия.
Общие сведения
Липосаркома - злокачественное новообразование из группы мезенхимальных опухолей. Развивается из липобластов (юных жировых клеток), обычно располагается межмышечном пространстве, реже - в подкожной жировой клетчатке. Липосаркома является второй по распространенности злокачественной опухолью мягких тканей после фибросаркомы. Очень редко диагностируется у детей. Частота развития увеличивается с возрастом и достигает максимума к 50-60 годам. Женщины страдают реже мужчин. Эндемичность отсутствует.
Уровень злокачественности различается в зависимости от степени дифференцировки липосаркомы. Высокодифференцированные опухоли растут медленно и протекают относительно благоприятно. Для низкодифференцированных форм липосаркомы характерен быстрый рост, гематогенное (в 35-40% случаев) и лимфогенное (в 6-9% случаев) метастазирование. Рецидивы возникают у 45-75% пациентов. Лечение осуществляют специалисты в области онкологии, ортопедии, неврологии и флебологии.
Причины липосаркомы
Этиология заболевания пока окончательно не выяснена. Установлено, что липосаркома может развиваться из липомы, однако такие случаи исключительно редки. Иногда злокачественные опухоли жировой ткани возникают вблизи нейрофибром, что позволяет предположить наличие определенной связи между липосаркомой и нейрофиброматозом. Многие исследователи в числе факторов риска указывают механические травмы, облучение или контакт с канцерогенными веществами.
Липосаркома представляет собой одиночный узел либо диффузный инфильтрат неправильной формы. Чаще возникает в межмышечном пространстве, реже формируется в подкожной жировой клетчатке. Обычно располагается в проксимальных отделах нижних конечностей. Второе место по распространенности занимают липосаркомы забрюшинного пространства, далее в порядке убывания располагаются опухоли паховой области, ягодичной области и коленных суставов. Очень редко поражаются молочная железа, голова, шея, область семенного канатика, стопы, кисти и большие половые губы. Как правило, новообразование одиночное, реже встречаются множественные липосаркомы.
Поверхность опухоли желтоватая либо белая с сероватым оттенком. На разрезе видна серовато-розовая полупросвечивающая ткань с характерными участками «рыбьего мяса». В ходе микроскопического исследования липосаркомы обнаруживаются как зрелые жировые клетки, так и атипичные липобласты с звездчатыми или веретенообразными ядрами. Клеточная цитоплазма содержит вкрапления жира, выявляющиеся при окрашивании суданом.
Классификация липосаркомы
С учетом особенностей строения и клинического течения различают следующие виды липосаркомы:
- Высокодифференцированная липосаркома. Отличается медленным ростом. Не метастазирует. По строению напоминает липому.
- Склерозирующая высокодифференцированная липосаркома. Состоит из скоплений зрелых жировых клеток, разделенных фиброзными прослойками, в которых располагаются атипичные клетки.
- Воспалительная высокодифференцированная липосаркома. По строению напоминает один из предыдущих типов опухоли, но отличается от них наличием выраженной лимфоплазмоцитарной инфильтрации.
- Миксоидная липосаркома. Часто рецидивирует, не склонна к метастазированию. Содержит зрелые жировые клетки, круглые и веретенообразные липобласты. Имеет мукоидную строму с большим количеством мелких сосудов. Иногда в ткани новообразования выявляются участки с более низким уровнем дифференцировки клеток, что рассматривается как прогностически неблагоприятный вариант.
- Круглоклеточная липосаркома. Представляет собой низкодифференцированный вариант миксоидной опухоли. При микроскопическом исследовании новообразования выявляются участки примитивных круглых клеток. Количество сосудов в таких участках меньше, чем в областях с высоким уровнем дифференцировки клеток.
- Плеоморфная липосаркома. Содержит гиганские плеоморфные липобласты и небольшое количество мелких веретенообразных или округлых липобластов.
- Недифференцированная липосаркома. Состоит из участков с высокой степенью дифференцировки и областей низкодифференцированных клеток, напоминающих плеоморфную фибросаркому или злокачественную фиброзную гистиоцитому.
Симптомы липосаркомы
Высокодифференцированные липосаркомы обычно протекают бессимптомно и становятся случайной находкой при возникновении локальной деформации или проведении обследования в связи с другими заболеваниями и травмами. Для начальных стадий низкодифференцированных липосарком также характерно бессимптомное течение. В последующем клинические проявления определяются поражением близлежащих анатомических структур. При сдавлении нервов возникают интенсивные боли, возможны нарушения чувствительности, парезы и параличи.
Сдавление сосудов осложняется отеком и нарушением питания конечности. При сдавлении венозных стволов могут развиваться флебиты и тромбозы глубоких вен. При сдавлении артерий наблюдается ишемия конечности. Поражение костей при липосаркоме выявляется очень редко, сопровождается развитием болевого синдрома. При прогрессировании процесса возникают симптомы общей интоксикации, лихорадка, истощение и анемия. В отдельных случаях липосаркома метастазирует в легкие, печень, почки, сердце, яичники и костный мозг. Метастазы в лимфатические узлы выявляются очень редко.
При пальпации определяется мягкоэластичная или плотная опухоль неправильной формы с неровными контурами. Диаметр узла может достигать 20 сантиметров. Некоторые новообразования имеют дольчатое строение. На начальных этапах липосаркома смещается в поперечном направлении, при прорастании кости узел становится неподвижным. Обычно опухоль достаточно четко отграничена от окружающих тканей, что в сочетании с экспансивным ростом создает впечатление доброкачественности новообразования. При этом на самом деле липосаркома распространяется по межмышечным пространствам.
Диагностика липосаркомы
Диагноз устанавливают на основании анамнеза, жалоб, данных внешнего осмотра и результатов инструментальных исследований. Проводят МРТ пораженного сегмента, выполняют биопсию с последующим гистологическим исследованием образца. Для исключения метастазов больного с липосаркомой направляют на УЗИ внутренних органов, рентгенографию грудной клетки, рентгенографию и сканирование костей конечностей. При поражении крупных сосудов осуществляют ангиографию.
Окончательный диагноз выставляют с учетом результатов морфологического исследования. Липосаркому дифференцируют с липомой, рабдомиомой, внутримышечной миксомой, миксоидной хондросаркомой, миксоидной злокачественной фиброзной гистиоцитомой, плеоморфной злокачественной фиброзной гистиоцитомой, лимфомой, нейробластомой, внекостной саркомой Юинга, овсяноклеточным раком и некоторыми другими злокачественными новообразованиями мягких тканей.
Лечение и прогноз при липосаркоме
Лечение хирургическое. Выполняют широкое иссечение опухоли с окружающими неизмененными тканями. Липосаркому удаляют вместе с группой мышц, между которыми расположено новообразование. При опухоли, плохо отграниченной от окружающих тканей и распространяющейся по межмышечным пространствам, проводят ампутацию или экзартикуляцию конечности. В послеоперационном периоде назначают лучевую терапию. Кроме того, радиотерапию применяют при отдаленных метастазах и местных рецидивах. При крупных быстрорастущих липосаркомах и при метастазировании опухоли хирургическое вмешательство и лучевую терапию дополняют химиотерапией.
Местные рецидивы выявляются у 45-75% пациентов. Вероятность рецидивирования определяется локализацией и видом липосаркомы. Высокодифференцированные опухоли подкожной жировой клетчатки не рецидивируют. При расположении таких же новообразований в межмышечных пространствах рецидивы возникают в 29% случаев, при локализации в забрюшинной клетчатке - в 37% случаев. Реже всего рецидивирование наблюдается при миксоидных липосаркомах. В большинстве случаев рецидивные опухоли менее дифференцированы по сравнению с первичными.
Отдаленное местастазирование выявляется в 15-45% случаев. Чаще всего метастазируют круглоклеточные липосаркомы, затем, в порядке убывания - плеоморфные, миксоидные и высокодифференцированные липосаркомы. Продолжительность жизни определяется видом и локализацией новообразования. Наиболее благоприятными считаются миксоидные и высокодифференцированные липосаркомы. Пятилетняя выживаемость при таких опухолях колеблется от 45 до 65%. Полное выздоровление наблюдается в 30-40% случаев. У детей прогноз более благоприятен, в детском возрасте пятилетняя выживаемость при липосаркоме составляет 80-90%.
Висцероптоз ( Синдром Гленара , Спланхноптоз , Энтероптоз )
Висцероптоз — это смещение книзу органов брюшной полости, прежде всего кишечных петель, по сравнению с их нормальным анатомическим расположением. Состояние проявляется хроническими запорами, болями в различных отделах живота, которые усиливаются в положении стоя. Для диагностики энтероптоза используют тест Гленарда и инструментальные методики — ирригографию, УЗИ брюшной полости, колоноскопию и сцинтиграфию. Консервативное лечение включает диетотерапию, упражнения ЛФК и ношение бандажа. При осложненных формах висцероптоза показано проведение оперативного вмешательства.
МКБ-10
Висцероптоз имеет несколько синонимов — энтероптоз, спланхноптоз, синдром Гленара. Истинная частота болезни неизвестна, поскольку только около 10-20% случаев висцероптоза проявляется клинически. Большинство патологий обнаруживается случайно при обращении по поводу других симптомов. Существует 2 пика выявления энтероптоза: в молодом возрасте и у пожилых (60-65 лет). Женщины страдают опущением абдоминальных органов в 3 раза чаще, чем мужчины. У детей висцероптоз бывает очень редко, чаще связан с врожденными аномалиями развития.
Причины висцероптоза
Точные этиологические факторы висцероптоза неизвестны. Некоторые ученые считают, что патологическая подвижность органов живота и их опущение является конституциональным вариантом нормы в тех случаях, если они не сопровождаются клиническими признаками. Более распространена теория, согласно которой висцероптоз возникает при нарушении комплекса стабилизирующих факторов. В современной гастроэнтерологии выделяют 3 группы причин энтероптоза:
- Слабость соединительной ткани. Нормальное положение органов достигается благодаря связочному аппарату брюшной полости. Вследствие дисплазии соединительной ткани происходит недоразвитие этих связок и фасций. Причинами висцероптоза служат синдром Марфана, синдром Элерса-Данлоса.
- Быстрое снижение веса. При резком похудении отмечается потеря жировой клетчатки, расположенной в брюшной полости и забрюшинном пространстве. Как следствие, все подвижные органы начинают смещаться книзу, что усугубляется при предрасположенности человека к анатомическому висцероптозу.
- Перерастяжение брюшных мышц. С этой причиной связаны частные случаи энтероптоза у многократно рожавших женщин, у которых прямые и косые мышцы живота перерастягиваются и становятся атрофичными. Риск висцероптоза увеличивается после больших вентральных грыж, рецидивирующего асцита.
Патогенез
Чаще всего при висцероптозе встречается поражение ободочной кишки, которая наиболее подвижна. Поперечная ободочная кишка приобретает U-образную форму, что затрудняет прохождение пищи и газов. Нарушение пассажа по желудочно-кишечному тракту — основной патофизиологический механизм, обуславливающий появление симптоматики. При продолжительном существовании энтероптоза возникают кишечные спайки и деформации.
Гистологически длительно протекающий висцероптоз представляет собой катаральное воспаление и атрофию отдельных участков кишечной стенки. Происходит инфильтрация подслизистой оболочки, при хроническом воспалительном процессе добавляются фиброзные изменения. Для энтероптоза характерна постепенная гибель интрамуральных нервных ганглиев, что провоцирует патологическое перерастяжение кишечника.
Классификация
По локализации выделяют правосторонний и левосторонний висцероптоз. В странах СНГ используют классификацию российского клинициста А.И. Иванова (1996 год), учитывающую тяжесть клинических симптомов болезни. Различают 3 степени энтероптоза: компенсированная (запор менее 3-4 дней), субкомпенсированная (задержка стула на протяжении 5-10 дней), декомпенсированная. По этиологическим факторам висцероптоз подразделяют на 2 категории:
- Приобретенный. Это вариант энтероптоза развивается при наличии предрасполагающих факторов и чаще сопровождается неприятными клиническими признаками.
- Конституциональный. Встречается у лиц астенического телосложения либо вследствие врожденных патологий связочного аппарата и удлинения брыжейки. В основном протекает бессимптомно.
Симптомы висцероптоза
Опущение тех или иных отделов толстой кишки проявляется различной клинической симптоматикой. Наиболее часто диагностируется висцероптоз печеночного или селезеночного изгиба ободочной кишки, основным симптомом которого служат запоры. Человек ощущает тяжесть в животе и боли, локализованные в околопупочной области. Беспокоит постоянное вздутие кишечника. Симптомы усугубляются в вертикальном положении.
При висцероптозе слепой кишки все вышеуказанные признаки локализованы в правой подвздошной области. Характерны приступы резких болей, которые напоминают клинику острого аппендицита. При энтероптозе сигмовидной кишки запоры чередуются с поносами, в стуле обычно наблюдаются включения слизи и крови. Больные жалуются на резкие схваткообразные боли в левой подвздошной области.
Наблюдается деформация и отвисание живота, которая усиливается при наклонах туловища вперед. На коже брюшной стенки возникают белые растяжки. При висцероптозе пациенты испытывают неудобства во время длительной ходьбе без бандажа, при работе в наклонном положении. Зачастую определяется диастаз — расхождение прямых мышц живота, которое можно заметить визуально или прощупать.
Длительно существующий висцероптоз приводит к хроническим запорам. Сначала у больных стул отсутствует в течение нескольких дней, в некоторых случаях возможна самостоятельная дефекация. По мере прогрессирования процесса запоры длятся до 10 дней и более, каловые массы выходят только после постановки клизмы. В результате эндогенной интоксикации появляется слабость, головокружение, нервозность.
Осложнения
Висцероптоз часто сочетается с растяжением и удлинением кишечника, что повышает риск инвагинации и заворота кишки. Эти состояния опасны, поскольку при неоказании медицинской помощи наблюдается ишемия и некроз тканей. Частым осложнением энтероптоза является синдром верхней брыжеечной артерии, сопровождающийся ишемическим кишечным некрозом.
Специалисты отмечают, что заболевание служит независимым фактором риска хронического колита и энтерита. Висцероптоз, протекающий на фоне хронического толстокишечного стаза, в 66% случаев вызывает рефлюкс-эзофагит. У 15% пациентов возникает дуоденальная непроходимость. Энтероптоз зачастую ассоциирован с гастроптозом (39%), нефроптозом (17,8%), гепатоптозом (5%).
Диагностика
Обследованием больных с подозрением на висцероптоз занимается врач-гастроэнтеролог. При физикальном исследовании патогномоничные проявления отсутствуют. Предположить наличие энтероптоза можно при положительном тесте Гленарда. Решающими в диагностике болезни являются инструментальные методы визуализации кишечника:
- УЗИ брюшных органов. Сонография — первичное диагностическое исследование, которое показывает нарушения анатомических взаимоотношений между органами брюшной полости. УЗИ информативно для обнаружения ассоциированной патологии, осложнений энтероптоза.
- Ирригография. Рентгенологическое исследование кишечника с контрастированием — наиболее информативный метод для обнаружения висцероптоза. Контрастирование выявляет опущение кишки, расширение некоторых ее отделов. При помощи отсроченных снимков проверяют скорость пассажа по кишечнику.
- Сцинтиграфия. Радионуклидный способ диагностики энтероптоза проводится для установления ранних функциональных отклонений в работе органов пищеварения. Сцинтиграфия более информативна, чем другие методы инструментальной диагностики, а также позволяет снизить лучевую нагрузку на пациента.
- Колоноскопия. Эндоскопическое исследование — вспомогательная методика диагностики, применяющаяся для оценки состояния слизистого слоя толстокишечной оболочки. Исследование используют для дифференциальной диагностики висцероптоза, если у больного есть жалобы на слизь и кровь в кале.
Лечение висцероптоза
Консервативная терапия
Основным методом лечения висцероптоза являются немедикаментозные методы. Больному подбирают специальную диету с дробным питанием, повышенным содержанием клетчатки и жидкости. Изменение рациона питания направлено на активацию кишечной моторики, уменьшение риска запоров. При выраженном опущении органов подбирают специальный бандаж, при ношении которого уменьшаются неприятные симптомы.
К немедикаментозным методам терапии энтероптоза относят специальные комплексы ЛФК, которые направлены на укрепление мышц передней брюшной стенки. Лекарственные препараты назначаются намного реже. При хронических запорах используются мягкие слабительные средства, масляные клизмы. При обнаружении воспалительных осложнений схема лечения подбирается индивидуально.
Хирургическое лечение
В суб- и декомпенсированных стадиях висцероптоза абдоминальные хирурги определяют показания к оперативному вмешательству. В последние годы техники проведения операций значительно усовершенствовались, поэтому хорошие отдаленные результаты наблюдаются у 93-95% пациентов. Обычно применяют различные варианты резекции толстой кишки с наложением анастомозов.
Прогноз и профилактика
В большинстве случаев висцероптоз не представляет угрозу для жизни и здоровья, поэтому врачи дают благоприятный прогноз. Даже в декомпенсированной стадии можно улучшить самочувствие больных с помощью современных оперативных вмешательств. Профилактика заболевания включает ношение бандажей во время беременности и после родов, упражнения для укрепления мышечного каркаса живота.
1. Симптоматология и диагностика правостороннего висцероптоза/ С.П. Боковой // Урологические ведомости. — 2017.
2. Хирургическое лечение правостороннего висцероптоза/ С.П. Боковой// Урологические ведомости. — 2018.
Опущение века
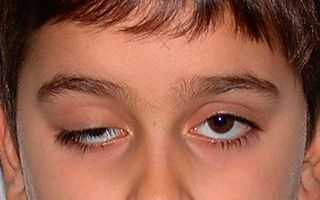
Опущение века или птоз — это состояние, которое может быть врожденным или приобретенным. Главная опасность состоит в том, что опущение века может являть собой не только неприятный косметический дефект, но и быть симптомом тяжелого заболевания.
В норме край верхнего века перекрывает глазное яблоко и радужную оболочку примерно на 1/3. Но это не столь важно для определения наличия птоза, так как опущение века, как правило, сразу заметно и больному, и окружающим, в сравнении со здоровым глазом.
Такое состояние, как опущение верхнего века, способно ограничивать видимость вследствие сужения глазной щели, приводить, таким образом, к излишней нагрузке на органы зрения, «перенапрягая» их. По этой причине опущение принято считать и офтальмологической патологией, которая может спровоцировать нарушение зрения. Однако, совершенно не лишним будет и визит к неврологу, об этом ниже.
Причины опущения века
Верхнее веко — это не просто кожный лоскут. Веко состоит из мышцы, присоединяющейся к хрящу в области глазницы. Мышца (она так и называется - мышца, поднимающее верхнее веко) находится в толще подкожно-жировой клетчатки.
Основные причины патологии:
- врожденное заболевание, которое связано с недостаточным развитием мышцы, призванной поднимать верхнее веко;
- травма мышцы, поднимающей верхнее веко;
- повреждение глазодвигательного нерва;
- растяжение сухожилия мышца, поднимающей верхнее веко (данное состояние характерно для пожилого возраста);
- поражение шейного симпатического сплетения (так называемый синдром Горнера, выражающийся в птозе, сужении зрачка и «западении» глазного яблока); , как причина метаболического повреждения мышцы и нерва;
- острое нарушение мозгового кровообращения (в этом случае опущение века сопровождается рядом других симптомов);
- опухоль головного мозга, спинного мозга или области шеи;
- нарушение нервно-мышечной передачи (миастения или миастенический синдром);
- поражение глазодвигательного нерва в рамках полинейропатии (в сочетании с поражением целого ряда других периферических нервов);
- осложнение введения ботулотоксина в косметических или лечебных целях;
- ботулизм.
Учитывая множество факторов, приводящих к опущению века — консультация врача необходима в обязательном порядке.
Неврологические заболевания, приводящие к птозу
- Миастения - тяжелое заболевание, при котором нарушается передача импульса от нерва к мышце. Для миастении характерна повышенная мышечная утомляемость. Заболевание поражает все мышцы, но наибольшие проявления могу затрагивать только мышцы глаз, вызывая птоз, двоение, снижение фокусировки. Для первичной диагностики миастении невролог проводит пробу с введением прозерина и исследует нервы и мышцы с помощью ЭНМГ (электронейромиографии).
- Миопатия, при которой также наблюдается двоение, опущение обоих век, при этом работоспособность мышцы, поднимающей веко, ослаблена, но присутствует. Миопатии по своему происхождению бывают разных типов. При обследовании используется игольчатая ЭМГ и ряд лабораторных исследований.
- Пальпебромандибулярная синкинезия - непроизвольные содружественные движения, сопровождающие жевание, отведения и размыкание нижней челюсти. К примеру, при открывании рта опущение может резко исчезнуть, после закрытия рта - восстановиться. Данное состояние может быть как самостоятельной болезнью, так и результатом неправильного восстановления двигательных волокон лицевого нерва после его поражения.
- Синдром Бернара-Горнера (выражается сочетанием опущением верхнего века, сужением зрачка и "западением" глазного яблока). Является проявлением патологии шейного симпатического сплетения. Иногда патология обнаруживается на фоне повышенного потоотделения на лице и неполного паралича плечевых нервов с больной стороны.
Опущение века после введения ботулотоксина
По статистике, после инъекций в области глаз ботулотоксина («Ботокса» и других препаратов, его содержащих) опущение века случается в 20% осложненных случаев, но это практически всегда связано с ошибками при проведении процедуры или же связано с индивидуальной особенностью человека.
Опущение века после введения ботокса неприятно, но, к счастью, его нельзя считать серьезной патологией, так как без дополнительной терапии признаки опущения полностью исчезают на протяжении 3-4 недель после инъекции препарата.
Лечение опущения века
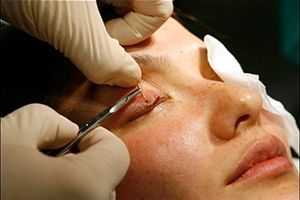
Если причиной опущения века стало неврологическое заболевание, такое как миастения или невропатия, то прежде всего проводится терапия основного заболевания. Так как птоз является симптомом, то на фоне излечения основной болезни уходит и он.
Однако, в ряде случаев, полное восстановление невозможно, и тогда проводится хирургическое лечение с косметической целью или, если птоз приводит к существенному нарушению жизнедеятельности в виду ухудшения зрения, то и с лечебной.
Детям такую операцию проводят не ранее 3-х летнего возраста, но это следует сделать как можно скорее, чтобы предупредить снижение зрения и развитие косоглазия.
С целью устранения косметического дефекта (когда зрение не нарушено) операцию рекомендовано производить после периода полового созревания, когда костный лицевой скелет окончательно сформирован.
Если опущение вызвано травмой, операцию можно проводить непосредственно при начальной обработке раневой поверхности хирургом, либо после заживления, то есть спустя 6-12 месяцев.
Так или иначе, решение о сроке проведения операции доктор принимает в зависимости от конкретного случая.
Профилактика развития опущения века
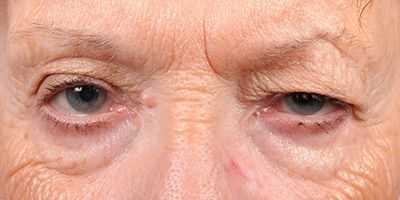
Важным моментом в профилактике опущения века является своевременное лечение любых заболеваний, которые могут спровоцировать данную патологию. К примеру, невриты лицевых нервов необходимо безотлагательно лечить у невролога, а возможность опущения век после инъекций ботокса следует обязательно обсудить с проводящим манипуляцию специалистом.
Если вы замечаете слабость век, связанную с возрастными изменениями, то здесь вам могут помочь косметические и народные средства. Методы профилактики включают в себя использование подтягивающих масок, масел и массажных процедур.
Массаж кожи век следует проводить при опущенных веках. Перед процедурой веки можно протереть лосьоном, чтобы удалить сальные чешуйки и открыть выводящие протоки сальных желез. Массажируют при помощи ватного тампона или диска, пропитанного антисептическим раствором или специальной мазью. Используют поглаживание с легким надавливанием, проводя круговые и прямолинейные движения, направляясь от внутреннего угла глаза к внешнему углу. Можно слегка поколачивать веки подушечками пальцев.
Существует специальная гимнастика при слабости глазных мышц.
Исходное положение - стоя, сидя или лежа.
- Смотрим по направлению вверх, не поднимая головы, затем резко вниз. Повторяем движения 6-8 раз.
- Смотрим кверху и вправо, потом по диагонали книзу и влево. Повторяем движения 6-8 раз.
- Смотрим кверху и влево, потом книзу и вправо. Повторяем движения 6-8 раз.
- Смотрим максимально влево, потом максимально вправо. Повторяем движения 6-8 раз.
- Вытягиваем руку вперед, держим её прямо. Смотрим на кончик указательного пальца и постепенно приближаем его, не прекращая смотреть до тех пор, пока картинка не начнет «двоиться». Повторяем движения 6-8 раз.
- Кладем указательный палец на переносицу. Переводим взгляд на палец попеременно правым и левым глазом. Повторяем 10-12 раз.
- Двигаем глазами по кругу вправо и влево. Повторяем движения 6-8 раз.
- Быстро моргаем на протяжении 15 секунд. Повторяем моргания до 4 раз.
- Крепко зажмуриваемся на 5 секунд, потом резко открываем глаза также на 5 секунд. Повторяем 10 раз.
- Закрываем глаза и массируем веки пальцем по кругу на протяжении 1 минуты.
- Переводим взгляд с ближайшей точки на дальнюю и наоборот.
Движения глазным яблоком во время упражнений должны быть максимально широкими, но не до боли. Двигательный темп можно со временем усложнять. Длительность такой профилактики - минимум 3 месяца.
Стоит отметить, что при миастении и миопатии подобные упражнения противопоказаны, так как способствуют усугублению опущения века вследствие «истощения» мышцы. Поэтому, прежде чем заниматься любым способом лечения, необходимо проконсультироваться со специалистом.
Эндокринная офтальмопатия

Следствием этого является ряд офтальмологических симптомов, среди которых сильнее всего выделяется пучеглазие — яркий симптом Базедовой болезни (болезнь Грейвса, диффузный токсический зоб).
Эндокринная офтальмопатия считается осложнением Базедовой болезни. По статистике, это состояние диагностируется у 25% пациентов с диффузным токсическим зобом. В 6% случаев наблюдается её тяжелая форма. У 0,3% пациентов эндокринная офтальмопатия сопровождается серьёзным риском потери зрения из-за поражения зрительного нерва.
У 20% пациентов пучеглазие и другие признаки офтальмопатии являются первыми симптомами Базедовой болезни. В 85% случаев между началом диффузного токсического зоба и возникновением офтальмопатии проходит не более 18 месяцев. Поражение ретробульбарной клетчатки и глазодвигательных мышц носит двухсторонний характер, с небольшим различием в выраженности симптомов. Только в 15% случаев офтальмопатия затрагивает один глаз. Чаще всего это осложнение диагностируется у женщин. Однако у мужчин симптомы офтальмопатии, как правило, более выражены и чаще приводят к тяжёлым последствиям.
Классификация эндокринной офтальмопатии
В зависимости от степени вовлечения мягких тканей глазницы в процесс различают следующие классы патологии:
- 0 класс — симптомы офтальмопатии отсутствуют;
- 1 класс — начальные признаки офтальмопатии: ретракция верхнего века, его отставание при закрытии глаза. Эти изменения делают взгляд больного удивлённым, пристальным или злобным;
- 2 класс — изменения мягких тканей глаза: отёк конъюнктивы, век, инъекция слизистой конъюнктивальной полости, склеры;
- 3 класс — визуально определяется проптоз глаза (пучеглазие);
- 4 класс — признаки вовлечения глазодвигательных мышц: двоение в глазах;
- 5 класс — патологические изменения роговицы (кератопатия, язва роговицы) глаза из-за лагофтальма (невозможность сомкнуть веки полностью из-за выпячивания глазного яблока);
- 6 класс — резкое снижение остроты зрения из-за вовлечения в патологический процесс зрительного нерва.
Клиническая классификация использует шкалу Европейской группы по изучению офтальмопатии Грейвса, позволяющую оценить степень активности патологии:
- спонтанная ретробульбарная боль;
- боль при взгляде верх или вниз;
- покраснение век;
- инъекция конъюнктивы;
- отек век;
- хемоз;
- воспаление карункулы.
Каждый пункт равен 1 баллу. При наличии 3 и более баллов ЭОП считается достаточно активной. Потеря зрения — самое тяжёлое осложнение, к которому может приводить эндокринная офтальмопатия, симптомы, возникающие при этом (прогрессирующее снижение зрения и/или повреждение роговицы глаза) является признаком тяжёлого течения патологии и требуют экстренного лечения. В противном случае возможны необратимые изменения в зрительном нерве и сетчатке, приводящие к слепоте.
Прогноз
Эндокринная офтальмопатия поддаётся лечению у большинства пациентов. Реальная угроза потери зрения при адекватной терапии возникает только у 0,3% больных. При своевременной диагностике и грамотном лечении прогноз благоприятный. Проблемы возникают у пациентов, обратившихся поздно, или лечившихся у офтальмологов (проявления ЭОП часто принимают за различные офтальмологические заболевания — конъюнктивиты, блефариты, инородные тела и т.п.). По этой причине требуется специализированная терапия в профильном лечебно-профилактическом учреждении всем больным с диагнозом эндокринная офтальмопатия.
Узнайте, в каких клиниках проводят лечение эндокринной офтальмопатии в Москве, на нашем сайте.
Причины эндокринной офтальмопатии
Причина эндокринной офтальмопатии связанна с основным заболеванием — диффузным токсическим зобом или болезнью Грейвса-Базедова-Флаяни. Это аутоиммунное воспаление щитовидной железы, протекающее с диффузным увеличением её объема и массы (зоб), возникающее в результате действия аутоантител к рецептору тиреотропного гормона.
Тиреотропный гормон или ТТГ — гормон гипофиза, стимулирующий секрецию трийодтиронина (Т3) и тироксина (Т4) щитовидной железой. В норме увеличение его уровней способствует росту концентрации тиреоидных гормонов в периферической крови и тканях. Снижение уровня ТТГ приводит к понижению секреции гормонов щитовидки. Таким образом осуществляет регуляция эндокринной функции железы.
Особенность диффузного токсического зоба в нарушении этого механизма из-за аутоиммунного процесса. По непонятным до конца причинам иммунная система начинает интенсивно продуцировать антитела к тканям щитовидной железы. Группа таких аутоантител специфична против рецепторов к тиреотропному гормону, имеющихся на поверхности мембраны фолликулярных клеток щитовидки (анти-рТТГ). Эти антитела присоединяются к рецептору, и из-за похожей структуры начинают оказывать стимулирующее воздействие на ткани щитовидной железы. В результате резко увеличивается секреция тиреоидных гормонов, что приводит к вторичному гипертиреозу (тиреотоксикозу).
Клетки соединительной и жировой ткани глазницы также имеют рецепторы к тиреоидному гормону, из-за чего они могут быть целью повреждающего действия аутоантител при Базедовой болезни. В результате возникает отёк глазодвигательных мышц и ретробульбарной клетчатки, давление в глазнице возрастает, из-за чего глаз фактически выдавливается наружу, подобно пробке в бутылке шампанского. Отёк также нарушает венозный отток, из-за чего страдает и сам глаз. По такому механизму возникает эндокринная офтальмопатия, лечение этой патологии может представлять трудности и требует обязательной терапии основного заболевания.
Симптомы эндокринной офтальмопатии
Разными учёными описано более 30 признаков и симптомов ЭОП. В основном причиной их возникновения считают отёк и воспаление мягких тканей орбиты. Клинически наиболее значимые симптомы:
- выпячивание глазного яблока (пучеглазие) — проптоз;
- появление полоски склеры между краем радужки и веком сверху — признак Кохера;
- расширение глазной щели из-за спазма век, придающее взгляду удивлённый вид — признак Дальримпля;
- дрожание закрытых век — признак Розенбаха;
- редкое или моргание — признак Штельвага;
- отставание или неподвижность верхнего века при взгляде вниз — признак Грефе;
- невозможность полностью сомкнуть веки — лагофтальм;
- отёк век — признак Энрота.
Неспецифические симптомы ЭОП включают в себя:
- распирающие боли за глазами, усиливающиеся при движении глазного яблока;
- чувство «песка» или инородного тела в глазах;
- слезотечение;
- фотофобия;
- пелена перед глазами, двоение;
- покраснение склеры глаза, конъюнктивы, сосудистая инъекция.
Неспецифические симптомы могут возникать из-за лагофтальма — неполное смыкание век приводит к раздражению роговицы, лишённой защиты от пересыхания и попадания инородных тел. В тяжёлых случаях следствием этого является кератопатия, кератит или язва роговицы. Лагофтальм увеличивает риск инфицирования конъюнктивы и склеры.
Нарушение венозного оттока может приводить к увеличению внутриглазного давления, из-за чего больные жалуются на боли в глазах, головные боли. По этой же причине возникают застойные явления в сетчатке, отёк зрительного нерва, ретинопатия. Ущемление или сдавливание зрительного нерва приводит к снижению зрения, сужению полей зрения, исчезновению роговичного рефлекса и потере цветового зрения. Эти признаки свидетельствуют о тяжёлой ЭОП. Степень проптоза варьирует. Его выраженность можно измерить в миллиметрах с помощью специального прибора — экзофтальмометра. При значительном экзофтальме возможен подвывих глазного яблока, приводящем к повреждению зрительного нерва.
Двоение в глазах является признаком миопатии глазодвигательных мышц. Из-за их воспаления могут быть ограничены движения глазного яблока. В начале заболевания эти симптомы могут возникать периодически, однако с течением времени приобретают хронический характер.
Особенность ЭОП — связь с табакокурением. У курящих пациентов симптомы и тяжесть патологии намного более выражены, по сравнению с некурящими. Риск возникновения глазных осложнений тиреотоксикоза у таких больных выше в 5 раз. Отказ от курения является обязательным требованием перед началом лечения, так как облегчает терапию и улучшает прогноз.
Диагностика эндокринной офтальмопатии
Диагностика ЭОП основывается на характерных признаках заболевания, которыми сопровождается эндокринная офтальмопатия. Симптомы, характерные для неё, хорошо известны любому врачу-эндокринологу. Но в некоторых случаях проптоз является признаком других патологий глазницы — опухолей, воспаления ретробульбарной клетчатки из-за инфекции, кровоизлияния, переломов глазницы, объёмных образований и т.д. По этой причине диагностика обязательно дополняется лабораторными и инструментальными исследованиями.
Лабораторная диагностика ЭОП
Лабораторная диагностика ЭОП проводится для оценки тиреоидного статуса пациента (гипертиреоз, гипотиреоз, эутиреоз), определения уровней тиреотропного гормона. Высокий уровень тиреоидных гормонов или тиреотоксикоз, низкий уровень ТТГ подтверждает эндокринную природу патологии. Затем проводится анализ крови на аутоантитела к рецепторам ТТГ, тиреоглобулину и тиреопероксидазе. При положительном результате диагноз диффузного токсического зоба, а также эндокринной офтальмопатии, более чем вероятен.
Инструментальная диагностика ЭОП
Инструментальные исследования — УЗИ, МСКТ и МРТ проводят для исключения объёмных образований глазницы. При этом выявляются признаки диффузного отёка ретробульбарной клетчатки, изолированный или диффузный отёк глазодвигательных мышц, диагностируется компрессия зрительного нерва. Такие изменения могут определяться и у пациентов без явных признаков патологии.
Лечение эндокринной офтальмопатии
Тактика лечения ЭОП зависит от тяжести состояния. При наличии угрозы потери зрения, ведётся агрессивная терапии, вплоть до хирургического вмешательства.
Лечение тяжёлой эндокринной офтальмопатии
Основой консервативной терапии тяжёлых форм ЭОП является системное назначение высоких доз глюкокортикостероидов (пульс-терапия) — преднизолона, метилпреднизолона. Предпочтительный метод введения препаратов — внутривенный (меньше осложнений, по сравнению с таблетированными средствами). Ретробульбарное введение ГКС не рекомендуется. Улучшение состояния наблюдается через 1-2 недели. При назначении глюкокортикостероидов необходимо учитывать вероятность рецидива после отмены препаратов (синдром отмены).
Существует много схем назначения глюкокортикостероидов при ЭОП. Доза препаратов варьирует от 60-80 мг в день, на протяжении нескольких месяцев, до 500 мг в неделю, на протяжении 6 недель, с последующим переходом на поддерживающую дозу или постепенную отмену. При отсутствии эффекта от системной гормональной терапии проводится хирургическая декомпрессия орбиты (удаляется часть костей глазницы).
Применение лучевой терапии на область орбиты имеет противоречивые сведения об эффективности у пациентов с диагнозом эндокринная офтальмопатия, лечение таким образом может привести к плохим результатам в долгосрочной перспективе. Суммарная доза облучения не должна превышать 20 грей. В целом, метод не считается приемлемой альтернативой глюкокортикостероидам.
Кератопатия или язва роговицы, возникающие как следствие неполного смыкания век, часто являются осложнением тяжёлой ЭОП. В таких случаях назначается местное лечение с помощью ежечасного нанесения антибактериальных, увлажняющих и заживляющих средств. Цель лечения — добиться полного закрытия глазной щели. В таких случаях декомпрессия орбиты является альтернативным способом предотвратить дальнейшее повреждение роговицы (с возможной перфорацией и потерей зрения).
При отсутствии эффекта от назначения ГКС возможно начало иммуносупрессивной терапии, подавляющей аутоиммунный процесс. Для лечения применяются циклоспорин, азатиоприн. Эффективность иммуносупрессивной терапии не доказана и многими учёнными считается терапией отчаяния — когда все возможные методы не дали эффекта.
Удаление щитовидной железы в сочетании с гормональной терапией или без у некоторых пациентов по эффективности сравнимо с назначением кортикостероидов. Однако однозначных рекомендаций и показаний к этому виду лечения нет.
Похожая тактика применяется и при ЭОП средней степени тяжести. В целом, даже такие экстремальные методы, как хирургическая декомпрессия, считаются достаточно безопасными. Лечение даёт положительный эффект у более чем 80% пациентов с тяжёлой офтальмопатией.
Лечение лёгкой ЭОП
У части больных офтальмопатия протекает в лёгкой форме. В таких случаях показанием к лечению с помощью глюкокортикостероидов является желание пациента улучшить свое качество жизни. В целом, для этой группы больных приём кортикостероидов не показан, так как риск их назначения превышает возможный положительный эффект. Вместо этого назначаются местные противовоспалительные препараты и средства, увлажняющие слизистую глаза.
Данная статья размещена исключительно с целью ознакомления в познавательных целях и не является научным материалом или профессиональным медицинским советом. За диагностикой и лечением обратитесь к врачу.
Введите ваши данные, и наши специалисты свяжутся с Вами, и бесплатно проконсультируют по волнующим вас вопросам.
Читайте также:
- Токсический отек. Признаки токсического отека легких.
- Синдром Баквина-Айгера (Bakwin-Eifger)
- КТ, цистография при нейрогенном мочевом пузыре
- Нейрома и нейрофиброма конъюнктивы: признаки, гистология, лечение, прогноз
- Химиотерапия при раке прямой кишки: препараты для химиотерапии, паллиативная химиотерапия при раке прямой кишки
