Равновесие мутаций и отбора при Х-сцепленных рецессивных мутациях
Добавил пользователь Евгений Кузнецов Обновлено: 28.01.2026
Х-связанный тяжелый комбинированный иммунодефицит ( X-SCID ) - это иммунодефицитное заболевание, при котором организм производит очень мало Т-клеток и NK-клеток .
В отсутствии клеточной помощи Т , В - клетки становятся дефектными. Это X-сцепленный рецессивный признак наследования , происходящий от мутированной (аномальной) версии гена IL2RG , расположенного на X-хромосоме . Этот ген кодирует общей гамма - цепи рецептора интерлейкина белок , который является рецептором цитокина суб-блок , который является частью рецепторов для ИЛ-2, ИЛ-4, ИЛ-7, ИЛ-9, ИЛ-15 и ИЛ-21.
СОДЕРЖАНИЕ
Симптомы и признаки
Люди, страдающие X-SCID, часто заболевают инфекциями в очень раннем возрасте, до трехмесячного возраста. Это происходит из-за снижения уровня иммуноглобулина G (IgG) у младенца в течение трехмесячного периода. За этим следуют вирусные инфекции, такие как пневмонит , воспаление легких, которое вызывает общие симптомы, такие как кашель, лихорадка, озноб и одышка. Верным признаком X-SCID является кандидоз , тип грибковой инфекции, вызываемой Candida albicans . Кандидоз поражает влажные участки тела, такие как кожа, рот, дыхательные пути и влагалище; Симптомы кандидоза полости рта включают затруднение глотания, боль при глотании и поражения полости рта. Рецидивирующие высыпания, похожие на экзему , также являются частым симптомом. Другие распространенные инфекции, с которыми сталкиваются люди с X-SCID, включают диарею , сепсис и средний отит . Некоторые другие распространенные симптомы, которые испытывают пациенты с X-SCID, включают в себя нарушение нормального развития , проблемы с кишечником, проблемы с кожей и мышечную гипотонию .
У некоторых пациентов симптомы могут не проявляться в течение первых шести месяцев после рождения. Вероятно, это связано с пассивным иммунитетом, полученным от матери, чтобы защитить ребенка от инфекций, пока новорожденный не сможет вырабатывать собственные антитела. В результате может быть период молчания, когда у ребенка не проявляются симптомы X-SCID, за которым следует развитие частых инфекций.
Генетика
X-SCID вызывается мутацией, происходящей в локусе xq13.1 Х-хромосомы. Чаще всего это заболевание поражает мужчин, мать которых является носителем ( гетерозиготной ). Поскольку у женщин есть две Х-хромосомы, мать не пострадает, если у нее будет только одна аномальная Х-хромосома, но у любых детей мужского пола будет 50% -ный шанс заболеть этим заболеванием из-за наследования дефектного гена. Точно так же ее дети женского пола будут иметь 50% шанс стать носителями иммунодефицита. X-SCID также может возникать в результате мутаций de novo и может быть предотвращен у женщин с помощью X-инактивации . При X-инактивации предпочтительный отбор немутантной X-хромосомы во время развития приводит к такому результату, что ни одна из зрелых женских клеток активно не экспрессирует мутацию X-SCID, они иммунологически не затронуты и не имеют нагрузки носителя. Мутация de novo - это изменение гена, вызванное мутацией в зародышевой клетке (яйцеклетке или сперме) или в самой оплодотворенной яйцеклетке, а не унаследованной от носителя. Поскольку только 1/3 всех пациентов с X-SCID имеют положительный семейный анамнез SCID, предполагается, что мутации de novo составляют значительный процент случаев. Х-инактивация происходит совершенно случайным образом у самок на очень ранних стадиях эмбрионального развития. После того, как X инактивирован, он остается инактивированным на протяжении всей жизни этой клетки и любой из ее дочерних клеток. Важно отметить, что X-инактивация обращена в женских половых клетках, так что все новые ооциты получают активный X. Независимо от того, какой X инактивирован в ее соматических клетках, у самки будет 50% шанс передачи болезни. всем детям мужского пола.
Патофизиология
Интерлейкины вырабатываются лимфоцитами, среди других типов клеток, и высвобождаются в ответ на антигенные и неантигенные стимулы . Ген IL2RG кодирует общий белок гамма-цепи , который является общей субъединицей индивидуальных рецепторов интерлейкина 2 , интерлейкина 4 , интерлейкина 7 , интерлейкина 9 , интерлейкина 15 и интерлейкина 21 . Передача сигналов от этих рецепторов обычно способствует росту и дифференцировке Т-клеток , В-клеток , естественных клеток-киллеров , глиальных клеток и клеток моноцитарного происхождения, в зависимости от типа клетки и активированного рецептора. Наиболее важными рецепторами для X-SCID являются рецепторы интерлейкина 2 , интерлейкина 4 , интерлейкина 7 и интерлейкина 15 . В частности, интерлейкин 2 и интерлейкин 7 ответственны за пролиферацию и выживание Т-клеток. Точно так же действие интерлейкина 4 и интерлейкина 15 приведет к пролиферации и дифференцировке B-клеток в плазматические клетки, секретирующие антитела. Наконец, интерлейкин 15 помогает генерировать развитые и созревшие естественные клетки-киллеры.
Ген, кодирующий общую гамма-цепь в этих рецепторах интерлейкина, мутирован в X-SCID. Мутация приводит к отсутствию или ненормальному функционированию общей гамма-цепи. Мутация может происходить через большие или даже одиночные нуклеотидные делеции в гене IL2RG, которые отключают общую гамма-цепь, так что она не может связываться с другими субъединицами рецептора и сигнализировать об активации цитокинов. Обычно, когда интерлейкин связывается с тримерным рецепторным белком, содержащим альфа, бета и гамма-субъединицы, общая гамма-субъединица активирует янус-киназу 3 (JAK3), что приводит к фосфорилированию сигнального преобразователя и активатора транскрипции 5, STAT5 . Белки STAT5 димеризуются и перемещаются в ядро, контролируя последующую передачу сигналов ниже по течению. Из-за того, что общая гамма-цепь отсутствует или ненормальна, этот нисходящий путь ингибируется. Это изменение не позволяет Т-лимфоцитам передавать сигналы другим клеткам, таким как В-лимфоциты и естественные клетки-киллеры. Поскольку эти клетки никогда не получают эти сигналы, они никогда не смогут созреть и дифференцироваться в полноценные иммунные клетки.
Диагностика
Диагностика X-SCID возможна с помощью подсчета лимфоцитов, функциональных тестов лимфоцитов и генетического тестирования. Здоровая иммунная система должна содержать большое количество лимфоцитов, но люди с X-SCID будут содержать необычно небольшое количество Т-клеток, нефункциональных В-клеток и некоторых естественных клеток-киллеров .
| Тип ячейки | Нормальное среднее количество лимфоцитов (диапазон) | Среднее количество X-SCID (диапазон) |
|---|---|---|
| Т-клетки | 3 680 (2 500-5 500) | 200 (0-800) |
| В-клетки | 730 (300-2 000) | 1300 (44 -> 3000) |
| NK-клетки | 420 (170-1 100) | |
| Общий | 0-3 месяца: 5 400 (3 400-7 300) |
У людей с X-SCID часто снижается функция лимфоцитов. Это можно проверить путем введения агентов в иммунную систему; затем наблюдается реакция лимфоцитов. При X-SCID ответы антител на введенные вакцины и инфекции отсутствуют, а ответы Т-клеток на митогены , вещества, которые стимулируют трансформацию лимфоцитов, недостаточны. Иммуноглобулины IgA и IgM , вещества, которые помогают бороться с инфекциями, очень низки.
Отсутствие тени тимуса на рентгеновских снимках грудной клетки также свидетельствует о рентгеновском исследовании ТКИД. У нормального ребенка можно увидеть характерную тень в форме парусника возле сердца. Вилочковая железа у здоровых пациентов будет постепенно уменьшаться в размерах, потому что потребность в вилочковой железе уменьшается. Уменьшение размеров вилочковой железы происходит потому, что в организме уже имеется достаточное количество развитых Т-клеток. Однако пациент с X-SCID родится с аномально маленькой вилочковой железой при рождении. Это указывает на то, что функция вилочковой железы по формированию развитых Т-клеток нарушена.
Поскольку мутация X-SCID является X-сцепленной, существуют генетические тесты для обнаружения носителей в родословных X-SCID . Один из методов - поиск семейных мутаций IL2RG . Наконец, если ни один из этих вариантов недоступен, существует необычный образец неслучайной инактивации Х-хромосомы на лимфоцитах носителей, поэтому поиск такой инактивации окажется полезным.
Если мать беременна и у семьи в анамнезе имеется иммунодефицит, врачи могут провести диагностику внутриутробно. Взятие пробы ворсин хориона, которое включает забор ткани плаценты с помощью катетера, введенного через шейку матки, можно проводить на 8-10 неделе беременности. В качестве альтернативы, амниоцентез, который влечет за собой забор образца жидкости, окружающей плод, может выполняться на 15-20 неделе беременности.
Раннее обнаружение X-SCID (и других типов SCID) также стало возможным благодаря обнаружению кругов удаления рекомбинации Т-клеток или TREC. TREC состоят из вырезанных фрагментов ДНК, которые образуются во время нормального сплайсинга рецепторов поверхностного антигена Т-клеток и созревания Т-клеток. Этот процесс созревания отсутствует во всех вариантах SCID, о чем свидетельствует низкое количество Т-лимфоцитов. Анализ проводится с использованием высушенной крови с карты Гатри , из которой извлекается ДНК. Затем проводится количественная ПЦР и определяется количество TREC. У людей с фенотипом SCID количество TREC будет менее 30 по сравнению с примерно 1020 для здорового ребенка. Низкое количество TREC указывает на недостаточное развитие Т-клеток в вилочковой железе. Этот метод позволяет прогнозировать ТКИД, даже если количество лимфоцитов находится в пределах нормы. Скрининг новорожденных на X-SCID на основе количества TREC в образцах высушенной крови недавно был введен в нескольких штатах США, включая Калифорнию, Колорадо, Коннектикут, Делавэр, Флориду, Массачусетс, Мичиган, Миннесоту, Миссисипи, Нью-Йорк, Техас и Висконсин. Кроме того, с 2013 года в нескольких других штатах проводятся пилотные испытания.
Лечение
Лечение Х-сцепленного ТКИД можно разделить на две основные группы: профилактическое лечение (т.е. профилактическое) и лечебное лечение. Первый пытается управлять условно-патогенными инфекциями, характерными для пациентов с ТКИН, а второй направлен на восстановление здоровой функции Т-лимфоцитов.
С конца 60-х до начала 70-х годов врачи начали использовать «пузыри», которые представляли собой пластиковые корпуса, используемые для размещения новорожденных с подозрением на SCIDS сразу после рождения. Пузырь, форма изоляции, представлял собой стерильную среду, которая означала, что младенец сможет избежать инфекций, вызванных обычными и смертельными патогенами. С другой стороны, профилактические методы лечения, используемые сегодня для лечения Х-сцепленного ТКИН, аналогичны тем, которые используются для лечения других первичных иммунодефицитов . Существует три типа профилактического лечения, а именно: использование лекарств, стерильная среда и внутривенная иммуноглобулиновая терапия (ВВИГ). Во-первых, для борьбы с оппортунистическими инфекциями вводятся антибиотики или противовирусные препараты, такие как флуконазол при кандидозе и ацикловир для предотвращения инфекции вируса герпеса. Кроме того, пациенту также могут вводить внутривенные добавки иммуноглобулина (ВВИГ). Здесь катетер вводится в вену, и жидкость, содержащая антитела, обычно вырабатываемые В-клетками, вводится в тело пациента. Антитела , Y-образные белки, созданные плазматическими клетками, распознают и нейтрализуют любые патогены в организме. Однако IVIG стоит дорого с точки зрения времени и финансов. Следовательно, вышеупомянутые методы лечения только предотвращают инфекции и ни в коем случае не являются лекарством от Х-сцепленного ТКИД.
Трансплантация костного мозга (ТКМ) - это стандартная лечебная процедура, которая приводит к полному восстановлению иммунитета, если лечение было успешным. Во-первых, трансплантация костного мозга требует совпадения лейкоцитарного антигена человека (HLA) между донором и реципиентом. HLA отличается от человека к человеку, что означает, что иммунная система использует HLA, чтобы отличать себя от чужеродных клеток. Кроме того, BMT может быть аллогенным или аутологичным, что означает, что донором и реципиентом костного мозга могут быть два разных человека или один и тот же человек, соответственно. Аутологический BMT включает полное соответствие HLA, тогда как аллогенный BMT включает полное или половинное (гаплоидентичное) соответствие HLA. В частности, при аллогенном BMT вероятность возникновения болезни «трансплантат против хозяина» высока, если соответствие донора и реципиента недостаточно близко. В этом случае Т-клетки в донорском костном мозге атакуют тело пациента, потому что тело чужеродно для этого трансплантата. Истощение Т-клеток в донорской ткани и близкое соответствие HLA уменьшают вероятность возникновения болезни « трансплантат против хозяина» . Более того, пациенты, которые получили точное соответствие HLA, имели нормальные функционирующие Т-клетки через четырнадцать дней. Однако у тех, кто получил гаплоидентичное совпадение HLA, их Т-клетки начали функционировать через четыре месяца. Кроме того, причина, по которой BMT является постоянным решением, заключается в том, что костный мозг содержит мультипотентные гемопоэтические стволовые клетки, которые становятся обычными лимфоидными или обычными миелоидными предшественниками. В частности, общий лимфоидный предшественник дает лимфоциты, участвующие в иммунном ответе (B-клетки, T-клетки, естественные клетки-киллеры). Следовательно, BMT приведет к полному восстановлению иммунитета, но есть аспекты BMT, которые необходимо улучшить (например, GvHD).
Генная терапия - еще один вариант лечения, доступный только для клинических испытаний. Х-сцепленный ТКИД является моногенным заболеванием, ген IL2RG мутирован, поэтому генная терапия заменит этот мутированный ген нормальным. Это приведет к нормальному функционированию белка гамма-цепи рецептора интерлейкина. Для переноса функционального гена в клетку-мишень можно использовать вирусные или невирусные векторы. Вирусные векторы, такие как ретровирус , которые включают ген в геном, приводят к долгосрочным эффектам. Это, в сочетании со стволовыми клетками костного мозга, было успешным при лечении людей с X-SCID. В одном конкретном исследовании, проведенном Cavazzana-Calvo et al., Десять детей получали генную терапию в младенчестве от X-SCID. Девять из десяти излечились от X-SCID. Однако примерно через три года после лечения у двоих детей развился Т-клеточный лейкоз из-за встраивания гена IL2RG рядом с геном LMO2 и, таким образом, активации гена LMO2 (известного онкогена ). У третьего ребенка лейкоз развился в течение двух лет после публикации этого исследования, вероятно, как прямой результат терапии. Это состояние известно как инсерционный мутагенез, когда случайная вставка гена мешает гену-супрессору опухоли или стимулирует онкоген. В настоящее время на рынке нет одобренной генной терапии, но есть много клинических испытаний, в которых могут участвовать пациенты с X-SCID. Поэтому исследования в области генной терапии сегодня и в будущем необходимы, чтобы избежать возникновения лейкемии. В частности, необходимы исследования использования инсуляторных и суицидных генов, поскольку это может предотвратить развитие рака. Ген инсулятора подавляет активацию соседних генов. С другой стороны, когда начинает формироваться опухоль, ген суицида стимулируется, и это приводит к деактивации терапевтического гена. Кроме того, изучается использование рестрикционных ферментов, таких как нуклеаза цинкового пальца (ZFN). ZFN позволяет исследователю выбрать место интеграции гена. Безопасность векторов важна в области генной терапии, поэтому векторы, которые самоинактивируют промотор и энхансер (SIN), и аденовирусы, не вызывающие иммунного ответа, являются важными областями исследований для биологов-переносчиков.
Прогноз
Х-сцепленный ТКИД - это известная педиатрическая неотложная помощь, которая в первую очередь поражает мужчин. Если соответствующее лечение, такое как внутривенное введение добавок иммуноглобулина, лекарства для лечения инфекций или трансплантация костного мозга, не применяется, то прогноз плохой. Пациенты с Х-сцепленным ТКИД обычно умирают через два года после рождения. По этой причине диагностику Х-сцепленного ТКИД необходимо проводить на ранней стадии, чтобы предотвратить заражение младенца какими-либо патогенами.
Однако у пациентов больше шансов на выживание, если диагноз Х-сцепленного ТКИД ставится сразу после рождения ребенка. Это включает в себя профилактические меры, чтобы избежать любых инфекций, которые могут вызвать смерть. Например, у Дэвида Веттера был высокий шанс получить Х-связанный ТКИД, потому что его старший брат умер из-за ТКИД. Это позволило врачам поместить Дэвида в пузырь и предотвратить инфекции. Кроме того, если известно, что Х-связанный ТКИД влияет на ребенка, не следует вводить живые вакцины, и это может спасти жизнь ребенка. Живые аттенуированные вакцины, которые состоят из ослабленных патогенов, введенных в организм для создания иммунного ответа, могут привести к смерти младенцев с Х-связанным ТКИД. Более того, при правильном лечении, таком как пересадка костного мозга, прогноз благоприятный. Трансплантация костного мозга оказалась успешной при лечении нескольких пациентов и привела к полному восстановлению иммунитета, и пациент может жить здоровой жизнью. Результаты трансплантации костного мозга наиболее успешны, когда обнаруживается наиболее близкое соответствие антигена лейкоцитов человека. Однако, если точное совпадение не обнаружено, существует вероятность возникновения болезни «трансплантат против хозяина», что означает, что донорский костный мозг атакует организм пациента. Следовательно, необходимо точное соответствие, чтобы предотвратить любые осложнения.
Эпидемиология
Информации о коэффициенте рождаемости / частоте рождений нет, но «ТКИН, связанный с Х-хромосомой, является наиболее распространенной формой ТКИД, и, по оценкам, на нее приходится от 46% до 70% всех случаев ТКИД».
Особенности мутационной изменчивости. Виды мутаций
Геномы живых организмов являются относительно стабильными, что необходимо для сохранения видовой структуры и преемственности развития. С целью поддержания стабильности в клетке работают различные системы репарации, исправляющие нарушения в структуре ДНК. Тем не менее, если бы изменения в структуре ДНК вообще не сохранялись, виды не могли бы адаптироваться к меняющимся условиям внешней среды и эволюционировать. В создании эволюционного потенциала, т.е. необходимого уровня наследственной изменчивости, основная роль принадлежит мутациям.
Термином “мутация” Г. де Фриз в своем классическом труде “Мутационная теория” (1901-1903) обозначил явление скачкообразного, прерывистого изменения признака. Он отметил ряд особенностей мутационной изменчивости:
- мутация — это качественно новое состояние признака;
- мутантные формы константны;
- одни и те же мутации могут возникать повторно;
- мутации могут быть полезными и вредными;
- выявление мутаций зависит от количества проанализированных особей.
В основе возникновения мутации лежит изменение структуры ДНК или хромосомы, поэтому мутации наследуются в последующих поколениях. Мутационная изменчивость универсальна; она имеет место у всех животных, высших и низших растений, бактерий и вирусов.
Условно мутационный процесс делят на спонтанный и индуцированный. Первый протекает под влиянием естественных факторов (внешних или внутренних), второй — при целенаправленном воздействии на клетку. Частота спонтанного мутагенеза очень низкая. У человека она лежит в пределах 10 -5 — 10 -3 на ген за поколение. В пересчете на геном это означает, что у каждого из нас имеется в среднем один ген, которого не было у родителей.
Большинство мутаций являются рецессивными, что очень важно, т.к. мутации нарушают сложившуюся норму (дикий тип) и поэтому оказываются вредными. Однако рецессивный характер мутантных аллелей позволяет им длительное время сохраняться в популяции в гетерозиготном состоянии и проявляться в результате комбинативной изменчивости. Если возникшая мутация оказывает благоприятное влияние на развитие организма, она будет сохраняться естественным отбором и распространяться среди особей популяции.
По характеру действия мутантного гена мутации делят на 3 вида:
- морфологические,
- физиологические,
- биохимические.
Морфологические мутации изменяют формирование органов и ростовые процессы у животных и растений. Примером данного вида изменений могут служить мутации по окраске глаз, форме крыла, окраске тела, форме щетинок у дрозофилы; коротконогость у овец, карликовость у растений, короткопалость (брахидактилия) у человека и др.
Физиологические мутации обычно понижают жизнеспособность особей, среди них много летальных и полулетальных мутаций. Примером физиологических мутаций являются дыхательные мутации у дрожжей, хлорофильные мутации у растений, гемофилия у человека.
К биохимическим мутациям относят такие, которые подавляют или нарушают синтез определенных химических веществ, обычно в результате отсутствия необходимого фермента. К этому типу относятся ауксотрофные мутации бактерий, определяющие неспособность клетки синтезировать какое-либо вещество (например, аминокислоту). Такие организмы способны жить только при наличии этого вещества в среде. У человека результатом биохимической мутации является тяжелое наследственное заболевание — фенилкетонурия, обусловленное отсутствием фермента синтезирующего тирозин из фенилаланина, в результате чего фенилаланин накапливается в крови. Если вовремя не установить наличие этого дефекта и не исключить фенилаланин из диеты новорожденных, то организму грозит гибель из-за сильного нарушения развития мозга.
Мутации могут быть генеративными и соматическими. Первые возникают в половых клетках, вторые — в клетках тела. Их эволюционная ценность различна и связана со способом размножения.
Генеративные мутации могут происходить на разных этапах развития половых клеток. Чем раньше они возникнут, тем большее количество гамет будет их нести, и, следовательно, увеличится шанс их передачи потомству. Аналогичная ситуация имеет место и в случае возникновения соматической мутации. Чем раньше она происходит, тем большее количество клеток будет ее нести. Особи, имеющие измененные участки тела, называются мозаиками, или химерами. Например, у дрозофилы наблюдается мозаицизм по окраске глаз: на фоне красной окраски в результате мутации возникают белые пятна (лишенные пигмента фасетки).
У организмов, размножающихся только половым способом, соматические мутации не представляют никакой ценности ни для эволюции, ни для селекции, т.к. они не наследуются. У растений, которые могут размножаться вегетативно, соматические мутации могут стать материалом для отбора. Например, почковые мутации, которые дают измененные побеги (спорты). От такого спорта И.В. Мичурин, используя метод прививки, получил новый сорт яблони Антоновка 600-граммовая.
Мутации разнообразны не только по своему фенотипическому проявлению, но и по тем изменениям, которые происходят в генотипе. Различают мутации генные, хромосомные и геномные.
Генные мутации
Генные мутации изменяют структуру отдельных генов. Среди них значительную часть составляют точковые мутации, при которых изменение затрагивает одну пару нуклеотидов. Чаще всего при точковых мутациях происходит замена нуклеотидов. Такие мутации бывают двух типов: транзиции и трансверсии. При транзициях в нуклеотидной паре пурин замещается на пурин или пиримидин на пиримидин, т.е. пространственная ориентация оснований не изменяется. При трансверсиях пурин замещается на пиримидин или пиримидин на пурин, что изменяет пространственную ориентацию оснований.
По характеру влияния замены оснований на структуру кодируемого геном белка выделяют три класса мутаций: missence-мутации, nonsence-мутации и samesence-мутации.
Missence-мутации изменяют смысл кодона, что приводит к появлению в составе белка одной неверной аминокислоты. Это может иметь очень серьезные последствия. Например, тяжелое наследственное заболевание — серповидно-клеточная анемия, одна из форм малокровия, вызвана заменой единственной аминокислоты в составе одной из цепей гемоглобина.
Nonsеnce-мутация — это появление (в результате замены одного основания) кодона-терминатора внутри гена. Если не включится система неоднозначности трансляции (см. выше), процесс синтеза белка будет прерван, и ген будет способен синтезировать только фрагмент полипептида (абортивный белок).
При samesence-мутации замена одного основания приводит к появлению кодона-синонима. В этом случае изменения генетического кода не происходит, и синтезируется нормальный белок.
Кроме замены нуклеотидов, точковые мутации могут быть вызваны вставкой или выпадением одной пары нуклеотидов. Эти нарушения приводят к изменению рамки считывания, соответственно, изменяется генетический код и синтезируется измененный белок.
К генным мутациям относят удвоение и потерю небольших участков гена, а также инсерции — вставки дополнительного генетического материала, источником которого чаще всего являются мобильные генетические элементы. Генные мутации являются причиной существования псевдогенов — неактивных копий функционирующих генов, у которых отсутствует экспрессия, т.е. не образуется функциональный белок. В псевдогенах мутации могут накапливаться. С активацией псевдогенов связывают процесс развития опухолей.
Для появления генных мутаций имеются две основные причины: ошибки в ходе процессов репликации, рекомбинации и репарации ДНК (ошибки трех Р) и действие мутагенных факторов. Примером ошибок в работе ферментных систем в ходе вышеуказанных процессов является неканоническое спаривание оснований. Оно наблюдается при включении в молекулу ДНК минорных оснований — аналогов обычных. Например, вместо тимина может включаться бромурацил, который достаточно легко соединяется с гуанином. Благодаря этому пара АТ замещается на GC.
Под действием мутагенов может происходить превращение одного основания в другое. Например, азотистая кислота путем дезаминирования превращает цитозин в урацил. В следующем цикле репликации он спаривается с аденином и исходная пара GC замещается на АТ.
Хромосомные мутации
Более серьезные изменения в генетическом материале происходят в случае хромосомных мутаций. Их называют хромосомными аберрациями, или хромосомными перестройками. Перестройки могут затрагивать одну хромосому (внутрихромосомные) или несколько (межхромосомные).
Внутрихромосомные перестройки могут быть трех типов: потеря (нехватка) участка хромосомы; удвоение участка хромосомы (дупликации); поворот участка хромосомы на 180° (инверсии). К межхромосомным перестройкам относятся транслокации — перемещение участка одной хромосомы на другую, не гомологичную ей хромосому.
Утрата внутреннего участка хромосомы, не затрагивающего теломеры, носит название делеции, а потеря концевого участка — дефишенси. Оторвавшийся участок хромосомы, если он лишен центромеры, теряется. Оба типа нехваток можно идентифицировать по характеру конъюгации гомологичных хромосом в мейозе. В случае концевой делеции один гомолог оказывается короче другого. При внутренней нехватке нормальный гомолог образует петлю против утраченного участка гомолога.
Нехватки приводят к утрате части генетической информации, поэтому они вредны для организма. Степень вредности зависит от размера утраченного участка и его генного состава. Гомозиготы по нехваткам редко бывают жизнеспособны. У низших организмов эффект нехваток менее ощутим, чем у высших. Бактериофаги могут терять значительную часть своего генома, замещая утраченный участок чужеродной ДНК, и при этом сохраняют функциональную активность. У высших даже гетерозиготность по нехваткам имеет свои пределы. Так, у дрозофилы утрата одним из гомологов участка, включающего более 50 дисков, имеет летальный эффект, несмотря на то, что второй гомолог нормален.
У человека с нехватками связан ряд наследственных заболеваний: тяжелая форма лейкемии (21-я хромосома), синдром кошачьего крика у новорожденных (5-я хромосома) и др.
Нехватки можно использовать для генетического картирования путем установления связи между утратой специфического участка хромосомы и морфологическими особенностями особи.
Дупликацией называют удвоение любого участка хромосомы нормального хромосомного набора. Как правило, дупликации приводят к усилению признака, который контролируется геном, локализованным в этом участке. Например, удвоение у дрозофилы гена Bar, вызывающего редукцию числа глазных фасеток, приводит к дальнейшему уменьшению их количества.
Дупликации легко выявляются цитологически по нарушению структурного рисунка гигантских хромосом, а генетически их можно выявить по отсутствию рецессивного фенотипа при скрещивании.
Инверсия — поворот участка на 180° — изменяет порядок расположения генов в хромосоме. Это очень распространенный вид хромосомных мутаций. Особенно много их обнаружено в геномах дрозофилы, хирономуса, традесканций. Различают два типа инверсий: парацентрические и перицентрические. Первые затрагивают только одно плечо хромосомы, не касаясь центромерного участка и не изменяя форму хромосом. Перицентрические инверсии захватывают район центромеры, включающий участки обоих плеч хромосом, и поэтому они могут значительно изменить форму хромосомы (если разрывы произойдут на разном расстоянии от центромеры).
В профазе мейоза гетерозиготную инверсию можно обнаружить по характерной петле, с помощью которой восстанавливается комплементарность нормального и инвертированного участков двух гомологов. Если в районе инверсии происходит одинарный перекрест, то он приводит к образованию аномальных хромосом: дицентрика (с двумя центромерами) и ацентрика (без центромеры). Если же инвертированный участок имеет значительную протяженность, то может осуществляться двойной кроссинговер, в результате которого образуются жизнеспособные продукты. При наличии двойных инверсий в одном участке хромосомы кроссинговер вообще подавляется, в связи с чем их называют “запирателями перекреста” и обозначают буквой С. Эту особенность инверсий используют при генетическом анализе, например при учете частоты мутаций (методы количественного учета мутаций Г. Меллера).
Межхромосомные перестройки — транслокации, если они имеют характер взаимного обмена участками между негомологичными хромосомами, носят название реципрокных. Если же разрыв затрагивает одну хромосому и оторвавшийся участок прикрепляется к другой хромосоме, то это — нереципрокная транслокация. Образующиеся хромосомы будут нормально функционировать при клеточном делении, если у каждой их них будет одна центромера. Гетерозиготность по транслокациям сильно изменяет процесс конъюгации в мейозе, т.к. гомологичное притяжение испытывают не две хромосомы, а четыре. Вместо бивалентов образуются квадриваленты, которые могут иметь различную конфигурацию в виде крестов, колец и др. Их неправильное расхождение часто приводит к образованию нежизнеспособных гамет.
При гомозиготных транслокациях хромосомы ведут себя как нормальные, при этом образуются новые группы сцепления. Если они сохраняются отбором, то возникают новые хромосомные расы. Таким образом, транслокации могут быть эффективным фактором видообразования, как это имеет место у некоторых видов животных (скорпионы, тараканы) и растений (дурман, пион, энотера). У вида Paeonia californica в транслокационный процесс вовлечены все хромосомы, и в мейозе образуется единый конъюгационный комплекс: 5 пар хромосом образуют кольцо (конъюгация “конец в конец”).
С хромосомными мутациями связано явление, обозначаемое как эффект положения гена. Оно заключается в том, что действие гена изменяется в зависимости от изменения положения самого гена или соседних с ним генов. В обоих случаях ген оказывается в новом окружении. Это явление может повлиять на уровень активности гена, а также на частоту его мутирования. Существенный эффект имеет перемещение гена в новый локус, расположенный рядом с крупным блоком гетерохроматина. Так, перемещение аллеля дикого типа, отвечающего за красную окраску глаз у дрозофилы, в новое место приводит к мозаицизму в проявлении этого признака у мух, гетерозиготных по мутации w (белые глаза).
Перейти к чтению других тем книги "Генетика и селекция. Теория. Задания. Ответы":
Особенности наследования при х - сцепленном рецессивном типе наследования.
Заболевания: гемофилия, дальтонизм, миопатия Дюшена.
Билет 14
Особенности наследования при Х-сцепленном доминантном типе наследования.
Для него хар - ны:
Заболевание прослеживается в каждом поколении
Если болен отец, то все его дочери будут больными, а все сыновья здоровыми
Если больна мать то вероятность рождения больного ребенка равна 50% независимо от пола
Болеют как женщины ток и мужчины, но женщины болеют в 2 раза чаще чем мужчины
Билет 15
У - сцепленное наследование
Сцеплены с у - хромосомным наследованием хар - ся тем, что гены расположены в у - хромосоме передаются только сыновьям от отца а его дочери остаются здоровыми(голландичное наследование)
Мохнатые ушки
У - хромосомы играют роль формирования пола у человека в случае ее отсутствия или отсутствия гена , которые определяют мужской пол, дальнейшее развитие происходит по женскому пути , мутации в у - хромосомах приводят к бесплодию
Билет 16
Роль генотипа и внешней среды в проявлении признаков. Виды изменчивости
Изменчивость - общее св -во живых организмов, приобретающих признаки различия между особями одного вида
Изменчивость бывает:
ненаследственная(фенотипическая или модификационная)
Модификационные изменения происходят под воздействием факторов внешней среды без изменения структуры генотипа.
Признак под влиянием факторов внешней среды изменяется и копирует признак организма к другим признакам
Мутации
Лишь в 20-х гг. ХХ века отечественные учёные С.С. Четвериков (1880-1956) и Н.И. Шмальгаузен (1884-1963) обосновали роль мутаций в эволюции. Было установлено, что любая природная популяция насыщена разнообразными мутациями. Последние чаще всего рецессивны и, находясь в гетерозиготном состоянии, не проявляются фенотипически. Такие мутации чаще всего и служат генетической основой эволюции. При скрещивании гетерозиготных особей эти мутации могут переходить у потомков в гомозиготное состояние и проявляться в фенотипе. Из поколения в поколение сохраняются особи с полезными мутациями, которые поддерживаются естественным отбором. Вредные мутации накапливаются в популяции в скрытом виде, создавая резерв изменчивости, что ведёт к изменению генофонда популяции. Резерв наследственной изменчивости увеличивается в результате перекомбинирования аллельных генов (комбинативной изменчивости).
Мутацию определяют как возникновение наследуемого изменения; в широком смысле это понятие приложимо как к отдельным генам, так и к целым хромосомам. Причинами индуцированных мутаций могут являться естественные и искусственные мутагенные факторы (рис. 143). В результате мутации возникают мутантный ген или мутантная хромосома, дающие начало мутантному признаку. Генные мутации могут возникнуть в любой момент, но их появление более вероятно в делящейся, а не в «покоящейся» клетке; при гаметогенезе появление мутаций наиболее вероятно во время мейоза. В генетическом отношении важны именно те мутации, которые возникают при гаметогенезе. Мутантный ген воспроизводится с высокой точностью до тех пор, пока он не изменится в результате новой мутации. В результате мутаций формируется элементарный эволюционный материал. Он используется далее в ходе эволюции как исходная основа для действия других элементарных эволюционных факторов.
И.И. Шмальгаузен пришёл к выводу, что практически любые мутации, нарушая нормальную сбалансированность процессов и функций в организме, вредны для организма, неблагоприятно влияют на фенотип. Поэтому поддерживаются отбором лишь их гетерозиготные состояния, благодаря чему рецессивные аллели могут накапливаться в популяции и «подгоняться» в ряду её поколений к старому генному комплексу. Очень редко возникают мутации, улучшающие фенотип, повышая его приспособленность к условиям среды. Однако именно они дают основной материал для естественного отбора.
Мутационный процесс протекает в целом очень медленно и, соответственно, обусловливает медленную перестройку генетической структуры популяции. Наряду с мутациями на генетическую структуру популяции оказывают влияние другие процессы, в том числе дрейф генов (рис. 144). Дрейф генов - это изменение частоты генов в популяции в ряду поколений под действием случайных (стохастических) факторов. Он приводит, как правило, к снижению наследственной изменчивости популяций. Термин «дрейф генов» введён в 40-х годах ХХ века американским генетиком С. Райтом (1889-1982). Независимо от него Д.Д. Ромашов (1899-1963) и Н.П. Дубинин (1907-1998) описали это явление под названием «генетико-автоматический процесс». Дрейф генов проявляется наиболее отчётливо при резком сокращении численности популяции в результате стихийных бедствий (лесной пожар, наводнение), массового распространения вредителей и т.д.
Характерная особенность динамики генотипической структуры популяции под влиянием дрейфа генов заключается в:
а) усилении процесса гомозиготизации организмов,который нарастает с уменьшением численности популяции. Это нарастание обусловлено тем, что в популяциях ограниченного размера увеличивается частота близкородственных скрещиваний. Маловероятно, но тем не менее возможно, что некоторые из выщепившихся гомозиготных форм окажутся в новых условиях среды приспособительно ценными и смогут выжить, а не устраниться (элиминироваться) отбором;
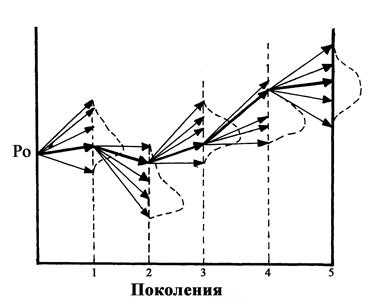
б) потере популяцией некоторых аллелей и закреплении других, что особенно проявляется при значительном размахе колебаний численности в последовательных поколениях.
Вторым явлением, ускоряющим перестройку генофондов популяций, является миграция (поток) генов, возникающая при перемещении особей из одной популяции в другую и скрещивании с представителями последней. Если у пришельцев исходные частоты аллелей другие, чем у старожилов, то частоты аллелей во второй популяции могут измениться. Перемещение особей из популяции-донора в популяцию-реципиент приводит к изменению частот аллелей в обеих популяциях.
Популяционное равновесие и пол
Закон Харди - Вайнберга и тесно связанный с ним закон Пирсона исходят из допущения о равенстве частот генов у самок и самцов. Если это условие не выполняется, то равновесие наступает только во втором поколении, поскольку в первом поколении происходит выравнивание соотношений аллелей у обоих полов.
Все приведенные рассуждения верны для аутосомных локусов. Для генов, сцепленных с половой хромосомой, наблюдаются отличия. Для видов, у которых женский пол гомогаметный (ХХ), частоты генотипов у самок совпадают с равновесными частотами, определяемыми законом Харди - Вайнберга, т. е. p 2 для АА, 2pq для Аа и q 2 для аа. У гетерогаметных самцов (ХY) частоты генотипов совпадают с частотами аллелей: pдля A и q для а.
Поскольку самцы всегда получают свою единственную Х-хромосому от матери, частоты их генотипов совпадают с частотами соответствующих аллелей матери в предыдущем поколении. Ясно также, что фенотипы, определяемые рецессивными аллелями в гомозиготном и гемизиготном состоянии соответственно, у самок встречаются реже (q 2 ), чем у самцов (q).
История создания и основные положения синтетической теории эволюции
Синтетическая теория эволюции - наиболее распространенное эволюционное учение ХХ века - сложилась к началу 1940-х гг. на основе синтеза классического дарвинизма и популяционной генетики.
Основные положения синтетической теории эволюции
1. Движущими силами эволюции являются борьба за существование и естественный отбор, которые определяют направление эволюции.
2. Борьба за существование - это всё многообразие отношений между организмами и средой их обитания. Этот термин отражает зависимость одного существа от другого, а также успех особи в оставлении после себя потомства
3. Естественный отбор - это совокупность биологических процессов, в результате которых наблюдаются дифференциальная смертность и дифференциальный успех в размножении.
4. Объектом действия естественного отбора является фенотип особи.
5. Естественный отбор действует по фенотипам, однако фенотип особи определяется её генотипом. Поэтому в результате отбора происходит дифференциальное воспроизведение генотипов.
6. Элементарной единицей эволюции является популяция. Изменения отдельных особей не приводят к эволюционным изменениям. Эволюционируют не особи, а группы особей, составляющие популяцию.
7. Элементарное эволюционное явление, с которого начинается видообразование в популяции, - это устойчивое изменение генофонда популяции (например, изменение частоты аллеля).
8. Изменение генофонда популяции происходит за счет действия элементарных эволюционных факторов, к которым относятся: мутационный процесс, рекомбинации, популяционные волны, миграция, изоляция, дрейф генов и другие.
9. Движущие силы эволюции и элементарные эволюционные факторы совместно действуют на популяцию и запускают в ней элементарные эволюционные процессы (микроэволюция), которые и приводят к появлению нового биологического вида. Вид - качественный этап эволюции, закрепляющий ее существенный результат.
10. Элементарным эволюционным материалом являются мутантные аллели. Именно на них в ходе микроэволюции действуют элементарные эволюционные факторы.
11. Элементарное адаптационное явление - это появление наследуемого признака, повышающего приспособленность популяции.
Элементарные эволюционные факторы: мутационный процесс, рекомбинации
Мутационный процесс
Изменения наследственного материала половых клеток в виде генных, хромосомных и геномных мутаций происходят постоянно. Особое место принадлежит генным мутациям. Они приводят к возникновению серий аллелей и, таким образом, к генетическому разнообразию.
Совокупность аллелей, возникающих в результате мутаций, представляет собой исходный элементарный эволюционный материал. В процессе видообразования он используется как объект действия других элементарных эволюционных факторов.
Хотя отдельная мутация - событие редкое, общее число мутаций значительно. По всем локусам за поколение в генофонде вида произойдет 10 -5 ∙ 10 4 ∙ 10 4 ∙ 10 3 = 10 6 мутаций. За среднее время существования вида, равное нескольким десяткам тысяч поколений, количество мутаций составит около 10 10 .
Большинство мутаций первоначально оказывает на фенотип особей неблагоприятное действие. Насыщенность популяции мутациями, снижающими ее приспособленность, называется генетическим грузом; это среднее число летальных мутаций на одну особь из данной популяции.
Доля полезных мутаций мала, однако их абсолютное количество в пересчете на поколение или период существования вида может быть большим. Допустим, что одна полезная мутация приходится на 1 млн вредных. Тогда в приведенном выше примере за все время существования вида его генофонд обогатится 10 4 полезными мутациями.
Мутационный процесс происходит на протяжении всего периода существования жизни, а отдельные мутации возникают многократно у разных организмов. Генофонды популяций испытывают непрерывное давление мутационного процесса. Это обеспечивает накопление мутаций, несмотря на высокую вероятность потери в ряду поколений единичной мутации.
Давление мутаций. Одна и та же мутация с одной и той же частотой р возникает в каждом поколении. В то же время мутантный аллель может быть утрачен под воздействием случайных факторов (в т.ч. и вследствие обратных мутаций). Если не учитывать обратных мутаций, то фактическая частота мутантного аллеля нелинейно возрастает. Зависимость частоты мутантного аллеля от порядкового номера поколения может быть примерно аппроксимирована логарифмической функцией. Расчеты показывают, что частота рецессивного селективно нейтрального мутантного аллеля (и вероятность его фенотипического проявления) возрастает примерно следующим образом:
| Поколение | Частота аллеля а, q ×10 - 6 | Частота генотипа аа, q 2 ×10 - 12 |
| 0 | 1 | 1 |
| 20 | 5 | 25 |
| 260 | 10 | 99 |
| 450 | 11 | 121 |
| 750 | 12 | 144 |
| 1250 | 13 | 169 |
| 2100 | 14 | 196 |
| 3550 | 15 | 225 |
В длительно существующей популяции вероятность фенотипического проявления рецессивного мутантного аллеля возрастает в десятки и сотни раз за счет давления мутаций.
Мейотический драйв - это сила, способная изменить механизм мейотического деления клетки таким образом, что соотношение производимых гетерозиготой гамет отклоняется от обычного (50 : 50). Ряд генов, обладающих таким действием, выявлен у мышей, у дрозофил.
Рекомбинации
Как правило, один фенотипический признак формируется под влиянием множества генетических факторов, то есть является полигенным. Поэтому разные мутации могут взаимодействовать между собой. В результате рекомбинаций (которые имеются у всех известных групп организмов) возможны следующие эффекты взаимодействия мутаций:
1. Различные способы межгенных взаимодействий: комплементарность, эпистаз, полимерия: аддитивная (простое суммирование фенотипических эффектов, при котором 1+1=2) и неаддитивная (нелинейное взаимодействие, при котором 1+1≠2).
2. Мутации в управляющих генах: ослабителях (супрессорах), усилителях (бустерах), модификаторах. Например, мутация в гене-модификаторе Х может превратить рецессивную мутацию в доминантную.
Для понимания значения мутационного процесса необходимо рассматривать не отдельные мутации, а все разнообразие возможных мутаций и их сочетаний в популяциях.
Организация стока поверхностных вод: Наибольшее количество влаги на земном шаре испаряется с поверхности морей и океанов (88‰).
Опора деревянной одностоечной и способы укрепление угловых опор: Опоры ВЛ - конструкции, предназначенные для поддерживания проводов на необходимой высоте над землей, водой.
© cyberpedia.su 2017-2020 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!
Читайте также:
- Клинический пример диэнцефалоза. Клиника и проявления диэнцефалоза
- Артериальная гипертензия в популяционных группах. Распространенность гипертензии среди американцев
- Болезни компьютерщиков. Какие компьютерные заболевания приводят к инвалидности?
- Асцит брюшной полости при онкологии: симптомы, жидкость в животе, водянка при раке
- Техника, этапы операции ограниченного артродеза при болезни Мюллера-Вайсса
