Регуляция реабсорбции ионов натрия. Альдостерон. Регуляция транспорта ионов кальция, фосфата, магния.
Добавил пользователь Евгений Кузнецов Обновлено: 21.01.2026
В норме человек должен потреблять воды столько, сколько бывает необходимо, чтобы возместить суточную ее потерю через почки и внепочечными путями. Оптимальный суточный диурез 1400—1600 мл. При нормальных температурных условиях и нормальной влажности воздуха организм теряет через кожу и дыхательные пути от 800 до 1000 мл воды — это так называемые неощутимые потери. Таким образом, общее суточное выведение воды (моча и перспирационные потери) должно составлять 2200—2600 мл. Организм в состоянии частично покрыть свои потребности за счет использования образующейся в нем метаболической воды, объем которой составляет около 150—220 мл. Нормальная сбалансированная суточная потребность человека в воде от 1000 до 2500 мл и зависит от массы тела, возраста, пола и других обстоятельств
Альдостерон - наиболее активный минера-локортикостероид, синтезирующийся в коре надпочечников из холестерола.
АКТГ. Однако наиболее важное влияние на секрецию альдостерона оказывает ренинангиотензиновая система.
Альдостерон не имеет специфических транспортных белков, но за счёт слабых взаимодействий может образовывать комплексы с альбумином. Гормон очень быстро захватывается печенью, где превращается в тетрагидроальдостерон-3-глюкуронид и экскретируется с мочой.
Механизм действия альдостерона
В клетках-мишенях гормон взаимодействует с рецепторами, которые могут быть локализованы как в ядре, так и в цитозоле клетки. Образовавшийся комплекс гормон-рецептор взаимодействует с определённым участком ДНК и изменяет скорость транскрипции специфических генов. Результат действия альдостерона - индукция синтеза: а) белков-транспортёров Na + из просвета канальца в эпителиальную клетку почечного канальца; б) Nа + ,К + ,-АТФ-азы, обеспечивающей удаление ионов натрия из клетки почечного канальца в межклеточное пространство и переносящей ионы калия из межклеточного пространства в клетку почечного канальца; в) белков-транспортёров ионов калия из клеток почечного канальца в первичную мочу; г) митохондриальных ферментов ЦТК, в частности цитратсинтазы, стимулирующих образование молекул АТФ, необходимых для активного транспорта ионов. Суммарным биологическим эффектом индуцируемых альдостероном белков является увеличение реабсорбции ионов натрия в канальцах нефронов, что вызывает задержку NaCl в организме, и возрастание экскреции калия.
Антидиуретический гормон
Антидиуретический гормон (АДГ), или вазопрессин - пептид с молекулярной массой около 1100 Д, содержащий 9 аминокислот, соединённых одним дисульфидным мостиком
Механизм действия
Для АДГ существуют 2 типа рецепторов: V1 и V2. Рецепторы V2, опосредующие главный физиологический эффект гормона, обнаружены на базолатеральной мембране клеток собирательных трубочек и дистальных канальцев - наиболее важных клеток-мишеней для АДГ, которые относительно непроницаемы для молекул воды. В отсутствие АДГ моча не концентрируется и может выделяться в количествах, превышающих 20 л в сутки (норма 1,0-1,5 л в сутки). Связывание АДГ с V2(рис. 11-32) стимулирует аденилатциклазную систему и активацию протеинкиназы А. В свою очередь, протеинкиназа А фосфорилирует белки, стимулирующие экспрессию гена мембранного белка - аквапорина-2. Аквапорин-2 перемещается к апикальной мембране собирательных канальцев и встраивается в неё, образуя водные каналы. Это обеспечивает избирательную проницаемость мембраны клеток для воды, которые свободно диффундируют в клетки почечных канальцев и затем поступают в интерстициальное пространство. Поскольку в результате происходит реабсорбция воды из почечных канальцев и экскреция малого объёма высококонцентрированной мочи (антидиурез), гормон называют антидиуретическим гормоном.
Роль системы ренин-ангиотензин- альдостерон в регуляции водно-солевого обмена
Главным механизмом регуляции синтеза и секреции альдостерона служит система ренинангиотензин.
Ренин - протеолитический фермент, продуцируемый юкстагломерулярными клетками, расположенными вдоль конечной части афферентных (приносящих) артериол, входящих в почечные клубочки
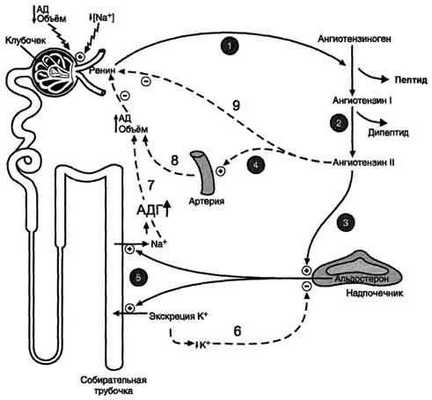
Система ренинангиотензинальдостерон. Ренин, протеолитический фермент, катализирует превращение ангиотензиногена (гликопротеина) в ангиотензин I (декапептид). 1 - ренин, протеолитический фермент, катализирует превращение ангиотензиногена (глйкопротеина) в ангиотензин I; 2 - ангиотензин I превращается в ангиотензин II под действием АПФ, отщепляющего два аминокислотных остатка от декапептида; 3 - ангиотензин II стимулирует синтез и секрецию альдостерона; 4 - ангйотензин II вызывает сужение сосудов периферических артерий; 5 - альдостерон стимулирует реабсорбцию Na + и экскрецию К + ; 6, 7, 8, 9 - торможение секреции ренина и альдостерона по механизму отрицательной обратной связи. Пунктирные линии - регуляция по принципу обратной связи.
4.Образование конечной мочи, ее состав и свойства. Реабсорбция в канальцах, механизм ее регуляции.
В сутки у человека образуется и выделяется от 0,7 до 2 л мочи. Эта величина носит название суточного диуреза и зависит от количества выпитой жидкости, так как здоровым человеком выделяется 65—80 % ее объема с мочой. Основное количество мочи образуется днем, тогда как ночью оно составляет не более половины дневного объема. Удельный вес мочи колеблется в широком диапазоне — от 1005 до 1025, обратно пропорционально объему принятой жидкости и образовавшейся мочи.
Реакция суточной мочи обычно слегка кислая, однако рН колеблется в зависимости от характера питания. При растительной пище моча приобретает щелочную реакцию, а при белковой — становится более кислой.
Моча обычно прозрачна, но имеет небольшой осадок, получаемый при центрифугировании и состоящий из малого количества эритроцитов, лейкоцитов и эпителиальных клеток. В осадке мочи, собранной за 12 ночных часов, содержится от 0 до 400 000 эритроцитов, от 300 000 до 1,8 миллионов лейкоцитов. Здесь также могут присутствовать кристаллы мочевой кислоты, уратов и оксалата кальция (в кислой моче) или кристаллы мочекислого аммония, фосфорнокислого и углекислого кальция (в щелочной моче). Белок и глюкоза в конечной моче практически отсутствуют, содержание аминокислот не превышает 0,5 г за сутки. Поскольку в канальцах нефрона происходит обратное всасывание основной части профильтровавшейся воды, солей и других веществ, то выделяется их с мочой от 45 % (мочевина) до 0,04 % (бикарбонат) от профильтровавшегося количества. Однако за счет всасывания воды и процессов концентрирования мочи, а также секреции в канальцах, содержание в конечной моче ряда веществ превышает их концентрацию в плазме крови: мочевины в 67 раз, калия в 7, сульфатов в 90, фосфатов в 16 раз, тем самым обеспечивается эффективность их экскреции из организма. В небольших количествах в мочу поступают производные продуктов гниения белков в кишечнике — индола, скатола, фенола. В моче содержится широкий спектр органических кислот, небольшие концентрации витаминов (кроме жирорастворимых), биогенные амины и их метаболиты, стероидные гормоны и их метаболиты, ферменты и пигменты, определяющие цвет мочи.
С мочой в разных концентрациях, зависящих от ее количества, выделяются практически все неорганические катионы и анионы, в том числе и широкий спектр микроэлементов.
Реабсорбция в канальцах, механизм .
При сравнении состава и количества первичной и конечной мочи выявляется, что в канальцах нефрона происходит процесс обратного всасывания воды и веществ, профильтровавшихся в клубочках, что необходимо для поддержания их внешнего баланса. Этот процесс называется канальцевой реабсорбцией и в зависимости от отдела канальцев, где он происходит, различают реабсорбцию проксимальную и дисталъную. В процессе реабсорбции вода и вещества из просвета канальцев через люминальную мембрану поступают в цитоплазму клеток эпителия, затем через базолатеральную мембрану выносятся из клеток эпителия в интерстициальное пространство, после чего поступают в перитубулярные (околоканальце-вые) капилляры. Такой путь реабсорбции носит название трансцеллюляр-ного, в его основе лежат общие механизмы транспорта веществ через плазматические мембраны. Кроме того, возможен путь реабсорбции через плотные соединения между клетками эпителия посредством простой диффузии или переносом вещества вместе с растворителем, что носит название парацеллюлярного пути реабсорбции. Реабсорбция представляет собой транспорт веществ из мочи в лимфу и кровь, и в зависимости от механизма выделяют пассивный, первично и вторично активный транспорт.
Проксимальная реабсорбция обеспечивает полное всасывание ряда веществ первичной мочи — глюкозы, белка, аминокислот и витаминов. В проксимальном отделе канальцев всасывается 2/з профильтровавшихся воды и ионов натрия (рис. 14.7), большие количества ионов калия, двухвалентных катионов, анионов хлора, бикарбоната, фосфата, а также мочевая кислота и мочевина. К концу проксимального отдела в его просвете остается только 1/3 объема ультрафильтрата, и, хотя его состав из-за неодинаковой реабсорбции разных компонентов уже существенно отличается от плазмы крови, осмотическое давление первичной мочи остается таким же, как в плазме.
Эпителий проксимального канальца хорошо проницаем для воды, благодаря наличию в апикальной мембране водных каналов, образованных особыми белковыми молекулами аквапоринами. В структурах нефрона описано 6 типов аквапоринов, первый из них (AQP-1) имеется в мембранах клеток проксимальных канальцев (рис. 14.8). Всасывание воды происходит пассивно путем простой диффузии по осмотическому градиенту и прямо зависит от реабсорбции ионов натрия хлорида, других осмотически активных веществ. Благодаря этому содержимое проксимального отдела остается изоосмотичным плазме крови.
Реабсорбция ионов натрия в проксимальном отделе осуществляется несколькими механизмами активного и пассивного транспорта. Во-первых, реабсорбция натрия осуществляется первично активным транспортом. Ионы натрия входит в клетки эпителия через апикальную мембрану пассивно через натриевые каналы по концентрационному градиенту, его выведение через базолатеральные мембраны эпителиальных клеток происходит активно с помощью натрий-калиевых насосов, использующих энергию АТФ. Именно деятельность этих насосов обеспечивает градиент концентрации ионов натрия между внутриканальцевой и внутриклеточной средами. Во-вторых, на апикальной мембране имеется электронейтральный переносчик, обеспечивающий активный обмен Na+ и Н+, при этом ион натрия поступает в клетку в обмен на удаляемый из клетки Н-ион. Такой механизм транспорта носит название антипорта.
Этот переносчик обеспечивает и всасывание бикарбонатного аниона. Профильтровавшийся бикарбонатный анион вместе с Н-ионом образуют угольную кислоту: HCO3 + Н+ = Н2С03. Располагающаяся на щеточной каемке эпителия канальца карбоангидраза катализирует разложение в канальцевой жидкости угольной кислоты: Н2С03 о Н20 + С02, после чего С02 диффундирует в клетку по градиенту концентрации. В клетке под влинием цитоплазменной карбоангидразы протекает обратная реакция: С02 + Н20=Н2С03, угольная кислота диссоциирует: Н2С03 о Н+ + HCO3. Бикарбонатный анион (НСОз) пассивно переносится в перитубулярную жидкость по электрохимическому градиенту, создаваемому активным переносом натрия через ба-золатеральную мембрану, а Н-ион через апикальную мембрану с помощью антипорта Na+-H+ выводится в просвет канальца. Таким образом, сопровождающим всасывающийся ион натрия в начальных отделах проксимального канальца анионом является бикарбонат. Анионы хлора всасываются в начальных отделах плохо из-за низкой проницаемости стенки. Объем мочи в канальце уменьшается из-за пассивной реабсорбции воды, и концентрация хлоридов в его содержимом растет. В конечных участках проксимальных канальцев межклеточные контакты уже проницаемы для хлоридов (концентрация которых повысилась) и они пассивно по градиенту концентрации всасываются из мочи путем парацеллюлярной диффузии, создавая электрохимический градиент для натрия. В-третьих, ион натрия реабсорбируется пассивно, по электрохимическому градиенту, вслед за анионом хлора. Такой пассивный транспорт одного иона (натрия) вместе с пассивным транспортом другого (хлорида) носит название котранспорта. В-четвертых, на апикальной мембране расположены переносчики-котранспортеры натрия и органических веществ (глюкозы, аминокислот), натрия и фосфата или сульфата.
Проксимальная реабсорбция глюкозы и аминокислот осуществляется с помощью специальных переносчиков щеточной каемки апикальной мембраны эпителиальных клеток. Эти переносчики транспортируют глюкозу или аминокислоту, только если одновременно связывают и переносят натрий. Пассивное перемещение натрия по градиенту концентрации внутрь клеток ведет к транспорту через мембрану и переносчика с глюкозой или аминокислотой. Для реализации этого процесса необходима низкая концентрация натрия в эпителиальной клетке, создающая градиент концентрации между внешней и внутриклеточной средой, что обеспечивается энергозависимой работой натрий-калиевого насоса базальной мембраны. Поскольку перенос глюкозы или аминокислоты связан с натрием, а его транспорт определяется активным удалением натрия из клетки, такой вид транспорта называют вторично активным, или симпортом, т. е. совместным пассивным транспортом одного вещества (глюкоза) из-за активного транспорта другого (натрия) с помощью одного переносчика.
Реабсорбция пептидов и белков осуществляется практически полностью в проксимальных канальцах. Количество профильтровавшегося белка относительно невелико и составляет около 1,8 г в сутки. Некоторую его часть составляют альбумины, но фильтрационный барьер клубочков проходят и полипептиды меньшего размера, и в первичную мочу фильтруются, например, соматотропин, а также лизоцим и др. В конечную мочу поступает не более 0,15 г белка в сутки (рис. 14.10). Молекулы альбуминов после связывания с рецепторами на люминальной мембране клеток эпителия канальцев подвергаются эндоцитозу, внутриклеточные пузырьки поглощенного белка сливаются с лизосомами и белковые молекулы гидролизуются пеп-тидазами (аналог внутриклеточного пищеварения). Продукты гидролиза, в основном аминокислоты, выводятся в интерстициальную жидкость и поступают в перитубулярные капилляры. Пептиды, особенно с короткой цепью, подвергаются гидролизу ферментами щеточной каемки (аналог мембранного пищеварения), образующиеся аминокислоты реабсорбируются из просвета канальцев.
Дистальная реабсорбция ионов и воды по объему значительно меньше проксимальной. Однако, существенно меняясь под влиянием регулирующих ее, преимущественно гормональных, воздействий, она определяет состав конечной мочи и способность почки выделять либо концентрированную, либо разведенную мочу (в зависимости от водного баланса организма).
В дистальном отделе нефрона происходит активная реабсорбция ионов натрия. Хотя здесь всасывается всего 10 % от профильтровавшегося количества катиона, этот процесс обеспечивает выраженное уменьшение его концентрации в моче и, напротив, повышение концентрации в интерстициальной жидкости, что создает значительный градиент осмотического давления между мочой и интерстицием, необходимый для всасывания из мочи воды.
Анион хлора всасывается в толстой восходящей части петли Генле благодаря наличию в апикальной мембране клеток эпителия переносчика-котранспортера ионов хлора, натрия и калия, а в дистальных извитых канальцах и собирательных трубочках анион хлора реабсорбируется пассивно по электрохимическому градиенту вслед за активным транспортом натрия. Способность эпителия дистальных канальцев секретировать в мочу Н-ионы связана с реабсорбцией ионов натрия, этот вид транспорта в виде обмена натрия на протон получил название «антипорт». Активно всасывается в дистальном отделе канальцев ионы калия, кальция и фосфатов.
Стенка дистального извитого канальца из-за отсутствия аквапоринов имеет низкую проницаемость для воды и, несмотря на реабсорбцию здесь ионов натрия и хлорида, вода почти не всасывается и в собирательные трубки поступает гипотоническая моча.
Регуляция канальцевой реабсорбции осуществляется как нервным, так и, в большей мере, гуморальным путем.
Нервные влияния реализуются преимущественно симпатическими проводниками и медиаторами через бета-адренорецепторы мембран клеток проксимальных и дистальных канальцев. Симпатические эффекты проявляются в виде активации процессов реабсорбции глюкозы, ионов натрия, воды и анионов фосфатов и осуществляются через систему вторичных посредников (аденилатциклаза — цАМФ). Нервная регуляция кровообращения в мозговом веществе почки увеличивает или уменьшает эффективность сосудистой противоточной системы и концентрирование мочи. Сосудистые эффекты нервной регуляции также опосредуются через внутри-почечные системы гуморальных регуляторов — ренин-ангиотензиновую, кининовую, простагландины и др.
Основным фактором регуляции реабсорбции воды в дистальных отделах нефрона является гормон вазопрессин, называвшийся ранее антидиуретическим гормоном. Этот гормон образуется в супраоптическом и паравен-трикулярных ядрах гипоталамуса, по аксонам нейронов транспортируется в нейрогипофиз, откуда и поступает в кровь. Влияние вазопрессина на проницаемость эпителия канальцев обусловлено наличием рецепторов к гормону, относящихся к V2-типу, на поверхности базолатеральной мембраны клеток эпителия. Образование гормон-рецепторного комплекса влечет за собой через посредство GS-белка и гуанилового нуклеотида активацию аденилатциклазы и образование цАМФ, активацию синтеза и встраивания аквапоринов 2-го типа («водных каналов») в апикальную мембрану клеток эпителия собирательных трубочек. Перестройка ультраструктур мембраны и цитоплазмы клетки ведет к образованию внутриклеточных специализированных структур, переносящих большие потоки воды по осмотическому градиенту от апикальной к базолатеральной мембране, не позволяя транспортируемой воде смешиваться с цитоплазмой и препятствуя набуханию клетки. Такой трансцеллюлярный транспорт воды через клетки эпителия реализуется вазопрессином в собирательных трубочках. Кроме того, в дистальных канальцах вазопрессин обусловливает активацию и выход из клеток гиалуронидаз, вызывающих расщепление гликозаминогликанов основного межклеточного вещества, тем самым способствуя межклеточному пассивному транспорту воды по осмотическому градиенту.
Канальцевая реабсорбция воды регулируется и другими гормонами. По механизму действия все гормоны, регулирующие реабсорбцию воды, делятся на шесть групп: • повышающие проницаемость мембран дистальных отделов нефрона для воды (вазопрессин, пролактин, хорионический гонадотропин); • меняющие чувствительность клеточных рецепторов к вазопрессину (паратирин, кальцитонин, кальцитриол, простагландины, альдостерон); • меняющие осмотический градиент интерстиция мозгового слоя почки и, соответственно, пассивный осмотический транспорт воды (паратирин, кальцитриол, тиреоидные гормоны, инсулин, вазопрессин); • меняющие активный транспорт натрия и хлорида, а за счет этого и пассивный транспорт воды (альдостерон, вазопрессин, атриопептид, прогестерон, глюкагон, кальцитонин, простагландины); • повышающие осмотическое давление канальцевой мочи за счет нере-абсорбированных осмотически активных веществ, например глюкозы (контринсулярные гормоны); • меняющие кровоток по прямым сосудам мозгового вещества и, тем самым, накопление или «вымывание» осмотически активных веществ из интерстиция (ангиотензин-П, кинины, простагландины, паратирин, вазопрессин, атриопептид).
Канальцевая реабсорбция электролитов, так же как и воды, регулируется преимущественно гормональными, а не нервными влияниями.
Реабсорбция ионов натрия в проксимальных канальцах активируется альдостероном и угнетается паратирином, в толстой части восходящего колена петли Генле реабсорбция натрия активируется вазопрессином, глюка-гоном, кальцитонином, а угнетается — простагландинами Е. В дистальном отделе канальцев главными регуляторами транспорта натрия являются альдостерон (активация), простагландины и атриопептид (угнетение). Основной активатор реабсорбции натрия — альдостерон — обеспечивает образование и активацию всех структур, необходимых для транспорта натрия: компонентов натрий-калиевого насоса базолатеральной мембраны и ферментов его энергетического обеспечения, структур натриевых каналов апикальной мембраны и переносчиков иона
Наиболее отчетливо выражена активация реабсорбции ионов натрия под влиянием альдостерона в корковом отделе собирательных трубочек. Действие альдостерона имеет место не только в почках, но также и в желудочно-кишечном тракте, железах внешней секреции — везде этот гормон способствует всасыванию натрия в кровь. В почках альдостерон стимулирует также секрецию ионов калия в мочу.
Регуляция канальцевого транспорта ионов кальция, фосфата и частично магния обеспечивается, в основном, кальций-регулирующими гормонами. Влияния паратирина отличаются в разных отделах канальцевого аппарата почки. В проксимальных канальцах (прямой отдел) всасывание кальция происходит параллельно с транспортом натрия и воды. Угнетение реабсорбции ионов натрия в этом отделе под влиянием паратирина сопровождается параллельным снижением реабсорбции ионов кальция.
За пределами проксимального канальца паратирин избирательно усиливает реабсорбцию кальция, особенно в дистальном извитом канальце и корковой части собирательных трубочек. Реабсорбция ионов кальция активируется также кальцитриолом, а подавляется кальцитонином. Всасывание анионов фосфата в канальцах почки угнетается и паратирином (проксимальная реабсорбция), и кальцитонином (дистальная реабсорбция), а усиливается кальцитриолом и соматотропином. Паратирин активирует реабсорбцию ионов магния в корковой части восходящего колена петли Генле и тормозит проксимальную реабсорбцию аниона бикарбоната.
123. Регуляция водно-солевого обмена. Строение и функции альдостерона и вазопрессина
Важнейшие параметры вводно-солевого гомеостаза - осмотическое давление, рН и объём внутриклеточной и внеклеточной жидкости. Изменение этих параметров может привести к изменению АД, ацидозу или алкалозу, дегидратации и отёкам тканей. Основные гормоны, участвующие в тонкой регуляции водно-солевого баланса и действующие на дистальные извитые канальцы и собирательные трубочки почек: антидиуретический гормон (АДГ), альдостерон и предсердный натриуретический фактор (ПНФ).
Антидиуретический гормон
Антидиуретический гормон (АДГ), или вазопрессин - пептид с молекулярной массой около 1100 Д, содержащий 9 аминокислот, соединённых одним дисульфидным мостиком.
Синтез и секреция антидиуретического гормона. АДГ синтезируется в нейронах гипоталамуса в виде предшественника препрогормона, который поступает в аппарат Гольджи и превращается в прогормон. В составе нейросекреторных гранул прогормон переносится в нервные окончания задней доли гипофиза (нейрогипофиз). Во время транспорта гранул происходит процессинг прогормона, в результате чего он расщепляется на зрелый гормон и транспортный белок - нейрофизин. Гранулы, содержащие зрелый антидиуретический гормон и нейрофизин, хранятся в терминальных расширениях аксонов в задней доле гипофиза, из которых секретируются в кровоток при соответствующей стимуляции. Стимулом, вызывающим секрецию АДГ, служит повышение концентрации ионов натрия и увеличение осмотического давления внеклеточной жидкости. При недостаточном потреблении воды, сильном потоотделении или после приёма большого количества соли осморецепторы гипоталамуса, чувствительные к колебаниям осмолярности, регистрируют повышение осмотического давления крови. Возникают нервные импульсы, которые передаются в заднюю долю гипофиза и вызывают высвобождение АДГ. Секреция АДГ происходит также в ответ на сигналы от барорецепторов предсердий. Изменение осмолярности всего на 1% приводит к заметным изменениям секреции АДГ.
Механизм действия. Для АДГ существуют 2 типа рецепторов: V1 и V2. Рецепторы V2, опосредующие главный физиологический эффект гормона, обнаружены на базолатеральной мембране клеток собирательных трубочек и дистальных канальцев - наиболее важных клеток-мишеней для АДГ, которые относительно непроницаемы для молекул воды. В отсутствие АДГ моча не концентрируется и может выделяться в количествах, превышающих 20 л в сутки (норма 1,0-1,5 л в сутки). Связывание АДГ с V2 стимулирует аденилатциклазную систему и активацию протеинкиназы А. В свою очередь, протеинкиназа А фосфорилирует белки, стимулирующие экспрессию гена мембранного белка - аквапорина-2. Аквапорин-2 перемещается к апикальной мембране собирательных канальцев и встраивается в неё, образуя водные каналы. Это обеспечивает избирательную проницаемость мембраны клеток для воды, которые свободно диффундируют в клетки почечных канальцев и затем поступают в интерстициальное пространство. Поскольку в результате происходит реабсорбция воды из почечных канальцев и экскреция малого объёма высококонцентрированной мочи (антидиурез), гормон называют антидиуретическим гормоном.
Рецепторы типа V1 локализованы в мембранах ГМК сосудов. Взаимодействие АДГ с рецептором V1 приводит к активации фосфолипазы С, которая гидролизует фосфатидилинозитол-4,5-бисфосфат с образованием инозитолтрифосфата и диацилглицерола. Инозитолтрифосфат вызывает высвобождение Са 2+ из ЭР. Результатом действия гормона через рецепторы V1 является сокращение гладкомышечного слоя сосудов. Сосудосуживающий эффект АДГ проявляется при высоких концентрациях гормона. Поскольку сродство АДГ к рецептору V2 выше, чем к рецептору V1, при физиологической концентрации гормона в основном проявляется его антидиуретическое действие.
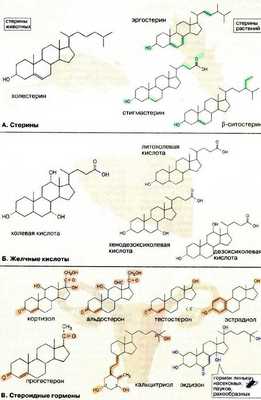
Альдостерон - наиболее активный минералокортикостероид, синтезирующийся в коре надпочечников из холестерола.
Синтез и секреция альдостерона клетками клубочковой зоны непосредственно стимулируются низкой концентрацией Na + и высокой концентрацией К + в плазме крови. На секрецию альдостерона влияют также простагландины, АКТГ. Однако наиболее важное влияние на секрецию альдостерона оказывает ренинангиотензиновая система. Альдостерон не имеет специфических транспортных белков, но за счёт слабых взаимодействий может образовывать комплексы с альбумином. Гормон очень быстро захватывается печенью, где превращается в тетрагидроальдостерон-3-глюкуронид и экскретируется с мочой.
Механизм действия альдостерона. В клетках-мишенях гормон взаимодействует с рецепторами, которые могут быть локализованы как в ядре, так и в цитозоле клетки. Образовавшийся комплекс гормон-рецептор взаимодействует с определённым участком ДНК и изменяет скорость транскрипции специфических генов. Результат действия альдостерона - индукция синтеза: а) белков-транспортёров Na + из просвета канальца в эпителиальную клетку почечного канальца; б) Nа + ,К + ,-АТФ-азы, обеспечивающей удаление ионов натрия из клетки почечного канальца в межклеточное пространство и переносящей ионы калия из межклеточного пространства в клетку почечного канальца; в) белков-транспортёров ионов калия из клеток почечного канальца в первичную мочу; г) митохондриальных ферментов ЦТК, в частности цитратсинтазы, стимулирующих образование молекул АТФ, необходимых для активного транспорта ионов. Суммарным биологическим эффектом индуцируемых альдостероном белков является увеличение реабсорбции ионов натрия в канальцах нефронов, что вызывает задержку NaCl в организме, и возрастание экскреции калия.
Водно-электролитный обмен в организме здорового человека: принципы регуляции

Регуляция водно-солевого обмена, как и большинство физиологических регуляций, включает афферентное, центральное и эфферентное звенья. Афферентное звено представлено массой рецепторных аппаратов сосудистого русла, тканей и органов, воспринимающих сдвиги осмотического давления, объема жидкостей и их ионного состава. В результате, в центральной нервной системе создается интегрированная картина состояния водно-солевого баланса в организме. Так, при увеличении концентрации электролитов и уменьшении объема циркулирующей жидкости (гиповолемии) появляется чувство жажды, а при увеличении объема циркулирующей жидкости (гиперволемии) оно уменьшается. Следствием центрального анализа является изменение питьевого и пищевого поведения, перестройка работы желудочно-кишечного тракта и системы выделения (прежде всего функции почек), реализуемая через эфферентные звенья регуляции. Последние представлены нервными и, в большей мере, гормональными влияниями. Увеличение объема циркулирующей жидкости за счет повышенного содержания воды в крови (гидремия) может быть компенсаторным, возникающим, например, после массивной кровопотери. Гидремия с аутогемодиллюцией представляет собой один из механизмов восстановления соответствия объема циркулирующей жидкости емкости сосудистого русла. Патологическая гидремия является следствием нарушения водно-солевого обмена, например при почечной недостаточности и др. У здорового человека может развиться кратковременная физиологическая гидремия после приема больших количеств жидкости.
Помимо перманентного обмена водой между организмом и окружающей средой важное значение имеет обмен водой между внутриклеточным, внеклеточным сектором и плазмой крови. Следует отметить, что механизмы водно-электролитного обмена между секторами не могут быть сведены только к физико-химическим процессам, так как распределение воды и электролитов связано также с особенностями функционирования мембран клеток. Наиболее динамичным является интерстициальный сектор, на котором прежде всего отражаются потеря, накопление и перераспределения воды и сдвиги электролитного баланса. Важными факторами, влияющими на распределение воды между сосудистым и интерстициальным секторами является степень проницаемости сосудистой стенки, а также соотношение и взаимодействие гидродинамических давлений секторов. В плазме содержание белков равна 65-80 г/л, а в интерстициальном секторе только 4 г\л. Это создает постоянную разность коллоидно-осмотического давления между секторами, обеспечивающую удержание воды в сосудистом русле. Роль гидродинамического и онкотического факторов в обмене воды между секторами была показана еще в 1896г. американским физиологом Э. Старлингом: переход жидкой части крови в межтканевое пространство и обратно обусловлен тем, что в артериальном капиллярном русле эффективное гидростатическое давление выше, чем эффективное онкотическое давление, а в венозном капилляре - наоборот.
Гуморальная регуляция водно-электролитного баланса в организме осуществляется следующими гормонами:
- антидиуретический гормон (АДГ, вазопрессин), воздействует на собирательные трубочки и дистальные канальцы почек, увеличивая реабсорбцию воды;
- натриуретический гормон (предсердный натриуретический фактор, ПНФ, атриопептин), расширяет приносящие артериолы в почках, что увеличивает почечный кровоток, скорость фильтрации и экскрецию Na+; ингибирует выделение ренина, альдостерона и АДГ;
- ренин-ангиотензин-альдостероновая система стимулирует реабсорбцию Na+ в почках, что вызывает задержку NaCl в организме и повышает осмотическое давление плазмы, что определяет задержку выведения жидкости.
- паратиреоидный гормон увеличивает абсорбцию калия почками и кишечником и выведение фосфатов и увеличение реабсорбции кальция.
Содержание натрия и организме регулируется в основном почками под контролем ЦНС через специфические натриорецепторы. реагирующие на изменение содержания натрия в жидкостях тела, а также волюморецепторы и осморецепторы, реагирующие на изменение объема циркулирующей жидкости и осмотического давления внеклеточной жидкости соответственно. Содержание натрия в организме контролируется ренин-ангиотензинной системой, альдостероном, натрийуретическими факторами. При уменьшении содержания воды в организме и повышении осмотического давления крови усиливается секреция вазопрессина (антидиуретического гормона), который вызывает увеличение обратною всасывания воды в почечных канальцах. Увеличение задержки натрия почками вызывает альдостерон, а усиление выведения натрия — натрийуретические гормоны, или натрийуретические факторы (атриопептиды, простагландины, уабаинподобное вещество).
Состояние водно-солевого обмена в значительной степени определяет содержание ионов Cl- во внеклеточной жидкости. Из организма ионы хлора выводятся в основном с мочой, желудочным соком, потом. Количество экскретируемого хлорида натрия зависит от режима питания, активной реабсорбции натрия, состояния канальцевого аппарата почек, кислотно-щелочного состояния. Обмен хлора в организме пассивно связан с обменом натрия и регулируется теми же нейрогуморальными факторами. Обмен хлоридов тесно связан с обменом воды: уменьшение отеков, рассасывание транссудата, многократная рвота, повышенное потоотделение и др. сопровождаются увеличением выведения ионов хлора из организма.
Баланс калия в организме поддерживается двумя способами:
изменением распределения калия между внутри- и внеклеточным компартментами, регуляцией почечной и внепочечной экскреции ионов калия.
Распределение внутриклеточного калия по отношению к внеклеточному поддерживается прежде всего Na-K-АТФазой, являющейся структурным компонентом мембран всех клеток организма. Поглощения калия клетками против градиента концентрации инициируют инсулин, катехоламины , альдостерон. Известно, что ацидоз способствует выходу калия из клеток, алкалоз — перемещению калия внутрь клеток.
Экскретируемая почками фракция калия обычно составляет приблизительно 10-15 % от всего фильтруемого калия плазмы. Задержка в организме или выделение калия почкой определяется тем, каково направление транспорта калия в связующем канальце и собирательной трубке коры почек. При высоком содержании калия в пище эти структуры секретируют его, а при низком - секреция калия отсутствует. Помимо почек калий выводится желудочно-кишечным трактом и при потоотделении. При обычном уровне ежедневного потребления калия (50-100 ммоль/сут) приблизительно 10 % удаляются со стулом.
Главные регуляторы обмена кальция и фосфора в организме: витамин D, паратгормон и кальцитонин. Витамин D (в результате преобразований в печени образуется витамин D3, в почках — кальцитриол) увеличивает всасывание кальция в пищеварительном тракте и транспорт кальция и фосфора к костям. Паратгормон выделяется при снижении уровня кальция в сыворотке крови, высокий же уровень кальция тормозит образование паратгормона. Паратгормон способствует повышению содержания кальция и снижению концентрации фосфора в сыворотке крови. Кальций резорбируется из костей, также увеличивается его всасывание в пищеварительном тракте, а фосфор удаляется из организма с мочой. Паратгормон также необходим для образования активной формы витамина D в почках. Увеличение уровня кальция в сыворотке крови способствует выработке кальцитонина. В противоположность паратгормону он вызывает накопление кальция в костях и снижает его уровень в сыворотке крови, уменьшая образование активной формы витамина D в почках. Увеличивает выделение фосфора с мочой и снижает его уровень в сыворотке крови.
Регуляция реабсорбции ионов натрия. Альдостерон. Регуляция транспорта ионов кальция, фосфата, магния.
Ткани и органы. Почки
Реабсорбция электролитов и воды
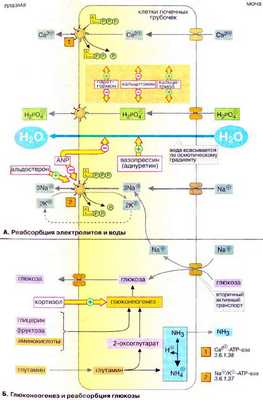
А. Реабсорбция * электролитов и воды
Электролиты и другие низкомолекулярные компоненты плазмы крови попадают в первичную мочу за счет ультрафильтрации (гломерулярный фильтрат) (на схеме справа). Большая часть профильтровавшихся веществ реабсорбируется за счет активного транспорта, связанного с затратой энергии. За счет пассивного транспорта всасывается вода, ионы хлора (2/3) и мочевина. Степень реабсорбции определяет абсолютное количество веществ, остающихся в моче и экскретируемых из организма. Процессы реабсорбции и секреции электролитов и неэлектролитов локализованы в различных отделах почечных канальцев. Здесь дана общая схема процессов реабсорбции, не имеющая прямого отношения к локализации транспортных процессов в различных отделах нефрона (см. учебник по физиологии).
Кальций- и фосфат-ионы. Ионы кальция (Са 2+ ) и фосфат-ионы почти полностью реабсорбируются в почечных канальцах, причем процесс идет с затратой энергии (в форме АТФ). Выход по Са 2+ составляет более 99%, по фосфат-ионам — 80-90%. Степень реабсорбции этих электролитов регулируется паратгормоном (паратирином), кальцитонином и кальцитриолом.
Пептидный гормон паратирин (ПТГ), секретируемый паращитовидной железой, стимулирует реабсорбцию ионов кальция и одновременно ингибирует реабсорбцию ионов фосфата. В сочетании с действием других гормонов костной ткани и кишечника это приводит к увеличению уровня ионов кальция в крови и снижению уровня фосфат-ионов.
Кальцитонин , пептидный гормон из С-клеток щитовидной железы, ингибирует реабсорбцию ионов кальция и фосфата. Это приводит к снижению уровня обоих ионов в крови. Соответственно, в отношении регуляции уровня ионов кальция кальцитонин является антагонистом паратирина.
Стероидный гормон кальцитриол, образующийся в почках (см. с. 322), стимулирует всасывание ионов кальция и фосфат-ионов в кишечнике, способствует минерализации костей, участвует в регуляции реабсорбции ионов кальция и фосфата в почечных канальцах.
Ионы натрия. Реабсорбция ионов Na + из первичной мочи является очень важной функцией почек. Это высокоэффективный процесс: всасывается около 97% Na + . Стероидный гормон альдостерон (см. рис. 63) стимулирует, а атриальный натрийуретический пептид [АНП (ANP)], синтезируемый в предсердии, напротив, ингибирует этот процесс. Оба гормона регулируют работу Na + /К + -АТФ-азы, локализованной на той стороне плазматической мембраны клеток канальцев (дистального отдела и собирательных трубочек нефрона), которая омывается плазмой крови. Этот натриевый насос выкачивает ионы Na + из первичной мочи в кровь в обмен на ионы К + (см. с. 318).
Вода. Реабсорбция воды — процесс пассивный , при котором вода всасывается в осмотически эквивалентном объеме вместе с ионами Na + . В дистальной части нефрона вода может всасываться только в присутствии пептидного гормона вазопрессина (антидиуретического гормона, АДГ), секретируемого гипоталамусом.
АНП ингибирует реабсорбцию воды. т. е. усиливает выведение воды из организма.
Б. Глюконеогенез и реабсорбция глюкозы
Наряду с печенью почки являются органом, в котором осуществляется синтез глюкозы de novo ( глюконеогенез, см. рис. 157). Субстратом является главным образом глутамин . Кроме того, могут использоваться другие аминокислоты и такие метаболиты, как лактат, глицерин и фруктоза , поступающие из крови. По аналогии с печенью, процесс глюконеогенеза индуцируется кортизолом (см. рис. 303). Так как почки одновременно потребляют глюкозу, общий баланс глюкозы сохраняется без изменений.
Независимо от процесса глюконеогенеза в почках идет процесс реабсорбции глюкозы из первичной мочи. Это энергозависимый процесс, сопряженный с гидролизом АТФ. Вместе с тем он сопровождается сопутствующим транспортом ионов Na + (по градиенту, так как концентрация Na + с первичной моче выше, чем в клетках). Этот процесс получил название «вторичного активного транспорта». По аналогичному механизму всасываются также аминокислоты и кетоновые тела.
* В медицине это явление принято называть резорбцией — Прим. перев.
Читайте также:
